3ч ТИ 1 курс -Молек. (МКТ) .ppt
- Количество слайдов: 18
 Лекция 3. Молекулярная физика 1. Молекулярно-кинетическая теория вещества. 2. Термодинамика.
Лекция 3. Молекулярная физика 1. Молекулярно-кинетическая теория вещества. 2. Термодинамика.
 а) облегчающие - тепловые явления связаны с обеспечением жизнедеятельности организма человека; занимают первостепенное место в производстве; определяющие процессы на Земле и в Галактике; б) трудности - многие стороны тепловых явлений связаны с внутренним строением вещества, не просматриваются непосредственно, визуально.
а) облегчающие - тепловые явления связаны с обеспечением жизнедеятельности организма человека; занимают первостепенное место в производстве; определяющие процессы на Земле и в Галактике; б) трудности - многие стороны тепловых явлений связаны с внутренним строением вещества, не просматриваются непосредственно, визуально.
 двух направлениях -исходя из внутреннего строения вещества (разработана строгая теория: молекулярнокинетическая теория вещества); - с энергетических позиций исследование состояния вещества (термодинамика).
двух направлениях -исходя из внутреннего строения вещества (разработана строгая теория: молекулярнокинетическая теория вещества); - с энергетических позиций исследование состояния вещества (термодинамика).
 1. Молекулярно-кинетическая теория вещества. Броуновское движение, явление диффузии и прямые наблюдения с помощью электронного микроскопа и другие эксперименты привели к системе закономерностей и созданию строгой теории молекулярно-кинетической теории строения вещества. Основные её положения, как видно и из названия: - все вещества состоят из молекул; - молекулы движутся, интенсивность движения связана с температурой; - молекулы взаимодействуют (притягиваются и отталкиваются); - размеры молекул малы, порядка ~10 -10 м; - между молекулами имеются пространство.
1. Молекулярно-кинетическая теория вещества. Броуновское движение, явление диффузии и прямые наблюдения с помощью электронного микроскопа и другие эксперименты привели к системе закономерностей и созданию строгой теории молекулярно-кинетической теории строения вещества. Основные её положения, как видно и из названия: - все вещества состоят из молекул; - молекулы движутся, интенсивность движения связана с температурой; - молекулы взаимодействуют (притягиваются и отталкиваются); - размеры молекул малы, порядка ~10 -10 м; - между молекулами имеются пространство.
 Масса (m; m 0 , mr , M), Количество вещества (ν = m/M=N/NA) Температура (0 C, K, Т, R) , Внутренняя энергия U, Количества теплоты Q, Равновесное состояние (t 1= t 2), Необратимости тепловых процессов и другие
Масса (m; m 0 , mr , M), Количество вещества (ν = m/M=N/NA) Температура (0 C, K, Т, R) , Внутренняя энергия U, Количества теплоты Q, Равновесное состояние (t 1= t 2), Необратимости тепловых процессов и другие
 Параметры: масса, объём, давление, температура. Масса молекулы mo, измеряемая в кг или в абсолютных единицах массы (а. е. м. ) 1 а. е. м. =1, 675· 10 -27 кг. Поскольку масса атома и молекулы малые величины используется понятие относительная масса Mr, отношение массы данного атома к 112 части атома углерода (относительная масса атомов указывается в таблице Менделеева), и молярная масса M, масса группы молекул с определенным числом молекул NA=6, 023· 1023 1моль - число Авогадро. Эта группа молекул принимается за единицу измерения количества вещества и называется молем ν=1 моль; ν = m /M=N/NA ; M= mo·NA.
Параметры: масса, объём, давление, температура. Масса молекулы mo, измеряемая в кг или в абсолютных единицах массы (а. е. м. ) 1 а. е. м. =1, 675· 10 -27 кг. Поскольку масса атома и молекулы малые величины используется понятие относительная масса Mr, отношение массы данного атома к 112 части атома углерода (относительная масса атомов указывается в таблице Менделеева), и молярная масса M, масса группы молекул с определенным числом молекул NA=6, 023· 1023 1моль - число Авогадро. Эта группа молекул принимается за единицу измерения количества вещества и называется молем ν=1 моль; ν = m /M=N/NA ; M= mo·NA.
 Температурные шкалы (0 С, К, F, R) Давление P Объём V Основное уравнение МКТ P =1/3 nm 0 V 2 ΔS Δl=VΔt P = F/S (1) , F = Σ Fi , где Fi = m 0 a = m 0(V-V 0)/Δt , F = NFi , ΔS F 1 = NFi/6 (3) N = nv = n ΔlΔS = n. VΔt ΔS (4), S = ΔS P = F/S (1) Fi=2 m 0 V/Δt (2) , P = F 1 / ΔS =[ n. V Δt ΔS · 2 m 0 V/ Δt ] / 6 ΔS = n m 0 V 2/3 P = 2/3 [n (m 0 V 2/2) ] = 2/3 [n E 0] E 0 ~ T , P = nk. T ( 5 `) - уравнение Клаузиса (5) 2/3 [E 0] ~ T , 2/3 [E 0] =k. T
Температурные шкалы (0 С, К, F, R) Давление P Объём V Основное уравнение МКТ P =1/3 nm 0 V 2 ΔS Δl=VΔt P = F/S (1) , F = Σ Fi , где Fi = m 0 a = m 0(V-V 0)/Δt , F = NFi , ΔS F 1 = NFi/6 (3) N = nv = n ΔlΔS = n. VΔt ΔS (4), S = ΔS P = F/S (1) Fi=2 m 0 V/Δt (2) , P = F 1 / ΔS =[ n. V Δt ΔS · 2 m 0 V/ Δt ] / 6 ΔS = n m 0 V 2/3 P = 2/3 [n (m 0 V 2/2) ] = 2/3 [n E 0] E 0 ~ T , P = nk. T ( 5 `) - уравнение Клаузиса (5) 2/3 [E 0] ~ T , 2/3 [E 0] =k. T
 Уравнение состояния (m, P, v, T) P = nk. T=(N/v)(k. T) P v/T=Nk=b=Const PV/T=Const или P 1 V 1/T 1 = P 2 V 2/T 2 ( 6 ) - уравнение Клапейрона Используя P V /T = Nk = Const , запишем это уравнение для 1 моля газа при нормальных условиях P 0 V 0/T 0=R , где R – универсальная газовая постоянная, R= NAk , для любого количества вещества газа получим P 0 V/T 0=νR или PV/T=νR PV=νRT ( 7 ) - уравнение Менделеева-Клапейрона С учётом размеров молекул и взаимодействия их на расстоянии для реального газа получим в виде (P+α/V)(V-b`)= ν·RT или (P+α/V)(V-b`)=m/M·RT (8) Уравнение-дер-Ваальса для реальных газов.
Уравнение состояния (m, P, v, T) P = nk. T=(N/v)(k. T) P v/T=Nk=b=Const PV/T=Const или P 1 V 1/T 1 = P 2 V 2/T 2 ( 6 ) - уравнение Клапейрона Используя P V /T = Nk = Const , запишем это уравнение для 1 моля газа при нормальных условиях P 0 V 0/T 0=R , где R – универсальная газовая постоянная, R= NAk , для любого количества вещества газа получим P 0 V/T 0=νR или PV/T=νR PV=νRT ( 7 ) - уравнение Менделеева-Клапейрона С учётом размеров молекул и взаимодействия их на расстоянии для реального газа получим в виде (P+α/V)(V-b`)= ν·RT или (P+α/V)(V-b`)=m/M·RT (8) Уравнение-дер-Ваальса для реальных газов.
 ИЗОПРОЦЕССЫ № пп ХАРАКТЕРИСТИКИ СОСТОЯНИЯ Р, V, T, M, m НАЗВАНИЕ ПРОЦЕССА НАЗВАНИЕ ЗАКОНА ВИД УРАВНЕНИЯ 1 P, V, T=Const ИЗОТЕРМИЧЕСКИЙ БОЙЛЯМАРИОТТА P 1 V 1 = P 2 V 2 2 V, T, P=Const ИЗОБАРИЧЕСКИЙ ГЕЙЛЮССАКА V 1 /V 2 =T 1 /T 2 3 T, P, V=Const ИЗОХОРИЧЕСКИЙ ШАРЛЯ P 1 /P 2 =T 1 /T 2 4 P, V, T, Q=0 АДИАБАТИЧЕСКИЙ ПУАССОНА T 1 V 1 g-1=T 2 V 2 g-1
ИЗОПРОЦЕССЫ № пп ХАРАКТЕРИСТИКИ СОСТОЯНИЯ Р, V, T, M, m НАЗВАНИЕ ПРОЦЕССА НАЗВАНИЕ ЗАКОНА ВИД УРАВНЕНИЯ 1 P, V, T=Const ИЗОТЕРМИЧЕСКИЙ БОЙЛЯМАРИОТТА P 1 V 1 = P 2 V 2 2 V, T, P=Const ИЗОБАРИЧЕСКИЙ ГЕЙЛЮССАКА V 1 /V 2 =T 1 /T 2 3 T, P, V=Const ИЗОХОРИЧЕСКИЙ ШАРЛЯ P 1 /P 2 =T 1 /T 2 4 P, V, T, Q=0 АДИАБАТИЧЕСКИЙ ПУАССОНА T 1 V 1 g-1=T 2 V 2 g-1
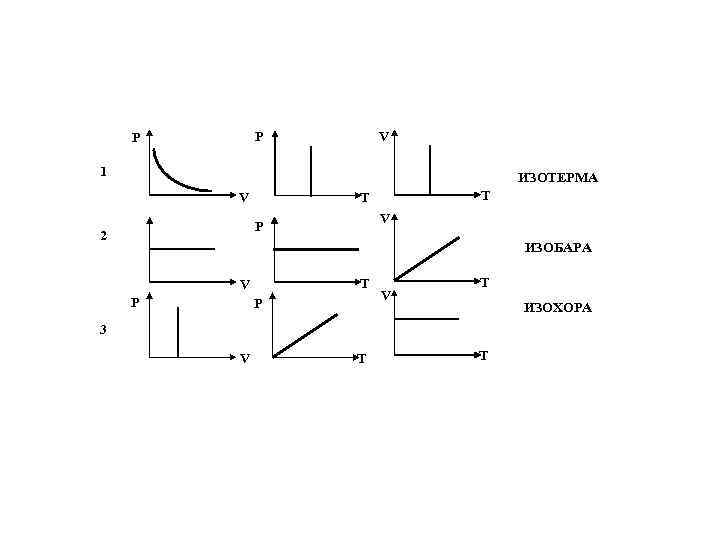 Р Р V 1 ИЗОТЕРМА V P 2 T T V ИЗОБАРА T V Р Р V T ИЗОХОРА 3 V T T
Р Р V 1 ИЗОТЕРМА V P 2 T T V ИЗОБАРА T V Р Р V T ИЗОХОРА 3 V T T

 Термодинамика. Внутренняя энергия. Изменение внутренней энергии двумя способами: за счёт совершаемой механической работы и при теплопередаче (теплопроводность, конвекция, излучение)
Термодинамика. Внутренняя энергия. Изменение внутренней энергии двумя способами: за счёт совершаемой механической работы и при теплопередаче (теплопроводность, конвекция, излучение)
 Суммарная энергия движения молекул тела (их суммарная кинетическая энергия) и их энергия взаимодействия (потенциальная энергия) составляет внутреннюю энергию тела (U). U=Е=E 0 N. Выражая N=νNA=m/MNA, получим для подсчёта внутренней энергии тела U=Е=E 0 N=E 0νNA=(m/M)E 0 NA=(m/M)(3/2)(k. T)NA =(m/M)(3/2)RT, где R=k. NA- универсальная газовая постоянная. Итак U=(3/2)(m/M)RT=3/2(νRT) для одноатомного газа или U=(ί/2)(m/M)RT для многоатомного газа, где ί – степень свободы (число возможных и заметных направлений движения). U= (ί/2)(m/M)RT; U=f(T); ΔU=(ί/2)(m/M)RΔT
Суммарная энергия движения молекул тела (их суммарная кинетическая энергия) и их энергия взаимодействия (потенциальная энергия) составляет внутреннюю энергию тела (U). U=Е=E 0 N. Выражая N=νNA=m/MNA, получим для подсчёта внутренней энергии тела U=Е=E 0 N=E 0νNA=(m/M)E 0 NA=(m/M)(3/2)(k. T)NA =(m/M)(3/2)RT, где R=k. NA- универсальная газовая постоянная. Итак U=(3/2)(m/M)RT=3/2(νRT) для одноатомного газа или U=(ί/2)(m/M)RT для многоатомного газа, где ί – степень свободы (число возможных и заметных направлений движения). U= (ί/2)(m/M)RT; U=f(T); ΔU=(ί/2)(m/M)RΔT
 Работа совершаемая газом А = F S cos α, А = F S, F = pσ, S=Δh, получим F A = pσΔh = pΔV Δh σ
Работа совершаемая газом А = F S cos α, А = F S, F = pσ, S=Δh, получим F A = pσΔh = pΔV Δh σ
 Первое начало термодинамики ΔU = Q + A 1 ΔU = Q - A Q = ΔU + A
Первое начало термодинамики ΔU = Q + A 1 ΔU = Q - A Q = ΔU + A
 Первое начало термодинамики Q = ΔU + A для изопроцессов 1. V=Const A=PΔV=0 2. T=Const ΔU=ί/2(m/M)RΔT=0 3. P=Const A=PΔV 4. Q=0 0=ΔU+A Q=ΔU Q=A Q=ΔU+PΔV A = - ΔU
Первое начало термодинамики Q = ΔU + A для изопроцессов 1. V=Const A=PΔV=0 2. T=Const ΔU=ί/2(m/M)RΔT=0 3. P=Const A=PΔV 4. Q=0 0=ΔU+A Q=ΔU Q=A Q=ΔU+PΔV A = - ΔU
 Второе начало термодинамики характеризует направление естественного процесса тепловых явлений в природе.
Второе начало термодинамики характеризует направление естественного процесса тепловых явлений в природе.
 Тепловые машины η = (Q 1 – Q 2) / Q 1 ηmax = (T 1 – T 2) / T 1 1. Паровые машины 2. Паровые турбины 3. Двигатели вн. сгорания 4. Реактивные двигатели (0, 5%; ) (40%) (25 -40%) (50%)
Тепловые машины η = (Q 1 – Q 2) / Q 1 ηmax = (T 1 – T 2) / T 1 1. Паровые машины 2. Паровые турбины 3. Двигатели вн. сгорания 4. Реактивные двигатели (0, 5%; ) (40%) (25 -40%) (50%)


