Л__ж_п_3.ppt
- Количество слайдов: 27

Лекция 3 Микрогетерогенные и грубодисперсные системы. Мицеллы коллоидных ПАВ. 1
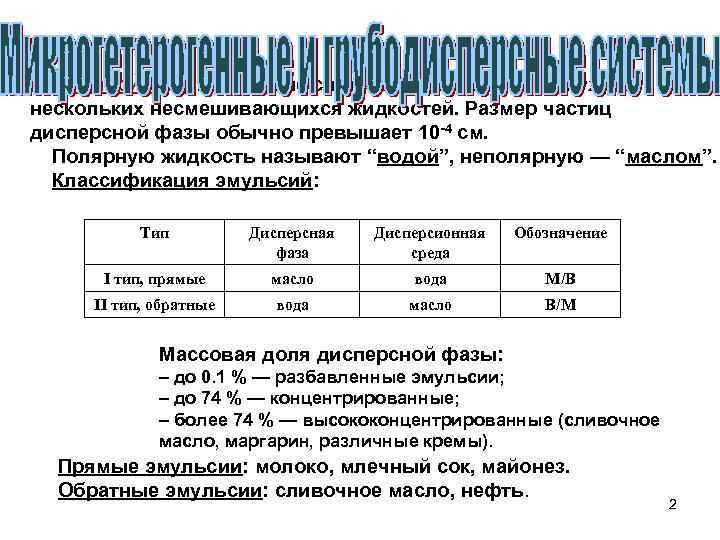
Эмульсии — дисперсные системы, состоящие из двух или нескольких несмешивающихся жидкостей. Размер частиц дисперсной фазы обычно превышает 10 4 см. Полярную жидкость называют “водой”, неполярную — “маслом”. Классификация эмульсий: Тип Дисперсная фаза Дисперсионная среда Обозначение I тип, прямые масло вода М/В II тип, обратные вода масло В/М Массовая доля дисперсной фазы: – до 0. 1 % — разбавленные эмульсии; – до 74 % — концентрированные; – более 74 % — высококонцентрированные (сливочное масло, маргарин, различные кремы). Прямые эмульсии: молоко, млечный сок, майонез. Обратные эмульсии: сливочное масло, нефть. 2

Эмульсии могут быть относительно устойчивыми только в присутствии стабилизаторов: ПАВ, порошков, ВМС (эмульгаторов). По сравнению с золями эмульсии менее устойчивы. На границе раздела жидкость – жидкость электрический поверхностный заряд распределяется диффузно в обеих жидкий фазах; это приводит к значительному снижению электростатического отталкивания. Агрегативная неустойчивость эмульсий проявляется в самопроизвольном слиянии капель дисперсной фазы – коалесценции. Этот процесс приводит к разрушени эмульсии и разделению ее на два жидких слоя. Оценки относительной устойчивости эмульсий: 1) Время жизни отдельной капли в контакте с другими каплями. 2) Скорость расслоения эмульсий на фазы: через 5 секунд высота столба отслоившейся фазы 2. 5 см, тогда скорость расслоения фаз U = 2. 5 / 5 = 0. 5 см/с. 3) “Время жизни” эмульсий: высота столба эмульсии 20 см, U = 0. 5 см/с; время жизни эмульсии τ = 20 / 0. 5 = 40 с. 3

Стабилизация эмульсий поверхностно активными веществами Схемы стабилизации: а) эмульсии масла в воде олеатом натрия С 17 Н 33 СООNa и б) эмульсии воды в масле олеатом кальция (С 17 Н 33 СОО)2 Са. а) Факторы устойчивости: электростатический, адсорбционно сольватный, структурно механический (ионогенные, растворимые в воде ПАВ). б) Факторы устойчивости: адсорбционно сольватный, структурно механический, энтропийный (неионогенные, труднорастворимые ПАВ). 4
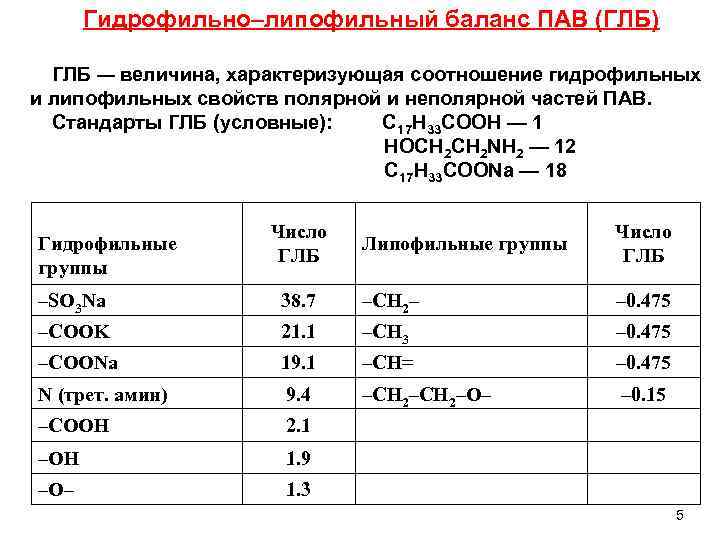
Гидрофильно–липофильный баланс ПАВ (ГЛБ) ГЛБ — величина, характеризующая соотношение гидрофильных и липофильных свойств полярной и неполярной частей ПАВ. Стандарты ГЛБ (условные): С 17 Н 33 СООН — 1 HOCH 2 NH 2 — 12 C 17 H 33 COONa — 18 Гидрофильные группы Число ГЛБ Липофильные группы Число ГЛБ –SO 3 Na 38. 7 –CH 2– – 0. 475 –COOK 21. 1 –CH 3 – 0. 475 –COONa 19. 1 –CH= – 0. 475 N (трет. амин) 9. 4 –CH 2–O– – 0. 15 –COOH 2. 1 –OH 1. 9 –O– 1. 3 5

Показатель ГЛБ является аддитивным; ГЛБ ПАВ определяют как алгебраическую сумму групповых чисел по следующей формуле: ГЛБ ПАВ = 7 + ГЛБ гидроф + ГЛБ липоф Эмульгаторы с ГЛБ от 8 до 20 дают прямые эмульсии, с ГЛБ от 3 до 6 обратные. При полной сбалансированности гидрофильности и липофильности эмульгатора (ГЛБ = 7) образуются множественные эмульсии, совмещающие типы В/М и М/В. ПАВ с ГЛБ меньшим 3 не являются эмульгаторами. Обращение фаз эмульсий При изменении характера эмульгатора прямая эмульсия может превратиться в обратную. Если в эмульсию, стабилизированную С 17 Н 33 СООК добавить Ca. Cl 2, то в результате реакции эмульгатор с ГЛБ = 20, превратится в эмульгатор с ГЛБ = 4. 3, в следствие чего происходит обращение фаз. 2 С 17 Н 33 СООК + Са. Сl 2 → (C 17 H 33 COO)2 Ca + 2 KCl 6

Стабилизация эмульсий порошками и ВМС Схемы стабилизации порошками: а) эмульсии М/В гидрофильным порошком и б) эмульсии В/М гидрофобным порошком Порошки с гидрофильными свойствами (глина, мел) стабилизируют прямые эмульсии. Гидрофобные порошки (сажа, гидрофобизированный силикагель) стабилизируют обратные эмульсии. При стабилизации порошками действует структурно механический фактор устойчивости. Особо сильным стабилизирующим действием по отношению к эмульсиям обладают высокомолекулярные соединения, например, белки и углеводы. Адсорбируясь на поверхности капель дисперсной фазы, они образуют гидратированные и структурированные пленки, что является мощным структурно механическим фактором устойчивости эмульсий. 7
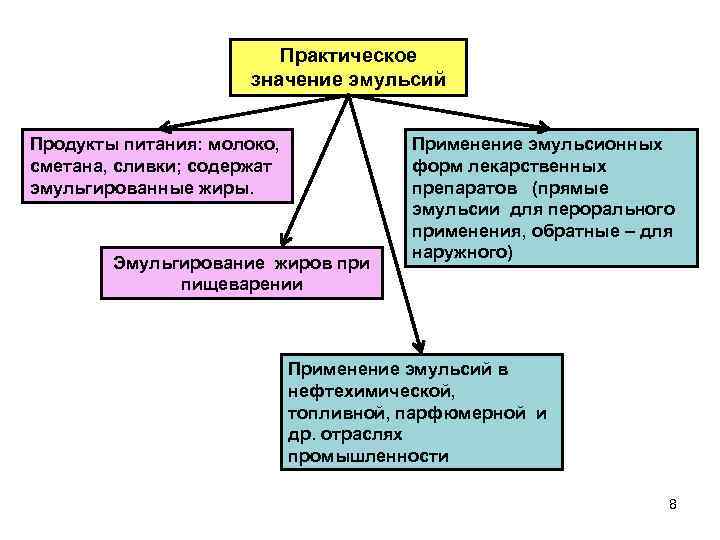
Практическое значение эмульсий Продукты питания: молоко, сметана, сливки; содержат эмульгированные жиры. Эмульгирование жиров при пищеварении Применение эмульсионных форм лекарственных препаратов (прямые эмульсии для перорального применения, обратные – для наружного) Применение эмульсий в нефтехимической, топливной, парфюмерной и др. отраслях промышленности 8

Пены это высококонцентрированные дисперсные системы с газовой дисперсной фазой и жидкой или твердой дисперсионной средой (мыльная пена, хлеб, пемза, пенопласт). В пене пузырьки газа плотно прижаты друг к другу и разделены пенными пленками. Пены относятся к грубодисперсным системам и обладают очень большой полидисперсностью. Из всех дисперсных систем с жидкой дисперсионной средой пены – самые неустойчивые. Время их жизни определяется временем существования пленки жидкости. Пены могут быть устойчивы только в присутствии стабилизаторов: ПАВ, белков и других ВМС (пенообразователей). Стабилизаторы обеспечивают либо электростатический фактор (ионогенные ПАВ), либо структурно механический фактор устойчивости (неионогенные ПАВ, белки). Возникающее расклинивающее давление препятствует разрыву пленок. 9

Характеристики пен: – устойчивость пен — время, в течение которого объем пены уменьшается вдвое (τ1/2); – кратность пен — отношение объема пены к объему жидкости, из которой она образовалась (β). Например, если из 15 мл раствора олеата калия образовалась пена, имеющая вместе с 10 мл оставшейся жидкости объем 50 мл, то ее кратность будет равна 50─10 ____ β = 15─10 = 8 10
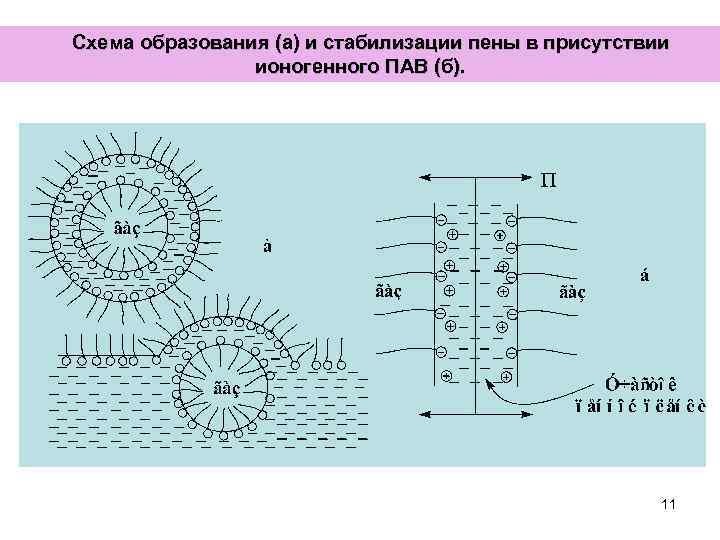
Схема образования (а) и стабилизации пены в присутствии ионогенного ПАВ (б). 11
Флотационные Мыльные Пены Противопожарные Пена, элементарной ячейкой которой является мыльный пузырь, находит все новые сферы практического применения. Лечебные «Мыльный пузырь не исчерпал себя и по сей день» П. А. Ребиндер Нежелательное пенообразование имеет место при травмах грудной клетки. В ходе операции пену разрушают механическим путем с помощью тампонов и электроотсоса. Образование пены наблюдается при развитии отека легких. Пена вызывает обструкцию альвеол , бронхиол и острую дыхательную недостаточность. Для гашения пены в легких используется аэрозольная ингаляция или внутривенное введение 30% го этилового спирта. 12

Аэрозоли — это дисперсные системы с газообразной дисперсионной средой и жидкой (туманы) или твердой (пыли, дымы) дисперсной фазой. Аэрозоли охватывают большой диапазон дисперсности – от 10 2 до 10 6 см, т. е. они могут существовать как в виде микрогетерогенных и грубодисперсных, так и в виде ультрамикрогетерогенных систем. Аэрозоли характеризуются высокой седиментационной и агрегативной неустойчивостью. Это обусловлено малой плотностью газовой среды и слабым взаимодействием ее с дисперсной фазой. В аэрозолях не могут возникнуть термодинамические факторы устойчивости, так как газовая дисперсионная среда не в состоянии создать поверхностный слой, снижающий поверхностное натяжение, или образовать двойной электрический слой. 13
Источники атмосферных аэрозолей Образование естественным путем: за счет ветровой эрозии почвы, генерации животными и растениями, извержения вулканов, испарения с поверхности воды, поступлений из космоса. Образование искусственным путем: промышленные процессы, транспорт, технологические и аварийные выбросы, взрывы. Заболевания – антракоз, силикоз, эндогенный гемосидероз и др. Использование аэрозолей Аэрозоли применяются во многих технологических процессах (горение топлива, сушка, интенсификация процессов окисления и восстановления, орошение посевов и пр. ), в промышленности, в медицине (аэрозольтерапия). 14

Разрушение эмульсий, пен и аэрозолей Химические методы: введение в эмульсии и пены минеральных кислот или солей с многозарядными катионами, высших спиртов, органических кислот, кремнийорганических или фосфорорганических соединений, органических растворителей. Физические методы: повышение температуры, центрифугирование, фильтрование через пористые материалы, не смачивающиеся дисперсной фазой, разбивание пен при помощи мешалок, действие ультразвука (для разрушения эмульсий и пен). Для разрушения аэрозолей используют электрофильтры, пылевые камеры, конденсация паров воды в среде аэрозоля. 15

Порошки и суспензии Порошки можно рассматривать как осажденные аэрозоли. В зависимости от размеров частиц для порошков приняты разные названия. Порошки с частицами от 10 1 до 10 3 см называют песками. Порошок с частицами от 10 3 до 10 4 см носит название пыль, а более мелкие порошки называют пудрой. Характерными свойствами порошков является текучесть (сыпучесть) и слеживаемость. Суспензии — грубодисперсные системы с твердой дисперсной фазой и жидкой дисперсионной средой. Суспензии имеют ряд общих свойств с порошками, эти системы подобны по дисперсности. Если порошок поместить в жидкость и перемешать, то получится суспензия, а при высушивании суспензии она снова превращается в порошок. В зависимости от дисперсности твердой фазы суспензии подразделяют на грубые (размер частиц более 10– 3 см) и тонкие (размер частиц от 10– 3 до 10– 5 см). Суспензии с вязкой дисперсионной средой в фармакологии называют мазями, а с высоким содержанием дисперсной фазы — пастами. Суспензии характеризуются седиментационной неустойчивостью. По своим электрическим свойствам (возникновение ДЭС), агрегативной устойчивости и способности к электролитной коагуляции они имеют 16 много общего с золями.

Коллоидные ПАВ — длинноцепочечные дифильные органические соединения с числом атомов углерода в радикале от 10 до 20. Классификация коллоидных ПАВ Ионогеннные: — анионные (поверхностно активный анион): C 17 H 33 COONa, C 8 H 17 C 6 H 4 SO 3 Na; — катионные (поверхностно активный анион): [C 18 H 37 NH 3]Cl, ; — амфолитные: NH 2(CH 2)12 COOH, в зависимости от р. Н среды либо анион–, либо катион–активные. Неионогенные: R С 6 Н 4 О (CH 2 О)n. Н, где R от 6 до 18 атомов С, n = 10 – 100. 17
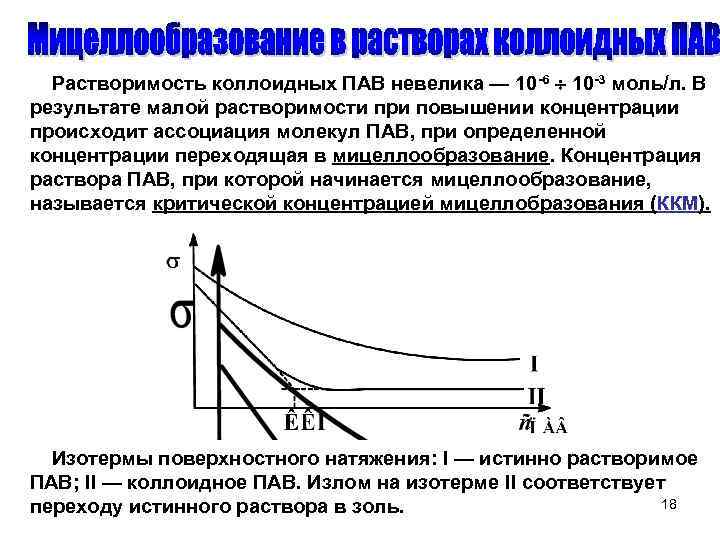
Растворимость коллоидных ПАВ невелика — 10 6 10 3 моль/л. В результате малой растворимости при повышении концентрации происходит ассоциация молекул ПАВ, при определенной концентрации переходящая в мицеллообразование. Концентрация раствора ПАВ, при которой начинается мицеллообразование, называется критической концентрацией мицеллобразования (ККМ). Изотермы поверхностного натяжения: I — истинно растворимое ПАВ; II — коллоидное ПАВ. Излом на изотерме II соответствует 18 переходу истинного раствора в золь.
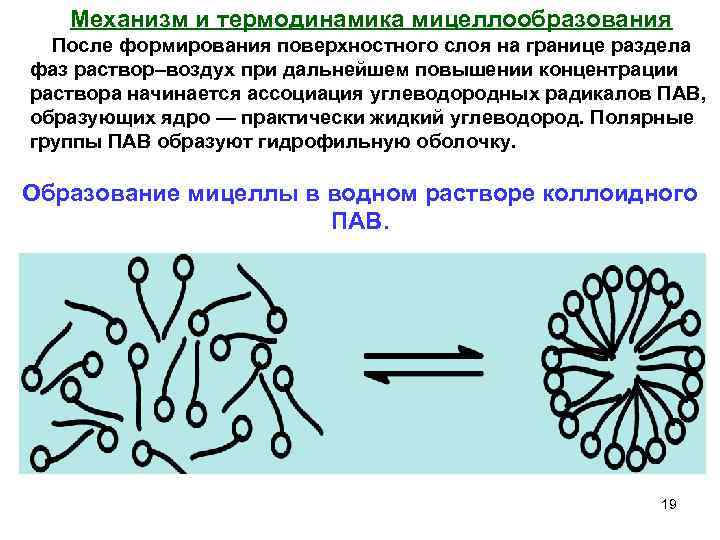
Механизм и термодинамика мицеллообразования После формирования поверхностного слоя на границе раздела фаз раствор–воздух при дальнейшем повышении концентрации раствора начинается ассоциация углеводородных радикалов ПАВ, образующих ядро — практически жидкий углеводород. Полярные группы ПАВ образуют гидрофильную оболочку. Образование мицеллы в водном растворе коллоидного ПАВ. 19

Движущая сила образования мицеллы — гидрофобные взаимодействия. Энтальпия взаимодействия радикалов ПАВ между собой меньше энтальпии взаимодействия их с водой, поэтому при образовании ядра мицеллы энтальпия системы уменьшается ( Н < 0). Вокруг радикалов ПАВ, находящихся в неассоциированном состоянии, образуются упорядоченные структуры из молекул воды. При ассоциации радикалов ПАВ эти структуры разрушаются, энтропия системы повышается ( S >0). Энергия Гиббса системы G = H T S при этом уменьшается ( G < 0), следовательно, мицеллообразование термодинамически выгодно и идет самопроизвольно. G на 1 моль групп –СН 2– составляет примерно 2600 Дж/моль. Строение мицелл коллоидных ПАВ в водных растворах При концентрациях ПАВ, несколько превышающих ККМ, образуются сферические мицеллы с определенным числом агрегации (от 20 до 100), которое зависит от длины радикала и способности полярной части молекул образовывать гидрофильную оболочку мицеллы. Диаметр сферических мицелл примерно равен удвоенной длине молекул ПАВ. При дальнейшем увеличении концентрации ПАВ выше ККМ мицеллярная система проходит ряд равновесных состояний, характеризуемых определенным числом агрегации и формой мицелл. 20
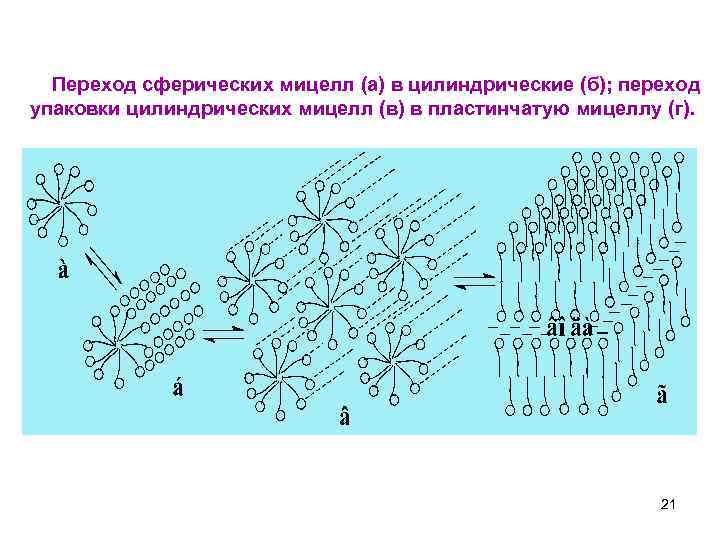
Переход сферических мицелл (а) в цилиндрические (б); переход упаковки цилиндрических мицелл (в) в пластинчатую мицеллу (г). 21
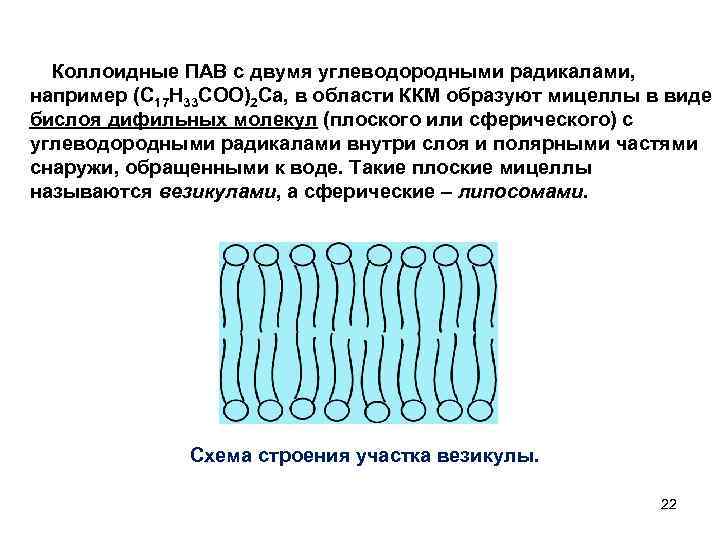
Коллоидные ПАВ с двумя углеводородными радикалами, например (С 17 Н 33 СОО)2 Са, в области ККМ образуют мицеллы в виде бислоя дифильных молекул (плоского или сферического) с углеводородными радикалами внутри слоя и полярными частями снаружи, обращенными к воде. Такие плоские мицеллы называются везикулами, а сферические – липосомами. Схема строения участка везикулы. 22
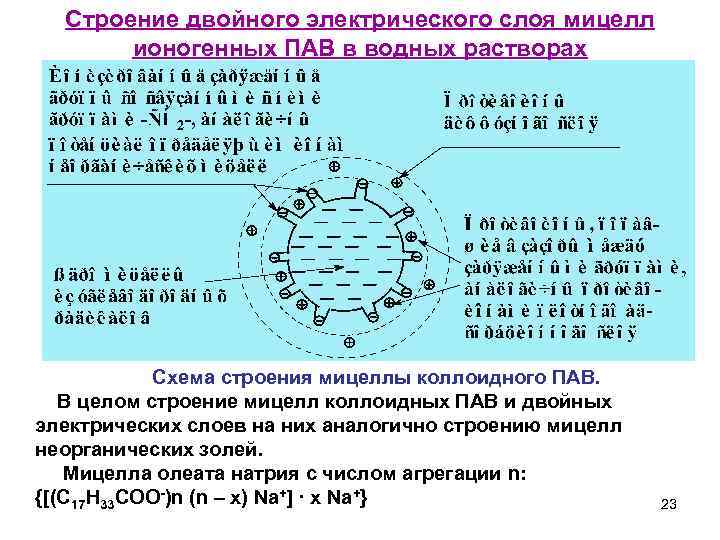
Строение двойного электрического слоя мицелл ионогенных ПАВ в водных растворах Схема строения мицеллы коллоидного ПАВ. В целом строение мицелл коллоидных ПАВ и двойных электрических слоев на них аналогично строению мицелл неорганических золей. Мицелла олеата натрия с числом агрегации n: {[(C 17 H 33 COO )n (n – x) Na+] ∙ x Na+} 23

Солюбилизация в растворах коллоидных ПАВ Солюбилизацией называется явление растворения веществ в мицеллах ПАВ. В водных мицеллярных растворах ПАВ солюбилизируются вещества, практически нерастворимые в воде, например, гептан, бензол, красители, жиры. Это обусловлено тем, что вводимые в раствор ПАВ вещества включаются в состав мицелл. Они растворяются в ядрах мицелл, обладающих свойствами неполярных жидкостей углеводородов. Вещество, растворяющееся в мицеллах — солюбилизат. Способ включения веществ в мицеллу зависит от природы солюбилизата. 24
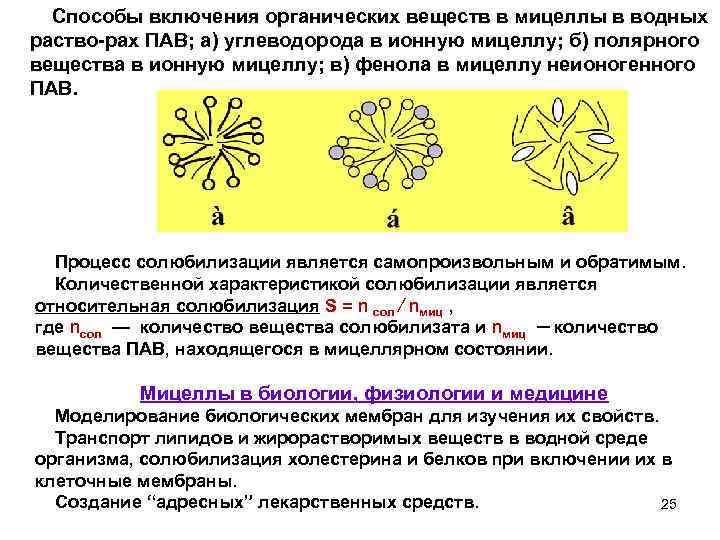
Способы включения органических веществ в мицеллы в водных раство рах ПАВ; а) углеводорода в ионную мицеллу; б) полярного вещества в ионную мицеллу; в) фенола в мицеллу неионогенного ПАВ. Процесс солюбилизации является самопроизвольным и обратимым. Количественной характеристикой солюбилизации является относительная солюбилизация S = n сол ⁄ nмиц , где nсол — количество вещества солюбилизата и nмиц ─ количество вещества ПАВ, находящегося в мицеллярном состоянии. Мицеллы в биологии, физиологии и медицине Моделирование биологических мембран для изучения их свойств. Транспорт липидов и жирорастворимых веществ в водной среде организма, солюбилизация холестерина и белков при включении их в клеточные мембраны. Создание “адресных” лекарственных средств. 25
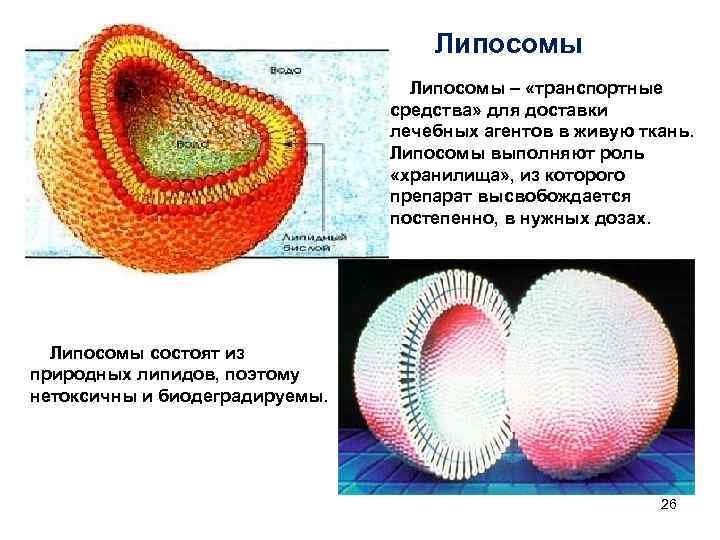
Липосомы – «транспортные средства» для доставки лечебных агентов в живую ткань. Липосомы выполняют роль «хранилища» , из которого препарат высвобождается постепенно, в нужных дозах. Липосомы состоят из природных липидов, поэтому нетоксичны и биодеградируемы. 26
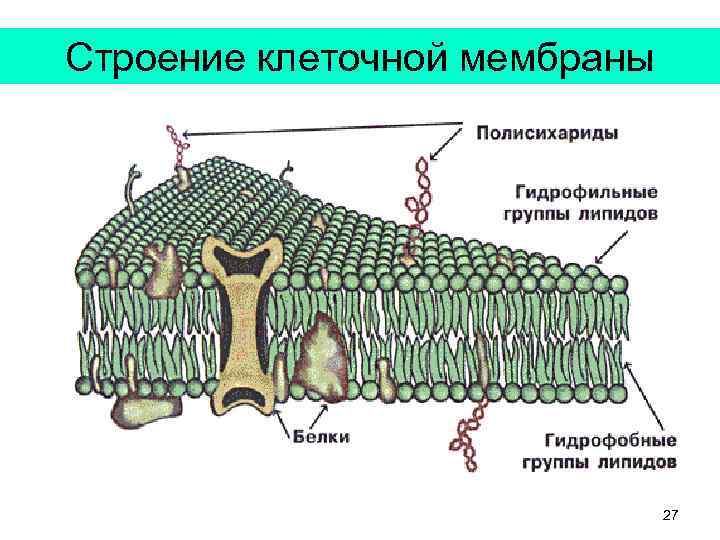
Строение клеточной мембраны 27
Л__ж_п_3.ppt