Лекция 3.pptx
- Количество слайдов: 44

Лекция 3 МЕТОДЫ ГЕНЕТИЧЕСКОГО ОБСЛЕДОВАНИЯ ЧЕЛОВЕКА

Основными методами генетического обследования человека являются: • Клинико-генеалогический; • Цитогенетический; • Молекулярно-цитогенетический; • Биохимические; • Дерматоглифический; • Микробиологические; • Инструментальные; • Популяционно-статистические; • Близнецовые.

КЛИНИКО-ГЕНЕАЛОГИЧЕСКИЙ МЕТОД Главный метод в медицинской генетике. Большинство диагнозов наследственной патологии можно установить с помощью этого метода анализа. Он требует полного и внимательного обследования больного, целенаправленного сбора анамнеза (о репродуктивной функции и наличии аналогичных поражений среди членов ядерной семьи в ряду поколений по материнской и отцовской линиям), а также клинического обследования и интервьюирования всех возможных родственников этого пробанда.

Исследования состояния внутренних органов традиционными методами пальпации, перкуссии и аускультации завершают клиническое обследование больного. При сборе анамнеза принципиальное значение имеют сведения о течении беременности, срок родов, масса и длина ребенка при рождении, акушерскогинекологический анамнез матери и семьи. Опрос и клиническое обследование как можно большего количества родственников пробанда имеет целью выявление носителей патологических генов как рецессивных, так и доминантных, а также сцепленных с полом. Рецессивные аллели клинически проявляются только в гомозиготном состоянии (имеет значение кровное родство родителей), доминантные — как в гомозиготном, так и в гетерозиготном наборе.
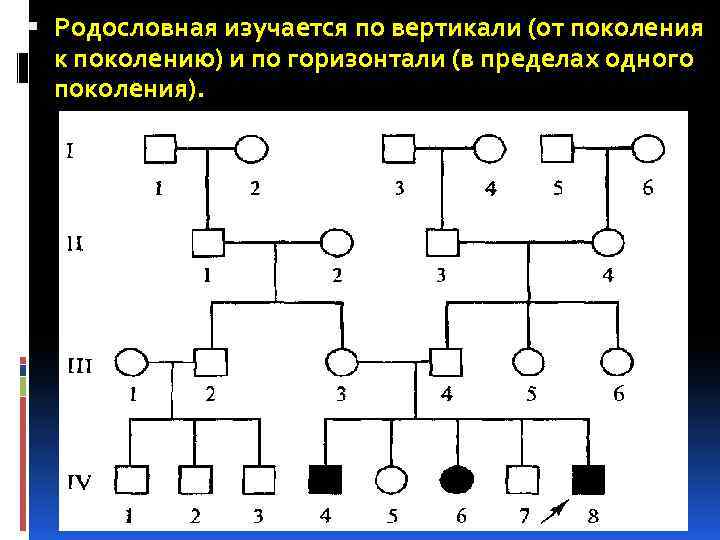
Родословная изучается по вертикали (от поколения к поколению) и по горизонтали (в пределах одного поколения).

В медицинской генетике термин экспрессивность используется относительно полноты выявления синдрома, а не только определенного симптома, потому что, именно синдром, а не симптом является последствием одной мутации (при менделевском наследовании). Нередко экспрессивность моногенного синдрома зависит от пола пробанда. Результатом клинико-генеалогического обследования семьи является описание фенотипа, родословная, определение типа наследования патологии и предварительный диагноз. Во время составления родословной используются графические символы, поколения обозначаются римскими цифрами, начиная с поколения пробанда (О), а каждый человек в одном поколении — арабскими цифрами. Пробанд (лицо, которое обратилось к врачу) обозначается стрелкой. Таким образом, каждый человек в родословной имеет свой номер и отношение к определенному поколению.

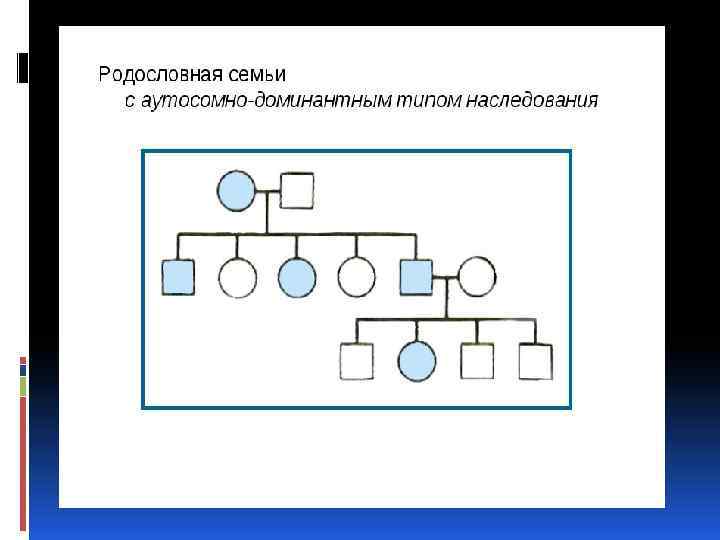

На основе медицинского заключения вырисовывается фенотип пробанда по особой схеме, которая отличается от записи в истории болезни, сделанной врачом не генетиком. Фенотип — совокупность внешних и внутренних признаков организма, приобретённых в результате онтогенеза (индивидуального развития). Описание фенотипа начинается с оценки поведения, физического развития (рост, масса тела), контактности больного, его психического состояния и умственного развития в зависимости от возраста.

Врач обращает внимание и отмечает особенности внешности пробанда: форма черепа, рост волос, его структура и размещение; форма и расположение ушных раковин (насечки на мочке уха), бровей, глазных щелей и расстояние между ними. Необходимо описать форму лба, носа, ротовой полости, губ, языка, нижней и верхней челюсти; наличие, количество, особенности формы и роста зубов; твердое небо, расщелина губы и/или неба; форму и размеры шеи, грудной клетки, позвоночника. Необходимо также детально обследовать верхние и нижние конечности, описать их форму, количество пальцев, дерматоглифические особенности (рисунки) ладоней и подошв, позиции ладони, подошв.

Поэтому внимание врача уделяется состоянию кожи, отмечается ее эластичность (или наоборот), рост волос, влажность, пигментация, наличие атипичных складок высыпания.

Все отмеченные симптомы соответственно записывается специальными терминами: акроцефалия (крутая голова, напоминающая башню), алопеция (отсутствие волос, облысение), ангиоматоз (патологическое состояние сосудов с формированием ангиом), сосками), диастема (широкое расстояние между передними зубами), макросомия (гигантизм), микрогнатия (недоразвитие верхней челюсти), микроцефалия (аномальное уменьшение головы), полифагия (повышенный аппетит). аниридия (отсутствие радужной оболочки), аплазия (врожденное отсутствие органа), брахицефалия (увеличение поперечного размера головы), гипертелоризм (аномальное расстояние между парными органами — глазами, грудными Возможность установить точный диагноз в большей степени зависит от того, насколько полно выявлены микроаномалии развития, на которые врачи, как правило, не обращают надлежащего внимания.
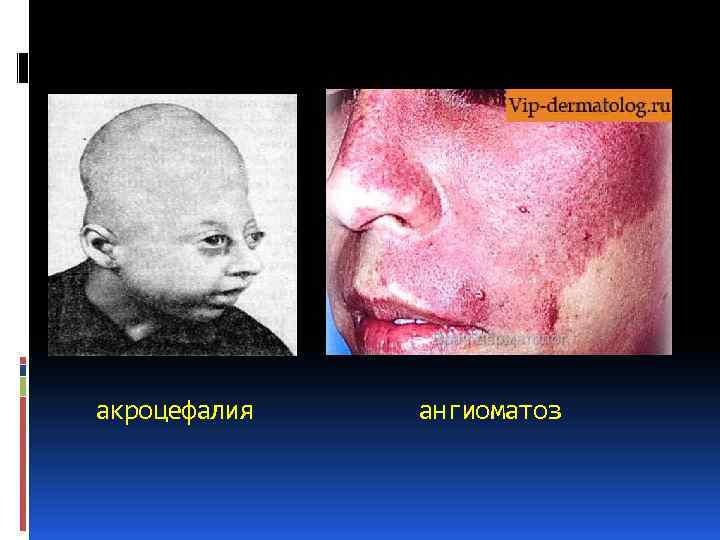
акроцефалия ангиоматоз
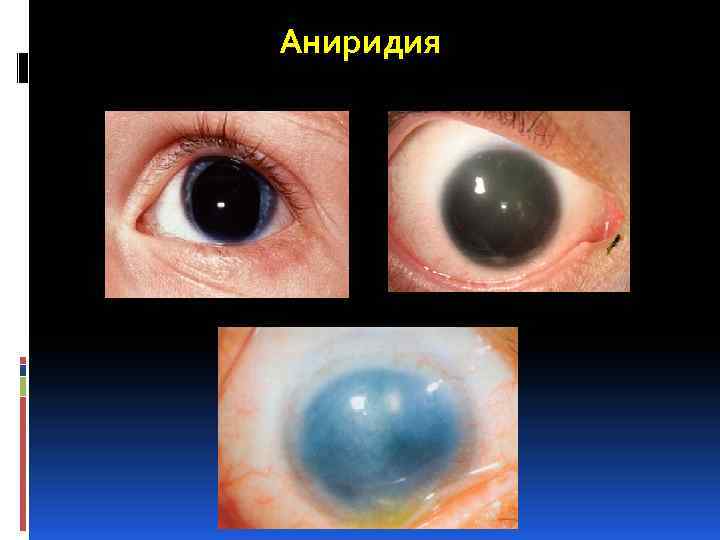
Аниридия
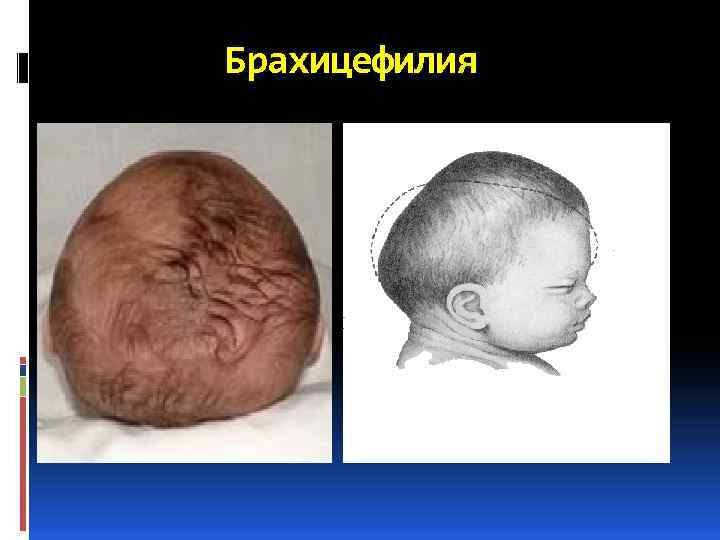
Брахицефилия
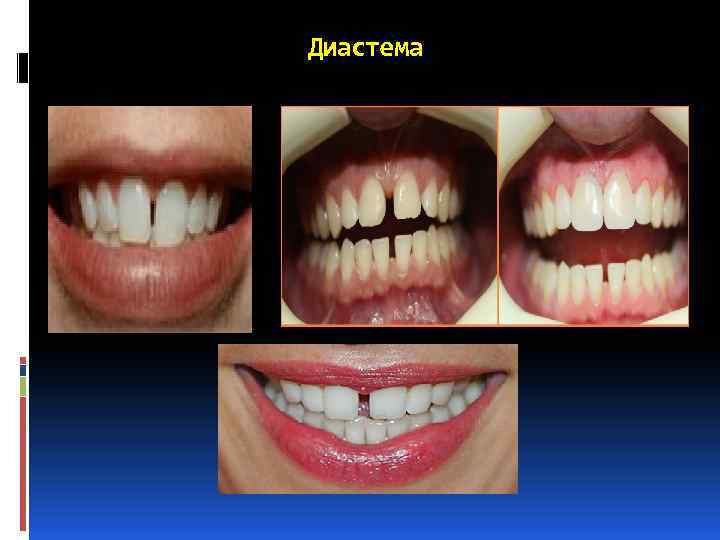
Диастема
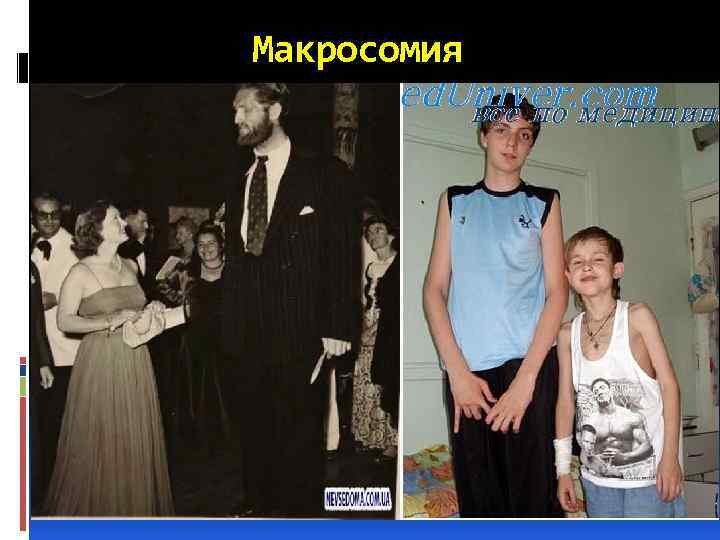
Макросомия
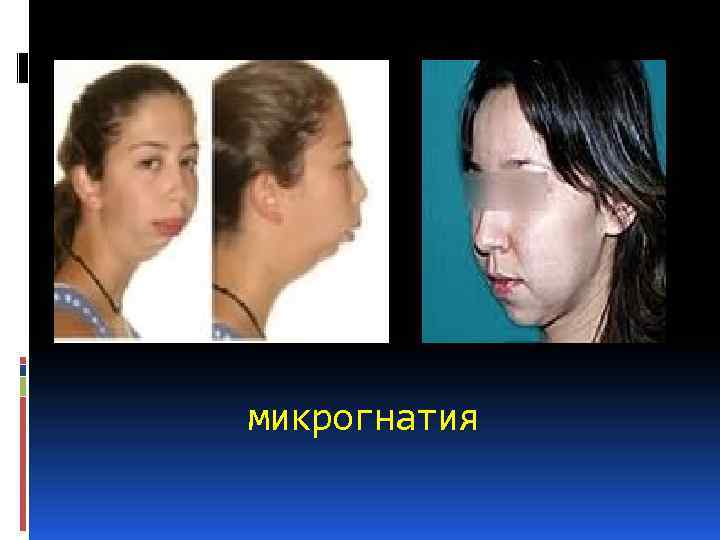
микрогнатия
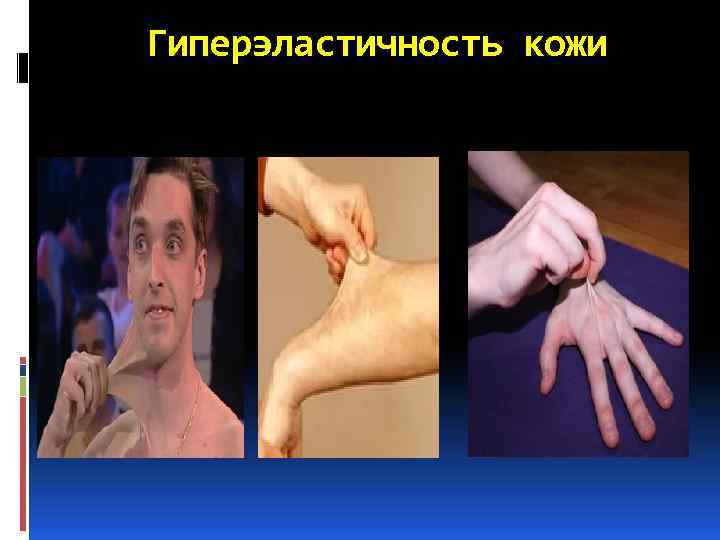
Гиперэластичность кожи
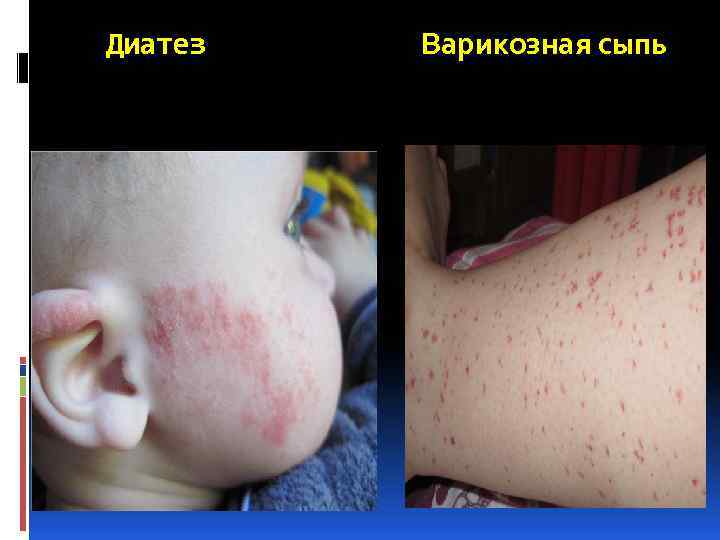
Диатез Варикозная сыпь

Микроцефалия

Следует помнить о том, что наличие и степень выраженности клинической симптоматики зависит от пенетрантности и экспрессивности определенного гена. Пенетрантность — частота или вероятность проявления любого доминантного гена, она обозначается процентным отношением количества лиц, у которых ген проявляется в фенотипе, ко всем носителям этого гена. Экспрессивность — степень фенотипического проявления гена, мера силы гена, который определяется степенью развития признака.

2 этапа медико-генетического обследования После установления на 1 этапе предварительного диагноза (на основе клинико-генеалогического анализа) необходимо провести дифференцированную диагностику с подобными по клинике синдромами, генокопиями и фенотипическими проявлениями этой патологии, с целью верификации диагноза. Необходимы консультации специалистов различных специальностей: офтальмолога, невропатолога, психиатра, кардиолога, ортопеда и других, состав которых определяется в каждом конкретном случае.

Второй этап медико-генетического обследования подразумевает назначение пробанду и членам его семьи лабораторных и аппаратных исследований: рентгенографии черепа, конечностей, позвоночника (установление костного возраста, выявление аномалий); ультразвукового исследования; общих анализов крови и мочи; функциональное и лабораторное обследование сердечнососудистой, пищеварительной, дыхательной, иммунной, эндокринной, мочеполовой и центральной нервной систем. Необходимо помнить, что комплекс этих обследований в каждом конкретном случае основывается на конкретных гипотезах относительно диагноза, наличия или отсутствия изменений, которые характерны для предполагаемой патологии. В некоторых случаях решающим может быть результат анализа эндокринного статуса больного, в других — иммунного статуса или гистологического исследования биоптата. Установить диагноз в семьях, которые ранее имели случаи детской смертности, помогут протоколы вскрытия.

Большинство наследственных синдромов встречается в популяции чрезвычайно редко (1 х103 — 1 х106), поэтому для верификации диагноза необходимо сравнивать каждый конкретный случай, с описанными в литературе (атласы, монографии, каталоги, компьютерные диагностические программы). В случае установления наследственной патологии точность диагностики определяет не только выбор правильной тактики лечения больного, прогноз его жизни и течения заболевания, но и успешность медико-генетического консультирования как больного (формирование адаптивной среды, выбор профессии, супружеской пары, прогноз деторождения), так и его членов семьи (своевременное выявление пораженных индивидов, преконцепционная профилактика, степень риска рождения больных детей).

Следовательно, диагностика наследственных болезней, успешность их лечения и профилактики зависит в большей степени от компетентности врача, владения им генетическим мышлением, чем от наличия дорогостоящей аппаратуры, реактивов и специализированных учреждений.

Лабораторные медико-генетические методы обследования имеют высокую чувствительность, что позволяет однозначно определить диагноз, характер и локализацию наследственного дефекта на уровне продукта гена, мутации в гене, хромосоме, геноме. Эти методы незаменимы при массовых скринингах патологии, пренатальной инвазивной диагностике, выявлении носителя патологического аллеля, установлении спорного отцовства, доклинической диагностике патологии.

Цитогенетический метод Позволяет исследовать количество и качество структуры хромосом, выявление хромосомной патологии, мозаицизма, установления носителей сбалансированной хромосомной аномалии.

Проведение цитогенетического анализа базируется на исследовании кариотипа человека. Кариотип — это совокупность морфологических особенностей полного хромосомного набора, типичного для клеток представителя данного биологического вида. Специфичность кариотипа определяется общим числом хромосом, их размером и формой, а числовая и структурная стабильность хромосом является наиболее важным условием формирования фенотипически нормального организма в процессе индивидуального развития.

Цель хромосомного анализа в клинической цитогенетике — оценка кариотипа с выявлением возможных количественных или структурных аномалий хромосом путем анализа метафазных или прометафазных препаратов хромосом и правильной записи и символизации. Эта система базируется на морфологических характеристиках хромосом, которые включают данные о размере хромосомы и положению центромеры. Согласно этих положений, хромосомы систематизируются по группам, которые обозначаются большими буквами английского алфавита от А до G, в порядке их длины. Заметный вклад в разработку этих методов внес отечественный ученый А. Ф. Захаров.

НЕПРЯМЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ПРЕПАРАТОВ ХРОМОСОМ Культивирование лимфоцитов периферической крови и технология приготовления хромосомных препаратов Материал: 1 -2 мл периферической крови человека; Оборудование, посуда: Ламинарный бокс; термостат, выставленный на t+370 C; весы; центрифуга для центрифужных пробирок на 1000 оборотов в минуту; флаконы одноразовые или шприцы для забора крови; флаконы для культивирования (пенициллиновые флаконы с резиновой пробкой); шприцы одноразовые на 1 мл для забора крови и 5 мл для внесения культурной среды во флаконы; шприцы одноразовые на 1 мл для забора ФГА; центрифужные пробирки; штативы; стаканчики для растворов Na. Cl и фиксатора; пипетка для раскатывания культуры; предметное стекло с полем и др. Реактивы, растворы: раствор гепарина, разведенный 0, 9% р-ром Na. Cl (1: 10); питательная среда (RPMI, 199, DMEM, F 10 разных производителей, прежде всего «Gibco» , «Sigma» , «Merk» , «Fluka» , «Панэко» ; сыворотка эмбриональная; фитогемагглютинин (ФГА) разных производителей ( «Gibco» , «Sigma» , «Merk» , «Fluka» , «Панэко» ); колхицин; раствор KCl; спирт метиловый или этиловый; ледяная уксусная кислота.

Техника метода: Постановка культуры: разлить во флаконы 5 мл питательной среды по 2 флакона на каждого пациента, добавить во флаконы по 0, 5 мл сыворотки и 0, 1 мл ФГА, затем добавить по 0, 5 мл крови и осторожно перемешать. Поместить флаконы в термостат при t+370 C, на 70 часу культивирования в каждый флакон добавить по 0, 3 мл раствора колхицина (в конечной концентрации 10 мк/мл) за 2 – 2, 5 часа до снятия культуры. Снятие культуры. Отцентрифугировать пробирки в течение 5 -7 минут, слить надосадочную жидкость, хорошо взболтать осадок, добавить р-р гипотонического раствора, предварительно подогретый до t+370 C; экспозиция в гипотоническом р-ре – 7 минут, затем снова отцентрифугировать пробирки 10 минут, слить надосадочную жидкость, размешать и добавить фиксирующую смесь на 30 минут, отцентрифугировать в течение 10 минут и эту процедуру повторить 3 раза, пока смесь не станет прозрачной. Раскапывание. Клеточную суспензию раскапывают дозатором (на высоте поднятой вверх руки) на мокрые охлажденные предметные стекла и высушивают над пламенем горелки.

ПРЯМЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ПРЕПАРАТОВ ХРОМОСОМ • Приготовление препаратов из костного мозга, биоптата ворсиночного хориона без культивирования. Материал, оборудование, посуда, реактивы и растворы – те же, что изложены выше. Техника метода заключается в следующем: поместить биоптат ворсиночного хориона во флаконе с культуральной смесью и колхицином (в концентрации 1 -5 мкг/мл) в термостат при t+370 C на 2 -2, 5 часа. Биоптат поместить в чашку Петри через 2 -2, 5 часа, слить культуральную смесь и провести процедуры гипотенизации и фиксации, аналогично приведенным выше, только экспозиция в фиксирующей смеси не 18 часов, а 20 минут, если результат необходимо получить через 24 часа.

Q-метод Позволяет идентифицировать индивидуальные хромосомы, выявлять структурные аномалии проведении пре- и постнатальной диагностики, выявить полиморфизм в перицентромерных районах хромосом 3 и 4, перицентромерных районах и сателлитах акроцентрических хромосом (13 -15 и 21 -22) и в дистальном отделе длинного плеча хромосомы Y.
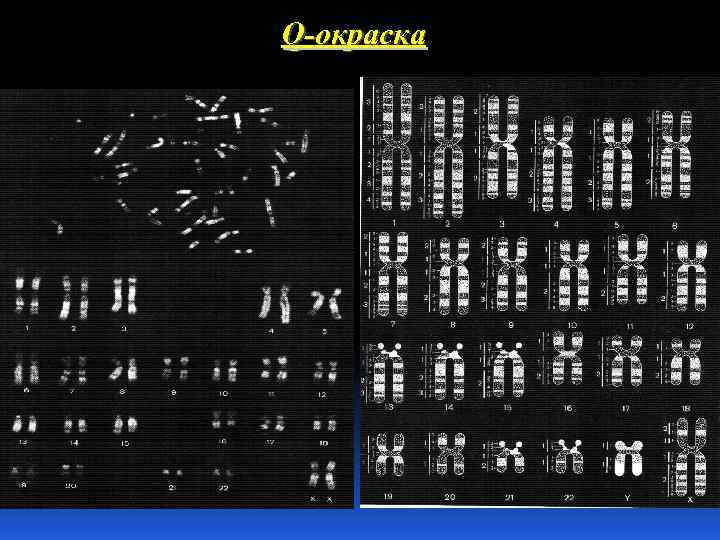
Q-окраска

G-метод Используется для идентификации индивидуальных хромосом и выявления структурных аномалий хромосом во всех медицинских учреждениях до настоящего времени, характер сегментации при G-методе подобен сегментации при Q-методе.

G-окраска

R-метод Позволяет визуализировать терминальные районы хромосом и R-позитивные сегменты, которые вовлечены в перестройку хромосом.

R-метод

С-метод Позволяет окрашивать центромерный район во всех хромосомах и гетерохроматин вторичных околоцентромерных перетяжек в хромосомах 1, 9, 16, гетерохроматин коротких плеч акроцентрических хромосом и длинного плеча хромосомы Y.

С-метод Используется для определения дицентрических хромосом, помогает идентифицировать некоторые прицентромерные инверсии, прицентромерный гетерохроматин в маркерных хромосомах, наличие Yхромосомы в кариотипе.
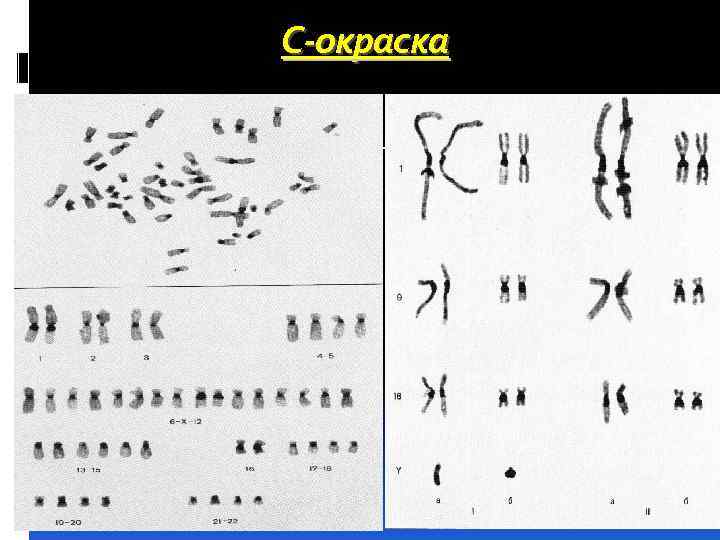
С-окраска

ОСНОВНЫЕ ПРИНЦИПЫ ОБОЗНАЧЕНИЯ НОРМАЛЬНОГО И АНОМАЛЬНОГО КАРИОТИПА:
![[ ] cen cgh chi chr cht del de novo dic dmin dup end [ ] cen cgh chi chr cht del de novo dic dmin dup end](https://present5.com/presentation/-58112762_442822702/image-44.jpg)
[ ] cen cgh chi chr cht del de novo dic dmin dup end fem fis fra g h i ins inv - скобки для обозначения количества хромосом центромера сравнительная геномная гибридизация химера хромосома хроматида делеция аномалия, возникшая впервые дицентрик парный фрагмент дупликация эндоредупликация женский пол расхождение центромер ломкий сайт пробел конститутивный гетерохроматин изохромосома инсерция инверсия
Лекция 3.pptx