Минералогия_лекция_3.ppt
- Количество слайдов: 18
 Лекция 3 КОНСТИТУЦИЯ МИНЕРАЛОВ Радиусы атомов и ионов в кристаллах
Лекция 3 КОНСТИТУЦИЯ МИНЕРАЛОВ Радиусы атомов и ионов в кристаллах
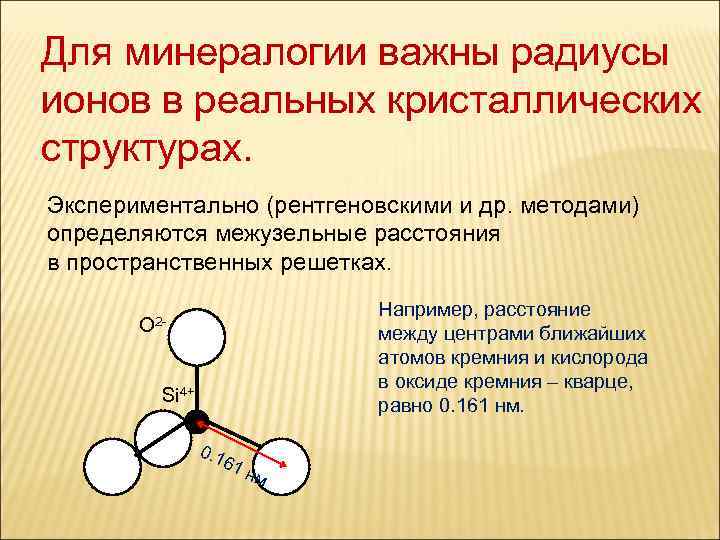 Для минералогии важны радиусы ионов в реальных кристаллических структурах. Экспериментально (рентгеновскими и др. методами) определяются межузельные расстояния в пространственных решетках. Например, расстояние между центрами ближайших атомов кремния и кислорода в оксиде кремния – кварце, равно 0. 161 нм. O 2 Si 4+ 0. 1 61 нм
Для минералогии важны радиусы ионов в реальных кристаллических структурах. Экспериментально (рентгеновскими и др. методами) определяются межузельные расстояния в пространственных решетках. Например, расстояние между центрами ближайших атомов кремния и кислорода в оксиде кремния – кварце, равно 0. 161 нм. O 2 Si 4+ 0. 1 61 нм
 Как определить размеры отдельных атомов и ионов в структуре минералов? Первая система радиусов (А. Ланде -1920 г. ) Он измерил межъядерные расстояния (в нм) в некоторых веществах со структурой Na. Cl: Mg-Se (0. 273), Mn-Se (0. 273), Mg-S (0. 260), Mg-O (0. 210), Mn-O (0. 210). Приняв идею о плотнейшей упаковке атомов в кристаллах, на основе простейших расчетов дал значения радиусов (в нм): S 2 - 0. 183, Se 2 - 0. 193, Mg 2+ 0. 076.
Как определить размеры отдельных атомов и ионов в структуре минералов? Первая система радиусов (А. Ланде -1920 г. ) Он измерил межъядерные расстояния (в нм) в некоторых веществах со структурой Na. Cl: Mg-Se (0. 273), Mn-Se (0. 273), Mg-S (0. 260), Mg-O (0. 210), Mn-O (0. 210). Приняв идею о плотнейшей упаковке атомов в кристаллах, на основе простейших расчетов дал значения радиусов (в нм): S 2 - 0. 183, Se 2 - 0. 193, Mg 2+ 0. 076.
 Вторая система радиусов (Вазашерна -1923 г. ) Теоретически рассчитал значения радиусов фтора - 0. 133 нм, и кислорода – 0. 132 нм. Третья система радиусов (В. М. Гольдшмидт -1926 г. ) Он на основе цифр Вазашерна вычислил радиусы всех химических элементов, например: S 2 - 0. 174, Se 2 - 0. 191, O 2 - 0. 132, F- 0. 133, K+ 0. 133, Na+0. 098, Ca 2+0. 106, Mg 2+ 0. 078, Zn 2+0. 083 нм (все значения даны для к. ч. 6). Относительные размеры радиусов и ионов в кристаллических решетках (по Гольдшмидту) Заряд иона 2 O S 1 - 0 1+ 2+ F Ne Na Mg Cl Ar K Ca 3+ Al 4+ Si 5+ P 6+ S Sc Ti V Cr
Вторая система радиусов (Вазашерна -1923 г. ) Теоретически рассчитал значения радиусов фтора - 0. 133 нм, и кислорода – 0. 132 нм. Третья система радиусов (В. М. Гольдшмидт -1926 г. ) Он на основе цифр Вазашерна вычислил радиусы всех химических элементов, например: S 2 - 0. 174, Se 2 - 0. 191, O 2 - 0. 132, F- 0. 133, K+ 0. 133, Na+0. 098, Ca 2+0. 106, Mg 2+ 0. 078, Zn 2+0. 083 нм (все значения даны для к. ч. 6). Относительные размеры радиусов и ионов в кристаллических решетках (по Гольдшмидту) Заряд иона 2 O S 1 - 0 1+ 2+ F Ne Na Mg Cl Ar K Ca 3+ Al 4+ Si 5+ P 6+ S Sc Ti V Cr
 Четвертая система радиусов (Л. Полинг) Определил расстояние F-F = 0. 231 нм (в веществе Na. F) и рассчитал радиус F- - 0. 136 нм, Na+ – 0. 095 нм. S 2 - 0. 184, Se 2 - 0. 198, O 2 - 0. 140, K+ 0. 133, Ca 2+0. 099, Mg 2+ 0. 065, Zn 2+0. 074 нм (все значения даны для к. ч. 6). Пятая система радиусов (В. Брэгг – 1920 г. ) Экспериментально определил межъядерное расстояние S-S = 0. 205 нм (в пирите Fe. S 2) и принял для радиуса S 2 - - 0. 103 нм. Далее он измерил расстояние Zn-S в сфалерите (=0. 235 нм) и Zn-О в цинките (=0. 197 нм). Отсюда: радиус Zn 2+ = 0. 132 нм, О 2 - = 0. 065 нм (т. е. у кислорода в 2 раза меньше, чем по Вазашерну и Гольдшидту, а цинк крупнее).
Четвертая система радиусов (Л. Полинг) Определил расстояние F-F = 0. 231 нм (в веществе Na. F) и рассчитал радиус F- - 0. 136 нм, Na+ – 0. 095 нм. S 2 - 0. 184, Se 2 - 0. 198, O 2 - 0. 140, K+ 0. 133, Ca 2+0. 099, Mg 2+ 0. 065, Zn 2+0. 074 нм (все значения даны для к. ч. 6). Пятая система радиусов (В. Брэгг – 1920 г. ) Экспериментально определил межъядерное расстояние S-S = 0. 205 нм (в пирите Fe. S 2) и принял для радиуса S 2 - - 0. 103 нм. Далее он измерил расстояние Zn-S в сфалерите (=0. 235 нм) и Zn-О в цинките (=0. 197 нм). Отсюда: радиус Zn 2+ = 0. 132 нм, О 2 - = 0. 065 нм (т. е. у кислорода в 2 раза меньше, чем по Вазашерну и Гольдшидту, а цинк крупнее).
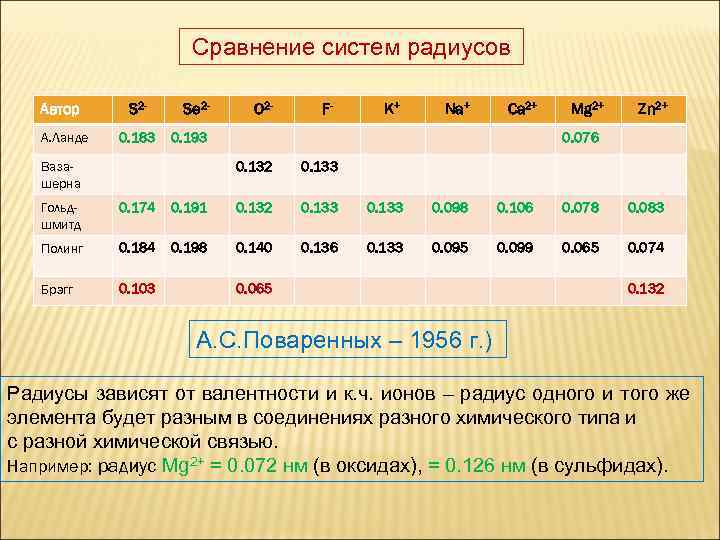 Сравнение систем радиусов Автор S 2 - А. Ланде 0. 183 Se 2 - O 2 - F- K+ Na+ Ca 2+ 0. 193 Вазашерна Mg 2+ Zn 2+ 0. 076 0. 132 0. 133 Гольдшмитд 0. 174 0. 191 0. 132 0. 133 0. 098 0. 106 0. 078 0. 083 Полинг 0. 184 0. 198 0. 140 0. 136 0. 133 0. 095 0. 099 0. 065 0. 074 Брэгг 0. 103 0. 065 0. 132 А. С. Поваренных – 1956 г. ) Радиусы зависят от валентности и к. ч. ионов – радиус одного и того же элемента будет разным в соединениях разного химического типа и с разной химической связью. Например: радиус Mg 2+ = 0. 072 нм (в оксидах), = 0. 126 нм (в сульфидах).
Сравнение систем радиусов Автор S 2 - А. Ланде 0. 183 Se 2 - O 2 - F- K+ Na+ Ca 2+ 0. 193 Вазашерна Mg 2+ Zn 2+ 0. 076 0. 132 0. 133 Гольдшмитд 0. 174 0. 191 0. 132 0. 133 0. 098 0. 106 0. 078 0. 083 Полинг 0. 184 0. 198 0. 140 0. 136 0. 133 0. 095 0. 099 0. 065 0. 074 Брэгг 0. 103 0. 065 0. 132 А. С. Поваренных – 1956 г. ) Радиусы зависят от валентности и к. ч. ионов – радиус одного и того же элемента будет разным в соединениях разного химического типа и с разной химической связью. Например: радиус Mg 2+ = 0. 072 нм (в оксидах), = 0. 126 нм (в сульфидах).
 рассеиваться или образовывать примеси в решетках других минералов. Изоморфизм (твердые растворы) Не все элементы обладают способностью строить собственные структуры и находить для себя устойчивые решетки. Часть элементов рассеивается или образует примеси в решетках других минералов. Э. Митчерлих Среди минералов нет химически чистых веществ, отвечающим идеальным формулам. Лишь условно можно разделить их на минералы постоянного и переменного состава. Минералы постоянного состава - Si. O 2, Fe 2 O 3 и др. В кварце (Si. O 2) соотношение чисел атомов Si и O всегда равно 1: 2 (примеси Al, Fe, Na и др. , (< 0. 1 мас. %) Изоморфизм – это способность элементов замещать друга в кристаллических структурах минералов переменного состава, не нарушая их строения (т. е. без коренного изменения их кристаллической решетки).
рассеиваться или образовывать примеси в решетках других минералов. Изоморфизм (твердые растворы) Не все элементы обладают способностью строить собственные структуры и находить для себя устойчивые решетки. Часть элементов рассеивается или образует примеси в решетках других минералов. Э. Митчерлих Среди минералов нет химически чистых веществ, отвечающим идеальным формулам. Лишь условно можно разделить их на минералы постоянного и переменного состава. Минералы постоянного состава - Si. O 2, Fe 2 O 3 и др. В кварце (Si. O 2) соотношение чисел атомов Si и O всегда равно 1: 2 (примеси Al, Fe, Na и др. , (< 0. 1 мас. %) Изоморфизм – это способность элементов замещать друга в кристаллических структурах минералов переменного состава, не нарушая их строения (т. е. без коренного изменения их кристаллической решетки).
 Вещество смешанные кристаллы – изоморфные смеси) Их состав и свойства непрерывно изменяются в определенном интервале изоморфные ряды Такой изоморфизм называют совершенным Свойства и состав изоморфных смесей аддитивны, т. е. являются непрерывными функциями процентного состава.
Вещество смешанные кристаллы – изоморфные смеси) Их состав и свойства непрерывно изменяются в определенном интервале изоморфные ряды Такой изоморфизм называют совершенным Свойства и состав изоморфных смесей аддитивны, т. е. являются непрерывными функциями процентного состава.
 Типы изоморфизма Изовалентный Гетеровалентный замещение межатомное – ион на ион, атом на атом Особый тип изоморфизма Блочный – в кристаллическую решетку одного вещества включены слои или блоки другого вещества субмикронных размеров (замещаются группировки, комплексы атомов)
Типы изоморфизма Изовалентный Гетеровалентный замещение межатомное – ион на ион, атом на атом Особый тип изоморфизма Блочный – в кристаллическую решетку одного вещества включены слои или блоки другого вещества субмикронных размеров (замещаются группировки, комплексы атомов)
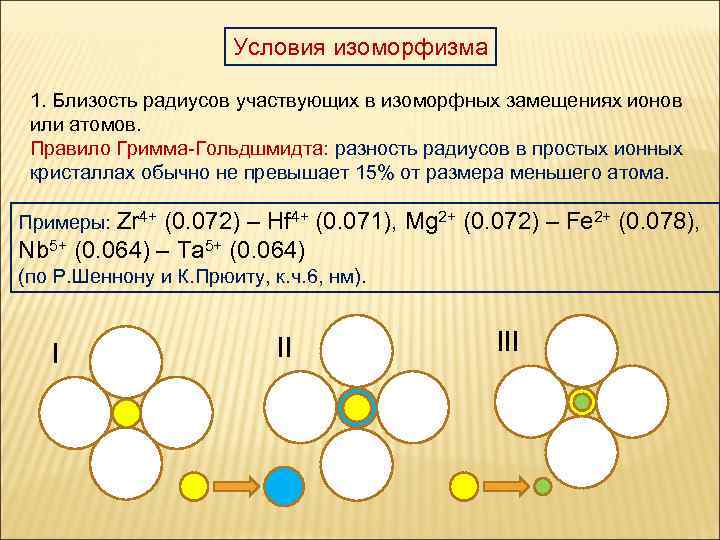 Условия изоморфизма 1. Близость радиусов участвующих в изоморфных замещениях ионов или атомов. Правило Гримма-Гольдшмидта: разность радиусов в простых ионных кристаллах обычно не превышает 15% от размера меньшего атома. Примеры: Zr 4+ (0. 072) – Hf 4+ (0. 071), Mg 2+ (0. 072) – Fe 2+ (0. 078), Nb 5+ (0. 064) – Ta 5+ (0. 064) (по Р. Шеннону и К. Прюиту, к. ч. 6, нм). I II III
Условия изоморфизма 1. Близость радиусов участвующих в изоморфных замещениях ионов или атомов. Правило Гримма-Гольдшмидта: разность радиусов в простых ионных кристаллах обычно не превышает 15% от размера меньшего атома. Примеры: Zr 4+ (0. 072) – Hf 4+ (0. 071), Mg 2+ (0. 072) – Fe 2+ (0. 078), Nb 5+ (0. 064) – Ta 5+ (0. 064) (по Р. Шеннону и К. Прюиту, к. ч. 6, нм). I II III
 2. Определенное сходство химических свойств заменяющих друга элементов, лучше всего, если они принадлежат к одной подгруппе периодической системы. Необходимо и определенное подобие в строении их внешних оболочек. Пример 1: в парах равных по размерам ионов Zr 4+ – Hf 4+, Fe 2+ – Ni 2+ имеется полная или почти полная аналогия в конфигурации внешних электронных оболочек атомов. Zr – 4 s 24 p 64 d 25 s 2 Fe – 3 s 23 p 63 d 24 s 2 Hf – 5 s 25 p 65 d 26 s 2 Ni 3 s 23 p 63 d 24 s 2 Пары Zr 4+ – Hf 4+ и Fe 2+ – Ni 2+ являются классическим примером химических элементов, легко участвующих в процессах изоморфизма.
2. Определенное сходство химических свойств заменяющих друга элементов, лучше всего, если они принадлежат к одной подгруппе периодической системы. Необходимо и определенное подобие в строении их внешних оболочек. Пример 1: в парах равных по размерам ионов Zr 4+ – Hf 4+, Fe 2+ – Ni 2+ имеется полная или почти полная аналогия в конфигурации внешних электронных оболочек атомов. Zr – 4 s 24 p 64 d 25 s 2 Fe – 3 s 23 p 63 d 24 s 2 Hf – 5 s 25 p 65 d 26 s 2 Ni 3 s 23 p 63 d 24 s 2 Пары Zr 4+ – Hf 4+ и Fe 2+ – Ni 2+ являются классическим примером химических элементов, легко участвующих в процессах изоморфизма.
 Пример 2: Na+ Cu- имеют одинаковую валентность Na – 2 s 22 p 63 s 2 Cu 3 s 23 p 63 d 104 s – химически они сильно различаются и потому не изоморфны. Пример 3: K+ (0. 133) ионов составляет 36%) K – 4 s 1 - Na+ (0. 098) (разница в размерах Na – 3 s 1 (полная аналогия в конфигурации электронных оболочек). Являются ли K и Na изоморфными элементами? Оказывается – да, но только при высоких температурах (увеличивается смесимость и наблюдается полный изоморфизм, т. е. K и Na могут замещать один другого; Пример – минерал санидин – (K, Na) [Al. Si 3 O 8]
Пример 2: Na+ Cu- имеют одинаковую валентность Na – 2 s 22 p 63 s 2 Cu 3 s 23 p 63 d 104 s – химически они сильно различаются и потому не изоморфны. Пример 3: K+ (0. 133) ионов составляет 36%) K – 4 s 1 - Na+ (0. 098) (разница в размерах Na – 3 s 1 (полная аналогия в конфигурации электронных оболочек). Являются ли K и Na изоморфными элементами? Оказывается – да, но только при высоких температурах (увеличивается смесимость и наблюдается полный изоморфизм, т. е. K и Na могут замещать один другого; Пример – минерал санидин – (K, Na) [Al. Si 3 O 8]
 3. Сохранение электронейтральности кристаллической структуры минерала. Изовалентный изоморфизм Валентности ионов одинаковые Пример 1. Минерал оливин (Mg, Fe 2+)2[Si. O 4] ионы Mg 2+ замещаются Fe 2+ Это записывается в виде такой схемы Mg 2+ Пример 2. Минерал колумбит (Fe 2+, Mn 2+)(Nb, ионы Fe 2+ замещаются Mn 2+ по схеме Fe 2+ Ta)2 O 6 Mn 2+ Одновременно и независимо идет изоморфизм по схеме Nb 5+ Ta 5+
3. Сохранение электронейтральности кристаллической структуры минерала. Изовалентный изоморфизм Валентности ионов одинаковые Пример 1. Минерал оливин (Mg, Fe 2+)2[Si. O 4] ионы Mg 2+ замещаются Fe 2+ Это записывается в виде такой схемы Mg 2+ Пример 2. Минерал колумбит (Fe 2+, Mn 2+)(Nb, ионы Fe 2+ замещаются Mn 2+ по схеме Fe 2+ Ta)2 O 6 Mn 2+ Одновременно и независимо идет изоморфизм по схеме Nb 5+ Ta 5+
 Гетеровалентный изоморфизм Три разновидности (по способу компенсации зарядов) 1. « 3 за 2 – «дырка» (ионы одного размера, но разной валентности) Пример– сфалерит Zn. S с примесью In 3+ (Zn 2+ = 0. 060 нм, In 3+ = 0. 060 нм) К. ч. 4. Ионы Zn 2+ в 3 -х узлах кристаллической решетки «уступают» место 2 -м ионам In 3+ и одной вакансии по схеме 3 Zn 2+ 2 In 3+ + Структура минерала становится дефектной. Это гетеровалентный изоморфизм с появлением дырочных вакансий.
Гетеровалентный изоморфизм Три разновидности (по способу компенсации зарядов) 1. « 3 за 2 – «дырка» (ионы одного размера, но разной валентности) Пример– сфалерит Zn. S с примесью In 3+ (Zn 2+ = 0. 060 нм, In 3+ = 0. 060 нм) К. ч. 4. Ионы Zn 2+ в 3 -х узлах кристаллической решетки «уступают» место 2 -м ионам In 3+ и одной вакансии по схеме 3 Zn 2+ 2 In 3+ + Структура минерала становится дефектной. Это гетеровалентный изоморфизм с появлением дырочных вакансий.
 2. Замещение ионов с разным радиусом и разной валентностью (+ компенсация) Пример– фиолетовый кварц – аметист Его окраска обусловлена примесью Fe 3+ (0. 01 мас. %) и щелочных металлов (Si 4+ = 0. 026 нм, Fe 3+ = 0. 049 нм, к. ч. 4). Схема замещения Si 4+ Fe 3+ + R+ Изоморфизм ограниченный. 3. Замещение пар ионов с разными радиусами и разной валентностью Пример– высокотемпературные плагиоклазы (кальциево-натриевые ПШ), для них имеются все промежуточные разновидности между альбитом Na[Al. Si 3 O 8] и анортитом Ca[Al 2 Si 2 O 8] Изоморфизм проходит по схеме Na+ + Si 4+ Ca 2+ + Al 3+ Количество атомов остается неизменным и сохраняется электронейтральность кристаллической решетки. Атомы Na и Ca, Si и Al располагаются в одних и тех же узлах пространственной решетки. Радиусы ионов Na+ = 0. 018 нм, Ca 2+ = 0. 112 нм (к. ч. 8) близки, Si 4+ = 0. 026 нм, Al 3+ = 0. 039 нм (к. ч. 4) – заметно отличаются. Изоморфизм возможен при высоких температурах образования, при ее понижении ниже определенного значения происходит переход в другие фазы.
2. Замещение ионов с разным радиусом и разной валентностью (+ компенсация) Пример– фиолетовый кварц – аметист Его окраска обусловлена примесью Fe 3+ (0. 01 мас. %) и щелочных металлов (Si 4+ = 0. 026 нм, Fe 3+ = 0. 049 нм, к. ч. 4). Схема замещения Si 4+ Fe 3+ + R+ Изоморфизм ограниченный. 3. Замещение пар ионов с разными радиусами и разной валентностью Пример– высокотемпературные плагиоклазы (кальциево-натриевые ПШ), для них имеются все промежуточные разновидности между альбитом Na[Al. Si 3 O 8] и анортитом Ca[Al 2 Si 2 O 8] Изоморфизм проходит по схеме Na+ + Si 4+ Ca 2+ + Al 3+ Количество атомов остается неизменным и сохраняется электронейтральность кристаллической решетки. Атомы Na и Ca, Si и Al располагаются в одних и тех же узлах пространственной решетки. Радиусы ионов Na+ = 0. 018 нм, Ca 2+ = 0. 112 нм (к. ч. 8) близки, Si 4+ = 0. 026 нм, Al 3+ = 0. 039 нм (к. ч. 4) – заметно отличаются. Изоморфизм возможен при высоких температурах образования, при ее понижении ниже определенного значения происходит переход в другие фазы.
 Во всех трех разновидностях гетеровалентного изоморфизма должно соблюдаться правило соразмерности ионов. А. Е. Ферсман ввел понятие о диагональных рядах изоморфизма периодической системы элементов (см. табл. ). В этих диагональных рядах атомы и ионы различаются по валентности, но имеют близкие размеры.
Во всех трех разновидностях гетеровалентного изоморфизма должно соблюдаться правило соразмерности ионов. А. Е. Ферсман ввел понятие о диагональных рядах изоморфизма периодической системы элементов (см. табл. ). В этих диагональных рядах атомы и ионы различаются по валентности, но имеют близкие размеры.
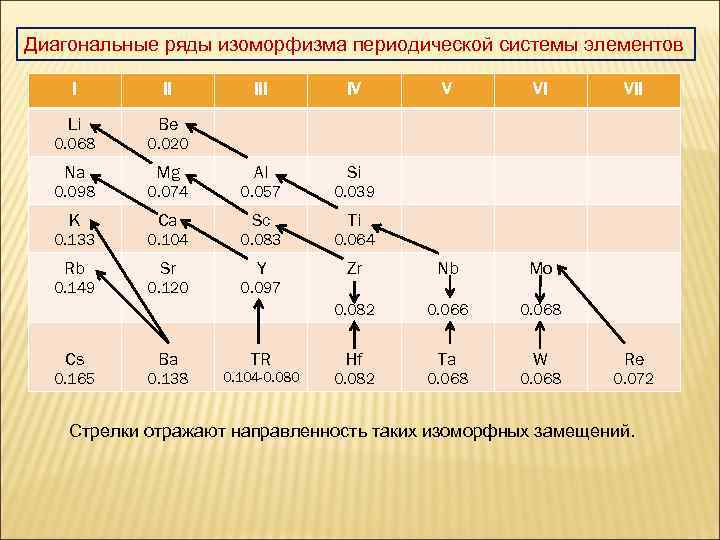 Диагональные ряды изоморфизма периодической системы элементов I II IV Li Be 0. 068 0. 020 Na V VI Mg Al Si 0. 098 0. 074 0. 057 0. 039 K Ca Sc Ti 0. 133 0. 104 0. 083 0. 064 Rb Sr Y Zr Nb 0. 149 0. 120 Mo 0. 082 0. 066 VII 0. 097 0. 068 Cs Ba TR Hf Ta W Re 0. 165 0. 138 0. 104 -0. 080 0. 082 0. 068 0. 072 Стрелки отражают направленность таких изоморфных замещений.
Диагональные ряды изоморфизма периодической системы элементов I II IV Li Be 0. 068 0. 020 Na V VI Mg Al Si 0. 098 0. 074 0. 057 0. 039 K Ca Sc Ti 0. 133 0. 104 0. 083 0. 064 Rb Sr Y Zr Nb 0. 149 0. 120 Mo 0. 082 0. 066 VII 0. 097 0. 068 Cs Ba TR Hf Ta W Re 0. 165 0. 138 0. 104 -0. 080 0. 082 0. 068 0. 072 Стрелки отражают направленность таких изоморфных замещений.
 Благодарю за внимание
Благодарю за внимание


