буферы.ppt
- Количество слайдов: 42
 Лекция № 3 Кислотно-основные равновесия в водном растворе БУФЕРНЫЕ РАСТВОРЫ
Лекция № 3 Кислотно-основные равновесия в водном растворе БУФЕРНЫЕ РАСТВОРЫ
 Теории кислот и оснований Электролитическая теория С. Аррениуса Протолитическая теория Бренстеда - Лоури Теория Г. Льюиса (кислота -акцептор пары (кислота – донор протона, основание – акцептор протона) электронов, основание донор пары электронов).
Теории кислот и оснований Электролитическая теория С. Аррениуса Протолитическая теория Бренстеда - Лоури Теория Г. Льюиса (кислота -акцептор пары (кислота – донор протона, основание – акцептор протона) электронов, основание донор пары электронов).
 Протолитическая теория Бренстеда - Лоури НА ↔ Н+ + А- кислота основание донор протонов акцептор Н+ НА + Н 2 О ↔ Н 3 О + + А к-та 1 В осн 1 + осн 2 к-та 2 сопряженная пара Н 2 О осн 1 ↔ ОН- + ВН+ к-та 2 осн 2 сопряженная пара к-та 1
Протолитическая теория Бренстеда - Лоури НА ↔ Н+ + А- кислота основание донор протонов акцептор Н+ НА + Н 2 О ↔ Н 3 О + + А к-та 1 В осн 1 + осн 2 к-та 2 сопряженная пара Н 2 О осн 1 ↔ ОН- + ВН+ к-та 2 осн 2 сопряженная пара к-та 1
 автопротолиз воды Н 2 О + Н 2 О = Н 3 О+ + ОНили упрощенно Н 2 О = Н+ + ОН Константа диссоциации: к. Н О = 2 Кислотность – [H + ]
автопротолиз воды Н 2 О + Н 2 О = Н 3 О+ + ОНили упрощенно Н 2 О = Н+ + ОН Константа диссоциации: к. Н О = 2 Кислотность – [H + ]
 Вывод ионного произведения воды к. Н О = 2 =1. 86 10 -16 [Н 2 О] = 1000/18= m /М=55, 5 моль/л [Н+][ОН-] = К [Н 2 О] = 10 -14 = КН О - 2 ионное произведение воды. КН Опостоянно для воды и разбавленных растворов при постоянной температуре. В чистой воде и нейтральных растворах: 2 [H+] = [OH-] = 10 -7 моль/л
Вывод ионного произведения воды к. Н О = 2 =1. 86 10 -16 [Н 2 О] = 1000/18= m /М=55, 5 моль/л [Н+][ОН-] = К [Н 2 О] = 10 -14 = КН О - 2 ионное произведение воды. КН Опостоянно для воды и разбавленных растворов при постоянной температуре. В чистой воде и нейтральных растворах: 2 [H+] = [OH-] = 10 -7 моль/л
 Для удобства в расчетах пользуются величинами водородного и гидроксильного показателей р. H и р. ОН, p. H - power Hydrogene Р – отрицательный логарифм (-lg) р. Н = – lg[H] Шкала р. Н р. ОН = – lg[OH] р. Н + р. ОН = 14 р. Н<7, р. ОН>7 р. Н = 7 р. Н>7, р. ОН<7
Для удобства в расчетах пользуются величинами водородного и гидроксильного показателей р. H и р. ОН, p. H - power Hydrogene Р – отрицательный логарифм (-lg) р. Н = – lg[H] Шкала р. Н р. ОН = – lg[OH] р. Н + р. ОН = 14 р. Н<7, р. ОН>7 р. Н = 7 р. Н>7, р. ОН<7
![[H+] = [OH-] = 10 -7 моль/л р. Н = 7 нейтральная среда ‹ [H+] = [OH-] = 10 -7 моль/л р. Н = 7 нейтральная среда ‹](https://present5.com/presentation/2640465_450703076/image-7.jpg) [H+] = [OH-] = 10 -7 моль/л р. Н = 7 нейтральная среда ‹ [H+] р. Н › [H+] р. Н 10 -7 моль/л 7 щелочная среда › ‹ 10 -7 моль/л 7 кислая среда р. Н + р. ОН = 17
[H+] = [OH-] = 10 -7 моль/л р. Н = 7 нейтральная среда ‹ [H+] р. Н › [H+] р. Н 10 -7 моль/л 7 щелочная среда › ‹ 10 -7 моль/л 7 кислая среда р. Н + р. ОН = 17
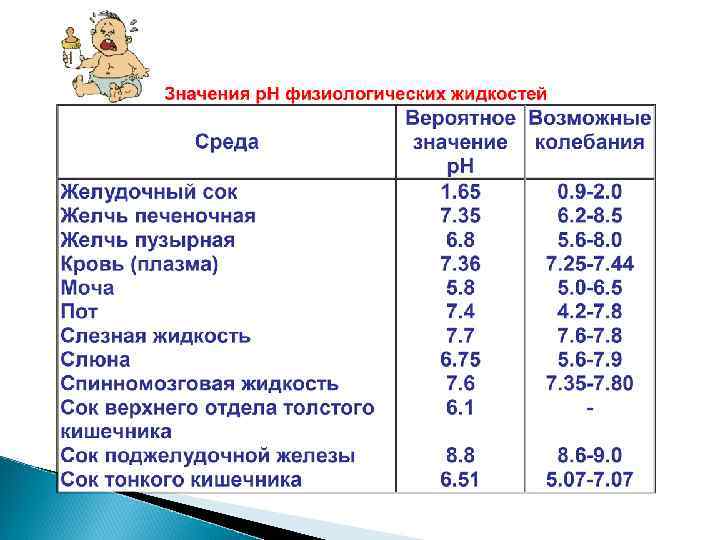
![Кислотность раствора - [H+] Сильные кислоты Слабые кислоты С – αС С → → Кислотность раствора - [H+] Сильные кислоты Слабые кислоты С – αС С → →](https://present5.com/presentation/2640465_450703076/image-9.jpg) Кислотность раствора - [H+] Сильные кислоты Слабые кислоты С – αС С → → αС С [H+] = С кислоты (нормальная конц. ) р. Н = - lg [H+] р. Н = - lg C Кислотность: Общая – С Активная – αС= [H+] Потенциальная - С – αС р. Н = - lg αС
Кислотность раствора - [H+] Сильные кислоты Слабые кислоты С – αС С → → αС С [H+] = С кислоты (нормальная конц. ) р. Н = - lg [H+] р. Н = - lg C Кислотность: Общая – С Активная – αС= [H+] Потенциальная - С – αС р. Н = - lg αС
 p. H растворов сильных электролитов Сильные кислоты p. H = -lg CN Сильные основания Ме. ОН → Ме+ + ОН[ОН-] = CN (основания) p. OH = -lg CN , р. Н = 14 - р. ОН p. H = 14 + lg CN
p. H растворов сильных электролитов Сильные кислоты p. H = -lg CN Сильные основания Ме. ОН → Ме+ + ОН[ОН-] = CN (основания) p. OH = -lg CN , р. Н = 14 - р. ОН p. H = 14 + lg CN
 р. Н растворов слабых электролитов р. Н слабой кислоты р. Н = - lg αС p. H = ½ (p. Ka – lg. C ) p. Ka = -lg. Кacid
р. Н растворов слабых электролитов р. Н слабой кислоты р. Н = - lg αС p. H = ½ (p. Ka – lg. C ) p. Ka = -lg. Кacid
 Действия с логарифмами lg x 10 a=x =a lg ab = lga + lgb lg a/b = lga - lgb x = x lga lg a
Действия с логарифмами lg x 10 a=x =a lg ab = lga + lgb lg a/b = lga - lgb x = x lga lg a
 р. Н растворов слабых электролитов р. Н слабого основания р. ОН = - lg αС p. ОH = ½ (p. Kв – lg. C ) р. Н + р. ОН = 14 p. H = 14 - ½ (p. Kв – lg. C ) p. Kв = -lg. Кbase
р. Н растворов слабых электролитов р. Н слабого основания р. ОН = - lg αС p. ОH = ½ (p. Kв – lg. C ) р. Н + р. ОН = 14 p. H = 14 - ½ (p. Kв – lg. C ) p. Kв = -lg. Кbase
 Почему важно поддержание постоянного р. Н ? Протоны – катализаторы многих биохимических реакций Активность ферментов и гормонов зависит от р. Н Изменение р. Н ведет к изменению осмотического давления
Почему важно поддержание постоянного р. Н ? Протоны – катализаторы многих биохимических реакций Активность ферментов и гормонов зависит от р. Н Изменение р. Н ведет к изменению осмотического давления
 Буферные растворы, р. Н которых сохраняется при разбавлении водой или добавлении сильной кислоты или сильного основания + + 1 капля щелочи – [H ] в миллион раз + + 1 капля кислоты - [H ] в 5000 раз -7 -4 (от 10 до 5 х10 ) -7 В фосфатном буфере от 1. 00 х10 -7 до 1. 01 х10
Буферные растворы, р. Н которых сохраняется при разбавлении водой или добавлении сильной кислоты или сильного основания + + 1 капля щелочи – [H ] в миллион раз + + 1 капля кислоты - [H ] в 5000 раз -7 -4 (от 10 до 5 х10 ) -7 В фосфатном буфере от 1. 00 х10 -7 до 1. 01 х10
 Классификация КИСЛОТНЫЕ СЛАБАЯ КИСЛОТА И ЕЕ СОЛЬ АМФОЛИТНЫЕ Аминокислоты, БЕЛКИ СЛАБОЕ ОСНОВАНИЕ И ЕГО СОЛЬ Ацетатная СН 3 СООН СН 3 СОО– Бикарбонатная Н 2 СО 3 НСО 3– Фосфатная Н 2 РО 4– НРO 42– ОСНОВНЫЕ Аммонийная (H 3 N+)m – Prot – (COOˉ)n ДОНОР ПРОТОНОВ НА сопр. к-та АКЦЕПТОР ПРОТОНОВ Н + + А- сопр. осн-е Донор NH 4+ Акцептор NH 3
Классификация КИСЛОТНЫЕ СЛАБАЯ КИСЛОТА И ЕЕ СОЛЬ АМФОЛИТНЫЕ Аминокислоты, БЕЛКИ СЛАБОЕ ОСНОВАНИЕ И ЕГО СОЛЬ Ацетатная СН 3 СООН СН 3 СОО– Бикарбонатная Н 2 СО 3 НСО 3– Фосфатная Н 2 РО 4– НРO 42– ОСНОВНЫЕ Аммонийная (H 3 N+)m – Prot – (COOˉ)n ДОНОР ПРОТОНОВ НА сопр. к-та АКЦЕПТОР ПРОТОНОВ Н + + А- сопр. осн-е Донор NH 4+ Акцептор NH 3
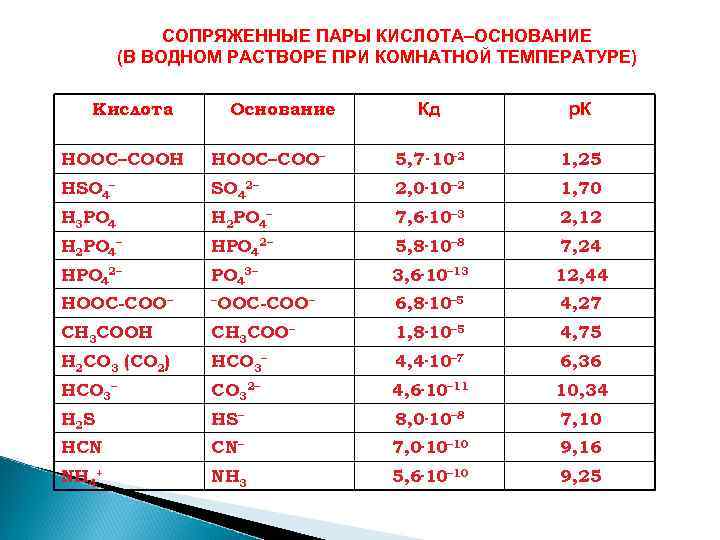 СОПРЯЖЕННЫЕ ПАРЫ КИСЛОТА–ОСНОВАНИЕ (В ВОДНОМ РАСТВОРЕ ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ) Кислота Основание Кд р. К НООС–СООН НООС–СОО– – 2 5, 7· 10 1, 25 HSO 4– SO 42– 2, 0· 10– 2 1, 70 Н 3 РО 4 H 2 PO 4– 7, 6· 10– 3 2, 12 Н 2 РО 4– НРO 42– 5, 8· 10– 8 7, 24 HPO 42– PO 43– 3, 6· 10– 13 12, 44 HOOC-COO– –OOC-COO – 6, 8· 10– 5 4, 27 СН 3 СООН СН 3 СОО– 1, 8· 10– 5 4, 75 Н 2 СО 3 (СО 2) НСО 3– 4, 4· 10– 7 6, 36 HCO 3– CO 32– 4, 6· 10– 11 10, 34 H 2 S HS– 8, 0· 10– 8 7, 10 HCN CN– 7, 0· 10– 10 9, 16 NH 4+ NH 3 5, 6· 10– 10 9, 25
СОПРЯЖЕННЫЕ ПАРЫ КИСЛОТА–ОСНОВАНИЕ (В ВОДНОМ РАСТВОРЕ ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ) Кислота Основание Кд р. К НООС–СООН НООС–СОО– – 2 5, 7· 10 1, 25 HSO 4– SO 42– 2, 0· 10– 2 1, 70 Н 3 РО 4 H 2 PO 4– 7, 6· 10– 3 2, 12 Н 2 РО 4– НРO 42– 5, 8· 10– 8 7, 24 HPO 42– PO 43– 3, 6· 10– 13 12, 44 HOOC-COO– –OOC-COO – 6, 8· 10– 5 4, 27 СН 3 СООН СН 3 СОО– 1, 8· 10– 5 4, 75 Н 2 СО 3 (СО 2) НСО 3– 4, 4· 10– 7 6, 36 HCO 3– CO 32– 4, 6· 10– 11 10, 34 H 2 S HS– 8, 0· 10– 8 7, 10 HCN CN– 7, 0· 10– 10 9, 16 NH 4+ NH 3 5, 6· 10– 10 9, 25
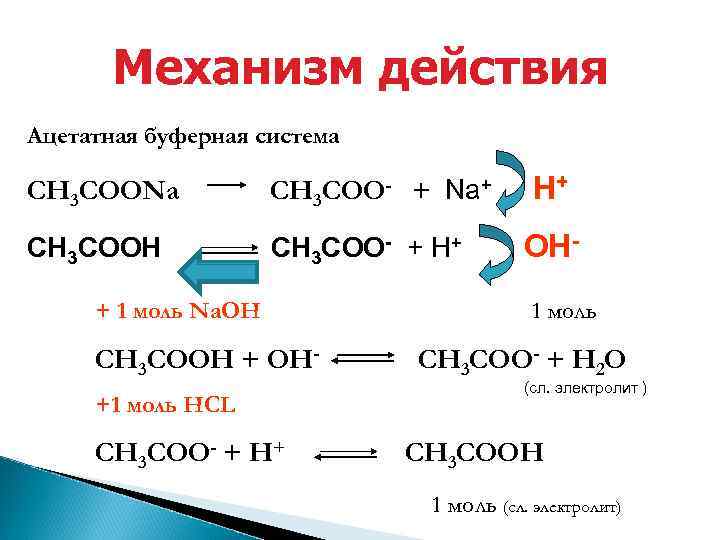 Механизм действия Ацетатная буферная система СН 3 СООNa СН 3 СОО- + Na+ СН 3 СООН СН 3 СОО- + Н+ + 1 моль Na. OH СН 3 СООН + ОН+1 моль HCL СН 3 СОО- + Н+ Н+ ОН 1 моль СН 3 СОО- + Н 2 О (сл. электролит ) СН 3 СООН 1 моль (сл. электролит)
Механизм действия Ацетатная буферная система СН 3 СООNa СН 3 СОО- + Na+ СН 3 СООН СН 3 СОО- + Н+ + 1 моль Na. OH СН 3 СООН + ОН+1 моль HCL СН 3 СОО- + Н+ Н+ ОН 1 моль СН 3 СОО- + Н 2 О (сл. электролит ) СН 3 СООН 1 моль (сл. электролит)
 Вывод формул р. Н
Вывод формул р. Н
 Уравнение Гендерсона-Хассельбаха
Уравнение Гендерсона-Хассельбаха
 приготовление БУФЕРНЫХ РАСТВОРОВ 1. Смешивание готовых растворов компонентов системы: -для кислотной буферной системы p. H = p. Ka + lg (Nc·Vc/Nк·Vк) -для основной буферной системы p. H = 14 – p. Kв – lg(Nc·Vc/No·Vo)
приготовление БУФЕРНЫХ РАСТВОРОВ 1. Смешивание готовых растворов компонентов системы: -для кислотной буферной системы p. H = p. Ka + lg (Nc·Vc/Nк·Vк) -для основной буферной системы p. H = 14 – p. Kв – lg(Nc·Vc/No·Vo)
 2. Частичная нейтрализация - Кислотный буфер nк-ты = nщел = nсоли СН 3 СООН + Na. OH = CH 3 COONa + H 2 O (избыток) p. H = p. Ka + lg Nщ·Vщ /(Nк·Vк –Nщ·Vщ) - Основный буфер NH 4 OH + HCL = NH 4 Cl + H 2 O (избыток) p. H = 14 – p. Kв – lg Nк·Vк / (Nо·Vо - Nк· Vк)
2. Частичная нейтрализация - Кислотный буфер nк-ты = nщел = nсоли СН 3 СООН + Na. OH = CH 3 COONa + H 2 O (избыток) p. H = p. Ka + lg Nщ·Vщ /(Nк·Vк –Nщ·Vщ) - Основный буфер NH 4 OH + HCL = NH 4 Cl + H 2 O (избыток) p. H = 14 – p. Kв – lg Nк·Vк / (Nо·Vо - Nк· Vк)
 БУФЕРНАЯ ЕМКОСТЬ МЕРА СПОСОБНОСТИ БУФЕРНОЙ СИСТЕМЫ ПРОТИВОСТОЯТЬ РЕАКЦИИ СРЕДЫ ПРИ ДОБАВЛЕНИИ КИСЛОТ ИЛИ ОСНОВАНИЙ ЕДИНИЦА ИЗМЕРЕНИЯ : МОЛЬ/Л*1 р. Н n – число мол. Ь эквивалентов сильной кислоты или щелочи Vбуф. р- р а – объем буферного раствора , л ∆р. Н – изменение р. Н в результате добавления сильной кислоты или щелочи
БУФЕРНАЯ ЕМКОСТЬ МЕРА СПОСОБНОСТИ БУФЕРНОЙ СИСТЕМЫ ПРОТИВОСТОЯТЬ РЕАКЦИИ СРЕДЫ ПРИ ДОБАВЛЕНИИ КИСЛОТ ИЛИ ОСНОВАНИЙ ЕДИНИЦА ИЗМЕРЕНИЯ : МОЛЬ/Л*1 р. Н n – число мол. Ь эквивалентов сильной кислоты или щелочи Vбуф. р- р а – объем буферного раствора , л ∆р. Н – изменение р. Н в результате добавления сильной кислоты или щелочи
 БУФЕРНАЯ ЕМКОСТЬ ЗАВИСИТ : От количества компонентов От соотношения количеств 100 экв сол/100 экв к-ты = 1 + 5 экв НСL: 95 / 105 = 0. 9 50 экв соли 50 экв к-ты = 1 + 10 экв Na. OH: 60/ 40 = 1. 5 10 экв соли/ 10 экв к-ты = 1 + 5 экв НСL: 5 /15 = 0. 33 80 экв соли 20 экв к-ты = 4 + 10 экв Na. OH: 90 /10 = 9 p. H = p. Ka + lg Ссоли/Ск-ты ЗОНА БУФЕРНОГО ДЕЙСТВИЯ СИСТЕМЫ: р. Н = р. К +- 1
БУФЕРНАЯ ЕМКОСТЬ ЗАВИСИТ : От количества компонентов От соотношения количеств 100 экв сол/100 экв к-ты = 1 + 5 экв НСL: 95 / 105 = 0. 9 50 экв соли 50 экв к-ты = 1 + 10 экв Na. OH: 60/ 40 = 1. 5 10 экв соли/ 10 экв к-ты = 1 + 5 экв НСL: 5 /15 = 0. 33 80 экв соли 20 экв к-ты = 4 + 10 экв Na. OH: 90 /10 = 9 p. H = p. Ka + lg Ссоли/Ск-ты ЗОНА БУФЕРНОГО ДЕЙСТВИЯ СИСТЕМЫ: р. Н = р. К +- 1
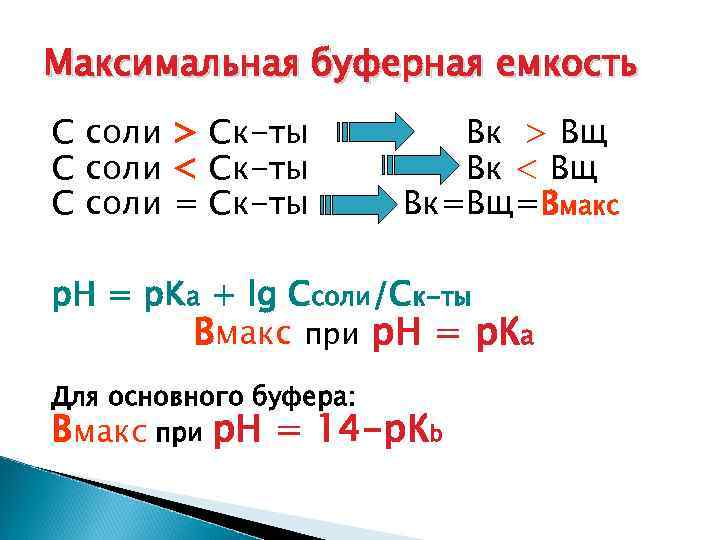 Максимальная буферная емкость С соли > Ск-ты С соли < Ск-ты С соли = Ск-ты Вк > Вщ Вк < Вщ Вк=Вщ=Вмакс p. H = p. Ka + lg Ссоли/Ск-ты Вмакс при р. Н = р. Ка Для основного буфера: Вмакс при р. Н = 14 -р. Кb
Максимальная буферная емкость С соли > Ск-ты С соли < Ск-ты С соли = Ск-ты Вк > Вщ Вк < Вщ Вк=Вщ=Вмакс p. H = p. Ka + lg Ссоли/Ск-ты Вмакс при р. Н = р. Ка Для основного буфера: Вмакс при р. Н = 14 -р. Кb
 Для приготовления буферного раствора с р. Н = 7. 36 и максимальной емкостью необходимо использовать буферный раствор: 1) ацетатный р. К = 4. 75; 2) фосфатный р. К = 7. 21; 3) бикарбонатный р. К = 6. 37.
Для приготовления буферного раствора с р. Н = 7. 36 и максимальной емкостью необходимо использовать буферный раствор: 1) ацетатный р. К = 4. 75; 2) фосфатный р. К = 7. 21; 3) бикарбонатный р. К = 6. 37.
 БУФЕРНЫЕ СИСТЕМЫ ОРГАНИЗМА 1. Минеральные бикарбонатная фосфатная 2. Белковые белковая гемоглобиновая (K) Na. HCO 3/H 2 CO 3 Na 2 HPO 4/Na. H 2 PO 4 3. Аминокислотные
БУФЕРНЫЕ СИСТЕМЫ ОРГАНИЗМА 1. Минеральные бикарбонатная фосфатная 2. Белковые белковая гемоглобиновая (K) Na. HCO 3/H 2 CO 3 Na 2 HPO 4/Na. H 2 PO 4 3. Аминокислотные
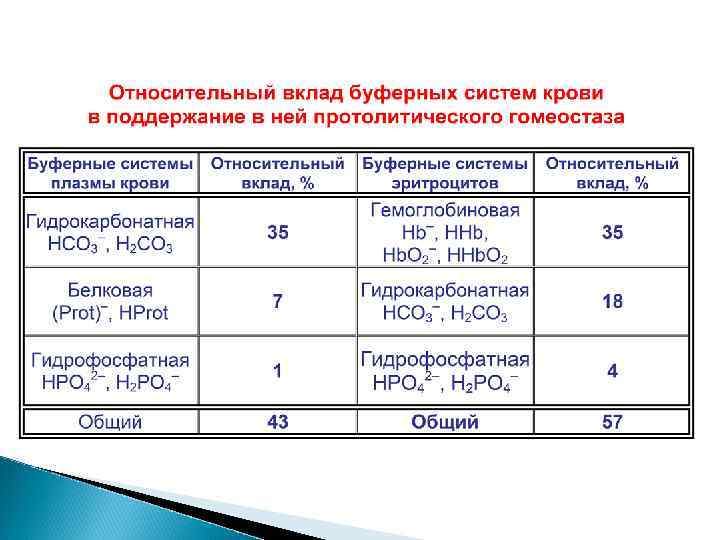
 Бикарбонатная буферная система Состав (K) Na. HCO 3/H 2 CO 3 Механизм действия Атмосфера СO 2 (г) H 2 O СO 2 (р-р) H+ + HСO 3 - H 2 СO 3 Воздушное пространство легких Плазма крови р. Н = p. Ka (H 2 СO 3) + lg C(Na. HCO 3)/C(H 2 CO 3) = = 6, 1 + lg. C(HCO 3 -) – lg аp(CO 2) p – альвеолярное давление углекислого газа Буферная емкость Вк = 40 ммоль/л Вщ = 1 -2
Бикарбонатная буферная система Состав (K) Na. HCO 3/H 2 CO 3 Механизм действия Атмосфера СO 2 (г) H 2 O СO 2 (р-р) H+ + HСO 3 - H 2 СO 3 Воздушное пространство легких Плазма крови р. Н = p. Ka (H 2 СO 3) + lg C(Na. HCO 3)/C(H 2 CO 3) = = 6, 1 + lg. C(HCO 3 -) – lg аp(CO 2) p – альвеолярное давление углекислого газа Буферная емкость Вк = 40 ммоль/л Вщ = 1 -2
![р. Н крови [НСО 3–]: [СО 2] = 20: 1 Вк > Вщ Это р. Н крови [НСО 3–]: [СО 2] = 20: 1 Вк > Вщ Это](https://present5.com/presentation/2640465_450703076/image-30.jpg) р. Н крови [НСО 3–]: [СО 2] = 20: 1 Вк > Вщ Это отвечает особенностям метаболизма организма: Н 2 СО 3 – до 13 моль/ сутки Серная, фосфорная, молочная и др. нелетучие – от 0. 03 до 0. 08 моль/ сутки
р. Н крови [НСО 3–]: [СО 2] = 20: 1 Вк > Вщ Это отвечает особенностям метаболизма организма: Н 2 СО 3 – до 13 моль/ сутки Серная, фосфорная, молочная и др. нелетучие – от 0. 03 до 0. 08 моль/ сутки
![[НСО 3–] Щелочной резерв крови Число мл СО 2, содержащееся в 100 мл крови [НСО 3–] Щелочной резерв крови Число мл СО 2, содержащееся в 100 мл крови](https://present5.com/presentation/2640465_450703076/image-31.jpg) [НСО 3–] Щелочной резерв крови Число мл СО 2, содержащееся в 100 мл крови (главным образом в виде гидрокарбонатов НСО 3 -) Норма: 50 -70 % (по объему) или 25 -30 ммоль/л
[НСО 3–] Щелочной резерв крови Число мл СО 2, содержащееся в 100 мл крови (главным образом в виде гидрокарбонатов НСО 3 -) Норма: 50 -70 % (по объему) или 25 -30 ммоль/л
 Фосфатная буферная система Состав 2 - HPO 4 /H 2 PO 4 Na 2 HPO 4/Na. H 2 PO 4 - Механизм действия H 2 PO 4 - HPO 42 - + H+ - H 2 PO 4 + OH - 2 - HPO 4 + H 2 O 2 - - р. Н = p. Ka (H 2 PO 4 ) + lg C(HPO 4 ) / C(H 2 PO 4 ) - Буферная емкость Вк = 1 -2 ммоль/л Вщ = 0. 5 ммоль/л
Фосфатная буферная система Состав 2 - HPO 4 /H 2 PO 4 Na 2 HPO 4/Na. H 2 PO 4 - Механизм действия H 2 PO 4 - HPO 42 - + H+ - H 2 PO 4 + OH - 2 - HPO 4 + H 2 O 2 - - р. Н = p. Ka (H 2 PO 4 ) + lg C(HPO 4 ) / C(H 2 PO 4 ) - Буферная емкость Вк = 1 -2 ммоль/л Вщ = 0. 5 ммоль/л
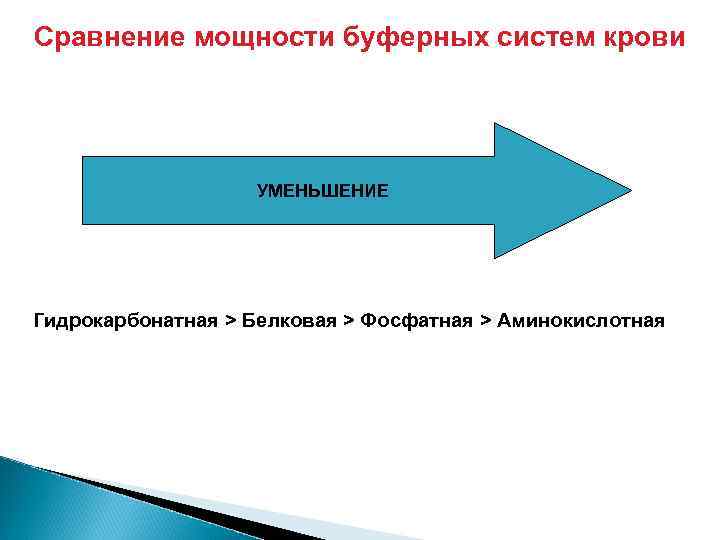 Сравнение мощности буферных систем крови УМЕНЬШЕНИЕ Гидрокарбонатная > Белковая > Фосфатная > Аминокислотная
Сравнение мощности буферных систем крови УМЕНЬШЕНИЕ Гидрокарбонатная > Белковая > Фосфатная > Аминокислотная
 Кооперативное действие буферных систем организма Kдисс. HHb < Kдисс. H 2 CO 3 < Kдисс. HHb. O 2 р. К = 8. 2 р. К = 6. 1 р. К = 6. 95 Более сильная кислота вытесняет более слабую из раствора ее соли Более сильная угольная кислота вытесняет более слабую гемоглобиновую, пополняя щелочной резерв крови ( концентрацию гидрокарбоната ) Механизм кооперативного действия гемоглобиновой и бикарбонатной буферных систем тесно связан с дыхательной функцией крови
Кооперативное действие буферных систем организма Kдисс. HHb < Kдисс. H 2 CO 3 < Kдисс. HHb. O 2 р. К = 8. 2 р. К = 6. 1 р. К = 6. 95 Более сильная кислота вытесняет более слабую из раствора ее соли Более сильная угольная кислота вытесняет более слабую гемоглобиновую, пополняя щелочной резерв крови ( концентрацию гидрокарбоната ) Механизм кооперативного действия гемоглобиновой и бикарбонатной буферных систем тесно связан с дыхательной функцией крови
 Совместное действие бикарбонатной и гемоглобиновой буферных систем В легких: 1. HHb + O 2→ HHb. O 2 2. HCO 3ˉ + HHb. O 2 → Hb. O 2ˉ + H 2 O +CO 2↑
Совместное действие бикарбонатной и гемоглобиновой буферных систем В легких: 1. HHb + O 2→ HHb. O 2 2. HCO 3ˉ + HHb. O 2 → Hb. O 2ˉ + H 2 O +CO 2↑
 Совместное действие бикарбонатной и гемоглобиновой буферных систем В тканях: 1. Hb. O 2ˉ → Hbˉ + O 2 CO 2 + H 2 O = H 2 CO 3 2. H 2 CO 3 + Hbˉ → HCO 3ˉ +HHb
Совместное действие бикарбонатной и гемоглобиновой буферных систем В тканях: 1. Hb. O 2ˉ → Hbˉ + O 2 CO 2 + H 2 O = H 2 CO 3 2. H 2 CO 3 + Hbˉ → HCO 3ˉ +HHb
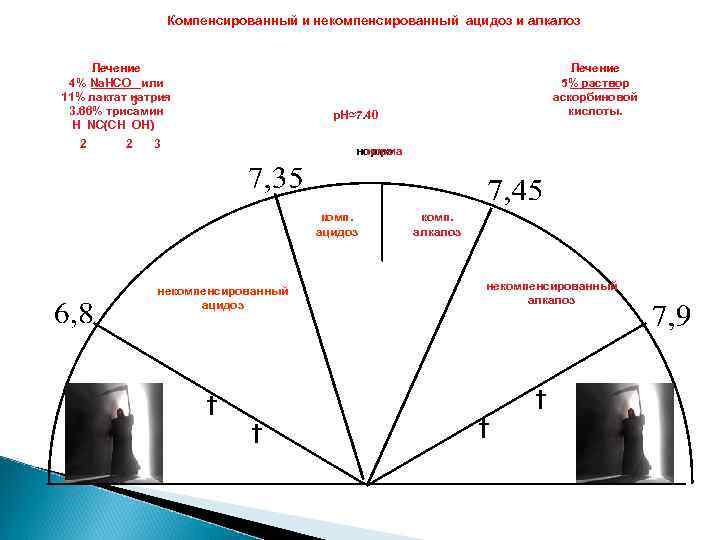 Компенсированный и некомпенсированный ацидоз и алкалоз Лечение 4% Na. HCO или 11% лактат натрия 3 3. 66% трисамин Н NС(СН ОН) 2 2 Лечение 5% раствор аскорбиновой кислоты. р. Н≈7. 40 3 норма комп. ацидоз некомпенсированный ацидоз комп. алкалоз некомпенсированный алкалоз † †
Компенсированный и некомпенсированный ацидоз и алкалоз Лечение 4% Na. HCO или 11% лактат натрия 3 3. 66% трисамин Н NС(СН ОН) 2 2 Лечение 5% раствор аскорбиновой кислоты. р. Н≈7. 40 3 норма комп. ацидоз некомпенсированный ацидоз комп. алкалоз некомпенсированный алкалоз † †



 Оцените кислотно-основное состояние крови больного на основании следующих показателей: р(СО 2) = 55 мм рт. ст. , р. Нплазмы крови = 7, 20. 1) 2) 3) Ацидоз Алкалоз Норма
Оцените кислотно-основное состояние крови больного на основании следующих показателей: р(СО 2) = 55 мм рт. ст. , р. Нплазмы крови = 7, 20. 1) 2) 3) Ацидоз Алкалоз Норма
 СПАСИБО ЗА ВНИМАНИЕ УЧИТЕ ХИМИЮ!!!
СПАСИБО ЗА ВНИМАНИЕ УЧИТЕ ХИМИЮ!!!


