лекция 3 карб кислоты.ppt
- Количество слайдов: 35

Лекция № 3 КАРБОНОВЫЕ КИСЛОТЫ. ГИДРОКСИ-, ОКСОКИСЛОТЫ План лекции • Классификация карбоновых кислот • Строение карбоксильной группы • Кислотность карбоновых кислот • Реакции нуклеофильного замещения монокарбоновых кислот • Изомерия • Реакции дикарбоновых кислот • Реакции оксикислот (гидроксикислот) • Реакции оксокислот. Кетоновые тела

Карбоновыми кислотами называют соединения, в составе есть карбоксильная группа –СООН. Классификация: 1. По природе органического радикала: ациклические насыщенные (Сn. H 2 n+1 COOH) ациклические ненасыщенные (CН 2=СН-СООН) ароматические (С 6 Н 5 СООН) 2. По числу карбоксильных групп -СООН: монокарбоновые (одна –СООН) СН 3 СООН дикарбоновые (две –СООН) НООС-СООН трикарбоновые (три –СООН)лимонная кислота 3. По наличию других функциональных групп гетерофункциональные: -ОН -гидроксикислоты (оксикислоты) (CН 3 СН(ОН)-СООН) >С=О - оксокислоты (ПВК) -NН 2 - аминокислоты
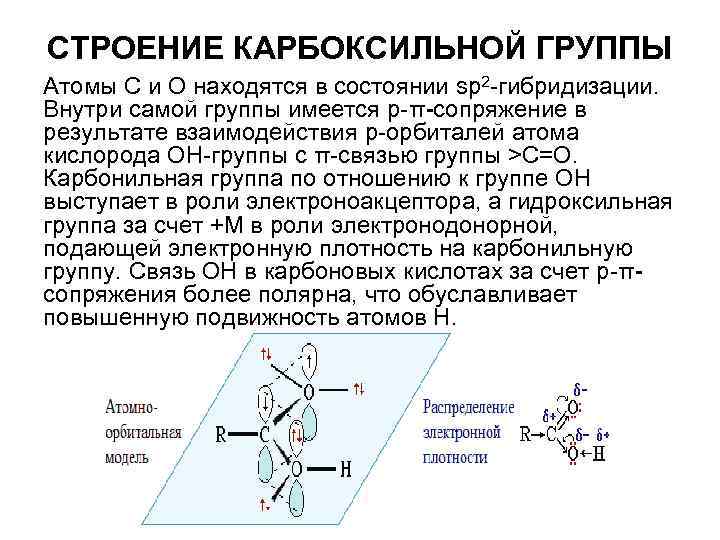
СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ Атомы С и О находятся в состоянии sр2 -гибридизации. Внутри самой группы имеется р-π-сопряжение в результате взаимодействия р-орбиталей атома кислорода ОН-группы с π-связью группы >С=О. Карбонильная группа по отношению к группе ОН выступает в роли электроноакцептора, а гидроксильная группа за счет +М в роли электронодонорной, подающей электронную плотность на карбонильную группу. Связь ОН в карбоновых кислотах за счет р-πсопряжения более полярна, что обуславливает повышенную подвижность атомов Н.

Кислотность карбоновых кислот Карбоновые кислоты проявляют кислотные свойства за счет способности отщеплять Н+. Их сила зависит от стабильности аниона (карбоксилат-иона), образующегося в результате отрыва Н+. В карбоксилат-ионе отрицательный заряд полностью делокализуется по рπ-сопряженнной системе с участием двух атомов О и распределен поровну между ними. Поэтому карбоновые кислоты более сильные кислоты, чем фенолы, спирты и тиолы.

Кислотность карбоновых кислот • Одноосновные карбоновые кислоты - слабые кислоты (слабее фосфорной, но сильнее угольной кислоты). Для карбоновых кислот значения р. Ка лежат в интервале 4, 2 -4, 9. • Сила карбоновых кислот зависит от - строения УВ радикала: кислотность в ряду карбоновых кислот уменьшается с увеличением R. Муравьиная кислота – самая сильная - природы заместителей, введенных в УВ радикал: электроноакцепторные заместители увеличивают кислотность, т. к. способствуют делокализации отрицательного заряда, стабилизируют анионы; электронодонорные заместители понижают кислотность.

Кислотность карбоновых кислот С увеличением числа электроноакцепторных заместителей (-I) происходит увеличение кислотности: Кислота р. Ка Уксусная СН 3 СООН 4, 76 Хлоруксусная СН 2 Сl. CООН 2, 86 Дихлоруксусная СНСl 2 CООН 1, 29 Трихлоруксусная ССl 3 CООН 0, 65 По мере удаления электроноакцепторной группы (Сl) от –СООН группы кислотность уменьшается (-I эффект быстро затухает по цепи) СН 3 -СН 2 -СН←СООН р. Ка=2, 84 ↓ -I Сl Cl←СН 2 ←СООН р. Ка=4, 52 -I
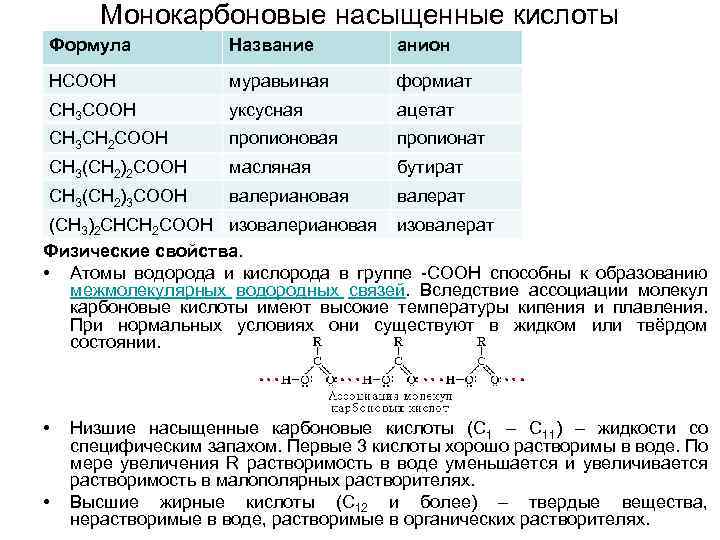
Монокарбоновые насыщенные кислоты Формула Название анион НСООН муравьиная формиат СН 3 СООН уксусная ацетат СН 3 СН 2 СООН пропионовая пропионат СН 3(СН 2)2 СООН масляная бутират СН 3(СН 2)3 СООН валериановая валерат (СН 3)2 СНСН 2 СООН изовалериановая изовалерат Физические свойства. • Атомы водорода и кислорода в группе -СООН способны к образованию межмолекулярных водородных связей. Вследствие ассоциации молекул карбоновые кислоты имеют высокие температуры кипения и плавления. При нормальных условиях они существуют в жидком или твёрдом состоянии. • • Низшие насыщенные карбоновые кислоты (С 1 – С 11) – жидкости со специфическим запахом. Первые 3 кислоты хорошо растворимы в воде. По мере увеличения R растворимость в воде уменьшается и увеличивается растворимость в малополярных растворителях. Высшие жирные кислоты (С 12 и более) – твердые вещества, нерастворимые в воде, растворимые в органических растворителях.

Реакции карбоновых кислот 1. СОЛЕОБРАЗОВАНИЕ Карбоновые кислоты взаимодействуют - с лакмусом (красный в растворах кислот) - со щелочами, основными оксидами - с активными металлами - с карбонатами и гидрокарбонатами
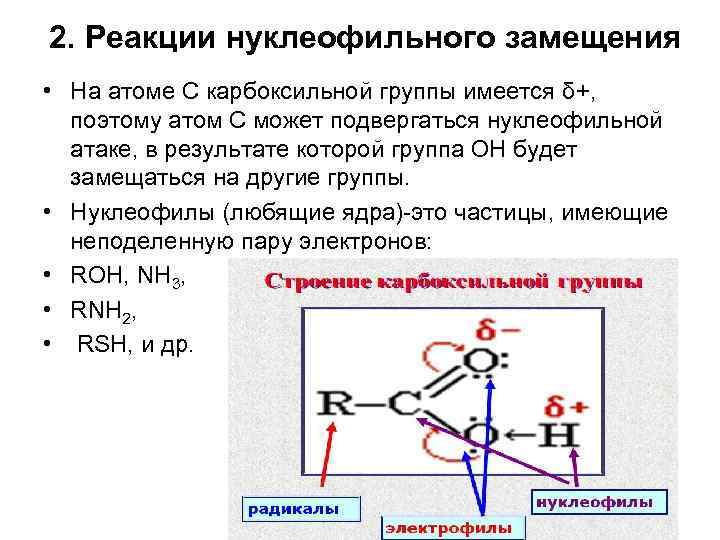
2. Реакции нуклеофильного замещения • На атоме С карбоксильной группы имеется δ+, поэтому атом С может подвергаться нуклеофильной атаке, в результате которой группа ОН будет замещаться на другие группы. • Нуклеофилы (любящие ядра)-это частицы, имеющие неподеленную пару электронов: • ROH, NH 3, • RNH 2, • RSH, и др.

РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ SN Нуклефильное замещение SN у sр2 -гибридизованного атома С карбоксильной группы – наиболее важная группа реакций карбоновых. Гидроксид-ион - плохая уходящая группой, поэтому реакции проводят в очень кислой среде, чтобы превратить плохую уходящую группу ОН- в молекулу Н 2 О. В результате этих реакций образуются функциональные производные карбоновых кислот: in vivo- , сложные эфиры (фосфатиды, триглице риды) галогенангидриды, ангидриды амиды RCONH 2, RCONHR, RCONR 2 ацил-Ко. А in vivo

2. 1. Образование сложных эфиров Реакция этерификации- взаимодействие карбоновых кислот со спиртами. Обратная реакция -гидролиз RCOOH + R 1 OH RCOOR 1 + H 2 O • Реакция этерификации и гидролиз сложных эфиров – это наиболее важные реакции SN, имеющие аналогии в биологических системах. Все стадии обратимы, поэтому образующиеся сложные эфиры являются нестойкими соединениями и гидролизуются в кислой среде. В щелочной среде гидролиз необратим, причиной этого является образование в щелочной среде стабильного ацилат-иона. • Сложными эфирами являются: - жиры и липиды, в образовании которых принимают участие глицерин и ВЖК -многие лекарственные препараты
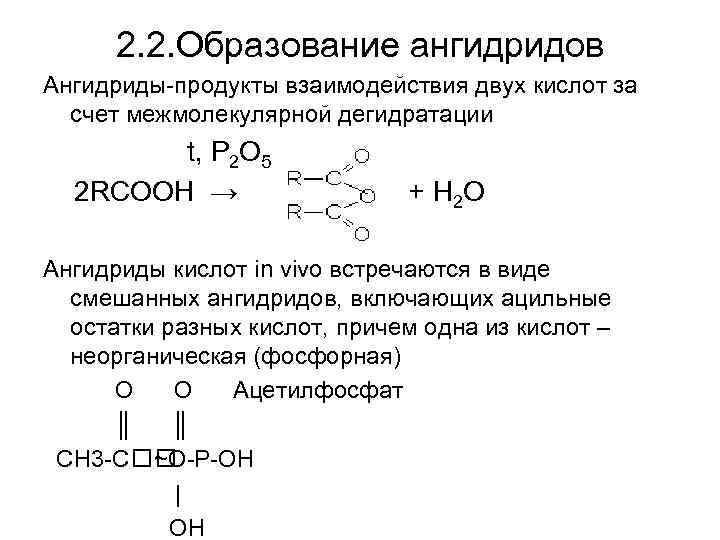
2. 2. Образование ангидридов Ангидриды-продукты взаимодействия двух кислот за счет межмолекулярной дегидратации t, Р 2 О 5 2 RCOOH → + Н 2 О Ангидриды кислот in vivo встречаются в виде смешанных ангидридов, включающих ацильные остатки разных кислот, причем одна из кислот – неорганическая (фосфорная) О О Ацетилфосфат ║ ║ СН 3 -С ~О-Р-ОН | ОН
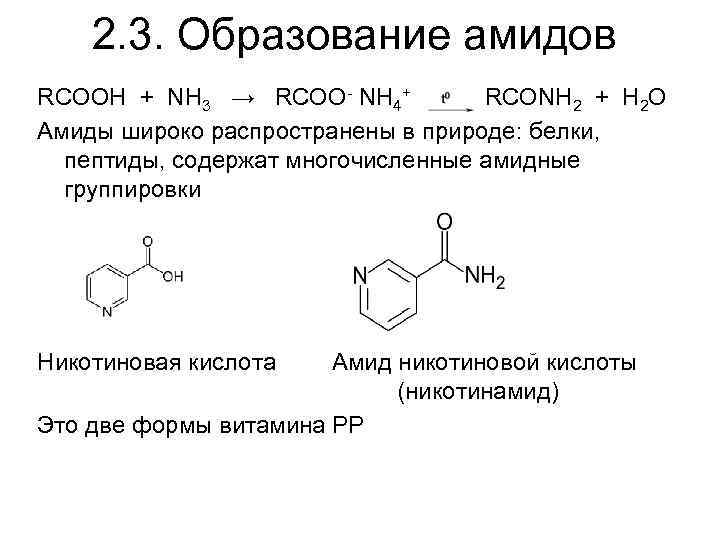
2. 3. Образование амидов RCOOH + NH 3 → RCOO- NH 4+ RCONH 2 + H 2 O Амиды широко распространены в природе: белки, пептиды, содержат многочисленные амидные группировки Никотиновая кислота Амид никотиновой кислоты (никотинамид) Это две формы витамина РР
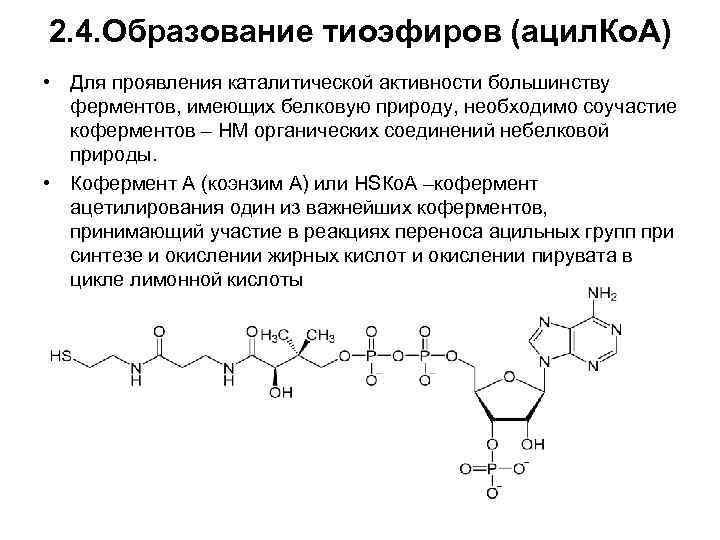
2. 4. Образование тиоэфиров (ацил. Ко. А) • Для проявления каталитической активности большинству ферментов, имеющих белковую природу, необходимо соучастие коферментов – НМ органических соединений небелковой природы. • Кофермент А (коэнзим А) или НSКо. А –кофермент ацетилирования один из важнейших коферментов, принимающий участие в реакциях переноса ацильных групп при синтезе и окислении жирных кислот и окислении пирувата в цикле лимонной кислоты

2. 4. Образование тиоэфиров (ацил. Ко. А) • Тиоэфиры –серные аналоги сложных эфиров, играют важную роль в организме. К ним относятся ацилкоферменты Ацил-Ко. А – макроэргические соединения – активированные производные карбоновых кислот, in vivo выполняющие функцию переносчиков ацильных групп. Из них важную роль играет ацетилкофермент А (ацетил. Ко. А). Он функционирует как тиоэфир. Ацетил. Ко. А производное карбоновой кислоты и тиола. • CH 3 COOH + HS-Kо. А + АТФ → CH 3 CO-SKо. А + (АМФ + Н 4 Р 2 О 7) Коэнзим А Ацетил-Ко. А
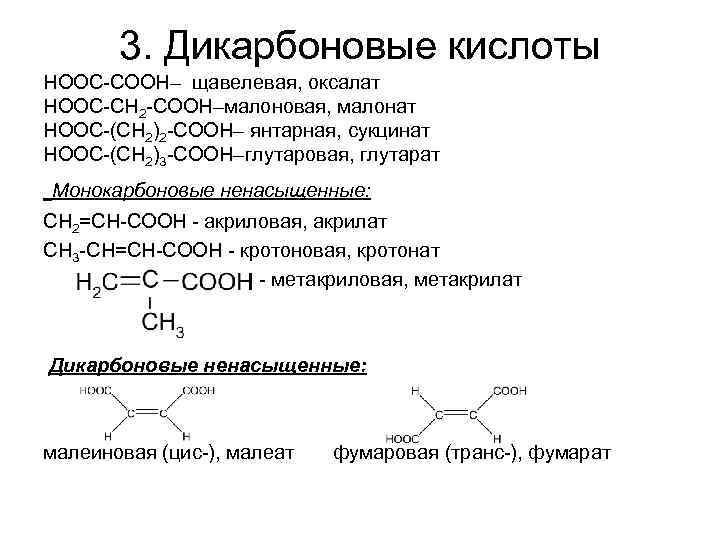
3. Дикарбоновые кислоты НООС-СООН– щавелевая, оксалат НООС-СН 2 -СООН–малоновая, малонат НООС-(СН 2)2 -СООН– янтарная, сукцинат НООС-(СН 2)3 -СООН–глутаровая, глутарат Монокарбоновые ненасыщенные: CН 2=СН-СООН - акриловая, акрилат СН 3 -СН=СН-СООН - кротоновая, кротонат - метакриловая, метакрилат Дикарбоновые ненасыщенные: малеиновая (цис-), малеат фумаровая (транс-), фумарат

Физические свойства: • Дикарбоновые кислоты - твердые кристаллические вещества, умеренно и хорошо растворимые в воде, при нагревании разлагаются. • Низшие ненасыщенные карбоновые кислоты – жидкие, введение двойных связей снижает т. пл. и растворимость в воде.

Реакции дикарбоновых кислот: 3. 1. Кислотные свойства • С накоплением групп –СОООН кислотные свойства соединений увеличиваются. Кислотность дикарбоновых кислот выше, чем монокарбоновых Щавелевая кислота (Н 2 С 2 О 4) р. Ка=1, 23 Уксусная кислота (СН 3 СООН) р. Ка=4, 76 • Это связано с –I группы –СООН, и благодаря этому более полной делокализации отрицательного заряда в сопряженном основании • Чем ближе заместитель к кислотному центру, тем сильнее его влияние • Дикарбоновые кислоты реагируют с основаниями, основными оксидами, активными металлами, солями

3. 2. Декарбоксилирование Реакции декарбоксилирования карбоновых кислот – энергетически выгодный процесс, т. к. в результате образуется устойчивая молекула СО 2. Декарбоксилирование характерно для кислот у которых в ά-положении имеется ЭА заместитель. Щавелевая и малоновая кислоты легко при нагревании декарбоксилируются, t, H 2 SO 4 НООС-СООН → НСООН + СО 2 щавелевая кислота ↓ СО 2 + Н 2 О t=1000 C НООС-СН 2 -СООН → СН 3 - СООН + СО 2 малоновая кислота уксусная кислота
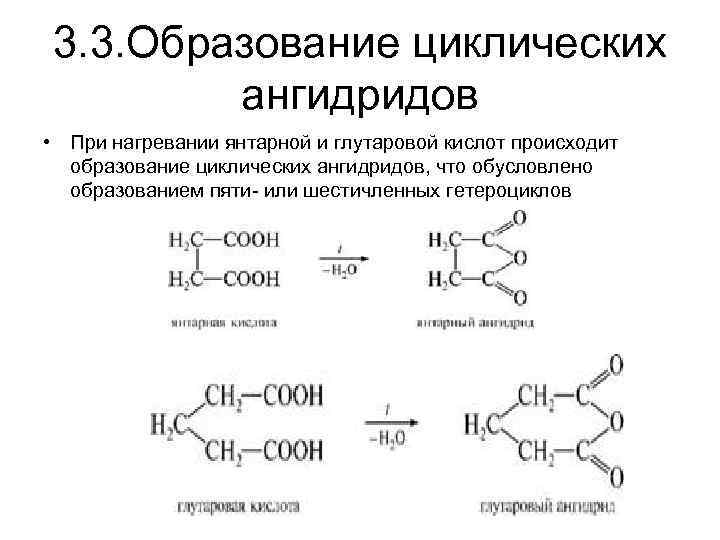
3. 3. Образование циклических ангидридов • При нагревании янтарной и глутаровой кислот происходит образование циклических ангидридов, что обусловлено образованием пяти- или шестичленных гетероциклов

3. 4. Окисление янтарной кислоты in vivo • Превращение in vivo янтарной кислоты в фумаровую является примером обратимой реакции дегидрирования ( окисления) и стереоспецифичной реакции, поскольку образуется только один изомер, имеющий транс-строение. фермент НООС-СН 2 -СОООН +ФАД ↔ ФАДН 2+ НООС-СН=СН -СООН транс-бутендиовая (фумаровая) • Флавинадениндинуклеотид( ФАД )является окислителем ( аналогично молекуле НАД +), содержит в своем составе рибофлавин - витамин В 2. В биохимических реакциях окисления и восстановления принимают участие ферменты – оксидоредуктазы. Белковые молекулы не могут осуществлять перенос электронов, поэтому в составе ферментов обязательно присутствуют органические молекулы, способные передавать электроны , то есть существовать в окисленной и восстановленной форме (кофермент НАД+ / НАДН/Н+ , ФАД / ФАДН 2 )

3. 5. Образование малонил. Ко. А • В реакциях in vivo взаимодействие диоксида углерода с ацетилкоферментом А (ацетил. Ко) приводит к образованию малонилкофермента А (малонил. Ко. А). Это ферментативная реакция карбоксилирования оксидом углерода( IV). Образование малонил. Ко. А происходит в процессе биосинтеза высших карбоновых кислот ( пальмитиновой, стеариновой ) в печени и клетках жировой ткани Н б+ О б- СООН б+ | Н – С → СОSКo. A + С ———> СН 2 – С О SКo. A | | активная форма малоновой кислоты Н б+ О малонил. Ко. А ( НООС-СН 2 - СОSКo. A )

Непредельные карбоновые кислоты, их свойства, реакции 4. 1. Реакция гидратации В клетках в условиях in vivo важное значение имеет реакция гидратации активной формы кротоновой кислоты (участвует фермент крононаза). Реакция идет в соответствии с распределением электронной плотности в молекуле. Oбразуется активная форма 3 гидроксибутановой кислоты. СН 3 - СН =СН – СОSКо. А + Н 2 О ——> СН 3 - СН -СН 2– СОSКо. А (R) (R) | ОН
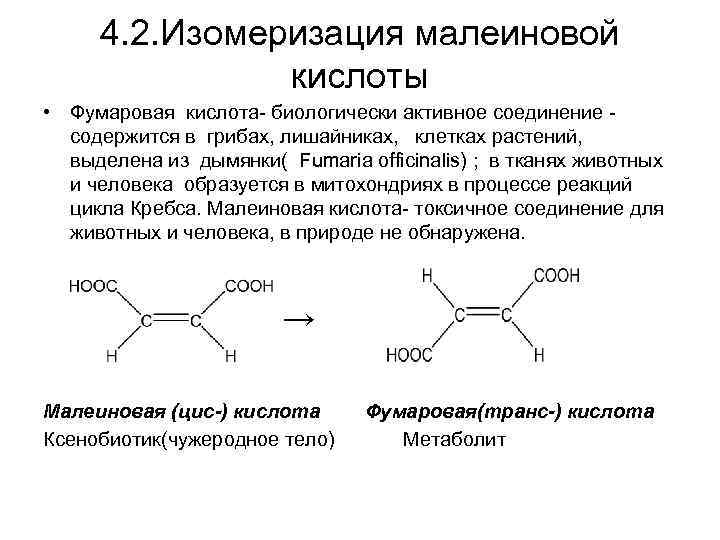
4. 2. Изомеризация малеиновой кислоты • Фумаровая кислота- биологически активное соединение - содержится в грибах, лишайниках, клетках растений, выделена из дымянки( Fumaria officinalis) ; в тканях животных и человека образуется в митохондриях в процессе реакций цикла Кребса. Малеиновая кислота- токсичное соединение для животных и человека, в природе не обнаружена. → Малеиновая (цис-) кислота Фумаровая(транс-) кислота Ксенобиотик(чужеродное тело) Метаболит

4. 3. Реакции присоединения • Малеиновая и фумаровая кислоты восстанавливаются в янтарную кислоту, in vivo это происходит с фумаровой кислотой с участием молекулы ФАДН 2 фермент НООС-СН=СН-СООН + ФАДН 2 → НООС-СН 2–СООН +ФАД фумаровая кислота янтарная кислота • В ферментативных реакциях in vivo присоединение воды к фумаровой кислоте ( гидратация) приводит к образованию одного определенного пространственного изомера яблочной кислоты (L) ЦТК фермент НООС- СН=СН - СООН + НОН →НООС - СН –СН 2– СООН | ОН яблочная кислота (малат)
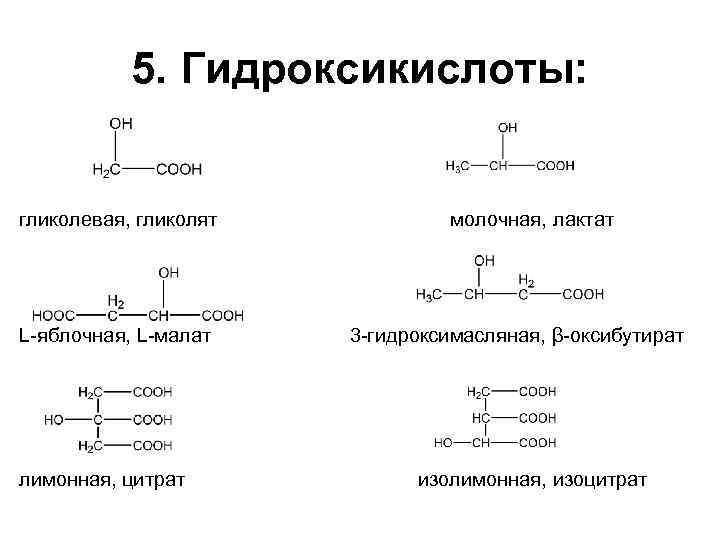
5. Гидроксикислоты: гликолевая, гликолят молочная, лактат L-яблочная, L-малат 3 -гидроксимасляная, β-оксибутират лимонная, цитрат изолимонная, изоцитрат
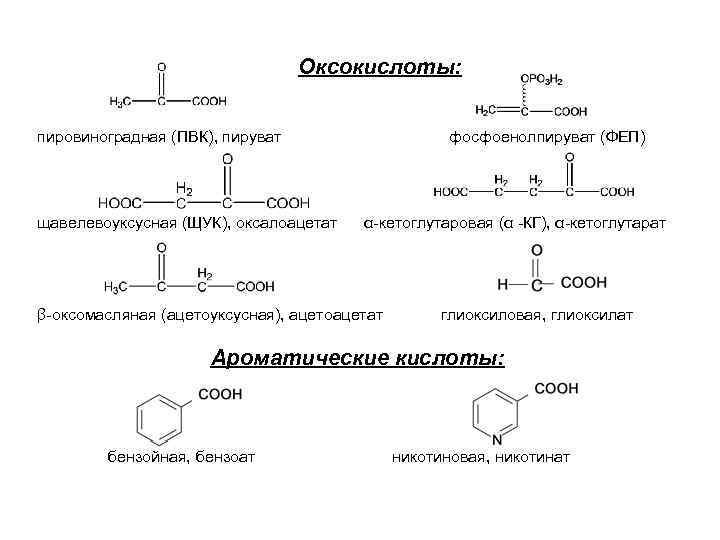
Оксокислоты: пировиноградная (ПВК), пируват фосфоенолпируват (ФЕП) щавелевоуксусная (ЩУК), оксалоацетат α-кетоглутаровая (α -КГ), α-кетоглутарат β-оксомасляная (ацетоуксусная), ацетоацетат глиоксиловая, глиоксилат Ароматические кислоты: бензойная, бензоат никотиновая, никотинат

ФИЗИЧЕСКИЕ СВОЙСТВА • Гидрокси- и оксокислоты – жидкие или твердые кристаллические вещества, умеренно и хорошо растворимые в воде, при нагревании разлагаются. Кислотность окси- оксокислот Кислотность гидроксикислот выше, чем незамещенных кислот. Чем ближе расположены обе функциональные группы, тем выше кислотные свойства. Кислотность оксокислот, выше, чем соответствующих оксикислот • Значение величин р. Ка биологически активных кислот цикла Кребса, гликолиза Кислота р. Ка изолимонная 3, 29 фумаровая 3, 02 лимонная 3, 13 щавелевоуксусная 2, 22 молочная 3, 73 яблочная 3, 46 пировиноградная 2, 93 янтарная 4, 21

Оптическая изомерия гидроксикислот 2 -гидроксипропановая кислота( молочная, лактат) - важнейший природный метаболит, образуется из углеводов( глюкозы, крахмала, гликогена) в условиях анаэробного обмена ( в отсутствии кислорода). • Содержит асимметрический( * ) атом углерода, существует в виде двух изомеров: L-лактата и D –лактата. энантиомеры-зеркальные изомеры • Впервые открыта химиком Шееле в кислом молоке. D –лактат образуется в мышцах и других органах человека и животных в процессе анаэробного превращения глюкозы

Реакции оксикислот: 1. Реакции окисления • В биохимических реакциях важную роль играет обратимая реакция окисления молочной кислоты в пировиноградную, которая протекает в печени, миокарде и других органах и тканях организма в присутствии кислорода. фермент СН 3 – СН- СООН + НАД+ ↔ СН 3 -С - СООН + НАДН /Н+ | | ОН О молочная кислота пировиноградная кислота (D-лактат) (пируват) • В биохимических реакциях окисления и восстановления принимают участие ферменты – оксидоредуктазы. Наиболее распространенным переносчиком атомов водорода является кофермент НАД+ (никотинамидадениндинуклеотид) в реакциях окисления и кофермент НАДН в реакциях восстановления( большинство реакций обратимы).

2. Реакции дегидратации Характерное свойство β-оксикислот – способность к элиминированию молекул воды фермент СН 3 – СН –СН 2 - СООН ↔ СН 3 – СН = СН - СООН + Н 2 О | ОН L -3 -гидроксибутановая к-та 2 -бутеновая( кротоновая) к-та (ß-оксимасляная) В биохимических реакциях in vivo реакция внутримолекулярной дегидратации имеет важное значение для протекания обмена веществ.

Реакции оксокислот: In vivo гидрокси- и оксокислоты с одинаковым скелетом способны взимопревращаться: L-малат ↔ ЩУК; β-оксибутират ↔ ацетоацетат (кетоновые тела); лактат ↔ пируват. 1. Реакции восстановления фермент СН 3 - С(О) –СООН + НАДН /Н + ↔ СН 3 –СН ( ОН ) –СООН + НАД+ ПВК (пируват) молочная к-та (лактат) 2. Реакции декарбоксилирования in vitro и in vivo СН 3 - С(О) –СООН → СН 3 – СНО + СО 2 уксусный альдегид 3. Реакция карбоксилирования in vivo фермент СО 2 + СН 3 - С(О) –СООН → НООС – СН 2 –С (О ) -СООН щавелевоуксусная кислота

Кетоновые тела 3 -оксобутановая (ацетоуксусная) -продукт окисления ßоксимасляной кислоты, образующейся in vivo из углеводов, жирных кислот СН 3 – СН –СН 2 - СООН +НАД + →СН 3 – С –СН 2 - СООН + НАДН/Н+ | | ОН ß-оксимасляная к-та О 3 -оксобутановая к-та ( ацетоуксусная) Все ß – кетокислоты чрезвычайно неустойчивы и легко декарбоксилируются при малейшем нагревании, а in vivo - при снижении р. Н крови( повышении кислотности среды). СН 3 – СН 2 – СООН → СН 3 – СН 3 + СО 2 | | | | нейротоксичное О О соединение- ацетон. Два биоактивных соединения в норме образуют кетоновые тела : 3 -гидроксибутановая кислота( ß -гидроксимасляная), 3 - оксобутановая( ацетоуксусная). Третье кетоновое тело ацетон свидетельствует о развитии патологических процессов.

Фосфоенолпируват • Производным ПВК является фосфоенолпировиноградная кислота (фосфат енольной формы кислоты). В организме анион этой кислоты – фосфоенолпируват (ФЕП) – образуется в процессе гликолиза и служит предшественником пирувата. Гликолиз-ферментативный процесс последовательного расщепления глюкозы в клетках, сопровождающийся синтезом АТФ. Гликолиз при аэробных условиях ведёт к образованию ПВК (пирувата) гликолиз в анаэробных условиях ведёт к образованию молочной кислоты (лактата) Фосфоенолпируват – макроэргическое соединение, с АДФ in vivo дает пируват и АТФ

ЦИКЛ КРЕБСА (ЦТК) • Ци кл трикарбо новых кисло т (цикл Кре бса, цитра тный цикл) – особый циклический биохимический процесс последовательных превращений трикарбоновых ( лимонной , цис-аконитовой , изолимонной ) и дикарбоновых кислот( янтарной, фумаровой, яблочной, ЩУК ), в ходе которого создаются условия для синтеза универсального макроэргического соединения АТФ. Цикл начинается с взаимодействия ЩУК с активной формой уксусной кислоты ацетил. Ко. А и заканчивается вновь образованием ЩУК: Щавелевоуксусная кислота + ацетил. Ко. А → лимонная кислота → цисаконитовая → изолимонная → α – кетоглутаровая →янтарная → фумаровая → яблочная → щавелевоуксусная кислота. - Н 2 О СООН + Н 2 О СООН Лимонная кислота ——> | СН 2 | С- СООН С - СООН | | С-Н ОН – С - Н | СООН СООН цис- аконитовая кислота изолимонная кислота
лекция 3 карб кислоты.ppt