ИЗОПРОЦЕССЫ - с анимацией.ppt
- Количество слайдов: 19
 Лекция № 3 : «ИЗОПРОЦЕССЫ В ИДЕАЛЬНОМ ГАЗЕ» 1. Состояния термодинамических систем 2. Первый закон термодинамики 3. Теплоемкость 4. Применение первого закона термодинамики к изопроцессам в идеальном газе
Лекция № 3 : «ИЗОПРОЦЕССЫ В ИДЕАЛЬНОМ ГАЗЕ» 1. Состояния термодинамических систем 2. Первый закон термодинамики 3. Теплоемкость 4. Применение первого закона термодинамики к изопроцессам в идеальном газе
 ЛИТЕРАТУРА 1. Ремизов А. Н. , Максина А. Г. , Потапенко А. Я. Медицинская и биологическая физика. М. , «Дрофа» , 2008, §§ 10. 1 -10. 4. 2. Ремизов А. Н. , Потапенко А. Я. Курс физики. М. , «Дрофа» , 2004, §§ 11. 1 -11. 3. 3. Физика и биофизика (под ред. Антонова В. Ф. ). М. , » ГЭОТАР-Медиа» , 2008, § 23. 2.
ЛИТЕРАТУРА 1. Ремизов А. Н. , Максина А. Г. , Потапенко А. Я. Медицинская и биологическая физика. М. , «Дрофа» , 2008, §§ 10. 1 -10. 4. 2. Ремизов А. Н. , Потапенко А. Я. Курс физики. М. , «Дрофа» , 2004, §§ 11. 1 -11. 3. 3. Физика и биофизика (под ред. Антонова В. Ф. ). М. , » ГЭОТАР-Медиа» , 2008, § 23. 2.
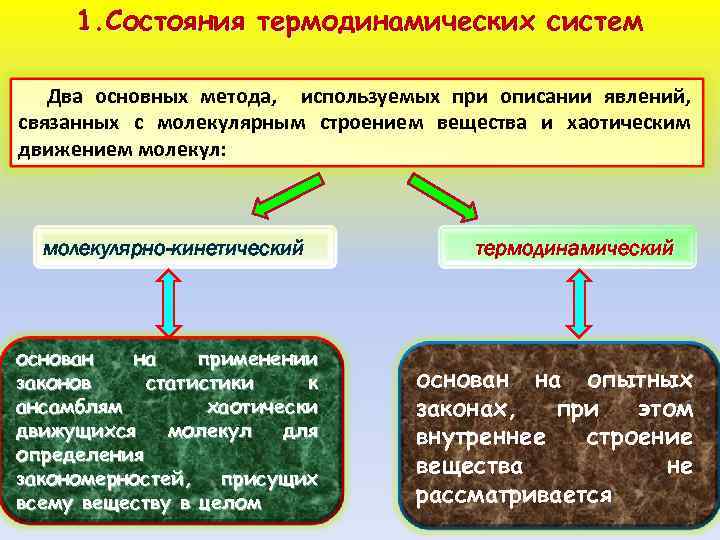 1. Состояния термодинамических систем Два основных метода, используемых при описании явлений, связанных с молекулярным строением вещества и хаотическим движением молекул: молекулярно-кинетический основан на применении законов статистики к ансамблям хаотически движущихся молекул для определения закономерностей, присущих всему веществу в целом термодинамический основан на опытных законах, при этом внутреннее строение вещества не рассматривается
1. Состояния термодинамических систем Два основных метода, используемых при описании явлений, связанных с молекулярным строением вещества и хаотическим движением молекул: молекулярно-кинетический основан на применении законов статистики к ансамблям хаотически движущихся молекул для определения закономерностей, присущих всему веществу в целом термодинамический основан на опытных законах, при этом внутреннее строение вещества не рассматривается
 Термодинамика - раздел физики, рассматривающий системы, между которыми возможен обмен энергией без учета макроскопического состояния тел, составляющих систему Состояние термодинамической системы характеризуется физическими величинами, называемыми параметрами: qобъем, qдавление, qтемпература, qплотность и т. д. Стационарное состояние: если параметры системы при ее взаимодействии с окружающими телами не изменяются с течением времени Стационарное состояние сохраняется за переноса энергии и вещества через систему счет
Термодинамика - раздел физики, рассматривающий системы, между которыми возможен обмен энергией без учета макроскопического состояния тел, составляющих систему Состояние термодинамической системы характеризуется физическими величинами, называемыми параметрами: qобъем, qдавление, qтемпература, qплотность и т. д. Стационарное состояние: если параметры системы при ее взаимодействии с окружающими телами не изменяются с течением времени Стационарное состояние сохраняется за переноса энергии и вещества через систему счет
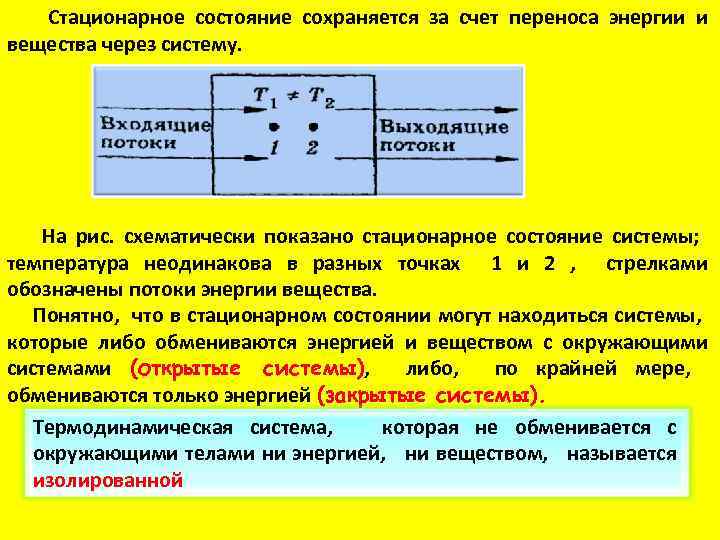 Стационарное состояние сохраняется за счет переноса энергии и вещества через систему. На рис. схематически показано стационарное состояние системы; температура неодинакова в разных точках 1 и 2 , стрелками обозначены потоки энергии вещества. Понятно, что в стационарном состоянии могут находиться системы, которые либо обмениваются энергией и веществом с окружающими системами (открытые системы), либо, по крайней мере, системы) обмениваются только энергией (закрытые системы). Термодинамическая система, которая не обменивается с окружающими телами ни энергией, ни веществом, называется изолированной
Стационарное состояние сохраняется за счет переноса энергии и вещества через систему. На рис. схематически показано стационарное состояние системы; температура неодинакова в разных точках 1 и 2 , стрелками обозначены потоки энергии вещества. Понятно, что в стационарном состоянии могут находиться системы, которые либо обмениваются энергией и веществом с окружающими системами (открытые системы), либо, по крайней мере, системы) обмениваются только энергией (закрытые системы). Термодинамическая система, которая не обменивается с окружающими телами ни энергией, ни веществом, называется изолированной
 Любая реальная термодинамическая система не будет изолированной хотя бы потому, что ее невозможно окружить теплонепроводящей оболочкой. Изолированную систему можно рассматривать как удобную термодинамическую модель Равновесное состояние изолированной системы :
Любая реальная термодинамическая система не будет изолированной хотя бы потому, что ее невозможно окружить теплонепроводящей оболочкой. Изолированную систему можно рассматривать как удобную термодинамическую модель Равновесное состояние изолированной системы :
 Удобной и простой моделью термодинамической системы является идеальный газ. Предположим, что газ, находящийся в цилиндрическом сосуде под поршнем, изобарно расширяется от до. При этом поршень перемещается на , а объем газа изменяется на Для работы, совершаемой газом при изменении его объема, можно получить , (1) Если при изменении объема газа его давление изменяется, то элементарная работа, соответствующая достаточно малому изменению объема d. V равна , (2)
Удобной и простой моделью термодинамической системы является идеальный газ. Предположим, что газ, находящийся в цилиндрическом сосуде под поршнем, изобарно расширяется от до. При этом поршень перемещается на , а объем газа изменяется на Для работы, совершаемой газом при изменении его объема, можно получить , (1) Если при изменении объема газа его давление изменяется, то элементарная работа, соответствующая достаточно малому изменению объема d. V равна , (2)
 После интегрирования получим работу, совершаемую газом: , (3) Для примера найдем работу газа при изотермическом процессе. Подставив в (3) вместо давления его выражение из уравнения Клапейрона-Менделеева , получим : , где m - масса газа, M -молярная масса, T -термодинамическая температура. (4)
После интегрирования получим работу, совершаемую газом: , (3) Для примера найдем работу газа при изотермическом процессе. Подставив в (3) вместо давления его выражение из уравнения Клапейрона-Менделеева , получим : , где m - масса газа, M -молярная масса, T -термодинамическая температура. (4)
 2. Первый закон термодинамики Закон сохранения энергии для тепловых процессов формулируется как первое начало термодинамики (первый закон термодинамики): Количество теплоты, переданное системе, идет на изменение внутренней энергии системы и совершение системой работы: , (5) Под внутренней энергией системы понимают сумму кинетической и потенциальной энергии частиц системы. Она является функцией состояния системы (для данного состояния имеет вполне определенное значение); представляет собой разность двух значений внутренней энергии, соответствующих конечному и начальному состоянию системы: , (6)
2. Первый закон термодинамики Закон сохранения энергии для тепловых процессов формулируется как первое начало термодинамики (первый закон термодинамики): Количество теплоты, переданное системе, идет на изменение внутренней энергии системы и совершение системой работы: , (5) Под внутренней энергией системы понимают сумму кинетической и потенциальной энергии частиц системы. Она является функцией состояния системы (для данного состояния имеет вполне определенное значение); представляет собой разность двух значений внутренней энергии, соответствующих конечному и начальному состоянию системы: , (6)
 Количество теплоты и работа, в отличие от внутренней энергии, являются функцией процесса (а не состояния). Их невозможно выразить в виде разности двух значений какого-либо параметра, соответствующих конечному и начальному состояниям. Для малых значений Q, U запишем в виде и А первый закон термодинамики , (7)
Количество теплоты и работа, в отличие от внутренней энергии, являются функцией процесса (а не состояния). Их невозможно выразить в виде разности двух значений какого-либо параметра, соответствующих конечному и начальному состояниям. Для малых значений Q, U запишем в виде и А первый закон термодинамики , (7)
 3. Теплоемкость Количество теплоты, необходимое для нагревания тела на 1 К, называется теплоемкостью тела. Количество теплоты, необходимое для нагревания 1 кг вещества на 1 К, называется удельной теплоемкостью вещества: , (8) где d. Q - количество теплоты, сообщенное телу массой m , d. T - изменение температуры тела. Для одного и того же тела различают удельные теплоемкости в изобарном и изохорном процессах, а также соответствующие молярные теплоемкости, для которых очевидно , , (9)
3. Теплоемкость Количество теплоты, необходимое для нагревания тела на 1 К, называется теплоемкостью тела. Количество теплоты, необходимое для нагревания 1 кг вещества на 1 К, называется удельной теплоемкостью вещества: , (8) где d. Q - количество теплоты, сообщенное телу массой m , d. T - изменение температуры тела. Для одного и того же тела различают удельные теплоемкости в изобарном и изохорном процессах, а также соответствующие молярные теплоемкости, для которых очевидно , , (9)
 4. Применение первого закона термодинамики к изопроцессам в идеальном газе а) Изохорный процесс. Работа при изохорном процессе равна нулю и первое начало термодинамики принимает вид , (10) Количество теплоты, сообщаемое газу, идет на увеличение его внутренней энергии. Из (8) с учетом (10) для элементарного изменения внутренней энергии при изохорном процессе получим , (11) Изменение внутренней энергии при переходе системы от состояния с температурой Т 0 в состояние с температурой Т :
4. Применение первого закона термодинамики к изопроцессам в идеальном газе а) Изохорный процесс. Работа при изохорном процессе равна нулю и первое начало термодинамики принимает вид , (10) Количество теплоты, сообщаемое газу, идет на увеличение его внутренней энергии. Из (8) с учетом (10) для элементарного изменения внутренней энергии при изохорном процессе получим , (11) Изменение внутренней энергии при переходе системы от состояния с температурой Т 0 в состояние с температурой Т :
 С учетом начальных условий имеем: , а для одного моля , (12) Учитывая формулу для внутренней энергии моля газа, из (12) получаем формулу для молярной теплоемкости при изохорном процессе: , (13) в) Изобарный процесс. Уравнение Майера. На основании (8) количество теплоты при изобарном процессе равно , (14) и первый закон термодинамики можно записать в виде: (15)
С учетом начальных условий имеем: , а для одного моля , (12) Учитывая формулу для внутренней энергии моля газа, из (12) получаем формулу для молярной теплоемкости при изохорном процессе: , (13) в) Изобарный процесс. Уравнение Майера. На основании (8) количество теплоты при изобарном процессе равно , (14) и первый закон термодинамики можно записать в виде: (15)
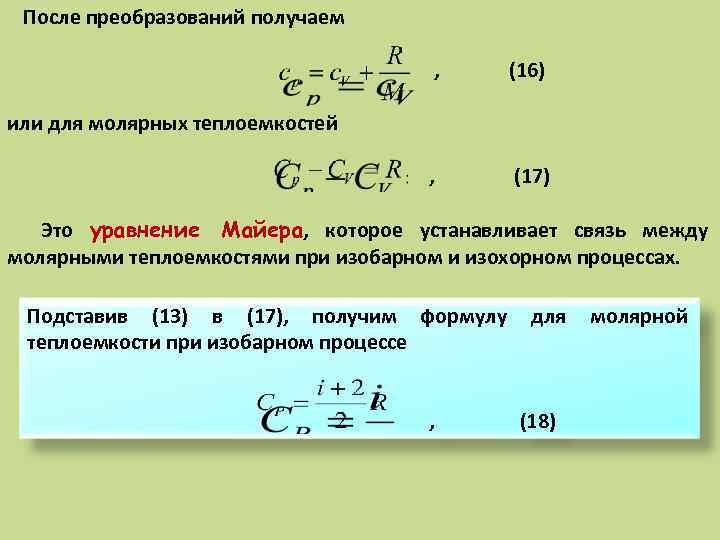 После преобразований получаем , (16) , (17) или для молярных теплоемкостей Это уравнение Майера, которое устанавливает связь между Майера молярными теплоемкостями при изобарном и изохорном процессах. Подставив (13) в (17), получим формулу теплоемкости при изобарном процессе , для (18) молярной
После преобразований получаем , (16) , (17) или для молярных теплоемкостей Это уравнение Майера, которое устанавливает связь между Майера молярными теплоемкостями при изобарном и изохорном процессах. Подставив (13) в (17), получим формулу теплоемкости при изобарном процессе , для (18) молярной
 с) Изотермический процесс. При этом процессе температура газа не изменяется, поэтому и внутренняя энергия остается постоянной. Первый закон термодинамики для этого процесса в идеальном газе: , (19) Количество теплоты, сообщенное газу, идет на совершение работы. На основании (19) и (4) можно записать , (20) d) Адиабатный процесс. Уравнение Пуассона. Адиабатным называется процесс, происходящий в системе без теплообмена с окружающими телами, т. е
с) Изотермический процесс. При этом процессе температура газа не изменяется, поэтому и внутренняя энергия остается постоянной. Первый закон термодинамики для этого процесса в идеальном газе: , (19) Количество теплоты, сообщенное газу, идет на совершение работы. На основании (19) и (4) можно записать , (20) d) Адиабатный процесс. Уравнение Пуассона. Адиабатным называется процесс, происходящий в системе без теплообмена с окружающими телами, т. е
 Такой процесс невозможно осуществить с абсолютной точностью, но если процесс происходит быстро или с хорошей термоизоляцией, то он будет близок к адиабатному. Первое начало термодинамики в этом случае имеет вид или , (21) Уравнение, связывающее в адиабатном процессе два параметра газа (например, давление и объем), называется уравнением Пуассона Оно имеет вид: где , - показатель адиабаты, всегда больше 1 ( согласно уравнению Майера) (22)
Такой процесс невозможно осуществить с абсолютной точностью, но если процесс происходит быстро или с хорошей термоизоляцией, то он будет близок к адиабатному. Первое начало термодинамики в этом случае имеет вид или , (21) Уравнение, связывающее в адиабатном процессе два параметра газа (например, давление и объем), называется уравнением Пуассона Оно имеет вид: где , - показатель адиабаты, всегда больше 1 ( согласно уравнению Майера) (22)
 Из (13) и (18) получаем , (23) Для одноатомных газов молярные теплоемкости CV и Cp постоянны и не зависят от температуры. Что касается многоатомных газов, то их теплоемкости остаются приблизительно постоянными только при нормальных температурах. При высоких температурах оказываются большими, а при низких – меньшими теоретически вычисленных значений. При низких температурах происходит как бы «вымерзание» вращательных степеней свободы, а при высоких температурах, наоборот, «возбуждение» каких-то новых степеней свободы.
Из (13) и (18) получаем , (23) Для одноатомных газов молярные теплоемкости CV и Cp постоянны и не зависят от температуры. Что касается многоатомных газов, то их теплоемкости остаются приблизительно постоянными только при нормальных температурах. При высоких температурах оказываются большими, а при низких – меньшими теоретически вычисленных значений. При низких температурах происходит как бы «вымерзание» вращательных степеней свободы, а при высоких температурах, наоборот, «возбуждение» каких-то новых степеней свободы.
 е) Политропный процесс. Рассмотренные выше процессы можно представить как частные случаи некоторого общего процесса, называемого политропным. Под политропным понимают такой процесс, при котором теплоемкость вещества (газа) не изменяется. Давление и объем в этом процессе связаны уравнением, включающим в себе все изопроцессы: , (24) где n-показатель политропы, зависящий от удельной теплоемкости при политропном процессе: , (25) Предположим, что при политропном процессе удельная теплоемкость равна нулю (с=0) ; такая ситуация соответствует адиабатному процессу. Из (25) находим
е) Политропный процесс. Рассмотренные выше процессы можно представить как частные случаи некоторого общего процесса, называемого политропным. Под политропным понимают такой процесс, при котором теплоемкость вещества (газа) не изменяется. Давление и объем в этом процессе связаны уравнением, включающим в себе все изопроцессы: , (24) где n-показатель политропы, зависящий от удельной теплоемкости при политропном процессе: , (25) Предположим, что при политропном процессе удельная теплоемкость равна нулю (с=0) ; такая ситуация соответствует адиабатному процессу. Из (25) находим
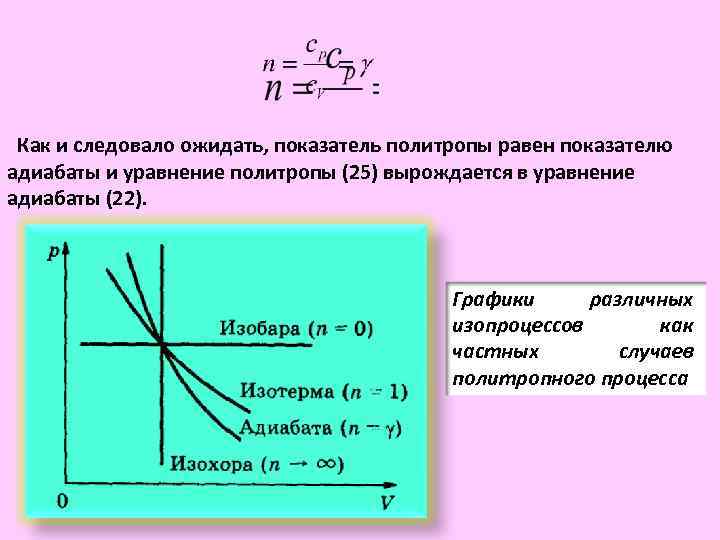 Как и следовало ожидать, показатель политропы равен показателю адиабаты и уравнение политропы (25) вырождается в уравнение адиабаты (22). Графики различных изопроцессов как частных случаев политропного процесса
Как и следовало ожидать, показатель политропы равен показателю адиабаты и уравнение политропы (25) вырождается в уравнение адиабаты (22). Графики различных изопроцессов как частных случаев политропного процесса


