лекция 3 (9 сем).ppt
- Количество слайдов: 17

Лекция 3. Группа веществ, изолируемых из объектов путём минерализации биологического материала. Дробный метод анализа «металлических» ядов в минерализате (деструктате) (Продолжение). Вопросы: 1. Исследование мышьяка в минерализате. 2. Химико-токсикологическое доказательство ртути в биологическом материале.

1. Исследование мышьяка в минерализате. As I этап Предварительное исследование (отрицательное значение) р. Зангер-Блека р. с раствором (ДДТК)Ag As 2 Hg 3 в пиридине Условия: (красно-фиолетовое 1) купированный Zn и Sn. Cl 2; окрашивание) 2) бумага, импрегнированная Условия: Hg. Cl 2 (Hg. Br 2); 1) купированный цинк и Sn. Cl 2 3) 3% р-р KJ; 2) безводный пиридин. 4) уксусно-свинцовая вата.

Примечание: к условиям реакции Зангера-Блека К дробному анализу мышьяка Условия проведения реакции Зангер-Блека 5+ 3+ 1) Sn. Cl 2 – для восстановления As → As 5+ 32+ + 3+ 24+ а) As O 4 + Sn + 8 H → As O +Sn + 4 H 2 O; арсенат-ион 5+ (H 3 As O 4) 3+ арсенит-ион 3+ (HAs O 2) 3 - б) As O 2 + 7[H] →As H 3↑ + H 2 O арсин
![2) Уксусно-свинцовая вата [Pb(CH 3 COO)2 – для связывания примеси (H 2 S)] а) 2) Уксусно-свинцовая вата [Pb(CH 3 COO)2 – для связывания примеси (H 2 S)] а)](https://present5.com/presentation/105439991_437283034/image-4.jpg)
2) Уксусно-свинцовая вата [Pb(CH 3 COO)2 – для связывания примеси (H 2 S)] а) H 2 SO 4 + 8[H] → H 2 S↑ + 4 H 2 O; конц. изб. б) на реактивной бумаге: H 2 S + Hg. Cl 2 → Hg. S↓ + 2 HCl чёрн. осад. в) Pb(CH 3 COO)2 + H 2 S → Pb. S↓ + 2 CH 3 COOH (порошок на вате) бел. осад.
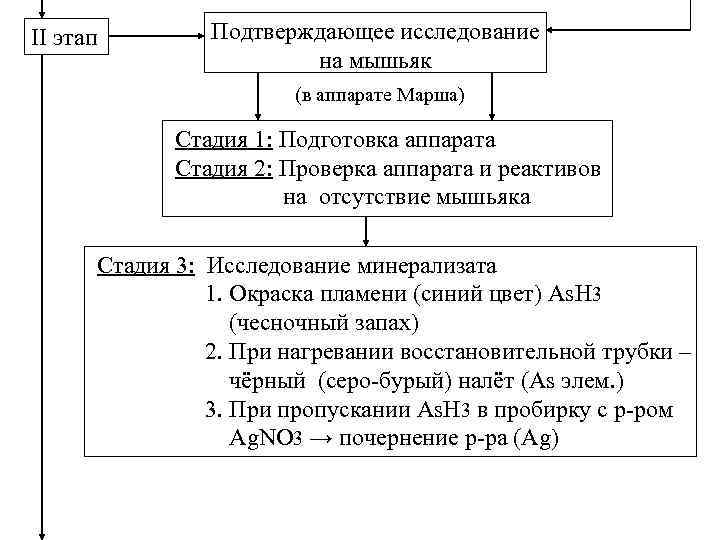
II этап Подтверждающее исследование на мышьяк (в аппарате Марша) Стадия 1: Подготовка аппарата Стадия 2: Проверка аппарата и реактивов на отсутствие мышьяка Стадия 3: Исследование минерализата 1. Окраска пламени (синий цвет) As. H 3 (чесночный запах) 2. При нагревании восстановительной трубки – чёрный (серо-бурый) налёт (As элем. ) 3. При пропускании As. H 3 в пробирку с р-ром Ag. NO 3 → почернение р-ра (Ag)
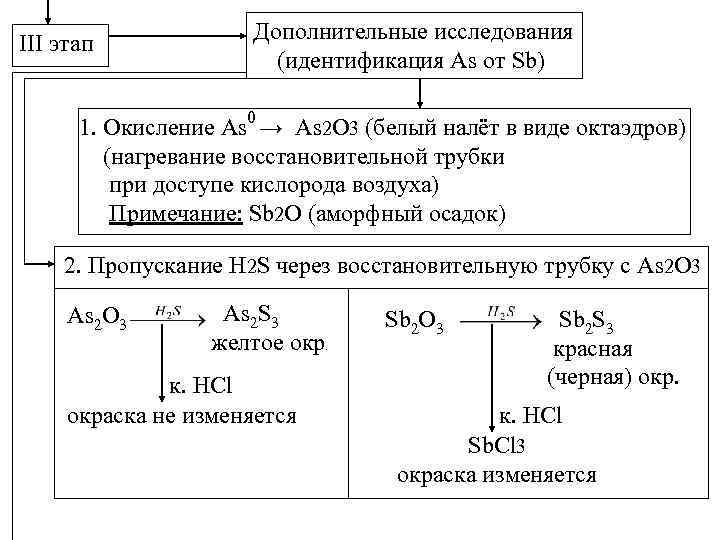
III этап Дополнительные исследования (идентификация As от Sb) 1. Окисление As 0 → As 2 O 3 (белый налёт в виде октаэдров) (нагревание восстановительной трубки при доступе кислорода воздуха) Примечание: Sb 2 O (аморфный осадок) 2. Пропускание H 2 S через восстановительную трубку с As 2 O 3 As 2 S 3 желтое окр. к. HCl окраска не изменяется Sb 2 O 3 Sb 2 S 3 красная (черная) окр. к. HCl Sb. Cl 3 окраска изменяется
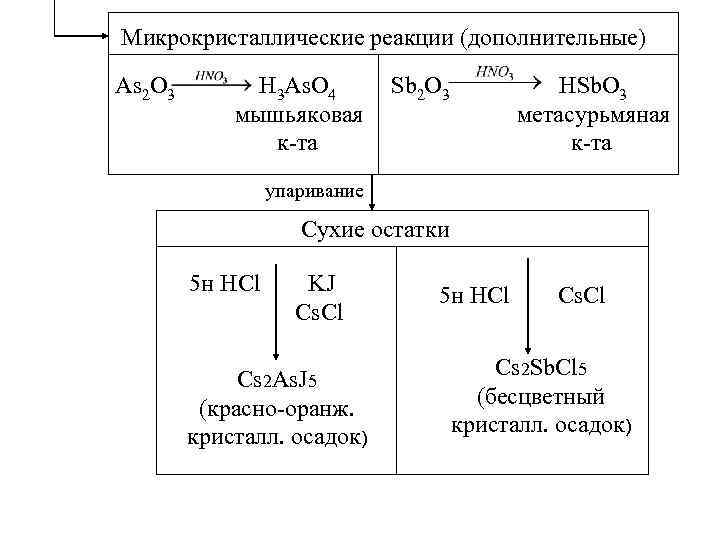
Микрокристаллические реакции (дополнительные) As 2 O 3 H 3 As. O 4 мышьяковая к-та HSb. O 3 метасурьмяная к-та Sb 2 O 3 упаривание Сухие остатки 5 н HCl KJ Cs. Cl Cs 2 As. J 5 (красно-оранж. кристалл. осадок) 5 н HCl Cs 2 Sb. Cl 5 (бесцветный кристалл. осадок)

2. Химико-токсикологическое доказательство ртути в биологическом материале. А. Изолирование ртути из биологического материала. При изолировании ртути из биологических объектов с помощью общих методов минерализации, происходят значительные потери (до 95 – 99 %%), за счёт летучести ртути при высоких температурах. В связи с этим, длительное время в химикотоксикологической практике настоятельно стояла задача по разработке частного метода изолирования ртути из биологического материала. И этот вопрос был успешно решён отечественными учёными:
![1. А. Н. Крылова [1968 г] - Деструктивный метод изолирования ртути из тканей внутренних 1. А. Н. Крылова [1968 г] - Деструктивный метод изолирования ртути из тканей внутренних](https://present5.com/presentation/105439991_437283034/image-9.jpg)
1. А. Н. Крылова [1968 г] - Деструктивный метод изолирования ртути из тканей внутренних органов 1. 1. А. А. Васильева [1962 г. ] – Частичная (деструктивная) минерализация объекта – тканей внутренних органов 1. 2. А. Н. Крылова [1968 г. ] – Усовершенствование процесса деструкции биологического объекта – тканей внутренних органов, применительно анализа ртути 2. А. Ф. Рубцов, А. Н. Крылова, [1975 г. ] – Ускоренный деструктивный метод изолирования ртути из мочи

Сущность метода, предложенного авторами, заключается в том, что в процессе деструкции биологического материала происходит только частичное разрушение органических веществ, в том числе разрушаются комплексы белков со ртутью, чаще всего по сульфгидрильным группам. При этом, окисление осуществляется азотной кислотой в присутствии катализатора – этилового спирта, при добавлении по каплям концентрированной серной кислоты (при комнатной температуре, что является отличием от общего метода минерализации).

Таким образом, деструкция объекта проходит в мягких условиях, без существенного повышения температуры, при этом важную роль в повышении активности окислительных свойств азотной кислоты играет катализатор – этиловый спирт.
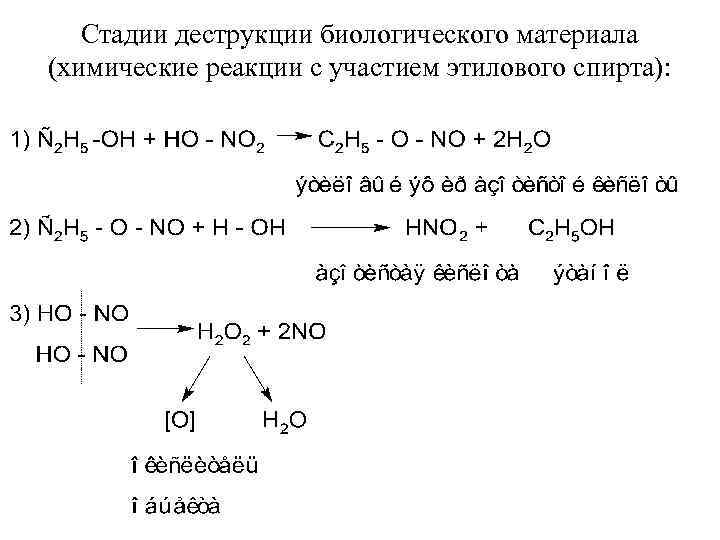
Стадии деструкции биологического материала (химические реакции с участием этилового спирта):

Б. Изолирование ртути из биологической жидкости (мочи). А. Ф. Рубцов и А. Н. Крылова [НИИСМ, 1975 г] предложили ускоренный деструктивный метод изолирования ртути из биологической жидкости (мочи). Окисление (деструкцию) объекта осуществляют с помощью окислителя калия перманганата в сернокислой среде.
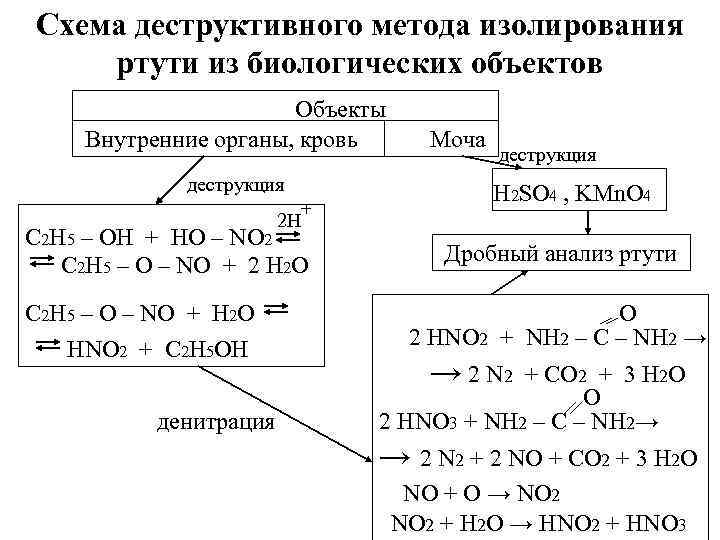
Схема деструктивного метода изолирования ртути из биологических объектов Объекты Внутренние органы, кровь деструкция + Моча деструкция H 2 SO 4 , KMn. O 4 2 H C 2 H 5 – OH + HO – NO 2 C 2 H 5 – O – NO + 2 H 2 O C 2 H 5 – O – NO + H 2 O HNO 2 + C 2 H 5 OH денитрация Дробный анализ ртути O 2 HNO 2 + NH 2 – C – NH 2 → → 2 N 2 + CO 2 + 3 H 2 O O 2 HNO 3 + NH 2 – C – NH 2→ → 2 N 2 + 2 NO + CO 2 + 3 H 2 O NO + O → NO 2 + H 2 O → HNO 2 + HNO 3
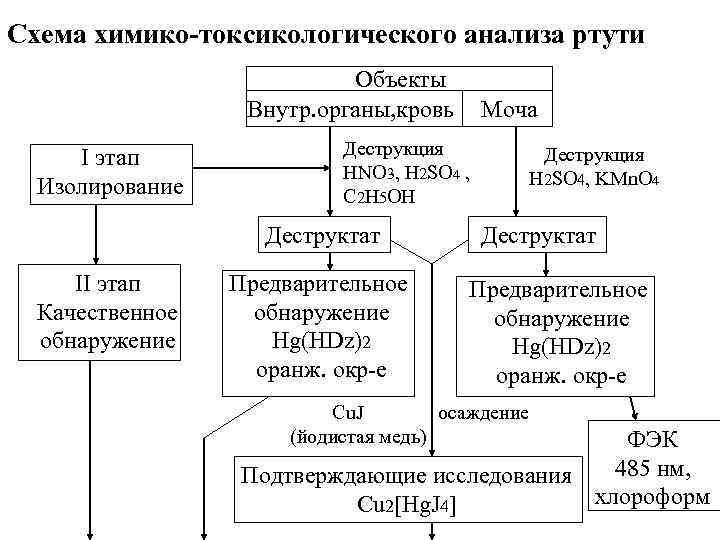
Схема химико-токсикологического анализа ртути Объекты Внутр. органы, кровь I этап Изолирование Деструкция HNO 3, H 2 SO 4 , C 2 H 5 OH Деструктат II этап Качественное обнаружение Моча Предварительное обнаружение Hg(HDz)2 оранж. окр-е Деструкция H 2 SO 4, KMn. O 4 Деструктат Предварительное обнаружение Hg(HDz)2 оранж. окр-е Cu. J осаждение (йодистая медь) ФЭК 485 нм, Подтверждающие исследования хлороформ Cu 2[Hg. J 4]
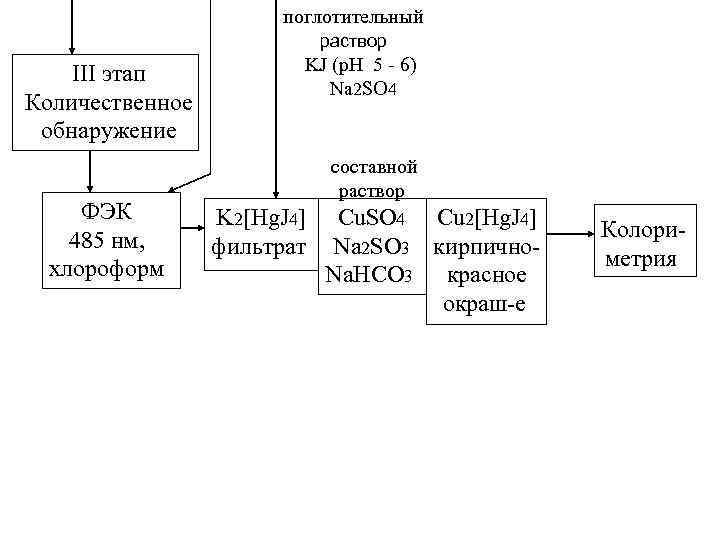
поглотительный раствор III этап Количественное обнаружение ФЭК 485 нм, хлороформ KJ (р. Н 5 - 6) Na 2 SO 4 составной раствор K 2[Hg. J 4] фильтрат Cu. SO 4 Cu 2[Hg. J 4] Na 2 SO 3 кирпично. Na. HCO 3 красное окраш-е Колориметрия

Спасибо за внимание!
лекция 3 (9 сем).ppt