Лекция 3 Парниковый эффект.pptx
- Количество слайдов: 89

Лекция 3 Глобальные экологические проблемы: разрушение стратосферного озона, физический смысл «парникового эффекта» , кислотные дожди.

Глобальная экология – это сложнейший раздел экологии. Задача глобальной экологии – изучение биосферы. Отличие глобальных проблем в том, что описываемые ими явления свойственны всему земному шару и касаются интересов существования всего человечества. Первоочередными глобальными проблемами современности являются: q проблемы загрязнения воздуха, воды, почв; q изменение температурного режима Земли; q уменьшение озонового экрана; q сохранение видового разнообразия жизни; q рост численности человечества и другие. В будущем, по-видимому, перед человечеством будут вставать всё новые и новые проблемы.

Разрушение стратосферного озона Серьёзную опасность представляет истончение озонового слоя. Образование озонового экрана, по мнению учёных, скорее всего, началось на раннем этапе Палеозойской эры 500 – 440 млн. лет назад. Достаточно мощным озоновый слой планеты стал в периоде палеозойской эры, более 400 млн. лет назад. Это способствовало образованию высокоорганизованной жизни на Земле.

История открытия Озоновый слой был открыт французскими физиками Шарлем Фабри и Анри Буиссоном. В 1913 году им удалось с помощью спектроскопических измерений ультрафиолетового излучения доказать существование озона в отдалённых от Земли слоях атмосферы.


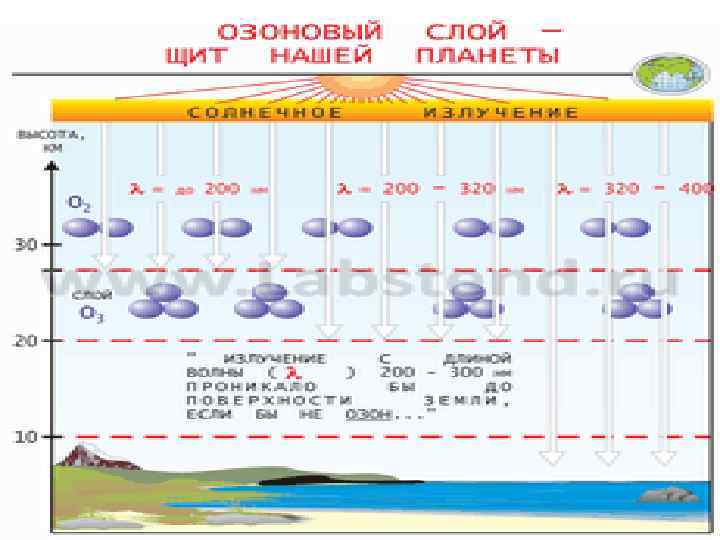
Озон – это трёхатомный кислород (О 3). В атмосфере Земли он присутствует до высоты 70 км. Основное количество озона сосредоточено в стратосфере на высоте от 10 до 50 км. В стратосфере его содержится 85 – 90 %. По этой причине стратосферу часто называют озоносферой. Максимальная концентрация озона на высоте 20 – 25 км. Основная часть озона образуется в стратосфере в результате воздействия УФизлучения Солнца с длиной волны менее 200 нм на кислород с образованием атомарного кислорода: О 2 + УФ → О + О При взаимодействии атомарного кислорода с молекулой кислорода (в присутствии третьих частиц – катализатора) образуется озон: О + О 2 + μ → О 3 + μ
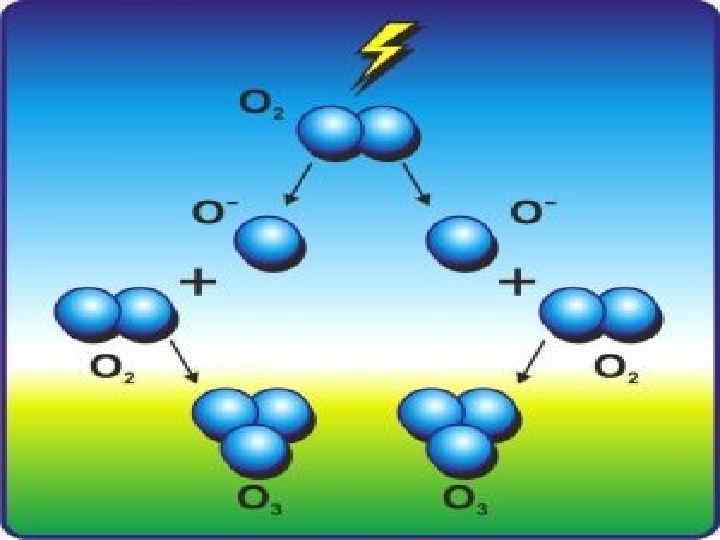

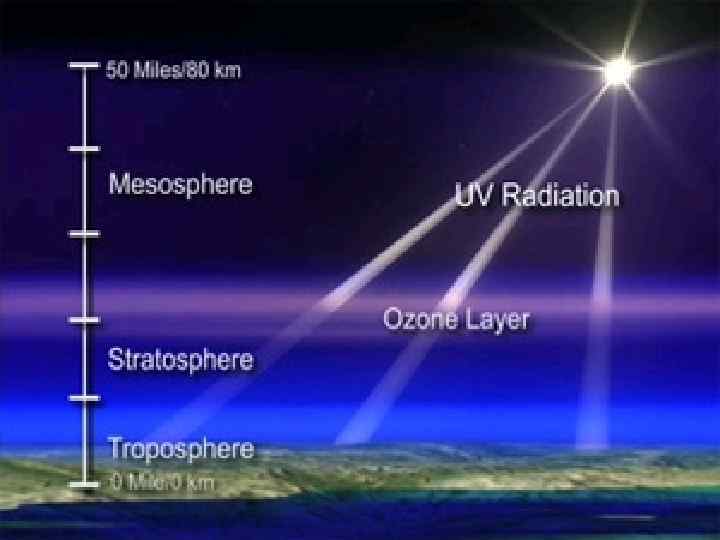

В приземных слоях атмосферы озон образуется из кислорода под воздействием электрического разряда (во время грозы) и других факторов. Основная масса озона образуется в экваториальной зоне и распространяется затем атмосферными движениями к полюсам. Низкое содержание озона на полюсах объясняется малой интенсивностью солнечного облучения полюсов. Содержание озона в атмосфере очень мало 3, 6 х10 -5. Если все молекулы озона из атмосферы распределить над поверхностью Земли, то толщина образовавшейся оболочки составит лишь 3 мм для среднегодовых среднеглобальных условий (т. е. при t=15°C и р=1 атм. у поверхности Земли).


Озон чрезвычайно ядовит. ПДК его в воздухе 0, 00001%. Его применяют для очистки воды и воздуха от микроорганизмов (озонирование). В отличии от кислорода озон неустойчив и легко переходит в двухатомный кислород. Озон более сильный окислитель, чем кислород. Он имеет исключительные свойства для сохранения жизни на Земле. Важное свойство озона – способность практически полностью поглощать коротковолновые УФ-излучения с λ=200 -280 нм и около 90% УФ - излучения с λ=280 -320 нм, которые губительны для всего живого на планете О 3 + УФ → О 2 + О


В целом озоновый слой поглощает около 13% солнечной энергии. До Земли доходят только длинноволновые УФ - излучения с λ=290 -380 нм. Содержание озона в атмосфере непостоянно, увеличивается весной и уменьшается осенью и зимой. В состоянии динамического равновесия между синтезом и распадом озона его концентрация периодически меняется на 0, 5 -1% от среднего уровня.

Начиная с 1980 г. содержание озона в атмосфере постепенно понижается, и значительно превысило нормальные колебания. Истончение озонового слоя началось предположительно с 70 -х годов ХХ века. За последние 10 лет содержание озона в северном полушарии уменьшилось по разным оценкам от 2 до 10% от нормы. Ученые считают, что на каждый процент сокращения концентрации озона происходит увеличение интенсивности УФ - излучений у поверхности Земли на 15%, поток УФ - излучений с λ<280 нм увеличивается.


Специалисты рассчитали, что при снижении концентрации озона на 1% количество заболеваний раком кожи возрастёт на 6 -10 тыс. человек в год, случаев катаракты увеличится на 100 тыс. человек в год, усилится парниковый эффект, снизится урожайность, увеличится число лесных пожаров и т. д.

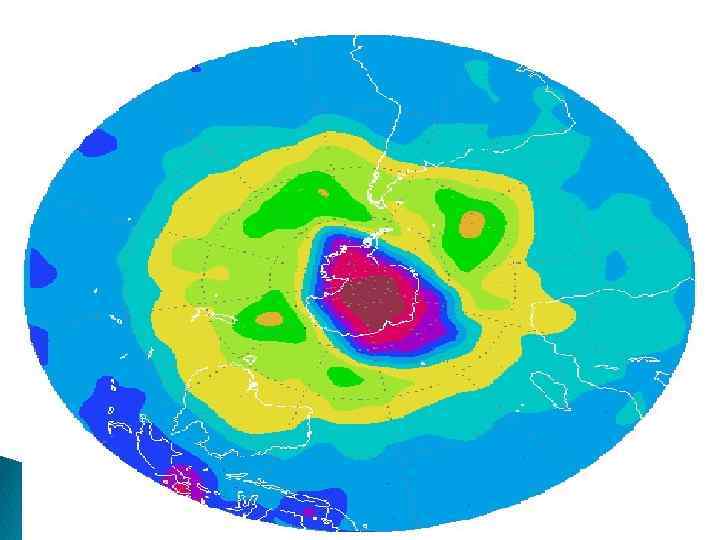
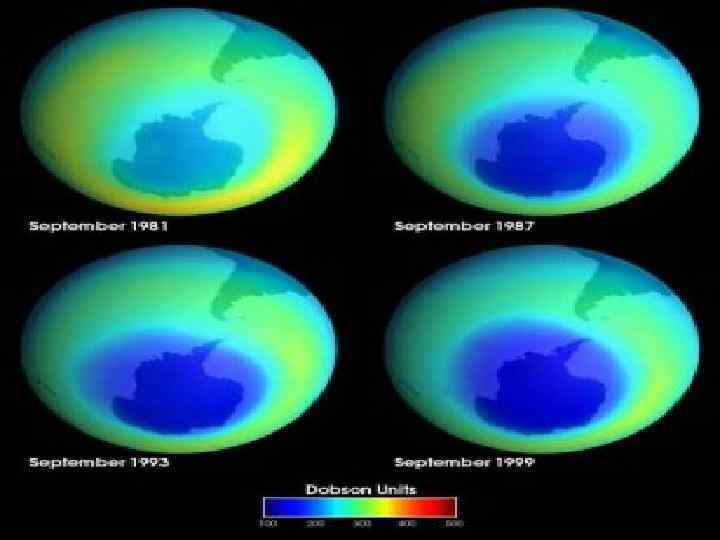
Пространство, в пределах которого регистрируется заметное уменьшение концентрации озона, называется «озоновой дырой» . «Озоновая дыра» впервые была обнаружена в 1985 году над Антарктидой американским учёным Д. Фарманом. За последние 30 лет количество озона здесь уменьшилось на 40 -50%. Меньшая по размерам «озоновая дыра» расположена над Антарктикой, содержание озона уменьшилось здесь на 20 -40% от нормы.

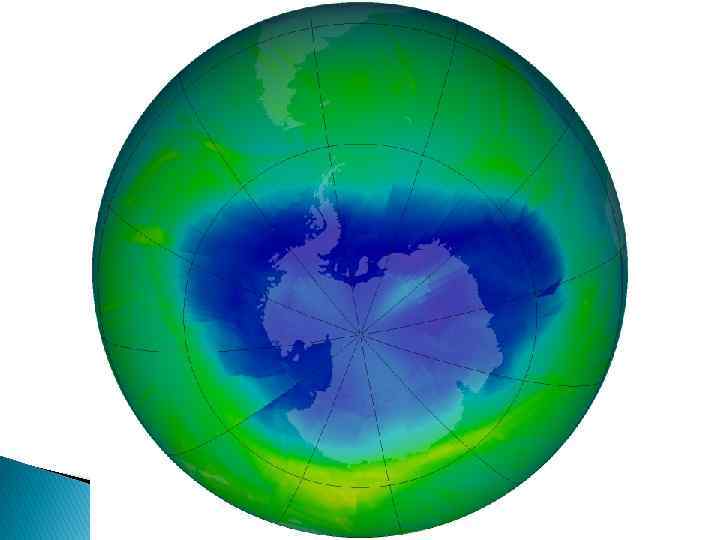
Антарктическая озоновая дыра
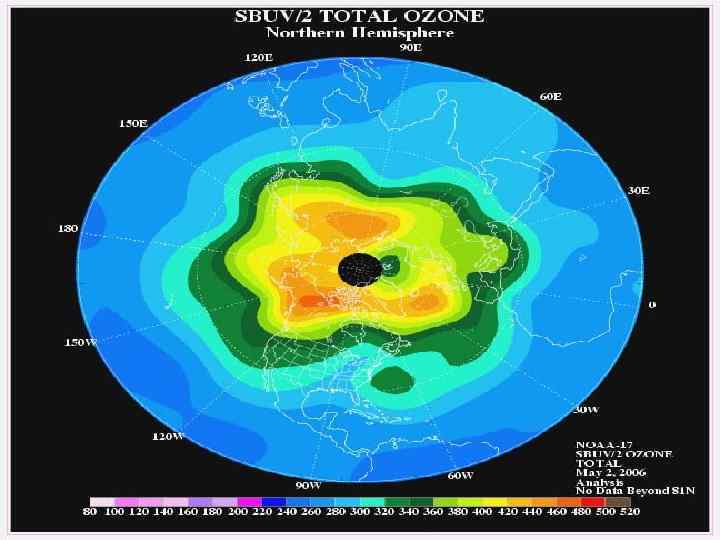

В других районах появляются т. н. «блуждающие дыры» площадью от 10 до 100 тыс. км 2, потери озона составляют от 20 до 40%. В последние годы озоновые дыры образуются над Сибирью, Западной и Центральной Европой. Концентрация озона уменьшилась здесь на 5% по сравнению со среднемноголетним значением. Размеры «озоновых дыр» и содержание в них озона могут изменяться в значительных пределах. Например, над Антарктидой «озоновая дыра» по площади составляет приблизительно 10 млн. км 2 и уже вышла за пределы этого континента.

Причины, вызывающие количества озона в атмосфере: колебания üЕстественные физико-географические факторы: циклические изменения солнечной активности (11 летние циклы); ü изменение притока УФ – радиации и космического излучения; üвыброс вулканических газов при извержениях, разрушающих озон; üсверхураганные скорости воздушных потоков, переносящих разрушители озона и сам озон на большие территории; üвихревые восходящие потоки над Антарктидой, способствующие рассеиванию озона и др.
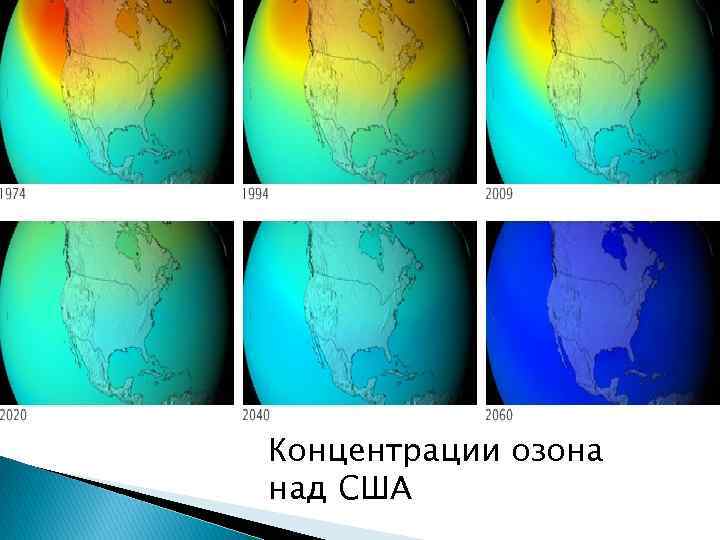
Концентрации озона над США

üАнтропогенные факторы: Основные причины уменьшения озона связаны с техногенным загрязнением атмосферы, выбросами промышленности и транспорта. Озон вступает в активные фотохимические реакции с фреонами (СFCl 3 – фреон-11, CF 2 Cl 2), оксидами азота (NO, NO 2) и др. газообразными загрязняющими веществами.


Наиболее опасный разрушитель (катализатор распада) озона – хлор. Значительная часть хлора и фтора образуется в стратосфере под действием УФ - излучений из фреонов, которые являются основным антропогенным фактором. Фреоны способны находиться в атмосфере от 70 до 100 лет, поэтому они всегда достигают озонового слоя и разрушают его. Много хлора попадает в атмосферу при утечках и авариях в химической промышленности. В результате фотохимической реакции фреоны разлагаются по радикальному механизму с образованием атомарного хлора: СFCl 3 + УФ → СFCl 2 + Cl CFCl 2 + УФ → CFCl + Cl

Атомарный хлор активно соединяется с озоном, образуя монооксид хлора и кислород: Сl + O 3 → Cl. O + O 2 Затем монооксид хлора легко присоединяет второй атом кислорода, при этом хлор освобождается и может присоединить второй атом озона: Cl. O + O → Cl + O 2 Одна молекула хлора за среднее время своего существования в верхних слоях атмосферы способна разложить до 100 тыс. молекул озона.

Менее активными разрушителями озона по сравнению с хлором являются оксиды азота. Одна молекула оксида азота разлагает около 10 молекул озона. Но содержание оксидов азота в воздухе намного больше чем хлора, поэтому этот фактор значительный. N 2 O + УФ → NO + N NO + УФ → NO 2 + N 2 NO 2 + УФ → 2 NO + O 2 Источниками попадания хлора и оксидов азота в атмосферу являются также выхлопы двигателей реактивной авиации, запуск космических ракет разного назначения, испытания атомного оружия в атмосфере, уничтожение лесов – основных поставщиков кислорода в атмосферу.



Менее значительные разрушители озона – оксид углерода (СО), водород, оксиды серы. Они связывают озон в отношении 1: 1 и, по сравнению с хлором и оксидами азота, могут

• -22 марта 1985 года Венская конвенция «Об охране озонового слоя» • 16 сентября 1987 года Монреальский протокол «По веществам, разрушающим озоновый слой» в 1990 году т. н. Лондонские изменения; - в 1992 году т. н. Копенгагенские изменения; - в 1997 году т. н. Монреальские изменения; - в 1999 году т. н. Пекинские изменения


Физический смысл «парникового эффекта» солнечная радиация. Она поставляет 99, 98% всего тепла на земную поверхность. Второй (незначительный) источник тепла – внутреннее тепло планеты. Большая часть солнечной энергии отражается (отражающая способность планеты называется альбедо; отражающие поверхности: облачный слой, полярные высокогорные льды, пустыни, запылённость атмосферы и пр. ) от верхней границы атмосферы, верхних слоёв облаков и земной поверхности – 33% и поглощается атмосферой – 20%. 47% всех видов солнечной энергии достигает земной поверхности в виде прямой и рассеянной радиации, нагревает её и участвует в фотохимических реакциях.


Исторические сведения Парниковый эффект был обнаружен Жозефом Фурье 1824 Впервые был количественно исследован Сванте Аррениусом 1896

Нагреваясь за счёт поглощения солнечной, главным образом коротковолновой, радиации, земная поверхность становится источником земного, в основном длинноволнового ИК - излучения, которое почти полностью поглощается атмосферой. Аккумуляция тепла – важнейшее свойство атмосферы. Основной поглотитель этого излучения – водяной пар. Благодаря этому современная средняя температура воздуха у поверхности Земли составляет 14, 6°С и отражает динамическое равновесие между приходящей и уходящей радиацией. Если бы тепло атмосферой не аккумулировалось, то температура равнялась бы минус 21°С. Биосфера Земли способна к саморегуляции теплового баланса.
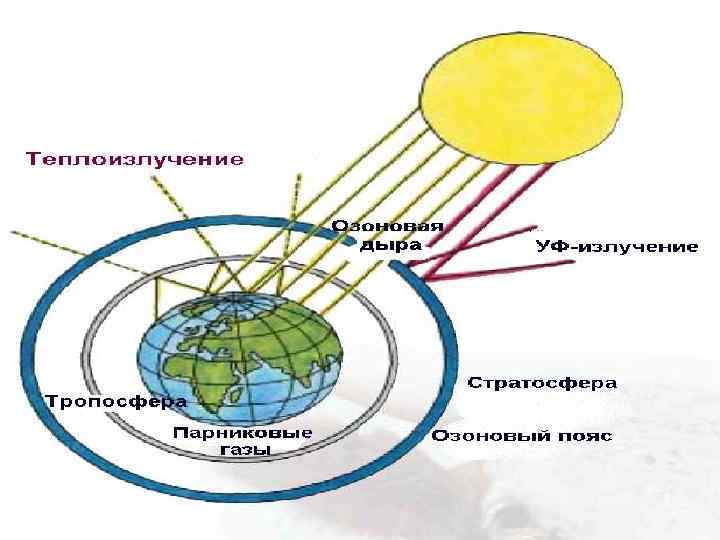

Другими интенсивными поглотителями инфракрасного излучения Земли являются некоторые газы-загрязнители. Они действуют как стекло в парнике. Они беспрепятственно пропускают к Земле УФ и видимые лучи солнечной радиации, но задерживают тепловое ИК-излучение Земли. В результате повышается температура поверхности Земли, изменяется погода и климат. Эти газы называются парниковые. Известно около 30 парниковых газов.

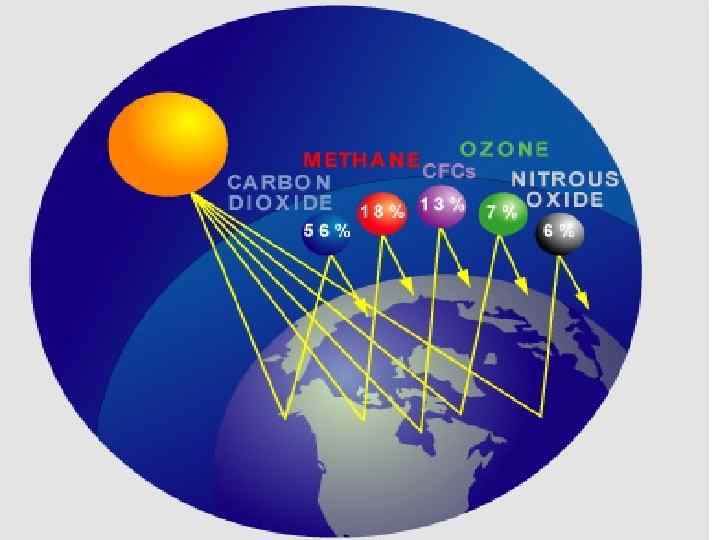


оосновной парниковый газ СО 2. Его вклад в парниковый эффект 50 -65%. Именно с ним связывают изменение климата. Отмечаются сезонные изменения, а также постоянное увеличение из года в год концентрации углекислого газа. Сезонные изменения объясняются большим потреблением СО 2 растениями весной и летом, уменьшая его в атмосфере. Основной антропогенный источник поступления СО 2 в атмосферу – сжигание углеродсодержащего топлива (уголь, нефть, мазут, метан и др. ) и вырубка лесов (основных поглотителей СО 2). Другими парниковыми газами являются: СН 4 (его доля в парниковом эффекте 20%); NO 2 (5%); фреоны, озон и др. газы (10 -25%).

Парниковый эффект – это возможное повышение глобальной температуры планеты в результате изменения теплового баланса, обусловленное постепенным накоплением парниковых газов в атмосфере.

Из-за парникового эффекта среднегодовая температура на Земле за последнее столетие повысилась на 0, 3 -0, 6°С. Концентрация СО 2 увеличивается на 0, 3 -0, 5% в год, содержание метана увеличивается на 1%, оксидов азота – на 0, 2% в год. При удвоении содержания парниковых газов среднегодовая температура планеты увеличится на 1 -3, 5°С. Как известно даже небольшие амплитуды всего на 1 -2°С изменения средних температур на поверхности Земли приводят к значительным, вплоть до катастрофических засухам или наводнениям, изменениям погодных условий на больших территориях. В связи с изменением климата учёные предполагают различные сценарии последствий.



Наиболее распространённое представление, что потепление климата вызовет таяние ледников Гренландии и Антарктиды, подъём уровня мирового океана и затопление низменных территорий, и другие неблагоприятные для человечества последствия. Многие учёные рассматривают это как катастрофу для биосферы в целом. За счёт увеличения температуры и таяния ледников и полярных льдов в ближайшие 25 лет ожидается увеличение уровня мирового океана на 10 см.



Одновременно с продуктами сгорания в атмосферу за год выбрасывается около 100 млн. т твёрдых частиц. С 1940 по 1980 гг. температура воздуха повысилась на 0, 6°С, а затем понизилась на 0, 4°С при постоянном росте СО 2. Предполагается, что охлаждение связано с выбросом в атмосферу техногенной пыли, которая уменьшает проницаемость для солнечных лучей.



Повышение t может увеличить содержание в атмосфере водяных паров, которые также адсорбируют инфракрасное излучение, и увеличит t. Или увеличение содержания водяных паров приведёт к усилению облачного покрова, уменьшая солнечную радиацию и смягчая t эффект. Можно утверждать, что >t повлечёт за собой уменьшение шапок полярного льда и снижение отражённой концентрации радиации. Или что >t воды в океане снизит интенсивность циркуляции воды и уменьшит поглощение СО 2.

Кислотные дожди. Еще одна острая проблема, являющаяся следствием резкого увеличения загрязнения атмосферы. Кислотность дождевой воды в норме должна составлять р. Н=5, 6 -5, 7. В последние 15 -20 лет кислотность дождей составляет р. Н<5. Основная причина выпадения кислотных дождей – попадание в атмосферу оксидов серы и азота. При взаимодействии их с атмосферной влагой образуются азотная и серная кислоты. К ним примешиваются органические кислоты.

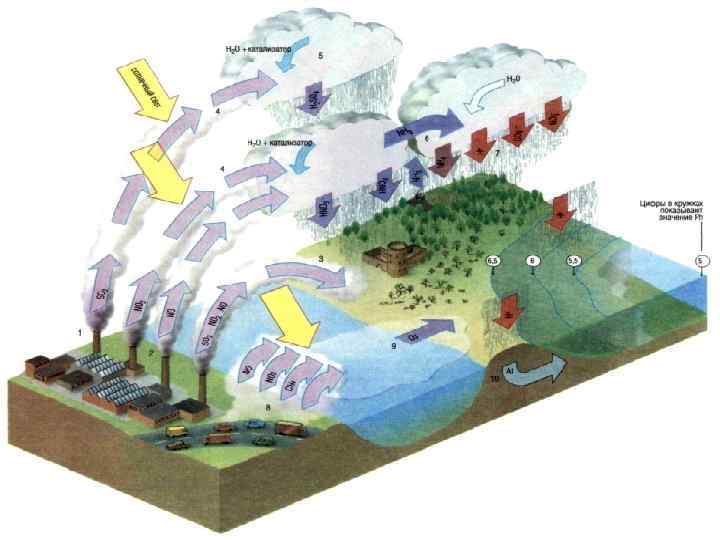

Tермин «кислотный дождь» был введен в 1872 году английским исследователем Робертом Ангусом Смитом во время изучения смога в Манчестере. Впервые кислотные дожди были отмечены в Западной Европе, в частности Скандинавии, и Северной Америке в 1950 -х гг. Сейчас эта проблема существует во всем Индустриальном мире и приобрела особое значение в связи с возросшими техногенными выбросами оксидов серы и азота

За несколько десятилетий размах этого бедствия стал настолько широк, а отрицательные последствия столь велики, что в 1982 г. в Стокгольме состоялась специальная международная конференция по кислотным дождям, в которой приняли участие представители 20 стран и ряда международных организаций. До сих пор острота этой проблемы сохраняется, она постоянно в центре внимания национальных правительств и международных Природоохранных организаций. Сообщили синоптики и тревожную новость. В дождях, которые пройдут в столице, может содержаться повышенное содержание кислотных и щелочных солей. Вредные вещества может принести в Московский регион облако, возникшее в результате извержения вулкана Эйяфьятлайокудль в Исландии 14 апреля, сообщили РИА «Новости» в Гидрометеобюро Москвы
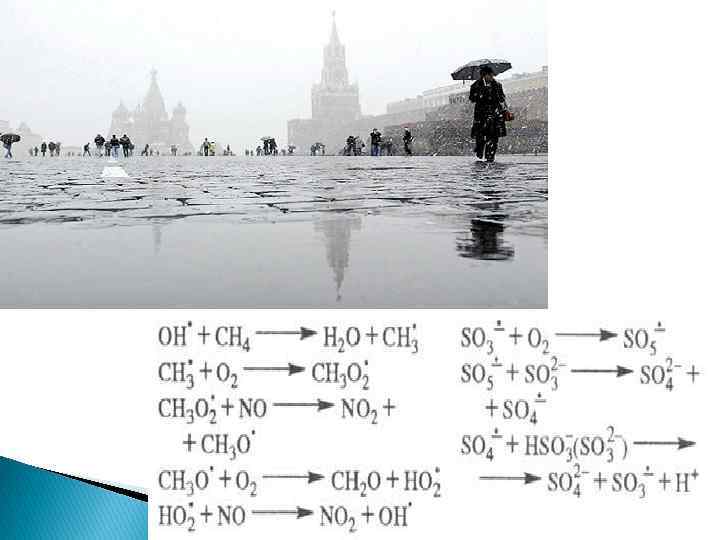

Специфическая особенность кислотных дождей – их трансграничный характер, обусловленный переносом кислотообразующих выбросов воздушными течениями на большие расстояния – сотни и даже тысячи километров. Этому в немалой степени способствует принятая некогда «политика высоких труб» как эффективное средство против загрязнения приземного воздуха. Почти все страны одновременно являются «экспортерами» своих и «импортерами» чужих выбросов. Наибольший вклад в трансграничное подкисление природной среды России соединениями серы вносят Украина, Польша, Германия. В свою очередь, из России больше всего окисленной серы направляется в страны Скандинавии.


Диоксид серы, попавший в атмосферу, претерпевает ряд химических превращений, ведущих к образованию кислот. Частично диоксид серы в результате фотохимического окисления превращается в триоксид серы (серный ангидрид) SО 3: 2 SO 2 + O 2 2 SO 3, который реагирует с водяным паром атмосферы, образуя аэрозоли серной кислоты: SO 3 + Н 2 O Н 2 SO 4. Основная часть выбрасываемого диоксида серы во влажном воздухе образует кислотный полигидрат SО 2 • n. H 2 O, который часто называют сернистой кислотой и изображают условной формулой Н 2 SО 3: SO 2 + H 2 O H 2 SO 3. Сернистая кислота во влажном воздухе постепенно окисляется до серной: 2 Н 2 SО 3 + О 2 2 Н 2 SO 4.

При сжигании топлива образуются твердые микрочастицы сульфатов металлов (в основном при сжигании угля), легко растворимые в воде, которые осаждаются на почву и растения, делая кислотными росы. Аэрозоли серной и сернистой кислот составляют около 2/3 кислотных осадков, остальное приходится на долю аэрозолей азотной и азотистой кислот, образующихся при Взаимодействии диоксида азота с водяным паром атмосферы: 2 NО 2 + Н 2 О НNО 3 + НNО 2.

Диоксид серы образуется при сжигании богатого серой Горючего, такого, как уголь и мазут (содержание серы в них колеблется от 0, 5 до 5– 6%), на электростанциях (~40% Антропогенного поступления в атмосферу), в металлургических производствах, при переработке содержащих серу руд, при различных химических технологических процессах и работе ряда предприятий машиностроительной отрасли промышленности (~50%). При сжигании каждого миллиона тонн угля выделяется около 25 тыс. т серы в виде главным бразом ее диоксида (до триоксида окисляется менее 3% серы); в 4– 5 раз меньше окисленной серы дает сжигание мазута.


Природные поступления в атмосферу оксидов азота связаны главным образом с электрическими разрядами, при которых образуется NО, в последcтвии – NО 2. Значительная часть оксидов азота природного происхождения перерабатывается в почве микроорганизмами, т. е. включена в биохимический круговорот. Оксиды азота техногенного происхождения образуются при сгорании топлива, особенно если температура превышает 1000 °С. При высоких температурах часть молекулярного азота окисляется до оксида азота NО, который в воздухе немедленно вступает в реакцию с кислородом, образуя диоксид NO 2 и N 2 O 4. Первоначально образующийся диоксид азота составляет лишь 10% выбросов всех оксидов азота в атмосферу, однако в воздухе значительная часть оксида азота превращается в диоксид – гораздо более опасное соединение.


Первыми жертвами кислотных дождей стали озера и реки. Сотни озер в Скандинавии, на северо-востоке США и на юговостоке Канады, в Шотландии превратились в кислотные водоемы. Кислотные дожди привели к резкому снижению продуктивности 2500 озер Швеции. В Норвегии примерно половина поверхностных вод имеет повышенную кислотность, из 5000 озер в 1750 исчезла рыба. В провинции Онтарио (Канада) пострадало 20% озер, а в провинции Квебек – до 60% озер. Закисленная и токсичная вода разрушает скелеты рыб и раковины моллюсков, а главное – снижает репродуктивные процессы. В свою очередь, это приводит к сокращению популяций наземных животных и птиц, связанных с водной биотой трофическими цепями (цепи питания).



Многие скульптуры и здания в Риме, Венеции и других городах, памятники зодчества за несколько последних Десятилетий получили значительно большие повреждения, чем за все предыдущее время. Металлы под действием кислотных дождей, туманов и рос разрушаются еще быстрее, чем строительные материалы и стекло. Корка образующегося на поверхности железных изделий гигроскопичного сульфата железа (II) окисляется кислородом воздуха, при этом образуется основная соль сульфата железа (III), являющаяся составной частью ржавчины:



Загрязнение воздуха кислотообразующими выбросами оказывает многообразное вредное влияние и на организм человека. Многочисленные исследования показали увеличение числа заболеваний дыхательных путей в районах, воздух которых загрязнен диоксидом азота NО. Попадая в дыхательные пути, он взаимодействует с гемоглобином крови, затрудняя перенос кислорода к органам и тканям, вызывает респираторные, астматические и сердечные заболевания. В феврале 1972 г. в Японии по этой причине заболело более 70 000 человек, для многих из них заболевание имело летальный исход.

Почвенное подкисление считается одной из основных причин усыхания лесов умеренной зоны северного полушария, причем этот фактор долгодействующий, который может проявиться через много лет после прекращения вредных кислотообразующих выбросов в атмосферу. Больше всего страдают елово-пихтовые и дубовые леса.


Кислотные дожди загрязняют и отрицательно влияют на все компоненты биосферы: почвы, водные экосистемы, животных и растения, а также разрушают памятники архитектуры, строения и др. объекты. Поступая в почву, кислотные дожди растворяют минералы (К, Са, Аl) и уносят их в подпочвенный слой, лишая растения основных источников питания. Аl, тяжелые металлы и нитраты вместе с кислотными дождями проникают в грунтовые воды, а затем в водопроводную сеть. Попадая в водоемы кислотные осадки повышают кислотность и жесткость воды.


Лекция 3 Парниковый эффект.pptx