organ_himia3.pptx
- Количество слайдов: 23
 Лекция 3 Гидроксисоединения – это вещества которые в своем составе содержат гидроксильную группу ОН. К ним относятся: спирты, фенолы, и др. классы органических соединений. Спирты – это гидроксильные соединения, в которых –ОН группы связаны с насыщенными атомами углерода, находящимся в состоянии Sp 3 – гибридизации. Общая формула спиртов: R – OH.
Лекция 3 Гидроксисоединения – это вещества которые в своем составе содержат гидроксильную группу ОН. К ним относятся: спирты, фенолы, и др. классы органических соединений. Спирты – это гидроксильные соединения, в которых –ОН группы связаны с насыщенными атомами углерода, находящимся в состоянии Sp 3 – гибридизации. Общая формула спиртов: R – OH.
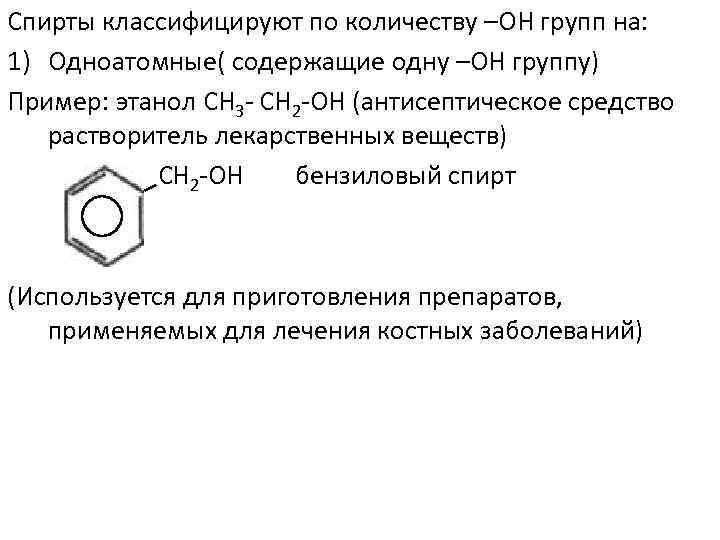 Спирты классифицируют по количеству –ОН групп на: 1) Одноатомные( содержащие одну –ОН группу) Пример: этанол СН 3 - СН 2 -ОН (антисептическое средство растворитель лекарственных веществ) СН 2 -ОН бензиловый спирт (Используется для приготовления препаратов, применяемых для лечения костных заболеваний)
Спирты классифицируют по количеству –ОН групп на: 1) Одноатомные( содержащие одну –ОН группу) Пример: этанол СН 3 - СН 2 -ОН (антисептическое средство растворитель лекарственных веществ) СН 2 -ОН бензиловый спирт (Используется для приготовления препаратов, применяемых для лечения костных заболеваний)
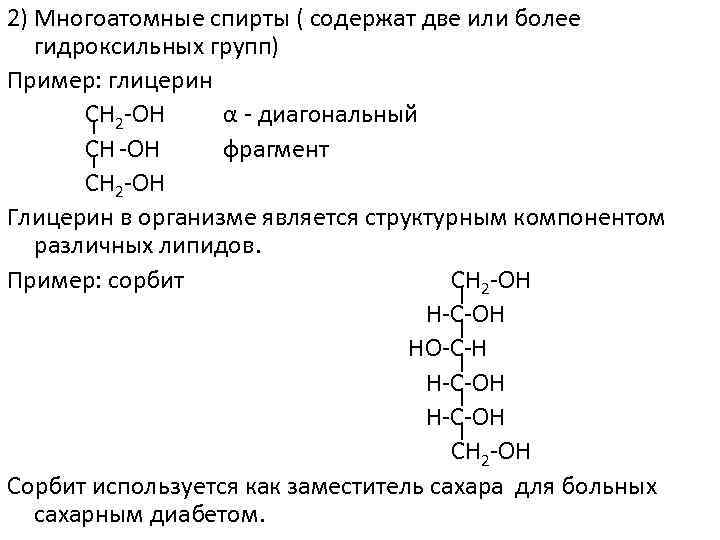 2) Многоатомные спирты ( содержат две или более гидроксильных групп) Пример: глицерин СН 2 -ОН α - диагональный СН -ОН фрагмент СН 2 -ОН Глицерин в организме является структурным компонентом различных липидов. Пример: сорбит СН 2 -ОН Н-С-ОН НО-С-Н Н-С-ОН СН 2 -ОН Сорбит используется как заместитель сахара для больных сахарным диабетом.
2) Многоатомные спирты ( содержат две или более гидроксильных групп) Пример: глицерин СН 2 -ОН α - диагональный СН -ОН фрагмент СН 2 -ОН Глицерин в организме является структурным компонентом различных липидов. Пример: сорбит СН 2 -ОН Н-С-ОН НО-С-Н Н-С-ОН СН 2 -ОН Сорбит используется как заместитель сахара для больных сахарным диабетом.
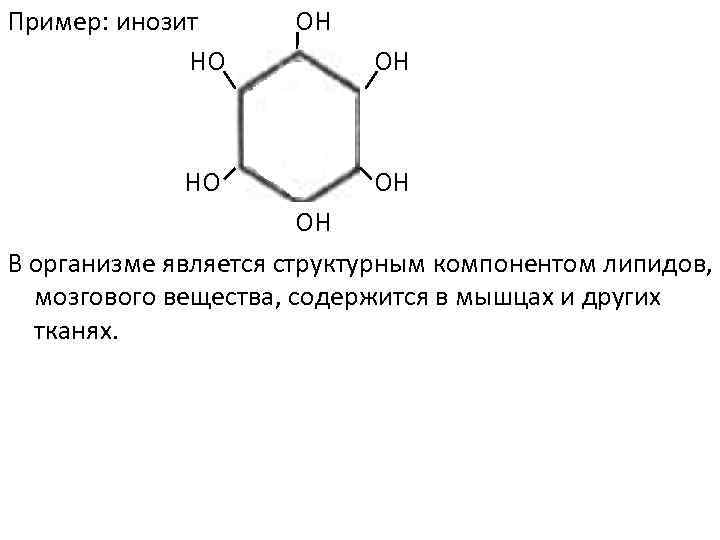 Пример: инозит НО НО ОН ОН В организме является структурным компонентом липидов, мозгового вещества, содержится в мышцах и других тканях.
Пример: инозит НО НО ОН ОН В организме является структурным компонентом липидов, мозгового вещества, содержится в мышцах и других тканях.
 В зависимости от характера звеньев атома углерода, с которыми соединены –ОН группы спирты классифицируются на: 1) Первичные, в которых –ОН группа связана с первичным звеном атома углерода. Пр. СН 3 -СН 2 -ОН Пропанол – 1 2) Вторичные, в которых –ОН группа находится у второго звена атома углерода. Пр. СН 3 -СН-СН 3 ОН Пропанол - 2
В зависимости от характера звеньев атома углерода, с которыми соединены –ОН группы спирты классифицируются на: 1) Первичные, в которых –ОН группа связана с первичным звеном атома углерода. Пр. СН 3 -СН 2 -ОН Пропанол – 1 2) Вторичные, в которых –ОН группа находится у второго звена атома углерода. Пр. СН 3 -СН-СН 3 ОН Пропанол - 2
 3) третичные, -ОН группа находится у третичного звена атома углерода. Пр. СН 3 -С-СН 3 2 – метилпропанол – 2 ОН Химические свойства спиртов 1) Реакции окисления спиртов В организме реакции окисления спиртов протекают в присутствии ферментов, в которых находится дегидрогеназы. При этом молекула спирта отщепляет два атома водорода что эквивалентно отдаче 2 -х протонов H+ , и двух электронов, или 1 H+ и 1 гидридиона H-
3) третичные, -ОН группа находится у третичного звена атома углерода. Пр. СН 3 -С-СН 3 2 – метилпропанол – 2 ОН Химические свойства спиртов 1) Реакции окисления спиртов В организме реакции окисления спиртов протекают в присутствии ферментов, в которых находится дегидрогеназы. При этом молекула спирта отщепляет два атома водорода что эквивалентно отдаче 2 -х протонов H+ , и двух электронов, или 1 H+ и 1 гидридиона H-
 а) окисление первичных спиртов Н Над+ Н СН 3 -СН 2 -СН-ОН СН 3 -СН 2 -С=О + Над. Н + H+ б) окисление вторичных спиртов Над+ СН 3 -СН-СН 3 -С-СН 3 + Над. Н + H+ ОН О т. е при окислении первичных спиртов образуются альдегиды, а при окислении вторичных – кетоны.
а) окисление первичных спиртов Н Над+ Н СН 3 -СН 2 -СН-ОН СН 3 -СН 2 -С=О + Над. Н + H+ б) окисление вторичных спиртов Над+ СН 3 -СН-СН 3 -С-СН 3 + Над. Н + H+ ОН О т. е при окислении первичных спиртов образуются альдегиды, а при окислении вторичных – кетоны.
 2) Реакции нуклеофильного замещения (Sn) S – замещение N – нуклеофильное α+ α- С – X + ν: -C–ν+X: субстрат нуклео- (продукт) уходящая группа нуклеофила фильный реагент Рассмотрим механизм реакции нуклеофильного замещения на примере получения хлорэтана из этанола.
2) Реакции нуклеофильного замещения (Sn) S – замещение N – нуклеофильное α+ α- С – X + ν: -C–ν+X: субстрат нуклео- (продукт) уходящая группа нуклеофила фильный реагент Рассмотрим механизм реакции нуклеофильного замещения на примере получения хлорэтана из этанола.
 Пр. Субстрат этанол Н СН 3 - СН 2 -ОН + НСL => СН 3 - СН 2 -О-Н + CL- : => СН 3 - СН 2 - CL + Плохая уход. Гр. Ион этилоксония прод. Хлорэтан. + Н 2 О хорошая уход. Гр. Поскольку – ОН группа в составе субстрата этана является плохоуходящей группой, то прямое нуклеофильное замещение осуществить невозможно, поэтому –ОН группу в присутствии ионов водорода H+, переводят в группировку, при этом образуется промежуточный ион этилоксония, от которого отделяется молекула воды – хорошо уходящая группа. Реагент – нуклеофил CL- : (с парой электронов) присоединяется к атому углерода субстрата, образуя продукт – хлорэтан, который в медицинской практике используется для ингаляционного наркоза.
Пр. Субстрат этанол Н СН 3 - СН 2 -ОН + НСL => СН 3 - СН 2 -О-Н + CL- : => СН 3 - СН 2 - CL + Плохая уход. Гр. Ион этилоксония прод. Хлорэтан. + Н 2 О хорошая уход. Гр. Поскольку – ОН группа в составе субстрата этана является плохоуходящей группой, то прямое нуклеофильное замещение осуществить невозможно, поэтому –ОН группу в присутствии ионов водорода H+, переводят в группировку, при этом образуется промежуточный ион этилоксония, от которого отделяется молекула воды – хорошо уходящая группа. Реагент – нуклеофил CL- : (с парой электронов) присоединяется к атому углерода субстрата, образуя продукт – хлорэтан, который в медицинской практике используется для ингаляционного наркоза.
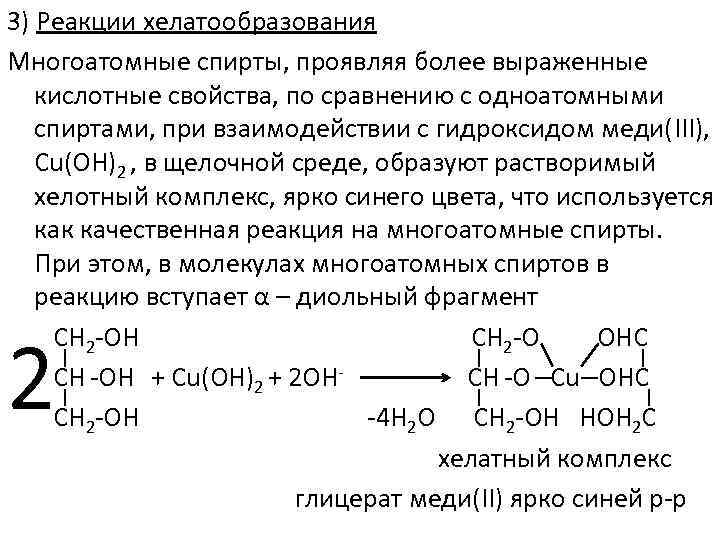 3) Реакции хелатообразования Многоатомные спирты, проявляя более выраженные кислотные свойства, по сравнению с одноатомными спиртами, при взаимодействии с гидроксидом меди(III), Cu(OH)2 , в щелочной среде, образуют растворимый хелотный комплекс, ярко синего цвета, что используется как качественная реакция на многоатомные спирты. При этом, в молекулах многоатомных спиртов в реакцию вступает α – диольный фрагмент СН 2 -ОН СН 2 -О OHC СН -ОН + Cu(OH)2 + 2 OHСН -О Сu OHC СН 2 -ОН -4 Н 2 О СН 2 -ОН HOН 2 С хелатный комплекс глицерат меди(II) ярко синей р-р 2
3) Реакции хелатообразования Многоатомные спирты, проявляя более выраженные кислотные свойства, по сравнению с одноатомными спиртами, при взаимодействии с гидроксидом меди(III), Cu(OH)2 , в щелочной среде, образуют растворимый хелотный комплекс, ярко синего цвета, что используется как качественная реакция на многоатомные спирты. При этом, в молекулах многоатомных спиртов в реакцию вступает α – диольный фрагмент СН 2 -ОН СН 2 -О OHC СН -ОН + Cu(OH)2 + 2 OHСН -О Сu OHC СН 2 -ОН -4 Н 2 О СН 2 -ОН HOН 2 С хелатный комплекс глицерат меди(II) ярко синей р-р 2
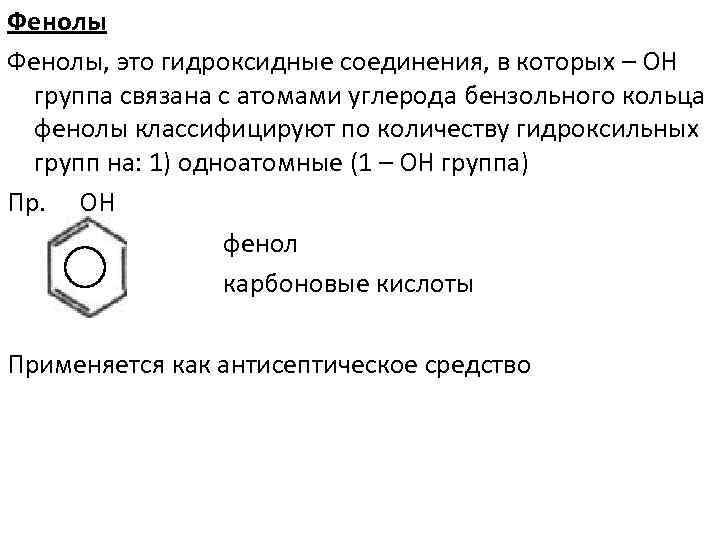 Фенолы, это гидроксидные соединения, в которых – ОН группа связана с атомами углерода бензольного кольца фенолы классифицируют по количеству гидроксильных групп на: 1) одноатомные (1 – ОН группа) Пр. ОН фенол карбоновые кислоты Применяется как антисептическое средство
Фенолы, это гидроксидные соединения, в которых – ОН группа связана с атомами углерода бензольного кольца фенолы классифицируют по количеству гидроксильных групп на: 1) одноатомные (1 – ОН группа) Пр. ОН фенол карбоновые кислоты Применяется как антисептическое средство
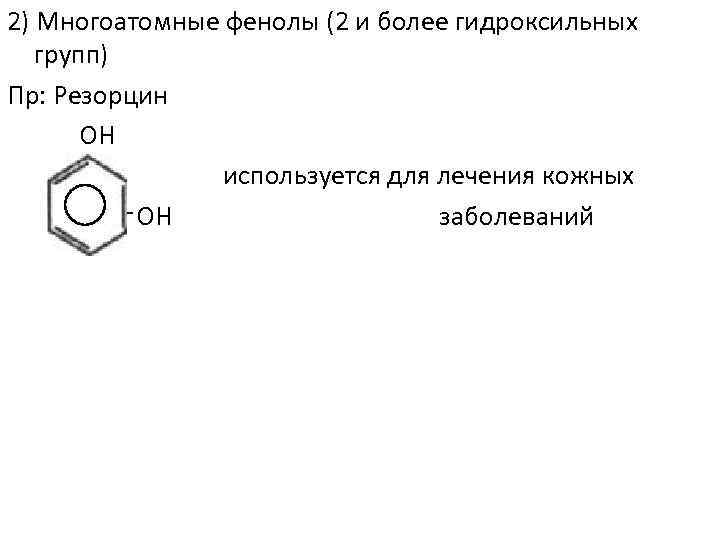 2) Многоатомные фенолы (2 и более гидроксильных групп) Пр: Резорцин ОН используется для лечения кожных ОН заболеваний
2) Многоатомные фенолы (2 и более гидроксильных групп) Пр: Резорцин ОН используется для лечения кожных ОН заболеваний
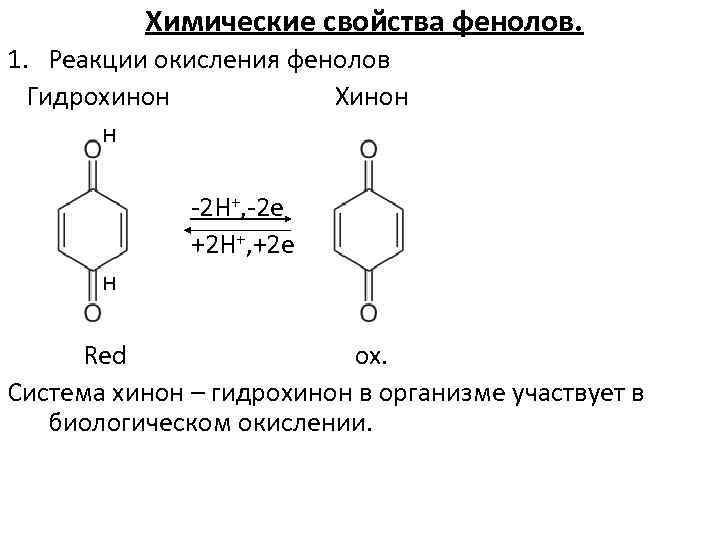 Химические свойства фенолов. 1. Реакции окисления фенолов Гидрохинон Хинон н -2 H+, -2 e +2 H+, +2 e н Red ox. Система хинон – гидрохинон в организме участвует в биологическом окислении.
Химические свойства фенолов. 1. Реакции окисления фенолов Гидрохинон Хинон н -2 H+, -2 e +2 H+, +2 e н Red ox. Система хинон – гидрохинон в организме участвует в биологическом окислении.
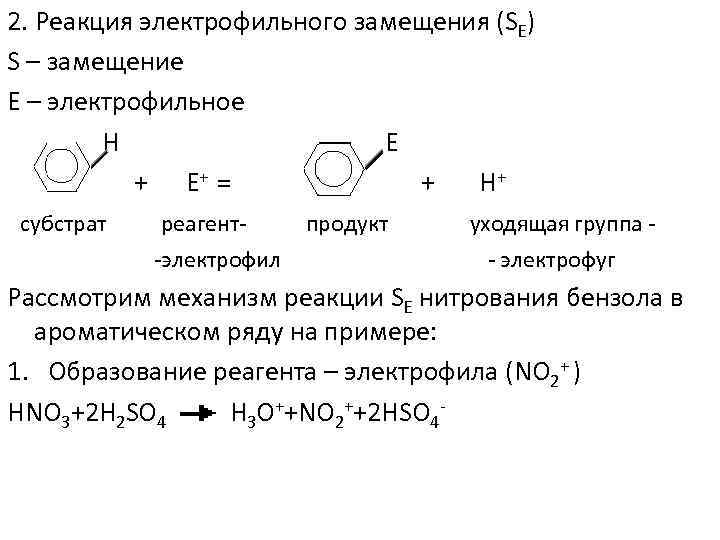 2. Реакция электрофильного замещения (SЕ) S – замещение Е – электрофильное Н Е + Е+ = + Н+ субстрат реагент-электрофил продукт уходящая группа - электрофуг Рассмотрим механизм реакции SЕ нитрования бензола в ароматическом ряду на примере: 1. Образование реагента – электрофила (NO 2+ ) HNO 3+2 H 2 SO 4 H 3 O++NO 2++2 HSO 4 -
2. Реакция электрофильного замещения (SЕ) S – замещение Е – электрофильное Н Е + Е+ = + Н+ субстрат реагент-электрофил продукт уходящая группа - электрофуг Рассмотрим механизм реакции SЕ нитрования бензола в ароматическом ряду на примере: 1. Образование реагента – электрофила (NO 2+ ) HNO 3+2 H 2 SO 4 H 3 O++NO 2++2 HSO 4 -
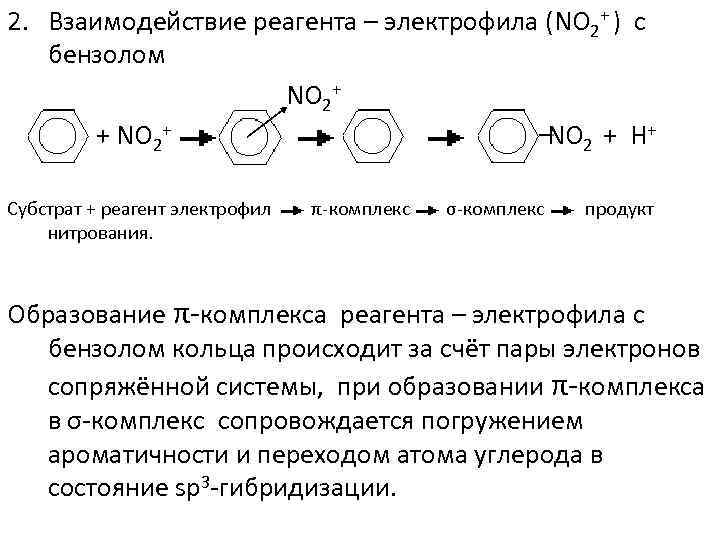 2. Взаимодействие реагента – электрофила (NO 2+ ) с бензолом NO 2+ + NO 2 + Н+ Субстрат + реагент электрофил нитрования. π-комплекс σ-комплекс продукт Образование π-комплекса реагента – электрофила с бензолом кольца происходит за счёт пары электронов сопряжённой системы, при образовании π-комплекса в σ-комплекс сопровождается погружением ароматичности и переходом атома углерода в состояние sp 3 -гибридизации.
2. Взаимодействие реагента – электрофила (NO 2+ ) с бензолом NO 2+ + NO 2 + Н+ Субстрат + реагент электрофил нитрования. π-комплекс σ-комплекс продукт Образование π-комплекса реагента – электрофила с бензолом кольца происходит за счёт пары электронов сопряжённой системы, при образовании π-комплекса в σ-комплекс сопровождается погружением ароматичности и переходом атома углерода в состояние sp 3 -гибридизации.
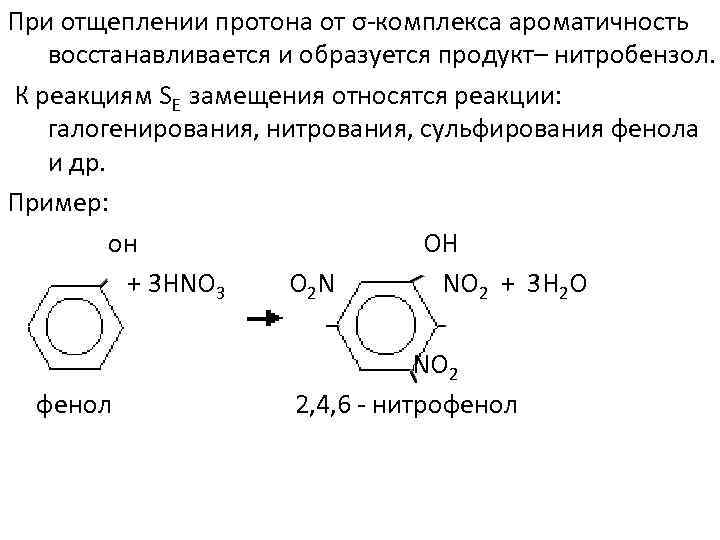 При отщеплении протона от σ-комплекса ароматичность восстанавливается и образуется продукт– нитробензол. К реакциям SЕ замещения относятся реакции: галогенирования, нитрования, сульфирования фенола и др. Пример: он OH + 3 HNO 3 O 2 N NO 2 + 3 Н 2 О фенол NO 2 2, 4, 6 - нитрофенол
При отщеплении протона от σ-комплекса ароматичность восстанавливается и образуется продукт– нитробензол. К реакциям SЕ замещения относятся реакции: галогенирования, нитрования, сульфирования фенола и др. Пример: он OH + 3 HNO 3 O 2 N NO 2 + 3 Н 2 О фенол NO 2 2, 4, 6 - нитрофенол
 Карбонильные соединения – это вещества, которые в своём составе содержат карбонильную группу >С=О. К ним относятся: альдегиды, кетоны, карбоновые кислоты. Электронное строение карбонильной группы: В карбонильной группе атом углерода находится в состоянии sp 2 -гибридизации. Его конфигурация плоская. Величина валентного угла составляет 1200. Атом углерода соединён двумя ковалентными связями с атомом кислорода: одна σ-связь, другая π-связь, возникающая за счёт перекрывания Рz-орбиталей атомов углерода и кислорода.
Карбонильные соединения – это вещества, которые в своём составе содержат карбонильную группу >С=О. К ним относятся: альдегиды, кетоны, карбоновые кислоты. Электронное строение карбонильной группы: В карбонильной группе атом углерода находится в состоянии sp 2 -гибридизации. Его конфигурация плоская. Величина валентного угла составляет 1200. Атом углерода соединён двумя ковалентными связями с атомом кислорода: одна σ-связь, другая π-связь, возникающая за счёт перекрывания Рz-орбиталей атомов углерода и кислорода.
 π-связь является сильно полярной, её электронная плотность смещена к более электроотрицательному атому кислорода, на котором возникает частично отрицательный заряд. На карбонильном атоме углерода – положительный заряд. _ >C = O В молекуле альдегидов выделяют следующие реакционные центры: R – CH – C O 1. H 3. H 2. 1. основной нуклеофильный центр 2. электрофильный центр 3. СН-кислотный центр
π-связь является сильно полярной, её электронная плотность смещена к более электроотрицательному атому кислорода, на котором возникает частично отрицательный заряд. На карбонильном атоме углерода – положительный заряд. _ >C = O В молекуле альдегидов выделяют следующие реакционные центры: R – CH – C O 1. H 3. H 2. 1. основной нуклеофильный центр 2. электрофильный центр 3. СН-кислотный центр
 Химические свойства альдегидов I. реакции нуклеофильного замещения (АN). А – присоединение N – нуклеофильное Рассмотрим такие реакции на прмере взаимодействия альдегидов со спиртами. Реакции ацетилизации: OH 1. СН 3 – СН 2 – С = О + HOСН 3 = СН 3 – СН 2 – СH H (реагент. OСН 3 -нуклеофил) 1 -метоксипропанол-1 Протекает в избытке спирта по типу реакций этерификации.
Химические свойства альдегидов I. реакции нуклеофильного замещения (АN). А – присоединение N – нуклеофильное Рассмотрим такие реакции на прмере взаимодействия альдегидов со спиртами. Реакции ацетилизации: OH 1. СН 3 – СН 2 – С = О + HOСН 3 = СН 3 – СН 2 – СH H (реагент. OСН 3 -нуклеофил) 1 -метоксипропанол-1 Протекает в избытке спирта по типу реакций этерификации.
 2. OH OСН 3 – СН 2 – СH + HOСН 3 = СН 3 – СН 2 – СH + Н 2 О OСН 3 (полуацеталь + метанол = ацеталь (1, 1 -диметоксипропан) + вода) Ацеталь и полуацеталь имеют важное биологическое значение, в организме в виде цикла полуацеталей присутствуют углеводы. Реакции образования ацеталей лежат в основе получения природных полисахаридов: крахмала, гликогена и др.
2. OH OСН 3 – СН 2 – СH + HOСН 3 = СН 3 – СН 2 – СH + Н 2 О OСН 3 (полуацеталь + метанол = ацеталь (1, 1 -диметоксипропан) + вода) Ацеталь и полуацеталь имеют важное биологическое значение, в организме в виде цикла полуацеталей присутствуют углеводы. Реакции образования ацеталей лежат в основе получения природных полисахаридов: крахмала, гликогена и др.
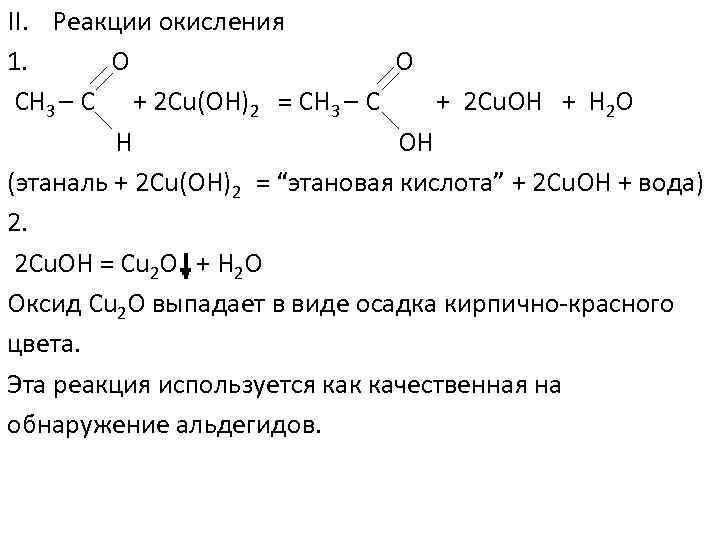 II. Реакции окисления 1. О О СН 3 – С + 2 Cu(ОН)2 = СН 3 – С + 2 Cu. OH + Н 2 О Н ОН (этаналь + 2 Cu(OH)2 = “этановая кислота” + 2 Cu. ОН + вода) 2. 2 Cu. ОН = Cu 2 О + Н 2 О Оксид Cu 2 O выпадает в виде осадка кирпично-красного цвета. Эта реакция используется как качественная на обнаружение альдегидов.
II. Реакции окисления 1. О О СН 3 – С + 2 Cu(ОН)2 = СН 3 – С + 2 Cu. OH + Н 2 О Н ОН (этаналь + 2 Cu(OH)2 = “этановая кислота” + 2 Cu. ОН + вода) 2. 2 Cu. ОН = Cu 2 О + Н 2 О Оксид Cu 2 O выпадает в виде осадка кирпично-красного цвета. Эта реакция используется как качественная на обнаружение альдегидов.
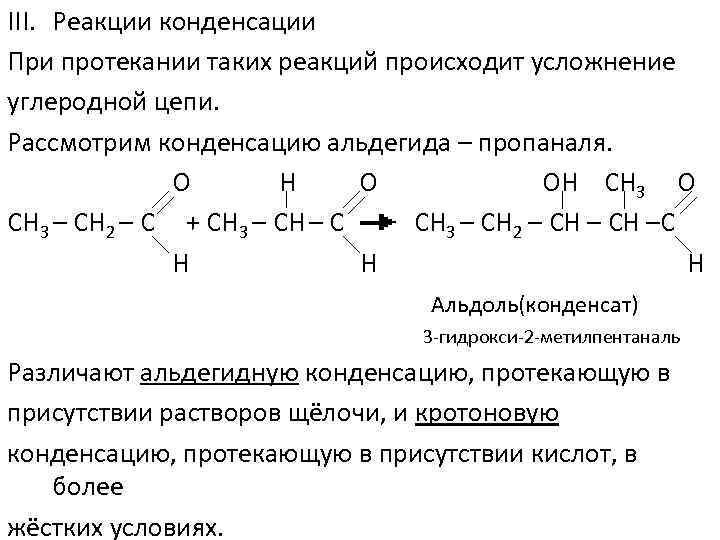 III. Реакции конденсации При протекании таких реакций происходит усложнение углеродной цепи. Рассмотрим конденсацию альдегида – пропаналя. О Н О ОН СН 3 О СН 3 – СН 2 – С + СН 3 – СН – С СН 3 – СН 2 – СН –С Н Н Н Альдоль(конденсат) 3 -гидрокси-2 -метилпентаналь Различают альдегидную конденсацию, протекающую в присутствии растворов щёлочи, и кротоновую конденсацию, протекающую в присутствии кислот, в более жёстких условиях.
III. Реакции конденсации При протекании таких реакций происходит усложнение углеродной цепи. Рассмотрим конденсацию альдегида – пропаналя. О Н О ОН СН 3 О СН 3 – СН 2 – С + СН 3 – СН – С СН 3 – СН 2 – СН –С Н Н Н Альдоль(конденсат) 3 -гидрокси-2 -метилпентаналь Различают альдегидную конденсацию, протекающую в присутствии растворов щёлочи, и кротоновую конденсацию, протекающую в присутствии кислот, в более жёстких условиях.
 В случае кротоновой конденсации от образующегося конденсата (альдоля) отщепляется молекула воды и образуется непредельное соединение. ОН СН 3 О СН 3 – СН 2 – СН –С СН 3 – СН 2 – СН = С – С Н Н (2 -метил-пентен-2 -аль) В организме конденсация альдегидов протекает с участием ферментов, которые называются альдолазы.
В случае кротоновой конденсации от образующегося конденсата (альдоля) отщепляется молекула воды и образуется непредельное соединение. ОН СН 3 О СН 3 – СН 2 – СН –С СН 3 – СН 2 – СН = С – С Н Н (2 -метил-пентен-2 -аль) В организме конденсация альдегидов протекает с участием ферментов, которые называются альдолазы.


