лекция иммунология-3-2014.ppt
- Количество слайдов: 70
 Лекция 3 Антигены – индукторы иммунного ответа Проф. , д. б. н. Климова Е. М. Харьков 2014
Лекция 3 Антигены – индукторы иммунного ответа Проф. , д. б. н. Климова Е. М. Харьков 2014
 Регуляторы иммунитета при нарушении барьерных факторов • 1. Индукция воспаления • 2. Активация факторов вторичного адаптивного иммунитета • 3. Клеточный сигналинг посредством медиаторов – цитокинов ( ИЛ-1, 6, ФНО - угнетает кроветворение) ИЛ-6 -активация -В • 4. Активация ИЛ-2, 3, 18, колониестимулирующих факторов и белков острой фазы. Ил 2 ---Тх1, Ил 3— рост СК, Ил 4 ---Тх2, рост В, антагонист- ИФ-гамма, синтез Ig. E
Регуляторы иммунитета при нарушении барьерных факторов • 1. Индукция воспаления • 2. Активация факторов вторичного адаптивного иммунитета • 3. Клеточный сигналинг посредством медиаторов – цитокинов ( ИЛ-1, 6, ФНО - угнетает кроветворение) ИЛ-6 -активация -В • 4. Активация ИЛ-2, 3, 18, колониестимулирующих факторов и белков острой фазы. Ил 2 ---Тх1, Ил 3— рост СК, Ил 4 ---Тх2, рост В, антагонист- ИФ-гамма, синтез Ig. E
 Этапы антигенной инициации факторов иммунитета • Миграция фагоцитов за счет хемоатрактантов. С 3 фрагмента комплемента • Адгезия –прикрепление микроорганизмов за счет опсонинов Ig. G и С 3 Ь фр. и патогенсвязывающих патернов (полсахариды и полинуклотиды) Фагоциты имеют специфич. Рецепторы передают информацию на нуклеарный фактор транскрипции с последующей активацией цитокинов -Ил 8 и костиулирующих молекул, стресс белков. TLR 2 для грамммпозитивных бактерий и TLR 3 для вирусов и • TLR 4 для граммнегативных бактерий, TLR 6 для зимозана грибов
Этапы антигенной инициации факторов иммунитета • Миграция фагоцитов за счет хемоатрактантов. С 3 фрагмента комплемента • Адгезия –прикрепление микроорганизмов за счет опсонинов Ig. G и С 3 Ь фр. и патогенсвязывающих патернов (полсахариды и полинуклотиды) Фагоциты имеют специфич. Рецепторы передают информацию на нуклеарный фактор транскрипции с последующей активацией цитокинов -Ил 8 и костиулирующих молекул, стресс белков. TLR 2 для грамммпозитивных бактерий и TLR 3 для вирусов и • TLR 4 для граммнегативных бактерий, TLR 6 для зимозана грибов
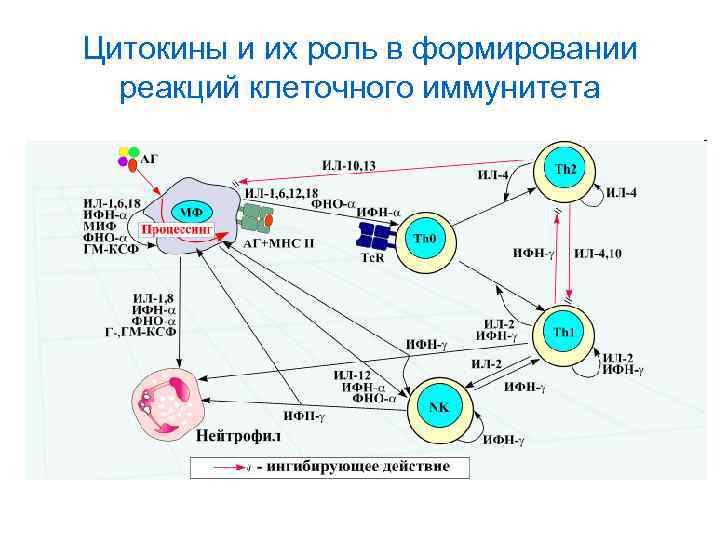 Цитокины и их роль в формировании реакций клеточного иммунитета
Цитокины и их роль в формировании реакций клеточного иммунитета
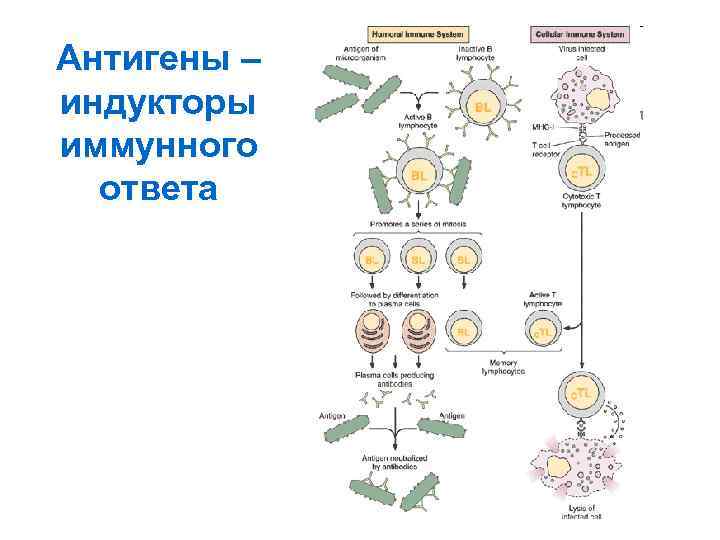 Антигены – индукторы иммунного ответа
Антигены – индукторы иммунного ответа
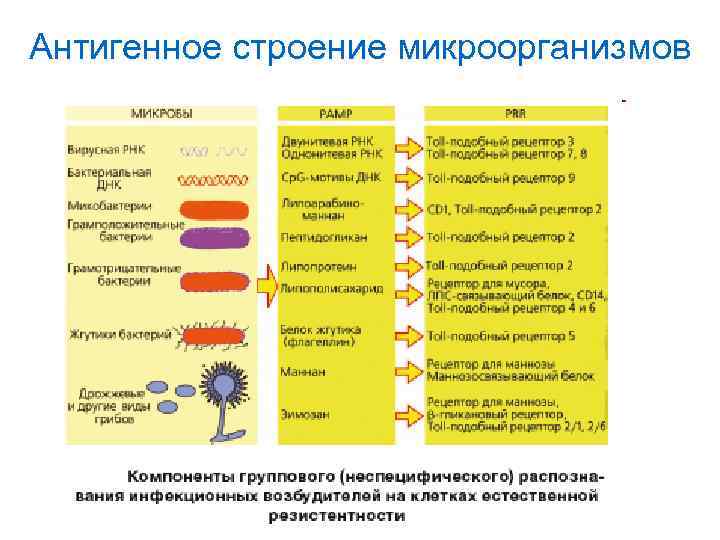 Антигенное строение микроорганизмов
Антигенное строение микроорганизмов
 Функция гуморального и клеточного ответа в реализации иммунного ответа на антигены Реализация иммунного ответа на чужеродные антигены осуществляется благодаря: • 1. Созреванию и отбору иммунокомпетентных клеток. Отбор или селекция (репертуара), осуществляется с помощью факторов микроокружения. Т-лимфоциты претерпевают отбор в тимусе, в результате чего происходит негативная селекция (уничтожение) аутореактивных Т-лимфоцитов и формирование их толерантности. Т- и В-лимфоциты, которые могут реагировать на собственные ткани и обладают авидностью к аутоантигенам, разрушаются в центральных органах иммунитета • 2. Индукция временной транзиторной анергии лимфоидных клеток осуществляется в первичных органах иммунной системы, где накапливаются клетки, толерантные к антигенам и обладающие невысокой авидностью • 3. Позитивная селекция и накопление в тимусе и костром мозге тимоцитов и В-лимфоцитов с клетками с низкой авидностью помимо толерантных клеток. Происходит дифференцировка гемопоэтических стволовых клеток, обладающих высокой специфичностью к антигенам. Они обладают быстрой иммунной активностью к антигенам
Функция гуморального и клеточного ответа в реализации иммунного ответа на антигены Реализация иммунного ответа на чужеродные антигены осуществляется благодаря: • 1. Созреванию и отбору иммунокомпетентных клеток. Отбор или селекция (репертуара), осуществляется с помощью факторов микроокружения. Т-лимфоциты претерпевают отбор в тимусе, в результате чего происходит негативная селекция (уничтожение) аутореактивных Т-лимфоцитов и формирование их толерантности. Т- и В-лимфоциты, которые могут реагировать на собственные ткани и обладают авидностью к аутоантигенам, разрушаются в центральных органах иммунитета • 2. Индукция временной транзиторной анергии лимфоидных клеток осуществляется в первичных органах иммунной системы, где накапливаются клетки, толерантные к антигенам и обладающие невысокой авидностью • 3. Позитивная селекция и накопление в тимусе и костром мозге тимоцитов и В-лимфоцитов с клетками с низкой авидностью помимо толерантных клеток. Происходит дифференцировка гемопоэтических стволовых клеток, обладающих высокой специфичностью к антигенам. Они обладают быстрой иммунной активностью к антигенам
 Дифференцировка иммунокомпетентных клеток (ИКК) • Гормоны тимуса обладают функцией активации на Т-лимфоцитах • После антиген-зависимой активации Т- и В-лимфоцитов происходит образование клонов лимфоцитов различных субпопуляций • Факторы микроокружения в большой концентрации обладают стимулирующим эффектом на лимфоциты, а в малых дозах – ингибируют действие на продукцию им факторов Т-лимфоцитов. • После распознавания антигенов и реализации иммунного ответа Тлимфоциты подвергаются пролиферации, в результате чего образуется целый клон клетки Т-лимфоцита. Появляются трансмембранные белки (кластеры дифференцировки СD). • Общим кластером дифференцировки для всех лимфоцитов является СD 3 кластер. • Встреча Т-лимфоцитов с определенной антигенной специфичностью микроорганизмов предполагает новый этап антиген-зависимой дифференцировки.
Дифференцировка иммунокомпетентных клеток (ИКК) • Гормоны тимуса обладают функцией активации на Т-лимфоцитах • После антиген-зависимой активации Т- и В-лимфоцитов происходит образование клонов лимфоцитов различных субпопуляций • Факторы микроокружения в большой концентрации обладают стимулирующим эффектом на лимфоциты, а в малых дозах – ингибируют действие на продукцию им факторов Т-лимфоцитов. • После распознавания антигенов и реализации иммунного ответа Тлимфоциты подвергаются пролиферации, в результате чего образуется целый клон клетки Т-лимфоцита. Появляются трансмембранные белки (кластеры дифференцировки СD). • Общим кластером дифференцировки для всех лимфоцитов является СD 3 кластер. • Встреча Т-лимфоцитов с определенной антигенной специфичностью микроорганизмов предполагает новый этап антиген-зависимой дифференцировки.
 Функция субпопуляций Т- и Влимфоцитов • Процесс распознавания антигена Т-лимфоцитом отличается от распознавания антигена В-лимфоцитом. • Для распознавания бактериальных клеток или вирусов Тлимфоцитам необходим промежуточный этап, на котором АПК подготавливает материал для распознавания. • Т-клетки имеют на своей поверхности кластеры дифференцировки СD 4 и СD 8. • Незрелые Т-лимфоциты могут одновременно нести на своей поверхности СD 4 и СD 8, но при их специализации на их поверхности присутствуют лишь один из них - СD 4 или СD 8. • СD 4 – это Т-хелперная субпопуляция (55%) • СD 8 – выполняют Т-киллерную или супрессорную функцию.
Функция субпопуляций Т- и Влимфоцитов • Процесс распознавания антигена Т-лимфоцитом отличается от распознавания антигена В-лимфоцитом. • Для распознавания бактериальных клеток или вирусов Тлимфоцитам необходим промежуточный этап, на котором АПК подготавливает материал для распознавания. • Т-клетки имеют на своей поверхности кластеры дифференцировки СD 4 и СD 8. • Незрелые Т-лимфоциты могут одновременно нести на своей поверхности СD 4 и СD 8, но при их специализации на их поверхности присутствуют лишь один из них - СD 4 или СD 8. • СD 4 – это Т-хелперная субпопуляция (55%) • СD 8 – выполняют Т-киллерную или супрессорную функцию.
 Рецепторы лимфоцитов и их функциональные резервы • Т-лимфоциты экспрессируют на своей поверхности различные рецепторы: к фитогемагглютинину, конканавалину. • Хелперные клетки СD 4 подразделяются на два типа: Т-хелпер 1 типа и Т-хелпер 2 типа. • Основная функция Т-хелперов – стимуляция В-лимфоцитов. Разделение субпопуляции на два типа заключается в том, что они вырабатывают различные цитокины. • Т-хелперы 1 типа продуцирует гамма-интерферон, ИЛ-2 и фактор некроза опухоли. Т-хелпер 1 типа активирует макрофаги и НКклетки • Т-хелперы 2 типа активируют В-лимфоциты, вырабатывают ИЛ 4, ИЛ-5, ИЛ-10 ИЛ-13 (отвечает за выработку IG-Е, приводящего к аллергической реакции и анафилактическому шоку.
Рецепторы лимфоцитов и их функциональные резервы • Т-лимфоциты экспрессируют на своей поверхности различные рецепторы: к фитогемагглютинину, конканавалину. • Хелперные клетки СD 4 подразделяются на два типа: Т-хелпер 1 типа и Т-хелпер 2 типа. • Основная функция Т-хелперов – стимуляция В-лимфоцитов. Разделение субпопуляции на два типа заключается в том, что они вырабатывают различные цитокины. • Т-хелперы 1 типа продуцирует гамма-интерферон, ИЛ-2 и фактор некроза опухоли. Т-хелпер 1 типа активирует макрофаги и НКклетки • Т-хелперы 2 типа активируют В-лимфоциты, вырабатывают ИЛ 4, ИЛ-5, ИЛ-10 ИЛ-13 (отвечает за выработку IG-Е, приводящего к аллергической реакции и анафилактическому шоку.
 Дифференцировка Т-лимфоцитов в тимусе • Т-лимфоциты обладают способностью различать генетически чужеродные антигены и координировать защитную функцию других клеток от микробных и других антигенных субстанций • Дифференцировка Т-лимфоцитов происходит в тимусе • Предшественники Т-лимфоцитов в кортикальной зоне тимуса подвергаются воздействию ДНК-полимеразы, после чего осуществляется перестройка нуклеотидной последовательности в сегменте ДНК, который кодирует вариабельные участки Т-клеточных рецепторов • Добавочные гены экспрессируют белки, которые представляют собой кластеры дифференцировки CD Т-лимфоцитов • На ранних стадиях экспрессируются CD 44/CD 25 маркеры • Затем синтезируется белковые молекулы, образующие CD 4, CD 8 кластеры дифференцировки • Антигены главного комплекса гистосовместимости HLA экспрессируются при активации протимоцитов
Дифференцировка Т-лимфоцитов в тимусе • Т-лимфоциты обладают способностью различать генетически чужеродные антигены и координировать защитную функцию других клеток от микробных и других антигенных субстанций • Дифференцировка Т-лимфоцитов происходит в тимусе • Предшественники Т-лимфоцитов в кортикальной зоне тимуса подвергаются воздействию ДНК-полимеразы, после чего осуществляется перестройка нуклеотидной последовательности в сегменте ДНК, который кодирует вариабельные участки Т-клеточных рецепторов • Добавочные гены экспрессируют белки, которые представляют собой кластеры дифференцировки CD Т-лимфоцитов • На ранних стадиях экспрессируются CD 44/CD 25 маркеры • Затем синтезируется белковые молекулы, образующие CD 4, CD 8 кластеры дифференцировки • Антигены главного комплекса гистосовместимости HLA экспрессируются при активации протимоцитов
 Миграция иммунокомпетентных клеток • С помощью молекул-интегринов Т-клетки мигрируют через сосудистый барьер • После их контакта с хемокинами дендритных клеток они приобретают функцию для активации В-лимфоцитов • В-лимфоциты под действием микроокружения костного мозга посредством адгезивных молекул CD 44 осуществляют пролиферацию с последующей экспрессией рецепторов к ИЛ -7
Миграция иммунокомпетентных клеток • С помощью молекул-интегринов Т-клетки мигрируют через сосудистый барьер • После их контакта с хемокинами дендритных клеток они приобретают функцию для активации В-лимфоцитов • В-лимфоциты под действием микроокружения костного мозга посредством адгезивных молекул CD 44 осуществляют пролиферацию с последующей экспрессией рецепторов к ИЛ -7
 Дифференцировка клеток В-лимфоцитов • На поверхности В-лимфоцитов появляются рецепторные Ig. M, которые обладают способностью распознавать антигены • Затем В-лимфоциты воспринимают клеточный сигналинг от Т-хелперных клеток и на их поверхности появляется новый репертуар рецепторных иммуноглобулинов класса A, МG, D • На каждом В-лимфоците имеются иммуноглобулины того или иного идиотипа, так кодируются одними и теми же генами • Антигены HLA присутствуют на всех зрелых Влимфоцитах
Дифференцировка клеток В-лимфоцитов • На поверхности В-лимфоцитов появляются рецепторные Ig. M, которые обладают способностью распознавать антигены • Затем В-лимфоциты воспринимают клеточный сигналинг от Т-хелперных клеток и на их поверхности появляется новый репертуар рецепторных иммуноглобулинов класса A, МG, D • На каждом В-лимфоците имеются иммуноглобулины того или иного идиотипа, так кодируются одними и теми же генами • Антигены HLA присутствуют на всех зрелых Влимфоцитах
 Взаимодействие антигена с иммунокомпетентными клетками (ИКК) • При взаимодействии антигенами с иммунными факторами происходит его элиминация • Антиген может быть уничтожен на уровне барьерных иммунных реакций в коже и слизистых • Иммунный ответ представляет собой не локальную реакцию, а генерализованную • Реакция иммунной системы на антиген подразделяют на этапы: • 1. Афферентный • 2. Центральный • 3. Эфферентный
Взаимодействие антигена с иммунокомпетентными клетками (ИКК) • При взаимодействии антигенами с иммунными факторами происходит его элиминация • Антиген может быть уничтожен на уровне барьерных иммунных реакций в коже и слизистых • Иммунный ответ представляет собой не локальную реакцию, а генерализованную • Реакция иммунной системы на антиген подразделяют на этапы: • 1. Афферентный • 2. Центральный • 3. Эфферентный
 1 этап взаимодействия Афферентный • На первом этапе происходит распознавание чужеродного антигена с помощью АПК с последующим его процессингом • На этом этапе активируется миграция в зону локализации антигена
1 этап взаимодействия Афферентный • На первом этапе происходит распознавание чужеродного антигена с помощью АПК с последующим его процессингом • На этом этапе активируется миграция в зону локализации антигена
 2 этап взаимодействия Центральный • Характеризуется межклеточным сигналингом • Сигналинг между Т- и В-клетками с последующим синтезом Ig
2 этап взаимодействия Центральный • Характеризуется межклеточным сигналингом • Сигналинг между Т- и В-клетками с последующим синтезом Ig
 3 этап взаимодействия Эфферентный • Происходит реализация иммунного ответа против антигена: • - цитотоксическими лимфоцитами • - макрофагами CD 14+ • - нейтрализация антителами экзотоксинов • - лизис внеклеточных бактерий антителами
3 этап взаимодействия Эфферентный • Происходит реализация иммунного ответа против антигена: • - цитотоксическими лимфоцитами • - макрофагами CD 14+ • - нейтрализация антителами экзотоксинов • - лизис внеклеточных бактерий антителами
 Распознавание инфекционных антигенов • Клеточный сигналинг осуществляется в распознавании антигенов и экзотоксинов микроорганизмов • В распознавании патогенов участвуют ЛПС-связывающий протеин, Среактивный белок, компоненты комплемента, иммуноглобулиновые антитела
Распознавание инфекционных антигенов • Клеточный сигналинг осуществляется в распознавании антигенов и экзотоксинов микроорганизмов • В распознавании патогенов участвуют ЛПС-связывающий протеин, Среактивный белок, компоненты комплемента, иммуноглобулиновые антитела
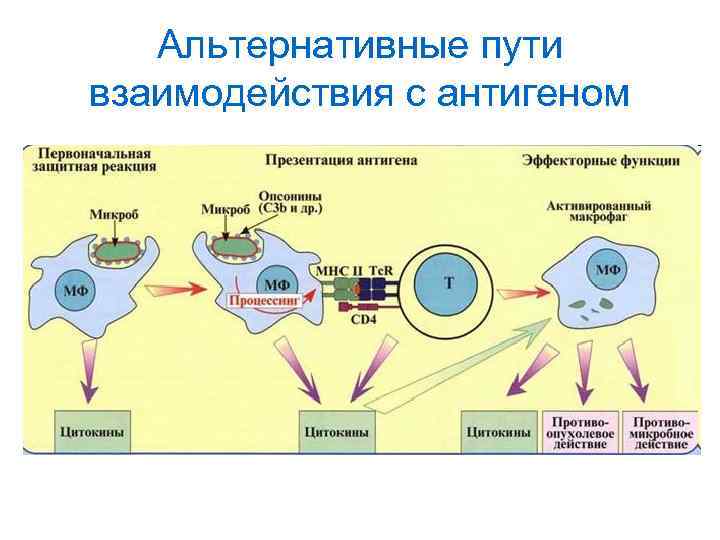 Альтернативные пути взаимодействия с антигеном
Альтернативные пути взаимодействия с антигеном
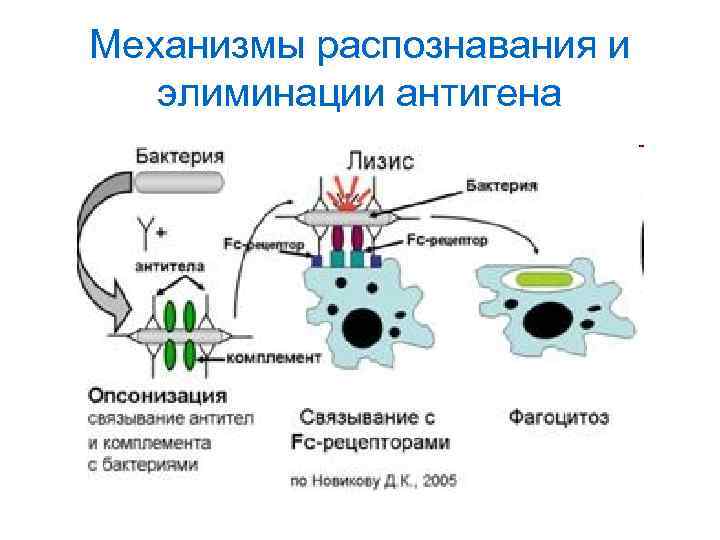 Механизмы распознавания и элиминации антигена
Механизмы распознавания и элиминации антигена
 Локализация иммунных реакций • Гуморальный ответ осуществляется в фолликулах лимфоузлов после дифференцировки В-лимфоцитов • Т-клеточный иммунитет осуществляется с помощью Т-киллеров, которые формируются в результате трансформации тимусзависимых лимфоцитов в крупные клетки с базофильной цитоплазмой с последующим образованием малых лимфоцитов
Локализация иммунных реакций • Гуморальный ответ осуществляется в фолликулах лимфоузлов после дифференцировки В-лимфоцитов • Т-клеточный иммунитет осуществляется с помощью Т-киллеров, которые формируются в результате трансформации тимусзависимых лимфоцитов в крупные клетки с базофильной цитоплазмой с последующим образованием малых лимфоцитов
 Взаимодействие патогенов с первичными и вторичными факторами иммунитета • Первичный иммунный ответ формируется при первом попадании антигена в макроорганизм • Вторичный иммунный ответ формируется при повторном попадании антигена в организм • Вторичный иммунный ответ формируется быстро на 5 -7 -е сутки • Вторичный иммунный ответ формируется за счет клеток иммунной памяти и остается на всю жизнь • Клетки памяти клеточного и гуморального иммунитета на первом этапе формируются факторами первичного иммунитета в ответ на антигенстимулированные предшественники цитотоксических Т-клеток, антигенстимулированных Т-хелперов и антигениндуцированных В-клеток • Активированные клетки сохраняются в лимфоидных органах • Первичный ответ характеризуется латентным индуцированным периодом, продуктивным образованием клонов лимфоцитов и нейтрализации антигенов и фазой снижения ответа • При вторичном иммунном ответе латентный период уменьшается
Взаимодействие патогенов с первичными и вторичными факторами иммунитета • Первичный иммунный ответ формируется при первом попадании антигена в макроорганизм • Вторичный иммунный ответ формируется при повторном попадании антигена в организм • Вторичный иммунный ответ формируется быстро на 5 -7 -е сутки • Вторичный иммунный ответ формируется за счет клеток иммунной памяти и остается на всю жизнь • Клетки памяти клеточного и гуморального иммунитета на первом этапе формируются факторами первичного иммунитета в ответ на антигенстимулированные предшественники цитотоксических Т-клеток, антигенстимулированных Т-хелперов и антигениндуцированных В-клеток • Активированные клетки сохраняются в лимфоидных органах • Первичный ответ характеризуется латентным индуцированным периодом, продуктивным образованием клонов лимфоцитов и нейтрализации антигенов и фазой снижения ответа • При вторичном иммунном ответе латентный период уменьшается
 Взаимодействие патогенов с гуморальными факторами Ig иммунитета • Гуморальные реакции осуществляются глобулярными белками-иммуноглобулинами, которые состоят из 4 полипептидных цепей – 2 тяжелые и 2 легкие • В каждой паре оба полипептида одинаковые, но в разных иммуноглобулинах они имеют разные строение • У человека 5 видов иммуноглобулинов: A, M, G, D, E
Взаимодействие патогенов с гуморальными факторами Ig иммунитета • Гуморальные реакции осуществляются глобулярными белками-иммуноглобулинами, которые состоят из 4 полипептидных цепей – 2 тяжелые и 2 легкие • В каждой паре оба полипептида одинаковые, но в разных иммуноглобулинах они имеют разные строение • У человека 5 видов иммуноглобулинов: A, M, G, D, E
 Антигены и гаптены • химические вещества с малой молекулярной массой, которые самостоятельно не вызывают иммунный ответ, но приобретают эту способность при конъюгации с высокомолекулярными белковыми носителями
Антигены и гаптены • химические вещества с малой молекулярной массой, которые самостоятельно не вызывают иммунный ответ, но приобретают эту способность при конъюгации с высокомолекулярными белковыми носителями
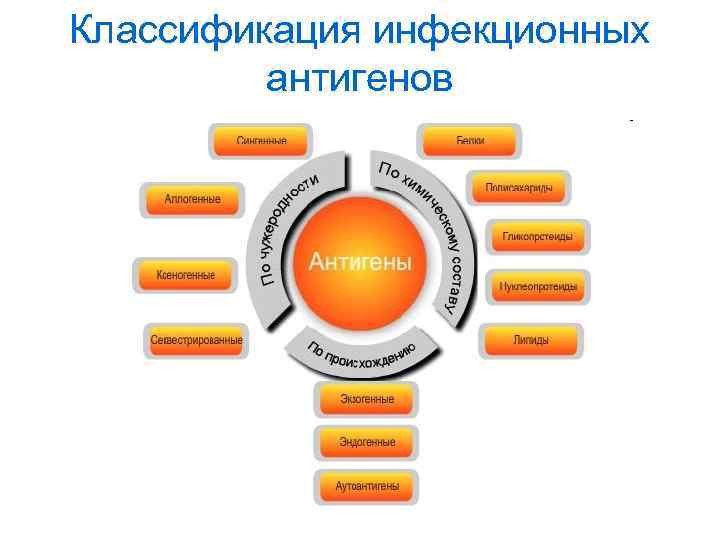 Классификация инфекционных антигенов
Классификация инфекционных антигенов

 Инфекционные антигены
Инфекционные антигены
 Взаимодействие иммуноглобулинов с инфекционными антигенами • Иммуноглобулины имеют на своих цепях N- и С-концы • На N-концах расположен функциональный центр антител – детерминанта антител • В тяжелых и легких цепях выделяют константные области «С» • Области, которые связываются с антигенами изменяются в зависимости от природы антигена и располагаются на вариабельных участках «V» • Для образования детерминант антител необходим N-концевой участок полипептидных цепей, как тяжелой, так и легкой • Специфичность антител определяется аминокислотной последовательностью, которая связывается с антигеном • N-концевые фрагменты реагируют с антигеном и называются Fabфрагментами, которые сосредоточены на длинной си молекулы иммуноглобулина и два тяжелых полипептида выгнуты в противоположные стороны • Угол, образованный между фрагментами позволяет связывать антиген • Fc-фрагмент определяет способность иммуноглобулинов посредством связи с фрагментами комплемента локализоваться в тканях
Взаимодействие иммуноглобулинов с инфекционными антигенами • Иммуноглобулины имеют на своих цепях N- и С-концы • На N-концах расположен функциональный центр антител – детерминанта антител • В тяжелых и легких цепях выделяют константные области «С» • Области, которые связываются с антигенами изменяются в зависимости от природы антигена и располагаются на вариабельных участках «V» • Для образования детерминант антител необходим N-концевой участок полипептидных цепей, как тяжелой, так и легкой • Специфичность антител определяется аминокислотной последовательностью, которая связывается с антигеном • N-концевые фрагменты реагируют с антигеном и называются Fabфрагментами, которые сосредоточены на длинной си молекулы иммуноглобулина и два тяжелых полипептида выгнуты в противоположные стороны • Угол, образованный между фрагментами позволяет связывать антиген • Fc-фрагмент определяет способность иммуноглобулинов посредством связи с фрагментами комплемента локализоваться в тканях
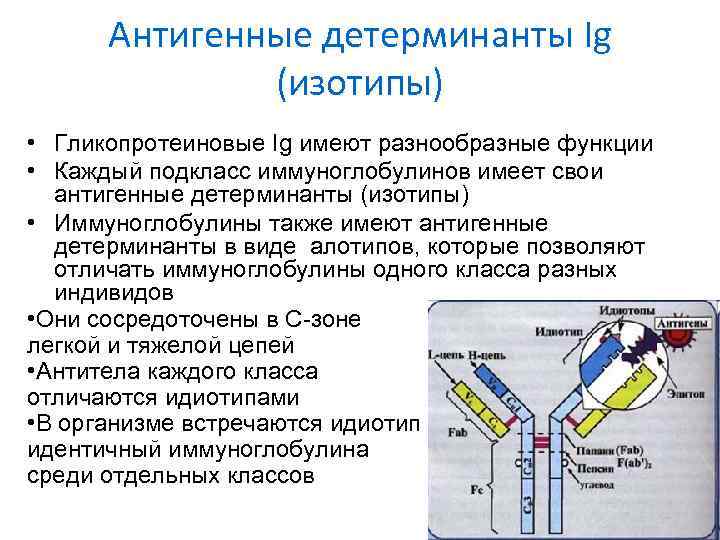 Антигенные детерминанты Ig (изотипы) • Гликопротеиновые Ig имеют разнообразные функции • Каждый подкласс иммуноглобулинов имеет свои антигенные детерминанты (изотипы) • Иммуноглобулины также имеют антигенные детерминанты в виде алотипов, которые позволяют отличать иммуноглобулины одного класса разных индивидов • Они сосредоточены в С-зоне легкой и тяжелой цепей • Антитела каждого класса отличаются идиотипами • В организме встречаются идиотип идентичный иммуноглобулина среди отдельных классов
Антигенные детерминанты Ig (изотипы) • Гликопротеиновые Ig имеют разнообразные функции • Каждый подкласс иммуноглобулинов имеет свои антигенные детерминанты (изотипы) • Иммуноглобулины также имеют антигенные детерминанты в виде алотипов, которые позволяют отличать иммуноглобулины одного класса разных индивидов • Они сосредоточены в С-зоне легкой и тяжелой цепей • Антитела каждого класса отличаются идиотипами • В организме встречаются идиотип идентичный иммуноглобулина среди отдельных классов
 Виды антигенных детерминант иммуноглобулинов • Изотипические – отражают разнообразие антител на уровне биологического вида (изотипы Ig. A, Ig. M, Ig. G, Ig. D, Ig. E) • Аллотипические – обусловлены генетическим разнообразием внутри вида (аллотипы Ig. G 1, Ig. G 2, Ig. G 3, Ig. G 4 ) • Идиотипические – участки в антигенсвязывающем центре молекулы иммуноглобулина, которые являются антигенными детерминантами. Антитела против таких антигенных детерминант называются антиидиотипическими
Виды антигенных детерминант иммуноглобулинов • Изотипические – отражают разнообразие антител на уровне биологического вида (изотипы Ig. A, Ig. M, Ig. G, Ig. D, Ig. E) • Аллотипические – обусловлены генетическим разнообразием внутри вида (аллотипы Ig. G 1, Ig. G 2, Ig. G 3, Ig. G 4 ) • Идиотипические – участки в антигенсвязывающем центре молекулы иммуноглобулина, которые являются антигенными детерминантами. Антитела против таких антигенных детерминант называются антиидиотипическими
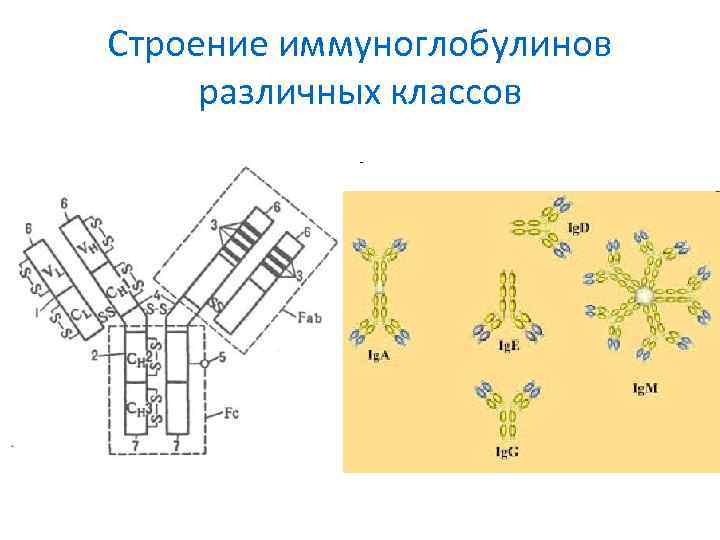 Строение иммуноглобулинов различных классов
Строение иммуноглобулинов различных классов
 Классификация иммуноглобулинов • Иммуноглобулины подразделяются на классы A, M, G, D, E • Ig. M максимально связывает комплемент, тем самым определяет мощную преципитацию • Ig. M циркулирует в крови • Ig. А слабо преципитирует и агглютинирует • Ig. А находятся во многих секретах, молоке • Ig. D обладает сильным аффинитетом и сорбируется на клетках, например в легких • Иммуноглобулиновые белки вариабельны • Ig. G подразделяют на 4 подкласса • Иммуноглобулины отвечают на поступление АГ в организм и взаимодействуют с ним
Классификация иммуноглобулинов • Иммуноглобулины подразделяются на классы A, M, G, D, E • Ig. M максимально связывает комплемент, тем самым определяет мощную преципитацию • Ig. M циркулирует в крови • Ig. А слабо преципитирует и агглютинирует • Ig. А находятся во многих секретах, молоке • Ig. D обладает сильным аффинитетом и сорбируется на клетках, например в легких • Иммуноглобулиновые белки вариабельны • Ig. G подразделяют на 4 подкласса • Иммуноглобулины отвечают на поступление АГ в организм и взаимодействуют с ним
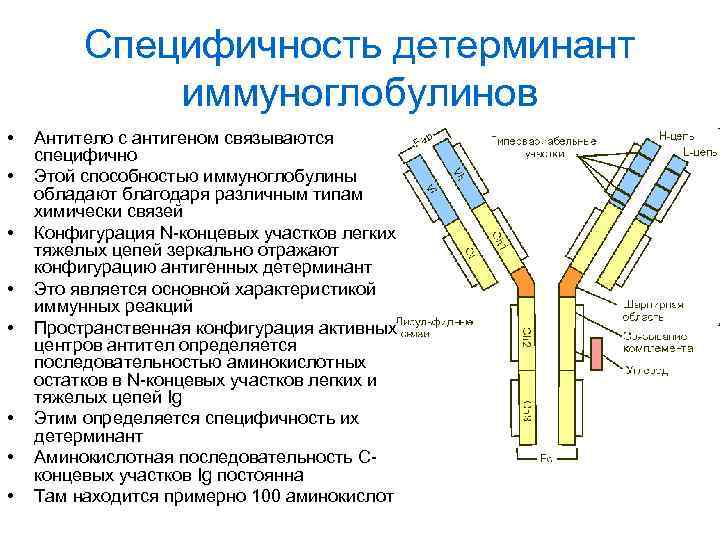 Специфичность детерминант иммуноглобулинов • • Антитело с антигеном связываются специфично Этой способностью иммуноглобулины обладают благодаря различным типам химически связей Конфигурация N-концевых участков легких тяжелых цепей зеркально отражают конфигурацию антигенных детерминант Это является основной характеристикой иммунных реакций Пространственная конфигурация активных центров антител определяется последовательностью аминокислотных остатков в N-концевых участков легких и тяжелых цепей Ig Этим определяется специфичность их детерминант Аминокислотная последовательность Сконцевых участков Ig постоянна Там находится примерно 100 аминокислот
Специфичность детерминант иммуноглобулинов • • Антитело с антигеном связываются специфично Этой способностью иммуноглобулины обладают благодаря различным типам химически связей Конфигурация N-концевых участков легких тяжелых цепей зеркально отражают конфигурацию антигенных детерминант Это является основной характеристикой иммунных реакций Пространственная конфигурация активных центров антител определяется последовательностью аминокислотных остатков в N-концевых участков легких и тяжелых цепей Ig Этим определяется специфичность их детерминант Аминокислотная последовательность Сконцевых участков Ig постоянна Там находится примерно 100 аминокислот
 Специфичность и вариабельность связывания иммуноглобулинов с АГ • Антитела одной специфичности могут иметь различное сродство к антигенам, что называется авидностью и определяет скорость образования комплекса АГ-АТ • Авидность определяется первичным строением активного центра АТ и степенью поверхностной конфигурации • Вариабельность авидности определяется небольшими изменениями в первичном строении активных центров, что при патологии может изменять специфичность Ig
Специфичность и вариабельность связывания иммуноглобулинов с АГ • Антитела одной специфичности могут иметь различное сродство к антигенам, что называется авидностью и определяет скорость образования комплекса АГ-АТ • Авидность определяется первичным строением активного центра АТ и степенью поверхностной конфигурации • Вариабельность авидности определяется небольшими изменениями в первичном строении активных центров, что при патологии может изменять специфичность Ig
 Реакция агглютинации • Эритроциты, связанные с анти-Rh -антителами, анализировались на агглютинацию при помощи специфической антисыворотки подклассов анти. Ig. G.
Реакция агглютинации • Эритроциты, связанные с анти-Rh -антителами, анализировались на агглютинацию при помощи специфической антисыворотки подклассов анти. Ig. G.
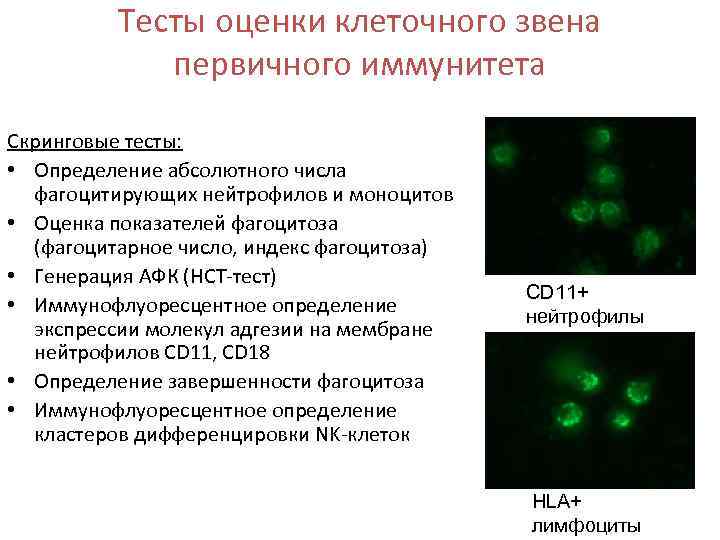 Тесты оценки клеточного звена первичного иммунитета Скринговые тесты: • Определение абсолютного числа фагоцитирующих нейтрофилов и моноцитов • Оценка показателей фагоцитоза (фагоцитарное число, индекс фагоцитоза) • Генерация АФК (НСТ-тест) • Иммунофлуоресцентное определение экспрессии молекул адгезии на мембране нейтрофилов CD 11, CD 18 • Определение завершенности фагоцитоза • Иммунофлуоресцентное определение кластеров дифференцировки NK-клеток CD 11+ нейтрофилы HLA+ лимфоциты
Тесты оценки клеточного звена первичного иммунитета Скринговые тесты: • Определение абсолютного числа фагоцитирующих нейтрофилов и моноцитов • Оценка показателей фагоцитоза (фагоцитарное число, индекс фагоцитоза) • Генерация АФК (НСТ-тест) • Иммунофлуоресцентное определение экспрессии молекул адгезии на мембране нейтрофилов CD 11, CD 18 • Определение завершенности фагоцитоза • Иммунофлуоресцентное определение кластеров дифференцировки NK-клеток CD 11+ нейтрофилы HLA+ лимфоциты
 Тесты оценки гуморальных факторов первичного иммунитета • Использование моноклональных антител (МКАТ) для выявления гуморальных факторов первичного иммунитета • Иммунотурбидиметрический метод определения фрагментов комплемента • ИФА-метод определения цитокинов
Тесты оценки гуморальных факторов первичного иммунитета • Использование моноклональных антител (МКАТ) для выявления гуморальных факторов первичного иммунитета • Иммунотурбидиметрический метод определения фрагментов комплемента • ИФА-метод определения цитокинов
 Шарль Рише (1913 г. Франция) показал, что нарушения механизмов защитных систем организма могут вызывать аутоиммунные заболевания • • 1972 г. (США / Великобритания) Ж. М. Эдельман, Р. Р. Портер получили нобелевскую премию за исследование химической структуры иммуноглобулиновых антител 1980 г. (США / Франция) Б. Бенацарраф, Дж. Доссе, Ж. Д. Снелл получили нобелевскую премию за открытие генетически детерминированных структур на клеточной поверхности • • 1960 г. австралийский ученый Ф. Бернет удостоен нобелевской премии за открытие приобретенной иммунологической толерантности • • Возможность определения органоспецифических антител стала возможной вследствие открытия и разработки гибридомной технологии и получения моноклональных антител (Дж. Кехлер, К. Милштейн, Германия/Швейцария, Аргентина/Великобритания, 1984 г. ) Дж. Блобел (1999 г. США), открытие сигнальной трансдукции
Шарль Рише (1913 г. Франция) показал, что нарушения механизмов защитных систем организма могут вызывать аутоиммунные заболевания • • 1972 г. (США / Великобритания) Ж. М. Эдельман, Р. Р. Портер получили нобелевскую премию за исследование химической структуры иммуноглобулиновых антител 1980 г. (США / Франция) Б. Бенацарраф, Дж. Доссе, Ж. Д. Снелл получили нобелевскую премию за открытие генетически детерминированных структур на клеточной поверхности • • 1960 г. австралийский ученый Ф. Бернет удостоен нобелевской премии за открытие приобретенной иммунологической толерантности • • Возможность определения органоспецифических антител стала возможной вследствие открытия и разработки гибридомной технологии и получения моноклональных антител (Дж. Кехлер, К. Милштейн, Германия/Швейцария, Аргентина/Великобритания, 1984 г. ) Дж. Блобел (1999 г. США), открытие сигнальной трансдукции
 • Нобелевская премия за исследования по генетической природе разнообразия антител (С. Тонигава, 1987 г. , Япония) • Нобелевская премия 1908 г. за открытие фагоцитоза (русский ученый И. Мечников) Нобелевская премия 1980 г. за синтез рекомбинантного интерферона (американские ученые У. Гилберт, П. Берг Ф. Сэнджер) • Дж. Блобел (1999 г. США), открыл сигнальные аминокислоты в белковых последовательностях – сигнальная трансдукция активного транспорта • • Н. К. Джерни (1984 г. Дания/Швейцария) – нобелевская премия за открытие идиотипической и антиидиотипической клональности лимфоцитов 1980 г. (США / Франция) Б. Бенацарраф, Дж. Доссе, Ж. Д. Снелл получили нобелевскую премию за открытие генетически детерминированных структур на клеточной поверхности
• Нобелевская премия за исследования по генетической природе разнообразия антител (С. Тонигава, 1987 г. , Япония) • Нобелевская премия 1908 г. за открытие фагоцитоза (русский ученый И. Мечников) Нобелевская премия 1980 г. за синтез рекомбинантного интерферона (американские ученые У. Гилберт, П. Берг Ф. Сэнджер) • Дж. Блобел (1999 г. США), открыл сигнальные аминокислоты в белковых последовательностях – сигнальная трансдукция активного транспорта • • Н. К. Джерни (1984 г. Дания/Швейцария) – нобелевская премия за открытие идиотипической и антиидиотипической клональности лимфоцитов 1980 г. (США / Франция) Б. Бенацарраф, Дж. Доссе, Ж. Д. Снелл получили нобелевскую премию за открытие генетически детерминированных структур на клеточной поверхности
 1908 г. Нобелевская премия за открытие гуморального иммунитета (немецкий ученый П. Эрлих) • • 1972 г. (США / Великобритания) Ж. М. Эдельман, Р. Р. Портер получили нобелевскую премию за исследование химической структуры иммуноглобулиновых антител Возможность определения органоспецифических антител стала возможной вследствие открытия и разработки гибридомной технологии и получения моноклональных антител (Дж. Кехлер, К. Милштейн, Германия/Швейцария, Аргентина/Великобритания, 1984 г. ) • • • С. Б. Прузинер (1997 г. США) - нобелевская премия за изучение конформационных изменений белков, открытие прионов 1919 г. бельгийский ученый Ж. Борде получил нобелевскую премию за открытие белков системы комплемента, феномена фиксации комплемента и диагностических возможностей этой реакции • П. С. Доэрти, Р. М. Зинкернагель (1996 г. Австралия, США). Нобелевская премия за открытие в регуляции специфического иммунного ответа (двойное распознавание)
1908 г. Нобелевская премия за открытие гуморального иммунитета (немецкий ученый П. Эрлих) • • 1972 г. (США / Великобритания) Ж. М. Эдельман, Р. Р. Портер получили нобелевскую премию за исследование химической структуры иммуноглобулиновых антител Возможность определения органоспецифических антител стала возможной вследствие открытия и разработки гибридомной технологии и получения моноклональных антител (Дж. Кехлер, К. Милштейн, Германия/Швейцария, Аргентина/Великобритания, 1984 г. ) • • • С. Б. Прузинер (1997 г. США) - нобелевская премия за изучение конформационных изменений белков, открытие прионов 1919 г. бельгийский ученый Ж. Борде получил нобелевскую премию за открытие белков системы комплемента, феномена фиксации комплемента и диагностических возможностей этой реакции • П. С. Доэрти, Р. М. Зинкернагель (1996 г. Австралия, США). Нобелевская премия за открытие в регуляции специфического иммунного ответа (двойное распознавание)
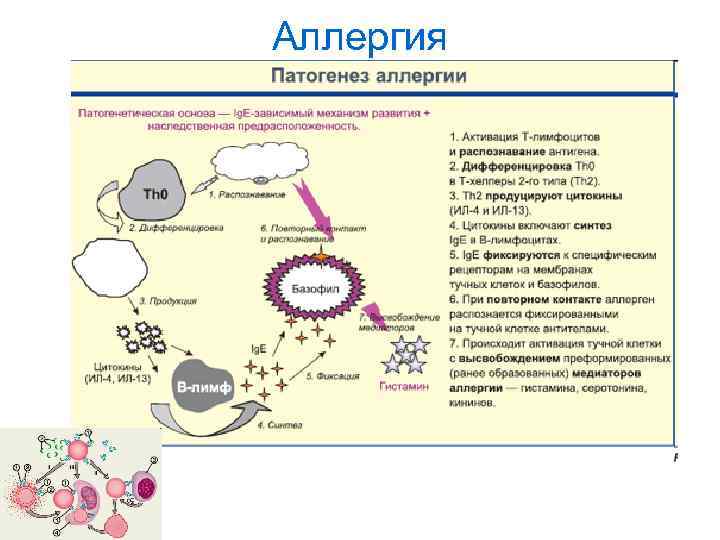 Аллергия
Аллергия
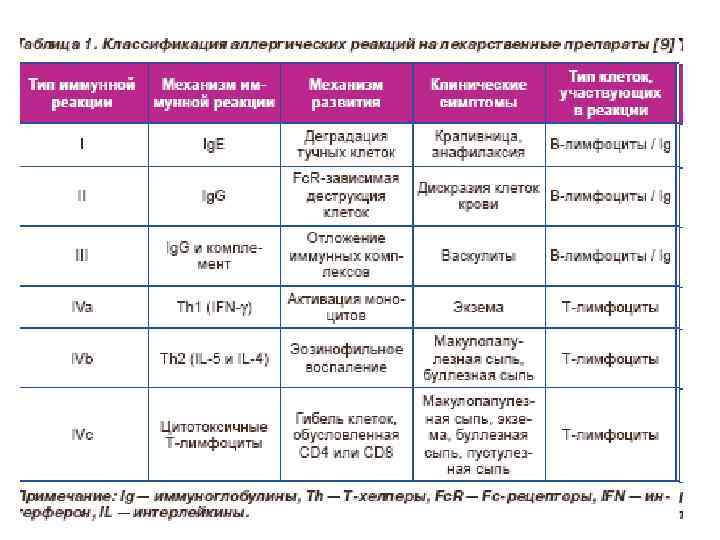
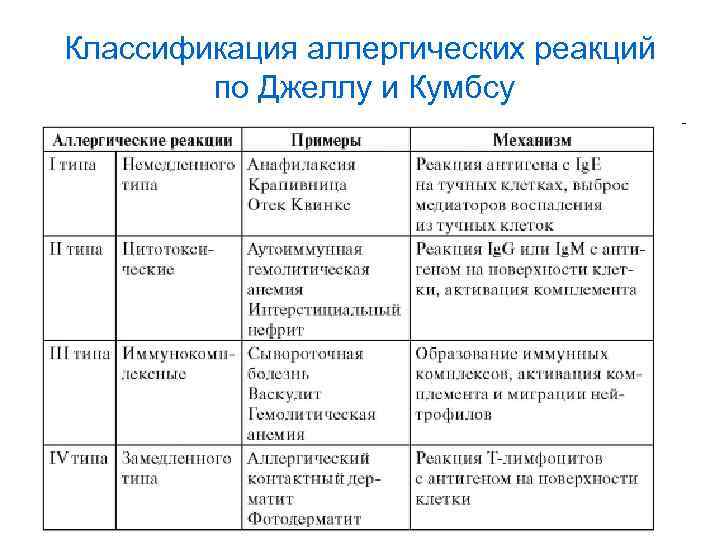 Классификация аллергических реакций по Джеллу и Кумбсу
Классификация аллергических реакций по Джеллу и Кумбсу
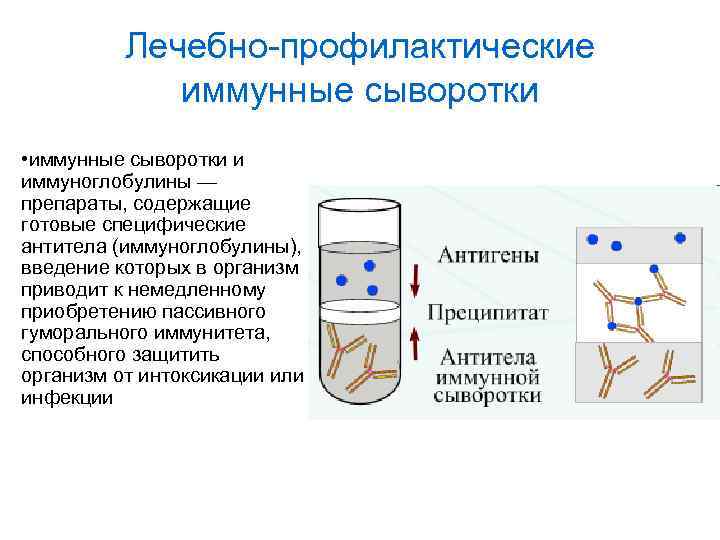 Лечебно-профилактические иммунные сыворотки • иммунные сыворотки и иммуноглобулины — препараты, содержащие готовые специфические антитела (иммуноглобулины), введение которых в организм приводит к немедленному приобретению пассивного гуморального иммунитета, способного защитить организм от интоксикации или инфекции
Лечебно-профилактические иммунные сыворотки • иммунные сыворотки и иммуноглобулины — препараты, содержащие готовые специфические антитела (иммуноглобулины), введение которых в организм приводит к немедленному приобретению пассивного гуморального иммунитета, способного защитить организм от интоксикации или инфекции
 История вакцинации • В Англии существовала примета, что доярки, переболевшие коровьей оспой (которая является неопасным заболеванием), никогда не заболевают натуральной оспой (которая в своё время была бичом человечества, вызывая массовые смертоносные эпидемии). • Английский аптекарь и хирург Дженнер решил проверить эту примету строгими наблюдениями, и она подтвердилась. Установив это, 14 мая 1796 г. Дженнер привил коровью оспу 8 -летнему Джеймсу Фипсу, а через полтора месяца — человеческую оспу — и мальчик не заболел. (т. е. сделал мальчику инокуляцию, сам Дженнер перенес ту же процедуру в 8 -летнем возрасте и , обладая иммунитетом от оспы, на себе проверить не мог). Так была экспериментально доказана возможность относительно безопасных профилактических прививок. • Однако в то время возможности этого метода были ограничены, так как он был основан на случайности, заключающейся в существовании в природе двух родственных болезней разной силы. Лишь сто лет спустя французскому микробиологу Луи Пастеру удалось целенаправленно ослабить болезнетворность возбудителей других заболеваний и приготовить из них препараты для прививок. В 1881 он создал прививку против сибирской язвы, а в 1885 – против бешенства. • Пастер предложил называть такие препараты вакцинами, а процедуру их применения - вакцинацией (от латинского «вакка» , что означает «корова» ).
История вакцинации • В Англии существовала примета, что доярки, переболевшие коровьей оспой (которая является неопасным заболеванием), никогда не заболевают натуральной оспой (которая в своё время была бичом человечества, вызывая массовые смертоносные эпидемии). • Английский аптекарь и хирург Дженнер решил проверить эту примету строгими наблюдениями, и она подтвердилась. Установив это, 14 мая 1796 г. Дженнер привил коровью оспу 8 -летнему Джеймсу Фипсу, а через полтора месяца — человеческую оспу — и мальчик не заболел. (т. е. сделал мальчику инокуляцию, сам Дженнер перенес ту же процедуру в 8 -летнем возрасте и , обладая иммунитетом от оспы, на себе проверить не мог). Так была экспериментально доказана возможность относительно безопасных профилактических прививок. • Однако в то время возможности этого метода были ограничены, так как он был основан на случайности, заключающейся в существовании в природе двух родственных болезней разной силы. Лишь сто лет спустя французскому микробиологу Луи Пастеру удалось целенаправленно ослабить болезнетворность возбудителей других заболеваний и приготовить из них препараты для прививок. В 1881 он создал прививку против сибирской язвы, а в 1885 – против бешенства. • Пастер предложил называть такие препараты вакцинами, а процедуру их применения - вакцинацией (от латинского «вакка» , что означает «корова» ).
 • Формирование иммунитета вакциначто в организм человека ми Смысл вакцинации заключается в том, вводятся вакцины: ослабленные или убитые возбудители различных инфекций (или искусственно синтезированные белки, которые идентичны белкам возбудителя). • Многие прививки можно делать одновременно. При этом существует ряд препаратов, которые изначально представляют собой смесь нескольких вакцин. Например, вакцина АКДС направлена против коклюша, дифтерии и столбняка. • Некоторые вакцины создают иммунитет с первого раза, другие приходится вводить повторно. Так называемая, ревакцинация — мероприятие, направленное на поддержание иммунитета, выработанного предыдущими прививками. Обычно она проводится через несколько лет после первой вакцинации. • Сегодня научными центрами разработаны специальные календари прививок. Они позволяют максимально защитить человека от заболевания тяжёлыми и опасными инфекциями. Если Вы планируете беременность или собираетесь в путешествие по экзотической стране — могут потребоваться дополнительные прививки.
• Формирование иммунитета вакциначто в организм человека ми Смысл вакцинации заключается в том, вводятся вакцины: ослабленные или убитые возбудители различных инфекций (или искусственно синтезированные белки, которые идентичны белкам возбудителя). • Многие прививки можно делать одновременно. При этом существует ряд препаратов, которые изначально представляют собой смесь нескольких вакцин. Например, вакцина АКДС направлена против коклюша, дифтерии и столбняка. • Некоторые вакцины создают иммунитет с первого раза, другие приходится вводить повторно. Так называемая, ревакцинация — мероприятие, направленное на поддержание иммунитета, выработанного предыдущими прививками. Обычно она проводится через несколько лет после первой вакцинации. • Сегодня научными центрами разработаны специальные календари прививок. Они позволяют максимально защитить человека от заболевания тяжёлыми и опасными инфекциями. Если Вы планируете беременность или собираетесь в путешествие по экзотической стране — могут потребоваться дополнительные прививки.
 Е. Дженер, 1725 г. Э. Беринг, 1890 г. Л. Пастер в лаборатории, 1878 г.
Е. Дженер, 1725 г. Э. Беринг, 1890 г. Л. Пастер в лаборатории, 1878 г.
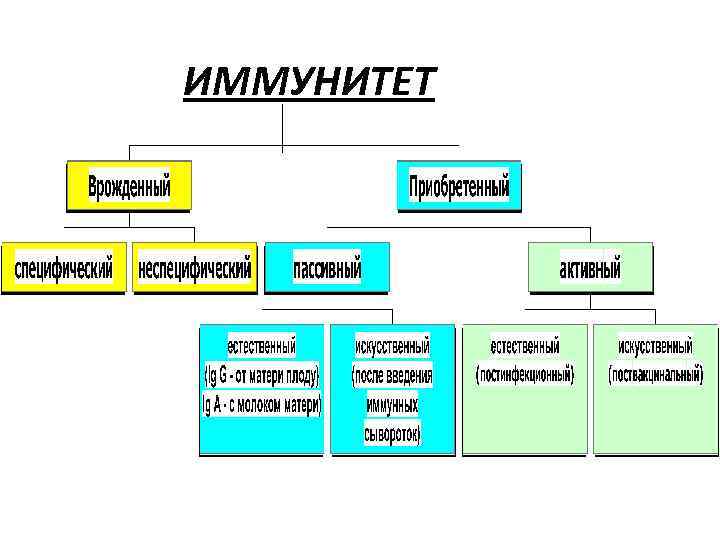 ИММУНИТЕТ
ИММУНИТЕТ
 Активный иммунитет. Искусственный Естественный После перенесенной инфекции Введение вакцин: Ø Ø Ø Ø Живые (аттенуированные); Убитые (инактивированные); Химические; Субкомпонентные; Генноинженерные; Антиидиотипические; ДНК-вакцины
Активный иммунитет. Искусственный Естественный После перенесенной инфекции Введение вакцин: Ø Ø Ø Ø Живые (аттенуированные); Убитые (инактивированные); Химические; Субкомпонентные; Генноинженерные; Антиидиотипические; ДНК-вакцины
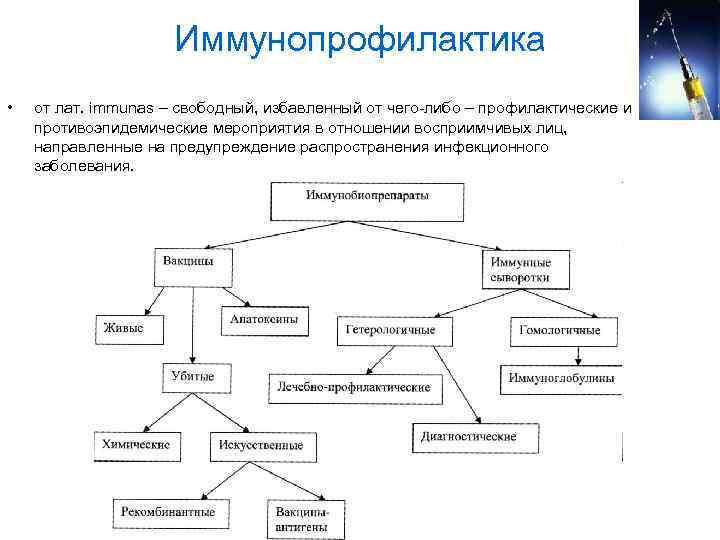 Иммунопрофилактика • от лат. immunas – свободный, избавленный от чего-либо – профилактические и противоэпидемические мероприятия в отношении восприимчивых лиц, направленные на предупреждение распространения инфекционного заболевания.
Иммунопрофилактика • от лат. immunas – свободный, избавленный от чего-либо – профилактические и противоэпидемические мероприятия в отношении восприимчивых лиц, направленные на предупреждение распространения инфекционного заболевания.
 Вакцинация • История иммунизации имеет давнюю историю. Начиная с позитивного опыта лекарей древней Индии и Китая, которые использовали инфекционные антигены от заболевших и инокулировали их на слизистые здоровых людей с цель вызвать в будущем защитную реакцию от данного инфекционного патогенна. Формирование научных взглядов, знаний и практических навыков в области формирования искусственного вторичного иммунитета принадлежит основателю микробиологии, иммунологии и вакцинации Луису Пастеру. Особенностью вторичного приобретенного или адаптивного иммунитета является способность иммунных клеток к соматической перегруппировке генов иммуноглобулинов и TCR. Эта способность не наследуется. потомство получает от родителя только набор зародышевых генов, а затем формирует свой спектр приобретенного иммунитета. Эмбрион имея только зародышевые гены, начинает строить свою иммунную систему в постнатальном развитии. • Благодаря этому феномену возможным стало применение вакцин для формирования искусственного иммунитета. Обсуждение триумфальных результатов вакцинации животных
Вакцинация • История иммунизации имеет давнюю историю. Начиная с позитивного опыта лекарей древней Индии и Китая, которые использовали инфекционные антигены от заболевших и инокулировали их на слизистые здоровых людей с цель вызвать в будущем защитную реакцию от данного инфекционного патогенна. Формирование научных взглядов, знаний и практических навыков в области формирования искусственного вторичного иммунитета принадлежит основателю микробиологии, иммунологии и вакцинации Луису Пастеру. Особенностью вторичного приобретенного или адаптивного иммунитета является способность иммунных клеток к соматической перегруппировке генов иммуноглобулинов и TCR. Эта способность не наследуется. потомство получает от родителя только набор зародышевых генов, а затем формирует свой спектр приобретенного иммунитета. Эмбрион имея только зародышевые гены, начинает строить свою иммунную систему в постнатальном развитии. • Благодаря этому феномену возможным стало применение вакцин для формирования искусственного иммунитета. Обсуждение триумфальных результатов вакцинации животных
 Вакцины • (от лат. vacca — корова) — медицинские или ветеринарные иммунобиологические препараты, предназначенные для создания активного иммунитета к возбудителям инфекционных заболеваний.
Вакцины • (от лат. vacca — корова) — медицинские или ветеринарные иммунобиологические препараты, предназначенные для создания активного иммунитета к возбудителям инфекционных заболеваний.
 Классификация вакцин • Корпускулярные - ослабленные или убитые клетки бактерий или компоненты вириона (вирионы) • Жидкие – протективные антигеныиммуногены (химические, анатоксины, субкомпонентные и др. )
Классификация вакцин • Корпускулярные - ослабленные или убитые клетки бактерий или компоненты вириона (вирионы) • Жидкие – протективные антигеныиммуногены (химические, анатоксины, субкомпонентные и др. )
 Живые (аттенуированные) вакцины Бактериальные Вирусные Для профилактики Для 1) Туберкулеза (БЦЖ); профилактики 1) Гриппа 2) Сибирской язвы 3) Чумы 4) Туляремии 2)Полиомиелита 3) Кори 4) Бешенства 5) Краснухи и другие Риккетсиозные Для профилактики Сыпного тифа
Живые (аттенуированные) вакцины Бактериальные Вирусные Для профилактики Для 1) Туберкулеза (БЦЖ); профилактики 1) Гриппа 2) Сибирской язвы 3) Чумы 4) Туляремии 2)Полиомиелита 3) Кори 4) Бешенства 5) Краснухи и другие Риккетсиозные Для профилактики Сыпного тифа
 Инактивированные (убитые) вакцины Бактериальные Для профилактики Ø Коклюша; Ø Брюшного тифа Вирусные Для профилактики Ø Полиомиелита (Солка) Ø Гепатита А Ø Гриппа Ø Бешенства Ø Клещевого энцефалита
Инактивированные (убитые) вакцины Бактериальные Для профилактики Ø Коклюша; Ø Брюшного тифа Вирусные Для профилактики Ø Полиомиелита (Солка) Ø Гепатита А Ø Гриппа Ø Бешенства Ø Клещевого энцефалита
 Анатоксины Для профилактики Ø Ø Столбняка Дифтерии Стафилококковой инфекции Холеры
Анатоксины Для профилактики Ø Ø Столбняка Дифтерии Стафилококковой инфекции Холеры
 Преобразование токсина в анатоксин химическое воздействие Токсическая часть молекулы Антигенная детерминанта
Преобразование токсина в анатоксин химическое воздействие Токсическая часть молекулы Антигенная детерминанта
 Вакцины будущего üАнтиидиотипические üДНК-вакцины üРекомбинантные
Вакцины будущего üАнтиидиотипические üДНК-вакцины üРекомбинантные
 Рекомбинантные вакцины • Для производства этих вакцин применяют методы генной инженерии, встраивая генетический материал микроорганизма в дрожжевые клетки, продуцирующие антиген. • После культивирования дрожжей из них выделяют нужный антиген, очищают и готовят вакцину (вакцина против гепатита В, а также вакцина против вируса папилломы человека).
Рекомбинантные вакцины • Для производства этих вакцин применяют методы генной инженерии, встраивая генетический материал микроорганизма в дрожжевые клетки, продуцирующие антиген. • После культивирования дрожжей из них выделяют нужный антиген, очищают и готовят вакцину (вакцина против гепатита В, а также вакцина против вируса папилломы человека).
 ДНК-вакцина в микроконтейнере ПОЛУЧЕНИЕ: • • • В многослойную биодеградируемую полимерную оболочку можно помещать белки, ДНК, другие молекулы вирусов или бактерий. Оболочка – из полимолочной кислоты, карбоната кальция, липидов. Микрокапсулы с активной «начинкой» из ДНК имеют размер 1 -2 мкм (эритроцит 89). Способ введения - подкожно/ внутривенно/ спрей. Иммунокомпетентные клетки «заглатывают» капсулы. При помощи ферментов оболочка растворяется, «начинака» выходит. • • ПРЕИМУЩЕСТВА: 1. Микрокапсулированная ДНК микроорганизмов, попав в клетки, позволяет организму самому производить достаточное количество антигена, формирующего иммунитет. 2. Выхода ДНК из капсул в организме происходит постепенно (минимум месяц). 3. Безинъекционное введение вакцины - СПРЕЙ.
ДНК-вакцина в микроконтейнере ПОЛУЧЕНИЕ: • • • В многослойную биодеградируемую полимерную оболочку можно помещать белки, ДНК, другие молекулы вирусов или бактерий. Оболочка – из полимолочной кислоты, карбоната кальция, липидов. Микрокапсулы с активной «начинкой» из ДНК имеют размер 1 -2 мкм (эритроцит 89). Способ введения - подкожно/ внутривенно/ спрей. Иммунокомпетентные клетки «заглатывают» капсулы. При помощи ферментов оболочка растворяется, «начинака» выходит. • • ПРЕИМУЩЕСТВА: 1. Микрокапсулированная ДНК микроорганизмов, попав в клетки, позволяет организму самому производить достаточное количество антигена, формирующего иммунитет. 2. Выхода ДНК из капсул в организме происходит постепенно (минимум месяц). 3. Безинъекционное введение вакцины - СПРЕЙ.
 АДЪЮВАНТЫ Антигенные и неантигенные субстанции, оказывающие неспецифическое стимулирующее влияние на иммунные реакции.
АДЪЮВАНТЫ Антигенные и неантигенные субстанции, оказывающие неспецифическое стимулирующее влияние на иммунные реакции.
 Типы адъювантов Неорганические ü Минеральные коллоиды ü Растворимые неорганические соединения ü Кристаллоиды Органические ü Липиды ü Углеводы ü Сложные вещества: (липополисахаридные комплексы, микробные клетки кислотоустойчивых бактерий, микробные липополисахариды и др. )
Типы адъювантов Неорганические ü Минеральные коллоиды ü Растворимые неорганические соединения ü Кристаллоиды Органические ü Липиды ü Углеводы ü Сложные вещества: (липополисахаридные комплексы, микробные клетки кислотоустойчивых бактерий, микробные липополисахариды и др. )
 Антивакцинаторство (противопрививочное движение) • — общественное движение, оспаривающее эффективность, безопасность и правомерность вакцинации, в частности — массовой вакцинации. • Согласно заключению экспертов ВОЗ большинство доводов антивакцинаторов не подтверждаются научными данными и характеризуются как «тревожное и опасное заблуждение» .
Антивакцинаторство (противопрививочное движение) • — общественное движение, оспаривающее эффективность, безопасность и правомерность вакцинации, в частности — массовой вакцинации. • Согласно заключению экспертов ВОЗ большинство доводов антивакцинаторов не подтверждаются научными данными и характеризуются как «тревожное и опасное заблуждение» .
 Иммунные сыворотки • Из сыворотки крови человека (гомологичные) – 1. Иммунитет сохраняется до 6 месяцев. 2. Наименее анитигенно чужеродные. • Из сыворотки крови животных (гетерологичные) – 1. Иммунитет сохраняется до 2 -3 недель. 2. Из-за антигенной чужеродности чаще встречаются побочные явления.
Иммунные сыворотки • Из сыворотки крови человека (гомологичные) – 1. Иммунитет сохраняется до 6 месяцев. 2. Наименее анитигенно чужеродные. • Из сыворотки крови животных (гетерологичные) – 1. Иммунитет сохраняется до 2 -3 недель. 2. Из-за антигенной чужеродности чаще встречаются побочные явления.
 Пассивная иммунизация Заболевание Источник антител Применение Дифтерия, столбняк человек, лошадь профилактика, лечение Ветряная оспа человек при иммунодефицитах Газовая гангрена, ботулизм, змеиный яд лошадь после заражения Бешенство человек после заражения Гипогамма-глобулинемия человек профилактика
Пассивная иммунизация Заболевание Источник антител Применение Дифтерия, столбняк человек, лошадь профилактика, лечение Ветряная оспа человек при иммунодефицитах Газовая гангрена, ботулизм, змеиный яд лошадь после заражения Бешенство человек после заражения Гипогамма-глобулинемия человек профилактика
 Преимущества и недостатки пассивной иммунизации преимущества недостатки Ú непродолжительность иммунитета; Ú немедленная защита Ú опасность возникновения сывороточной болезни; Ú риск заражения гепатитами и СПИДом.
Преимущества и недостатки пассивной иммунизации преимущества недостатки Ú непродолжительность иммунитета; Ú немедленная защита Ú опасность возникновения сывороточной болезни; Ú риск заражения гепатитами и СПИДом.
 Реакции гиперчувствительности, обусловленные введением сывороток • Анафилактический шок Анафилаксия - форма измененной реактивности, состояние повышенной чувствительности организма, вызванное повторным введением чужеродных белков • Сывороточная болезнь Это форма гиперчувствительности немедленного типа. Развивается через 8 -12 суток после однократного первичного введения больших доз сыворотки
Реакции гиперчувствительности, обусловленные введением сывороток • Анафилактический шок Анафилаксия - форма измененной реактивности, состояние повышенной чувствительности организма, вызванное повторным введением чужеродных белков • Сывороточная болезнь Это форма гиперчувствительности немедленного типа. Развивается через 8 -12 суток после однократного первичного введения больших доз сыворотки
 Симптомы анафилактического шока • Возбуждение, страх, резкая головная боль. • Бледность, цианоз кожных покровов, высыпания. • Отек гортани, трахеи и, как результат удушье. • Бронхоспазм. • Падение АД. • Потеря сознания, судороги.
Симптомы анафилактического шока • Возбуждение, страх, резкая головная боль. • Бледность, цианоз кожных покровов, высыпания. • Отек гортани, трахеи и, как результат удушье. • Бронхоспазм. • Падение АД. • Потеря сознания, судороги.
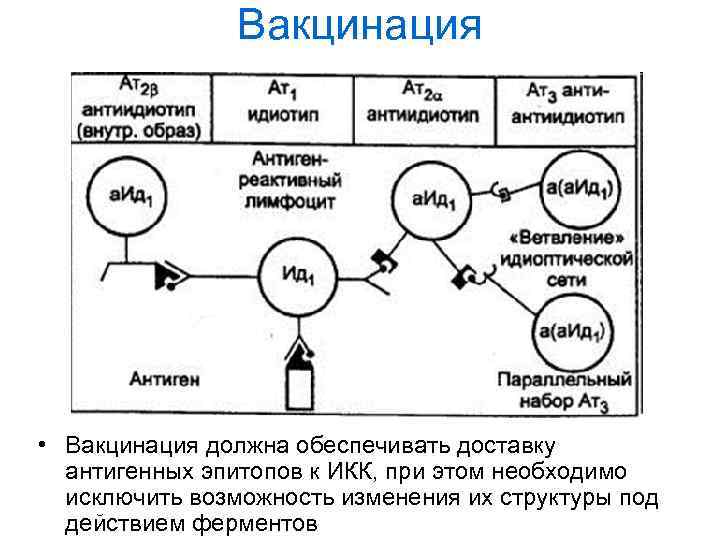 Вакцинация • Вакцинация должна обеспечивать доставку антигенных эпитопов к ИКК, при этом необходимо исключить возможность изменения их структуры под действием ферментов
Вакцинация • Вакцинация должна обеспечивать доставку антигенных эпитопов к ИКК, при этом необходимо исключить возможность изменения их структуры под действием ферментов
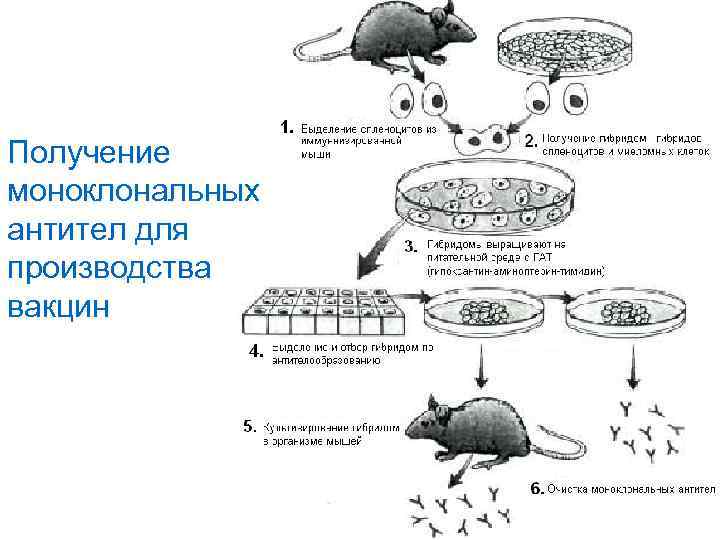 Получение моноклональных антител для производства вакцин
Получение моноклональных антител для производства вакцин


