Lektsia_3-2012.ppt
- Количество слайдов: 14
 Лекция 3 Алкены
Лекция 3 Алкены
 Алкены. (Этиленовые, ненасыщенные, непредельные углеводороды, олефины). Алкены – это углеводороды, в молекулах которых имеется двойная связь. Общая формула – Сn. Н 2 n.
Алкены. (Этиленовые, ненасыщенные, непредельные углеводороды, олефины). Алкены – это углеводороды, в молекулах которых имеется двойная связь. Общая формула – Сn. Н 2 n.
 1. Общие сведения. 1). Строение, гибридизация Атомы углерода при двойной связи находятся в состоянии гибридизации sp 2. Три равноценные sp 2 гибридизованные связи атома углерода находятся в одной плоскости под углом 120 o. С друг к другу. Четвертая, негибридизованная орбиталь, находится в плоскости, перпендикулярной плоскости расположения остальных орбиталей. Три сигма-связи атома углерода при двойной связи образуются за счет осевого перекрывания sp 2 гибридизованных орбиталей с орбиталями соседних атомов. Негибридизованные p- орбитали соседних атомов углерода перекрываются боком, образуя π - связь. π –связь менее прочна, чем сигма – связи, и раскрывается с образованием новых сигма-связей при действии многих реагентов. Сочетание сигма (σ) и пи (π)- связей и называется двойной связью.
1. Общие сведения. 1). Строение, гибридизация Атомы углерода при двойной связи находятся в состоянии гибридизации sp 2. Три равноценные sp 2 гибридизованные связи атома углерода находятся в одной плоскости под углом 120 o. С друг к другу. Четвертая, негибридизованная орбиталь, находится в плоскости, перпендикулярной плоскости расположения остальных орбиталей. Три сигма-связи атома углерода при двойной связи образуются за счет осевого перекрывания sp 2 гибридизованных орбиталей с орбиталями соседних атомов. Негибридизованные p- орбитали соседних атомов углерода перекрываются боком, образуя π - связь. π –связь менее прочна, чем сигма – связи, и раскрывается с образованием новых сигма-связей при действии многих реагентов. Сочетание сигма (σ) и пи (π)- связей и называется двойной связью.
 2). Изомерия а) Структурная 1 - по строению углеродного скелета 2 - по положению двойной связи в цепи б) Пространственная Геометрическая цис- трансизомерия.
2). Изомерия а) Структурная 1 - по строению углеродного скелета 2 - по положению двойной связи в цепи б) Пространственная Геометрическая цис- трансизомерия.
 В) межклассовая изомерия ¡ Алкены изомерны циклоалканам
В) межклассовая изомерия ¡ Алкены изомерны циклоалканам
 3). Номенклатура а)Названия непредельных радикалов Углеводород СН 2 = СН 2 этен (этилен) СН 2 = СН- СН 3 пропен (пропилен) Радикал Название радикала СН 2 = СН- Винил, СН 2=СН-СН 2 - аллил СН 2 = С-СН 3 этенил 2 - пропенил Изопропенил 1 -метилэтенил
3). Номенклатура а)Названия непредельных радикалов Углеводород СН 2 = СН 2 этен (этилен) СН 2 = СН- СН 3 пропен (пропилен) Радикал Название радикала СН 2 = СН- Винил, СН 2=СН-СН 2 - аллил СН 2 = С-СН 3 этенил 2 - пропенил Изопропенил 1 -метилэтенил
 Б) Рациональная номенклатура - все алкены называются как производные родоначальника ряда этилена ¡ ¡ В) Систематическая номенклатура 1. Выбирают самую длинную углеродную цепь, включающую двойную связь 2. Цепочку нумеруют, начиная с того края, к которому ближе двойная связь 3. Перечисляют заместители в алфавитном порядке. Цифрой указывают их положение в цепи. Умножающие приставки в алфавитном перечне не учитываются.
Б) Рациональная номенклатура - все алкены называются как производные родоначальника ряда этилена ¡ ¡ В) Систематическая номенклатура 1. Выбирают самую длинную углеродную цепь, включающую двойную связь 2. Цепочку нумеруют, начиная с того края, к которому ближе двойная связь 3. Перечисляют заместители в алфавитном порядке. Цифрой указывают их положение в цепи. Умножающие приставки в алфавитном перечне не учитываются.
 4. Называют самую длинную цепь, при этом окончание «ан» соответствующего алкана меняют на окончание «ен» . Цифрой указывают положение двойной связи в цепи. ¡ : Г) Примеры: ¡ название ¡ тривиальное ¡ ¡ ¡ ¡ рац. Систем. СН 2=СН 2 этилен этен СН 2=СН-СН 3 пропилен метилэтилен пропен СН 2=С-СН 3 изобутилен несим. диметилэтилен 2 метилпропен-1 СН 3 2 1 5 4 3/ СН=СН 2 СН 3–СН- СН-СН 3 3, 4 -диметил- 1 -пентен СН 3
4. Называют самую длинную цепь, при этом окончание «ан» соответствующего алкана меняют на окончание «ен» . Цифрой указывают положение двойной связи в цепи. ¡ : Г) Примеры: ¡ название ¡ тривиальное ¡ ¡ ¡ ¡ рац. Систем. СН 2=СН 2 этилен этен СН 2=СН-СН 3 пропилен метилэтилен пропен СН 2=С-СН 3 изобутилен несим. диметилэтилен 2 метилпропен-1 СН 3 2 1 5 4 3/ СН=СН 2 СН 3–СН- СН-СН 3 3, 4 -диметил- 1 -пентен СН 3
 2. Методы получения 1. Низкомолекулярные алкены в природе не встречаются. Высокомолекулярные алкены встречаются в незначительном количестве в нефтях, в растительном мире, при этом двойная связь содержится, как правило, в каком-либо циклическом фрагменте высокомолекулярной молекулы. 2. Дегидрирование алканов (катализатор Cr 2 O 3, t ~ 400 C) СН 3 – СН 2 – СН 3 3. Термический СН 2= СН – СН 3 + Н 2 и каталитический крекинг алканов (t > 400 C) CН 3 -СН 2–СН 3 СН 2 = СН 2 + СН 3–СН 2–СН 3
2. Методы получения 1. Низкомолекулярные алкены в природе не встречаются. Высокомолекулярные алкены встречаются в незначительном количестве в нефтях, в растительном мире, при этом двойная связь содержится, как правило, в каком-либо циклическом фрагменте высокомолекулярной молекулы. 2. Дегидрирование алканов (катализатор Cr 2 O 3, t ~ 400 C) СН 3 – СН 2 – СН 3 3. Термический СН 2= СН – СН 3 + Н 2 и каталитический крекинг алканов (t > 400 C) CН 3 -СН 2–СН 3 СН 2 = СН 2 + СН 3–СН 2–СН 3
 4. Дегидрогалогенирование галогенпроизводных под действием спиртового раствора щелочи. Проходит по правилу Зайцева: при отщеплении галогеноводорода от галогенпроизводного углеводорода водород отщепляется от соседнего с галогеном атома углерода. КОН СН 3–СН – СН 2– СН 3 Сl ¡ ¡ ¡ ¡ ¡ СН 3 -СН = СН-СН 3 + КСl + Н 2 О спирт 5. Дегидратация спиртов – проходит также по правилу Зайцева. В качестве катализаторов используются серная кислота, оксид алюминия при нагревании. / СН 3 -СН –СН -СН 3 ОН Al 2 O 3 t~300 o. C / СН 3 - СН = С – СН 3 6. Дегалогенирование дигалогенпроизводных. Zn СН 2–СН–СН 3 CH 2=CH–CH 3 + Br Br + Н 2 О Zn. Br 2
4. Дегидрогалогенирование галогенпроизводных под действием спиртового раствора щелочи. Проходит по правилу Зайцева: при отщеплении галогеноводорода от галогенпроизводного углеводорода водород отщепляется от соседнего с галогеном атома углерода. КОН СН 3–СН – СН 2– СН 3 Сl ¡ ¡ ¡ ¡ ¡ СН 3 -СН = СН-СН 3 + КСl + Н 2 О спирт 5. Дегидратация спиртов – проходит также по правилу Зайцева. В качестве катализаторов используются серная кислота, оксид алюминия при нагревании. / СН 3 -СН –СН -СН 3 ОН Al 2 O 3 t~300 o. C / СН 3 - СН = С – СН 3 6. Дегалогенирование дигалогенпроизводных. Zn СН 2–СН–СН 3 CH 2=CH–CH 3 + Br Br + Н 2 О Zn. Br 2
 3. Физические свойства Алкены С 2 - С 4 - газы, С 5 - С 17 жидкости, С 18 и выше – твердые вещества. ¡ Алкены плохо растворимы в воде, но лучше, чем парафины; хорошо растворяются в органических растворителях. ¡
3. Физические свойства Алкены С 2 - С 4 - газы, С 5 - С 17 жидкости, С 18 и выше – твердые вещества. ¡ Алкены плохо растворимы в воде, но лучше, чем парафины; хорошо растворяются в органических растворителях. ¡
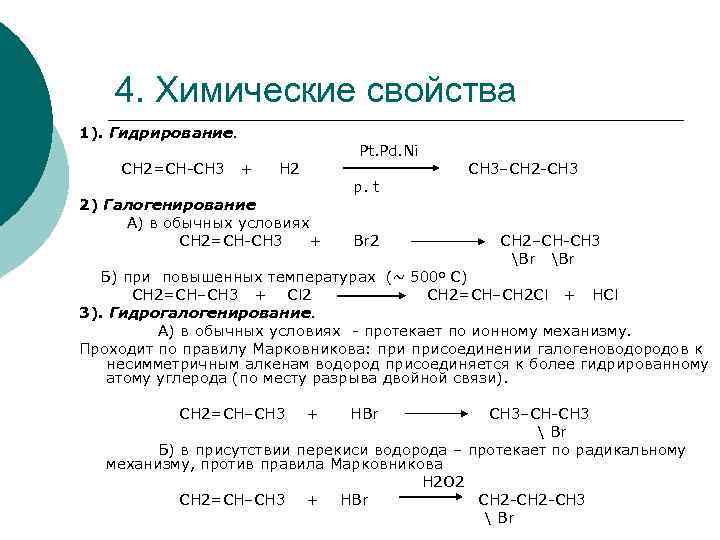 4. Химические свойства 1). Гидрирование. СН 2=СН-СН 3 + Pt. Pd. Ni Н 2 2) Галогенирование А) в обычных условиях СН 2=СН-СН 3 + p. t Br 2 СН 3–СН 2 -СН 3 СН 2–СН-СН 3 Br Б) при повышенных температурах (~ 500 o С) СН 2=СН–СН 3 + Cl 2 CH 2=CH–CH 2 Cl + HCl 3). Гидрогалогенирование. А) в обычных условиях - протекает по ионному механизму. Проходит по правилу Марковникова: присоединении галогеноводородов к несимметричным алкенам водород присоединяется к более гидрированному атому углерода (по месту разрыва двойной связи). СН 2=СН–СН 3 + НBr СН 3–СН-СН 3 Br Б) в присутствии перекиси водорода – протекает по радикальному механизму, против правила Марковникова H 2 O 2 СН 2=СН–СН 3 + НBr СН 2 -СН 3 Br
4. Химические свойства 1). Гидрирование. СН 2=СН-СН 3 + Pt. Pd. Ni Н 2 2) Галогенирование А) в обычных условиях СН 2=СН-СН 3 + p. t Br 2 СН 3–СН 2 -СН 3 СН 2–СН-СН 3 Br Б) при повышенных температурах (~ 500 o С) СН 2=СН–СН 3 + Cl 2 CH 2=CH–CH 2 Cl + HCl 3). Гидрогалогенирование. А) в обычных условиях - протекает по ионному механизму. Проходит по правилу Марковникова: присоединении галогеноводородов к несимметричным алкенам водород присоединяется к более гидрированному атому углерода (по месту разрыва двойной связи). СН 2=СН–СН 3 + НBr СН 3–СН-СН 3 Br Б) в присутствии перекиси водорода – протекает по радикальному механизму, против правила Марковникова H 2 O 2 СН 2=СН–СН 3 + НBr СН 2 -СН 3 Br
 Химические свойства 4) Гидратация. СН 2 = СН 2 + Н 2 О Н 2 SO 4 СН 3 –СН 2 - ОН t На этом методе основано промышленное получение этилового спирта. При гидратации несимметричных алкенов реакция проходит по правилу Марковникова. 5) Полимеризация. n CH 2 = CH 2 (-CH 2 – CH 2 -)n полиэтилен n CH 2= CH – CH 3 (-CH 2 - CH-)n CH 3 полипропилен 6) Окисление. А) горение (полное окисление) СН 2 = СН 2 + 3 О 2 2 СО 2 + 2 Н 2 О Б) окисление в мягких условиях (разбавленным раствором КМn. О 4, реакция Вагнера) KMn. O 4 CH 2= CH – CH 3 CH 2 - CH – CH 3 пропиленгликоль H 2 O OH OH В) окисление в жестких условиях ( KMn. O 4, конц. Н 2 SO 4, кипячение) СН 3 - CH= CH –СН 2 - CH 3 СН 3 -СООН + СН 3 СН 2 СООН Г) окисление над серебряным катализатором. Ag CH 2= CH – CH 3 + O 2 CH 2 - CH – CH 3 оксид пропилена O
Химические свойства 4) Гидратация. СН 2 = СН 2 + Н 2 О Н 2 SO 4 СН 3 –СН 2 - ОН t На этом методе основано промышленное получение этилового спирта. При гидратации несимметричных алкенов реакция проходит по правилу Марковникова. 5) Полимеризация. n CH 2 = CH 2 (-CH 2 – CH 2 -)n полиэтилен n CH 2= CH – CH 3 (-CH 2 - CH-)n CH 3 полипропилен 6) Окисление. А) горение (полное окисление) СН 2 = СН 2 + 3 О 2 2 СО 2 + 2 Н 2 О Б) окисление в мягких условиях (разбавленным раствором КМn. О 4, реакция Вагнера) KMn. O 4 CH 2= CH – CH 3 CH 2 - CH – CH 3 пропиленгликоль H 2 O OH OH В) окисление в жестких условиях ( KMn. O 4, конц. Н 2 SO 4, кипячение) СН 3 - CH= CH –СН 2 - CH 3 СН 3 -СООН + СН 3 СН 2 СООН Г) окисление над серебряным катализатором. Ag CH 2= CH – CH 3 + O 2 CH 2 - CH – CH 3 оксид пропилена O
 5. Применение алкенов Главная область применения алкенов – получение полимерных материалов по реакции полимеризации. ¡ Алкены также широко используются для получения спиртов, галогенпроизводных, алкилароматических и других ценных соединений. ¡
5. Применение алкенов Главная область применения алкенов – получение полимерных материалов по реакции полимеризации. ¡ Алкены также широко используются для получения спиртов, галогенпроизводных, алкилароматических и других ценных соединений. ¡


