химия 4 12.pptx
- Количество слайдов: 49
 Лекция 3 2013 Органическая химия 1. Электронное строение органических соединений Лекцию читает проф. Иван Юрьевич Белавин 1 1
Лекция 3 2013 Органическая химия 1. Электронное строение органических соединений Лекцию читает проф. Иван Юрьевич Белавин 1 1
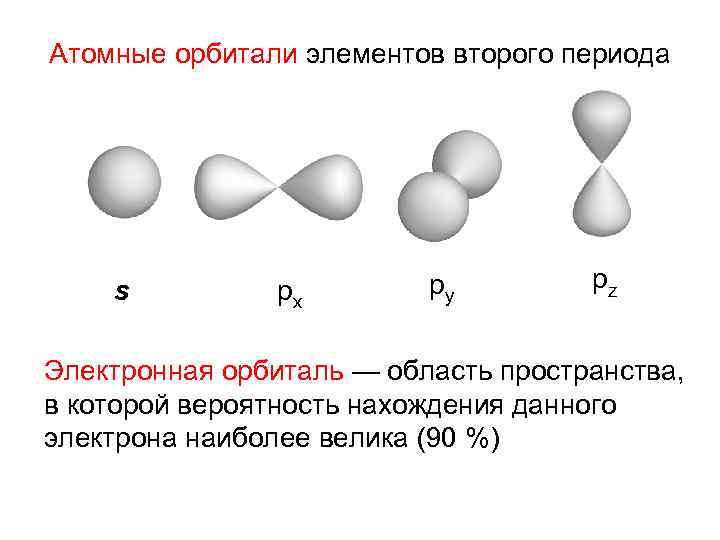 Атомные орбитали элементов второго периода s px py pz Электронная орбиталь — область пространства, в которой вероятность нахождения данного электрона наиболее велика (90 %)
Атомные орбитали элементов второго периода s px py pz Электронная орбиталь — область пространства, в которой вероятность нахождения данного электрона наиболее велика (90 %)
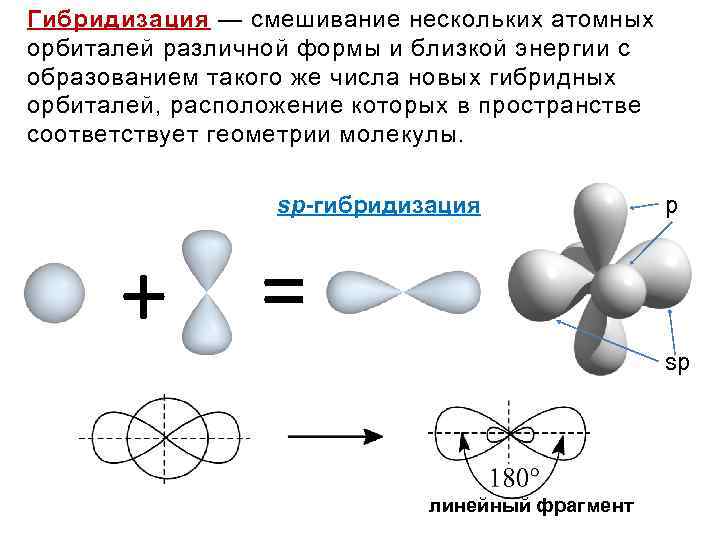 Гибридизация — смешивание нескольких атомных орбиталей различной формы и близкой энергии с образованием такого же числа новых гибридных орбиталей, расположение которых в пространстве соответствует геометрии молекулы. sp-гибридизация + = p sp линейный фрагмент
Гибридизация — смешивание нескольких атомных орбиталей различной формы и близкой энергии с образованием такого же числа новых гибридных орбиталей, расположение которых в пространстве соответствует геометрии молекулы. sp-гибридизация + = p sp линейный фрагмент
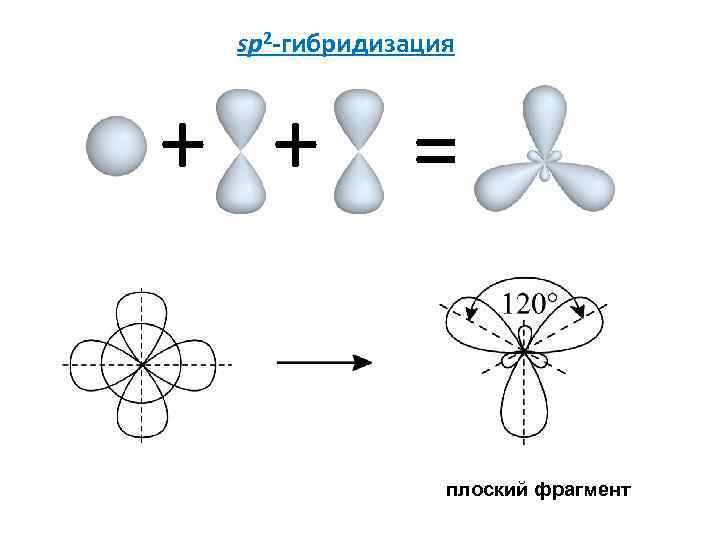 sp 2 -гибридизация + + = плоский фрагмент
sp 2 -гибридизация + + = плоский фрагмент
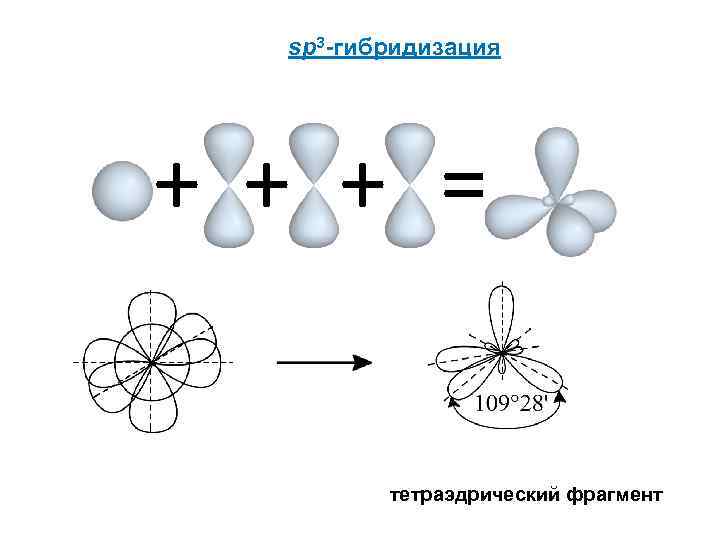 sp 3 -гибридизация + + + = тетраэдрический фрагмент
sp 3 -гибридизация + + + = тетраэдрический фрагмент
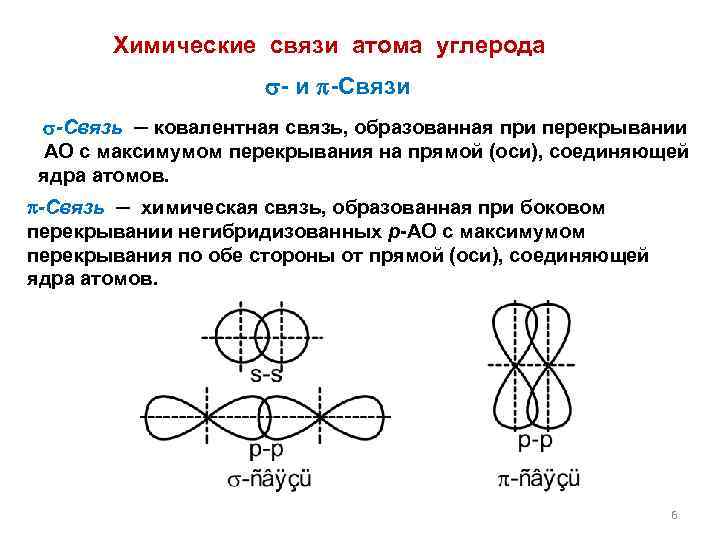 Химические связи атома углерода - и -Связь ─ ковалентная связь, образованная при перекрывании АО с максимумом перекрывания на прямой (оси), соединяющей ядра атомов. -Связь ─ химическая связь, образованная при боковом перекрывании негибридизованных р-АО с максимумом перекрывания по обе стороны от прямой (оси), соединяющей ядра атомов. 6
Химические связи атома углерода - и -Связь ─ ковалентная связь, образованная при перекрывании АО с максимумом перекрывания на прямой (оси), соединяющей ядра атомов. -Связь ─ химическая связь, образованная при боковом перекрывании негибридизованных р-АО с максимумом перекрывания по обе стороны от прямой (оси), соединяющей ядра атомов. 6
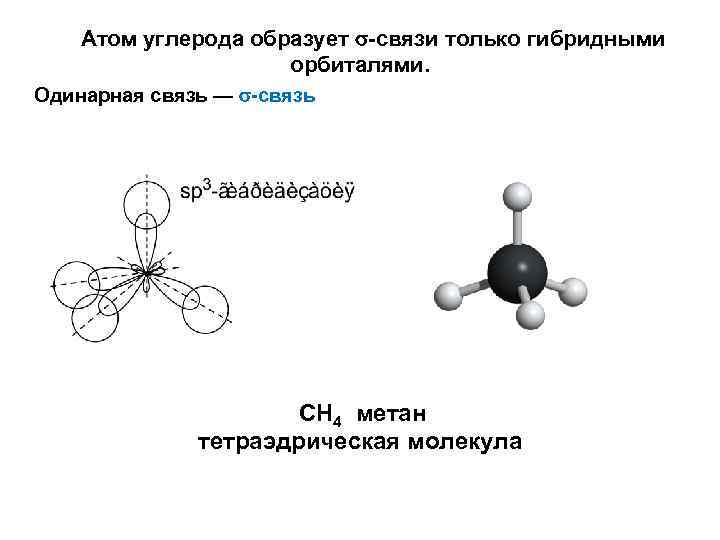 Атом углерода образует -связи только гибридными орбиталями. Одинарная связь — -связь СН 4 метан тетраэдрическая молекула
Атом углерода образует -связи только гибридными орбиталями. Одинарная связь — -связь СН 4 метан тетраэдрическая молекула
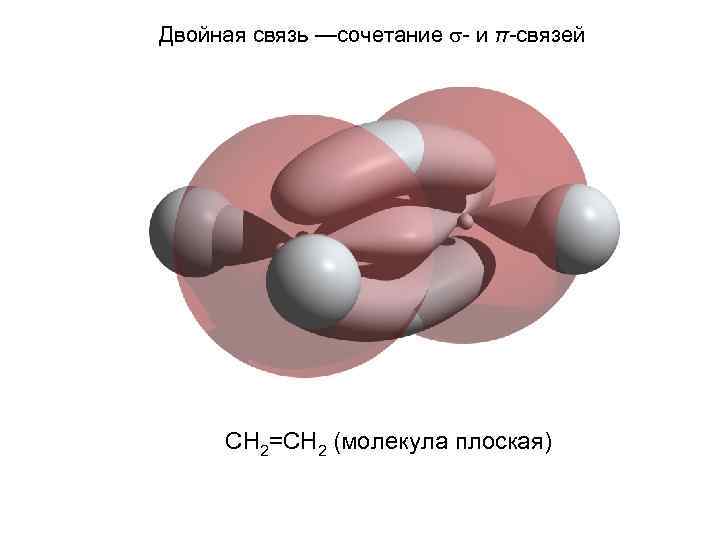 Двойная связь —сочетание - и π-связей СН 2=СН 2 (молекула плоская)
Двойная связь —сочетание - и π-связей СН 2=СН 2 (молекула плоская)
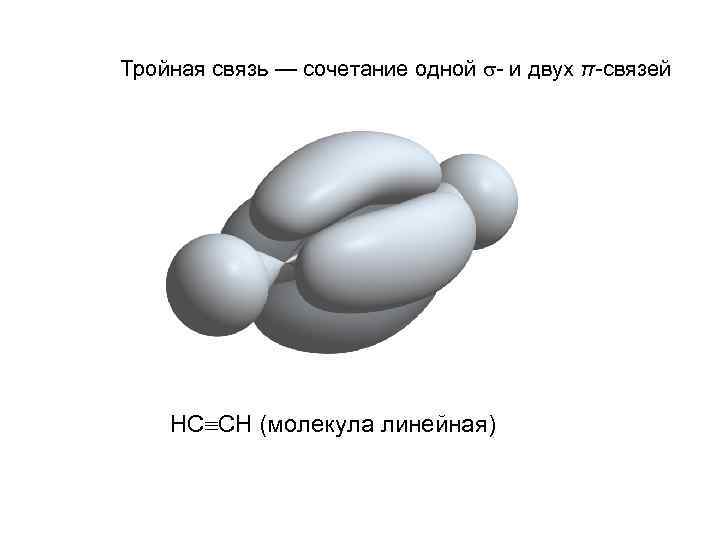 Тройная связь — сочетание одной - и двух π-связей НС СН (молекула линейная)
Тройная связь — сочетание одной - и двух π-связей НС СН (молекула линейная)
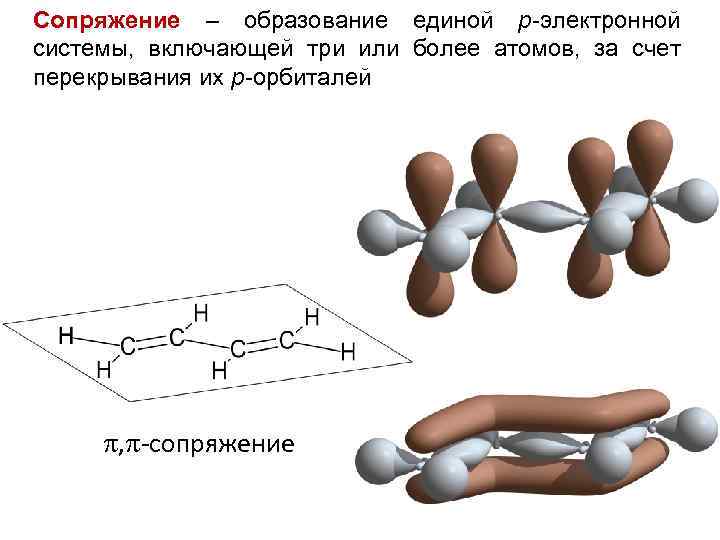 Сопряжение – образование единой р-электронной системы, включающей три или более атомов, за счет перекрывания их p-орбиталей , -сопряжение
Сопряжение – образование единой р-электронной системы, включающей три или более атомов, за счет перекрывания их p-орбиталей , -сопряжение
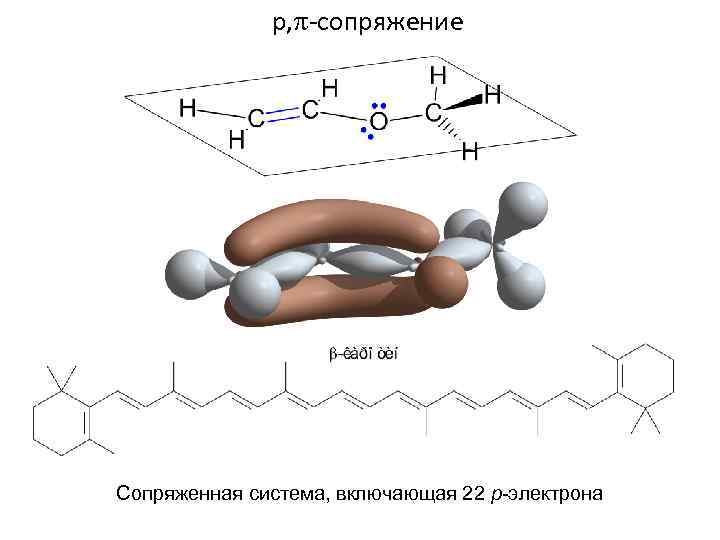 p, -cопряжение Сопряженная система, включающая 22 р-электрона
p, -cопряжение Сопряженная система, включающая 22 р-электрона
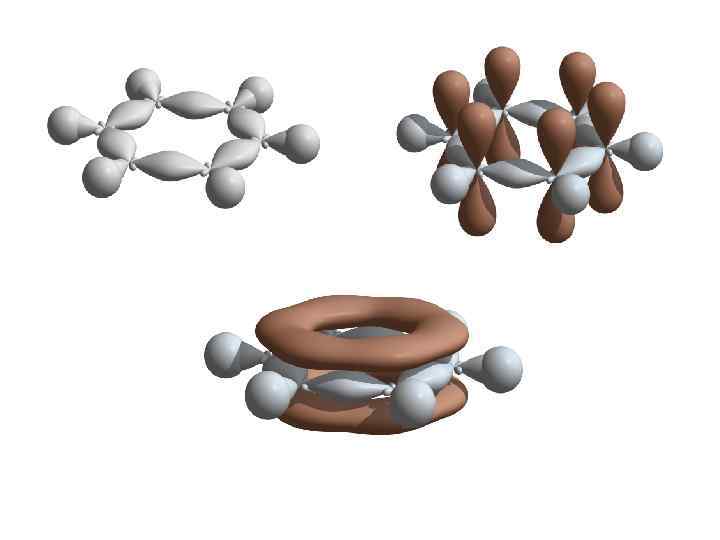
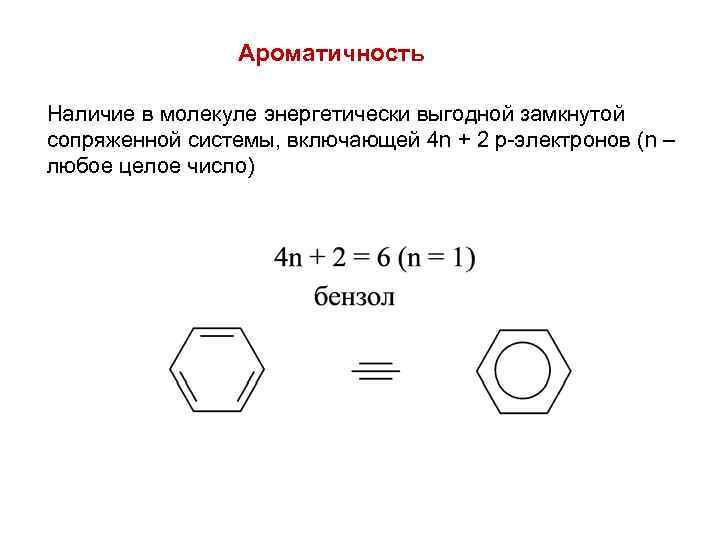 Ароматичность Наличие в молекуле энергетически выгодной замкнутой сопряженной системы, включающей 4 n + 2 р-электронов (n – любое целое число)
Ароматичность Наличие в молекуле энергетически выгодной замкнутой сопряженной системы, включающей 4 n + 2 р-электронов (n – любое целое число)
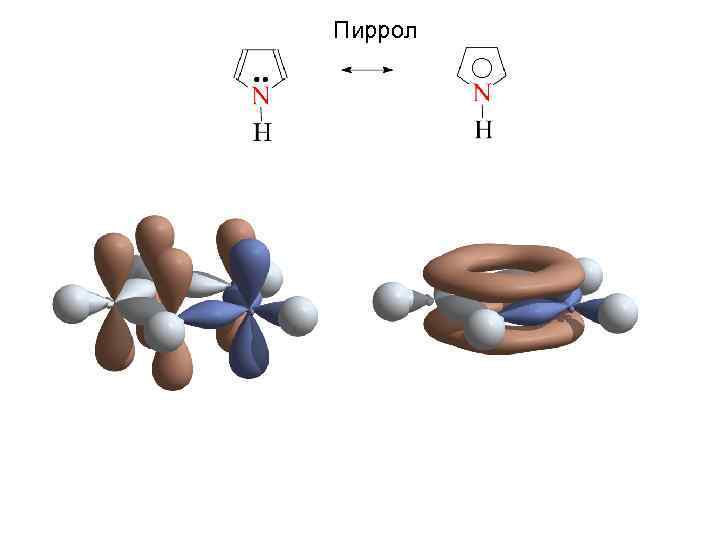 Пиррол
Пиррол
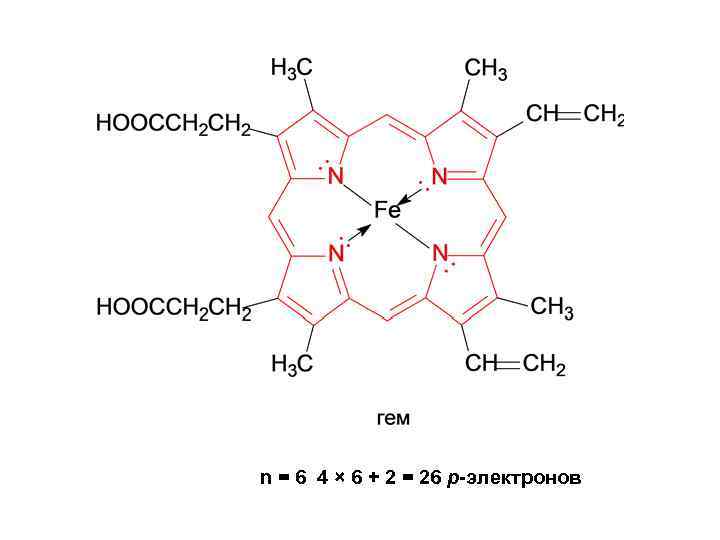 n = 6 4 × 6 + 2 = 26 p-электронов
n = 6 4 × 6 + 2 = 26 p-электронов
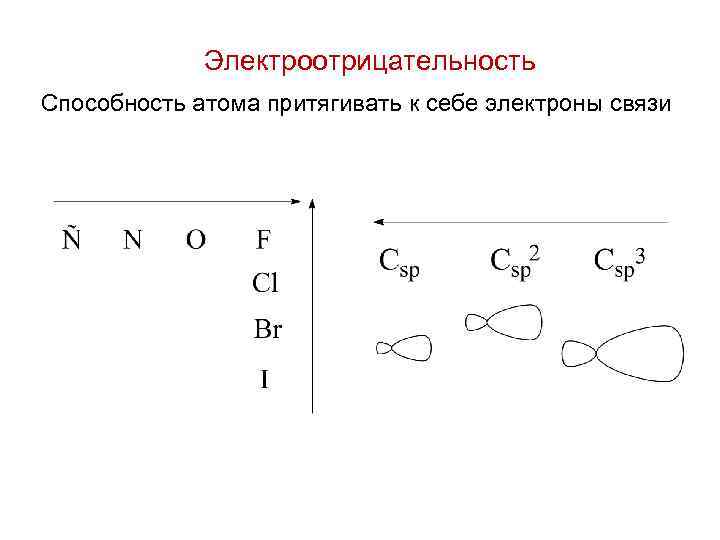 Электроотрицательность Способность атома притягивать к себе электроны связи
Электроотрицательность Способность атома притягивать к себе электроны связи
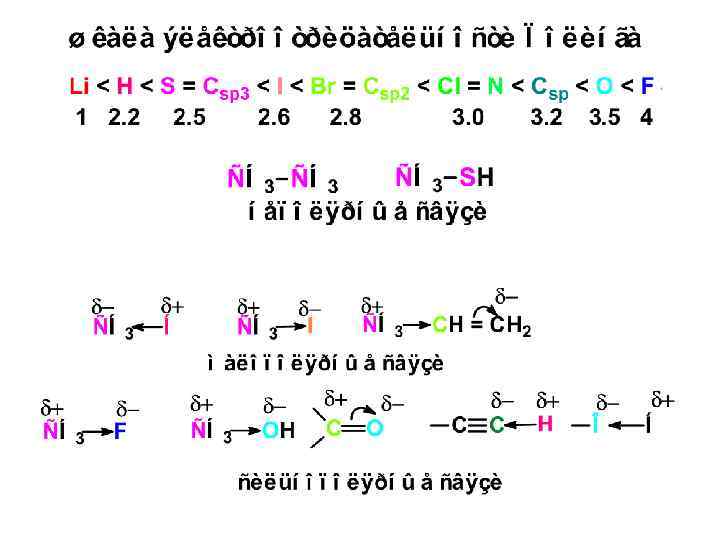

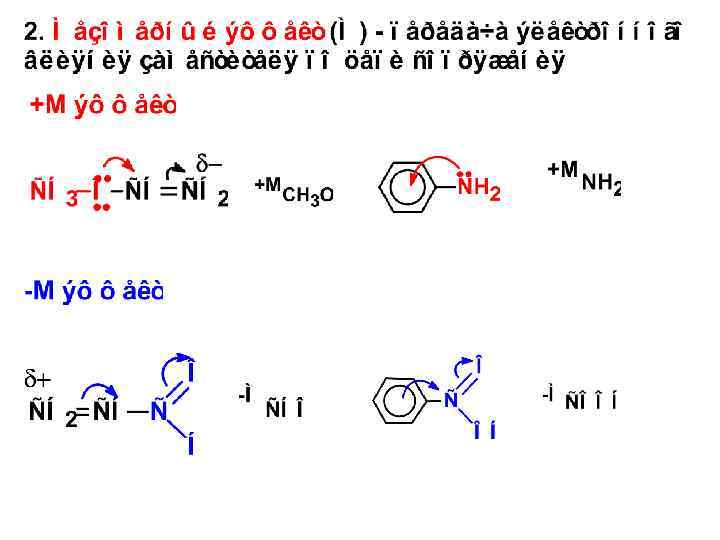
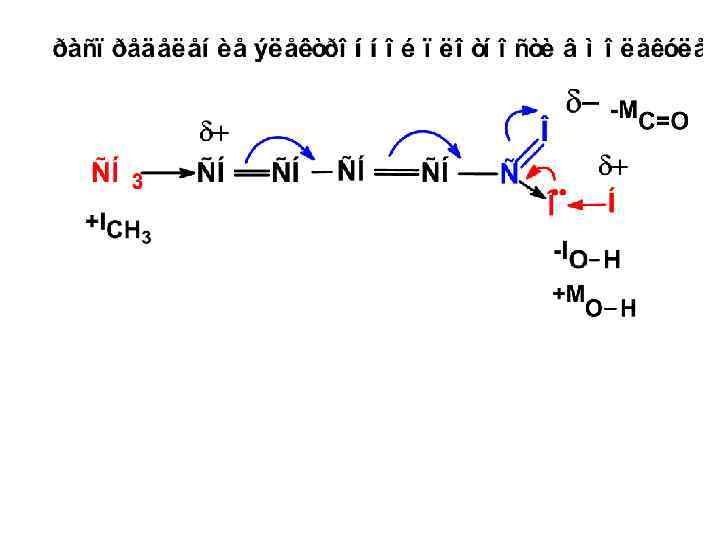
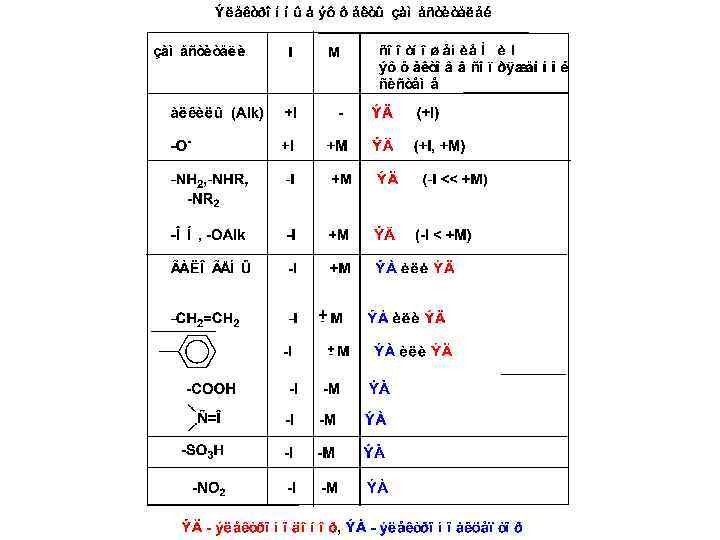
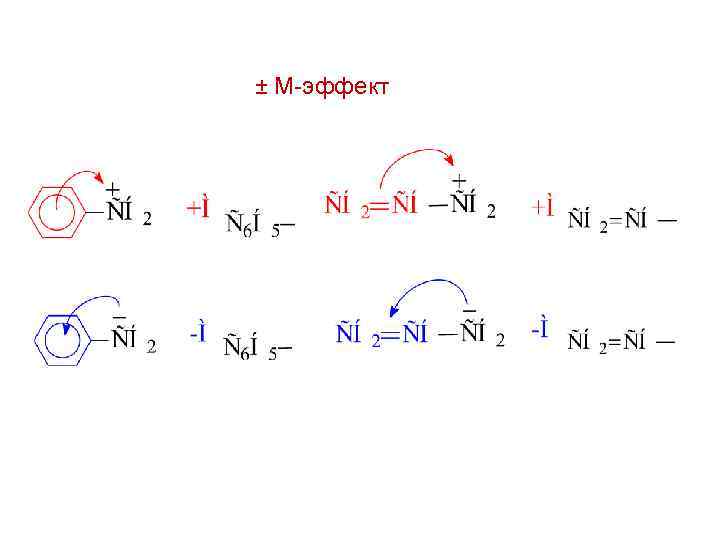 ± М-эффект
± М-эффект
 2. Кислотно-основные свойства органических соединений
2. Кислотно-основные свойства органических соединений
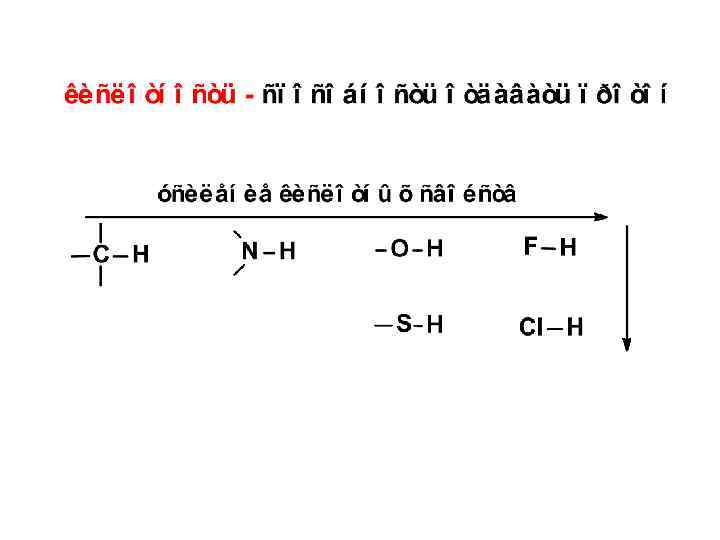
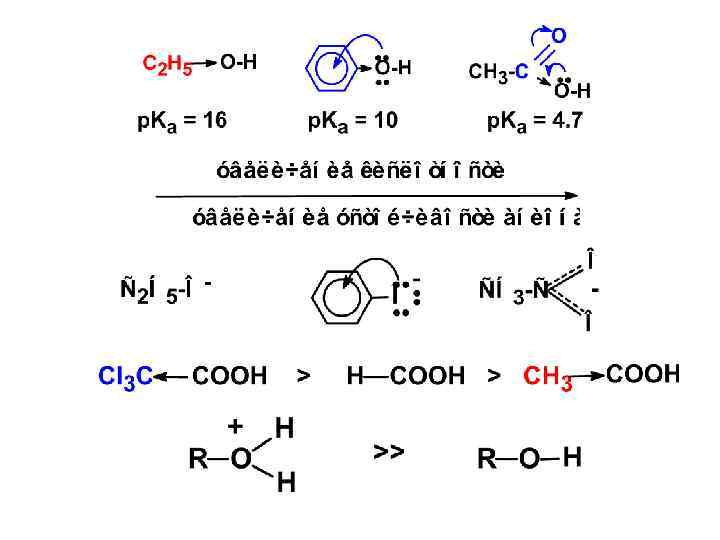
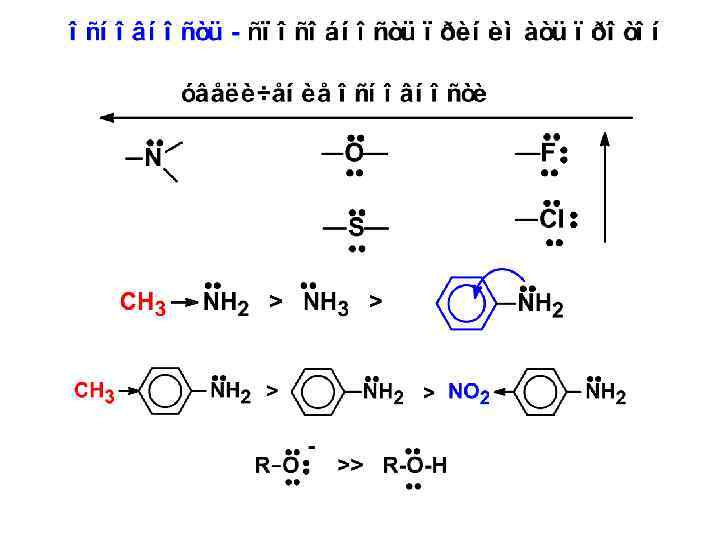
 Типы органических кислот и оснований
Типы органических кислот и оснований
 3. Реакционная способность органических соединений Реакционная способность – способность вещества вступать в ту или иную химическую реакцию и реагировать с большей или меньшей легкостью. Реакционный центр – атом или группа атомов в молекуле, непосредственно участвующие в химической реакции. Субстрат – вещество, подвергающееся изменениям в результате химической реакции. Реагент – его партнер
3. Реакционная способность органических соединений Реакционная способность – способность вещества вступать в ту или иную химическую реакцию и реагировать с большей или меньшей легкостью. Реакционный центр – атом или группа атомов в молекуле, непосредственно участвующие в химической реакции. Субстрат – вещество, подвергающееся изменениям в результате химической реакции. Реагент – его партнер
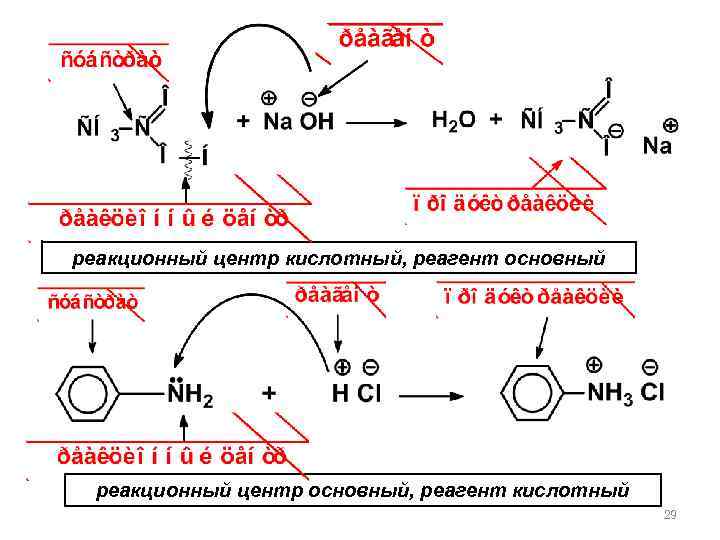 реакционный центр кислотный, реагент основный реакционный центр основный, реагент кислотный 29
реакционный центр кислотный, реагент основный реакционный центр основный, реагент кислотный 29
 Типы реагентов Кислотные реагенты (кислоты) отношению к реакционному партнеру – доноры протона по Основные реагенты (основания) – акцепторы протона по отношению к реакционному партнеру Нуклеофильные реагенты (нуклеофилы) – частицы, образующие новую ковалентную связь за счет своей электронной пары (нуклеофил заряжен отрицательно или имеет неподеленную пару электронов или -связь) Электрофильные реагенты (электрофилы) – частицы, образующие новую ковалентную связь за счет пары электронов партнера (имеют атом, несущий частичный или полный положительный заряд или обладают вакантной орбиталью) Радикальные реагенты (радикалы) – свободные атомы или частицы с неспаренным электроном. Окислители и восстановители – акцепторы или доноры электронов (или атомов водорода) 30
Типы реагентов Кислотные реагенты (кислоты) отношению к реакционному партнеру – доноры протона по Основные реагенты (основания) – акцепторы протона по отношению к реакционному партнеру Нуклеофильные реагенты (нуклеофилы) – частицы, образующие новую ковалентную связь за счет своей электронной пары (нуклеофил заряжен отрицательно или имеет неподеленную пару электронов или -связь) Электрофильные реагенты (электрофилы) – частицы, образующие новую ковалентную связь за счет пары электронов партнера (имеют атом, несущий частичный или полный положительный заряд или обладают вакантной орбиталью) Радикальные реагенты (радикалы) – свободные атомы или частицы с неспаренным электроном. Окислители и восстановители – акцепторы или доноры электронов (или атомов водорода) 30
 Способы разрыва ковалентной связи 1. Гомолитический (свободнорадикальный) образующиеся активные промежуточные частицы – свободные радикалы 2. Гетеролитический (ионный) образующиеся активные органические промежуточные частицы – карбокатионы (положительный заряд на атоме С) или – карбоанионы (отрицательный заряд на атоме углерода). 31
Способы разрыва ковалентной связи 1. Гомолитический (свободнорадикальный) образующиеся активные промежуточные частицы – свободные радикалы 2. Гетеролитический (ионный) образующиеся активные органические промежуточные частицы – карбокатионы (положительный заряд на атоме С) или – карбоанионы (отрицательный заряд на атоме углерода). 31
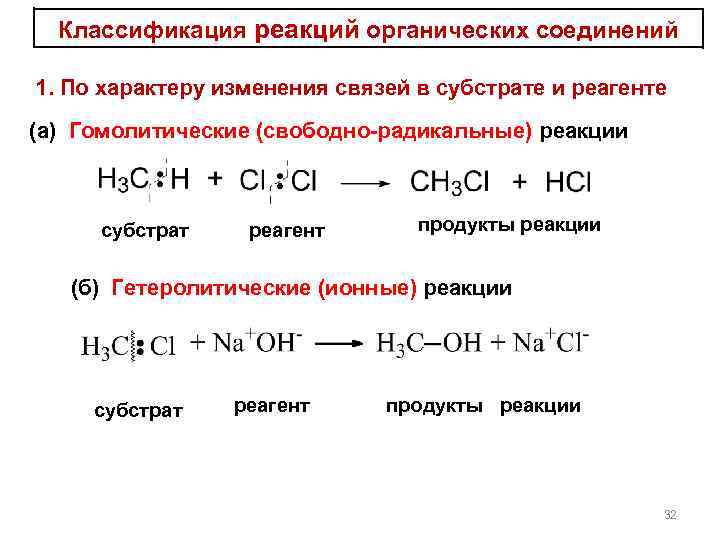 Классификация реакций органических соединений 1. По характеру изменения связей в субстрате и реагенте (а) Гомолитические (свободно-радикальные) реакции субстрат реагент продукты реакции (б) Гетеролитические (ионные) реакции субстрат реагент продукты реакции 32
Классификация реакций органических соединений 1. По характеру изменения связей в субстрате и реагенте (а) Гомолитические (свободно-радикальные) реакции субстрат реагент продукты реакции (б) Гетеролитические (ионные) реакции субстрат реагент продукты реакции 32
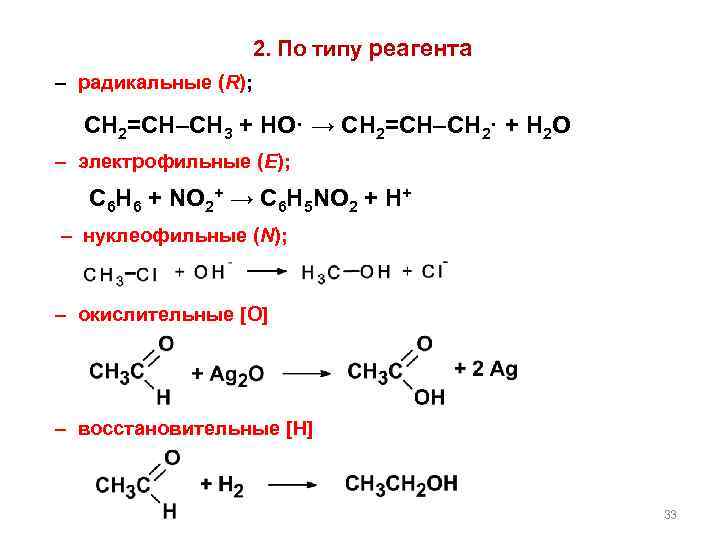 2. По типу реагента – радикальные (R); СН 2=СН–СН 3 + НО· → СН 2=СН–СН 2· + Н 2 О – электрофильные (E); С 6 Н 6 + NO 2+ → C 6 H 5 NO 2 + H+ – нуклеофильные (N); – окислительные [O] – восстановительные [H] 33
2. По типу реагента – радикальные (R); СН 2=СН–СН 3 + НО· → СН 2=СН–СН 2· + Н 2 О – электрофильные (E); С 6 Н 6 + NO 2+ → C 6 H 5 NO 2 + H+ – нуклеофильные (N); – окислительные [O] – восстановительные [H] 33
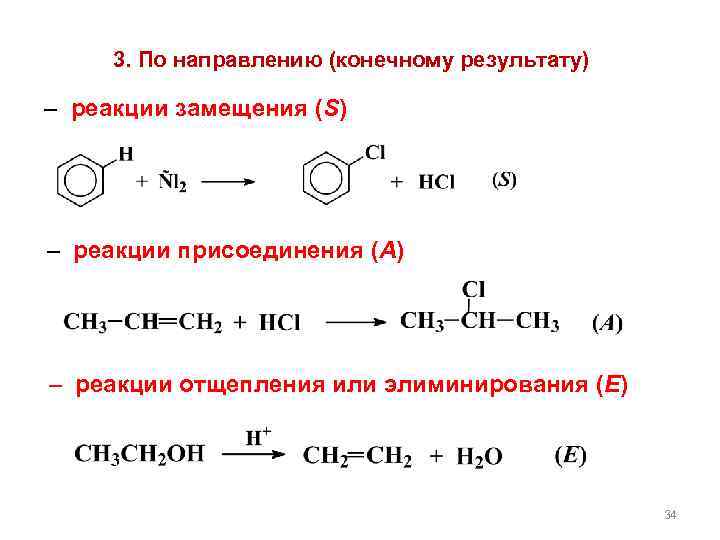 3. По направлению (конечному результату) – реакции замещения (S) – реакции присоединения (A) – реакции отщепления или элиминирования (E) 34
3. По направлению (конечному результату) – реакции замещения (S) – реакции присоединения (A) – реакции отщепления или элиминирования (E) 34
 – реакции перегруппировки (изомеризации) пропанол-1 пропанол-2 – реакции циклизации 4 -гидроксибутановая кислота (ГОМК) -бутиролактон 35
– реакции перегруппировки (изомеризации) пропанол-1 пропанол-2 – реакции циклизации 4 -гидроксибутановая кислота (ГОМК) -бутиролактон 35
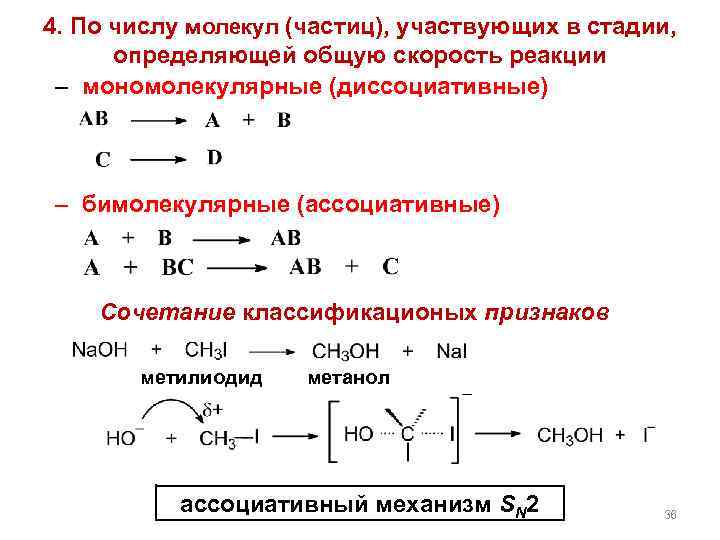 4. По числу молекул (частиц), участвующих в стадии, определяющей общую скорость реакции – мономолекулярные (диссоциативные) – бимолекулярные (ассоциативные) Сочетание классификационых признаков метилиодид метанол ассоциативный механизм SN 2 36
4. По числу молекул (частиц), участвующих в стадии, определяющей общую скорость реакции – мономолекулярные (диссоциативные) – бимолекулярные (ассоциативные) Сочетание классификационых признаков метилиодид метанол ассоциативный механизм SN 2 36
 Понятие о механизме реакции Механизм реакции – детальное описание процесса, в результате которого исходные вещества превращаются в конечные продукты. Включает: (1) элементарные стадии реакции; (2) способ разрыва и образования связей на каждой стадии. (3) стереохимию процесса – пространственное строение исходных продуктов, переходных состояний, промежуточно образующихся частиц и продуктов реакции; (4) кинетические закономерности процесса; (5) термодинамику процесса. 37
Понятие о механизме реакции Механизм реакции – детальное описание процесса, в результате которого исходные вещества превращаются в конечные продукты. Включает: (1) элементарные стадии реакции; (2) способ разрыва и образования связей на каждой стадии. (3) стереохимию процесса – пространственное строение исходных продуктов, переходных состояний, промежуточно образующихся частиц и продуктов реакции; (4) кинетические закономерности процесса; (5) термодинамику процесса. 37
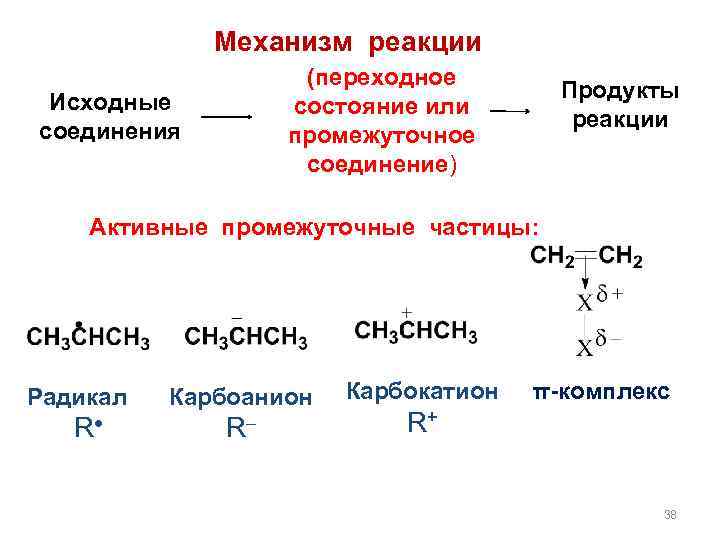 Механизм реакции (переходное состояние или промежуточное соединение) Исходные соединения Продукты реакции Активные промежуточные частицы: Радикал R Карбоанион R Карбокатион π-комплекс R+ 38
Механизм реакции (переходное состояние или промежуточное соединение) Исходные соединения Продукты реакции Активные промежуточные частицы: Радикал R Карбоанион R Карбокатион π-комплекс R+ 38
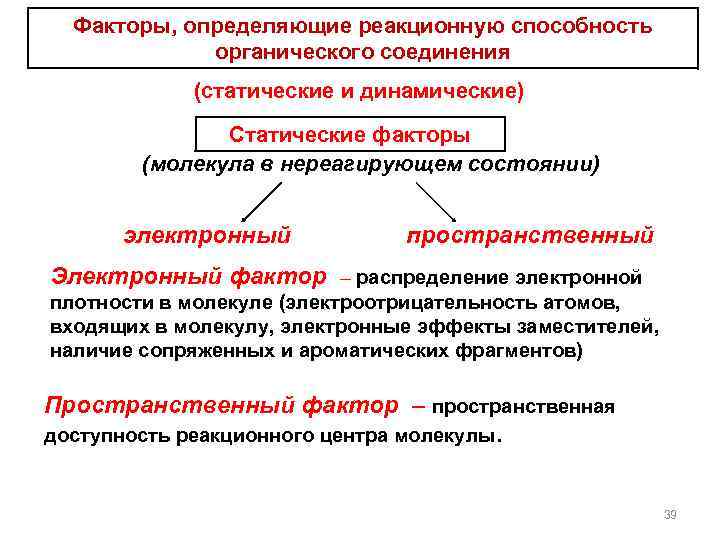 Факторы, определяющие реакционную способность органического соединения (статические и динамические) Статические факторы (молекула в нереагирующем состоянии) электронный пространственный Электронный фактор – распределение электронной плотности в молекуле (электроотрицательность атомов, входящих в молекулу, электронные эффекты заместителей, наличие сопряженных и ароматических фрагментов) Пространственный фактор – пространственная доступность реакционного центра молекулы. 39
Факторы, определяющие реакционную способность органического соединения (статические и динамические) Статические факторы (молекула в нереагирующем состоянии) электронный пространственный Электронный фактор – распределение электронной плотности в молекуле (электроотрицательность атомов, входящих в молекулу, электронные эффекты заместителей, наличие сопряженных и ароматических фрагментов) Пространственный фактор – пространственная доступность реакционного центра молекулы. 39
 Динамические факторы Определяются энергией промежуточных частиц или переходного состояния. Чем больше возможностей для делокализации (рассредоточения) электронной плотности в промежуточной частице (свободном радикале, катионе, анионе, -комплексе), или в переходном состоянии, тем более они устойчивы (стабильны), тем ниже их энергия и тем легче идет реакция. 40
Динамические факторы Определяются энергией промежуточных частиц или переходного состояния. Чем больше возможностей для делокализации (рассредоточения) электронной плотности в промежуточной частице (свободном радикале, катионе, анионе, -комплексе), или в переходном состоянии, тем более они устойчивы (стабильны), тем ниже их энергия и тем легче идет реакция. 40
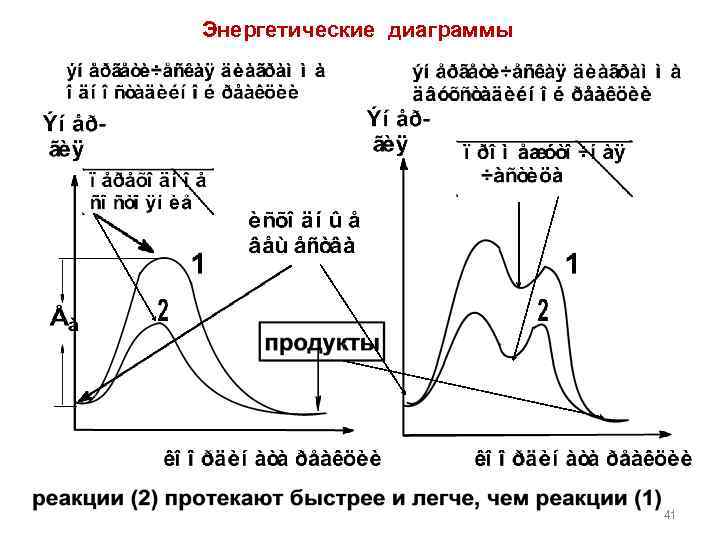 Энергетические диаграммы 41
Энергетические диаграммы 41
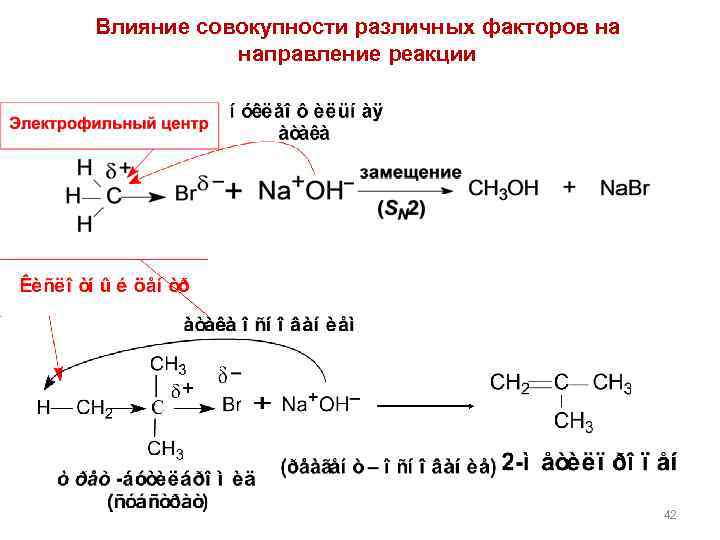 Влияние совокупности различных факторов на направление реакции 42
Влияние совокупности различных факторов на направление реакции 42
 4. Типичные реакции органических соединений
4. Типичные реакции органических соединений
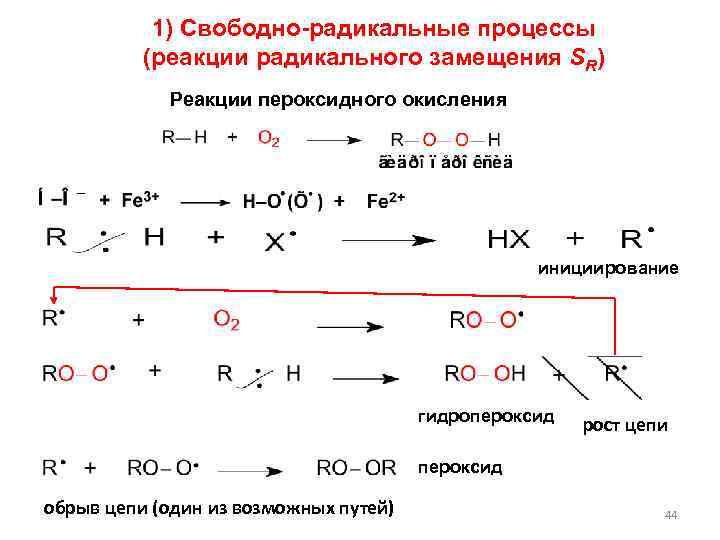 1) Свободно-радикальные процессы (реакции радикального замещения SR) Реакции пероксидного окисления инициирование гидропероксид рост цепи пероксид обрыв цепи (один из возможных путей) 44
1) Свободно-радикальные процессы (реакции радикального замещения SR) Реакции пероксидного окисления инициирование гидропероксид рост цепи пероксид обрыв цепи (один из возможных путей) 44
 Региоселективность реакций радикального замещения q Региоселективность – предпочтительное протекание реакции по одному из нескольких реакционных центров одинаковой химической природы. статистически: 25% 75% Статический фактор: энергия разрыва связи (к. Дж/моль) 45
Региоселективность реакций радикального замещения q Региоселективность – предпочтительное протекание реакции по одному из нескольких реакционных центров одинаковой химической природы. статистически: 25% 75% Статический фактор: энергия разрыва связи (к. Дж/моль) 45
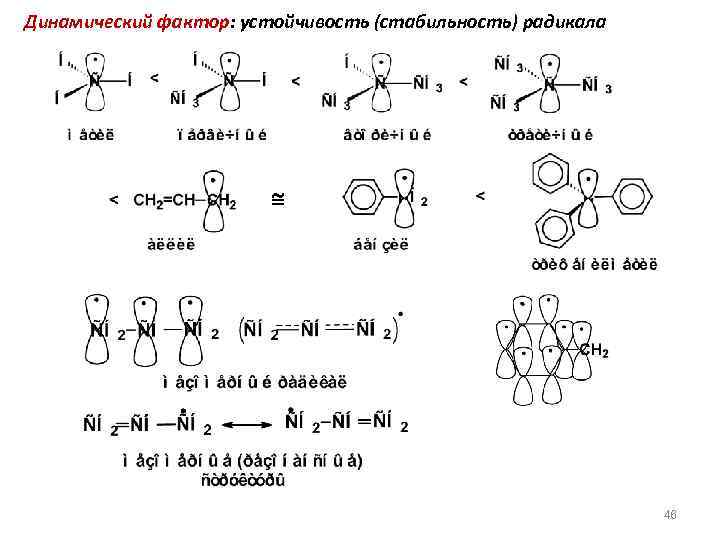 Динамический фактор: устойчивость (стабильность) радикала 46
Динамический фактор: устойчивость (стабильность) радикала 46
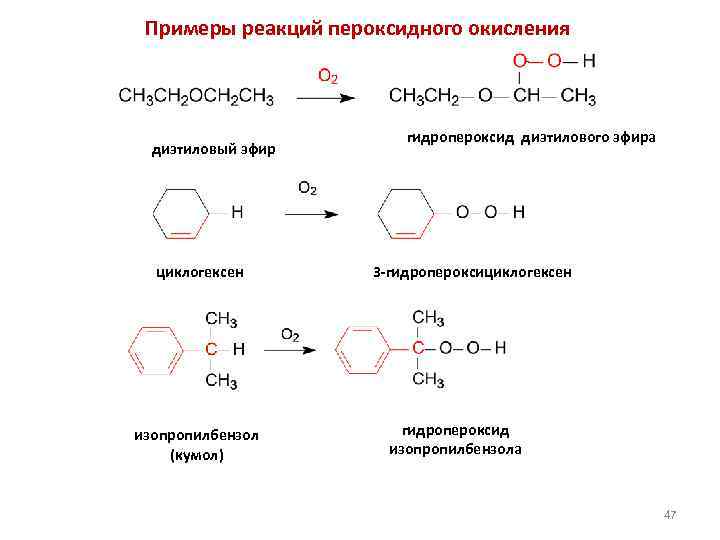 Примеры реакций пероксидного окисления диэтиловый эфир циклогексен изопропилбензол (кумол) гидропероксид диэтилового эфира 3 -гидропероксициклогексен гидропероксид изопропилбензола 47
Примеры реакций пероксидного окисления диэтиловый эфир циклогексен изопропилбензол (кумол) гидропероксид диэтилового эфира 3 -гидропероксициклогексен гидропероксид изопропилбензола 47
 Пероксидное окисление липидов остаток олеиновой кислоты или О 2 Продукты распада 48
Пероксидное окисление липидов остаток олеиновой кислоты или О 2 Продукты распада 48
 Ежедневно каждая клетка нашего организма подвергается нападению 10 000 свободных радикалов. Такое нападение повреждает мембраны клеток и вызывает разрушение их ядер, что, в свою очередь, открывает путь к развитию рака клеток. Повреждения клеточных мембран ускоряет старение организма и подрывает иммунитет. 49
Ежедневно каждая клетка нашего организма подвергается нападению 10 000 свободных радикалов. Такое нападение повреждает мембраны клеток и вызывает разрушение их ядер, что, в свою очередь, открывает путь к развитию рака клеток. Повреждения клеточных мембран ускоряет старение организма и подрывает иммунитет. 49


