Лекция 26 Кислоты с функциями.ppt
- Количество слайдов: 29
 Лекция 26. Галоген-, окси-, оксокислоты n n n 1. Галогенсодержащие кислоты. 2. Оксикислоты 3. Оксокарбоновые кислоты 1
Лекция 26. Галоген-, окси-, оксокислоты n n n 1. Галогенсодержащие кислоты. 2. Оксикислоты 3. Оксокарбоновые кислоты 1
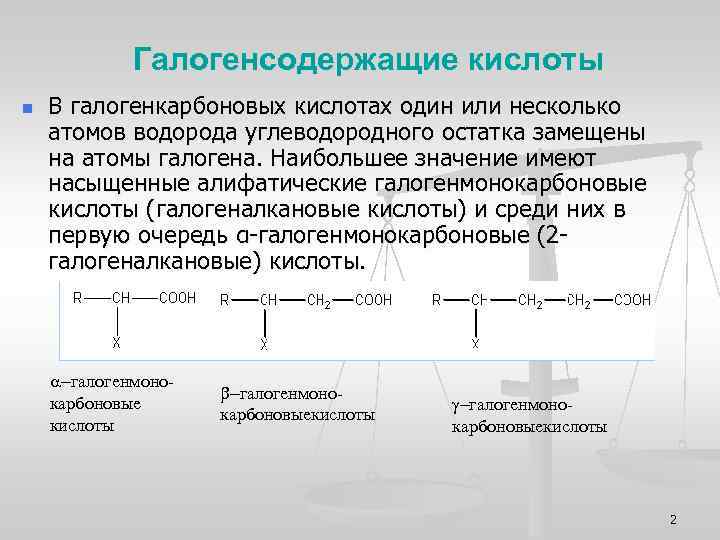 Галогенсодержащие кислоты n В галогенкарбоновых кислотах один или несколько атомов водорода углеводородного остатка замещены на атомы галогена. Наибольшее значение имеют насыщенные алифатические галогенмонокарбоновые кислоты (галогеналкановые кислоты) и среди них в первую очередь α-галогенмонокарбоновые (2 галогеналкановые) кислоты. a-галогенмонокарбоновые кислоты b-галогенмонокарбоновыекислоты g-галогенмонокарбоновыекислоты 2
Галогенсодержащие кислоты n В галогенкарбоновых кислотах один или несколько атомов водорода углеводородного остатка замещены на атомы галогена. Наибольшее значение имеют насыщенные алифатические галогенмонокарбоновые кислоты (галогеналкановые кислоты) и среди них в первую очередь α-галогенмонокарбоновые (2 галогеналкановые) кислоты. a-галогенмонокарбоновые кислоты b-галогенмонокарбоновыекислоты g-галогенмонокарбоновыекислоты 2
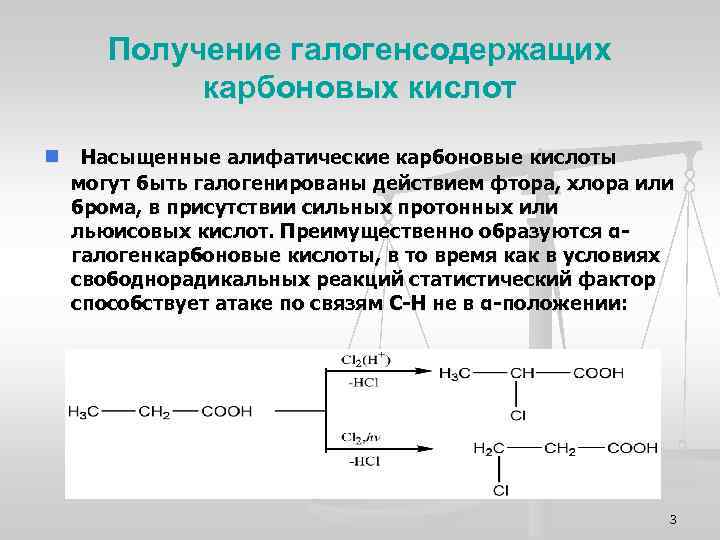 Получение галогенсодержащих карбоновых кислот n Насыщенные алифатические карбоновые кислоты могут быть галогенированы действием фтора, хлора или брома, в присутствии сильных протонных или льюисовых кислот. Преимущественно образуются αгалогенкарбоновые кислоты, в то время как в условиях свободнорадикальных реакций статистический фактор способствует атаке по связям С-Н не в α-положении: 3
Получение галогенсодержащих карбоновых кислот n Насыщенные алифатические карбоновые кислоты могут быть галогенированы действием фтора, хлора или брома, в присутствии сильных протонных или льюисовых кислот. Преимущественно образуются αгалогенкарбоновые кислоты, в то время как в условиях свободнорадикальных реакций статистический фактор способствует атаке по связям С-Н не в α-положении: 3
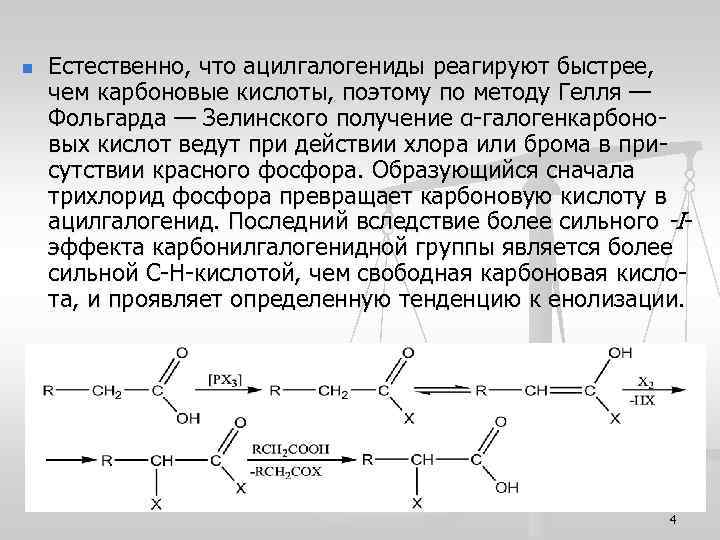 n Естественно, что ацилгалогениды реагируют быстрее, чем карбоновые кислоты, поэтому по методу Гелля — Фольгарда — Зелинского получение α-галогенкарбоновых кислот ведут при действии хлора или брома в присутствии красного фосфора. Образующийся сначала трихлорид фосфора превращает карбоновую кислоту в ацилгалогенид. Последний вследствие более сильного -Iэффекта карбонилгалогенидной группы является более сильной С-Н-кислотой, чем свободная карбоновая кислота, и проявляет определенную тенденцию к енолизации. 4
n Естественно, что ацилгалогениды реагируют быстрее, чем карбоновые кислоты, поэтому по методу Гелля — Фольгарда — Зелинского получение α-галогенкарбоновых кислот ведут при действии хлора или брома в присутствии красного фосфора. Образующийся сначала трихлорид фосфора превращает карбоновую кислоту в ацилгалогенид. Последний вследствие более сильного -Iэффекта карбонилгалогенидной группы является более сильной С-Н-кислотой, чем свободная карбоновая кислота, и проявляет определенную тенденцию к енолизации. 4
 n n n Бензойная кислота может галогенироваться в условиях электрофильного замещения, при этом заместитель вступает в м-положение. При присоединении галогеноводорода к α, βненасыщенных карбоновых кислот получаются βгалогенкарбоновые кислоты. Реакция протекает с ориентацией против правила Марковникова. γ-, δ-, ε- и ω- Галогенкарбоновые кислоты имеют свои специфические методы получения. В лаборатории их можно получить из соответствующих гидроксикислот. 5
n n n Бензойная кислота может галогенироваться в условиях электрофильного замещения, при этом заместитель вступает в м-положение. При присоединении галогеноводорода к α, βненасыщенных карбоновых кислот получаются βгалогенкарбоновые кислоты. Реакция протекает с ориентацией против правила Марковникова. γ-, δ-, ε- и ω- Галогенкарбоновые кислоты имеют свои специфические методы получения. В лаборатории их можно получить из соответствующих гидроксикислот. 5
 Реакции галогенсодержащих карбоновых кислот n n а) Галогенкарбоновые кислоты вследствие -I-эффекта атома галогена являются более сильными кислотами по сравнению с соответствующими незамещенными кислотами. Наиболее сильной карбоновой кислотой является трифторуксусная. Индукционный эффект атомов галогена увеличивается в ряду I, Br, Cl, F и его действие уменьшается с увеличением расстояния от реакционного центра. б) Галогенкарбоновые кислоты образуют все известные функциональные производные, например ацилхлориды, сложные эфиры, амиды: 6
Реакции галогенсодержащих карбоновых кислот n n а) Галогенкарбоновые кислоты вследствие -I-эффекта атома галогена являются более сильными кислотами по сравнению с соответствующими незамещенными кислотами. Наиболее сильной карбоновой кислотой является трифторуксусная. Индукционный эффект атомов галогена увеличивается в ряду I, Br, Cl, F и его действие уменьшается с увеличением расстояния от реакционного центра. б) Галогенкарбоновые кислоты образуют все известные функциональные производные, например ацилхлориды, сложные эфиры, амиды: 6
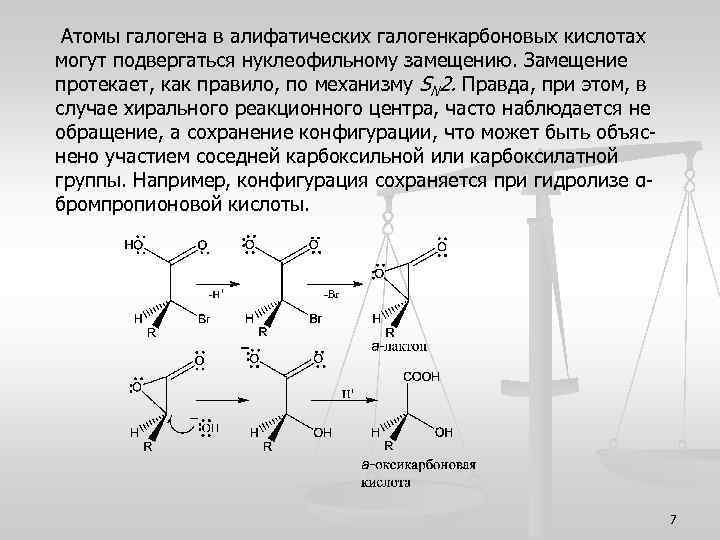 Атомы галогена в алифатических галогенкарбоновых кислотах могут подвергаться нуклеофильному замещению. Замещение протекает, как правило, по механизму SN 2. Правда, при этом, в случае хирального реакционного центра, часто наблюдается не обращение, а сохранение конфигурации, что может быть объяснено участием соседней карбоксильной или карбоксилатной группы. Например, конфигурация сохраняется при гидролизе αбромпропионовой кислоты. 7
Атомы галогена в алифатических галогенкарбоновых кислотах могут подвергаться нуклеофильному замещению. Замещение протекает, как правило, по механизму SN 2. Правда, при этом, в случае хирального реакционного центра, часто наблюдается не обращение, а сохранение конфигурации, что может быть объяснено участием соседней карбоксильной или карбоксилатной группы. Например, конфигурация сохраняется при гидролизе αбромпропионовой кислоты. 7
 Поведение галогенкарбоновых кислот по отношению к растворам щелочей зависит от взаимного положения атома галогена и карбоксильной группы. α- Галогенкарбоновые кислоты реагируют с образованием α- оксикарбоновых кислот. β-Галогенкарбоновые кислоты превращаются в β-оксикарбоновые кислоты, которые при повышенных температурах, естественно с отщеплением воды, переходят в α, β-ненасыщенные карбоновые кислоты. γ- и δ-Галогенкарбоновые кислоты при действии щелочей за счет эффекта участия соседней группы дают γ- или соответственно δ-лактоны, а ε-галогенкарбоновые кислоты превращаются в ε-оксикарбоновые кислоты. Как побочная реакция при этом часто наблюдается распад соли βгалогенкарбоновой кислоты 8
Поведение галогенкарбоновых кислот по отношению к растворам щелочей зависит от взаимного положения атома галогена и карбоксильной группы. α- Галогенкарбоновые кислоты реагируют с образованием α- оксикарбоновых кислот. β-Галогенкарбоновые кислоты превращаются в β-оксикарбоновые кислоты, которые при повышенных температурах, естественно с отщеплением воды, переходят в α, β-ненасыщенные карбоновые кислоты. γ- и δ-Галогенкарбоновые кислоты при действии щелочей за счет эффекта участия соседней группы дают γ- или соответственно δ-лактоны, а ε-галогенкарбоновые кислоты превращаются в ε-оксикарбоновые кислоты. Как побочная реакция при этом часто наблюдается распад соли βгалогенкарбоновой кислоты 8
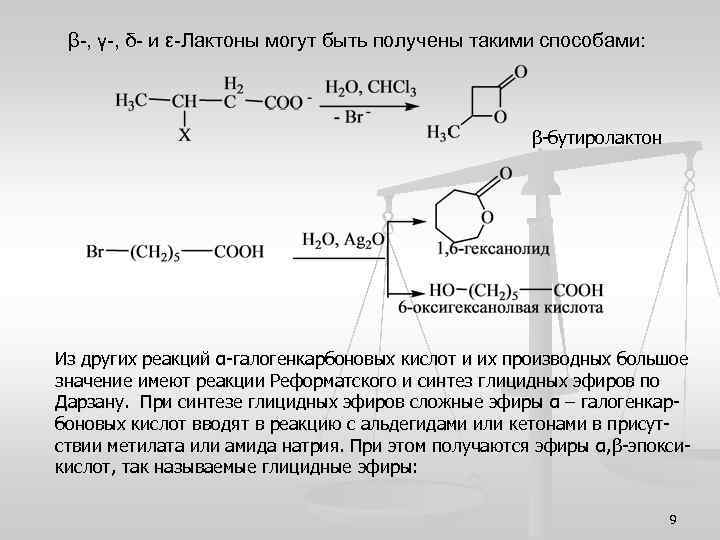 β-, γ-, δ- и ε-Лактоны могут быть получены такими способами: β-бутиролактон Из других реакций α-галогенкарбоновых кислот и их производных большое значение имеют реакции Реформатского и синтез глицидных эфиров по Дарзану. При синтезе глицидных эфиров сложные эфиры α – галогенкарбоновых кислот вводят в реакцию с альдегидами или кетонами в присутствии метилата или амида натрия. При этом получаются эфиры α, β-эпоксикислот, так называемые глицидные эфиры: 9
β-, γ-, δ- и ε-Лактоны могут быть получены такими способами: β-бутиролактон Из других реакций α-галогенкарбоновых кислот и их производных большое значение имеют реакции Реформатского и синтез глицидных эфиров по Дарзану. При синтезе глицидных эфиров сложные эфиры α – галогенкарбоновых кислот вводят в реакцию с альдегидами или кетонами в присутствии метилата или амида натрия. При этом получаются эфиры α, β-эпоксикислот, так называемые глицидные эфиры: 9
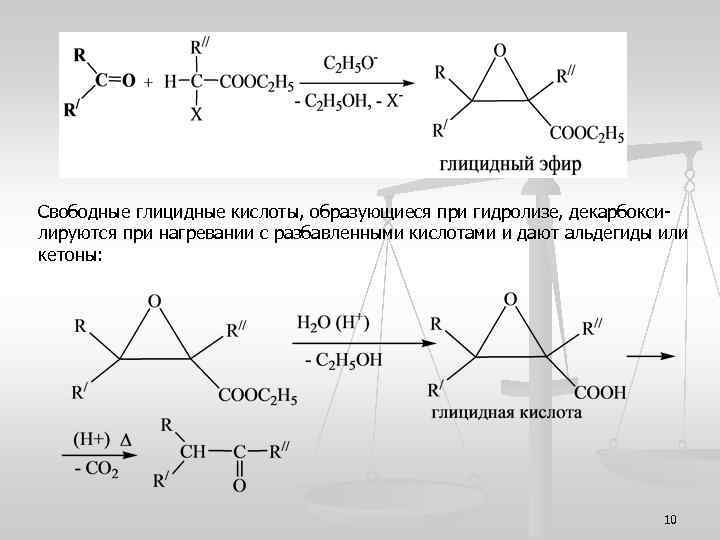 Свободные глицидные кислоты, образующиеся при гидролизе, декарбоксилируются при нагревании с разбавленными кислотами и дают альдегиды или кетоны: 10
Свободные глицидные кислоты, образующиеся при гидролизе, декарбоксилируются при нагревании с разбавленными кислотами и дают альдегиды или кетоны: 10
 Оксикислоты и методы их получения n n α-Гидроксикислоты легко получают щелочным гидролизом αгалогенкарбоновых кислот. При каталитическом гидрировании сложных эфиров оксокарбоновых кислот образуются эфиры оксикарбоновых кислот, которые при гидролизе превращаются в свободные оксикислоты: 11
Оксикислоты и методы их получения n n α-Гидроксикислоты легко получают щелочным гидролизом αгалогенкарбоновых кислот. При каталитическом гидрировании сложных эфиров оксокарбоновых кислот образуются эфиры оксикарбоновых кислот, которые при гидролизе превращаются в свободные оксикислоты: 11
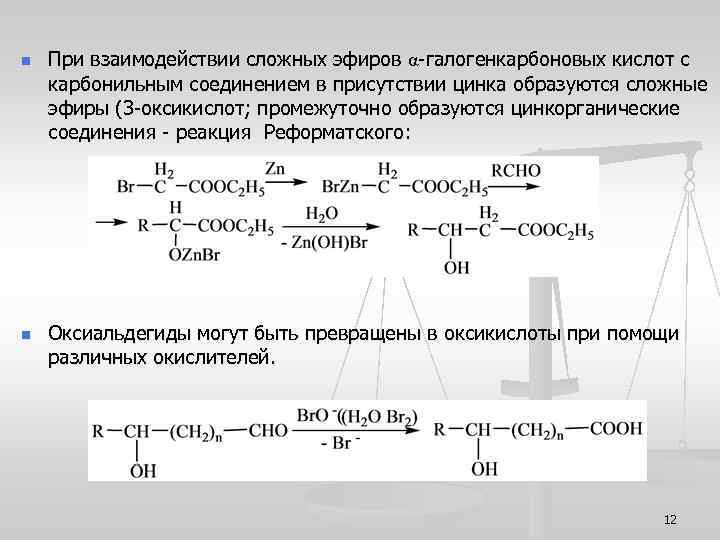 n n При взаимодействии сложных эфиров α-галогенкарбоновых кислот с карбонильным соединением в присутствии цинка образуются сложные эфиры (3 -оксикислот; промежуточно образуются цинкорганические соединения - реакция Реформатского: Оксиальдегиды могут быть превращены в оксикислоты при помощи различных окислителей. 12
n n При взаимодействии сложных эфиров α-галогенкарбоновых кислот с карбонильным соединением в присутствии цинка образуются сложные эфиры (3 -оксикислот; промежуточно образуются цинкорганические соединения - реакция Реформатского: Оксиальдегиды могут быть превращены в оксикислоты при помощи различных окислителей. 12
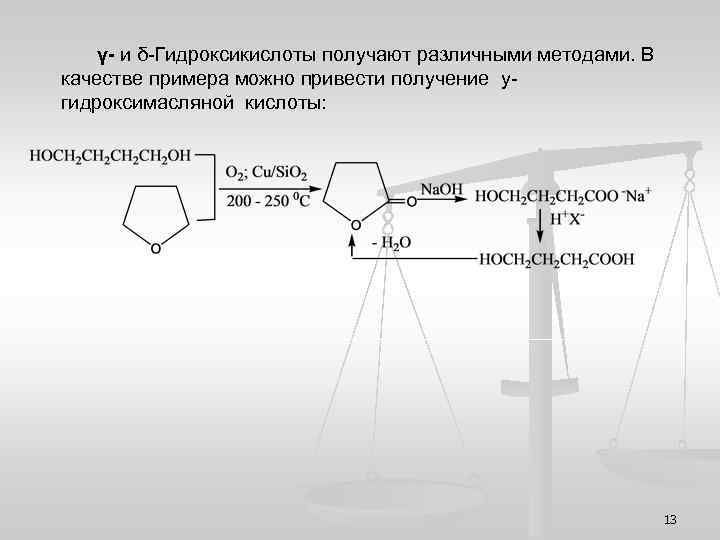 γ- и δ-Гидроксикислоты получают различными методами. В качестве примера можно привести получение угидроксимасляной кислоты: 13
γ- и δ-Гидроксикислоты получают различными методами. В качестве примера можно привести получение угидроксимасляной кислоты: 13
 Реакции карбоксильной группы n Для гидроксикислот характерны обычные реакции карбоновых кислот: ионизация карбоксильной группы, образование солей, сложных эфиров, амидов, ацилхлоридов. Отчасти, осуществлению этих реакций мешает присутствие гидроксилыюй группы, которая тоже может вступать в реакции. Поэтому ее обычно «защищают» , превращая в простую или сложноэфирную группировку: 14
Реакции карбоксильной группы n Для гидроксикислот характерны обычные реакции карбоновых кислот: ионизация карбоксильной группы, образование солей, сложных эфиров, амидов, ацилхлоридов. Отчасти, осуществлению этих реакций мешает присутствие гидроксилыюй группы, которая тоже может вступать в реакции. Поэтому ее обычно «защищают» , превращая в простую или сложноэфирную группировку: 14
 Реакции гидроксильной группы n n Гидроксикислотам свойственны обычные реакции спиртов, например, они образуют простые и сложные эфиры, окисляются и др. Проведению отдельных реакций мешает карбоксильная группа, поэтому ее защищают превращением в сложноэфирную группировку. На примере реакции (S)-(—)-яблочной кислоты с пентахлоридом фосфора Вальден в 1896 г. открыл явление обращения конфигурации при SN 2 -реакциях, получившее его имя (Вальденовское обращение, ): 15
Реакции гидроксильной группы n n Гидроксикислотам свойственны обычные реакции спиртов, например, они образуют простые и сложные эфиры, окисляются и др. Проведению отдельных реакций мешает карбоксильная группа, поэтому ее защищают превращением в сложноэфирную группировку. На примере реакции (S)-(—)-яблочной кислоты с пентахлоридом фосфора Вальден в 1896 г. открыл явление обращения конфигурации при SN 2 -реакциях, получившее его имя (Вальденовское обращение, ): 15
 Реакции, в которых карбоксильная и гидроксильная группы участвуют совместно (отношение к нагреванию) n n При повышенных температурах оксикислоты дегидратируются различным способом. Характерной реакцией α-оксикислот является отщепление муравьиной кислоты, которое происходит при нагревании с разбавленными серной или соляной кислотами. 16
Реакции, в которых карбоксильная и гидроксильная группы участвуют совместно (отношение к нагреванию) n n При повышенных температурах оксикислоты дегидратируются различным способом. Характерной реакцией α-оксикислот является отщепление муравьиной кислоты, которое происходит при нагревании с разбавленными серной или соляной кислотами. 16
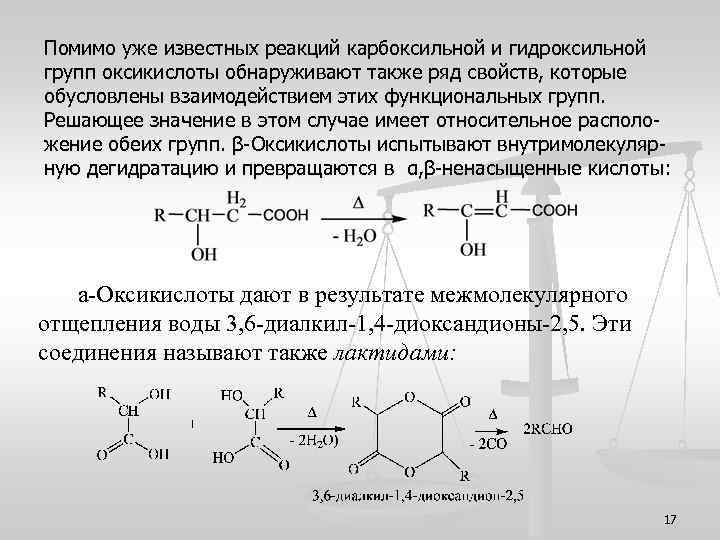 Помимо уже известных реакций карбоксильной и гидроксильной групп оксикислоты обнаруживают также ряд свойств, которые обусловлены взаимодействием этих функциональных групп. Решающее значение в этом случае имеет относительное расположение обеих групп. β-Оксикислоты испытывают внутримолекулярную дегидратацию и превращаются в α, β-ненасыщенные кислоты: а-Оксикислоты дают в результате межмолекулярного отщепления воды 3, 6 -диалкил-1, 4 -диоксандионы-2, 5. Эти соединения называют также лактидами: 17
Помимо уже известных реакций карбоксильной и гидроксильной групп оксикислоты обнаруживают также ряд свойств, которые обусловлены взаимодействием этих функциональных групп. Решающее значение в этом случае имеет относительное расположение обеих групп. β-Оксикислоты испытывают внутримолекулярную дегидратацию и превращаются в α, β-ненасыщенные кислоты: а-Оксикислоты дают в результате межмолекулярного отщепления воды 3, 6 -диалкил-1, 4 -диоксандионы-2, 5. Эти соединения называют также лактидами: 17
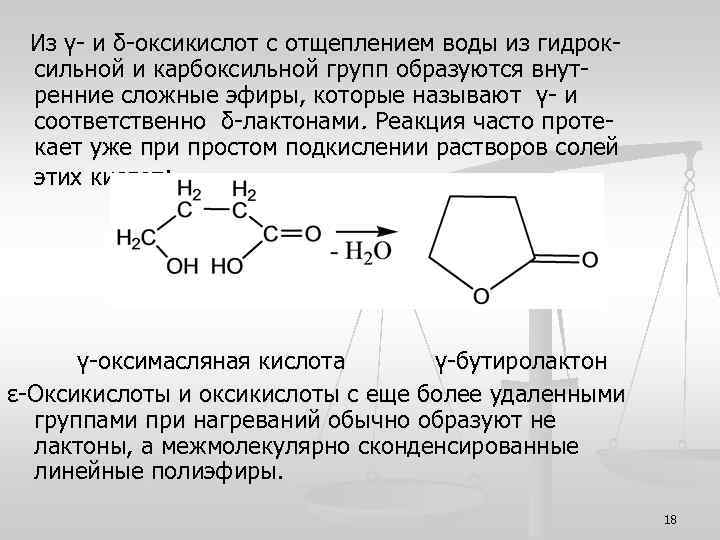 Из γ- и δ-оксикислот с отщеплением воды из гидроксильной и карбоксильной групп образуются внутренние сложные эфиры, которые называют γ- и соответственно δ-лактонами. Реакция часто протекает уже при простом подкислении растворов солей этих кислот: γ-оксимасляная кислота γ-бутиролактон ε-Оксикислоты и оксикислоты с еще более удаленными группами при нагреваний обычно образуют не лактоны, а межмолекулярно сконденсированные линейные полиэфиры. 18
Из γ- и δ-оксикислот с отщеплением воды из гидроксильной и карбоксильной групп образуются внутренние сложные эфиры, которые называют γ- и соответственно δ-лактонами. Реакция часто протекает уже при простом подкислении растворов солей этих кислот: γ-оксимасляная кислота γ-бутиролактон ε-Оксикислоты и оксикислоты с еще более удаленными группами при нагреваний обычно образуют не лактоны, а межмолекулярно сконденсированные линейные полиэфиры. 18
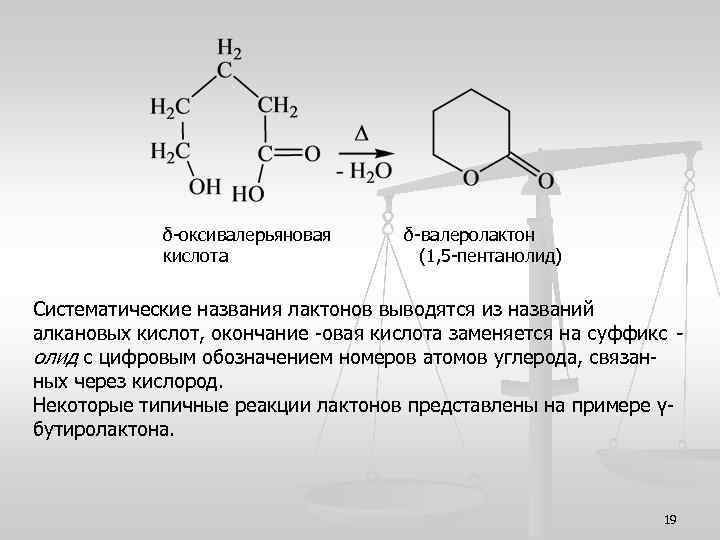 δ-оксивалерьяновая кислота δ-валеролактон (1, 5 -пентанолид) Систематические названия лактонов выводятся из названий алкановых кислот, окончание -овая кислота заменяется на суффикс олид с цифровым обозначением номеров атомов углерода, связанных через кислород. Некоторые типичные реакции лактонов представлены на примере γбутиролактона. 19
δ-оксивалерьяновая кислота δ-валеролактон (1, 5 -пентанолид) Систематические названия лактонов выводятся из названий алкановых кислот, окончание -овая кислота заменяется на суффикс олид с цифровым обозначением номеров атомов углерода, связанных через кислород. Некоторые типичные реакции лактонов представлены на примере γбутиролактона. 19
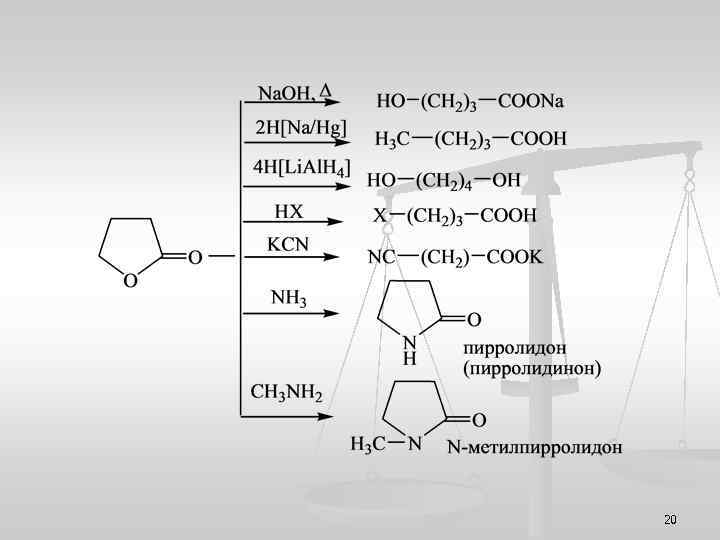 20
20
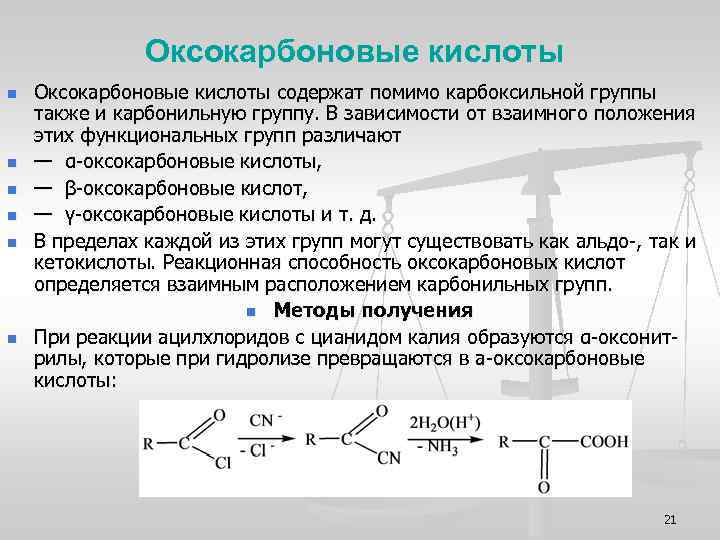 Оксокарбоновые кислоты n n n Оксокарбоновые кислоты содержат помимо карбоксильной группы также и карбонильную группу. В зависимости от взаимного положения этих функциональных групп различают — α-оксокарбоновые кислоты, — β-оксокарбоновые кислот, — γ-оксокарбоновые кислоты и т. д. В пределах каждой из этих групп могут существовать как альдо-, так и кетокислоты. Реакционная способность оксокарбоновых кислот определяется взаимным расположением карбонильных групп. n Методы получения При реакции ацилхлоридов с цианидом калия образуются α-оксонитрилы, которые при гидролизе превращаются в а-оксокарбоновые кислоты: 21
Оксокарбоновые кислоты n n n Оксокарбоновые кислоты содержат помимо карбоксильной группы также и карбонильную группу. В зависимости от взаимного положения этих функциональных групп различают — α-оксокарбоновые кислоты, — β-оксокарбоновые кислот, — γ-оксокарбоновые кислоты и т. д. В пределах каждой из этих групп могут существовать как альдо-, так и кетокислоты. Реакционная способность оксокарбоновых кислот определяется взаимным расположением карбонильных групп. n Методы получения При реакции ацилхлоридов с цианидом калия образуются α-оксонитрилы, которые при гидролизе превращаются в а-оксокарбоновые кислоты: 21
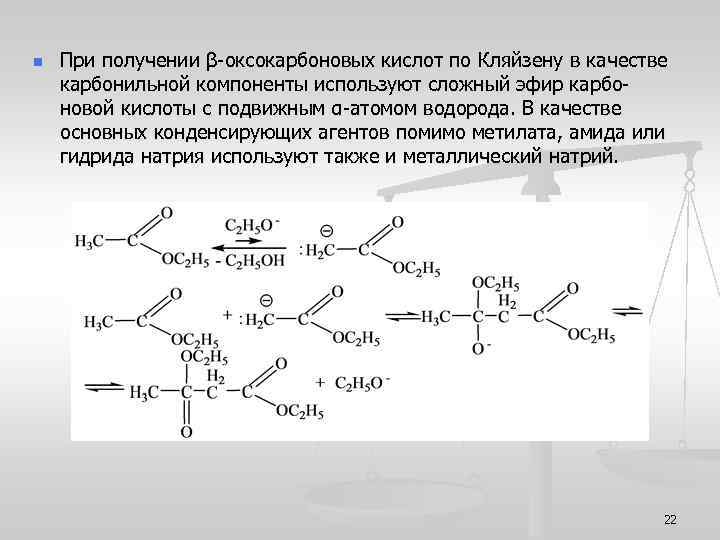 n При получении β-оксокарбоновых кислот по Кляйзену в качестве карбонильной компоненты используют сложный эфир карбоновой кислоты с подвижным α-атомом водорода. В качестве основных конденсирующих агентов помимо метилата, амида или гидрида натрия используют также и металлический натрий. 22
n При получении β-оксокарбоновых кислот по Кляйзену в качестве карбонильной компоненты используют сложный эфир карбоновой кислоты с подвижным α-атомом водорода. В качестве основных конденсирующих агентов помимо метилата, амида или гидрида натрия используют также и металлический натрий. 22
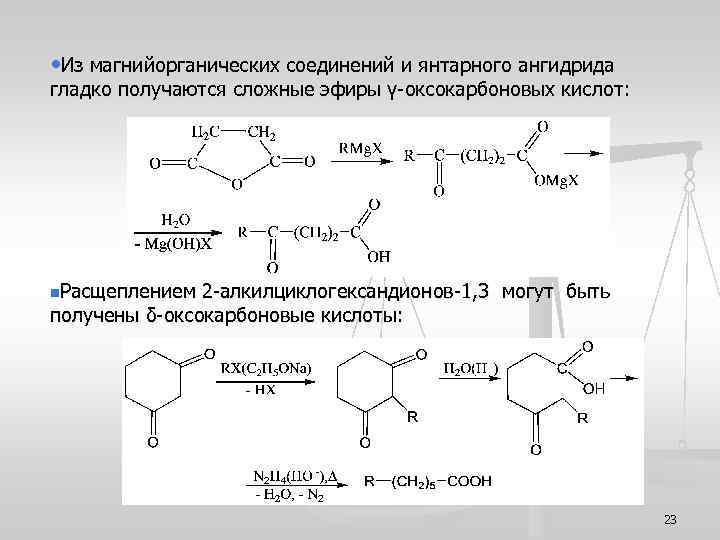 • Из магнийорганических соединений и янтарного ангидрида гладко получаются сложные эфиры γ-оксокарбоновых кислот: n. Расщеплением 2 -алкилциклогександионов-1, 3 могут быть получены δ-оксокарбоновые кислоты: 23
• Из магнийорганических соединений и янтарного ангидрида гладко получаются сложные эфиры γ-оксокарбоновых кислот: n. Расщеплением 2 -алкилциклогександионов-1, 3 могут быть получены δ-оксокарбоновые кислоты: 23
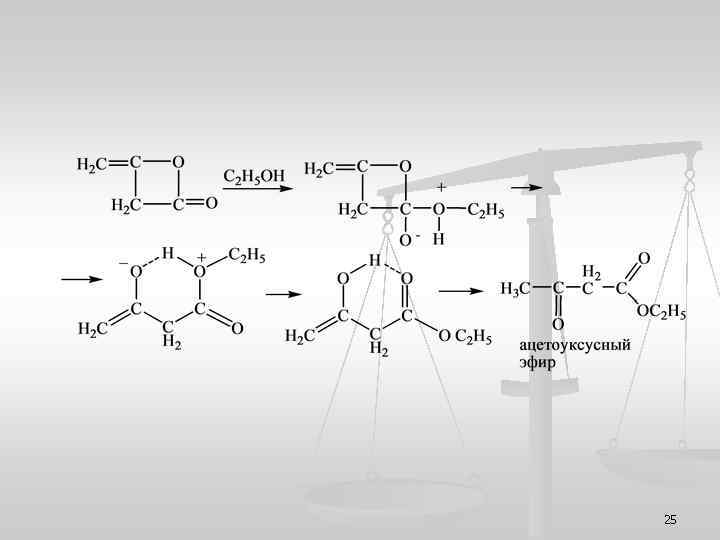
 n n Свойства α-оксокарбоновыхе кислот Типичными реакциями α-кетокарбоновых кислот являются их декарбоксилирование под действием теплой разбавленной серной кислоты и декарбонилирование при нагревании с концентрированной серной кислотой n Свойства β-оксокарбоновыхе кислот их эфиров Ацетоуксусный эфир, устойчив и имеет большое значение. Его получают кляйзеновской конденсацией этилацетата или присо-единением этанола к дикетену 24
n n Свойства α-оксокарбоновыхе кислот Типичными реакциями α-кетокарбоновых кислот являются их декарбоксилирование под действием теплой разбавленной серной кислоты и декарбонилирование при нагревании с концентрированной серной кислотой n Свойства β-оксокарбоновыхе кислот их эфиров Ацетоуксусный эфир, устойчив и имеет большое значение. Его получают кляйзеновской конденсацией этилацетата или присо-единением этанола к дикетену 24
 25
25
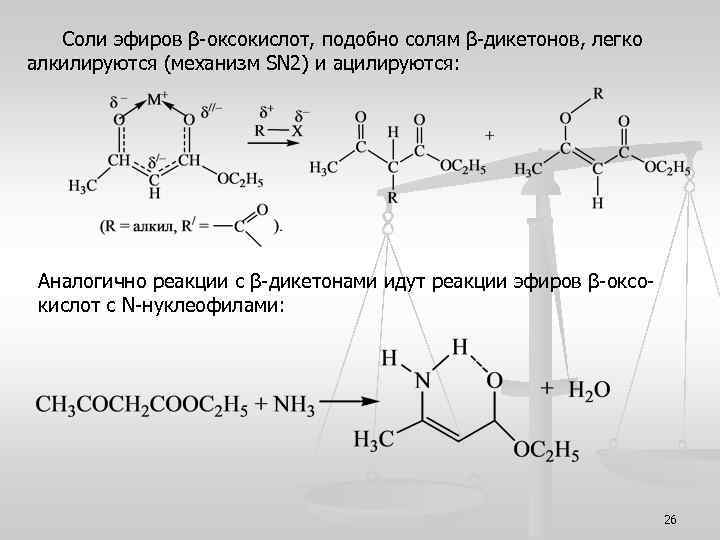 Соли эфиров β-оксокислот, подобно солям β-дикетонов, легко алкилируются (механизм SN 2) и ацилируются: Аналогично реакции с β-дикетонами идут реакции эфиров β-оксокислот с N-нуклеофилами: 26
Соли эфиров β-оксокислот, подобно солям β-дикетонов, легко алкилируются (механизм SN 2) и ацилируются: Аналогично реакции с β-дикетонами идут реакции эфиров β-оксокислот с N-нуклеофилами: 26
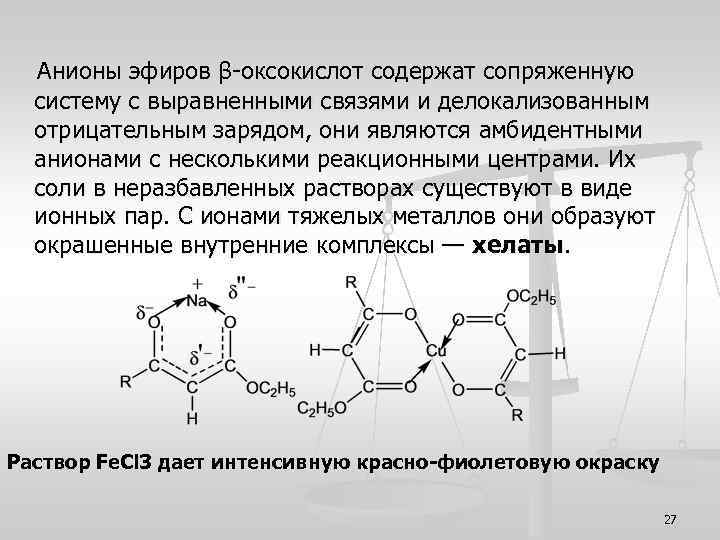 Анионы эфиров β-оксокислот содержат сопряженную систему с выравненными связями и делокализованным отрицательным зарядом, они являются амбидентными анионами с несколькими реакционными центрами. Их соли в неразбавленных растворах существуют в виде ионных пар. С ионами тяжелых металлов они образуют окрашенные внутренние комплексы — хелаты. Раствор Fe. Cl 3 дает интенсивную красно-фиолетовую окраску 27
Анионы эфиров β-оксокислот содержат сопряженную систему с выравненными связями и делокализованным отрицательным зарядом, они являются амбидентными анионами с несколькими реакционными центрами. Их соли в неразбавленных растворах существуют в виде ионных пар. С ионами тяжелых металлов они образуют окрашенные внутренние комплексы — хелаты. Раствор Fe. Cl 3 дает интенсивную красно-фиолетовую окраску 27
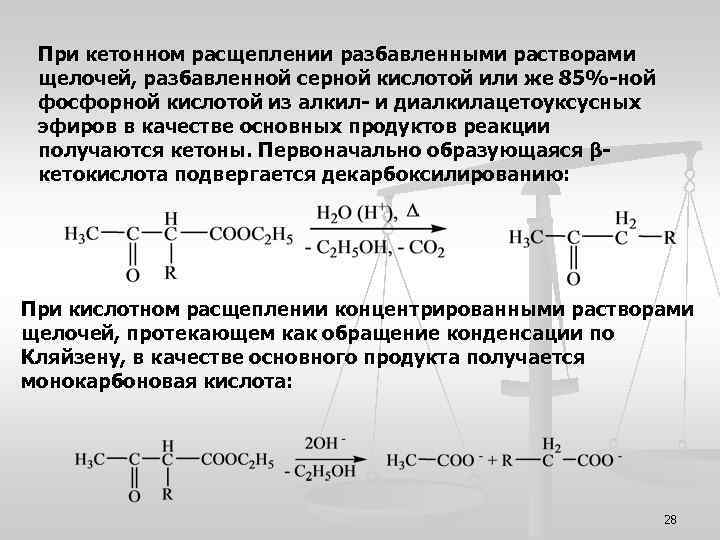 При кетонном расщеплении разбавленными растворами щелочей, разбавленной серной кислотой или же 85%-ной фосфорной кислотой из алкил- и диалкилацетоуксусных эфиров в качестве основных продуктов реакции получаются кетоны. Первоначально образующаяся βкетокислота подвергается декарбоксилированию: При кислотном расщеплении концентрированными растворами щелочей, протекающем как обращение конденсации по Кляйзену, в качестве основного продукта получается монокарбоновая кислота: 28
При кетонном расщеплении разбавленными растворами щелочей, разбавленной серной кислотой или же 85%-ной фосфорной кислотой из алкил- и диалкилацетоуксусных эфиров в качестве основных продуктов реакции получаются кетоны. Первоначально образующаяся βкетокислота подвергается декарбоксилированию: При кислотном расщеплении концентрированными растворами щелочей, протекающем как обращение конденсации по Кляйзену, в качестве основного продукта получается монокарбоновая кислота: 28
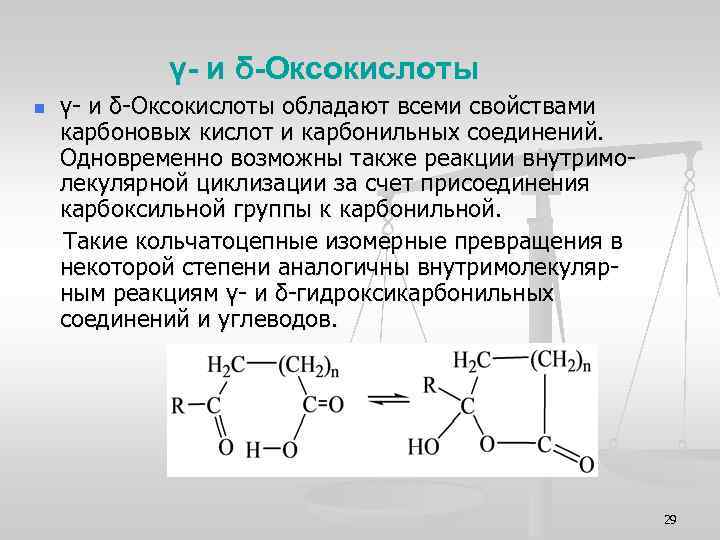 γ- и δ-Оксокислоты n γ- и δ-Оксокислоты обладают всеми свойствами карбоновых кислот и карбонильных соединений. Одновременно возможны также реакции внутримолекулярной циклизации за счет присоединения карбоксильной группы к карбонильной. Такие кольчатоцепные изомерные превращения в некоторой степени аналогичны внутримолекулярным реакциям γ- и δ-гидроксикарбонильных соединений и углеводов. 29
γ- и δ-Оксокислоты n γ- и δ-Оксокислоты обладают всеми свойствами карбоновых кислот и карбонильных соединений. Одновременно возможны также реакции внутримолекулярной циклизации за счет присоединения карбоксильной группы к карбонильной. Такие кольчатоцепные изомерные превращения в некоторой степени аналогичны внутримолекулярным реакциям γ- и δ-гидроксикарбонильных соединений и углеводов. 29


