ЛЕКЦИЯ 21.ppt
- Количество слайдов: 21

ЛЕКЦИЯ 21 Декарбоксилирование аминокислот Аммиак и пути его обезвреживания

ПЛАН • Декарбоксилирование орнитина, лизина, серина, цистеиновой кислоты, тирозина. Значение. • Окислительное дезаминирование глутамата. Значение. • Восстановительное аминирование. Значение. • Источники аммиака в организме. Токсичность аммиака. • Пути обезвреживания аммиака в клетке: аминирование глутамата и аспартата, восстановительное аминирование. • Глюкозо-аланиновый цикл.
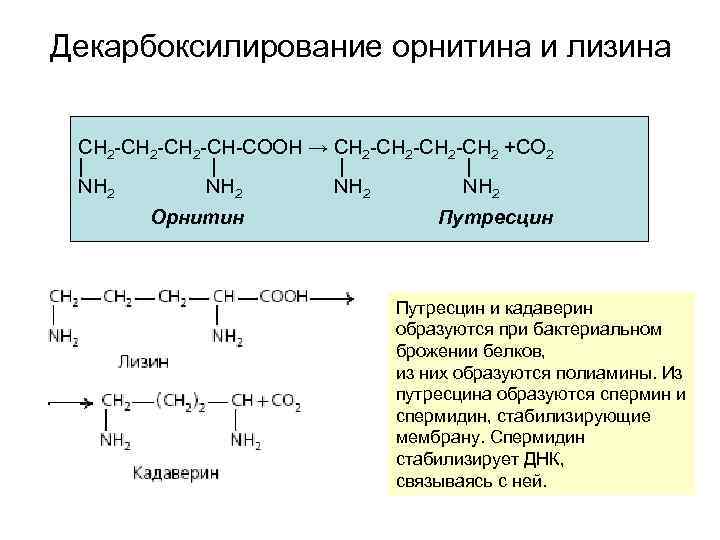
Декарбоксилирование орнитина и лизина СН 2 -СН-СООН → СН 2 -СН 2 +CO 2 | | NH 2 Орнитин Путресцин и кадаверин образуются при бактериальном брожении белков, из них образуются полиамины. Из путресцина образуются спермин и спермидин, стабилизирующие мембрану. Спермидин стабилизирует ДНК, связываясь с ней.
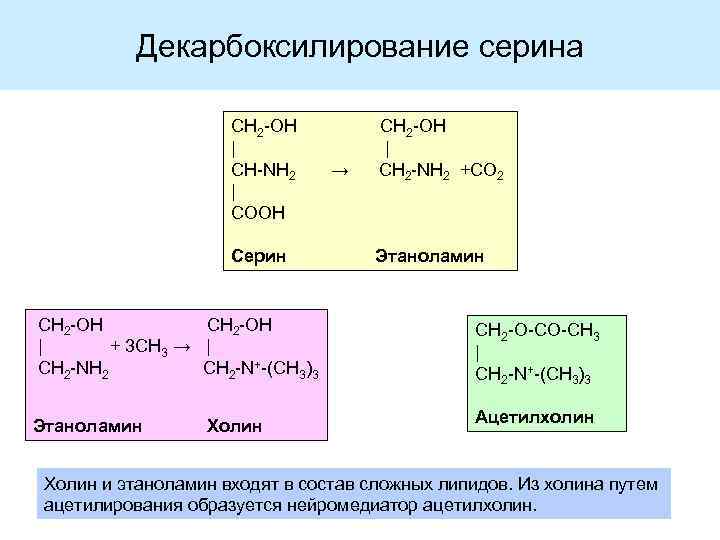
Декарбоксилирование серина СН 2 -ОН | CH-NH 2 | COOH Серин → СН 2 -ОН | CH 2 -NH 2 +CO 2 Этаноламин СН 2 -ОН | + 3 CH 3 → | CH 2 -NH 2 CH 2 -N+-(СH 3)3 СН 2 -О-СО-СН 3 | CH 2 -N+-(СH 3)3 Этаноламин Ацетилхолин Холин и этаноламин входят в состав сложных липидов. Из холина путем ацетилирования образуется нейромедиатор ацетилхолин.
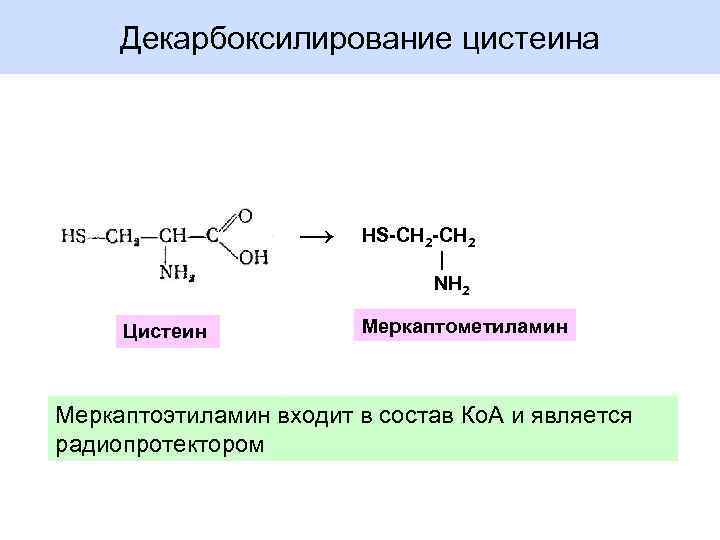
Декарбоксилирование цистеина → Цистеин HS-CH 2 | NH 2 Меркаптометиламин Меркаптоэтиламин входит в состав Ко. А и является радиопротектором

Декарбоксилирование цистеиновой кислоты СН 2 -SO 2 H | CH-NH 2 | COOH → CH 2 -SO 2 H | CH 2 -NH 2 Таурин Цистеиновая кислота Таурин входит в состав таурохолевой кислоты (желчная кислота) и является нейрорегулятором
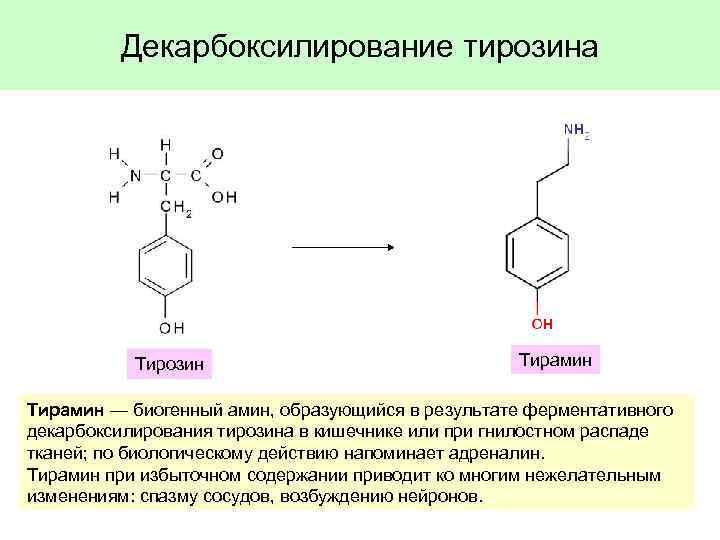
Декарбоксилирование тирозина Тирозин Тирамин — биогенный амин, образующийся в результате ферментативного декарбоксилирования тирозина в кишечнике или при гнилостном распаде тканей; по биологическому действию напоминает адреналин. Тирамин при избыточном содержании приводит ко многим нежелательным изменениям: спазму сосудов, возбуждению нейронов.
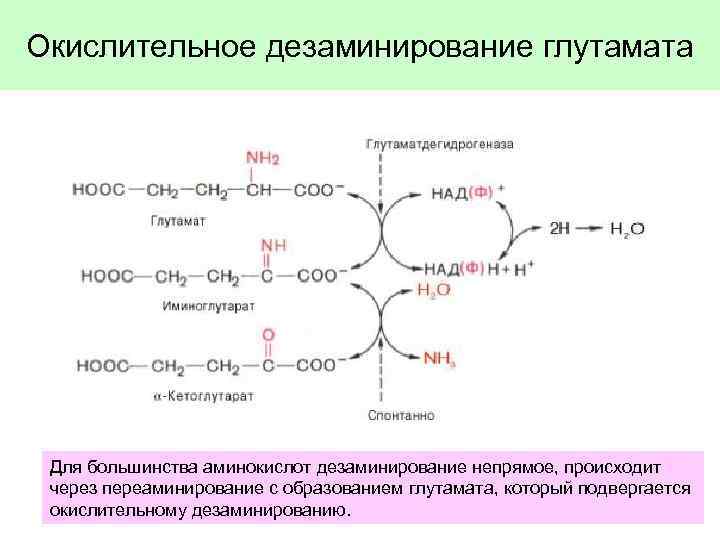
Окислительное дезаминирование глутамата Для большинства аминокислот дезаминирование непрямое, происходит через переаминирование с образованием глутамата, который подвергается окислительному дезаминированию.

Окислительное дезаминирование глутамата • Происходит в митохондриях под влиянием высокоактивного фермента глутаматдегидрогеназы • Активность тормозится АТФ, увеличивается АДФ • Продукты реакции – 2 -оксоглутарат (окисляется в ЦТК), NH 3 (обезвреживается), НАДН (окисляется в дыхательной цепи). • Имеет энергетическое значение, особенно в головном мозге, так как в аварийных ситуациях поставляет энергию, например, при гипогликемии)
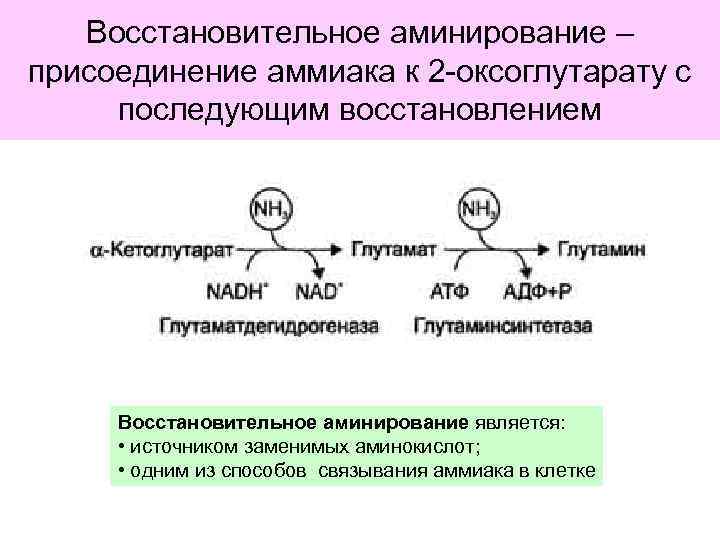
Восстановительное аминирование – присоединение аммиака к 2 -оксоглутарату с последующим восстановлением Восстановительное аминирование является: • источником заменимых аминокислот; • одним из способов связывания аммиака в клетке
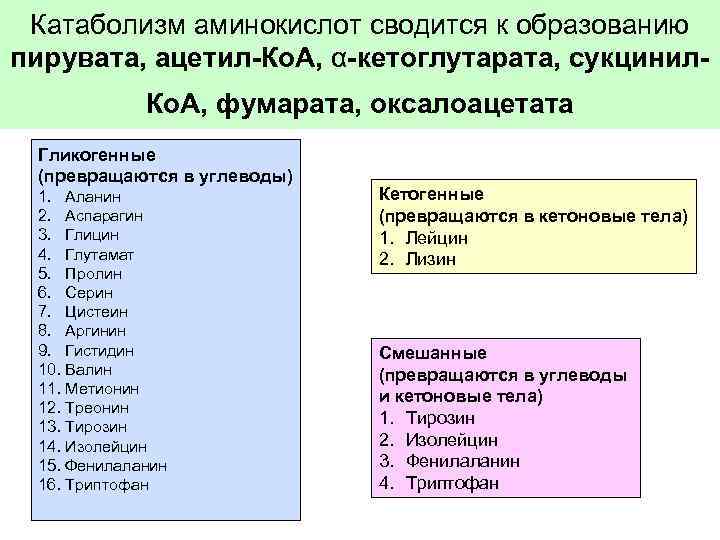
Катаболизм аминокислот сводится к образованию пирувата, ацетил-Ко. А, α-кетоглутарата, сукцинил. Ко. А, фумарата, оксалоацетата Гликогенные (превращаются в углеводы) 1. Аланин 2. Аспарагин 3. Глицин 4. Глутамат 5. Пролин 6. Серин 7. Цистеин 8. Аргинин 9. Гистидин 10. Валин 11. Метионин 12. Треонин 13. Тирозин 14. Изолейцин 15. Фенилаланин 16. Триптофан Кетогенные (превращаются в кетоновые тела) 1. Лейцин 2. Лизин Смешанные (превращаются в углеводы и кетоновые тела) 1. Тирозин 2. Изолейцин 3. Фенилаланин 4. Триптофан
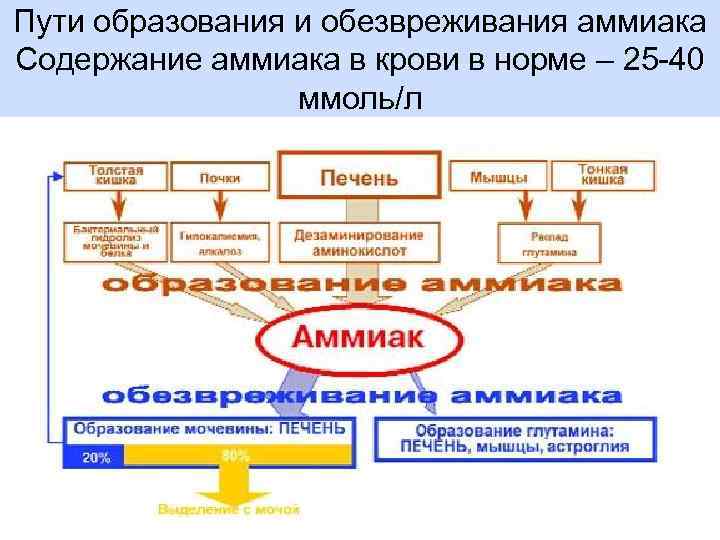
Пути образования и обезвреживания аммиака Содержание аммиака в крови в норме – 25 -40 ммоль/л

Причины токсичности аммиака • Сдвигает глутамат. ДГ в сторону образования глутамата, в результате чего снижается содержание α-кетоглутарата. Это угнетает переаминирование аминокислот и подавление цикла Кребса. • Усиливает синтез глутамина из глутамата. Нарушает обмен нейромедиаторов (γ-аминомасляной кислоты), проведение нервного импульса и вызывает судороги. • NH 4+ нарушает трансмембранный перенос Na+ и K+ и проведение нервного импульса. • Вызывает метаболический алкалоз.
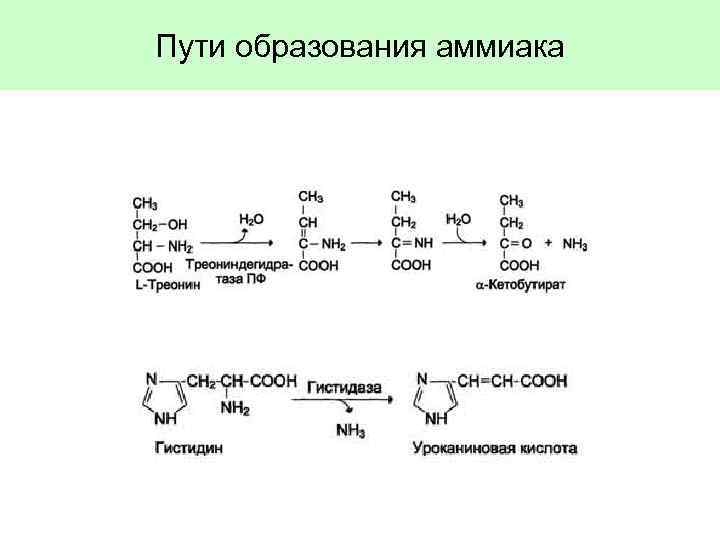
Пути образования аммиака

Пути детоксикации аммиака • Использование на восстановительное аминирование. • Использование на образование амидов (аспарагина и глутамина), которые переносятся в печень и почки, где дезаминируются глутаминазой и аспарагиназой до глутамата или аспартата и аммиака. В печени аммиак используется на образование карбамоилфосфата и выводится из почек в виде аммонийных солей с мочой. • В мышцах аммиак используется для образования аланина, который в печени используется для синтеза глюкозы. • Обмен метаболитами (аланином и глюкозой) между печенью и мышцей называется глюкозо-аланиновым циклом.
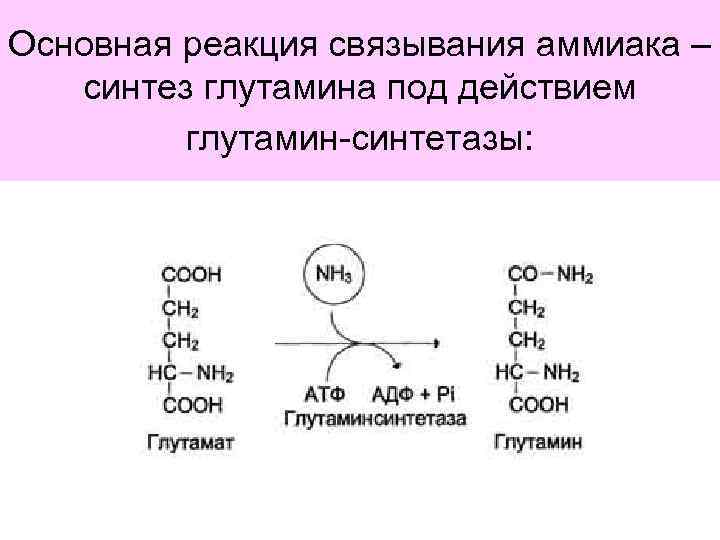
Основная реакция связывания аммиака – синтез глутамина под действием глутамин-синтетазы:
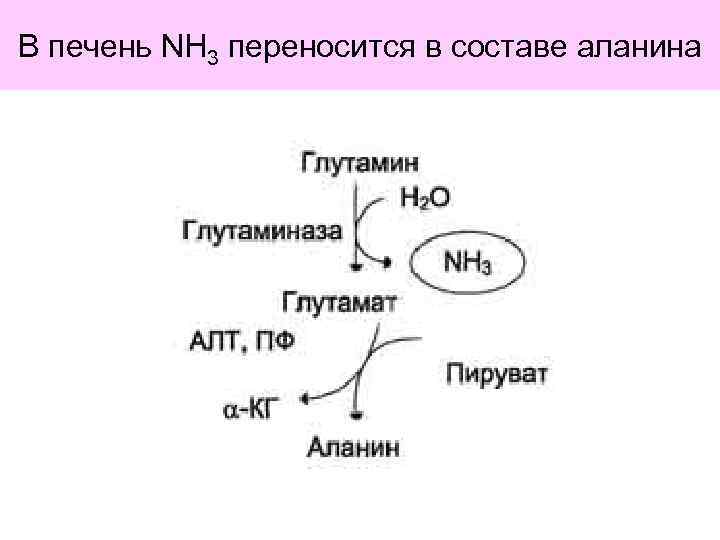
В печень NH 3 переносится в составе аланина
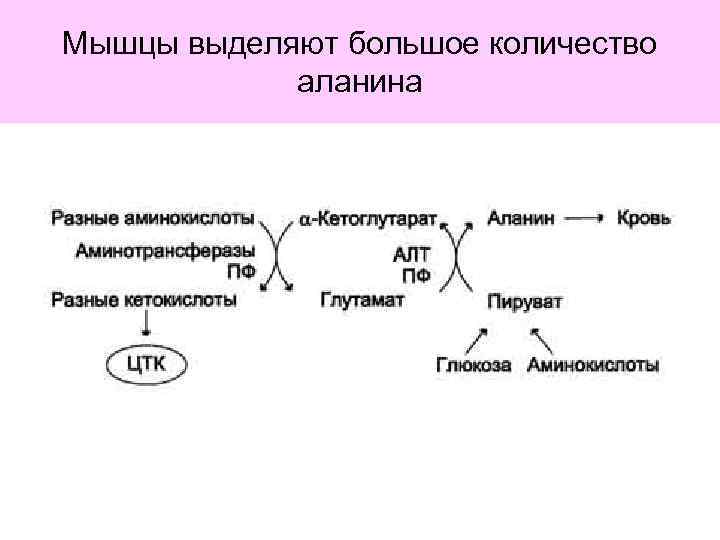
Мышцы выделяют большое количество аланина
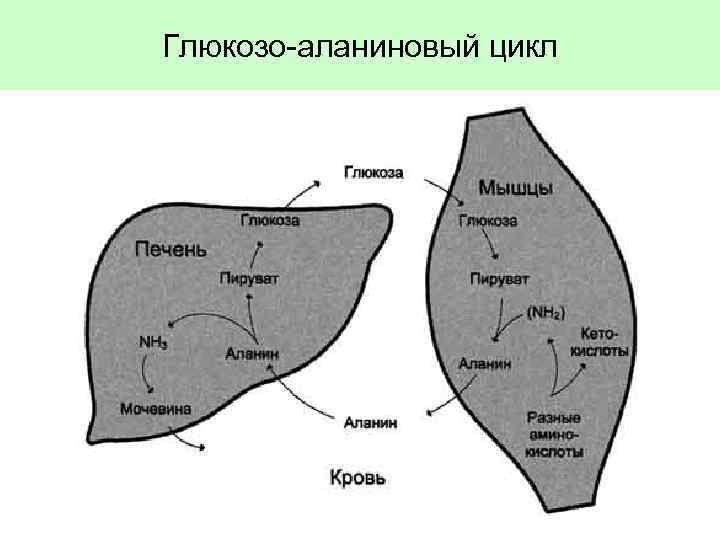
Глюкозо-аланиновый цикл
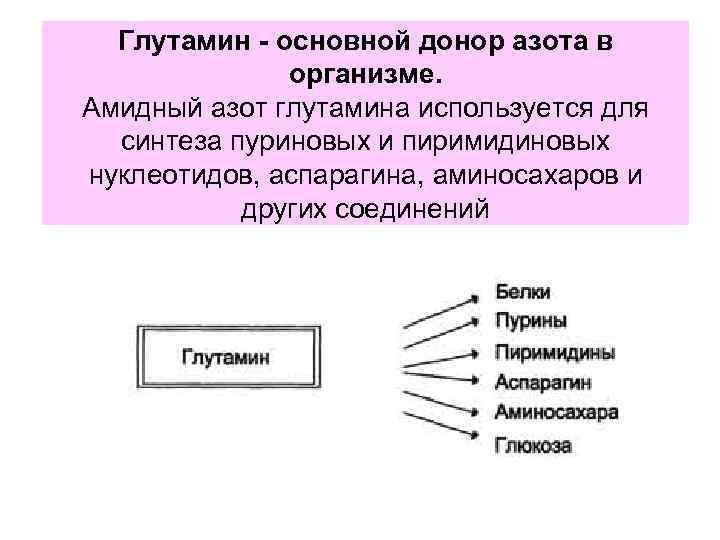
Глутамин - основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров и других соединений
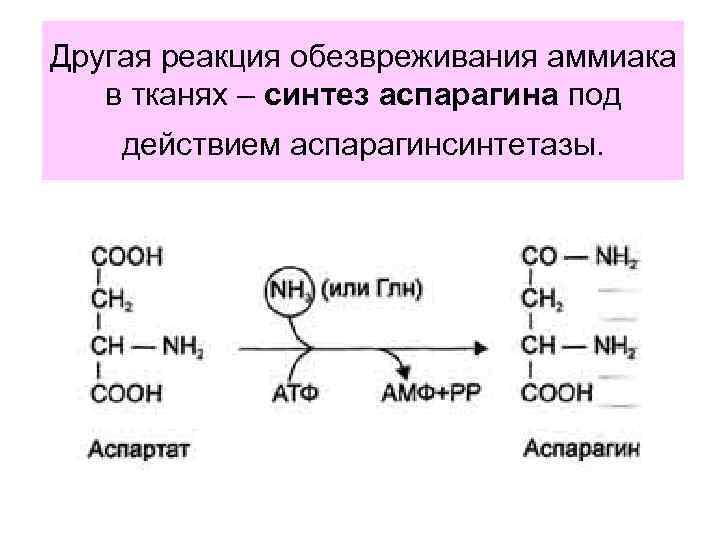
Другая реакция обезвреживания аммиака в тканях – синтез аспарагина под действием аспарагинсинтетазы.
ЛЕКЦИЯ 21.ppt