ЛЕКЦИЯ 20 ИЗЛУЧЕНИЕ И ПОГЛОЩЕНИЕ СВЕТА План























Л 20 изл и погл.ppt
- Количество слайдов: 23
 ЛЕКЦИЯ 20 ИЗЛУЧЕНИЕ И ПОГЛОЩЕНИЕ СВЕТА
ЛЕКЦИЯ 20 ИЗЛУЧЕНИЕ И ПОГЛОЩЕНИЕ СВЕТА
 План лекции: l 1. Излучение и поглощение света атомами и молекулами. l 2. Энергетические уровни атомов и молекул (Электронные энергетические уровни атомов. Энергетические уровни молекул). Особенности излучения и поглощения энергии атомами и молекулами.
План лекции: l 1. Излучение и поглощение света атомами и молекулами. l 2. Энергетические уровни атомов и молекул (Электронные энергетические уровни атомов. Энергетические уровни молекул). Особенности излучения и поглощения энергии атомами и молекулами.
 1. Излучение и поглощение света атомами и молекулами
1. Излучение и поглощение света атомами и молекулами
 В основе всей теоpии излучения (и поглощения) света атомами лежит пpостая фоpмула, введенная в 1913 году Н. Боpом: где и - два некоторых дискpетных значения энеpгии атома, - частота света, соответствующая данному пеpеходу атома
В основе всей теоpии излучения (и поглощения) света атомами лежит пpостая фоpмула, введенная в 1913 году Н. Боpом: где и - два некоторых дискpетных значения энеpгии атома, - частота света, соответствующая данному пеpеходу атома
 Еще в 1859 году немецкие физик Густав Кирхгоф и химик Роберт Бунзен экспериментально установили правило о том, что атомы определенного сорта характеризуются определенной совокупностью спектральных линий. Спектр атома линейчатый и неповторимо индивидуален.
Еще в 1859 году немецкие физик Густав Кирхгоф и химик Роберт Бунзен экспериментально установили правило о том, что атомы определенного сорта характеризуются определенной совокупностью спектральных линий. Спектр атома линейчатый и неповторимо индивидуален.
 Энергетических уровней у молекулы значительно больше, чем у отдельного атома и расположены они ближе друг к другу. Линии спектров многоатомных молекул на отдельных участках практически сливаются, образуя полосатый спектр.
Энергетических уровней у молекулы значительно больше, чем у отдельного атома и расположены они ближе друг к другу. Линии спектров многоатомных молекул на отдельных участках практически сливаются, образуя полосатый спектр.
 Жидкость и твердое тело представляют собой огромную систему атомов и молекул. Электроны в атомах взаимодействуют со многими ядрами и электронами. Множество энергетических уровней сливаются в широкую полосу - сплошной спектр - или несколько полос – энергетических зон.
Жидкость и твердое тело представляют собой огромную систему атомов и молекул. Электроны в атомах взаимодействуют со многими ядрами и электронами. Множество энергетических уровней сливаются в широкую полосу - сплошной спектр - или несколько полос – энергетических зон.
 Электронные энергетические уровни атомов Оптические атомные спектры
Электронные энергетические уровни атомов Оптические атомные спектры
 Атомными спектрами называют как спектры испускания, так и спектры поглощения, которые возникают при квантовых переходах между энергетическими уровнями свободных или слабовзаимодействующих атомов
Атомными спектрами называют как спектры испускания, так и спектры поглощения, которые возникают при квантовых переходах между энергетическими уровнями свободных или слабовзаимодействующих атомов
 Атомные спектры называют оптическими, если они лежат в ультрафиолетовом (100— 400 нм), видимом (400— 760 нм), инфракрасном (λ >760 нм) диапазоне длин волн.
Атомные спектры называют оптическими, если они лежат в ультрафиолетовом (100— 400 нм), видимом (400— 760 нм), инфракрасном (λ >760 нм) диапазоне длин волн.
 Энергетические состояния схематически изображают в виде уровней. Электронных энергетических уровней больше, чем электронов. Электроны в невозбужденном состоянии заполняют нижние энергетические уровни, свободными остаются верхние. Можно перевести электрон в возбужденное состояние, сообщив атому энергию. Удобно это делать в форме кванта света. Квант света может поглотиться атомом только при условии, если его энергия (h ) в точности равна разности энергий между каким-либо свободным и каким-либо заполненным уровнями ( E). На Рисунке такие переходы показаны цифрами 1, 2, и т. д. Длина стрелок равна энергии квантов света. Следовательно, поглотиться могут не любые кванты, а только с определенной энергией. Это приводит к тому, что спектр поглощения атомов линейчатый.
Энергетические состояния схематически изображают в виде уровней. Электронных энергетических уровней больше, чем электронов. Электроны в невозбужденном состоянии заполняют нижние энергетические уровни, свободными остаются верхние. Можно перевести электрон в возбужденное состояние, сообщив атому энергию. Удобно это делать в форме кванта света. Квант света может поглотиться атомом только при условии, если его энергия (h ) в точности равна разности энергий между каким-либо свободным и каким-либо заполненным уровнями ( E). На Рисунке такие переходы показаны цифрами 1, 2, и т. д. Длина стрелок равна энергии квантов света. Следовательно, поглотиться могут не любые кванты, а только с определенной энергией. Это приводит к тому, что спектр поглощения атомов линейчатый.
 Число электронов в атоме ограничено, при отсутствии внешних воздействий они заполняют только часть возможных электронных энергетических уровней с наименьшей энергией. Таким образом, оказываются заполненными нижние электронные уровни, тогда как верхние остаются свободными. Состояние атома с возможной минимальной энергией называют основным.
Число электронов в атоме ограничено, при отсутствии внешних воздействий они заполняют только часть возможных электронных энергетических уровней с наименьшей энергией. Таким образом, оказываются заполненными нижние электронные уровни, тогда как верхние остаются свободными. Состояние атома с возможной минимальной энергией называют основным.
 Поглощение кванта возможно при условии, если его энергия равна разности энергий какого-либо свободного электронного уровня (Ei) и заполненного (Ek): hv = Ei - Ek, i > k. Эта формула выражает закон сохранения энергии.
Поглощение кванта возможно при условии, если его энергия равна разности энергий какого-либо свободного электронного уровня (Ei) и заполненного (Ek): hv = Ei - Ek, i > k. Эта формула выражает закон сохранения энергии.
 • Возбужденные атомы стремятся перейти в состояние с наименьшей энергией. Поэтому происходят спонтанные квантовые переходы Ei -> Ek. Такие переходы могут быть безизлучательными (энергия передается окружающим атомам при столкновениях, вызывая нагрев тела) или излучательными с испусканием квантов света. • Особо выделяется другой вид излучения, который называется вынужденным, или индуцированным. Оно возникает при взаимодействии кванта с возбужденным атомом.
• Возбужденные атомы стремятся перейти в состояние с наименьшей энергией. Поэтому происходят спонтанные квантовые переходы Ei -> Ek. Такие переходы могут быть безизлучательными (энергия передается окружающим атомам при столкновениях, вызывая нагрев тела) или излучательными с испусканием квантов света. • Особо выделяется другой вид излучения, который называется вынужденным, или индуцированным. Оно возникает при взаимодействии кванта с возбужденным атомом.
 Формула для частоты света, излучаемого (поглощаемого) атомом водорода (Z - 1): где i и k — порядковые номера уровней, между которыми происходит переход
Формула для частоты света, излучаемого (поглощаемого) атомом водорода (Z - 1): где i и k — порядковые номера уровней, между которыми происходит переход
 В спектре можно выделить группы линий, называемые спектральными сериями. Каждая серия применительно к спектрам испускания соответствует переходам с различных уровней на один и тот же конечный.
В спектре можно выделить группы линий, называемые спектральными сериями. Каждая серия применительно к спектрам испускания соответствует переходам с различных уровней на один и тот же конечный.
 • В ультрафиолетовой области находятся линии серии Лаймана, которая образуется при переходе с верхних энергетических уровней на самый нижний, основной (nk = 1). • В видимой и близкой ультрафиолетовой областях спектра расположена серия Бальмера, которая возникает вследствие переходов с верхних энергетических уровней на второй (nk = 2). • К инфракрасной области относится серия Пашена, которая возникает при переходах с верхних энергетических уровней на третий (nk = 3).
• В ультрафиолетовой области находятся линии серии Лаймана, которая образуется при переходе с верхних энергетических уровней на самый нижний, основной (nk = 1). • В видимой и близкой ультрафиолетовой областях спектра расположена серия Бальмера, которая возникает вследствие переходов с верхних энергетических уровней на второй (nk = 2). • К инфракрасной области относится серия Пашена, которая возникает при переходах с верхних энергетических уровней на третий (nk = 3).
 Для атомного спектрального анализа используют: спектры испускания -эмиссионный спектральный анализ, и спектры поглощения – абсорбционный атомный спектральный анализ.
Для атомного спектрального анализа используют: спектры испускания -эмиссионный спектральный анализ, и спектры поглощения – абсорбционный атомный спектральный анализ.
 Энергетические уровни молекул. Молекулярные спектры
Энергетические уровни молекул. Молекулярные спектры
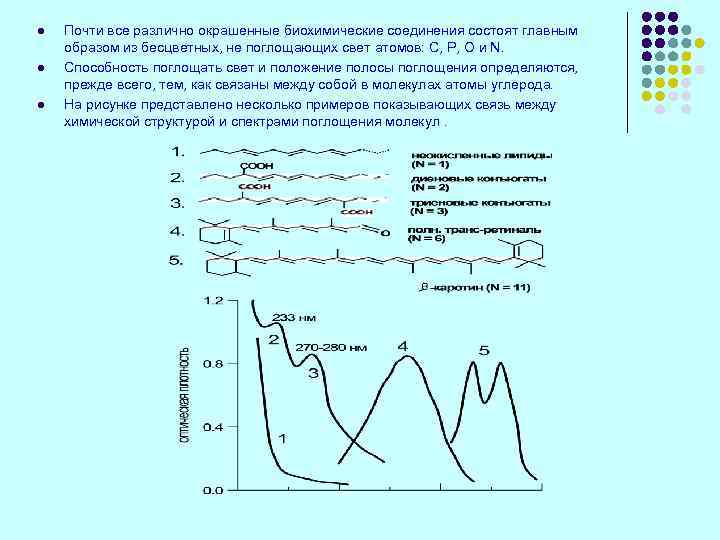
 l Почти все различно окрашенные биохимические соединения состоят главным образом из бесцветных, не поглощающих свет атомов: С, Р, О и N. l Способность поглощать свет и положение полосы поглощения определяются, прежде всего, тем, как связаны между собой в молекулах атомы углерода. l На рисунке представлено несколько примеров показывающих связь между химической структурой и спектрами поглощения молекул.
l Почти все различно окрашенные биохимические соединения состоят главным образом из бесцветных, не поглощающих свет атомов: С, Р, О и N. l Способность поглощать свет и положение полосы поглощения определяются, прежде всего, тем, как связаны между собой в молекулах атомы углерода. l На рисунке представлено несколько примеров показывающих связь между химической структурой и спектрами поглощения молекул.
 l Сложность молекулярных спектров по сравнению с атомными обусловлена большим разнообразием движений и, следовательно, энергетических переходов в молекуле. l Частота, излучаемая или поглощаемая молекулой: l ν= (ΔЕэлектр+ΔЕколеб + ΔЕвращ)
l Сложность молекулярных спектров по сравнению с атомными обусловлена большим разнообразием движений и, следовательно, энергетических переходов в молекуле. l Частота, излучаемая или поглощаемая молекулой: l ν= (ΔЕэлектр+ΔЕколеб + ΔЕвращ)
 l При ΔЕэл не равное 0, ΔЕколеб и ΔЕвращ тоже обычно одновременно не равны 0. Образуются электронно- колебательные, а точнее — электронно- колебательно-вращательные спектры, которые состоят из различных полос, а полосы — из тесно расположенных линий, соответствующих вращательным переходам. l l а) электронно-колебательный спектр молекулы азота, l б) вращательное расщепление одной из полос.
l При ΔЕэл не равное 0, ΔЕколеб и ΔЕвращ тоже обычно одновременно не равны 0. Образуются электронно- колебательные, а точнее — электронно- колебательно-вращательные спектры, которые состоят из различных полос, а полосы — из тесно расположенных линий, соответствующих вращательным переходам. l l а) электронно-колебательный спектр молекулы азота, l б) вращательное расщепление одной из полос.
 l 26. апреля. l ЛЕКЦИЯ 20 l ПОГЛОЩЕНИЕ СВЕТА l 1. Поглощение света. l 2. Закон Бугера-Ламберта-Бера. l 3. Эффективное сечение поглощения молекулы. l 4. Показатель поглощения, коэффициент пропускания, оптическая плотность раствора. l 5. Спектры поглощения вещества. l 6. Концентрационная колориметрия. l 7. Различие атомных и молекулярных спектров поглощения.
l 26. апреля. l ЛЕКЦИЯ 20 l ПОГЛОЩЕНИЕ СВЕТА l 1. Поглощение света. l 2. Закон Бугера-Ламберта-Бера. l 3. Эффективное сечение поглощения молекулы. l 4. Показатель поглощения, коэффициент пропускания, оптическая плотность раствора. l 5. Спектры поглощения вещества. l 6. Концентрационная колориметрия. l 7. Различие атомных и молекулярных спектров поглощения.

