биоокисление лекция3 рус.ppt
- Количество слайдов: 29
ЛЕКЦИЯ№ 2 ТЕМА: Общие закономерности обмена веществ и энергии. Цикл трикарбоновых кислот

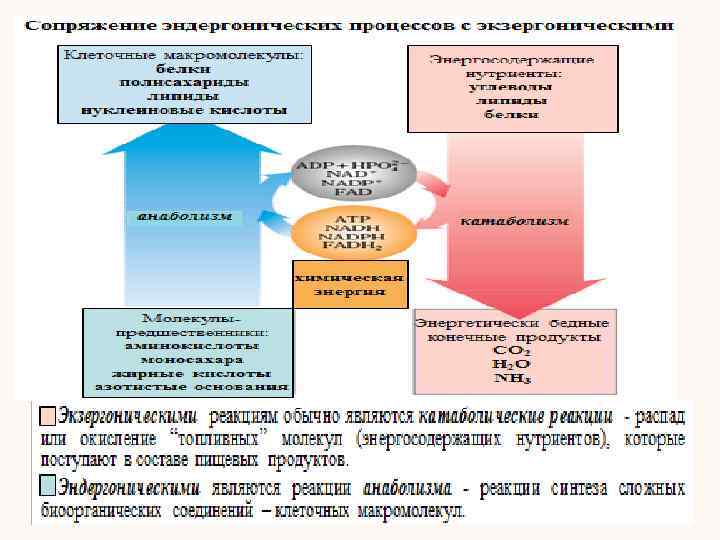
Биоэнергетика – раздел биохимии, изучающий превращения энергии в живых системах Обмен веществ (или метаболизм) - это совокупность биохимических реакций превращения химических соединений, которые происходят в живых организмах. Обмен веществ состоит из нескольких последовательных стадий: 1. Поступление биополимеров (белков, липидов, углеводов), витаминов, минеральных элементов, воды в организм в составе продуктов питания. 2. Превращение этих веществ в пищеварительном тракте в более простые соединения (мономеры: аминокислоты, моносахариды, жирные кислоты, глицерин), которые всасываются эпителием слизистой оболочки желудка и кишечника. 3. Транспорт молекул кровью и лимфой, поступление через мембраны в клетки. 4. Внутриклеточный метаболизм биомолекул. 5. Выделение (экскреция) из организма конечных продуктов обмена веществ (СО 2, NH 3, мочевины, воды, продуктов конъюгации)

Биологическое окисление Это основной способ распада соединений в клетке Виды реакций биологического окисления: - присоединение атомов О 2 - отщепление атомов Н - перенос электронов (е)

Варианты окисления веществ в клетке 1. При аэробном окислении на последнем этапе водород передается на О 2 , который мы получаем при дыхании, и образуется вода - конечный продукт обмена. 2 НАДН+Н+ + О = Н 2 О + 2 НАД+ 2. При анаэробном окислении (гликолизе) происходит восстановление пировиноградной кислоты (ПВК) до молочной кислоты: СН 3 -СО- СООН + НАДН+Н+ = СН 3 -СНОН- СООН + НАД+ ПВК молочная кислота
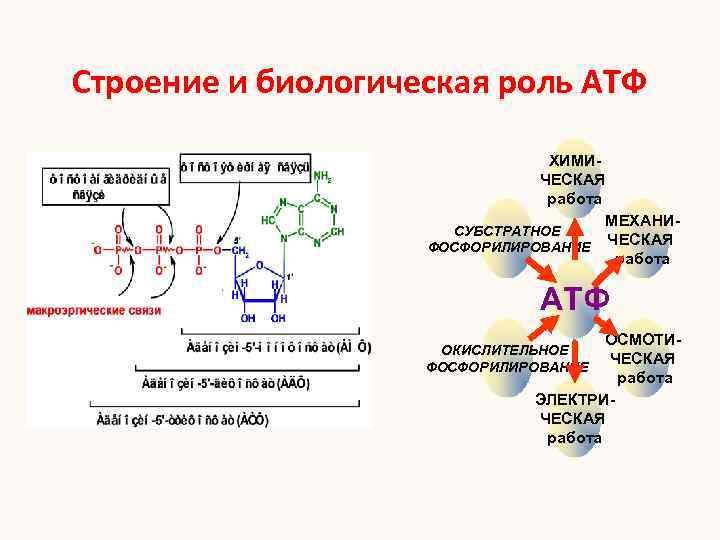
Строение и биологическая роль АТФ ХИМИЧЕСКАЯ работа МЕХАНИСУБСТРАТНОЕ ЧЕСКАЯ ФОСФОРИЛИРОВАНИЕ работа АТФ ОСМОТИЧЕСКАЯ работа ЭЛЕКТРИЧЕСКАЯ работа ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ

Энергетический обмен Это совокупность биохимических процессов в результате которых синтезируется АТФ Пути синтеза АТФ 1. Окислительное фосфорилирование (аэробный путь) АДФ + Н 3 РО 4 + энергия = АТФ 2. Субстратное фосфорилирование (анаэробный путь) АДФ + S ~ Ф = АТФ + S
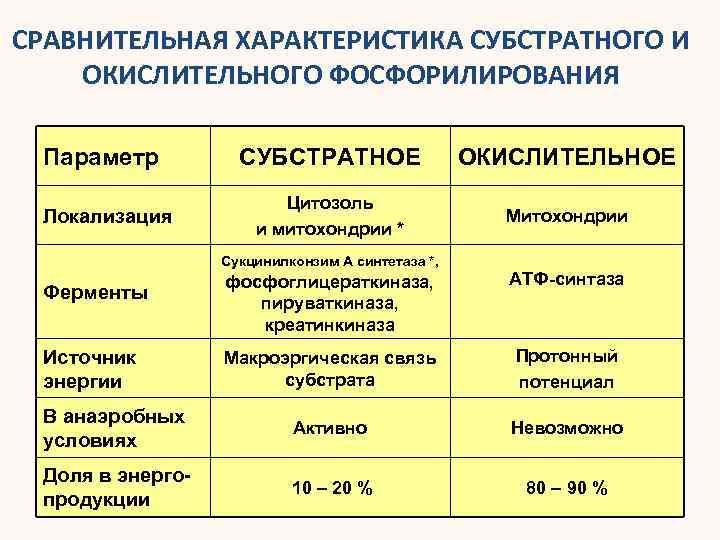
СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА СУБСТРАТНОГО И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Параметр Локализация СУБСТРАТНОЕ ОКИСЛИТЕЛЬНОЕ Цитозоль и митохондрии * Митохондрии Сукцинилконзим А синтетаза *, фосфоглицераткиназа, пируваткиназа, креатинкиназа АТФ-синтаза Макроэргическая связь субстрата Протонный потенциал В анаэробных условиях Активно Невозможно Доля в энергопродукции 10 – 20 % 80 – 90 % Ферменты Источник энергии

ОСНОВНОЙ ПРИНЦИП РЕГУЛЯЦИИ ЭНЕРГЕТИЧЕСКОГО ОБМЕНА: продукция АТФ регулируется потребностью клетки в энергии 1. Аллостерическая регуляция ферментов ЦТК: а) активаторы: НАД+, АМФ, АДФ. б) ингибиторы: НАДН+Н+, АТФ. 2. Гормональная регуляция: Инсулин стимулирует окислительное декарбоксилирование α-кетоглутарата за счет дефосфорилирования полиферментного комплекса. Тиреоидные гормоны стимулируют перенос АДФ в митохондрию и синтез АТФ.

Этапы энергетического обмена

Этапы энергетического обмена 1 этап–подготовительный (гидролитический) Протекает в пищеварительной системе. Молекулы белков, жиров и углеводов пищи расщепляются до мономеров пищеварительными ферментами – гидролазами. Белки + Н 2 О аминокислоты пептидаза Жиры + Н 2 О ВЖК + церин липаза Крахмал + Н 2 О n (глюкоза) амилаза Выделенная энергия рассеивается в виде тепла
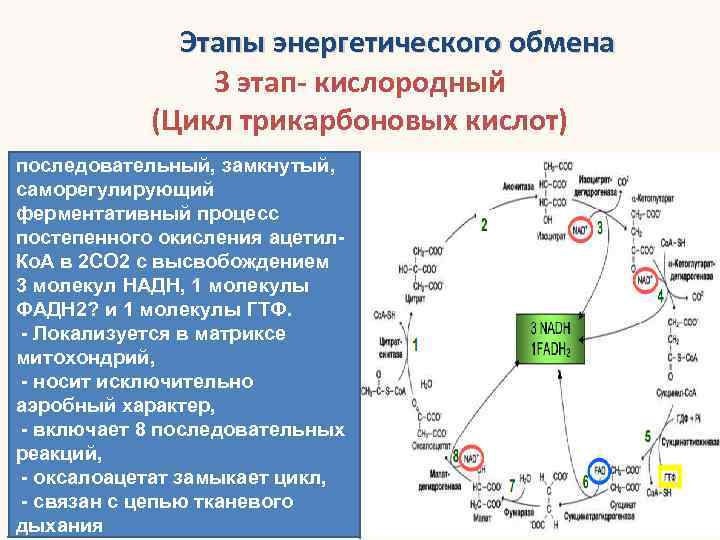
Этапы энергетического обмена 3 этап- кислородный (Цикл трикарбоновых кислот) последовательный, замкнутый, саморегулирующий ферментативный процесс постепенного окисления ацетил. Ко. А в 2 СО 2 с высвобождением 3 молекул НАДН, 1 молекулы ФАДН 2? и 1 молекулы ГТФ. - Локализуется в матриксе митохондрий, - носит исключительно аэробный характер, - включает 8 последовательных реакций, - оксалоацетат замыкает цикл, - связан с цепью тканевого дыхания

Итог цикла трикарбоновых кислот • Суммарная реакция цикла Кребса: Ацетил-SKo. A+ 3 НАД++ ФАД+ + ГДФ + Фн + Н 2 О 2 СО 2 + 3 НАДН+Н+ + ФАДН 2 + ГТФ + НSKo. A • Образующаяся в цикле Кребса ГТФ дает АТФ по реакции : ГТФ + АДФ = ГДФ + АТФ

Функции цикла трикарбоновых кислот 1. Интегративная функция — цикл является связующим звеном между реакциями анаболизма и катаболизма. 2. Катаболическая функция — превращение различных веществ в субстраты цикла: Жирные кислоты, пируват, Лей, Фен — Ацетил-Ко. А. Арг, Гис, Глу — α-кетоглутарат. Фен, тир — фумарат. 3. Анаболическая функция — использование субстратов цикла на синтез органических веществ: Оксалацетат — глюкоза, Асп, Асн. Сукцинил-Ко. А — синтез гема. CО 2 — реакции карбоксилирования.

Функции цикла трикарбоновых кислот 4. Водорододонорная функция — цикл Кребса поставляет на дыхательную цепь митохондрий протоны в виде трех НАДН+Н+ и одного ФАДН 2. 5. Энергетическая функция — 3 НАДН+Н+ дает 7, 5 моль АТФ, 1 ФАДН 2 дает 1, 5 моль АТФ на дыхательной цепи. Кроме того в цикле путем субстратного фосфорилирования синтезируется 1 ГТФ, а затем из него синтезируется АТФ посредствам трансфосфорилирования: ГТФ + АДФ = АТФ + ГДФ.

Регуляция цикла трикарбоновых кислот Наиболее существенное влияние на скорость ЦТК имеет концентрация ацетил-Ко. А и оксалоацетат. Регуляторные ферменты: цитратсинтаза, α-кетоглутаратдегидрогеназа, изоцитрандегидраза. Аллостерични регуляторы ферментов ЦТК а) активаторы: НАД +, АМФ, АДФ. б) ингибиторы: НАДН 2, АТФ. Гормональная регуляция: Инсулин стимулируют окислительное декарбоксилирование α-кетоглутарата за счет дефосфорилювання полиферментные комплекса. Тиреоидные гормоны стимулируют перенос АДФ в митохондрии и синтез АТФ.

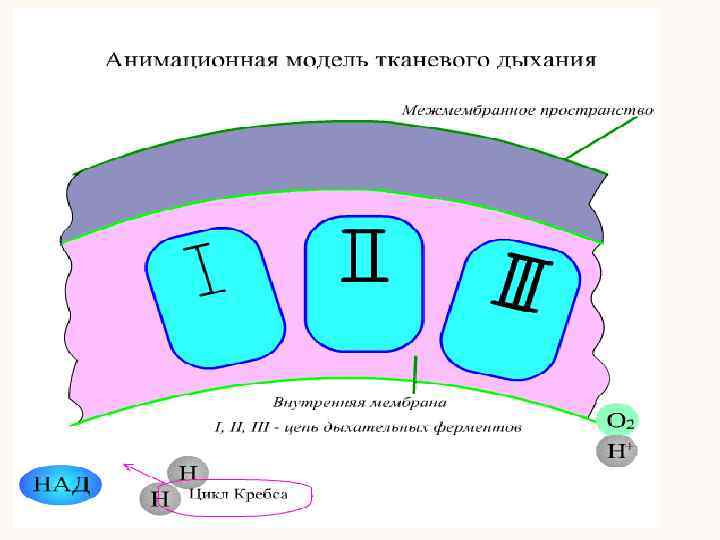
Этапы энергетического обмена 4 этап- тканевое дыхание (ТД) и окислительное фосфорилирование (ОФ) Протекает на внутренней мембране митохондрий. Состоит из двух сопряженных процессов: тканевого дыхания и окислительного фосфорилирования. Тканевое дыхание – это процесс переноса электронов по цепи дыхательных ферментов на кислород с образованием электрохимического потенциала и тепла. Окислительное фосфорилирование – синтез АТФ на внутренней мембране митохондрий из АДФ и фосфорной кислоты (Н 3 РО 4) за счет энергии электрохимического потенциала.

БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ тканевого дыхания (ТД) и окислительного фосфорилирования (ОФ) 1. ТД – главный потребитель кислорода, ОФ – главный поставщик АТФ. 2. Обеспечивают конечный этап окисления органических веществ до неорганических – образуется метаболическая вода. БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ: 3. Поддержание постоянной температуры (несократительный термогенез).
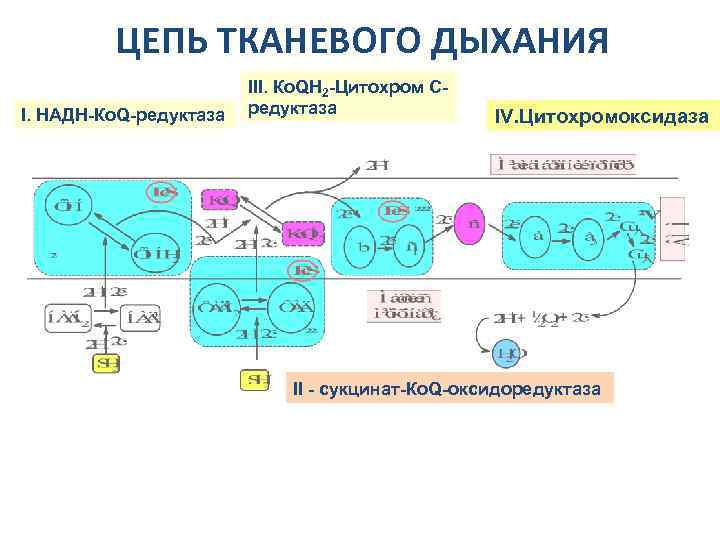
ЦЕПЬ ТКАНЕВОГО ДЫХАНИЯ І. НАДН-Ко. Q-редуктаза ІІІ. Ко. QН 2 -Цитохром Средуктаза IV. Цитохромоксидаза II - сукцинат-Ко. Q-оксидоредуктаза

• Ферменты тканевого дыхания Комплекс I – НАДН-дегидрогеназа – флавопротеин, содержащий ФМН. Этот фермент окисляет НАДН и передает два водорода (2 Н+2 е-) на коэнзим Q. В комплекс входят также Fe-S-белки. • Комплекс II – сукцинатдегидрогеназа – флавопротеин, содержащий ФАД. Этот фермент окисляет сукцинат и передает два водорода (2 Н+2 е-) на коэнзим Q. В составе комплекса есть Fe-S-белки. • Комплекс III – убихинондегидрогеназа – ферментный комплекс, состоящий из цитохрома b, Fe-S-белка и цитохрома с1. Этот комплекс транспортирует электроны 2 е- от восстановленного убихинона Ко. QН 2 на цитохром с (небольшой по размерам водорастворимый белок, находится на внешней стороне внутренней мембраны).

Ферменты тканевого дыхания • Комплекс IV – цитохром с-оксидаза – ферментный комплекс, состоящий из цитохромов а и а 3. Эти ферменты осуществляют последнюю стадию биологического окисления – восстановление электронами 2 е- молекулярного кислорода • Комплекс V - Н+-зависимая АТФ-синтаза seu Н+-зависимая АТФаза (два разных названия связаны с полной обратимостью катализируемой реакции), обладающий значительной молекулярной массой–более, чем 500 к. Да. Состоит из двух субъединиц: FO и F 1 представляет из себя грибовидный вырост на матриксной поверхности внутренней митохондриальной мембраны, FO же пронизывает эту мембрану насквозь. В толще FO расположен протонный канал, позволяющий протонам возвращаться обратно в матрикс по градиенту их концентраций. F 1 способна связывать АДФ и фосфат на своей поверхности с образованием АТФ - без затраты энергии, но обязательно в комплексе с ферментом. Энергия необходима лишь для освобождения АТФ из этого комплекса. Эта энергия выделяется в результате тока протонов через протонный канал FO.

РЕДОКС-ПОТЕНЦИАЛ РОП обуславливает порядок направления движения электронов в дыхательной цепи, начиная с окисляемого субстрата (АН 2), имеющего редокс-потенциал -0, 7 V и заканчивая кислородом с редокспотенциалом +0, 8 V. Увеличение редокс-потенциала в дыхательной цепи обуславливает движение электронов по дыхательной цепи к кислороду, электроны движутся от соединений с меньшим редокспотенциалом к большему, поэтому наблюдается такой строгий порядок расположения ферментов и коферментов в дыхательной цепи. В участках цепи тканевого дыхания , где перепад РОП > 0, 22 V, движение е- сопряжено с синтезом АТФ

ХЕМИОСМОТИЧЕСКАЯ ТЕОРИЯ 1. Митохондриальная дыхательная цепь, находящаяся во внутренней мембране, способна перемещать протоны; при прохождении электронов по дыхательной цепи происходит «откачивание» Н+ из матрикса. 2. Митохондриальный АТФ-синтетазный комплекс тоже перемещает протоны через внутреннюю мембрану. 3. Внутренняя мембрана митохондрий непроницаема для Н +, ОН- и вообще всех анионов и катионов. 4. Внутренняя митохондриальная мембрана содержит ряд белков- переносчиков, осуществляющих транспорт нужных метаболитов и неорганических ионов. Движение электронов по дыхательной цепи служит источником энергии для переноса протонов через мембрану В итоге на внутренней мембране создается электрохимический протонный градиент. Трансмембранный электрохимический потенциал служит сопрягающим звеном между тканевым дыханием и окислительным фосфорилированием
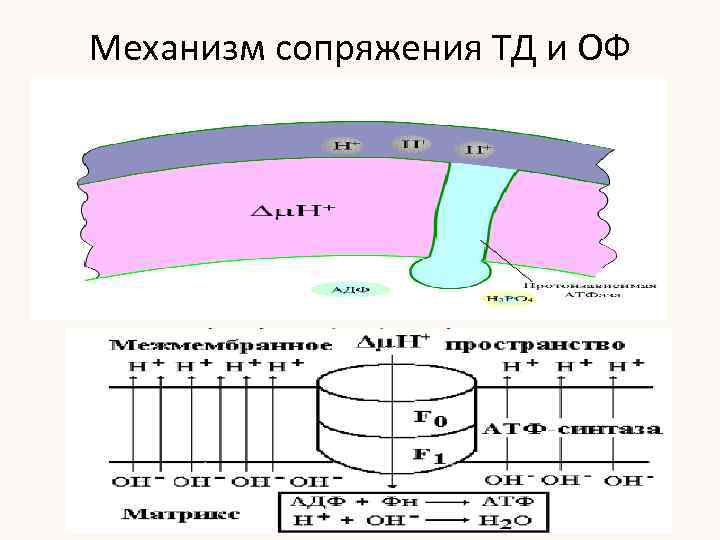
Механизм сопряжения ТД и ОФ

Коэффициент Р/О- показывает число молекул неорганического фосфата (Фн), которое перешло в органические (АТФ) в расчете на каждый поглощенный атом кислорода. При окислении 1 молекулы НАДН+Н образуется 3 молекулы АТФ 1 молекулы ФАДН 2 образуется 2 молекулы АТФ. Дыхательный контроль Ускорение окислительного фосфорилирования и дыхания при повышении концентрации ADP называется дыхательным контролем.
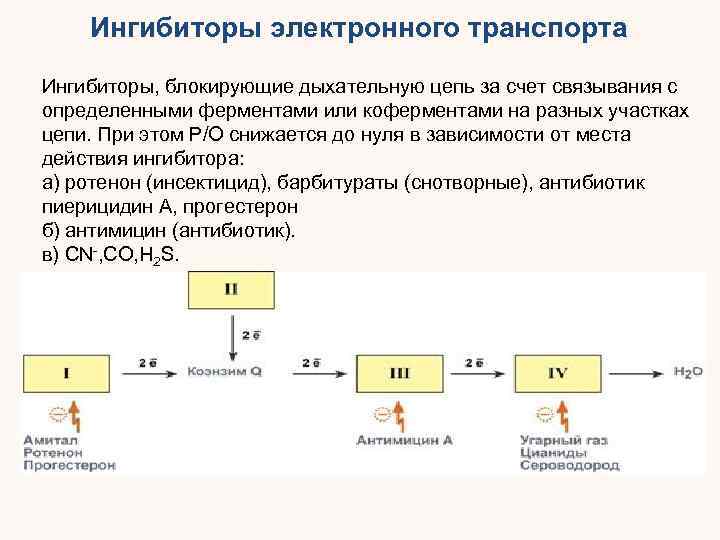
Ингибиторы электронного транспорта Ингибиторы, блокирующие дыхательную цепь за счет связывания с определенными ферментами или коферментами на разных участках цепи. При этом Р/О снижается до нуля в зависимости от места действия ингибитора: а) ротенон (инсектицид), барбитураты (снотворные), антибиотик пиерицидин А, прогестерон б) антимицин (антибиотик). в) CN-, CO, H 2 S.

Ингибиторы окислительного фосфорилирования Ингибитор окислительного фосфорилирования: олигомицин – антибиотик, ингибирует функцию АТФ-синтетазы (не действует на тканевое дыхание). • Разобщители окислительного фосфорилирования – липофильные вещества, которые способны принимать протоны и переносить их через внутреннюю мембрану митохондрий минуя V комплекс(его протонный канал). Разобщители: • Естественные — продукты перекисного окисления липидов, жирных кислот с длинной цепью; тироксин, билирубин • Искусственные — 2, 4 -динитрофенол, эфир, салициловая кислота, дикумарин.

БУДЬТЕ ЗДОРОВЫ!
биоокисление лекция3 рус.ppt