Лекция 2. Строение,св-ва и роль белков.ppt
- Количество слайдов: 23

Лекция 2. Строение, свойства, биологическая роль белков 1 СТАТИЧЕСКАЯ БИОХИМИЯ

Аминокислоты - карбоновые кислоты, содержащие карбоксильную (-СООН) и аминную (-NH 2) группы, которые находятся у одного и того же атома углерода. В организме человека найдено около 70 аминокислот, 20 из них входят в состав белков и называются протеиногенными. Химическим путем удалось синтезировать уже более 600 аминокислот. 2 СТАТИЧЕСКАЯ БИОХИМИЯ

Классифицировать аминокислоты можно по полярности их радикалов, о чем ниже. По функциональному значению аминокислоты условно можно разделить на три группы: 1. Никогда не входят в белки: β-аланин, орни-тин, γ- и ωаминомасляные к-ты и др. 2. Стандартные = протеиногенные = канонические. Это 20 вариантов α-аминокислот, как мономеров полипептида. На них рассчитан генетический код, т. е. способ записи, хранения и воспроизведения наследственной информации. 3. Редкие, минорные модификации стандартных аминокислот с помощью ферментов, уже после синтеза, при формировании полипеп 3 тидов ~100.

Общая формула α-аминокислот R—CH—COОН NH 2 4 СТАТИЧЕСКАЯ БИОХИМИЯ

Аминокислоты подразделяются на 4 основные класса: • неполярные, или гидрофобные (аланин, валин, лейцин, изолейцин, пролин, фенилаланин, триптофан, метионин); • полярные, но незаряженные (глицин, серин, треонин, цистеин, тирозин, аспарагин, глутамин); • положительно заряженные (лизин, гистидин, аргинин); • отрицательно заряженные (аспарагиновая кислота, глутаминовая кислота). 5 СТАТИЧЕСКАЯ БИОХИМИЯ
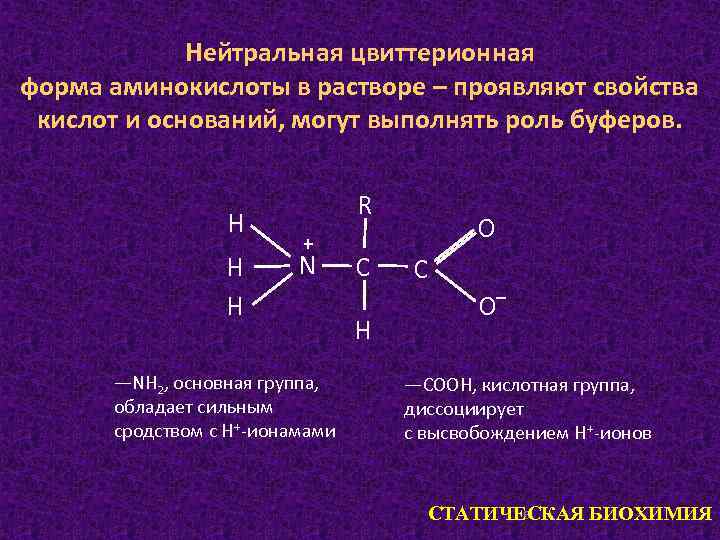
Нейтральная цвиттерионная форма аминокислоты в растворе – проявляют свойства кислот и оснований, могут выполнять роль буферов. Н Н Н R + N —NH 2, основная группа, обладает сильным сродством с Н+-ионамами С Н О С _ О —СООН, кислотная группа, диссоциирует с высвобождением Н+-ионов 6 СТАТИЧЕСКАЯ БИОХИМИЯ
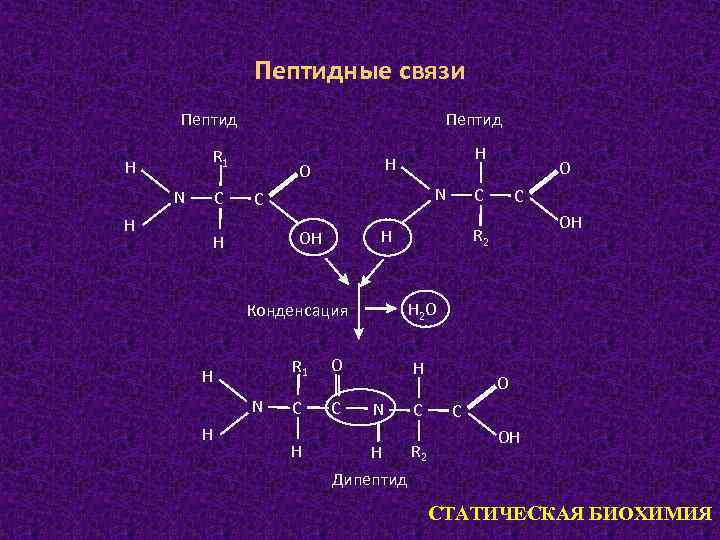
Пептидные связи Пептид R 1 Н N С Н О N С R 1 N О С С Н С ОН R 2 Н 2 О Конденсация Н О С Н ОН Н Н N Н С R 2 О С ОН Дипептид 7 СТАТИЧЕСКАЯ БИОХИМИЯ
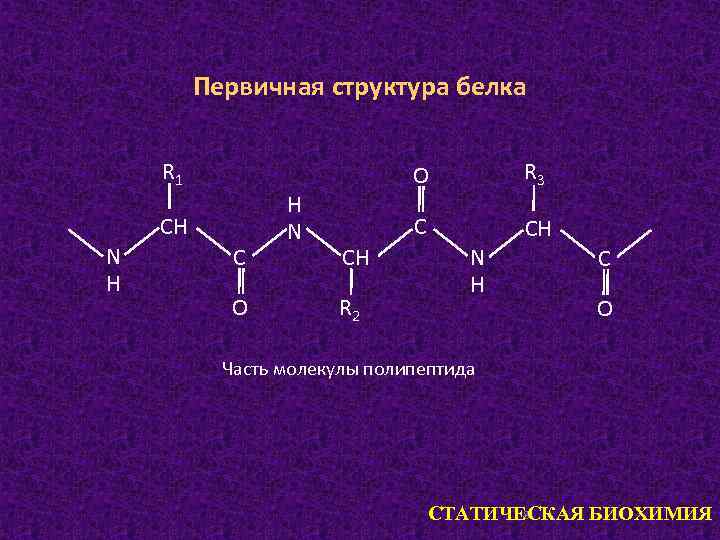
Первичная структура белка R 1 О СН N Н С О Н N С СН R 2 R 3 СН N Н С О Часть молекулы полипептида 8 СТАТИЧЕСКАЯ БИОХИМИЯ
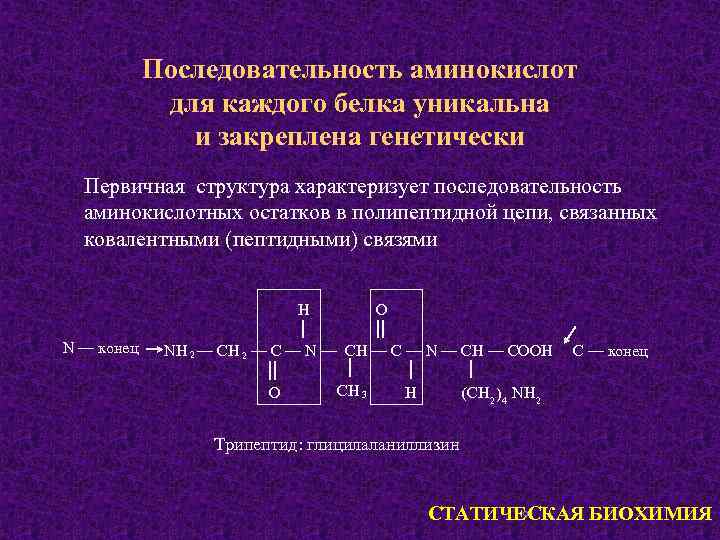
Последовательность аминокислот для каждого белка уникальна и закреплена генетически Первичная структура характеризует последовательность аминокислотных остатков в полипептидной цепи, связанных ковалентными (пептидными) связями H N — конец O NH 2 — C — N — CH — COOH O СH 3 C — конец (CH 2 ) 4 NH 2 H Трипептид: глицилаланиллизин 9 СТАТИЧЕСКАЯ БИОХИМИЯ
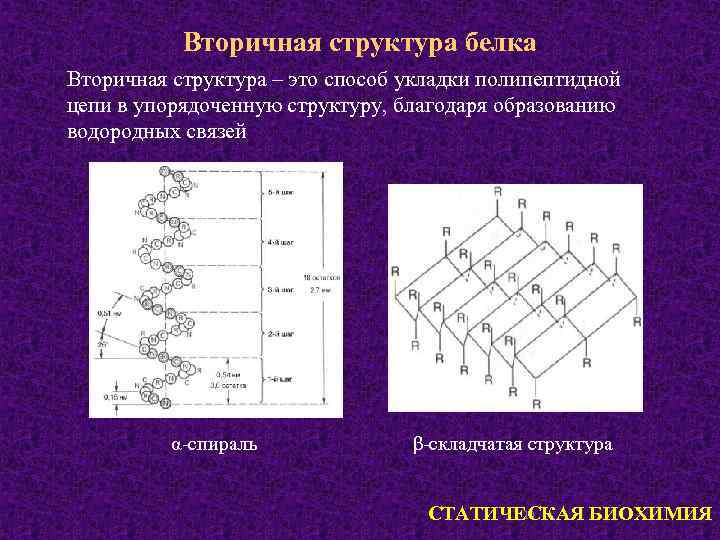
Вторичная структура белка Вторичная структура – это способ укладки полипептидной цепи в упорядоченную структуру, благодаря образованию водородных связей α-спираль β-складчатая структура 10 СТАТИЧЕСКАЯ БИОХИМИЯ

Водородная связь – как основа вторичной (пространственной) структуры белка Электроположительные водородные атомы, соединенные с кислородом или азотом в группах –ОН или –NH, стремятся обобществить электроны с находящимся по соседству электроотрицательным атомом кислорода, например, с кислородом группы =СО. Локализованное электростатическое притяжение – ОН. . . ОС 11 СТАТИЧЕСКАЯ БИОХИМИЯ
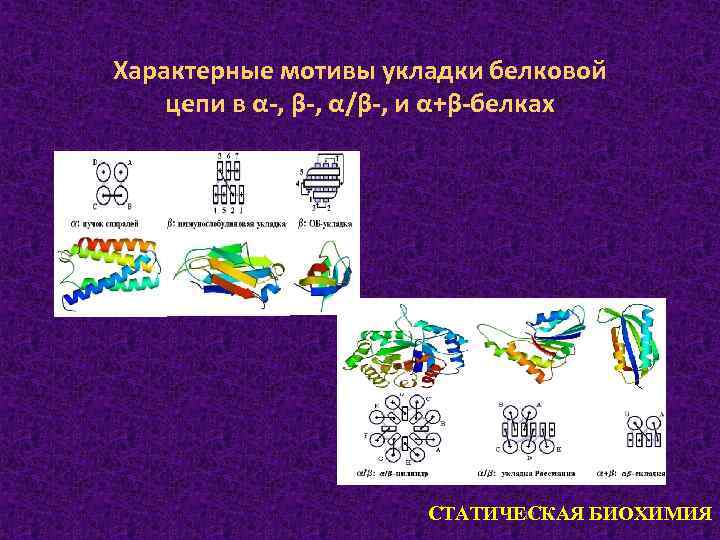
Характерные мотивы укладки белковой цепи в α-, β-, α/β-, и α+β-белках 12 СТАТИЧЕСКАЯ БИОХИМИЯ
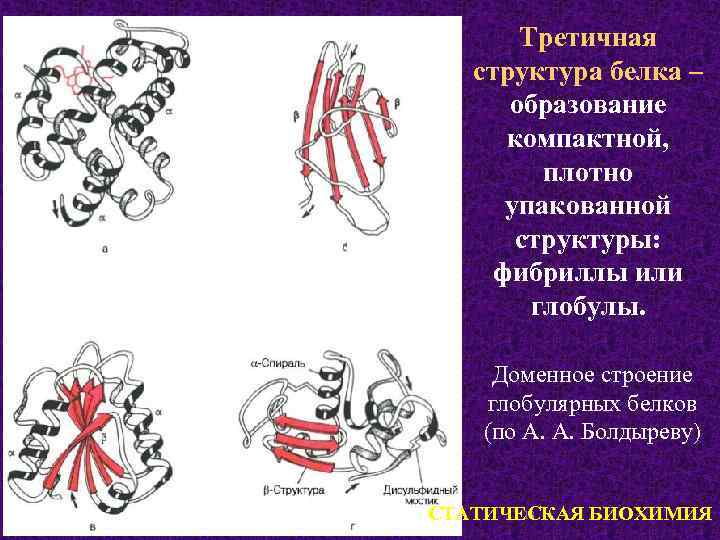
Третичная структура белка – образование компактной, плотно упакованной структуры: фибриллы или глобулы. Доменное строение глобулярных белков (по А. А. Болдыреву) 13 СТАТИЧЕСКАЯ БИОХИМИЯ

Четвертичная структура белка а а – гемоглобин, состоящий из четырех субъединиц (двух α-цепей и двух β-цепей), б – одна субъединица, в – простетическая группа гемоглобина б в 14 СТАТИЧЕСКАЯ БИОХИМИЯ

Функциональная классификация белков: • Каталитические – ферменты; • Транспортные – альбумины, липопротеины высокой, низкой, очень низкой плотности; • Регуляторные – гормон инсулин; • Защитные – антитела и иммуноглобулины, фибриноген; • Сократительные – коллаген и ретикулин; • Рецепторные ; • Запасные и питательные – глютеин, проламин, овальбумин; • Токсические. 15

Классификация белков по химическому составу Простые – содержащие в составе только белковую молекулу Сложные – содержащие в составе помимо белковой части содержат простетическую группу разной химической природы 16
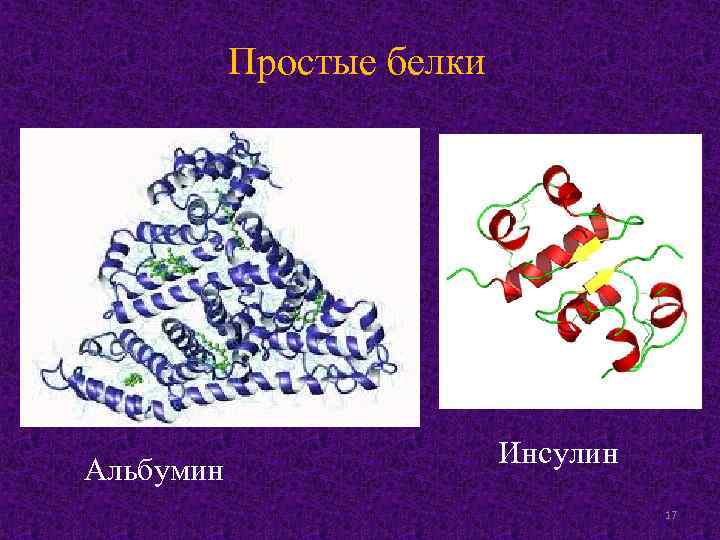
Простые белки Альбумин Инсулин 17
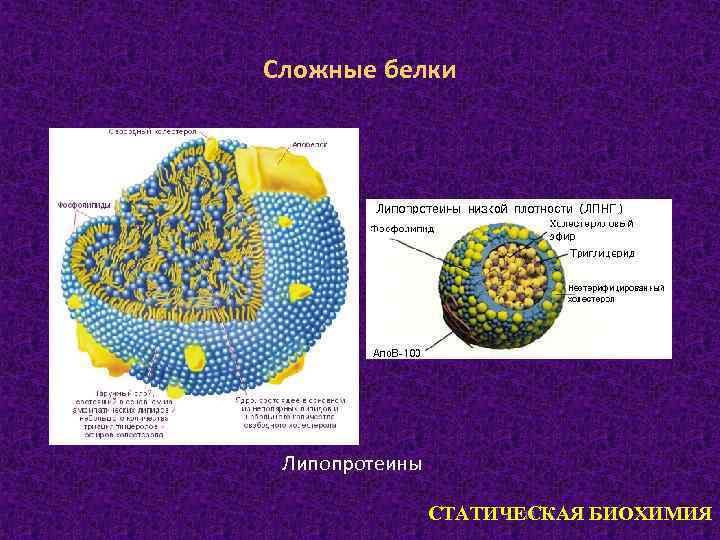
Сложные белки Липопротеины 18 СТАТИЧЕСКАЯ БИОХИМИЯ
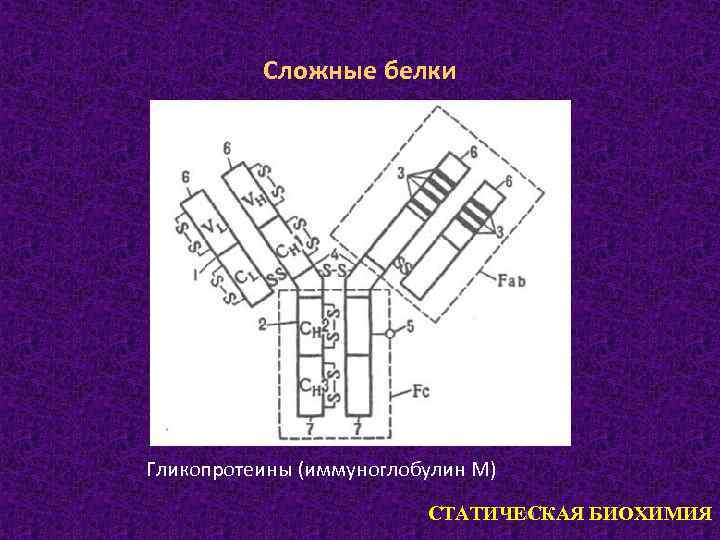
Сложные белки Гликопротеины (иммуноглобулин М) 19 СТАТИЧЕСКАЯ БИОХИМИЯ
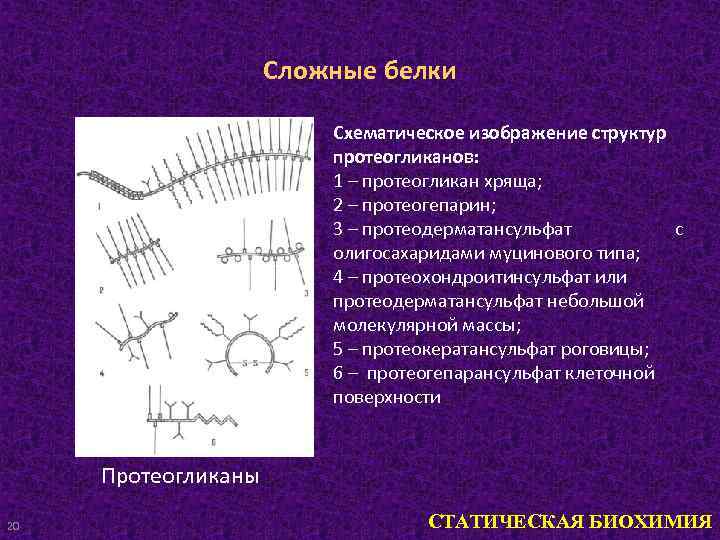
Сложные белки Схематическое изображение структур протеогликанов: 1 – протеогликан хряща; 2 – протеогепарин; 3 – протеодерматансульфат с олигосахаридами муцинового типа; 4 – протеохондроитинсульфат или протеодерматансульфат небольшой молекулярной массы; 5 – протеокератансульфат роговицы; 6 – протеогепарансульфат клеточной поверхности Протеогликаны 20 СТАТИЧЕСКАЯ БИОХИМИЯ
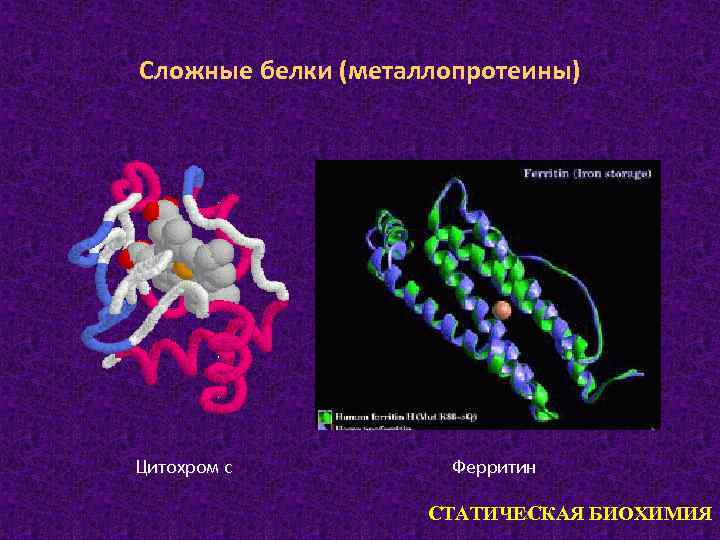
Сложные белки (металлопротеины) Цитохром с Ферритин 21 СТАТИЧЕСКАЯ БИОХИМИЯ
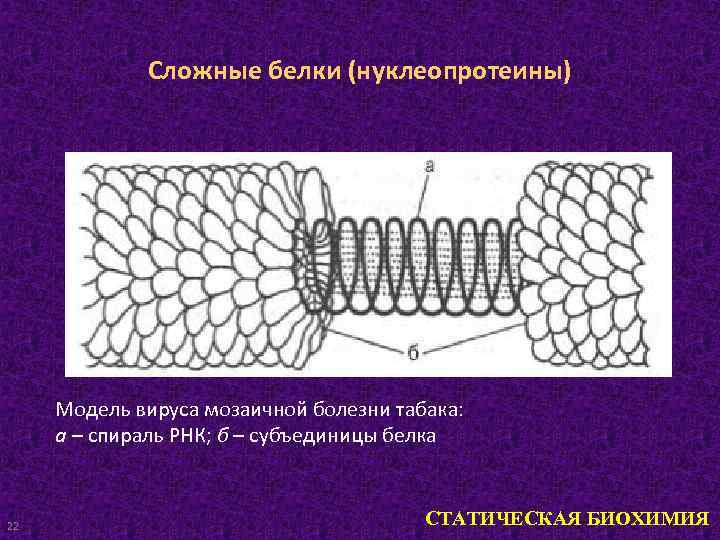
Сложные белки (нуклеопротеины) Модель вируса мозаичной болезни табака: а – спираль РНК; б – субъединицы белка 22 СТАТИЧЕСКАЯ БИОХИМИЯ
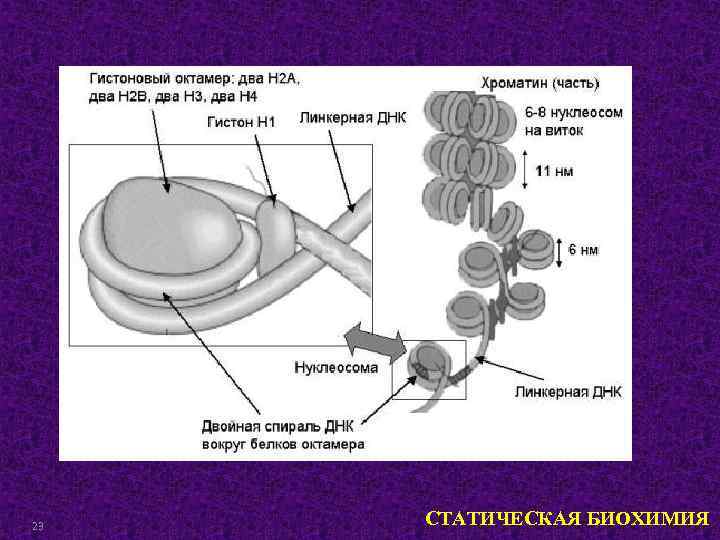
23 СТАТИЧЕСКАЯ БИОХИМИЯ
Лекция 2. Строение,св-ва и роль белков.ppt