 Лекция № 2 Строение атомов. Периодическая система элементов
Лекция № 2 Строение атомов. Периодическая система элементов
 Бериллий Ве 1 s 22 s 2 4 s-семейство Валентные электроны 2 s 2 к =0 Возбуждённое состояние к= 2
Бериллий Ве 1 s 22 s 2 4 s-семейство Валентные электроны 2 s 2 к =0 Возбуждённое состояние к= 2
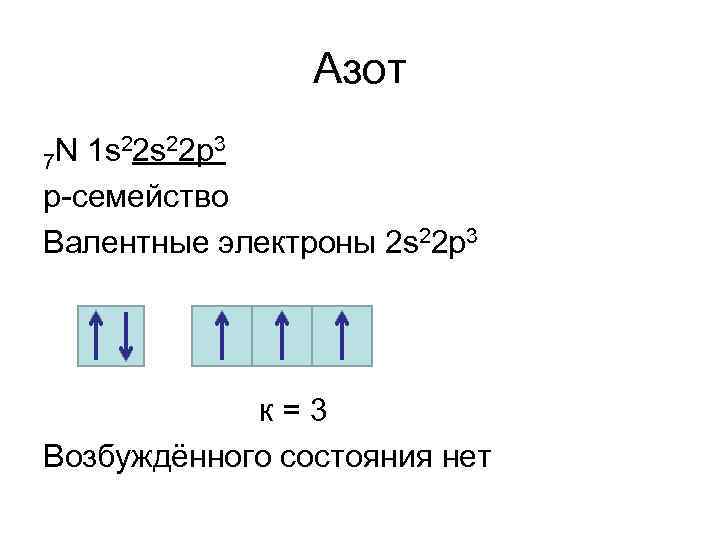 Азот N 1 s 22 р3 7 р-семейство Валентные электроны 2 s 22 р3 к=3 Возбуждённого состояния нет
Азот N 1 s 22 р3 7 р-семейство Валентные электроны 2 s 22 р3 к=3 Возбуждённого состояния нет
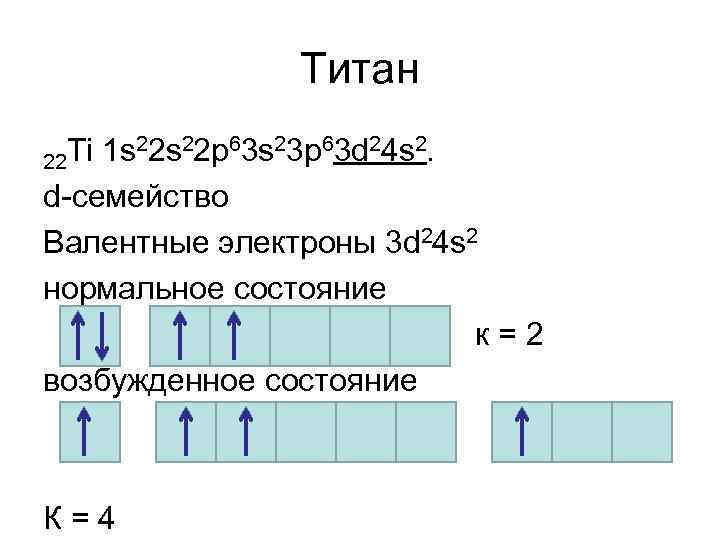 Титан Ti 1 s 22 р63 s 23 р63 d 24 s 2. 22 d-семейство Валентные электроны 3 d 24 s 2 нормальное состояние к=2 возбужденное состояние К=4
Титан Ti 1 s 22 р63 s 23 р63 d 24 s 2. 22 d-семейство Валентные электроны 3 d 24 s 2 нормальное состояние к=2 возбужденное состояние К=4
 «Проскок» электрона Переход электронов с s-подуровня внешнего энергетического уровня ns на d-подуровень предвнешнего уровня (n – 1)d. «Проскок» электрона происходит в атомах некоторых d-элементов, например, 24 Сr, 29 Cu, 42 Mo, 47 Ag, 79 Au, 41 Nb, 44 Ru, 45 Rh, 46 Pd.
«Проскок» электрона Переход электронов с s-подуровня внешнего энергетического уровня ns на d-подуровень предвнешнего уровня (n – 1)d. «Проскок» электрона происходит в атомах некоторых d-элементов, например, 24 Сr, 29 Cu, 42 Mo, 47 Ag, 79 Au, 41 Nb, 44 Ru, 45 Rh, 46 Pd.
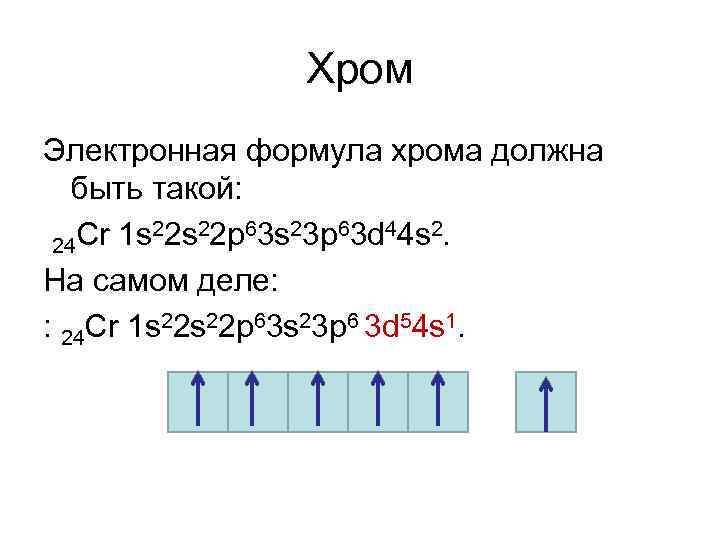 Хром Электронная формула хрома должна быть такой: Cr 1 s 22 p 63 s 23 p 63 d 44 s 2. 24 На самом деле: : 24 Cr 1 s 22 p 63 s 23 p 6 3 d 54 s 1.
Хром Электронная формула хрома должна быть такой: Cr 1 s 22 p 63 s 23 p 63 d 44 s 2. 24 На самом деле: : 24 Cr 1 s 22 p 63 s 23 p 6 3 d 54 s 1.
 Изменение радиусов атомов
Изменение радиусов атомов
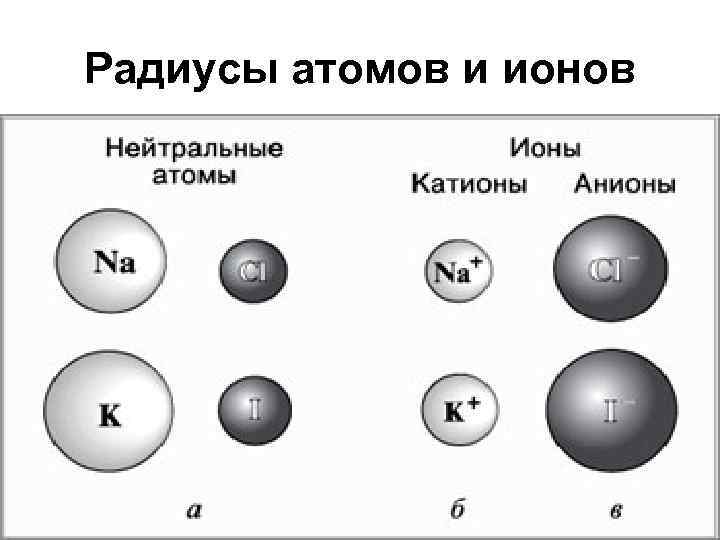 Радиусы атомов и ионов
Радиусы атомов и ионов
 Лантаноидное сжатие
Лантаноидное сжатие
 Лекция № 3 Химическая связь. Строение молекул
Лекция № 3 Химическая связь. Строение молекул