2_stereoizomeria_2015.pptx
- Количество слайдов: 74
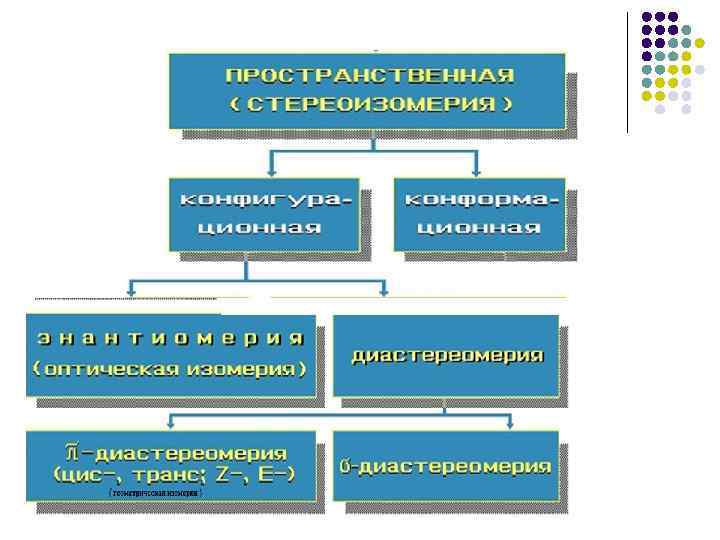
 Лекция № 2. «Стереоизомерия органических соединений» Геометрическая изомерия. Оптическая изомерия. Конформационная изомерия. Циклоалканы.
Лекция № 2. «Стереоизомерия органических соединений» Геометрическая изомерия. Оптическая изомерия. Конформационная изомерия. Циклоалканы.
 Изомерия (от греч. isos — равный), Берцелиус, 1830 г. Изомеры — это вещества, которые имеют одинаковую молекулярную формулу, но отличаются последовательностью связывания атомов и (или) расположением их в пространстве и обладают разными свойствами.
Изомерия (от греч. isos — равный), Берцелиус, 1830 г. Изомеры — это вещества, которые имеют одинаковую молекулярную формулу, но отличаются последовательностью связывания атомов и (или) расположением их в пространстве и обладают разными свойствами.
 БЕРЦЕЛИУС (Berzelius), Йёнс Якоб. 1779 г. – 1848 г Знаменитый шведский химик. С 1807 профессор медицины и фармации в Стокгольме.
БЕРЦЕЛИУС (Berzelius), Йёнс Якоб. 1779 г. – 1848 г Знаменитый шведский химик. С 1807 профессор медицины и фармации в Стокгольме.
 Стереоизомерия Стереохимия (от греч. stereos - пространственный) – это «химия в трех измерениях, 3 D)
Стереоизомерия Стереохимия (от греч. stereos - пространственный) – это «химия в трех измерениях, 3 D)
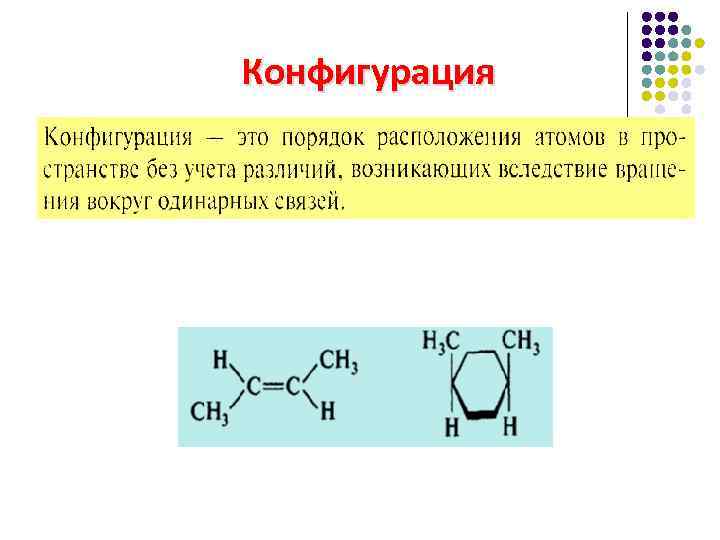 Конфигурация
Конфигурация
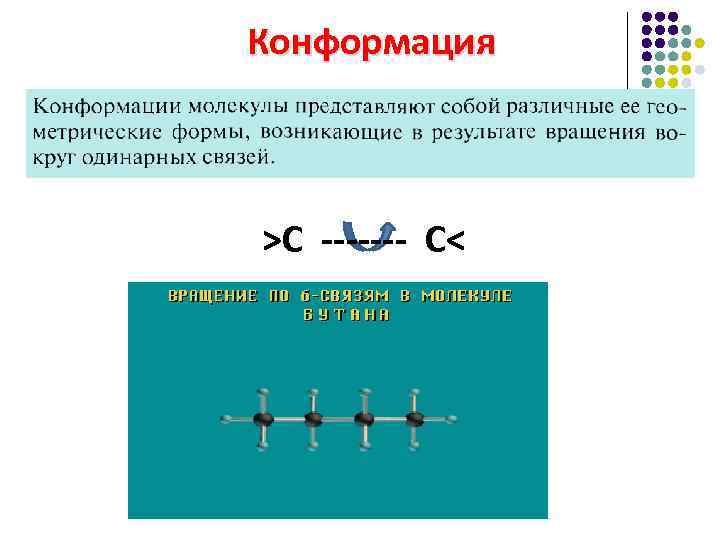 Конформация >С ------- С<
Конформация >С ------- С<
 Геометрическая изомерия Геометрические изомеры – отличаются расположением атомов или групп атомов в пространстве относительно жестких элементов структуры: 1. плоскости двойной связи или малого цикла;
Геометрическая изомерия Геометрические изомеры – отличаются расположением атомов или групп атомов в пространстве относительно жестких элементов структуры: 1. плоскости двойной связи или малого цикла;
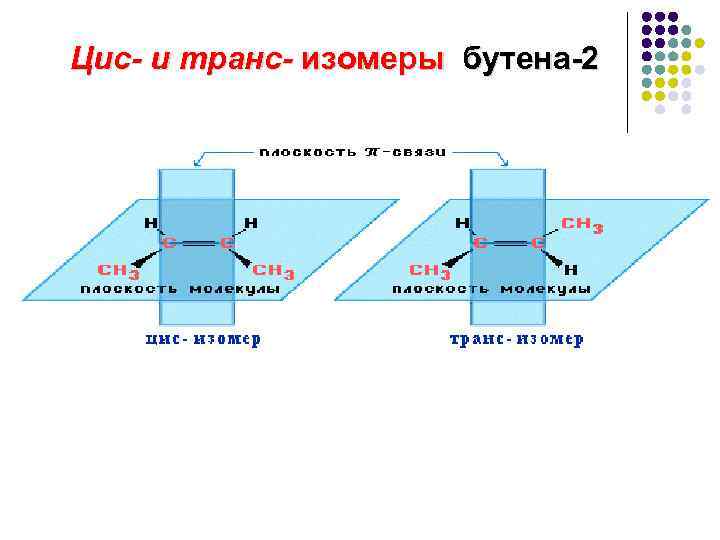 Цис- и транс- изомеры бутена-2
Цис- и транс- изомеры бутена-2
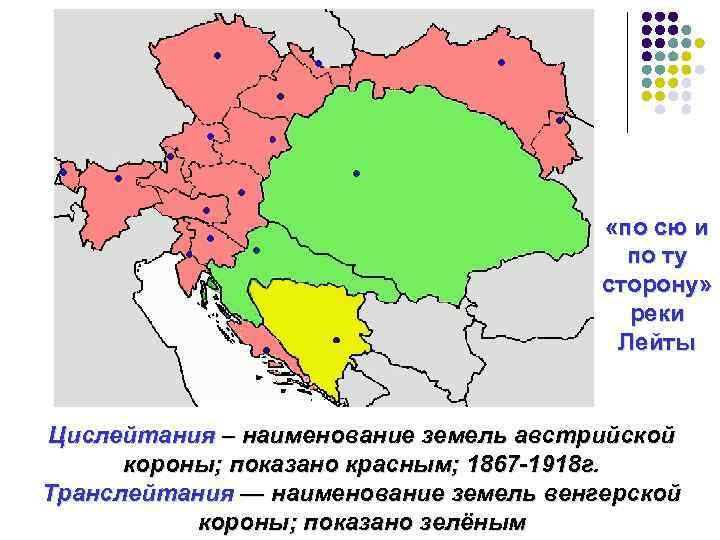 «по сю и по ту сторону» реки Лейты Цислейтания – наименование земель австрийской короны; показано красным; 1867 -1918 г. Транслейтания — наименование земель венгерской короны; показано зелёным
«по сю и по ту сторону» реки Лейты Цислейтания – наименование земель австрийской короны; показано красным; 1867 -1918 г. Транслейтания — наименование земель венгерской короны; показано зелёным
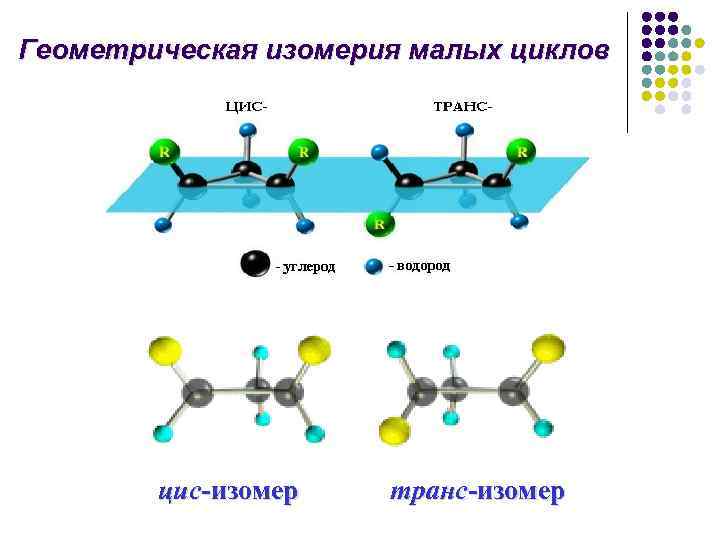 Геометрическая изомерия малых циклов цис-изомер транс-изомер
Геометрическая изомерия малых циклов цис-изомер транс-изомер
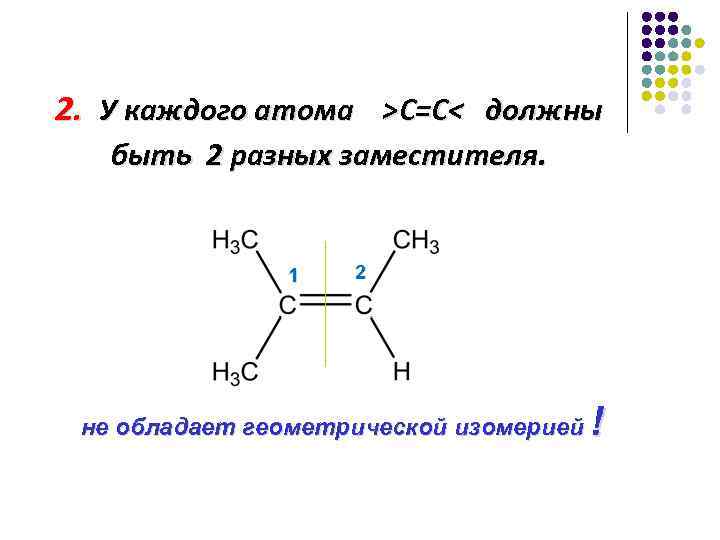 2. У каждого атома >C=C< должны быть 2 разных заместителя. 1 2 не обладает геометрической изомерией !
2. У каждого атома >C=C< должны быть 2 разных заместителя. 1 2 не обладает геометрической изомерией !
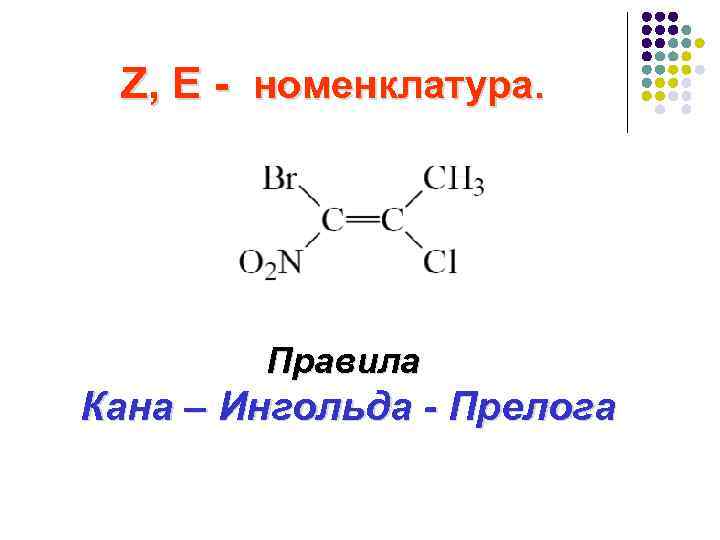 Z, E - номенклатура. Правила Кана – Ингольда - Прелога
Z, E - номенклатура. Правила Кана – Ингольда - Прелога
 Правила старшинства заместителей: 1) Атом с большим атомным номером в ПС является старшим относительно атома с меньшим атомным номером: I > Br > Cl > S > P > F > O > N > C > H ; 2) Если имеются группы атомов, то судят по атомному номеру в ПС первого элемента: -O 8 H > -N 7 H 2 > - C 6 H 3 > H 1 ; 3) Если первые атомы одинаковы, то необходимо провести аналогичное сравнение следующих атомов в группе ( «второго слоя» ): -CH 2 OH > -CH 2 NH 2 > -CH 2 CH 3 > -H.
Правила старшинства заместителей: 1) Атом с большим атомным номером в ПС является старшим относительно атома с меньшим атомным номером: I > Br > Cl > S > P > F > O > N > C > H ; 2) Если имеются группы атомов, то судят по атомному номеру в ПС первого элемента: -O 8 H > -N 7 H 2 > - C 6 H 3 > H 1 ; 3) Если первые атомы одинаковы, то необходимо провести аналогичное сравнение следующих атомов в группе ( «второго слоя» ): -CH 2 OH > -CH 2 NH 2 > -CH 2 CH 3 > -H.
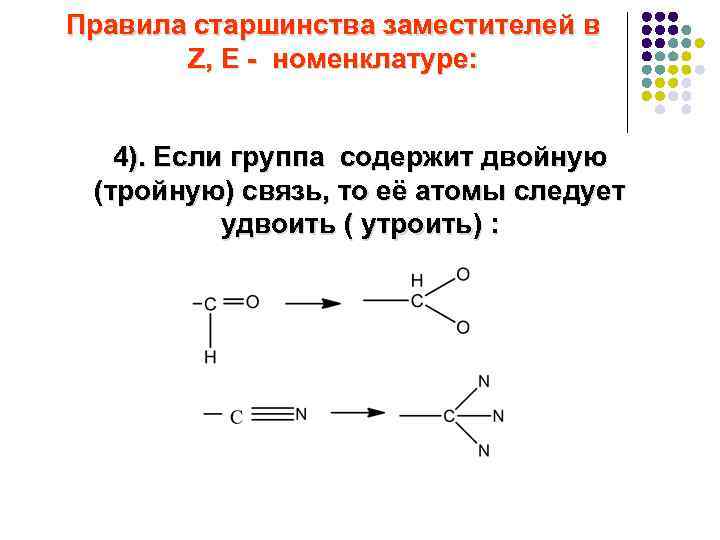 Правила старшинства заместителей в Z, E - номенклатуре: 4). Если группа содержит двойную (тройную) связь, то её атомы следует удвоить ( утроить) :
Правила старшинства заместителей в Z, E - номенклатуре: 4). Если группа содержит двойную (тройную) связь, то её атомы следует удвоить ( утроить) :
 Если две старшие группы расположены по одну сторону от плоскости π-связи, то конфигурация заместителей обозначается символом Z (от нем. zusammen вместе). Если же эти группы находятся по разные стороны от плоскости π-связи, то конфигурацию обозначают символом Е (от нем. entgegen напротив).
Если две старшие группы расположены по одну сторону от плоскости π-связи, то конфигурация заместителей обозначается символом Z (от нем. zusammen вместе). Если же эти группы находятся по разные стороны от плоскости π-связи, то конфигурацию обозначают символом Е (от нем. entgegen напротив).
 Z, E - номенклатура. 1 2 Е - изомер 1 2 Z - изомер
Z, E - номенклатура. 1 2 Е - изомер 1 2 Z - изомер
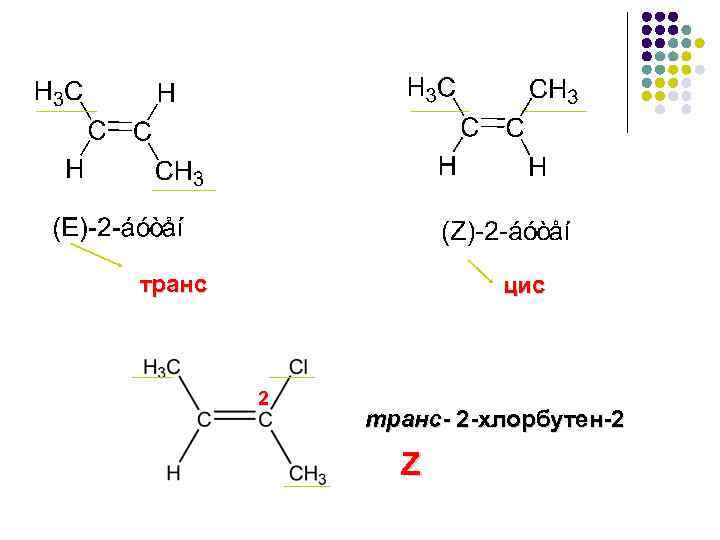 транс цис 2 транс- 2 -хлорбутен-2 Z
транс цис 2 транс- 2 -хлорбутен-2 Z
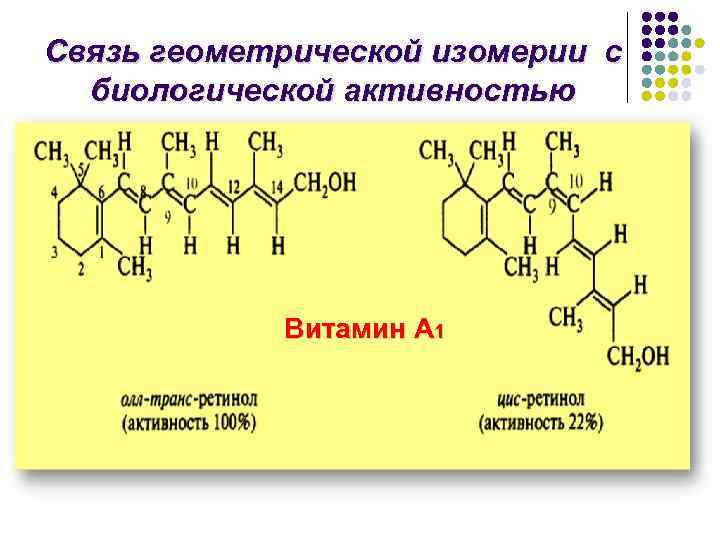 Связь геометрической изомерии с биологической активностью Витамин А 1
Связь геометрической изомерии с биологической активностью Витамин А 1
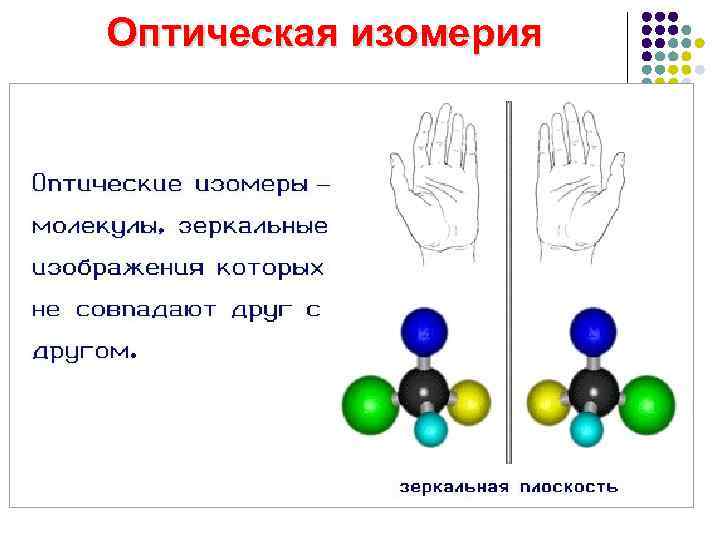 Оптическая изомерия
Оптическая изомерия
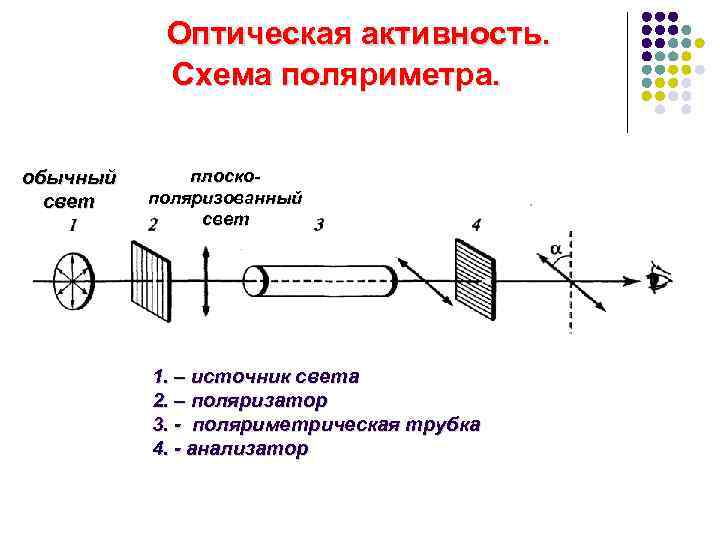 Оптическая активность. Схема поляриметра. обычный свет плоскополяризованный свет 1. – источник света 2. – поляризатор 3. - поляриметрическая трубка 4. - анализатор
Оптическая активность. Схема поляриметра. обычный свет плоскополяризованный свет 1. – источник света 2. – поляризатор 3. - поляриметрическая трубка 4. - анализатор
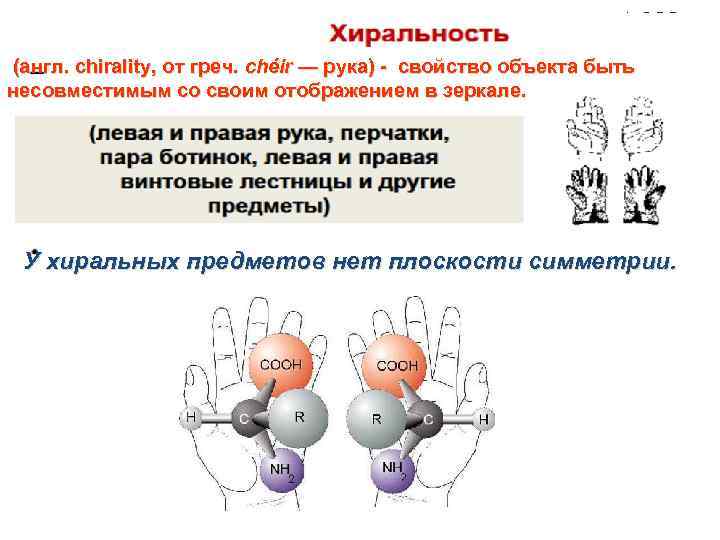 (англ. chirality, от греч. chéir — рука) - свойство объекта быть несовместимым со своим отображением в зеркале. У хиральных предметов нет плоскости симметрии.
(англ. chirality, от греч. chéir — рука) - свойство объекта быть несовместимым со своим отображением в зеркале. У хиральных предметов нет плоскости симметрии.
 С* - атом С в состоянии sp 3 гибридизации, связанный с 4 различными атомами или группами атомов.
С* - атом С в состоянии sp 3 гибридизации, связанный с 4 различными атомами или группами атомов.
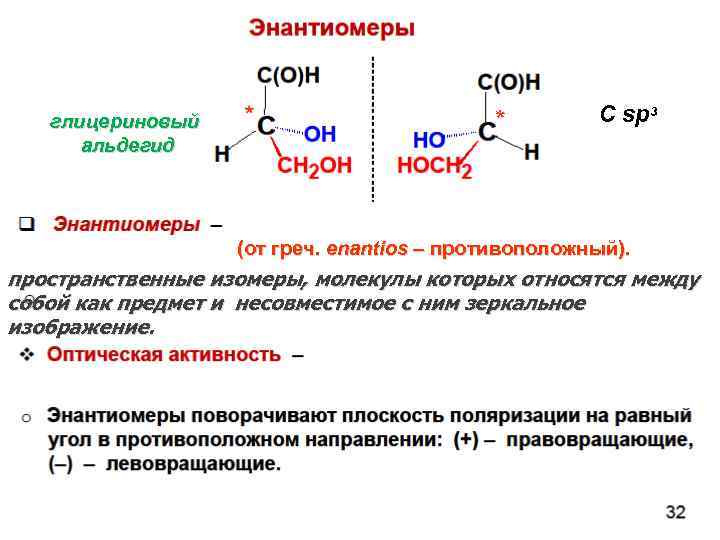 глицериновый альдегид * С sp 3 (от греч. enantios – противоположный). пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
глицериновый альдегид * С sp 3 (от греч. enantios – противоположный). пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
 Фишер (Fischer) Эмиль Герман 1852 – 1919 немецкий химикорганик и биохимик
Фишер (Fischer) Эмиль Герман 1852 – 1919 немецкий химикорганик и биохимик
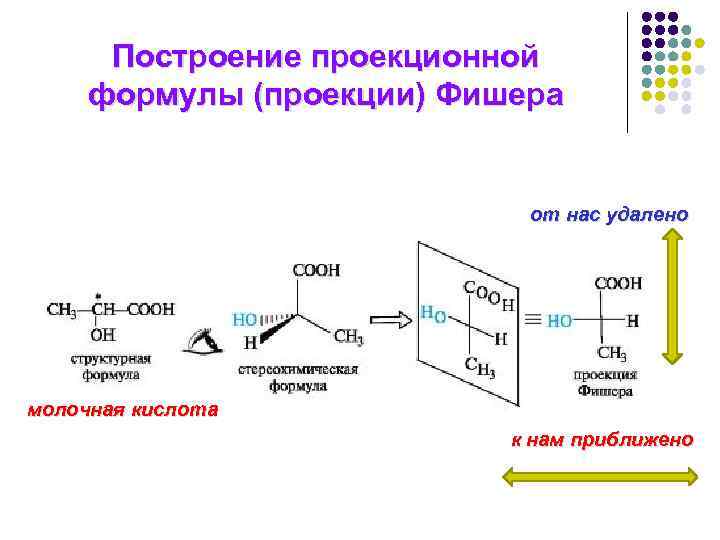 Построение проекционной формулы (проекции) Фишера от нас удалено молочная кислота к нам приближено
Построение проекционной формулы (проекции) Фишера от нас удалено молочная кислота к нам приближено
 Проекции Фишера можно преобразовать: l 1. чётное число перестановок заместителей не меняет формулу; l 2. допускается поворот всей формулы в плоскости чертежа на 180.
Проекции Фишера можно преобразовать: l 1. чётное число перестановок заместителей не меняет формулу; l 2. допускается поворот всей формулы в плоскости чертежа на 180.
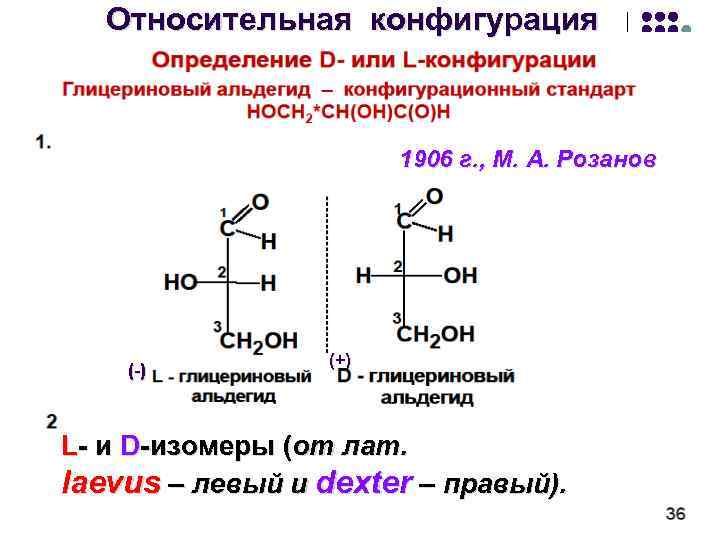 Относительная конфигурация 1906 г. , М. А. Розанов (-) (+) L- и D-изомеры (от лат. laevus – левый и dexter – правый).
Относительная конфигурация 1906 г. , М. А. Розанов (-) (+) L- и D-изомеры (от лат. laevus – левый и dexter – правый).
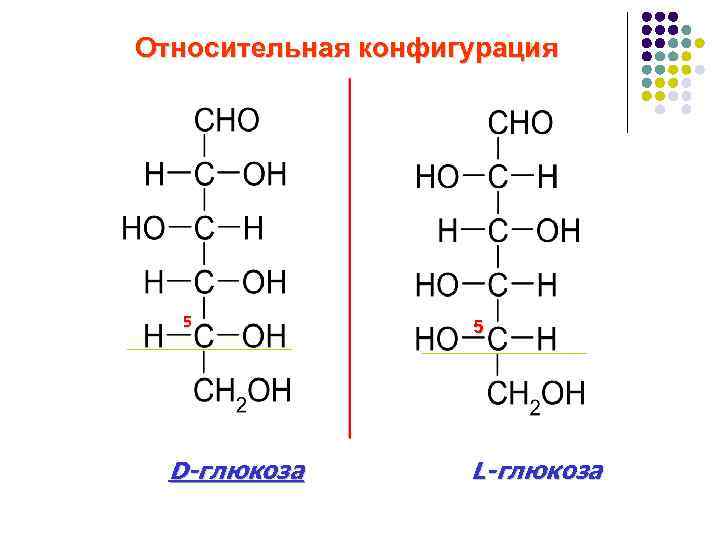 Относительная конфигурация 5 D-глюкоза 5 L-глюкоза
Относительная конфигурация 5 D-глюкоза 5 L-глюкоза
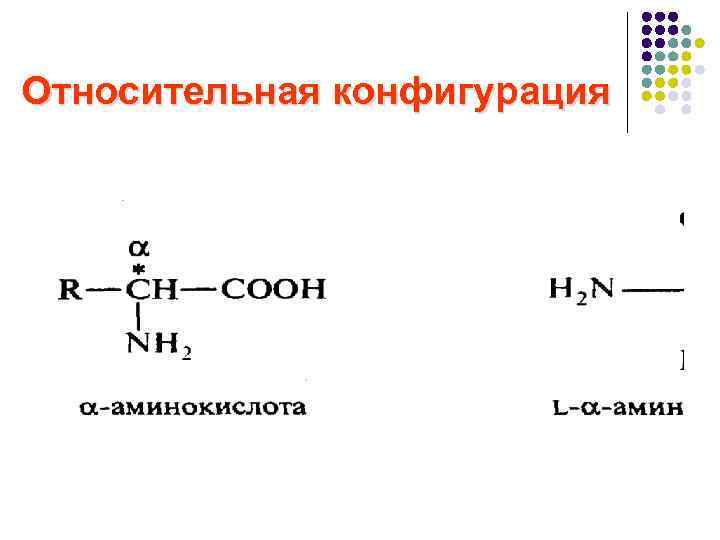 Относительная конфигурация
Относительная конфигурация
 Абсолютная конфигурация Система Кана–Ингольда–Прелога ? Роберт Сидни Кан Ингольд Кристофер (9. 06. 1899 -15. 09. 1981) (Великобритания) Прелог Владимир (28. 10. 1893– 8. 10. 1970) (23. 07. 1906– 07. 01. 1998) (Великобритания) (Швейцария)
Абсолютная конфигурация Система Кана–Ингольда–Прелога ? Роберт Сидни Кан Ингольд Кристофер (9. 06. 1899 -15. 09. 1981) (Великобритания) Прелог Владимир (28. 10. 1893– 8. 10. 1970) (23. 07. 1906– 07. 01. 1998) (Великобритания) (Швейцария)
 Абсолютная конфигурация. R, S – номенклатура (1956). Система Кана-Ингольда-Прелога: 1) определяем старшинство заместителей по атомному № в ПС ( № 1>2>3>4); 2) младший заместитель ( № 4 ) должен быть от нас удален ! 3) определяем падение старшинства заместителей: R R (лат. rectus – правый) S S (от лат. sinister – левый)
Абсолютная конфигурация. R, S – номенклатура (1956). Система Кана-Ингольда-Прелога: 1) определяем старшинство заместителей по атомному № в ПС ( № 1>2>3>4); 2) младший заместитель ( № 4 ) должен быть от нас удален ! 3) определяем падение старшинства заместителей: R R (лат. rectus – правый) S S (от лат. sinister – левый)
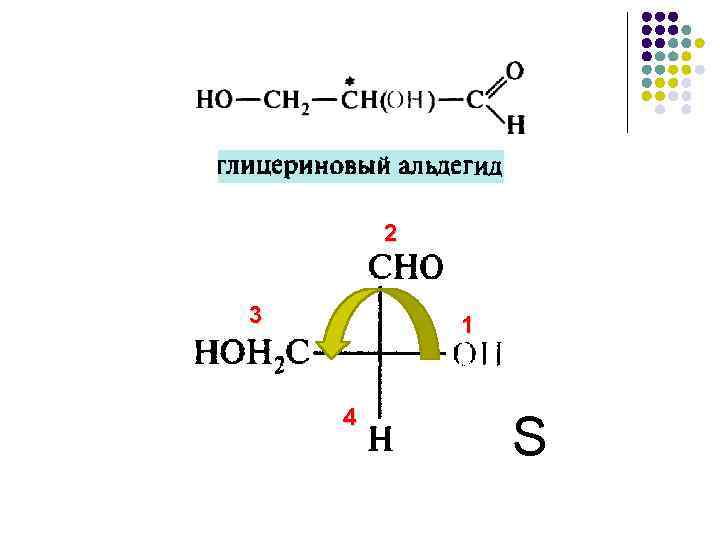 2 3 1 4 S
2 3 1 4 S
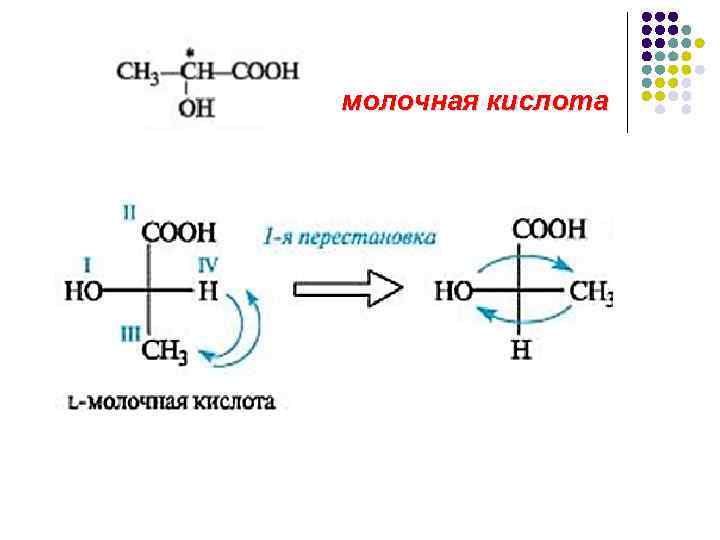 молочная кислота
молочная кислота
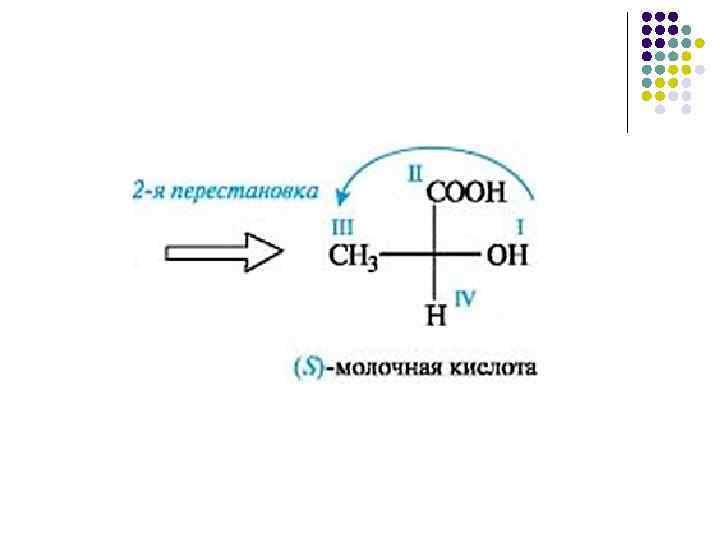
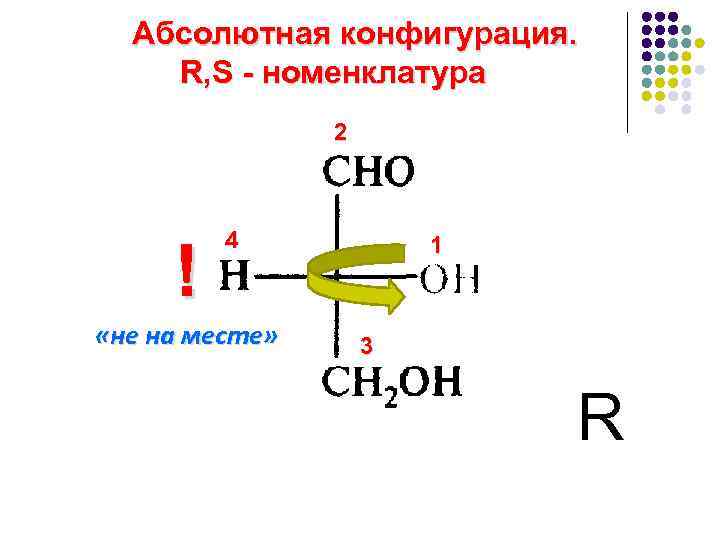 Абсолютная конфигурация. R, S - номенклатура 2 ! 4 «не на месте» 1 3 R
Абсолютная конфигурация. R, S - номенклатура 2 ! 4 «не на месте» 1 3 R
 Соединения с несколькими хиральными центрами. Общее число оптических изомеров определяется формулой N = 2 n , n число центров хиральности.
Соединения с несколькими хиральными центрами. Общее число оптических изомеров определяется формулой N = 2 n , n число центров хиральности.
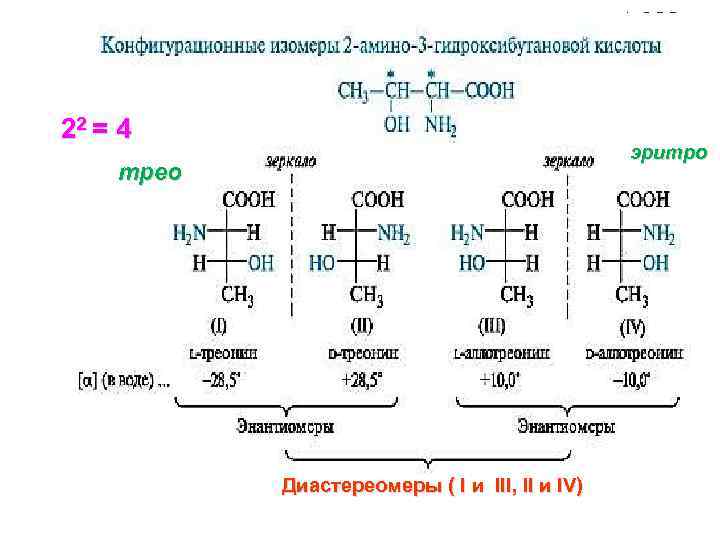 22 = 4 эритро трео Диастереомеры ( I и III, II и IV)
22 = 4 эритро трео Диастереомеры ( I и III, II и IV)
 Диастереомеры стереоизомеры, которые не относятся друг к другу, как предмет и несовместимое с ним зеркальное отражение, т. е. не являются энантиомерами. Эпимеры – диастереомеры, отличающиеся конфигурацией только одного асимметрического центра
Диастереомеры стереоизомеры, которые не относятся друг к другу, как предмет и несовместимое с ним зеркальное отражение, т. е. не являются энантиомерами. Эпимеры – диастереомеры, отличающиеся конфигурацией только одного асимметрического центра
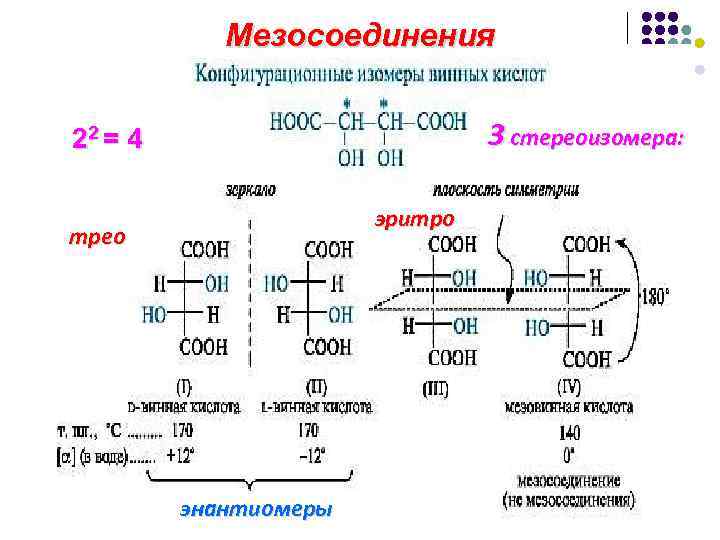 Мезосоединения 3 стереоизомера: 22 = 4 эритро трео энантиомеры
Мезосоединения 3 стереоизомера: 22 = 4 эритро трео энантиомеры
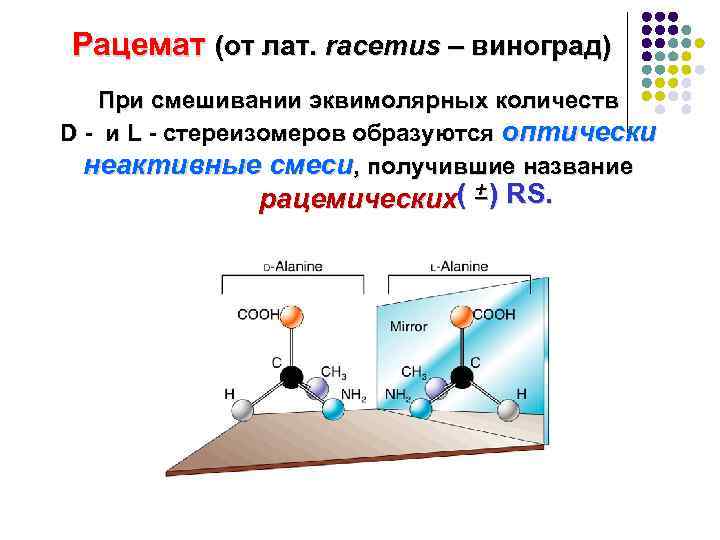 Рацемат (от лат. racemus – виноград) При смешивании эквимолярных количеств D - и L - стереизомеров образуются оптически неактивные смеси, получившие название рацемических( + ) RS. рацемических
Рацемат (от лат. racemus – виноград) При смешивании эквимолярных количеств D - и L - стереизомеров образуются оптически неактивные смеси, получившие название рацемических( + ) RS. рацемических
 ВЗАИМОСВЯЗЬ СТЕРЕОХИМИЧЕСКОГО СТРОЕНИЯ С ПРОЯВЛЕНИЕМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ.
ВЗАИМОСВЯЗЬ СТЕРЕОХИМИЧЕСКОГО СТРОЕНИЯ С ПРОЯВЛЕНИЕМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ.
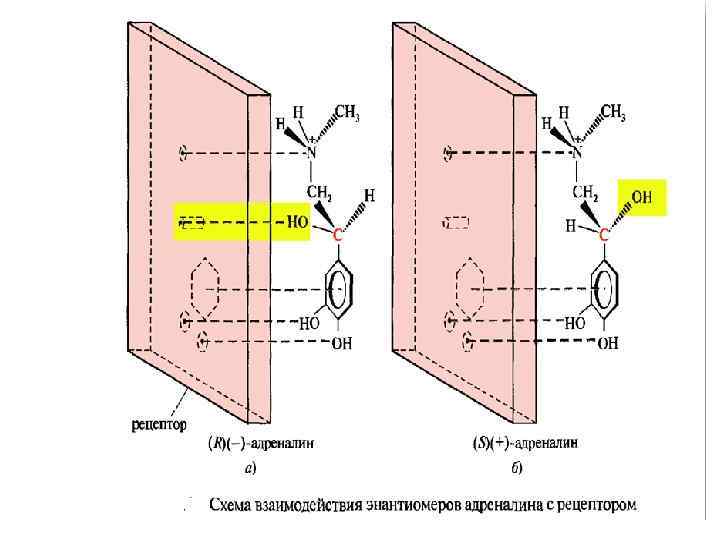
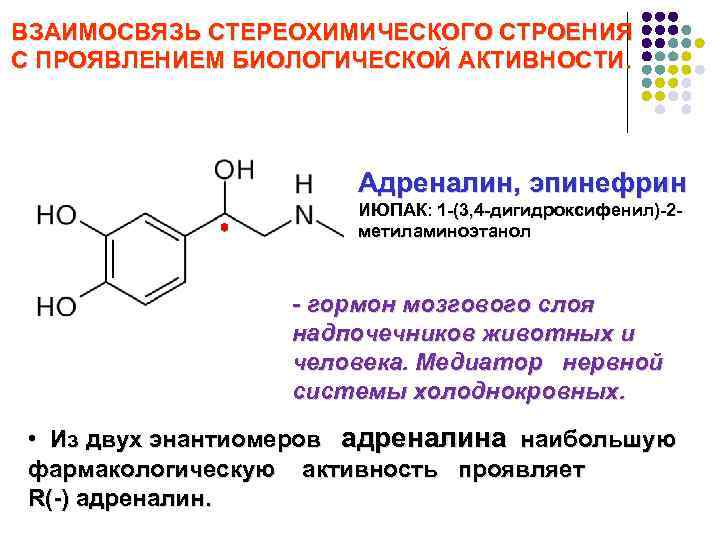 ВЗАИМОСВЯЗЬ СТЕРЕОХИМИЧЕСКОГО СТРОЕНИЯ С ПРОЯВЛЕНИЕМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ. Адреналин, эпинефрин ИЮПАК: 1 -(3, 4 -дигидроксифенил)-2 метиламиноэтанол - гормон мозгового слоя надпочечников животных и человека. Медиатор нервной системы холоднокровных. • Из двух энантиомеров адреналина наибольшую фармакологическую активность проявляет R(-) адреналин.
ВЗАИМОСВЯЗЬ СТЕРЕОХИМИЧЕСКОГО СТРОЕНИЯ С ПРОЯВЛЕНИЕМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ. Адреналин, эпинефрин ИЮПАК: 1 -(3, 4 -дигидроксифенил)-2 метиламиноэтанол - гормон мозгового слоя надпочечников животных и человека. Медиатор нервной системы холоднокровных. • Из двух энантиомеров адреналина наибольшую фармакологическую активность проявляет R(-) адреналин.
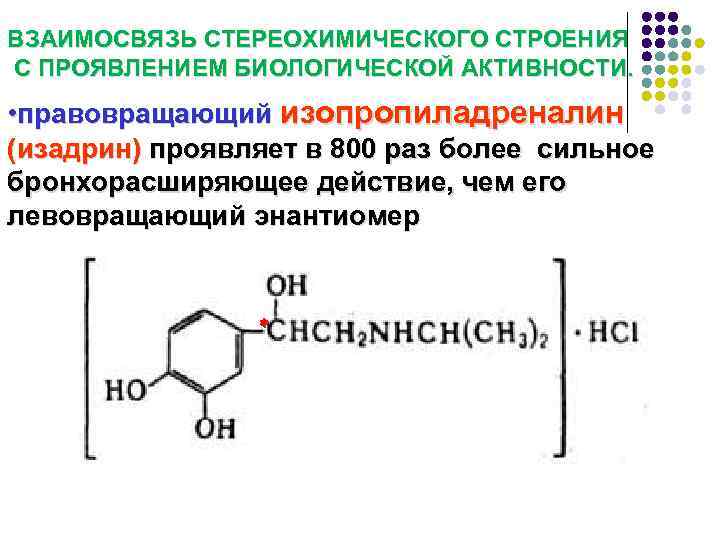 ВЗАИМОСВЯЗЬ СТЕРЕОХИМИЧЕСКОГО СТРОЕНИЯ С ПРОЯВЛЕНИЕМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ. • правовращающий изопропиладреналин (изадрин) проявляет в 800 раз более сильное бронхорасширяющее действие, чем его левовращающий энантиомер
ВЗАИМОСВЯЗЬ СТЕРЕОХИМИЧЕСКОГО СТРОЕНИЯ С ПРОЯВЛЕНИЕМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ. • правовращающий изопропиладреналин (изадрин) проявляет в 800 раз более сильное бронхорасширяющее действие, чем его левовращающий энантиомер
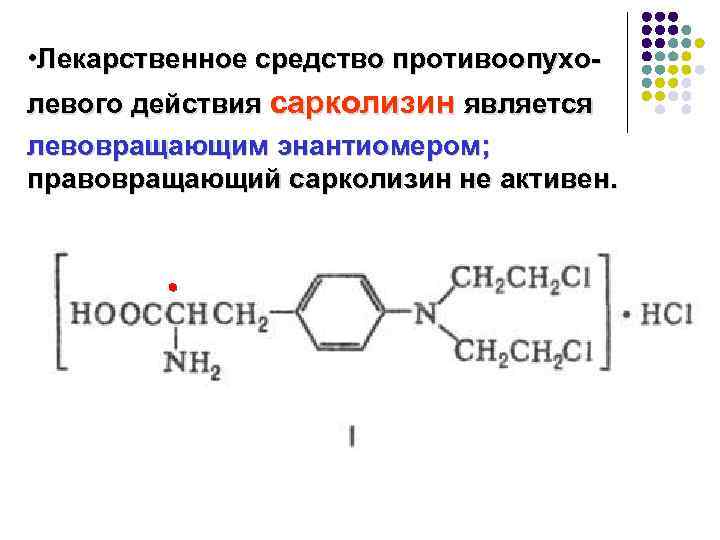 • Лекарственное средство противоопухолевого действия сарколизин является левовращающим энантиомером; правовращающий сарколизин не активен.
• Лекарственное средство противоопухолевого действия сарколизин является левовращающим энантиомером; правовращающий сарколизин не активен.
 «Жизнь – это особая форма существования биополимерных тел (систем), характеризующихся хиральной чистотой и способностью к самоорганизации и саморепликации в условиях постоянного обмена с окружающей средой веществом, энергией и информацией» (акад. В. Гольданский, 1986 г. ) Виталий Иосифович Гольданский
«Жизнь – это особая форма существования биополимерных тел (систем), характеризующихся хиральной чистотой и способностью к самоорганизации и саморепликации в условиях постоянного обмена с окружающей средой веществом, энергией и информацией» (акад. В. Гольданский, 1986 г. ) Виталий Иосифович Гольданский
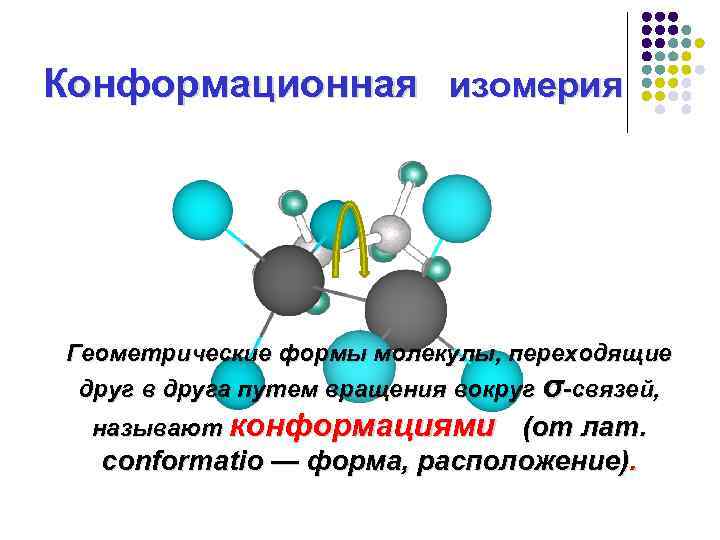 Конформационная изомерия Геометрические формы молекулы, переходящие друг в друга путем вращения вокруг σ-связей, называют конформациями (от лат. conformatio — форма, расположение).
Конформационная изомерия Геометрические формы молекулы, переходящие друг в друга путем вращения вокруг σ-связей, называют конформациями (от лат. conformatio — форма, расположение).
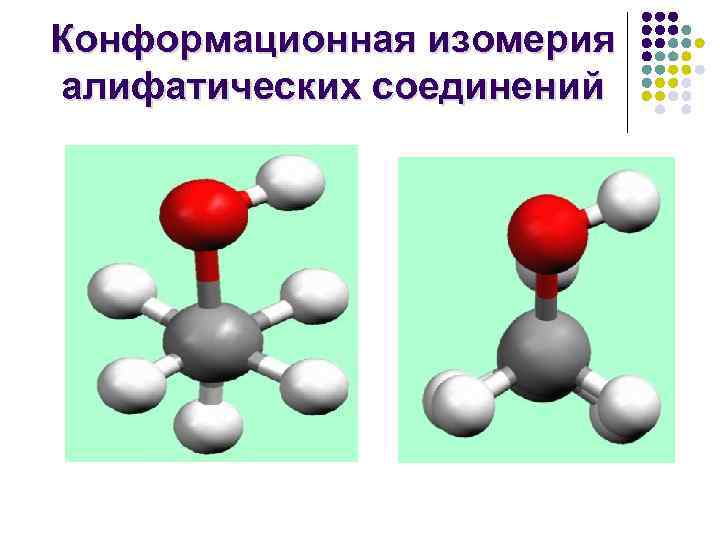 Конформационная изомерия алифатических соединений
Конформационная изомерия алифатических соединений
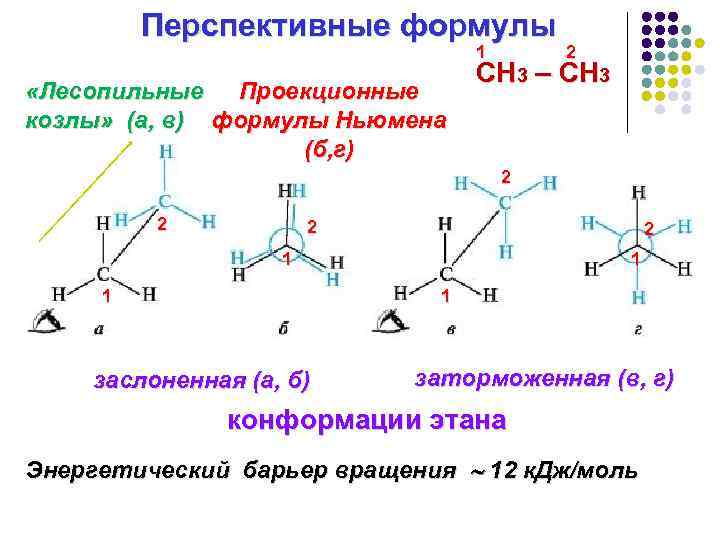 Перспективные формулы 1 «Лесопильные Проекционные козлы» (а, в) формулы Ньюмена (б, г) 2 СН 3 – СН 3 2 2 1 1 заслоненная (а, б) заторможенная (в, г) конформации этана Энергетический барьер вращения 12 к. Дж/моль
Перспективные формулы 1 «Лесопильные Проекционные козлы» (а, в) формулы Ньюмена (б, г) 2 СН 3 – СН 3 2 2 1 1 заслоненная (а, б) заторможенная (в, г) конформации этана Энергетический барьер вращения 12 к. Дж/моль
 Торсионное напряжение увеличение энергии (Е) молекулы, вызванное заслонённым положением σ связей ( С - Н ). Ван-дер-Ваальсово напряжение – обусловлено силами отталкивания между валентно не связанными большими по объёму заместителями. -
Торсионное напряжение увеличение энергии (Е) молекулы, вызванное заслонённым положением σ связей ( С - Н ). Ван-дер-Ваальсово напряжение – обусловлено силами отталкивания между валентно не связанными большими по объёму заместителями. -
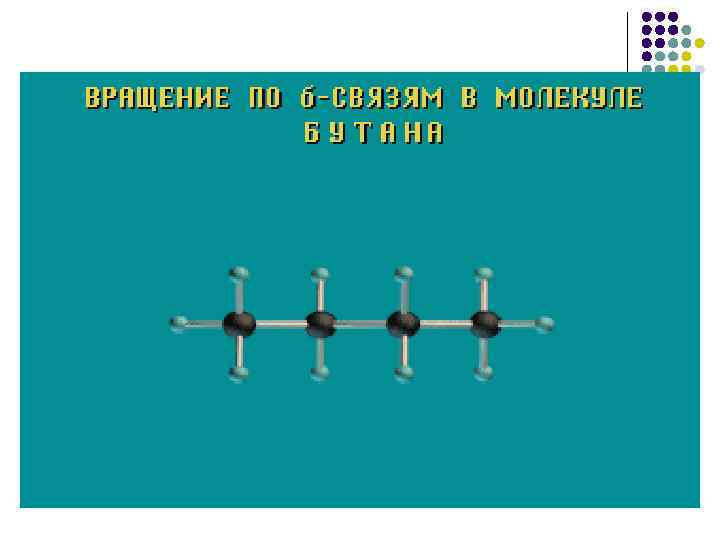
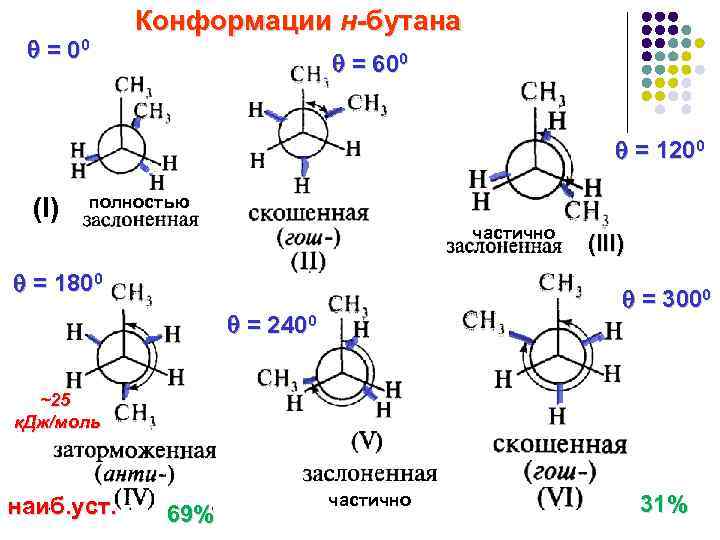 = 00 Конформации н-бутана = 600 = 1200 (I) полностью частично = 1800 (III) = 3000 = 2400 ~25 к. Дж/моль наиб. уст. 69% частично 31%
= 00 Конформации н-бутана = 600 = 1200 (I) полностью частично = 1800 (III) = 3000 = 2400 ~25 к. Дж/моль наиб. уст. 69% частично 31%
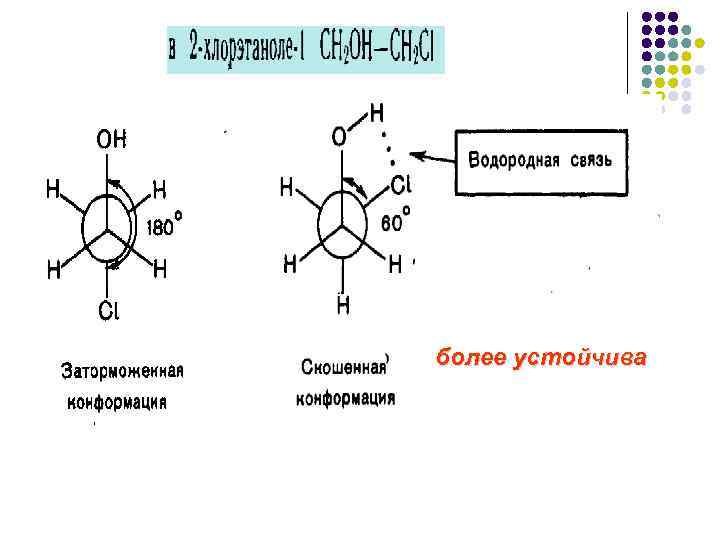 более устойчива
более устойчива
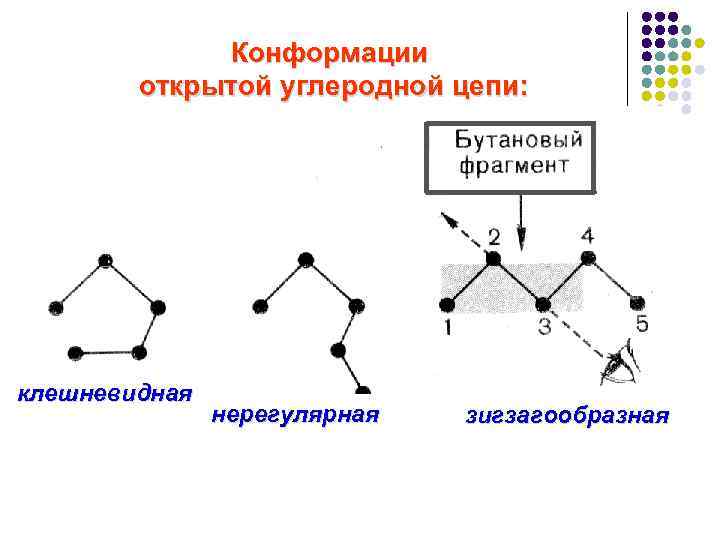 Конформации открытой углеродной цепи: клешневидная нерегулярная зигзагообразная
Конформации открытой углеродной цепи: клешневидная нерегулярная зигзагообразная
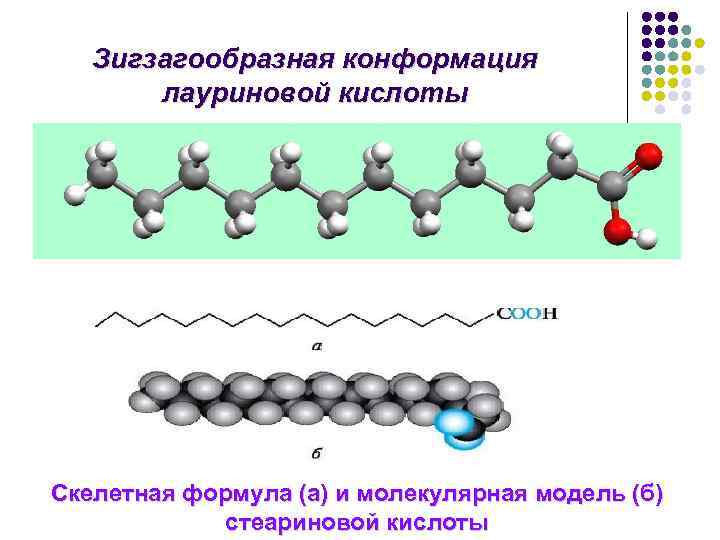 Зигзагообразная конформация лауриновой кислоты Скелетная формула (а) и молекулярная модель (б) стеариновой кислоты
Зигзагообразная конформация лауриновой кислоты Скелетная формула (а) и молекулярная модель (б) стеариновой кислоты
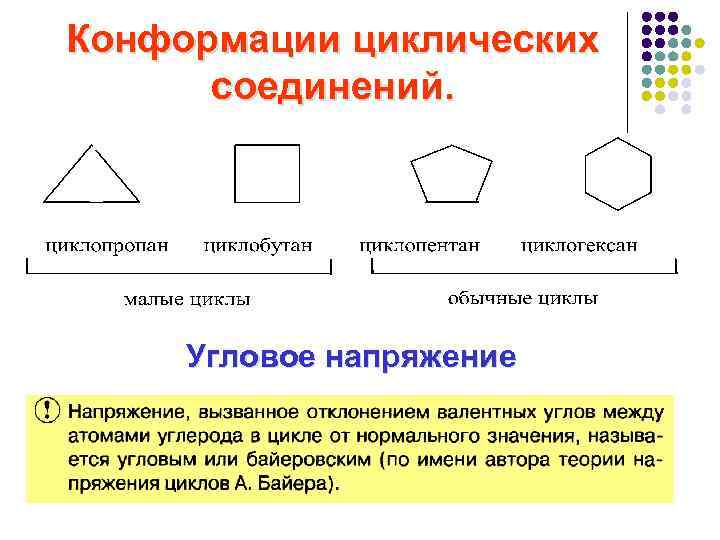 Конформации циклических соединений. Угловое напряжение
Конформации циклических соединений. Угловое напряжение
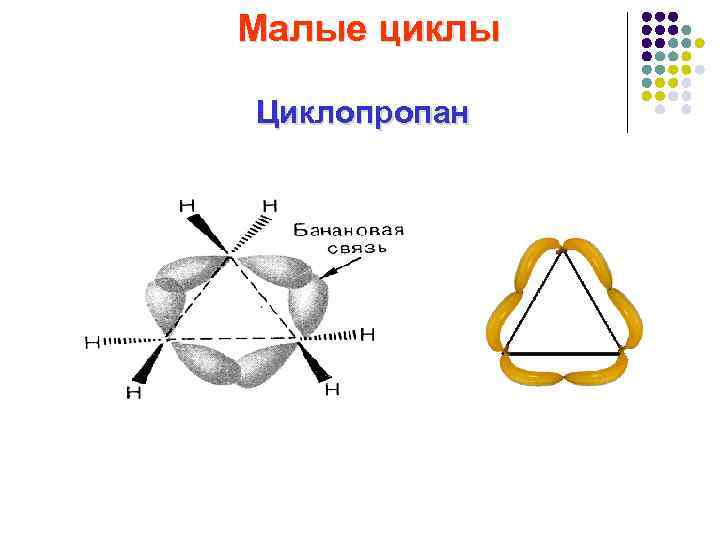 Малые циклы Циклопропан
Малые циклы Циклопропан
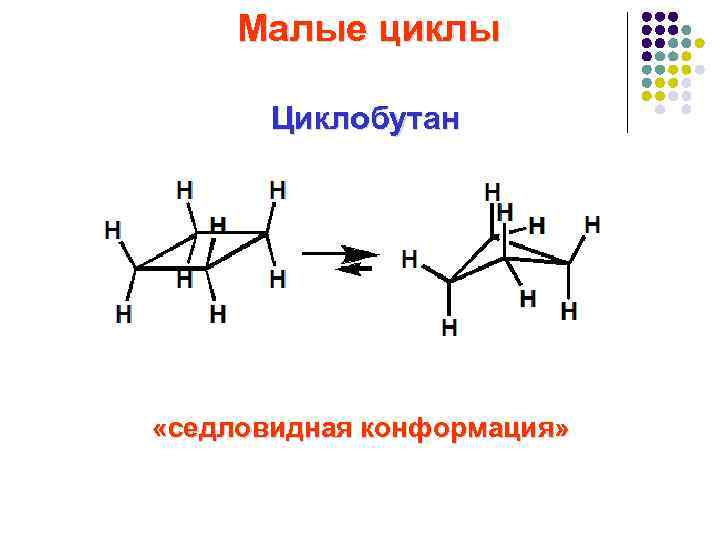 Малые циклы Циклобутан «седловидная конформация»
Малые циклы Циклобутан «седловидная конформация»

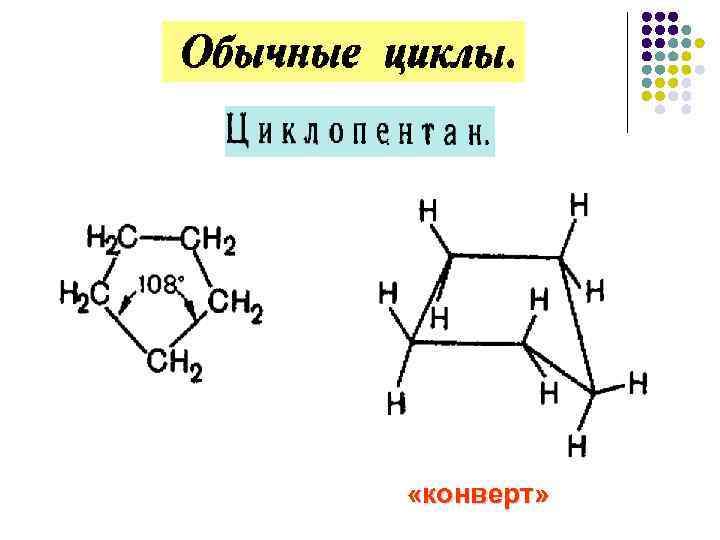 «конверт»
«конверт»
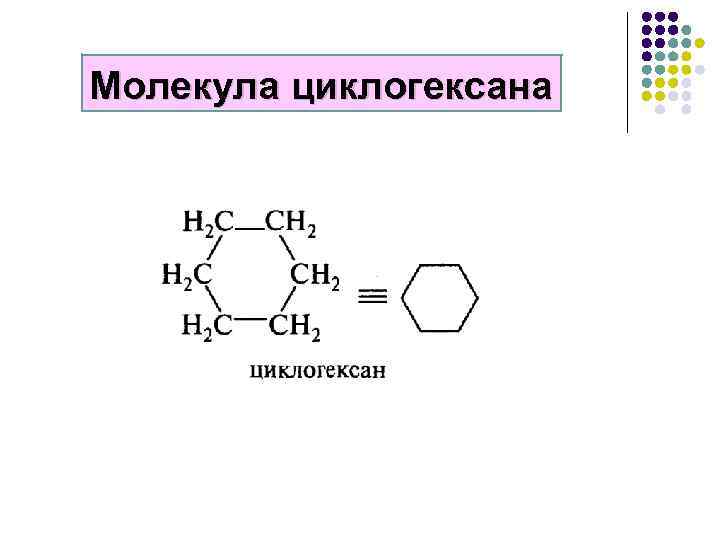 Молекула циклогексана
Молекула циклогексана
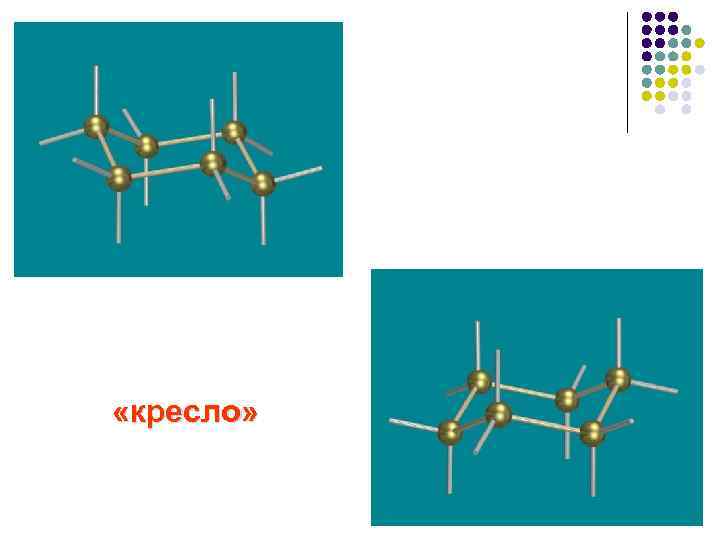 «кресло»
«кресло»
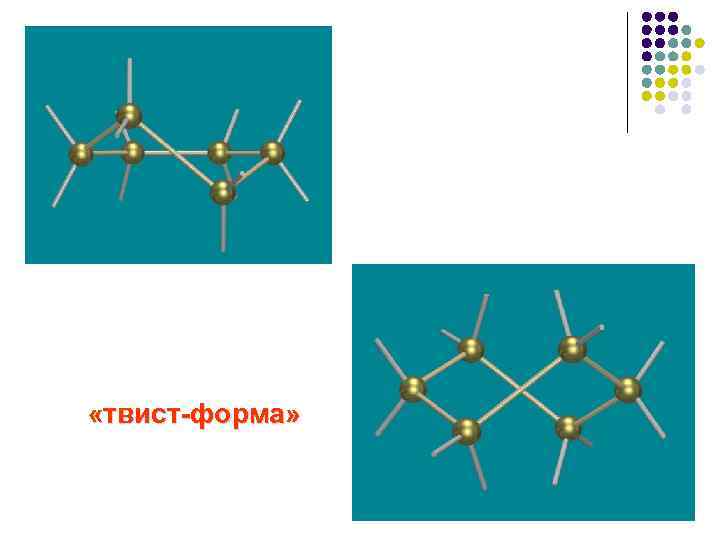 «твист-форма»
«твист-форма»
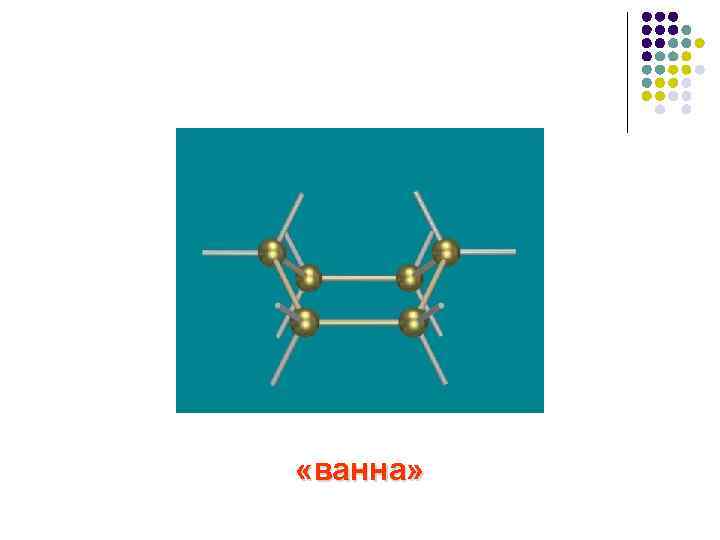 «ванна»
«ванна»
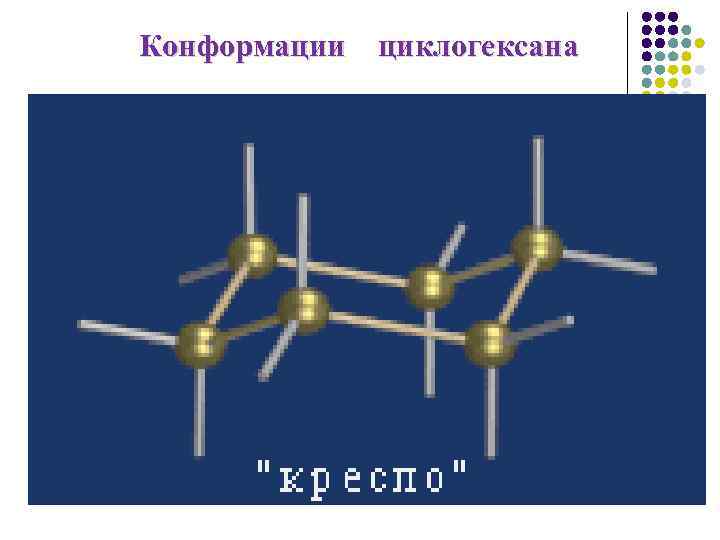 Конформации циклогексана
Конформации циклогексана
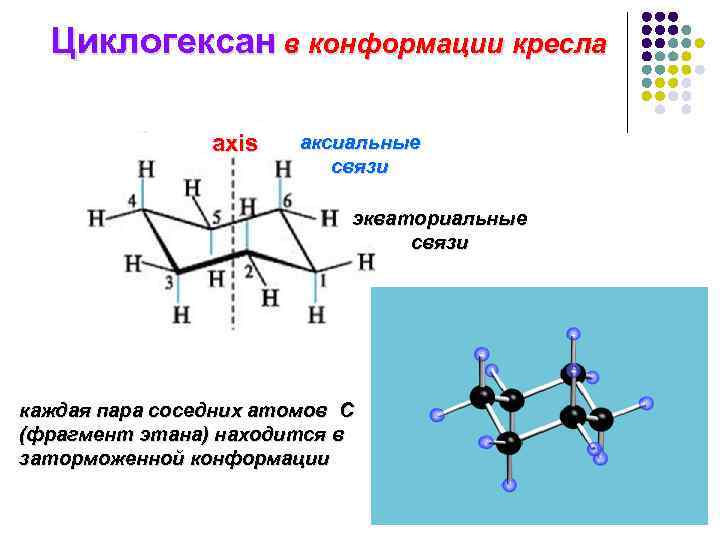 Циклогексан в конформации кресла axis аксиальные связи экваториальные связи каждая пара соседних атомов С (фрагмент этана) находится в заторможенной конформации
Циклогексан в конформации кресла axis аксиальные связи экваториальные связи каждая пара соседних атомов С (фрагмент этана) находится в заторможенной конформации
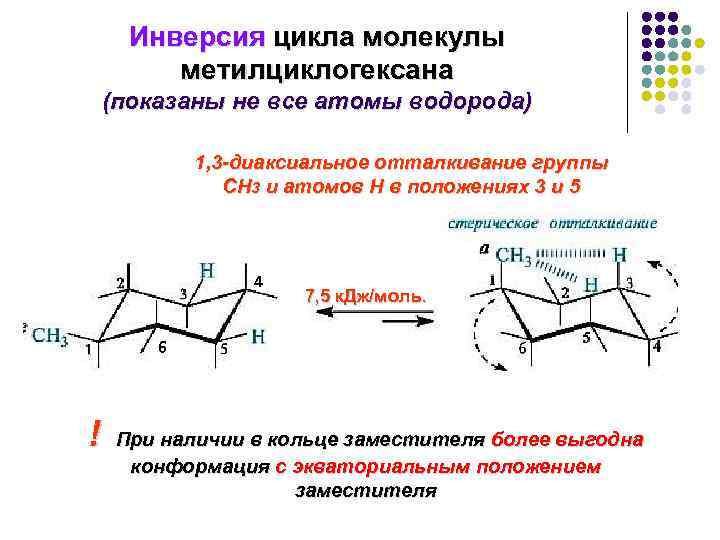 Инверсия цикла молекулы метилциклогексана (показаны не все атомы водорода) 1, 3 -диаксиальное отталкивание группы СН 3 и атомов Н в положениях 3 и 5 4 7, 5 к. Дж/моль. 6 ! При наличии в кольце заместителя более выгодна конформация с экваториальным положением заместителя
Инверсия цикла молекулы метилциклогексана (показаны не все атомы водорода) 1, 3 -диаксиальное отталкивание группы СН 3 и атомов Н в положениях 3 и 5 4 7, 5 к. Дж/моль. 6 ! При наличии в кольце заместителя более выгодна конформация с экваториальным положением заместителя
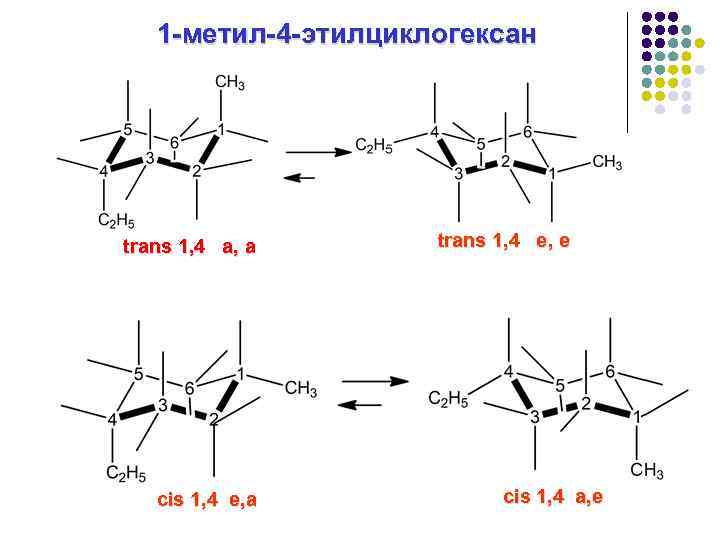 1 -метил-4 -этилциклогексан trans 1, 4 a, a cis 1, 4 e, a trans 1, 4 e, e cis 1, 4 a, e
1 -метил-4 -этилциклогексан trans 1, 4 a, a cis 1, 4 e, a trans 1, 4 e, e cis 1, 4 a, e
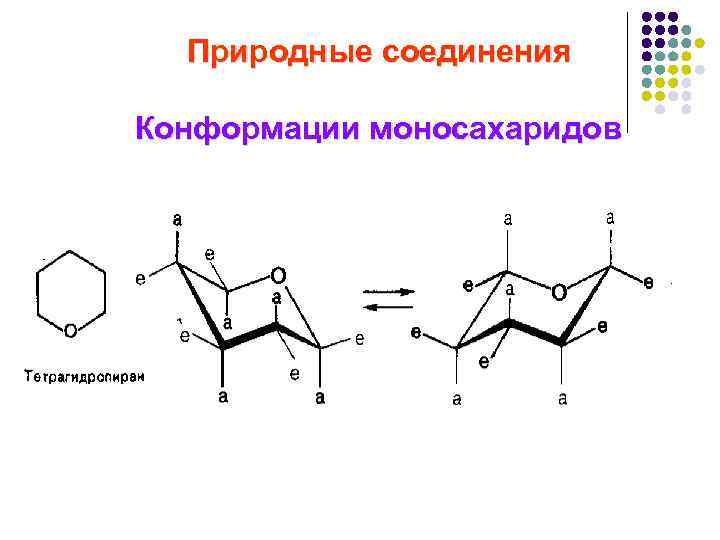 Природные соединения Конформации моносахаридов
Природные соединения Конформации моносахаридов
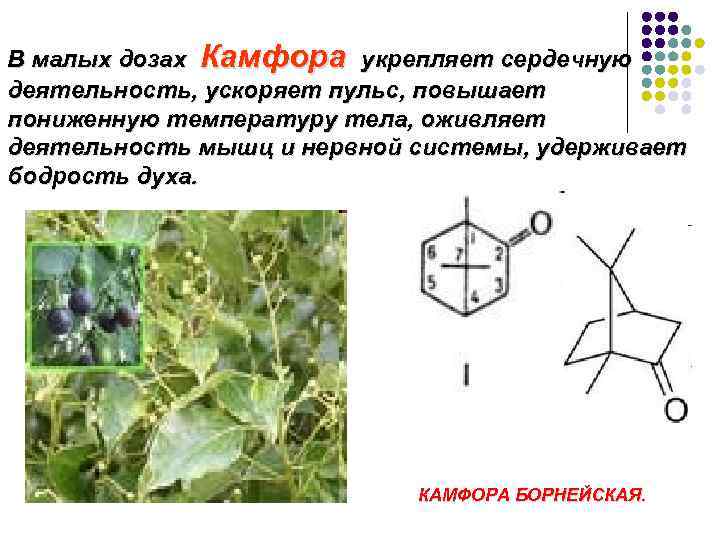 В малых дозах Камфора укрепляет сердечную деятельность, ускоряет пульс, повышает пониженную температуру тела, оживляет деятельность мышц и нервной системы, удерживает бодрость духа. КАМФОРА БОРНЕЙСКАЯ.
В малых дозах Камфора укрепляет сердечную деятельность, ускоряет пульс, повышает пониженную температуру тела, оживляет деятельность мышц и нервной системы, удерживает бодрость духа. КАМФОРА БОРНЕЙСКАЯ.
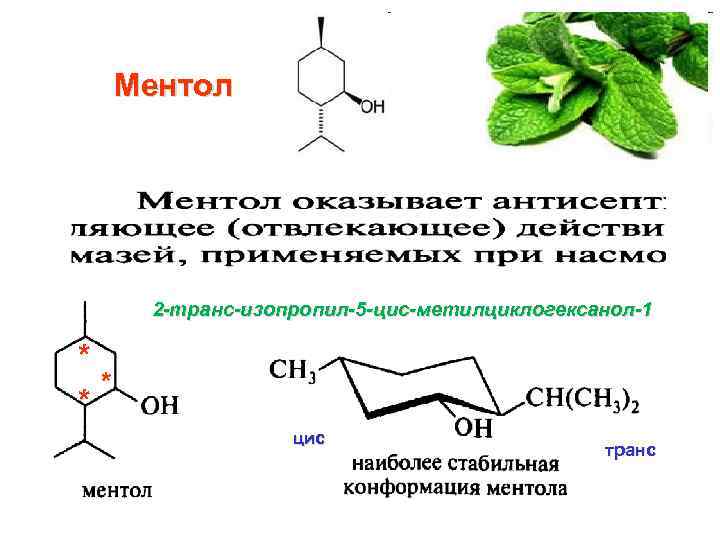 Ментол 2 -транс-изопропил-5 -цис-метилциклогексанол-1 * * * цис транс
Ментол 2 -транс-изопропил-5 -цис-метилциклогексанол-1 * * * цис транс



