Экол_хим_2_SNP.ppt
- Количество слайдов: 28
 Лекция 2 Соединения серы, азота, фосфора Элементы V и VI групп периодической таблицы играют важную роль в химических и биохимических почвенных процессах. Азот и сера являются необходимыми элементами для формирования белков, фосфор играет важную роль в энергетических процессах. Сера, азот, фосфор – типичные органогены. Соотношение между ними в гумусовых горизонтах почв одного типа относительно постоянное. Так, в органическом веществе: отношение C: N меняется от 8 до 15, содержание органического Р в 4 -5 раз меньше, чем содержание N, а отношение С: Р составляет 100: 1. В живых организмах содержится: 0, 3% азота, 0. 07% фосфора, 0. 05% серы; в золе растений – 7% Р и 5% S. Азот накапливается преимущественно в живых организмах и почвах, но не в осадочных или изверженных породах. Это обусловлено неустойчивостью соеди-нений азота вне живых организмов, их быстрым разложением, минерализацией и активной миграцией в биосфере. В почвах азот связан с живым органическим веществом или гумусом. Фосфор и сера образуют трудно растворимые соединения, такие как гипс, фосфориты. Пройдя через стадию аккумуляции в организмах, они накапливаются не только в толще почв, но и в осадочных породах. Сера, азот, фосфор – типичные неметаллы с большим числом валентных электронов, геохимическая общность рассматриваемой группы элементов проявляется в том, что их миграция и аккумуляция, подвижность и реакционная способность зависят от присутствия органических веществ, окислительно-восстановительных и кислотно-основных условий.
Лекция 2 Соединения серы, азота, фосфора Элементы V и VI групп периодической таблицы играют важную роль в химических и биохимических почвенных процессах. Азот и сера являются необходимыми элементами для формирования белков, фосфор играет важную роль в энергетических процессах. Сера, азот, фосфор – типичные органогены. Соотношение между ними в гумусовых горизонтах почв одного типа относительно постоянное. Так, в органическом веществе: отношение C: N меняется от 8 до 15, содержание органического Р в 4 -5 раз меньше, чем содержание N, а отношение С: Р составляет 100: 1. В живых организмах содержится: 0, 3% азота, 0. 07% фосфора, 0. 05% серы; в золе растений – 7% Р и 5% S. Азот накапливается преимущественно в живых организмах и почвах, но не в осадочных или изверженных породах. Это обусловлено неустойчивостью соеди-нений азота вне живых организмов, их быстрым разложением, минерализацией и активной миграцией в биосфере. В почвах азот связан с живым органическим веществом или гумусом. Фосфор и сера образуют трудно растворимые соединения, такие как гипс, фосфориты. Пройдя через стадию аккумуляции в организмах, они накапливаются не только в толще почв, но и в осадочных породах. Сера, азот, фосфор – типичные неметаллы с большим числом валентных электронов, геохимическая общность рассматриваемой группы элементов проявляется в том, что их миграция и аккумуляция, подвижность и реакционная способность зависят от присутствия органических веществ, окислительно-восстановительных и кислотно-основных условий.
 Сера (S) Естественные и антропогенные источники Природные источники. Сера - S - характерный представитель группы активно дегазируемых элементов. В то же время поступление серы в атмосферу по сравнению инертными газами и СО 2 сильно затруднено. Это связано со следующими обстоятельствами. Среди газообразных соединений серы, выделяющихся с вулканическими газами, наиболее распространенными являются диоксид серы (SO 2) и сероводород (H 2 S). В процессе активного дегазирования мантии и прохождения через толщи горных пород газы растворяются в подземных водах. При этом H 2 S активно восстанавливает тяжелые металлы, образуя трудно растворимые сульфиды, главным образом дисульфид железа ( пирит – Fe. S 2), а SO 2 частично связывается в составе также плохо растворимых сульфатов кальция, бария, стронция (Ca. SO 4 и т. д. ). В результате указанных реакций значительная часть дегазируемых соединений серы трансформируется в твердые минералы, среди которых наиболее распространен пирит. Часть диффундирующих через земную кору газообразных соединений серы, а также сернистые газы вулканических выбросов и газово-жидких выделений наземных и подводных гидротерм поступает в систему Мирового океана и педосферу. При этом значительная часть газов захватывается бактериями в своеобразный микробиологический круговорот. Таким образом, дегазируемые соединения серы по пути в атмосферу должны преодолевать двойной фильтр: физико-химический в земной коре и биогеохимический на поверхности Мировой суши и в океане.
Сера (S) Естественные и антропогенные источники Природные источники. Сера - S - характерный представитель группы активно дегазируемых элементов. В то же время поступление серы в атмосферу по сравнению инертными газами и СО 2 сильно затруднено. Это связано со следующими обстоятельствами. Среди газообразных соединений серы, выделяющихся с вулканическими газами, наиболее распространенными являются диоксид серы (SO 2) и сероводород (H 2 S). В процессе активного дегазирования мантии и прохождения через толщи горных пород газы растворяются в подземных водах. При этом H 2 S активно восстанавливает тяжелые металлы, образуя трудно растворимые сульфиды, главным образом дисульфид железа ( пирит – Fe. S 2), а SO 2 частично связывается в составе также плохо растворимых сульфатов кальция, бария, стронция (Ca. SO 4 и т. д. ). В результате указанных реакций значительная часть дегазируемых соединений серы трансформируется в твердые минералы, среди которых наиболее распространен пирит. Часть диффундирующих через земную кору газообразных соединений серы, а также сернистые газы вулканических выбросов и газово-жидких выделений наземных и подводных гидротерм поступает в систему Мирового океана и педосферу. При этом значительная часть газов захватывается бактериями в своеобразный микробиологический круговорот. Таким образом, дегазируемые соединения серы по пути в атмосферу должны преодолевать двойной фильтр: физико-химический в земной коре и биогеохимический на поверхности Мировой суши и в океане.
 Несмотря на интенсивное дегазирование серы из недр Земли, природные уровни концентрации сернистых газов (H 2 S; SO 2) в атмосфере весьма незначительны благодаря активному связыванию этого элемента в земной коре, гидросфере и живом веществе. Содержание H 2 S и SO 2 в атмосфере очень непостоянно. С учетом вклада антропогенных факторов концентрация каждого из газов в атмосфере оценивается около 2 10 -8%. К природным источникам SO 2 относят также • лесные пожары, • морскую пену, • микробиологические превращения серосодержащих соединений. Антропогенные источники. Диоксид серы - SO 2 - антропогенного происхождения образуется при сгорании угля и нефти, в металлургических производствах, при переработке содержащих серу руд, при различных химических технологических процессах. Большая часть антропогенных выбросов SO 2 - около 87% - связана с энергетикой и промышленностью. Только в ФРГ по приблизительной оценке ежегодно в атмосферу выбрасывается 3 -4 млн. т SO 2, что почти в два раза больше количества SO 2 естественного происхождения, поступающего в атмосферу на всей планете. Диоксид серы составляет более 95% всех техногенных выбросов серосодержащих веществ в атмосферу. Для атмосферы основным источником восстановленной серы служит биота океанов и континентов. Основное соединение серы (+2, H 2 S), выделяющееся из морской воды – диметилсульфид (СН 3 SСН 3); континентальные источники, кроме этого вещества, продуцируют значительные количества CS 2 (сероуглерод), COS (карбонилсульфид) и H 2 S, а также меркаптанов RSH.
Несмотря на интенсивное дегазирование серы из недр Земли, природные уровни концентрации сернистых газов (H 2 S; SO 2) в атмосфере весьма незначительны благодаря активному связыванию этого элемента в земной коре, гидросфере и живом веществе. Содержание H 2 S и SO 2 в атмосфере очень непостоянно. С учетом вклада антропогенных факторов концентрация каждого из газов в атмосфере оценивается около 2 10 -8%. К природным источникам SO 2 относят также • лесные пожары, • морскую пену, • микробиологические превращения серосодержащих соединений. Антропогенные источники. Диоксид серы - SO 2 - антропогенного происхождения образуется при сгорании угля и нефти, в металлургических производствах, при переработке содержащих серу руд, при различных химических технологических процессах. Большая часть антропогенных выбросов SO 2 - около 87% - связана с энергетикой и промышленностью. Только в ФРГ по приблизительной оценке ежегодно в атмосферу выбрасывается 3 -4 млн. т SO 2, что почти в два раза больше количества SO 2 естественного происхождения, поступающего в атмосферу на всей планете. Диоксид серы составляет более 95% всех техногенных выбросов серосодержащих веществ в атмосферу. Для атмосферы основным источником восстановленной серы служит биота океанов и континентов. Основное соединение серы (+2, H 2 S), выделяющееся из морской воды – диметилсульфид (СН 3 SСН 3); континентальные источники, кроме этого вещества, продуцируют значительные количества CS 2 (сероуглерод), COS (карбонилсульфид) и H 2 S, а также меркаптанов RSH.
 Поведение соединений серы в биосфере Атмосфера. В природе сера проявляет все известные для нее степени окисления (-2), (+4), (+6). Это обусловливает существенную роль окислительно-восстановительных реакций и разнообразие процессов миграции. В отличие от СО 2, оказывающего влияние в основном только на распределение энергии в атмосфере (благодаря поглощению ИК-лучей), диоксид серы SO 2 может оказать и прямое токсическое действие на живые организмы. Кроме того, реакционная способность SO 2 значительно выше, чем у СО 2. Время пребывания SO 2 в атмосфере в среднем исчисляется двумя неделями. Этот промежуток времени слишком мал, чтобы газ мог распространяться в глобальном масштабе. Во время переноса диоксид серы лишь в очень малой степени теряет свою химическую активность. Сток SO 2 из атмосферы. 1 - Нейтрализация может происходить лишь в том случае, если в воздухе, одновременно с SO 2 находится пыль, содержащая гидроксиды щелочных и щелочноземельных металлов. Атмосфера очищается от SO 2 главным образом при - 2 - вымывании кислых газов водой или снегом ( «мокрое» осаждение, «кислотные дожди» ), а также при – 3 - их «сухом» осаждении, т. е. в виде самого газа, адсорбированного на мельчайших частицах пыли. Кроме того, - 4 - диоксид серы растворяется в мельчайших капельках тумана, которые после осаждения также относят к сухой части загрязнений; в Европе к этой части относят 2/3 всех осадков серы.
Поведение соединений серы в биосфере Атмосфера. В природе сера проявляет все известные для нее степени окисления (-2), (+4), (+6). Это обусловливает существенную роль окислительно-восстановительных реакций и разнообразие процессов миграции. В отличие от СО 2, оказывающего влияние в основном только на распределение энергии в атмосфере (благодаря поглощению ИК-лучей), диоксид серы SO 2 может оказать и прямое токсическое действие на живые организмы. Кроме того, реакционная способность SO 2 значительно выше, чем у СО 2. Время пребывания SO 2 в атмосфере в среднем исчисляется двумя неделями. Этот промежуток времени слишком мал, чтобы газ мог распространяться в глобальном масштабе. Во время переноса диоксид серы лишь в очень малой степени теряет свою химическую активность. Сток SO 2 из атмосферы. 1 - Нейтрализация может происходить лишь в том случае, если в воздухе, одновременно с SO 2 находится пыль, содержащая гидроксиды щелочных и щелочноземельных металлов. Атмосфера очищается от SO 2 главным образом при - 2 - вымывании кислых газов водой или снегом ( «мокрое» осаждение, «кислотные дожди» ), а также при – 3 - их «сухом» осаждении, т. е. в виде самого газа, адсорбированного на мельчайших частицах пыли. Кроме того, - 4 - диоксид серы растворяется в мельчайших капельках тумана, которые после осаждения также относят к сухой части загрязнений; в Европе к этой части относят 2/3 всех осадков серы.
 Особенности геохимического поведения SO 2 в атмосфере. В атмосфере диоксид серы претерпевает ряд химических превращений, важнейшее из них – окисление и образование кислоты. Окисление может происходить разными путями и в силу разных причин. Например, УФ-излучение может перевести молекулу SO 2 в возбужденное состояние, которая затем реагирует с кислородом воздуха и через радикалы SO 4 превращается в молекулу SO 3. Большее значение все же имеет окисление с помощью радикала ОН (уравнения 2. 1 и 2. 2): • • 310 нм О 3 О 2 + О О 2 - + Н 2 О ОН- + ОНSO 2 + 2 OH- H 2 SO 4 (2. 0) (2. 1) (2. 2) При этом возможна и реакция с озоном: SO 2 + O 3 SO 3 + O 2 (2. 3) Во влажной атмосфере таким образом образуется серная кислота - H 2 SO 4. Синтез серной кислоты может проходить и другим путем. Так, в насыщенной парами воды фазе, например в облаках, SO 2 через промежуточный продукт - сернистую кислоту (H 2 SO 3) - образует серную кислоту. Кроме описанного выше гомогенного газофазового окисления сернистого газа, в атмосфере также протекают реакции гетерогенного окисления SO 2 на поверхности твердых аэрозолей. Особо отмечают высокую сорбционную емкость по отношению к диоксиду серы летучей золы и сажи (дымовые факелы ТЭС, например). Считается, что аэрозоли адсорбируют также молекулы и радикалы окисляющих агентов, способствующих образованию серной кислоты и сульфатов.
Особенности геохимического поведения SO 2 в атмосфере. В атмосфере диоксид серы претерпевает ряд химических превращений, важнейшее из них – окисление и образование кислоты. Окисление может происходить разными путями и в силу разных причин. Например, УФ-излучение может перевести молекулу SO 2 в возбужденное состояние, которая затем реагирует с кислородом воздуха и через радикалы SO 4 превращается в молекулу SO 3. Большее значение все же имеет окисление с помощью радикала ОН (уравнения 2. 1 и 2. 2): • • 310 нм О 3 О 2 + О О 2 - + Н 2 О ОН- + ОНSO 2 + 2 OH- H 2 SO 4 (2. 0) (2. 1) (2. 2) При этом возможна и реакция с озоном: SO 2 + O 3 SO 3 + O 2 (2. 3) Во влажной атмосфере таким образом образуется серная кислота - H 2 SO 4. Синтез серной кислоты может проходить и другим путем. Так, в насыщенной парами воды фазе, например в облаках, SO 2 через промежуточный продукт - сернистую кислоту (H 2 SO 3) - образует серную кислоту. Кроме описанного выше гомогенного газофазового окисления сернистого газа, в атмосфере также протекают реакции гетерогенного окисления SO 2 на поверхности твердых аэрозолей. Особо отмечают высокую сорбционную емкость по отношению к диоксиду серы летучей золы и сажи (дымовые факелы ТЭС, например). Считается, что аэрозоли адсорбируют также молекулы и радикалы окисляющих агентов, способствующих образованию серной кислоты и сульфатов.
 Соединения серы в породах, почвах, растениях. Антропогенный вклад соединений серы в экосистемы урбанизированных территорий существенно превышает воздействие природных источников, а в геохимически чистой – наоборот, природный фактор. Установлено, что в индустриальных районах до 60% почвенной кислотности определяется образованием в атмосфере серной кислоты. Биогеохимические циклы природной и антропогенной серы связаны с уровнями ее содержания в породах, почвах, живых организмах. Известно, что содержание серы в осадочных породах выше, чем в изверженных. Наиболее богаты серой глины, несколько меньше ее в карбонатных породах, еще меньше в песчаниках. Среди изверженных магматических пород высокое содержание серы отмечается в интрузиях, к которым приурочены сульфидные руды. В настоящее время большой научный и практический интерес представляют суль- фидные рудопроявления вблизи выходов гидротермальных растворов на океаническом дне, поскольку, как оказалось, эти отложения содержат очень высокие концентрации многих рудных металлов. Сера в почвах представлена органическими и неорганическими соединениями, соотношение которых зависит от типа почвы и от глубины залегания генетического горизонта. Наиболее доступная растениям сульфатная форма составляет 10 -25% от общего содержания. Основные поступления серы в почву происходят с пылью и кислыми ( «кислотными» ) дождями, причем с пылевой фракцией серы
Соединения серы в породах, почвах, растениях. Антропогенный вклад соединений серы в экосистемы урбанизированных территорий существенно превышает воздействие природных источников, а в геохимически чистой – наоборот, природный фактор. Установлено, что в индустриальных районах до 60% почвенной кислотности определяется образованием в атмосфере серной кислоты. Биогеохимические циклы природной и антропогенной серы связаны с уровнями ее содержания в породах, почвах, живых организмах. Известно, что содержание серы в осадочных породах выше, чем в изверженных. Наиболее богаты серой глины, несколько меньше ее в карбонатных породах, еще меньше в песчаниках. Среди изверженных магматических пород высокое содержание серы отмечается в интрузиях, к которым приурочены сульфидные руды. В настоящее время большой научный и практический интерес представляют суль- фидные рудопроявления вблизи выходов гидротермальных растворов на океаническом дне, поскольку, как оказалось, эти отложения содержат очень высокие концентрации многих рудных металлов. Сера в почвах представлена органическими и неорганическими соединениями, соотношение которых зависит от типа почвы и от глубины залегания генетического горизонта. Наиболее доступная растениям сульфатная форма составляет 10 -25% от общего содержания. Основные поступления серы в почву происходят с пылью и кислыми ( «кислотными» ) дождями, причем с пылевой фракцией серы
 Black Smoker
Black Smoker
 White Smokers
White Smokers
 Northern part of the Yogi mound (North Fiji Basin); the picture shows huge blocks of dm- to-m-large rounded fragments of eroded and oxidized chimney relics in an extinct hydrothermal field. (copyright: FU Berlin).
Northern part of the Yogi mound (North Fiji Basin); the picture shows huge blocks of dm- to-m-large rounded fragments of eroded and oxidized chimney relics in an extinct hydrothermal field. (copyright: FU Berlin).
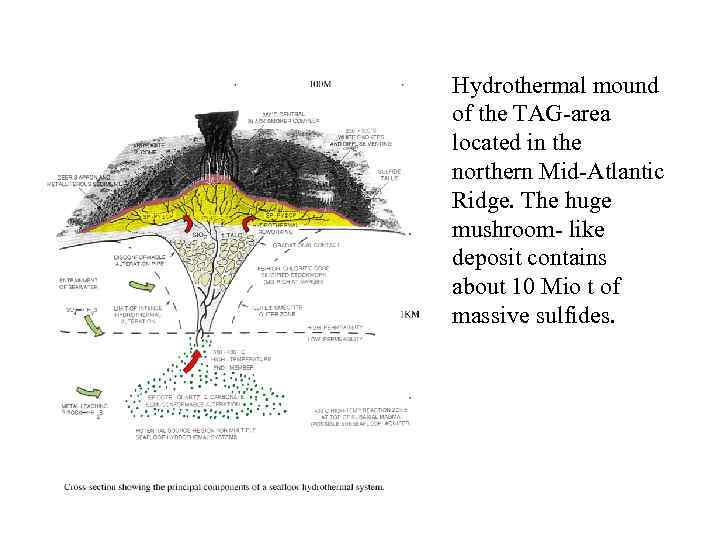 Hydrothermal mound of the TAG-area located in the northern Mid-Atlantic Ridge. The huge mushroom- like deposit contains about 10 Mio t of massive sulfides.
Hydrothermal mound of the TAG-area located in the northern Mid-Atlantic Ridge. The huge mushroom- like deposit contains about 10 Mio t of massive sulfides.
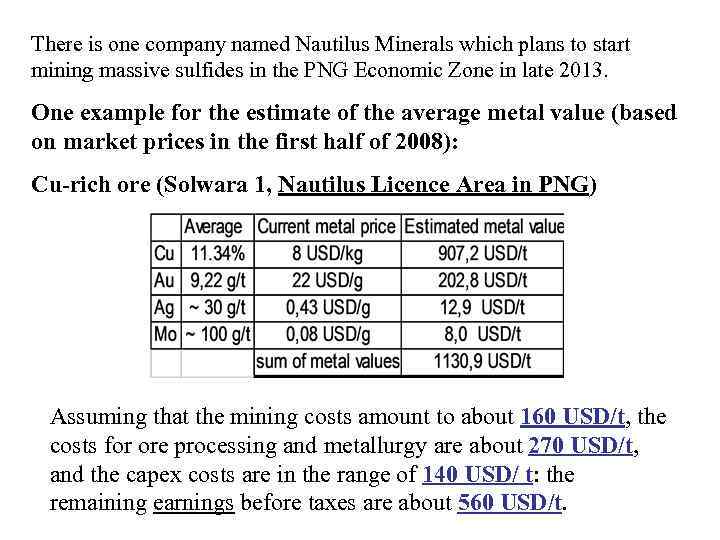 There is one company named Nautilus Minerals which plans to start mining massive sulfides in the PNG Economic Zone in late 2013. One example for the estimate of the average metal value (based on market prices in the first half of 2008): Cu-rich ore (Solwara 1, Nautilus Licence Area in PNG) Assuming that the mining costs amount to about 160 USD/t, the costs for ore processing and metallurgy are about 270 USD/t, and the capex costs are in the range of 140 USD/ t: the remaining earnings before taxes are about 560 USD/t.
There is one company named Nautilus Minerals which plans to start mining massive sulfides in the PNG Economic Zone in late 2013. One example for the estimate of the average metal value (based on market prices in the first half of 2008): Cu-rich ore (Solwara 1, Nautilus Licence Area in PNG) Assuming that the mining costs amount to about 160 USD/t, the costs for ore processing and metallurgy are about 270 USD/t, and the capex costs are in the range of 140 USD/ t: the remaining earnings before taxes are about 560 USD/t.
 Часть серы, поступившей в почву из атмосферы, закрепляется в подстилке, часть мигрирует вниз по профилю. В среднем количество поглощенной подстилкой серы может составлять до 1/3 от количества элемента, поступившего с атмосферными осадками (Лозановская и др. , 1998). Кислые атмосферные выпадения проявляются прежде всего в изменении структурных и физико-химических характеристик почвы – содержании элементов в обменной и водо-растворимой фазах (см. ниже). Если некоторые из элементов, такие как Al, Mn, Fe, Zn, появляются в почвенных растворах в повышенных концентрациях, то другие могут связываться в форме малорастворимых солей, например, Са. SO 4. Поступающий с осадками сульфат-ион SO 42 - (а также NO 3 -) поглощается живыми организмами, а при избытке этих анионов – взаимодействует с твердыми фазами почвы, оставшиеся же не израсходованными количества сульфат-ионов могут мигрировать в составе почвенного раствора, грунтовых вод. Микробиологическое восстановление части сульфатов до летучих газообразных соединений – H 2 S, СS 2 – приводит к потере почвой серы. Избыток ионов - SO 42 -- может поглощаться путем хемосорбции на оксидах Fe и Al, при этом выделяется ОН-, нейтрализующий Н+ (c образованием Н 2 О): 2 Fe. OOH + SO 42 - (Fe. O)2 SO 4 + 2 OH(2. 4) Закрепление сульфат-ионов в почве может происходить также в результате взаимодействия серной кислоты с карбонатами щелочноземельных металлов, приводя к образованию нерастворимых в водной фазе соединений Са. SO 4, Ba. SO 4 и др. Сa. CO 3 + H 2 SO 4 Ca. SO 4 + H 2 CO 3 H+ + HCO 3 - (2. 5)
Часть серы, поступившей в почву из атмосферы, закрепляется в подстилке, часть мигрирует вниз по профилю. В среднем количество поглощенной подстилкой серы может составлять до 1/3 от количества элемента, поступившего с атмосферными осадками (Лозановская и др. , 1998). Кислые атмосферные выпадения проявляются прежде всего в изменении структурных и физико-химических характеристик почвы – содержании элементов в обменной и водо-растворимой фазах (см. ниже). Если некоторые из элементов, такие как Al, Mn, Fe, Zn, появляются в почвенных растворах в повышенных концентрациях, то другие могут связываться в форме малорастворимых солей, например, Са. SO 4. Поступающий с осадками сульфат-ион SO 42 - (а также NO 3 -) поглощается живыми организмами, а при избытке этих анионов – взаимодействует с твердыми фазами почвы, оставшиеся же не израсходованными количества сульфат-ионов могут мигрировать в составе почвенного раствора, грунтовых вод. Микробиологическое восстановление части сульфатов до летучих газообразных соединений – H 2 S, СS 2 – приводит к потере почвой серы. Избыток ионов - SO 42 -- может поглощаться путем хемосорбции на оксидах Fe и Al, при этом выделяется ОН-, нейтрализующий Н+ (c образованием Н 2 О): 2 Fe. OOH + SO 42 - (Fe. O)2 SO 4 + 2 OH(2. 4) Закрепление сульфат-ионов в почве может происходить также в результате взаимодействия серной кислоты с карбонатами щелочноземельных металлов, приводя к образованию нерастворимых в водной фазе соединений Са. SO 4, Ba. SO 4 и др. Сa. CO 3 + H 2 SO 4 Ca. SO 4 + H 2 CO 3 H+ + HCO 3 - (2. 5)
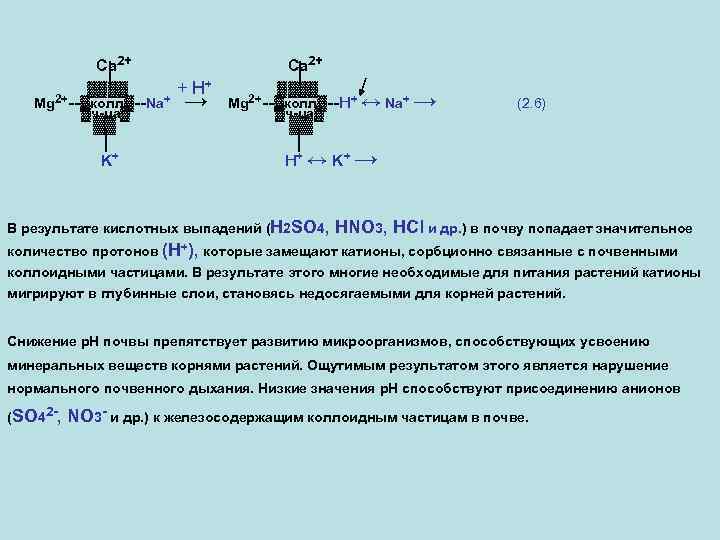 Ca 2+ │ ▓▓▓▓ Mg 2+--▓колл▓--Na+ ▓ч-ца▓ ▓▓ │ K+ Ca 2+ + H+ → │ ▓▓▓▓ Mg 2+--▓колл▓--H+ ▓ч-ца▓ ↔ Na+ → (2. 6) ▓▓ │ H+ ↔ K+ → В результате кислотных выпадений (H 2 SO 4, HNO 3, HCl и др. ) в почву попадает значительное количество протонов (Н+), которые замещают катионы, сорбционно связанные с почвенными коллоидными частицами. В результате этого многие необходимые для питания растений катионы мигрируют в глубинные слои, становясь недосягаемыми для корней растений. Снижение р. Н почвы препятствует развитию микроорганизмов, способствующих усвоению минеральных веществ корнями растений. Ощутимым результатом этого является нарушение нормального почвенного дыхания. Низкие значения р. Н способствуют присоединению анионов (SO 42 -, NO 3 - и др. ) к железосодержащим коллоидным частицам в почве.
Ca 2+ │ ▓▓▓▓ Mg 2+--▓колл▓--Na+ ▓ч-ца▓ ▓▓ │ K+ Ca 2+ + H+ → │ ▓▓▓▓ Mg 2+--▓колл▓--H+ ▓ч-ца▓ ↔ Na+ → (2. 6) ▓▓ │ H+ ↔ K+ → В результате кислотных выпадений (H 2 SO 4, HNO 3, HCl и др. ) в почву попадает значительное количество протонов (Н+), которые замещают катионы, сорбционно связанные с почвенными коллоидными частицами. В результате этого многие необходимые для питания растений катионы мигрируют в глубинные слои, становясь недосягаемыми для корней растений. Снижение р. Н почвы препятствует развитию микроорганизмов, способствующих усвоению минеральных веществ корнями растений. Ощутимым результатом этого является нарушение нормального почвенного дыхания. Низкие значения р. Н способствуют присоединению анионов (SO 42 -, NO 3 - и др. ) к железосодержащим коллоидным частицам в почве.
 Восстановленные соединения серы, такие как сульфиды и элементная сера, достаточно быстро окисляются в почвах при доступе атмосферного воздуха. Эти реакции ускоряются в аэробных условиях при участии различных групп тионовых и серобактерий. Элементная сера (S) появляется в почвах как промежуточный продукт окисления сульфидов железа или при химическом загрязнении. Конечным продуктом окислительного процесса является серная кислота или сульфаты: S S 2 O 32 - S 4 O 62 - SO 32 - SO 42 - Окисление пирита, присутствующего в почве, кислородом воздуха также приводит к накоплению серной кислоты: 2 Fe. S 2 + 2 H 2 O + 7 O 2 2 Fe. SO 4 + 2 H 2 SO 4 (2. 8) С помощью некоторых типов бактерий сульфат железа (II) окисляется до сульфата железа (III) и закрепляется в почвенном субстрате: 4 Fe. SO 4 + O 2 + 2 H 2 SO 4 2 Fe 2(SO 4)3 + 2 H 2 O (2. 9) Следует подчеркнуть, что сульфаты достаточно неустойчивы в анаэробных условиях, а при значительном содержании органического вещества и при катализирующем действии сульфатредуцирующих бактерий, восстанавливаются с подщелачиванием среды: Na 2 SO 4 + Fe(OH)3 + 9 H+ Fe. S + 2 Na. OH + 6 H 2 O (2. 10) Из приведенного уравнения реакции (2. 10) видно, что деятельность сульфатредуцирующих бактерий способствует накоплению в таких почвах сульфидов железа.
Восстановленные соединения серы, такие как сульфиды и элементная сера, достаточно быстро окисляются в почвах при доступе атмосферного воздуха. Эти реакции ускоряются в аэробных условиях при участии различных групп тионовых и серобактерий. Элементная сера (S) появляется в почвах как промежуточный продукт окисления сульфидов железа или при химическом загрязнении. Конечным продуктом окислительного процесса является серная кислота или сульфаты: S S 2 O 32 - S 4 O 62 - SO 32 - SO 42 - Окисление пирита, присутствующего в почве, кислородом воздуха также приводит к накоплению серной кислоты: 2 Fe. S 2 + 2 H 2 O + 7 O 2 2 Fe. SO 4 + 2 H 2 SO 4 (2. 8) С помощью некоторых типов бактерий сульфат железа (II) окисляется до сульфата железа (III) и закрепляется в почвенном субстрате: 4 Fe. SO 4 + O 2 + 2 H 2 SO 4 2 Fe 2(SO 4)3 + 2 H 2 O (2. 9) Следует подчеркнуть, что сульфаты достаточно неустойчивы в анаэробных условиях, а при значительном содержании органического вещества и при катализирующем действии сульфатредуцирующих бактерий, восстанавливаются с подщелачиванием среды: Na 2 SO 4 + Fe(OH)3 + 9 H+ Fe. S + 2 Na. OH + 6 H 2 O (2. 10) Из приведенного уравнения реакции (2. 10) видно, что деятельность сульфатредуцирующих бактерий способствует накоплению в таких почвах сульфидов железа.
 В почвах с непромывным водным режимом и при аэробных условиях сера накапливается в виде гипса или в составе легкорастворимых солей. Известно, что в обычных почвах, подверженных техногенному загрязнению, происходит значительное возрастание валового содержания серы, в первую очередь за счет водорастворимых сульфатов. Содержание серы в растениях - зависит от физических особенностей вида. Мхи, папоротники, хвощи содержат более 2% серы в золе (Перельман, 1976). Среди двудольных растений обогащена серой зола лебедовых (5%), крестоцветных (4%), в хвое содержание серы не превышает 0. 06% для незагрязненных биогеоценозов (Лозановская и др. , 1998). Растения избирательно поглощают серу в соответствии с физиологическими потребностями; при долговременном воздействии даже низких концентраций SO 2 содержание элемента в тканях растений может возрастать в 2 -2. 5 раза по сравнению с фоновым уровнем. Поэтому аккумуляция серы в растениях может служить индикатором техногенных воздействий.
В почвах с непромывным водным режимом и при аэробных условиях сера накапливается в виде гипса или в составе легкорастворимых солей. Известно, что в обычных почвах, подверженных техногенному загрязнению, происходит значительное возрастание валового содержания серы, в первую очередь за счет водорастворимых сульфатов. Содержание серы в растениях - зависит от физических особенностей вида. Мхи, папоротники, хвощи содержат более 2% серы в золе (Перельман, 1976). Среди двудольных растений обогащена серой зола лебедовых (5%), крестоцветных (4%), в хвое содержание серы не превышает 0. 06% для незагрязненных биогеоценозов (Лозановская и др. , 1998). Растения избирательно поглощают серу в соответствии с физиологическими потребностями; при долговременном воздействии даже низких концентраций SO 2 содержание элемента в тканях растений может возрастать в 2 -2. 5 раза по сравнению с фоновым уровнем. Поэтому аккумуляция серы в растениях может служить индикатором техногенных воздействий.
 Соединения азота (N) Азот – важнейший элемент питания, необходимый для нормального развития растений. Он входит в состав белков (до 16 -18% их массы), нуклеиновый кислот, нуклеопротеидов, хлорофилла, гемоглобина, фосфатидов, алкалоидов. Соединения азота играют большую роль в процессах фотосинтеза, обмена веществ, образовании новых клеток. В формировании почвенного покрова и плодородия экосистем, в повышении продуктивности земледелия и улучшении белкового питания человека азот столь же незаменим, как и углерод. • Основные запасы азота на планете – (4 -6) · 1015 т – приходятся на атмосферу, • в осадочных породах земной коры, сформировавшихся при участии биологических факторов, накопилось – около 6 · 1014 т, • в Мировом океане – до 2 · 1013 т, • биомасса суши содержит - ~ 1 · 1010 т, • биомасса океана – до 1 · 1011 т. Главным источником азота в почве является гумус. Планетарные запасы азота в почвенном гумусе составляют ~ 6 · 1010 т, однако он находится в недоступной для растений форме и непосредственно для их питания не используется. Азот гумуса переходит в растворимые и доступные формы лишь постепенно, в результате ряда сложных и длительных микробиологических превращений. В биосфере азот присутствует в газообразной форме – N 2, NH 3, NO 2 , в виде соединений азотной и азотистой кислот (нитраты, нитриты), солей аммония, входит в состав многих органических соединений (веществ). Приблизительный баланс азота в биосфере приведен в табл. 1. Табл. 1. Элементы баланса азота в биосфере. Сканировать!
Соединения азота (N) Азот – важнейший элемент питания, необходимый для нормального развития растений. Он входит в состав белков (до 16 -18% их массы), нуклеиновый кислот, нуклеопротеидов, хлорофилла, гемоглобина, фосфатидов, алкалоидов. Соединения азота играют большую роль в процессах фотосинтеза, обмена веществ, образовании новых клеток. В формировании почвенного покрова и плодородия экосистем, в повышении продуктивности земледелия и улучшении белкового питания человека азот столь же незаменим, как и углерод. • Основные запасы азота на планете – (4 -6) · 1015 т – приходятся на атмосферу, • в осадочных породах земной коры, сформировавшихся при участии биологических факторов, накопилось – около 6 · 1014 т, • в Мировом океане – до 2 · 1013 т, • биомасса суши содержит - ~ 1 · 1010 т, • биомасса океана – до 1 · 1011 т. Главным источником азота в почве является гумус. Планетарные запасы азота в почвенном гумусе составляют ~ 6 · 1010 т, однако он находится в недоступной для растений форме и непосредственно для их питания не используется. Азот гумуса переходит в растворимые и доступные формы лишь постепенно, в результате ряда сложных и длительных микробиологических превращений. В биосфере азот присутствует в газообразной форме – N 2, NH 3, NO 2 , в виде соединений азотной и азотистой кислот (нитраты, нитриты), солей аммония, входит в состав многих органических соединений (веществ). Приблизительный баланс азота в биосфере приведен в табл. 1. Табл. 1. Элементы баланса азота в биосфере. Сканировать!
 Почва Устойчивые соединения азота в почвах представлены формами со степенями окисления -3 (NH+4) и +5 (NO-3). Биофильность азота сравнима с таковой для углерода (С). Вне живых организмов азот в биосфере представлен молекулами N 2, неорганическими соединениями (преимущественно NH+4, NO-3, NO-2) и органическими формами. В биоценозах на долю минеральных соединений азота приходится не > 1 -10%. В почвах в свободной форме аммиак NH 3 практически не встречается. Обычно он продуцируется при разложении органических удобрений. Преобладающая часть соединений азота в почвах относится к органическим: в гумусовых горизонтах почв содержится до 93 -99% азота в составе органических соединений. Минеральные соединения азота помимо аммонийных (NH+4) представлены нитратами (NO-3) и нитритами (NO-2). Содержание нитритов – наименьшее среди перечисленных выше, и составляет десятые доли мг на 1 кг почвы. Несмотря на это, нитритам принадлежит существенная роль в реакциях превращений азота в почвах. Они образуются как промежуточные соединения при (см. ниже): • нитрификации в аэробных условиях • денитрификации в анаэробных условиях. В почвенных условиях нитриты обычно малоустойчивы и при их разложении происходят (вероятно) реакции 2 -х основных типов: 3 HNO 2 → HNO 3 + 2 NO + H 2 O 2 HNO 2 → NO + NO 2 + H 2 O Органические соединения почвы представлены следующими группами: азот аминокислот, азот амидов и т. д. Сканировать!
Почва Устойчивые соединения азота в почвах представлены формами со степенями окисления -3 (NH+4) и +5 (NO-3). Биофильность азота сравнима с таковой для углерода (С). Вне живых организмов азот в биосфере представлен молекулами N 2, неорганическими соединениями (преимущественно NH+4, NO-3, NO-2) и органическими формами. В биоценозах на долю минеральных соединений азота приходится не > 1 -10%. В почвах в свободной форме аммиак NH 3 практически не встречается. Обычно он продуцируется при разложении органических удобрений. Преобладающая часть соединений азота в почвах относится к органическим: в гумусовых горизонтах почв содержится до 93 -99% азота в составе органических соединений. Минеральные соединения азота помимо аммонийных (NH+4) представлены нитратами (NO-3) и нитритами (NO-2). Содержание нитритов – наименьшее среди перечисленных выше, и составляет десятые доли мг на 1 кг почвы. Несмотря на это, нитритам принадлежит существенная роль в реакциях превращений азота в почвах. Они образуются как промежуточные соединения при (см. ниже): • нитрификации в аэробных условиях • денитрификации в анаэробных условиях. В почвенных условиях нитриты обычно малоустойчивы и при их разложении происходят (вероятно) реакции 2 -х основных типов: 3 HNO 2 → HNO 3 + 2 NO + H 2 O 2 HNO 2 → NO + NO 2 + H 2 O Органические соединения почвы представлены следующими группами: азот аминокислот, азот амидов и т. д. Сканировать!
 Эти соединения азота входят в состав: • Неспецифических органических соединений почвы • Гумусовых кислот Соотношение различных соединений азота в разных по генезису почвах довольно постоянно (табл. 2). Таб. 2. Содержание соединений азота в почвах разного генезиса, кг/га (в слое 0 – 20 см). Группа Дерновоподзол истая Типичный чернозем Серозем Весь азот 3560 9890 3420 Азот аминогрупп 425 1010 400 Аммонийный азот 500 1040 650 Азот аминосахаров 400 670 220 Негидролизуемый азот 1080 4340 1400 Так, во всех почвах преобладают негидролизуемые соединения N, причем: • в черноземе они составляют около 40 -45% всего запаса N • в сероземе – около 40% • в дерново-подзолистой – около 30%. Это соотношение обусловлено повышенной биологической активностью чернозема и серозема, в которых происходит преимущественное разложение лабильных (подвижных) соединений и накопление более устойчивых негидролизуемых форм. Трансформация соединений азота в почвах включает процессы: 1. Фиксация атмосферного N свободноживущими и клубеньковыми бактериями; 2. Превращение азотсодержащих соединений органических остатков в гумусовые кислоты; 3. Аммонификация органических азотсодержащих соединений; 4. Нитрификация; 5. Денитрификация и потеря N в атмосферу; 6. Фиксация иона NH+4 глинистыми минералами; 7. Вымывание различных соединений N с внутрипочвенным и поверхностным стоком.
Эти соединения азота входят в состав: • Неспецифических органических соединений почвы • Гумусовых кислот Соотношение различных соединений азота в разных по генезису почвах довольно постоянно (табл. 2). Таб. 2. Содержание соединений азота в почвах разного генезиса, кг/га (в слое 0 – 20 см). Группа Дерновоподзол истая Типичный чернозем Серозем Весь азот 3560 9890 3420 Азот аминогрупп 425 1010 400 Аммонийный азот 500 1040 650 Азот аминосахаров 400 670 220 Негидролизуемый азот 1080 4340 1400 Так, во всех почвах преобладают негидролизуемые соединения N, причем: • в черноземе они составляют около 40 -45% всего запаса N • в сероземе – около 40% • в дерново-подзолистой – около 30%. Это соотношение обусловлено повышенной биологической активностью чернозема и серозема, в которых происходит преимущественное разложение лабильных (подвижных) соединений и накопление более устойчивых негидролизуемых форм. Трансформация соединений азота в почвах включает процессы: 1. Фиксация атмосферного N свободноживущими и клубеньковыми бактериями; 2. Превращение азотсодержащих соединений органических остатков в гумусовые кислоты; 3. Аммонификация органических азотсодержащих соединений; 4. Нитрификация; 5. Денитрификация и потеря N в атмосферу; 6. Фиксация иона NH+4 глинистыми минералами; 7. Вымывание различных соединений N с внутрипочвенным и поверхностным стоком.
 • • Пояснения к трансформациям соединений азота: Азот поступает в почву: С атмосферными осадками в виде NH 3 и NO-3. Другим естественным источником N является его фиксация свободноживущими микро- организмами и клубеньковыми бактериями (из атмосферы). • Появление соединений N при разложении растительных и животных остатков. • Существенным источником N являются техногенные поступления в виде удобрений и отходов. Органические остатки гумифицируются и аммонифицируются. Ион NH+4 усваивается растениями, вовлекается в процессы гумификации, частично вымываются или фиксируются, а также подвергается нитрификации. Нитрат-ион (NO-3) частично вымывается, поглощается растениями, подвергается денитрификации, замыкая биогеохимический цикл азота. Аммонификация – процесс разложения органических в-в, протекающий с участием аммонифицирующих микроорганизмов и ведущий к образованию NH 3 или NH+4. Ион аммония (NH+4) может быть выщелочен или поглощён в почвенном комплексе или необменно фиксирован трёхслойными глинистыми минералами с расширяющейся решёткой. Содержание фиксированного аммония в почвах меняется от 1 -2 до 10 -12 мэкв/100 г почвы. Аммонификация – первая стадия минерализации азотсодержащих органических соединений. Нитрификация – окисление аммиака (NH 3, или аммония - NH+4 ) до нитритов (NO-2) и нитратов (NO-3). Этот процесс протекает в 2 этапа: 1. Окисление NH 3 → HNO 2 через гидроксиламин NH 2 OH и гипонитриты (соли азотноватистой к-ты HO — N ═ N — OH): NH 3 → NH 2 OH → HO — N ═ N — OH → HO — N ═ O (при участии бактерий Nitrosomonas);
• • Пояснения к трансформациям соединений азота: Азот поступает в почву: С атмосферными осадками в виде NH 3 и NO-3. Другим естественным источником N является его фиксация свободноживущими микро- организмами и клубеньковыми бактериями (из атмосферы). • Появление соединений N при разложении растительных и животных остатков. • Существенным источником N являются техногенные поступления в виде удобрений и отходов. Органические остатки гумифицируются и аммонифицируются. Ион NH+4 усваивается растениями, вовлекается в процессы гумификации, частично вымываются или фиксируются, а также подвергается нитрификации. Нитрат-ион (NO-3) частично вымывается, поглощается растениями, подвергается денитрификации, замыкая биогеохимический цикл азота. Аммонификация – процесс разложения органических в-в, протекающий с участием аммонифицирующих микроорганизмов и ведущий к образованию NH 3 или NH+4. Ион аммония (NH+4) может быть выщелочен или поглощён в почвенном комплексе или необменно фиксирован трёхслойными глинистыми минералами с расширяющейся решёткой. Содержание фиксированного аммония в почвах меняется от 1 -2 до 10 -12 мэкв/100 г почвы. Аммонификация – первая стадия минерализации азотсодержащих органических соединений. Нитрификация – окисление аммиака (NH 3, или аммония - NH+4 ) до нитритов (NO-2) и нитратов (NO-3). Этот процесс протекает в 2 этапа: 1. Окисление NH 3 → HNO 2 через гидроксиламин NH 2 OH и гипонитриты (соли азотноватистой к-ты HO — N ═ N — OH): NH 3 → NH 2 OH → HO — N ═ N — OH → HO — N ═ O (при участии бактерий Nitrosomonas);
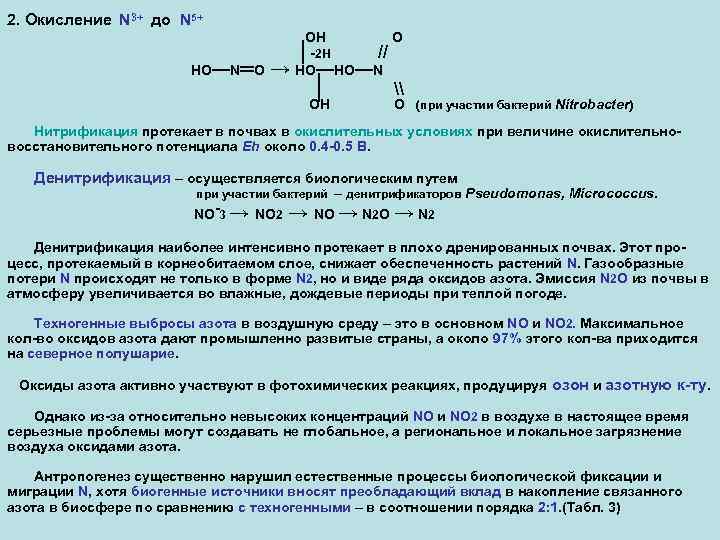 2. Окисление N 3+ до N 5+ OH HO—N═O │-2 H // → HO—HO—N │ OH O \ O (при участии бактерий Nitrobacter) Нитрификация протекает в почвах в окислительных условиях при величине окислительновосстановительного потенциала Eh около 0. 4 -0. 5 В. Денитрификация – осуществляется биологическим путем при участии бактерий – денитрификаторов Pseudomonas, Micrococcus. NO-3 → NO 2 → NO → N 2 Денитрификация наиболее интенсивно протекает в плохо дренированных почвах. Этот процесс, протекаемый в корнеобитаемом слое, снижает обеспеченность растений N. Газообразные потери N происходят не только в форме N 2, но и виде ряда оксидов азота. Эмиссия N 2 O из почвы в атмосферу увеличивается во влажные, дождевые периоды при теплой погоде. Техногенные выбросы азота в воздушную среду – это в основном NO и NO 2. Максимальное кол-во оксидов азота дают промышленно развитые страны, а около 97% этого кол-ва приходится на северное полушарие. Оксиды азота активно участвуют в фотохимических реакциях, продуцируя озон и азотную к-ту. Однако из-за относительно невысоких концентраций NO и NO 2 в воздухе в настоящее время серьезные проблемы могут создавать не глобальное, а региональное и локальное загрязнение воздуха оксидами азота. Антропогенез существенно нарушил естественные процессы биологической фиксации и миграции N, хотя биогенные источники вносят преобладающий вклад в накопление связанного азота в биосфере по сравнению с техногенными – в соотношении порядка 2: 1. (Табл. 3)
2. Окисление N 3+ до N 5+ OH HO—N═O │-2 H // → HO—HO—N │ OH O \ O (при участии бактерий Nitrobacter) Нитрификация протекает в почвах в окислительных условиях при величине окислительновосстановительного потенциала Eh около 0. 4 -0. 5 В. Денитрификация – осуществляется биологическим путем при участии бактерий – денитрификаторов Pseudomonas, Micrococcus. NO-3 → NO 2 → NO → N 2 Денитрификация наиболее интенсивно протекает в плохо дренированных почвах. Этот процесс, протекаемый в корнеобитаемом слое, снижает обеспеченность растений N. Газообразные потери N происходят не только в форме N 2, но и виде ряда оксидов азота. Эмиссия N 2 O из почвы в атмосферу увеличивается во влажные, дождевые периоды при теплой погоде. Техногенные выбросы азота в воздушную среду – это в основном NO и NO 2. Максимальное кол-во оксидов азота дают промышленно развитые страны, а около 97% этого кол-ва приходится на северное полушарие. Оксиды азота активно участвуют в фотохимических реакциях, продуцируя озон и азотную к-ту. Однако из-за относительно невысоких концентраций NO и NO 2 в воздухе в настоящее время серьезные проблемы могут создавать не глобальное, а региональное и локальное загрязнение воздуха оксидами азота. Антропогенез существенно нарушил естественные процессы биологической фиксации и миграции N, хотя биогенные источники вносят преобладающий вклад в накопление связанного азота в биосфере по сравнению с техногенными – в соотношении порядка 2: 1. (Табл. 3)
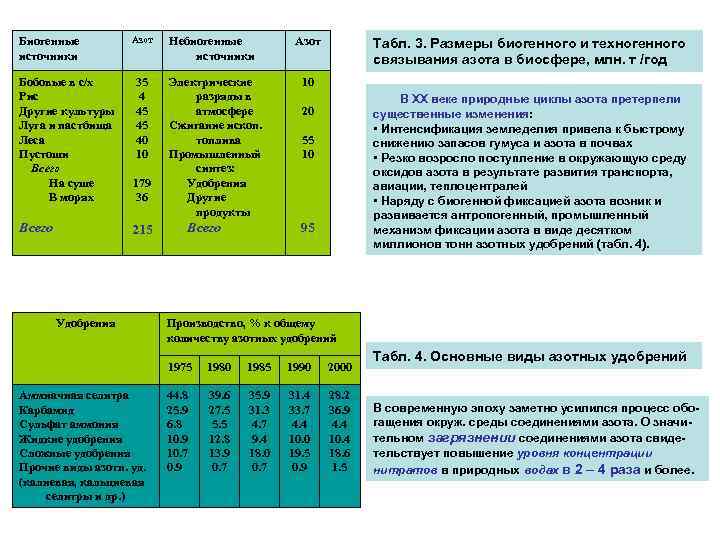 Биогенные источники Азот Бобовые в с/х Рис Другие культуры Луга и пастбища Леса Пустоши Всего На суше В морях 35 4 45 45 40 10 179 36 Всего 215 Удобрения Небиогенные источники Электрические разряды в атмосфере Сжигание ископ. топлива Промышленный синтез: Удобрения Другие продукты Всего Азот Табл. 3. Размеры биогенного и техногенного связывания азота в биосфере, млн. т /год 10 В ХХ веке природные циклы азота претерпели существенные изменения: • Интенсификация земледелия привела к быстрому снижению запасов гумуса и азота в почвах • Резко возросло поступление в окружающую среду оксидов азота в результате развития транспорта, авиации, теплоцентралей • Наряду с биогенной фиксацией азота возник и развивается антропогенный, промышленный механизм фиксации азота в виде десятком миллионов тонн азотных удобрений (табл. 4). 20 55 10 95 Производство, % к общему количеству азотных удобрений 1975 Аммиачная селитра Карбамид Сульфат аммония Жидкие удобрения Сложные удобрения Прочие виды азотн. уд. (калиевая, кальциевая селитры и др. ) 1980 1985 1990 2000 44. 8 25. 9 6. 8 10. 9 10. 7 0. 9 39. 6 27. 5 5. 5 12. 8 13. 9 0. 7 35. 9 31. 3 4. 7 9. 4 18. 0 0. 7 31. 4 33. 7 4. 4 10. 0 19. 5 0. 9 28. 2 36. 9 4. 4 10. 4 18. 6 1. 5 Табл. 4. Основные виды азотных удобрений В современную эпоху заметно усилился процесс обогащения окруж. среды соединениями азота. О значительном загрязнении соединениями азота свидетельствует повышение уровня концентрации нитратов в природных водах в 2 – 4 раза и более.
Биогенные источники Азот Бобовые в с/х Рис Другие культуры Луга и пастбища Леса Пустоши Всего На суше В морях 35 4 45 45 40 10 179 36 Всего 215 Удобрения Небиогенные источники Электрические разряды в атмосфере Сжигание ископ. топлива Промышленный синтез: Удобрения Другие продукты Всего Азот Табл. 3. Размеры биогенного и техногенного связывания азота в биосфере, млн. т /год 10 В ХХ веке природные циклы азота претерпели существенные изменения: • Интенсификация земледелия привела к быстрому снижению запасов гумуса и азота в почвах • Резко возросло поступление в окружающую среду оксидов азота в результате развития транспорта, авиации, теплоцентралей • Наряду с биогенной фиксацией азота возник и развивается антропогенный, промышленный механизм фиксации азота в виде десятком миллионов тонн азотных удобрений (табл. 4). 20 55 10 95 Производство, % к общему количеству азотных удобрений 1975 Аммиачная селитра Карбамид Сульфат аммония Жидкие удобрения Сложные удобрения Прочие виды азотн. уд. (калиевая, кальциевая селитры и др. ) 1980 1985 1990 2000 44. 8 25. 9 6. 8 10. 9 10. 7 0. 9 39. 6 27. 5 5. 5 12. 8 13. 9 0. 7 35. 9 31. 3 4. 7 9. 4 18. 0 0. 7 31. 4 33. 7 4. 4 10. 0 19. 5 0. 9 28. 2 36. 9 4. 4 10. 4 18. 6 1. 5 Табл. 4. Основные виды азотных удобрений В современную эпоху заметно усилился процесс обогащения окруж. среды соединениями азота. О значительном загрязнении соединениями азота свидетельствует повышение уровня концентрации нитратов в природных водах в 2 – 4 раза и более.
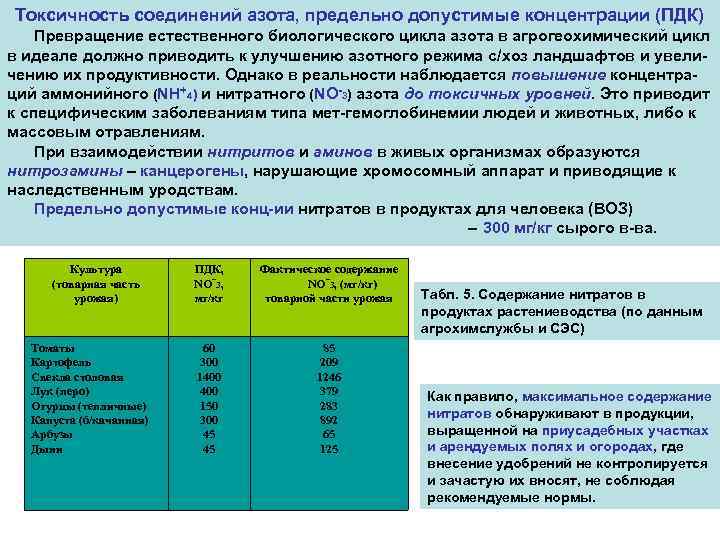 Токсичность соединений азота, предельно допустимые концентрации (ПДК) Превращение естественного биологического цикла азота в агрогеохимический цикл в идеале должно приводить к улучшению азотного режима с/хоз ландшафтов и увеличению их продуктивности. Однако в реальности наблюдается повышение концентраций аммонийного (NH+4) и нитратного (NO-3) азота до токсичных уровней. Это приводит к специфическим заболеваниям типа мет-гемоглобинемии людей и животных, либо к массовым отравлениям. При взаимодействии нитритов и аминов в живых организмах образуются нитрозамины – канцерогены, нарушающие хромосомный аппарат и приводящие к наследственным уродствам. Предельно допустимые конц-ии нитратов в продуктах для человека (ВОЗ) – 300 мг/кг сырого в-ва. Культура (товарная часть урожая) Томаты Картофель Свекла столовая Лук (перо) Огурцы (тепличные) Капуста (б/качанная) Арбузы Дыни ПДК, NO-3, мг/кг Фактическое содержание NO-3, (мг/кг) товарной части урожая 60 300 1400 150 300 45 45 85 209 1246 379 283 892 65 125 Табл. 5. Содержание нитратов в продуктах растениеводства (по данным агрохимслужбы и СЭС) Как правило, максимальное содержание нитратов обнаруживают в продукции, выращенной на приусадебных участках и арендуемых полях и огородах, где внесение удобрений не контролируется и зачастую их вносят, не соблюдая рекомендуемые нормы.
Токсичность соединений азота, предельно допустимые концентрации (ПДК) Превращение естественного биологического цикла азота в агрогеохимический цикл в идеале должно приводить к улучшению азотного режима с/хоз ландшафтов и увеличению их продуктивности. Однако в реальности наблюдается повышение концентраций аммонийного (NH+4) и нитратного (NO-3) азота до токсичных уровней. Это приводит к специфическим заболеваниям типа мет-гемоглобинемии людей и животных, либо к массовым отравлениям. При взаимодействии нитритов и аминов в живых организмах образуются нитрозамины – канцерогены, нарушающие хромосомный аппарат и приводящие к наследственным уродствам. Предельно допустимые конц-ии нитратов в продуктах для человека (ВОЗ) – 300 мг/кг сырого в-ва. Культура (товарная часть урожая) Томаты Картофель Свекла столовая Лук (перо) Огурцы (тепличные) Капуста (б/качанная) Арбузы Дыни ПДК, NO-3, мг/кг Фактическое содержание NO-3, (мг/кг) товарной части урожая 60 300 1400 150 300 45 45 85 209 1246 379 283 892 65 125 Табл. 5. Содержание нитратов в продуктах растениеводства (по данным агрохимслужбы и СЭС) Как правило, максимальное содержание нитратов обнаруживают в продукции, выращенной на приусадебных участках и арендуемых полях и огородах, где внесение удобрений не контролируется и зачастую их вносят, не соблюдая рекомендуемые нормы.
 Озоновый слой. В настоящее время большую проблему представляет нарушение толщины озонового слоя, на уменьшение которого могут оказывать влияние неполные оксиды азота, вступающие в реакции окисления от N 2 О до NO 2 и использующие кислород озонового слоя. Разрушение озонового слоя связывают с оксидом азота - NO, который служит источником образования других оксидов, катализирующих фотохимическую реакцию разложения молекул озона. Так, например, молекула озона, поглощая квант света, образует атомарный кислород: O 3 + hν → O + O 2 Затем атомарный кислород реагирует с диоксидом NO 2 азота, образуя оксид NO, а последний с молекулой озона вновь образует диоксид: O + NO 2 → NO + O 2 NO + O 3 → NO 2 + O 2 В результате чего две молекулы озона – O 3 – трансформируются в три молекулы кислорода: 2 O 3 → 3 O 2 Основным путем образования оксида азота N 2 О в почвах и водах является процесс денитрификации, хотя некоторые его количества могут возникать при нитрификации, а также при разложении нитрит-иона NO-2 или гидроксиламина NH 2 OH в кислых почвах. Т. о. , избыточное вовлечение соединений азота в биосферу представляется весьма опасным. Целесообразно использовать совместное внесение в почву органических и минеральных удобрений, а баланс азота регулировать точным выбором удобрений, времени и способа их внесения. Меры защиты окр. среды от избытка соединений азота: • Уменьшение норм внесения минеральных удобрений (не более 100 -200 кг/га N) при одновременном увеличении доли органических удобрений (навоз, зеленые удобрения). • Запрещение внесения удобрений по снегу, с самолетов. • Создание минеральных азотных удобрений с небольшой скоростью растворения. • Рациональное использование жидких органических удобрений; запрещение сброса отходов животноводства в окр. среду. Природный процесс денитрификации, составлявший в прошлом 20 -25% в мировом балансе азота, не компенсируется в наст. Время энергичным поступлением соединений азота. Ежегодный избыток соединений N в биосфере составляет около 10 млн. т. В качестве одного из средств регулирования азотного цикла в природных и агробиоценозах может быть применение ингибиторов нитрификации.
Озоновый слой. В настоящее время большую проблему представляет нарушение толщины озонового слоя, на уменьшение которого могут оказывать влияние неполные оксиды азота, вступающие в реакции окисления от N 2 О до NO 2 и использующие кислород озонового слоя. Разрушение озонового слоя связывают с оксидом азота - NO, который служит источником образования других оксидов, катализирующих фотохимическую реакцию разложения молекул озона. Так, например, молекула озона, поглощая квант света, образует атомарный кислород: O 3 + hν → O + O 2 Затем атомарный кислород реагирует с диоксидом NO 2 азота, образуя оксид NO, а последний с молекулой озона вновь образует диоксид: O + NO 2 → NO + O 2 NO + O 3 → NO 2 + O 2 В результате чего две молекулы озона – O 3 – трансформируются в три молекулы кислорода: 2 O 3 → 3 O 2 Основным путем образования оксида азота N 2 О в почвах и водах является процесс денитрификации, хотя некоторые его количества могут возникать при нитрификации, а также при разложении нитрит-иона NO-2 или гидроксиламина NH 2 OH в кислых почвах. Т. о. , избыточное вовлечение соединений азота в биосферу представляется весьма опасным. Целесообразно использовать совместное внесение в почву органических и минеральных удобрений, а баланс азота регулировать точным выбором удобрений, времени и способа их внесения. Меры защиты окр. среды от избытка соединений азота: • Уменьшение норм внесения минеральных удобрений (не более 100 -200 кг/га N) при одновременном увеличении доли органических удобрений (навоз, зеленые удобрения). • Запрещение внесения удобрений по снегу, с самолетов. • Создание минеральных азотных удобрений с небольшой скоростью растворения. • Рациональное использование жидких органических удобрений; запрещение сброса отходов животноводства в окр. среду. Природный процесс денитрификации, составлявший в прошлом 20 -25% в мировом балансе азота, не компенсируется в наст. Время энергичным поступлением соединений азота. Ежегодный избыток соединений N в биосфере составляет около 10 млн. т. В качестве одного из средств регулирования азотного цикла в природных и агробиоценозах может быть применение ингибиторов нитрификации.
 Соединения фосфора (Р) - один из важнейших биогенных элементов. Он входит в состав: нуклеопротеидов, сахарофосфатов, фосфатидов и др. соединений. Фосфор активно участвует в процессах обмена веществ и синтеза белка, определяет энергетику клетки, активно влияет на рост растений, концентрируясь в семенах и точках роста. Соединения Р входят в состав тканей живых организмов – мозга, костей, панциря. Наиболее характерные степени окисления фосфора: -3, например, фосфин PH 3; +3, например, гидрид фосфора PCl 3; +5, например, (орто-)фосфорная к-та H 3 PO 4. Среднее содержание Р в земной коре – до 0. 09%, причем его водная и воздушная миграция относительно невысока. Несмотря на значительное разнообразие минеральных и органических соединений Р, в природе в виде минералов встречаются практически только производные (орто-) фосфорной к-ты – (орто-)фосфаты, среди которых до 95% - это фосфаты кальция Ca 3(PO 4)2. В земной коре значит. часть соединений Р представлена разновидностями апатита, преимущественно фторапатитом Ca 10(PO 4)6 F 2, а также гидроксилапатитом Ca 10(PO 4)6(OH)2, хлорапатитом Ca 10(PO 4)6 Cl 2. Кроме того присутствуют дикальций фосфат Ca. HPO 4, трикальцийфосфат β-Ca 3(PO 4)2, штренгит Fe. PO 4 · 2 H 2 O. В настоящее время известно > 200 фосфорсодержащих минералов. В почвах различают следующие группы соединений P: 1. Гидроксилапатит и фторапатит – малорастворимые в слабощелочной и нейтральной среде, но подвижные в кислой среде. 2. Фосфаты полуторных окислов (например, штренгит или варисцит – Al. PO 4 · 2 H 2 O), малорастворимые при низких значениях p. H (кислая среда). 3. Фосфаты щелочей, моно- и дикальциевые (магниевые) фосфаты (см. выше), растворимые, подвижные и доступные растениям. 4. Полифосфаты, активизирующие деятельность микроорганизмов, способствующие повышению растворимости органических в-в и соединений ряда элементов в почвах – Ca, Mn, Zn, Al, Fe.
Соединения фосфора (Р) - один из важнейших биогенных элементов. Он входит в состав: нуклеопротеидов, сахарофосфатов, фосфатидов и др. соединений. Фосфор активно участвует в процессах обмена веществ и синтеза белка, определяет энергетику клетки, активно влияет на рост растений, концентрируясь в семенах и точках роста. Соединения Р входят в состав тканей живых организмов – мозга, костей, панциря. Наиболее характерные степени окисления фосфора: -3, например, фосфин PH 3; +3, например, гидрид фосфора PCl 3; +5, например, (орто-)фосфорная к-та H 3 PO 4. Среднее содержание Р в земной коре – до 0. 09%, причем его водная и воздушная миграция относительно невысока. Несмотря на значительное разнообразие минеральных и органических соединений Р, в природе в виде минералов встречаются практически только производные (орто-) фосфорной к-ты – (орто-)фосфаты, среди которых до 95% - это фосфаты кальция Ca 3(PO 4)2. В земной коре значит. часть соединений Р представлена разновидностями апатита, преимущественно фторапатитом Ca 10(PO 4)6 F 2, а также гидроксилапатитом Ca 10(PO 4)6(OH)2, хлорапатитом Ca 10(PO 4)6 Cl 2. Кроме того присутствуют дикальций фосфат Ca. HPO 4, трикальцийфосфат β-Ca 3(PO 4)2, штренгит Fe. PO 4 · 2 H 2 O. В настоящее время известно > 200 фосфорсодержащих минералов. В почвах различают следующие группы соединений P: 1. Гидроксилапатит и фторапатит – малорастворимые в слабощелочной и нейтральной среде, но подвижные в кислой среде. 2. Фосфаты полуторных окислов (например, штренгит или варисцит – Al. PO 4 · 2 H 2 O), малорастворимые при низких значениях p. H (кислая среда). 3. Фосфаты щелочей, моно- и дикальциевые (магниевые) фосфаты (см. выше), растворимые, подвижные и доступные растениям. 4. Полифосфаты, активизирующие деятельность микроорганизмов, способствующие повышению растворимости органических в-в и соединений ряда элементов в почвах – Ca, Mn, Zn, Al, Fe.
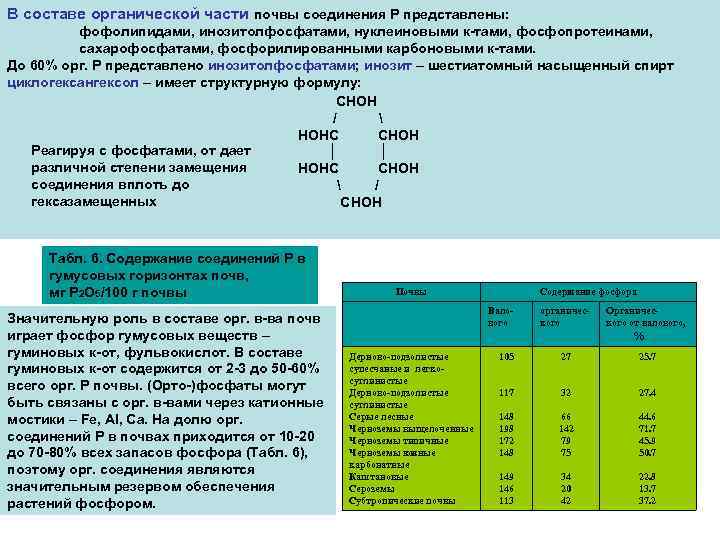 В составе органической части почвы соединения Р представлены: фофолипидами, инозитолфосфатами, нуклеиновыми к-тами, фосфопротеинами, сахарофосфатами, фосфорилированными карбоновыми к-тами. До 60% орг. Р представлено инозитолфосфатами; инозит – шестиатомный насыщенный спирт циклогексангексол – имеет структурную формулу: CHOH / HOHC CHOH Реагируя с фосфатами, от дает │ │ различной степени замещения HOHC CHOH соединения вплоть до / гексазамещенных CHOH Табл. 6. Содержание соединений Р в гумусовых горизонтах почв, мг Р 2 О 5/100 г почвы Значительную роль в составе орг. в-ва почв играет фосфор гумусовых веществ – гуминовых к-от, фульвокислот. В составе гуминовых к-от содержится от 2 -3 до 50 -60% всего орг. Р почвы. (Орто-)фосфаты могут быть связаны с орг. в-вами через катионные мостики – Fe, Al, Ca. На долю орг. соединений Р в почвах приходится от 10 -20 до 70 -80% всех запасов фосфора (Табл. 6), поэтому орг. соединения являются значительным резервом обеспечения растений фосфором. Почвы Содержание фосфора Валового органического Органического от валового, % Дерново-подзолистые супесчаные и легкосуглинистые Дерново-подзолистые суглинистые Серые лесные Черноземы выщелоченные Черноземы типичные Черноземы южные карбонатные Каштановые Сероземы Субтропические почвы 105 27 25. 7 117 32 27. 4 148 198 172 148 66 142 79 75 44. 6 71. 7 45. 9 50. 7 149 146 113 34 20 42 22. 8 13. 7 37. 2
В составе органической части почвы соединения Р представлены: фофолипидами, инозитолфосфатами, нуклеиновыми к-тами, фосфопротеинами, сахарофосфатами, фосфорилированными карбоновыми к-тами. До 60% орг. Р представлено инозитолфосфатами; инозит – шестиатомный насыщенный спирт циклогексангексол – имеет структурную формулу: CHOH / HOHC CHOH Реагируя с фосфатами, от дает │ │ различной степени замещения HOHC CHOH соединения вплоть до / гексазамещенных CHOH Табл. 6. Содержание соединений Р в гумусовых горизонтах почв, мг Р 2 О 5/100 г почвы Значительную роль в составе орг. в-ва почв играет фосфор гумусовых веществ – гуминовых к-от, фульвокислот. В составе гуминовых к-от содержится от 2 -3 до 50 -60% всего орг. Р почвы. (Орто-)фосфаты могут быть связаны с орг. в-вами через катионные мостики – Fe, Al, Ca. На долю орг. соединений Р в почвах приходится от 10 -20 до 70 -80% всех запасов фосфора (Табл. 6), поэтому орг. соединения являются значительным резервом обеспечения растений фосфором. Почвы Содержание фосфора Валового органического Органического от валового, % Дерново-подзолистые супесчаные и легкосуглинистые Дерново-подзолистые суглинистые Серые лесные Черноземы выщелоченные Черноземы типичные Черноземы южные карбонатные Каштановые Сероземы Субтропические почвы 105 27 25. 7 117 32 27. 4 148 198 172 148 66 142 79 75 44. 6 71. 7 45. 9 50. 7 149 146 113 34 20 42 22. 8 13. 7 37. 2
 К природным источникам Р относятся также: • изверженные породы (габбро, андезиты, сиениты), при выветривании к-ых Р поступает в биосферу • осадочные породы типа апатитов, фосфоритов желваковых и конкреционных, вивианита, вевеллита • в составе космической пыли и метеоритов. Техногенные пути поступления соединений Р в биосферу, круговорот Р в природе. Значительная часть соединений Р входит в состав: • моющих средств и с их остатками попадает в сточные воды. Стиральные порошки содержат 10 -12% пирофосфата калия HPO 3 или от 4 -5 до 40 -50% триполифосфата натрия и некоторые другие фосфорсодержащие компоненты; • инсектицидов, например, хлорофоса: OH O OCH 3 │ ║⁄ CCl 3—CH— P OCH 3 Вместе с промышленными и бытовыми сточными водами техногенные соединения Р могут поступать в почвы и почвенно-грунтовые воды. Особенности миграции и аккумуляции Р в биосфере заключаются в практически полном отсутствии газообразных соединений в биокруговороте, тогда как обязательными элементами биокруговорота C, S, N являются их газообразные формы. Круговорот Р представляется достаточно простым, незамкнутым циклом: • • • фосфор присутствует в наземных экосистемах в качестве важнейшей части цитоплазмы; затем орг. соединения Р минерализуются в фосфаты; затем фосфаты потребляются корнями растений. В процессе разрушения горных пород соединения фосфора: поступают в наземные экосистемы; значительная часть фосфатов вовлекается в круговорот воды посредством выщелачивания и поступает в воды морей и океанов; здесь соединения Р включаются в пищевые цепи морских экосистем, а какая-то их часть теряется в глубинных отложениях. Частичный возврат Р в биосферу происходит в форме органических удобрений при внесении на поля костнорыбной муки. Таким путем в круговорот возвращается ~60 тыс. т Р, но, конечно, не компенсирует расход в 2 млн. т фосфатов, добываемых из залежей и выщелачивающихся при использовании в качестве удобрений.
К природным источникам Р относятся также: • изверженные породы (габбро, андезиты, сиениты), при выветривании к-ых Р поступает в биосферу • осадочные породы типа апатитов, фосфоритов желваковых и конкреционных, вивианита, вевеллита • в составе космической пыли и метеоритов. Техногенные пути поступления соединений Р в биосферу, круговорот Р в природе. Значительная часть соединений Р входит в состав: • моющих средств и с их остатками попадает в сточные воды. Стиральные порошки содержат 10 -12% пирофосфата калия HPO 3 или от 4 -5 до 40 -50% триполифосфата натрия и некоторые другие фосфорсодержащие компоненты; • инсектицидов, например, хлорофоса: OH O OCH 3 │ ║⁄ CCl 3—CH— P OCH 3 Вместе с промышленными и бытовыми сточными водами техногенные соединения Р могут поступать в почвы и почвенно-грунтовые воды. Особенности миграции и аккумуляции Р в биосфере заключаются в практически полном отсутствии газообразных соединений в биокруговороте, тогда как обязательными элементами биокруговорота C, S, N являются их газообразные формы. Круговорот Р представляется достаточно простым, незамкнутым циклом: • • • фосфор присутствует в наземных экосистемах в качестве важнейшей части цитоплазмы; затем орг. соединения Р минерализуются в фосфаты; затем фосфаты потребляются корнями растений. В процессе разрушения горных пород соединения фосфора: поступают в наземные экосистемы; значительная часть фосфатов вовлекается в круговорот воды посредством выщелачивания и поступает в воды морей и океанов; здесь соединения Р включаются в пищевые цепи морских экосистем, а какая-то их часть теряется в глубинных отложениях. Частичный возврат Р в биосферу происходит в форме органических удобрений при внесении на поля костнорыбной муки. Таким путем в круговорот возвращается ~60 тыс. т Р, но, конечно, не компенсирует расход в 2 млн. т фосфатов, добываемых из залежей и выщелачивающихся при использовании в качестве удобрений.
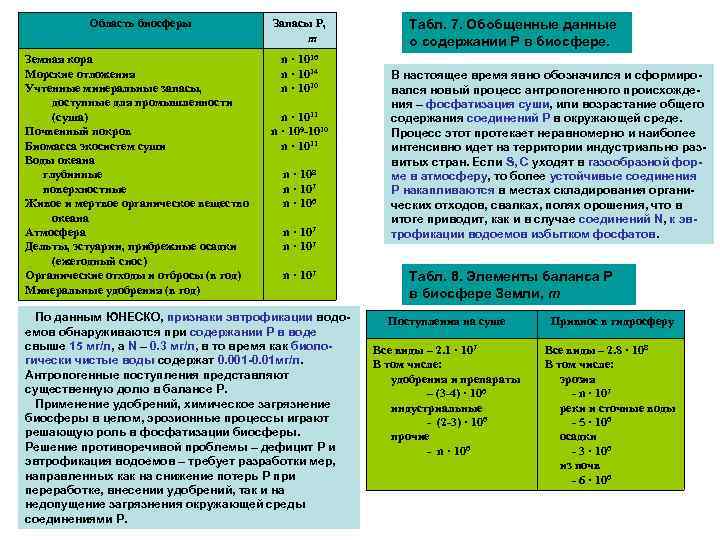 Область биосферы Запасы Р, т Земная кора Морские отложения Учтенные минеральные запасы, доступные для промышленности (суша) Почвенный покров Биомасса экосистем суши Воды океана глубинные поверхностные Живое и мертвое органическое вещество океана Атмосфера Дельты, эстуарии, прибрежные осадки (ежегодный снос) Органические отходы и отбросы (в год) Минеральные удобрения (в год) n · 1016 n · 1014 n · 1010 n · 1011 n · 109 -1010 n · 1011 n · 108 n · 107 n · 106 n · 107 По данным ЮНЕСКО, признаки эвтрофикации водоемов обнаруживаются при содержании Р в воде свыше 15 мг/л, а N – 0. 3 мг/л, в то время как биологически чистые воды содержат 0. 001 -0. 01 мг/л. Антропогенные поступления представляют существенную долю в балансе Р. Применение удобрений, химическое загрязнение биосферы в целом, эрозионные процессы играют решающую роль в фосфатизации биосферы. Решение противоречивой проблемы – дефицит Р и эвтрофикация водоемов – требует разработки мер, направленных как на снижение потерь Р при переработке, внесении удобрений, так и на недопущение загрязнения окружающей среды соединениями Р. Табл. 7. Обобщенные данные о содержании Р в биосфере. В настоящее время явно обозначился и сформировался новый процесс антропогенного происхождения – фосфатизация суши, или возрастание общего содержания соединений Р в окружающей среде. Процесс этот протекает неравномерно и наиболее интенсивно идет на территории индустриально развитых стран. Если S, C уходят в газообразной форме в атмосферу, то более устойчивые соединения Р накапливаются в местах складирования органических отходов, свалках, полях орошения, что в итоге приводит, как и в случае соединений N, к эвтрофикации водоемов избытком фосфатов. Табл. 8. Элементы баланса Р в биосфере Земли, т Поступления на суше Привнос в гидросферу Все виды – 2. 1 · 107 В том числе: удобрения и препараты – (3 -4) · 106 индустриальные - (2 -3) · 106 прочие - n · 106 Все виды – 2. 8 · 108 В том числе: эрозия - n · 107 реки и сточные воды - 5 · 106 осадки - 3 · 106 из почв - 6 · 106
Область биосферы Запасы Р, т Земная кора Морские отложения Учтенные минеральные запасы, доступные для промышленности (суша) Почвенный покров Биомасса экосистем суши Воды океана глубинные поверхностные Живое и мертвое органическое вещество океана Атмосфера Дельты, эстуарии, прибрежные осадки (ежегодный снос) Органические отходы и отбросы (в год) Минеральные удобрения (в год) n · 1016 n · 1014 n · 1010 n · 1011 n · 109 -1010 n · 1011 n · 108 n · 107 n · 106 n · 107 По данным ЮНЕСКО, признаки эвтрофикации водоемов обнаруживаются при содержании Р в воде свыше 15 мг/л, а N – 0. 3 мг/л, в то время как биологически чистые воды содержат 0. 001 -0. 01 мг/л. Антропогенные поступления представляют существенную долю в балансе Р. Применение удобрений, химическое загрязнение биосферы в целом, эрозионные процессы играют решающую роль в фосфатизации биосферы. Решение противоречивой проблемы – дефицит Р и эвтрофикация водоемов – требует разработки мер, направленных как на снижение потерь Р при переработке, внесении удобрений, так и на недопущение загрязнения окружающей среды соединениями Р. Табл. 7. Обобщенные данные о содержании Р в биосфере. В настоящее время явно обозначился и сформировался новый процесс антропогенного происхождения – фосфатизация суши, или возрастание общего содержания соединений Р в окружающей среде. Процесс этот протекает неравномерно и наиболее интенсивно идет на территории индустриально развитых стран. Если S, C уходят в газообразной форме в атмосферу, то более устойчивые соединения Р накапливаются в местах складирования органических отходов, свалках, полях орошения, что в итоге приводит, как и в случае соединений N, к эвтрофикации водоемов избытком фосфатов. Табл. 8. Элементы баланса Р в биосфере Земли, т Поступления на суше Привнос в гидросферу Все виды – 2. 1 · 107 В том числе: удобрения и препараты – (3 -4) · 106 индустриальные - (2 -3) · 106 прочие - n · 106 Все виды – 2. 8 · 108 В том числе: эрозия - n · 107 реки и сточные воды - 5 · 106 осадки - 3 · 106 из почв - 6 · 106



