ОХ_2.ppt (Химия 1 курс)
- Количество слайдов: 44
 Лекция № 2 Развитие представлений о строении атома • СЛОЖНОСТЬ СТРУКТУРЫ АТОМА • прохождение электрического тока через газы и растворы — электрон, катодные лучи • прохождение электрического тока через растворы электролита — катионы и анионы, равенство минимального заряда иона и электрона • А. Беккерель (1896 г. ) открытие радиоактивности • В. Томсон и Д. Д. Томсон (1904 г. ) — модель строения атома (рождественский пудинг) • X. Нагаока 1904 г. — модель строения атома (Сатурн) • Э. Резерфорд (1906— 1911 гг. ) —ядерная модель атома
Лекция № 2 Развитие представлений о строении атома • СЛОЖНОСТЬ СТРУКТУРЫ АТОМА • прохождение электрического тока через газы и растворы — электрон, катодные лучи • прохождение электрического тока через растворы электролита — катионы и анионы, равенство минимального заряда иона и электрона • А. Беккерель (1896 г. ) открытие радиоактивности • В. Томсон и Д. Д. Томсон (1904 г. ) — модель строения атома (рождественский пудинг) • X. Нагаока 1904 г. — модель строения атома (Сатурн) • Э. Резерфорд (1906— 1911 гг. ) —ядерная модель атома
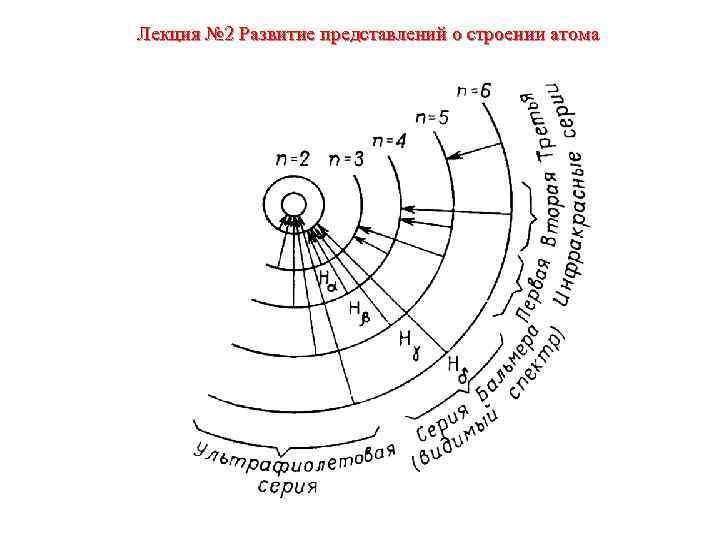
 Лекция № 2 Развитие представлений о строении атома • АТОМНЫЕ СПЕКТРЫ • формулы Бальмера, Ридберга
Лекция № 2 Развитие представлений о строении атома • АТОМНЫЕ СПЕКТРЫ • формулы Бальмера, Ридберга
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома • Квантовая механика базируется на трех основных положениях: • энергетические изменения, происходящие в микросистемах, носят дискретный характер (принцип квантования энергии); • поведение микрочастиц (в том числе и электронов) определяется двойственностью их природы (корпускулярно-волновой дуализм); • законы микромира обусловлены статистическим (вероятностным) характером.
Лекция № 2 Развитие представлений о строении атома • Квантовая механика базируется на трех основных положениях: • энергетические изменения, происходящие в микросистемах, носят дискретный характер (принцип квантования энергии); • поведение микрочастиц (в том числе и электронов) определяется двойственностью их природы (корпускулярно-волновой дуализм); • законы микромира обусловлены статистическим (вероятностным) характером.
 Лекция № 2 Развитие представлений о строении атома • Квантование энергии. Для объяснения особенностей излучения нагретых тел М. Планк в 1900 г. выдвинул предположение, что энергия излучается и поглощается не непрерывно, а дискретно отдельными порциями— квантами. Энергия Е кванта зависит от частоты электромагнитного излучения : • где h — постоянная Планка; = с/ ( — длина волны излучения); с— скорость света. Идея о квантовании энергии позволила объяснить фотоэлектрический эффект (А. Эйнштейн, 1905) и линейчатую структуру атомных спектров (Н. Бор, 1913).
Лекция № 2 Развитие представлений о строении атома • Квантование энергии. Для объяснения особенностей излучения нагретых тел М. Планк в 1900 г. выдвинул предположение, что энергия излучается и поглощается не непрерывно, а дискретно отдельными порциями— квантами. Энергия Е кванта зависит от частоты электромагнитного излучения : • где h — постоянная Планка; = с/ ( — длина волны излучения); с— скорость света. Идея о квантовании энергии позволила объяснить фотоэлектрический эффект (А. Эйнштейн, 1905) и линейчатую структуру атомных спектров (Н. Бор, 1913).
 Лекция № 2 Развитие представлений о строении атома • Корпускулярно-волновой дуализм характеризует способность любого объекта проявлять одновременно волновые и материальные свойства. Двойственная природа микромира была впервые установлена для излучения. С одной стороны, для излучения характерны такие явления, как интерференция и дифракция, которые характеризуют его волновую природу. С другой стороны, излучение проявляет свойства частиц, о чем свидетельствует явление фотоэффекта. Эйнштейн предположил, что излучение испускается в виде частиц, названных фотонами или квантами. Каждый фотон обладает энергией, определяемой уравнением Планка.
Лекция № 2 Развитие представлений о строении атома • Корпускулярно-волновой дуализм характеризует способность любого объекта проявлять одновременно волновые и материальные свойства. Двойственная природа микромира была впервые установлена для излучения. С одной стороны, для излучения характерны такие явления, как интерференция и дифракция, которые характеризуют его волновую природу. С другой стороны, излучение проявляет свойства частиц, о чем свидетельствует явление фотоэффекта. Эйнштейн предположил, что излучение испускается в виде частиц, названных фотонами или квантами. Каждый фотон обладает энергией, определяемой уравнением Планка.
 Лекция № 2 Развитие представлений о строении атома • В силу корпускулярной природы излучения фотоны должны обладать определенной массой. Масса покоя фотона равна нулю, а при движении фотон приобретает динамическую массу. Для вычисления этой массы Эйнштейн обосновал применение уравнения эквивалентности массы и энергии:
Лекция № 2 Развитие представлений о строении атома • В силу корпускулярной природы излучения фотоны должны обладать определенной массой. Масса покоя фотона равна нулю, а при движении фотон приобретает динамическую массу. Для вычисления этой массы Эйнштейн обосновал применение уравнения эквивалентности массы и энергии:
 Лекция № 2 Развитие представлений о строении атома • Французский физик JI. де Бройль в 1923 г. предположил, что двойственной природой обладает не только свет, но и любой материальный объект (в частности, электрон). Длина волны любого движущегося объекта • где m — масса частицы; v — скорость движения частицы; — длина волны объекта, называемая длиной волны де Бройля. Из этого выражения следует, что чем меньше масса частицы, тем больше длина ее волны и тем значительнее проявляются ее волновые свойства.
Лекция № 2 Развитие представлений о строении атома • Французский физик JI. де Бройль в 1923 г. предположил, что двойственной природой обладает не только свет, но и любой материальный объект (в частности, электрон). Длина волны любого движущегося объекта • где m — масса частицы; v — скорость движения частицы; — длина волны объекта, называемая длиной волны де Бройля. Из этого выражения следует, что чем меньше масса частицы, тем больше длина ее волны и тем значительнее проявляются ее волновые свойства.
 Лекция № 2 Развитие представлений о строении атома • Уравнение де Бройля в 1927 г. было подтверждено экспериментально. Американские физики Дж. Дэвиссон и А. Джермер обнаружили дифракцию электронов на монокристаллах никеля Ni. Позднее способность к дифракции была обнаружена у других микрообъектов (атомов гелия Не, молекул водорода Н 2, нейтронов). • В макромире волновые свойства не проявляются — перемещение тел хорошо описывается как движение частиц. Причина заключается в том, что постоянная Планка очень мала (6, 63*10 -34 Дж/Гц), поэтому длины волн оказываются соизмеримыми с размерами частиц только в микромире.
Лекция № 2 Развитие представлений о строении атома • Уравнение де Бройля в 1927 г. было подтверждено экспериментально. Американские физики Дж. Дэвиссон и А. Джермер обнаружили дифракцию электронов на монокристаллах никеля Ni. Позднее способность к дифракции была обнаружена у других микрообъектов (атомов гелия Не, молекул водорода Н 2, нейтронов). • В макромире волновые свойства не проявляются — перемещение тел хорошо описывается как движение частиц. Причина заключается в том, что постоянная Планка очень мала (6, 63*10 -34 Дж/Гц), поэтому длины волн оказываются соизмеримыми с размерами частиц только в микромире.
 Лекция № 2 Развитие представлений о строении атома • Волновые свойства микрочастиц выражаются также в ограниченности применения к ним некоторых понятий классической механики, а именно координаты и импульса. Например, один из способов наблюдения за объектомвоздействие на него электромагнитного излучения (свет, радиоволны) и регистрация отраженного сигнала, что широко используется в радиолокации, эхолокации. Причем сильнее воздействие на наблюдаемый объект, тем сильнее отраженный сигнал.
Лекция № 2 Развитие представлений о строении атома • Волновые свойства микрочастиц выражаются также в ограниченности применения к ним некоторых понятий классической механики, а именно координаты и импульса. Например, один из способов наблюдения за объектомвоздействие на него электромагнитного излучения (свет, радиоволны) и регистрация отраженного сигнала, что широко используется в радиолокации, эхолокации. Причем сильнее воздействие на наблюдаемый объект, тем сильнее отраженный сигнал.
 Лекция № 2 Развитие представлений о строении атома • Если ведется наблюдение за макрообъектами, то действие на них электромагнитного излучения не изменяет ни их положения, ни их скорости. В случае наблюдения за объектами микромира (например, электронами) ситуация выглядит иначе. При действии кванта света (фотона) на микрочастицу ее скорость не остается без изменения. Зная положение микрочастицы в какой-то момент времени, нельзя в это же мгновение определить ее скорость, поскольку она уже изменилась.
Лекция № 2 Развитие представлений о строении атома • Если ведется наблюдение за макрообъектами, то действие на них электромагнитного излучения не изменяет ни их положения, ни их скорости. В случае наблюдения за объектами микромира (например, электронами) ситуация выглядит иначе. При действии кванта света (фотона) на микрочастицу ее скорость не остается без изменения. Зная положение микрочастицы в какой-то момент времени, нельзя в это же мгновение определить ее скорость, поскольку она уже изменилась.
 Лекция № 2 Развитие представлений о строении атома • В. Гейзенберг в 1927 г. предложил соотношения, которые получили название принципа неопределенности. Согласно этому принципу, невозможно одновременно точно определить координаты частицы и ее импульс. • Математически принцип неопределенности формулируется следующим образом: • Из этих соотношений следует, что чем точнее определены координаты электрона, тем с меньшей точностью будет найден его импульс, и наоборот.
Лекция № 2 Развитие представлений о строении атома • В. Гейзенберг в 1927 г. предложил соотношения, которые получили название принципа неопределенности. Согласно этому принципу, невозможно одновременно точно определить координаты частицы и ее импульс. • Математически принцип неопределенности формулируется следующим образом: • Из этих соотношений следует, что чем точнее определены координаты электрона, тем с меньшей точностью будет найден его импульс, и наоборот.
 Лекция № 2 Развитие представлений о строении атома • Движущейся частице можно поставить в соответствие волновой процесс с длиной волны по уравнению де Бройля, тогда этот процесс будет характеризоваться частотой и волновой функцией — величиной, определяющей волнообразно распространяющееся возмущение.
Лекция № 2 Развитие представлений о строении атома • Движущейся частице можно поставить в соответствие волновой процесс с длиной волны по уравнению де Бройля, тогда этот процесс будет характеризоваться частотой и волновой функцией — величиной, определяющей волнообразно распространяющееся возмущение.
 Лекция № 2 Развитие представлений о строении атома • УРАВНЕНИЕ ШРЕДИНГЕРА • принцип неопределенности Гейзенберга (1925 г. )
Лекция № 2 Развитие представлений о строении атома • УРАВНЕНИЕ ШРЕДИНГЕРА • принцип неопределенности Гейзенберга (1925 г. )
 Лекция № 2 Развитие представлений о строении атома • Н. Бор 1913 г. • 1. Электрон может вращаться по определенным круговым орбитам, не излучая энергии. • 2. Ближайшая к ядру орбита отвечает нормальному, наиболее устойчивому состоянию атома. • 3. Поглощение и излучение атомом энергии происходит лишь при перескоке электрона с одной орбиты на другую.
Лекция № 2 Развитие представлений о строении атома • Н. Бор 1913 г. • 1. Электрон может вращаться по определенным круговым орбитам, не излучая энергии. • 2. Ближайшая к ядру орбита отвечает нормальному, наиболее устойчивому состоянию атома. • 3. Поглощение и излучение атомом энергии происходит лишь при перескоке электрона с одной орбиты на другую.
 Лекция № 2 Развитие представлений о строении атома • КВАНТОВЫЕ ЧИСЛА. • n = 1, 2, 3, . . . , • l = 0, 1, 2, . . . , (n— 1) • m= (0; ± 1, ± 2, . . . , ±l) • s= ± 1/2 • l 0 1 2 3 4 5 • s р d f g h
Лекция № 2 Развитие представлений о строении атома • КВАНТОВЫЕ ЧИСЛА. • n = 1, 2, 3, . . . , • l = 0, 1, 2, . . . , (n— 1) • m= (0; ± 1, ± 2, . . . , ±l) • s= ± 1/2 • l 0 1 2 3 4 5 • s р d f g h
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
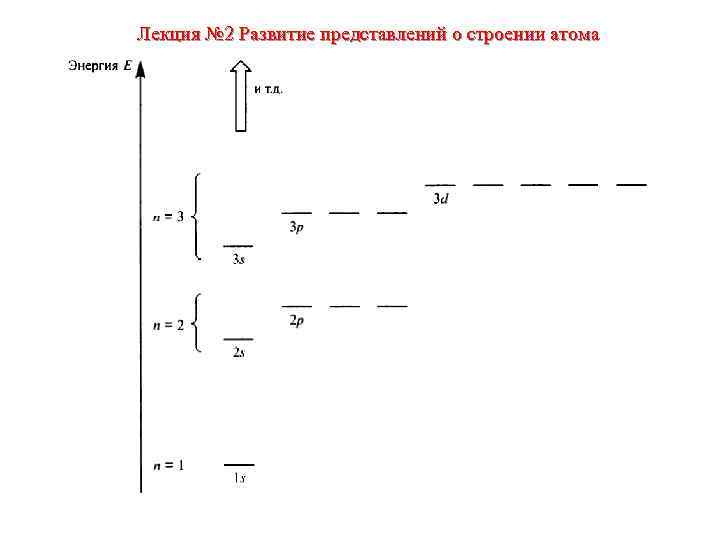
 Лекция № 2 Развитие представлений о строении атома • принцип минимальной энергии электронные уровни заполняются в направлении нарастания энергии уровня • правило Хунда наиболее устойчивое распределение электронов по орбиталям имеет максимальный суммарный спин • запрет Паули в многоэлектронном атоме или ионе не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы. • принцип Клечковского энергия электронных уровней нарастает в направлении роста суммы главного и орбитального квантовых чисел
Лекция № 2 Развитие представлений о строении атома • принцип минимальной энергии электронные уровни заполняются в направлении нарастания энергии уровня • правило Хунда наиболее устойчивое распределение электронов по орбиталям имеет максимальный суммарный спин • запрет Паули в многоэлектронном атоме или ионе не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы. • принцип Клечковского энергия электронных уровней нарастает в направлении роста суммы главного и орбитального квантовых чисел
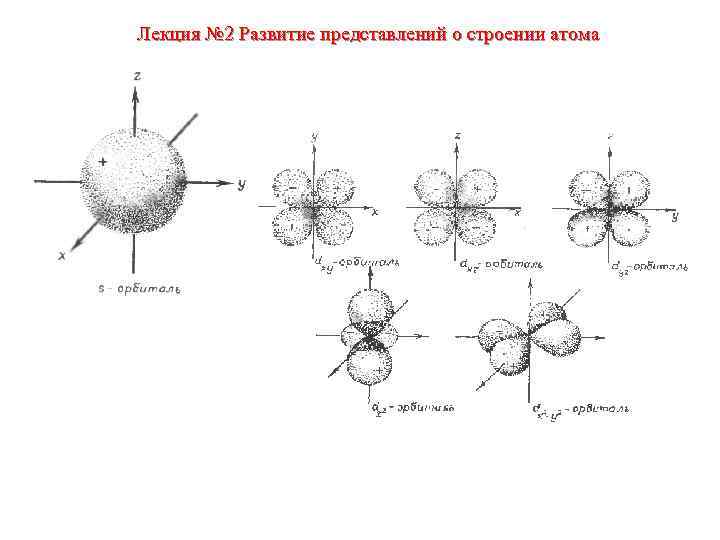
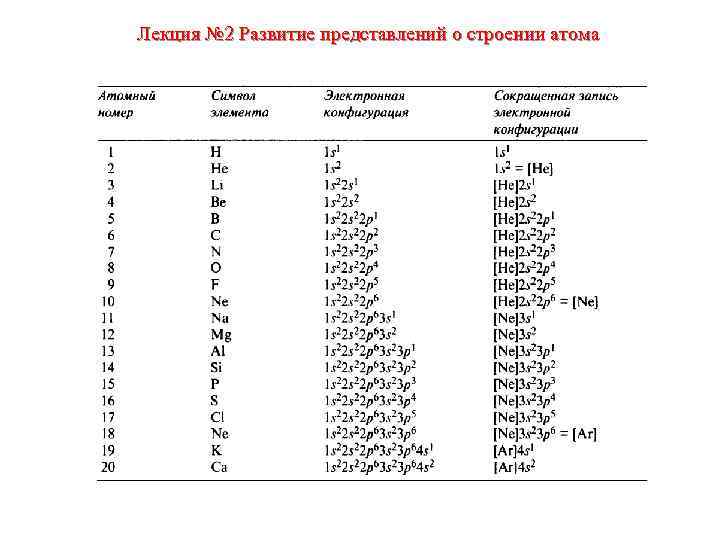
 Лекция № 2 Развитие представлений о строении атома • п = 1 • Если п = 1, то l = 0 и m = 0. • Величина l = 0 соответствует однократно вырожденной sорбитали. • Существует только одно разрешенное значение для m (m=0). • Тогда, для п = 1 разрешена 1 s-атомная орбиталь.
Лекция № 2 Развитие представлений о строении атома • п = 1 • Если п = 1, то l = 0 и m = 0. • Величина l = 0 соответствует однократно вырожденной sорбитали. • Существует только одно разрешенное значение для m (m=0). • Тогда, для п = 1 разрешена 1 s-атомная орбиталь.
 Лекция № 2 Развитие представлений о строении атома • п = 2 • Если п = 2, то l = 0 или 1. • Рассмотрим отдельно каждое значение l. • Для 1 = 0 существует одна s-орбиталь, это 2 S-орбиталь. • Для l= 1 разрешенные значения для т 1, 0, -1 соответствуют трем р-орбиталям. • Итак, для п = 2 разрешенными орбиталями являются 2 s, 2 рх, 2 ру и 2 pz
Лекция № 2 Развитие представлений о строении атома • п = 2 • Если п = 2, то l = 0 или 1. • Рассмотрим отдельно каждое значение l. • Для 1 = 0 существует одна s-орбиталь, это 2 S-орбиталь. • Для l= 1 разрешенные значения для т 1, 0, -1 соответствуют трем р-орбиталям. • Итак, для п = 2 разрешенными орбиталями являются 2 s, 2 рх, 2 ру и 2 pz
 Лекция № 2 Развитие представлений о строении атома • п=3 • Если п = 3, то l = 2, 1 или 0. • Рассмотрим отдельно каждое значение l. • Для l = 0 существует одна s-орбиталь, обозначаемая 3 s. • Для l= 1 разрешенные значения для m 1, 0, -1 соответствуют трем р-орбиталям. • Для l= 2 m может быть равно 2, 1, 0, -1 и -2, это соответствует набору из пяти d-орбиталей. • Следовательно, для п = 3 разрешены 3 s-, 3 рх, 3 ру и 3 pz- и пять d-орбиталей.
Лекция № 2 Развитие представлений о строении атома • п=3 • Если п = 3, то l = 2, 1 или 0. • Рассмотрим отдельно каждое значение l. • Для l = 0 существует одна s-орбиталь, обозначаемая 3 s. • Для l= 1 разрешенные значения для m 1, 0, -1 соответствуют трем р-орбиталям. • Для l= 2 m может быть равно 2, 1, 0, -1 и -2, это соответствует набору из пяти d-орбиталей. • Следовательно, для п = 3 разрешены 3 s-, 3 рх, 3 ру и 3 pz- и пять d-орбиталей.
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
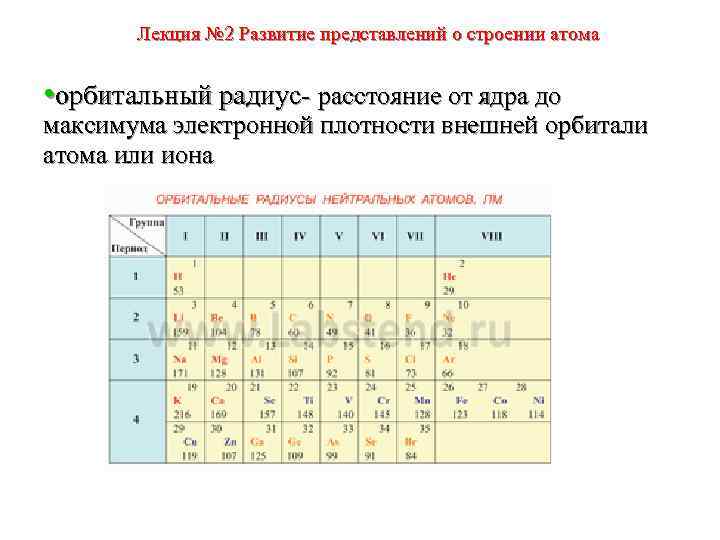 Лекция № 2 Развитие представлений о строении атома • орбитальный радиус- расстояние от ядра до максимума электронной плотности внешней орбитали атома или иона
Лекция № 2 Развитие представлений о строении атома • орбитальный радиус- расстояние от ядра до максимума электронной плотности внешней орбитали атома или иона
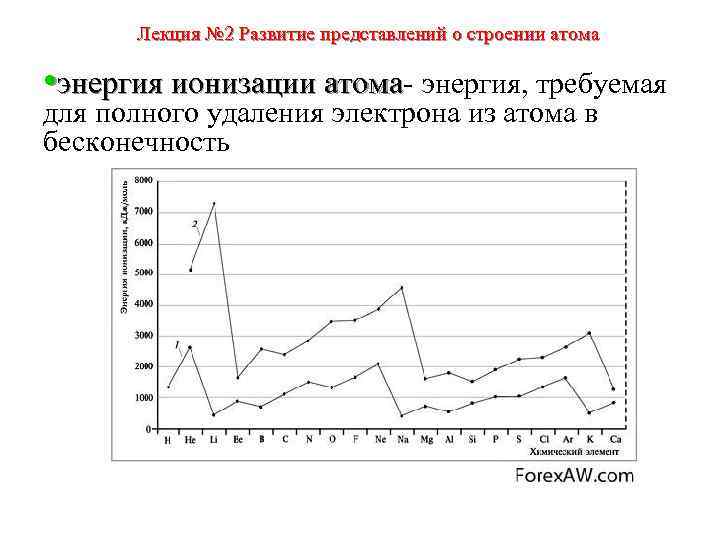 Лекция № 2 Развитие представлений о строении атома • энергия ионизации атома- энергия, требуемая атома для полного удаления электрона из атома в бесконечность
Лекция № 2 Развитие представлений о строении атома • энергия ионизации атома- энергия, требуемая атома для полного удаления электрона из атома в бесконечность
 Лекция № 2 Развитие представлений о строении атома • сродство к электрону- изменение энергии присоединении одного электрона атомом
Лекция № 2 Развитие представлений о строении атома • сродство к электрону- изменение энергии присоединении одного электрона атомом
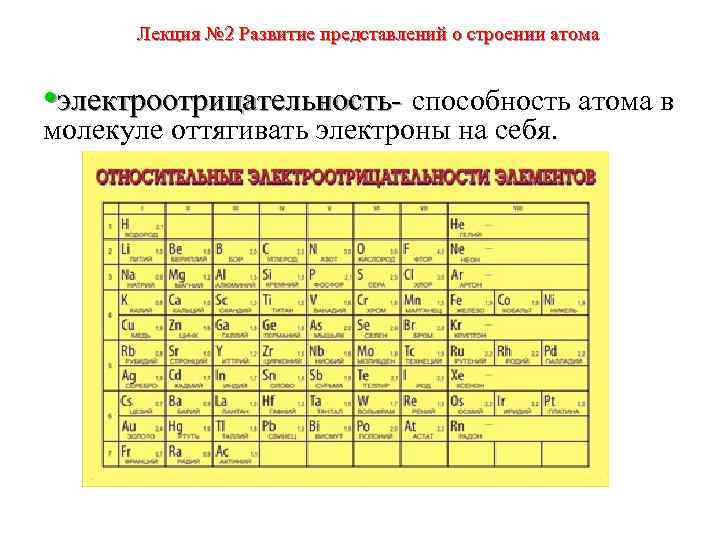 Лекция № 2 Развитие представлений о строении атома • электроотрицательность- способность атома в молекуле оттягивать электроны на себя.
Лекция № 2 Развитие представлений о строении атома • электроотрицательность- способность атома в молекуле оттягивать электроны на себя.
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома
 Лекция № 2 Развитие представлений о строении атома
Лекция № 2 Развитие представлений о строении атома


