 Лекция 2. Растворы
Лекция 2. Растворы
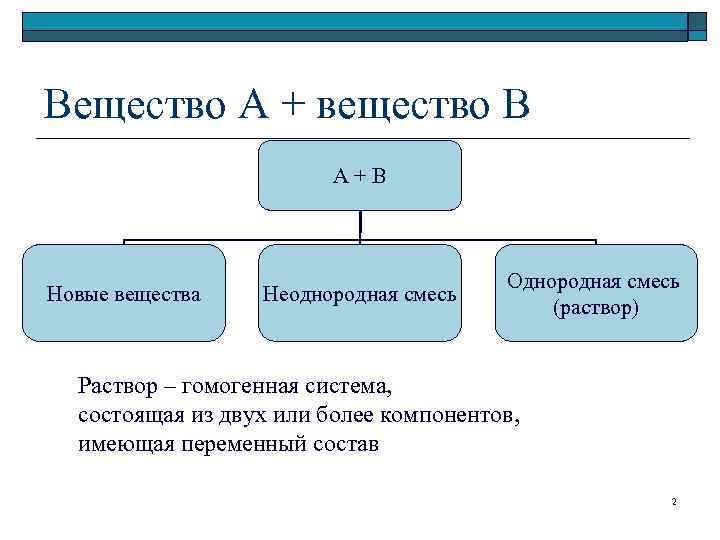 Вещество А + вещество В А + В Новые вещества Неоднородная смесь Однородная смесь (раствор) Раствор – гомогенная система, состоящая из двух или более компонентов, имеющая переменный состав 2
Вещество А + вещество В А + В Новые вещества Неоднородная смесь Однородная смесь (раствор) Раствор – гомогенная система, состоящая из двух или более компонентов, имеющая переменный состав 2
 Смеси веществ o o o Смеси Грубодисперсные системы (взвеси) Тонкодисперсные системы (коллоидные системы) Истинные растворы o Размеры частиц более 100 нм o 1 – 100 нм o менее 1 нм 3
Смеси веществ o o o Смеси Грубодисперсные системы (взвеси) Тонкодисперсные системы (коллоидные системы) Истинные растворы o Размеры частиц более 100 нм o 1 – 100 нм o менее 1 нм 3
 Истинные растворы o o o Агрегатное состояние: газообразные, жидкие, твердые растворы Состав раствора: растворитель + растворенное вещество Параметры раствора: температура, давление, содержание растворенного вещества 4
Истинные растворы o o o Агрегатное состояние: газообразные, жидкие, твердые растворы Состав раствора: растворитель + растворенное вещество Параметры раствора: температура, давление, содержание растворенного вещества 4
 Способы выражения концентрации растворов o o o Массовая доля Молярная концентрация (молярность), моль/л Эквивалентная концентрация (нормальность), моль/л Мольная доля Моляльная концентрация (моляльность), моль/кг 5
Способы выражения концентрации растворов o o o Массовая доля Молярная концентрация (молярность), моль/л Эквивалентная концентрация (нормальность), моль/л Мольная доля Моляльная концентрация (моляльность), моль/кг 5
 Растворы o Ненасыщенные n o Вт → Вр Насыщенные n o Концентрация вещества меньше его растворимости Растворимость вещества – его концентрация в насыщенном растворе Вт Вр; истинное равновесие Пересыщенные n Вр; метастабильное равновесие Концентрация вещества больше его растворимости 6
Растворы o Ненасыщенные n o Вт → Вр Насыщенные n o Концентрация вещества меньше его растворимости Растворимость вещества – его концентрация в насыщенном растворе Вт Вр; истинное равновесие Пересыщенные n Вр; метастабильное равновесие Концентрация вещества больше его растворимости 6
 Растворимость газов в жидкостях Если нет химического взаимодействия Ar(г) Ar(р) Влияние давления = 1 0 (принцип Ле Шателье) Увеличение давления → (растворимость увеличивается) Уменьшение давления ← (растворимость уменьшается) 7
Растворимость газов в жидкостях Если нет химического взаимодействия Ar(г) Ar(р) Влияние давления = 1 0 (принцип Ле Шателье) Увеличение давления → (растворимость увеличивается) Уменьшение давления ← (растворимость уменьшается) 7
 Растворимость газов в жидкостях Влияние температуры Qразрыв связей ≈ 0 Qрастворение > 0 Qобразование связей > 0 Процесс экзотермический (принцип Ле Шателье) Уменьшение температуры → (растворимость увеличивается) Увеличение температуры ← (растворимость уменьшается) 8
Растворимость газов в жидкостях Влияние температуры Qразрыв связей ≈ 0 Qрастворение > 0 Qобразование связей > 0 Процесс экзотермический (принцип Ле Шателье) Уменьшение температуры → (растворимость увеличивается) Увеличение температуры ← (растворимость уменьшается) 8
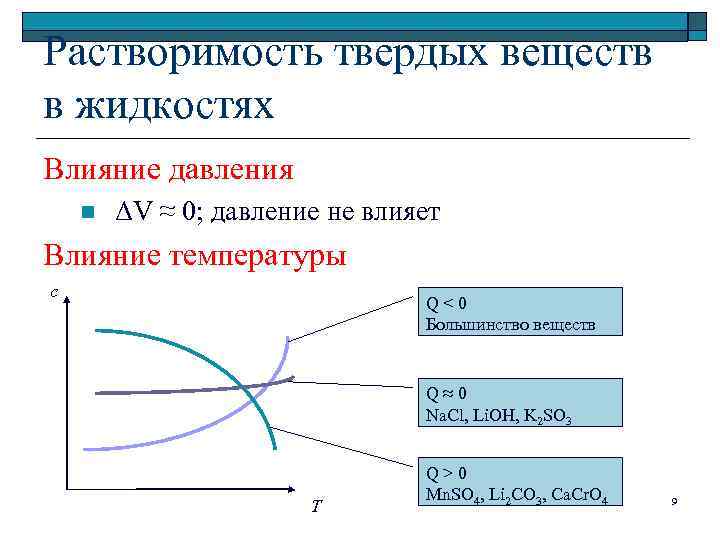 Растворимость твердых веществ в жидкостях Влияние давления n ΔV ≈ 0; давление не влияет Влияние температуры с Q < 0 Большинство веществ Q ≈ 0 Na. Cl, Li. OH, K 2 SO 3 Т Q > 0 Mn. SO 4, Li 2 CO 3, Ca. Cr. O 4 9
Растворимость твердых веществ в жидкостях Влияние давления n ΔV ≈ 0; давление не влияет Влияние температуры с Q < 0 Большинство веществ Q ≈ 0 Na. Cl, Li. OH, K 2 SO 3 Т Q > 0 Mn. SO 4, Li 2 CO 3, Ca. Cr. O 4 9
 Растворы электролитов Электролитическая диссоциация
Растворы электролитов Электролитическая диссоциация
 Степень диссоциации - отношение количества электролита, распавшегося на ионы, к общему количеству растворенного электролита: 0 = nр/no , где 0 - истинная степень ЭД, nр - количество молекул (формульных единиц) электролита, распавшихся на ионы в растворе; no - общее число молекул (формульных единиц) электролита, перешедшее в раствор. Степень диссоциации прямо пропорциональна • полярности и поляризуемости химической связи в электролите, • диэлектрической проницаемости среды, • температуре раствора и обратно пропорциональна концентрации раствора По степени ЭД все электролиты делятся на 2 типа: сильные электролиты ( 0 > 0, 7) и слабые электролиты (0< 0< 0, 1). Сильными электролиты: сильные кислоты, щелочи и большинство солей (НС 1, H 2 SО 4, HNO 3, КОН, Na. OH, Ba(OH)2, Na. Cl, KN 03). Слабые электролиты: слабые кислоты и слабые основания (СН 3 СООН, Н 2 СО 3, HCN, HF, HNO 2, NH 3 • H 2 O) и H 2 O.
Степень диссоциации - отношение количества электролита, распавшегося на ионы, к общему количеству растворенного электролита: 0 = nр/no , где 0 - истинная степень ЭД, nр - количество молекул (формульных единиц) электролита, распавшихся на ионы в растворе; no - общее число молекул (формульных единиц) электролита, перешедшее в раствор. Степень диссоциации прямо пропорциональна • полярности и поляризуемости химической связи в электролите, • диэлектрической проницаемости среды, • температуре раствора и обратно пропорциональна концентрации раствора По степени ЭД все электролиты делятся на 2 типа: сильные электролиты ( 0 > 0, 7) и слабые электролиты (0< 0< 0, 1). Сильными электролиты: сильные кислоты, щелочи и большинство солей (НС 1, H 2 SО 4, HNO 3, КОН, Na. OH, Ba(OH)2, Na. Cl, KN 03). Слабые электролиты: слабые кислоты и слабые основания (СН 3 СООН, Н 2 СО 3, HCN, HF, HNO 2, NH 3 • H 2 O) и H 2 O.
![Сильные электролиты MA M+(р) + A–(р) [MA] = 0, [M+] = [A–] = c Сильные электролиты MA M+(р) + A–(р) [MA] = 0, [M+] = [A–] = c](https://present5.com/presentation/-72216801_303122090/image-12.jpg) Сильные электролиты MA M+(р) + A–(р) [MA] = 0, [M+] = [A–] = c 0 Степень диссоциации: 12
Сильные электролиты MA M+(р) + A–(р) [MA] = 0, [M+] = [A–] = c 0 Степень диссоциации: 12
![Слабые электролиты MA(р) + M+(р) + A–(р) [MA] > 0, [M+] = [A–] < Слабые электролиты MA(р) + M+(р) + A–(р) [MA] > 0, [M+] = [A–] <](https://present5.com/presentation/-72216801_303122090/image-13.jpg) Слабые электролиты MA(р) + M+(р) + A–(р) [MA] > 0, [M+] = [A–] < c 0 Степень диссоциации: 13
Слабые электролиты MA(р) + M+(р) + A–(р) [MA] > 0, [M+] = [A–] < c 0 Степень диссоциации: 13
 Слабые электролиты Mx. Ay(р) x Ma+(р) + y Ab–(р) Константа диссоциации KD 14
Слабые электролиты Mx. Ay(р) x Ma+(р) + y Ab–(р) Константа диссоциации KD 14
 Слабые многоосновные кислоты и слабые многокислотные основания диссоциируют в несколько этапов ( ступенчато ): I cтупень: Н 2 СО 3 ↔ Н+ + НСО 3 - KD 1= ; II ступень: НСО 3 - ↔ H+ + CO 32 - KD 2 = Суммарно ЭД H 2 CO 3 ↔ 2 H+ + CO 32 - KD(общ) = . KD 1 >> KD 2 >> KD 3 и т. д.
Слабые многоосновные кислоты и слабые многокислотные основания диссоциируют в несколько этапов ( ступенчато ): I cтупень: Н 2 СО 3 ↔ Н+ + НСО 3 - KD 1= ; II ступень: НСО 3 - ↔ H+ + CO 32 - KD 2 = Суммарно ЭД H 2 CO 3 ↔ 2 H+ + CO 32 - KD(общ) = . KD 1 >> KD 2 >> KD 3 и т. д.
![Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+] Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+]](https://present5.com/presentation/-72216801_303122090/image-16.jpg) Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+] = [A–] = c 0 [MA] = (1 – ) c 0 KD = 2 c 0 / (1 – ) если << 1 ( < 0, 05) KD = 2 c 0 o α 1 c 0 16
Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+] = [A–] = c 0 [MA] = (1 – ) c 0 KD = 2 c 0 / (1 – ) если << 1 ( < 0, 05) KD = 2 c 0 o α 1 c 0 16
 Классическая теория кислот и оснований Аррениуса. 17
Классическая теория кислот и оснований Аррениуса. 17
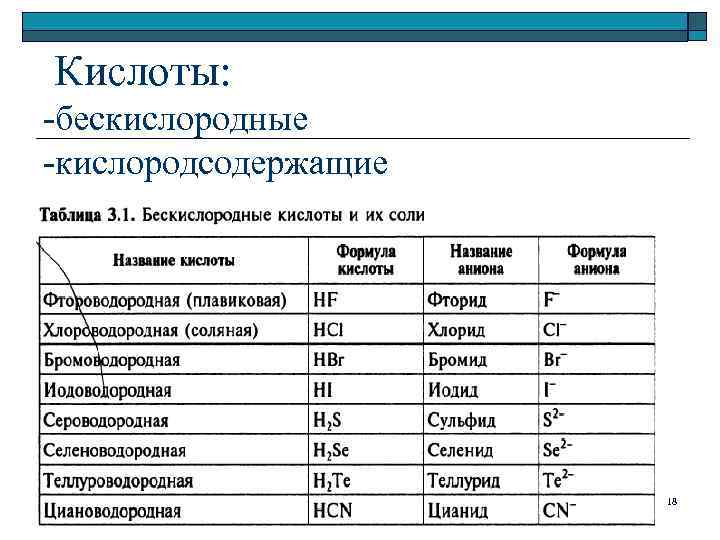 Кислоты: -бескислородные -кислородсодержащие 18
Кислоты: -бескислородные -кислородсодержащие 18
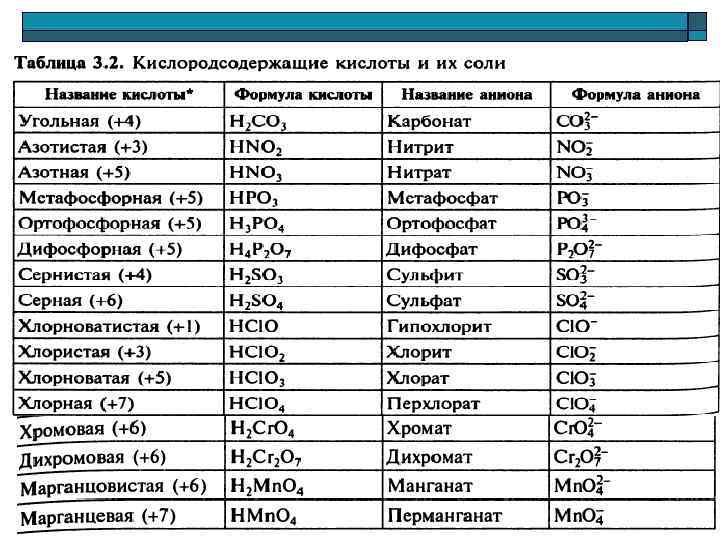 19
19
 Основания 20
Основания 20
 Протолитическая теория кислот и оснований 1923 г. Йоханес Брёнстед Томас Лаури
Протолитическая теория кислот и оснований 1923 г. Йоханес Брёнстед Томас Лаури
 В 1923 г. И. Бренстед и Т. Лоури предложили общую протолитическую теорию кислот и оснований. Кислота - молекула или ион, способные отдавать катион водорода (протон). Кислота - донор протонов. СН 3 СООH H+ + СН 3 СОО– слабая сопряж. к-та сопряж. основание Основание — молекула или ион, способные присоединять катион водорода (протон). Основание - акцептор протонов. ОН- + Н+ = Н 2 О NH 3 +Н+= = NH 4+ отдавая протон, кислота превращается в основание, которое называют сопряженным этой кислоте
В 1923 г. И. Бренстед и Т. Лоури предложили общую протолитическую теорию кислот и оснований. Кислота - молекула или ион, способные отдавать катион водорода (протон). Кислота - донор протонов. СН 3 СООH H+ + СН 3 СОО– слабая сопряж. к-та сопряж. основание Основание — молекула или ион, способные присоединять катион водорода (протон). Основание - акцептор протонов. ОН- + Н+ = Н 2 О NH 3 +Н+= = NH 4+ отдавая протон, кислота превращается в основание, которое называют сопряженным этой кислоте
 Амфолиты — молекулы или ионы, способные как отдавать, так и присоединять протон, а следовательно, вступать в реакции, характерные как для кислот, так и для оснований. Н 2 О + НСl = Н 3 О+ + СГ Н 2 О + NH 3 = NH 4+ + ОНАмфолитами являются v гидроксиды некоторых металлов (Zn, Al, Pb, Sn, Cr) v гидроанионы многоосновных кислот, например НСОз-, НРО 42 v соединения, молекулы которых содержат две различные кислотно-основные группы, H 2 N—CHR—СООН 23
Амфолиты — молекулы или ионы, способные как отдавать, так и присоединять протон, а следовательно, вступать в реакции, характерные как для кислот, так и для оснований. Н 2 О + НСl = Н 3 О+ + СГ Н 2 О + NH 3 = NH 4+ + ОНАмфолитами являются v гидроксиды некоторых металлов (Zn, Al, Pb, Sn, Cr) v гидроанионы многоосновных кислот, например НСОз-, НРО 42 v соединения, молекулы которых содержат две различные кислотно-основные группы, H 2 N—CHR—СООН 23
 кислотные или основные свойства частиц обусловлены их способностью отдавать или присоединять катион водорода (протон Н+) Н+ NH 4+ + S 2– NH 3 + HS– Кт Ос Кт Пары "сопряженная кислота / сопряженное основание": NH 4+/NH 3 и HS –/ S 2– 24
кислотные или основные свойства частиц обусловлены их способностью отдавать или присоединять катион водорода (протон Н+) Н+ NH 4+ + S 2– NH 3 + HS– Кт Ос Кт Пары "сопряженная кислота / сопряженное основание": NH 4+/NH 3 и HS –/ S 2– 24
 Растворители o Апротонные: n o C 6 H 6, CS 2, CCl 4 Протонные n H 2 O, NH 3, C 2 H 5 OH (амфолиты) Автопротолиз: H+ HL H 2 L+ + L– o Константа автопротолиза (ионное произведение): KS = [H 2 L+] [L–] o 25
Растворители o Апротонные: n o C 6 H 6, CS 2, CCl 4 Протонные n H 2 O, NH 3, C 2 H 5 OH (амфолиты) Автопротолиз: H+ HL H 2 L+ + L– o Константа автопротолиза (ионное произведение): KS = [H 2 L+] [L–] o 25
 Ионное произведение воды H+ H+ H 2 O + H 2 O H 3 O+ + OH– При стандартной температуре 298 К (25 С): KB (Kw) = [H 3 O+] [OH–] KB (Kw) = [H+] [OH–]= 1. 10– 14 В чистой воде при 25 С [H+] = [OH–] = KB = 10– 7 моль/л 26
Ионное произведение воды H+ H+ H 2 O + H 2 O H 3 O+ + OH– При стандартной температуре 298 К (25 С): KB (Kw) = [H 3 O+] [OH–] KB (Kw) = [H+] [OH–]= 1. 10– 14 В чистой воде при 25 С [H+] = [OH–] = KB = 10– 7 моль/л 26
![Водородный показатель (р. Н) р. Н = –lg[H+] = 10–р. Н Гидроксидный показатель (р. Водородный показатель (р. Н) р. Н = –lg[H+] = 10–р. Н Гидроксидный показатель (р.](https://present5.com/presentation/-72216801_303122090/image-27.jpg) Водородный показатель (р. Н) р. Н = –lg[H+] = 10–р. Н Гидроксидный показатель (р. ОН) p. OH = –lg[OH–] = 10–р. ОН р. Н + р. ОН = –lg. KB = 14 27
Водородный показатель (р. Н) р. Н = –lg[H+] = 10–р. Н Гидроксидный показатель (р. ОН) p. OH = –lg[OH–] = 10–р. ОН р. Н + р. ОН = –lg. KB = 14 27
 Водородный показатель (р. Н) В чистой воде при 25 С р. Н = р. ОН = 7 Среда нейтральная Если [H+] > 1. 10– 7, то р. Н < 7 Среда кислая Если [OH–] > 1. 10– 7, то р. ОН < 7 и p. H > 7 Среда щелочная Следовательно, р. Н и р. ОН являются сопряжёнными величинами: если р. Н = 3, то р. ОН = 14 – 3 = 11. р. Н крови = 7, 3 -7, 4 р. Н желудочного сока = 0, 9 -1, 5 [взр. ], § у новорожденных — 7, 0; § у детей 4 -7 лет — 2, 5; § у детей 14 лет — 2, 0 28 р. Н слюны = 7, 3 -7, 9
Водородный показатель (р. Н) В чистой воде при 25 С р. Н = р. ОН = 7 Среда нейтральная Если [H+] > 1. 10– 7, то р. Н < 7 Среда кислая Если [OH–] > 1. 10– 7, то р. ОН < 7 и p. H > 7 Среда щелочная Следовательно, р. Н и р. ОН являются сопряжёнными величинами: если р. Н = 3, то р. ОН = 14 – 3 = 11. р. Н крови = 7, 3 -7, 4 р. Н желудочного сока = 0, 9 -1, 5 [взр. ], § у новорожденных — 7, 0; § у детей 4 -7 лет — 2, 5; § у детей 14 лет — 2, 0 28 р. Н слюны = 7, 3 -7, 9
![Шкала р. Н При [H+] = 0, 1 моль/л (например, в 0, 1 М Шкала р. Н При [H+] = 0, 1 моль/л (например, в 0, 1 М](https://present5.com/presentation/-72216801_303122090/image-29.jpg) Шкала р. Н При [H+] = 0, 1 моль/л (например, в 0, 1 М растворе HCl) p. H = 1 (нижний предел). При [OH–] = 0, 1 моль/л (например, в 0, 1 М растворе KOH) р. Н = 13 (верхний предел). 29
Шкала р. Н При [H+] = 0, 1 моль/л (например, в 0, 1 М растворе HCl) p. H = 1 (нижний предел). При [OH–] = 0, 1 моль/л (например, в 0, 1 М растворе KOH) р. Н = 13 (верхний предел). 29
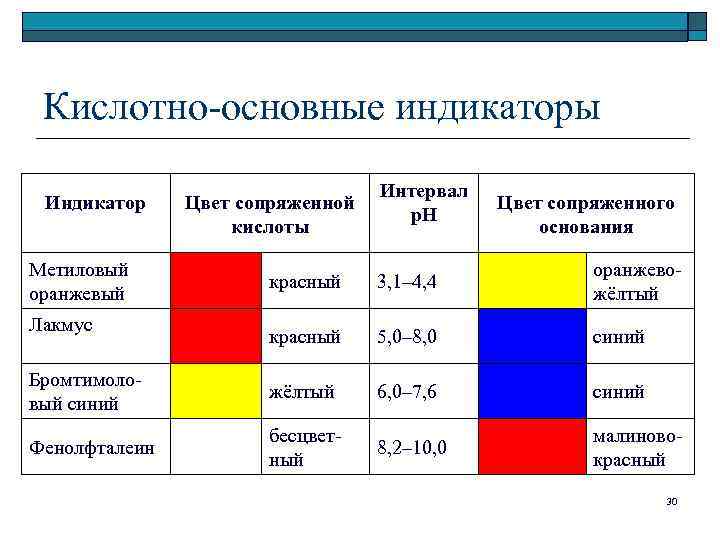 Кислотно-основные индикаторы Индикатор Метиловый оранжевый Цвет сопряженной кислоты Интервал p. H Цвет сопряженного основания красный 3, 1– 4, 4 оранжевожёлтый красный 5, 0– 8, 0 синий Бромтимоловый синий жёлтый 6, 0– 7, 6 синий Фенолфталеин бесцветный 8, 2– 10, 0 малиновокрасный Лакмус 30
Кислотно-основные индикаторы Индикатор Метиловый оранжевый Цвет сопряженной кислоты Интервал p. H Цвет сопряженного основания красный 3, 1– 4, 4 оранжевожёлтый красный 5, 0– 8, 0 синий Бромтимоловый синий жёлтый 6, 0– 7, 6 синий Фенолфталеин бесцветный 8, 2– 10, 0 малиновокрасный Лакмус 30


