Лекция № 2 Поверхностное натяжение






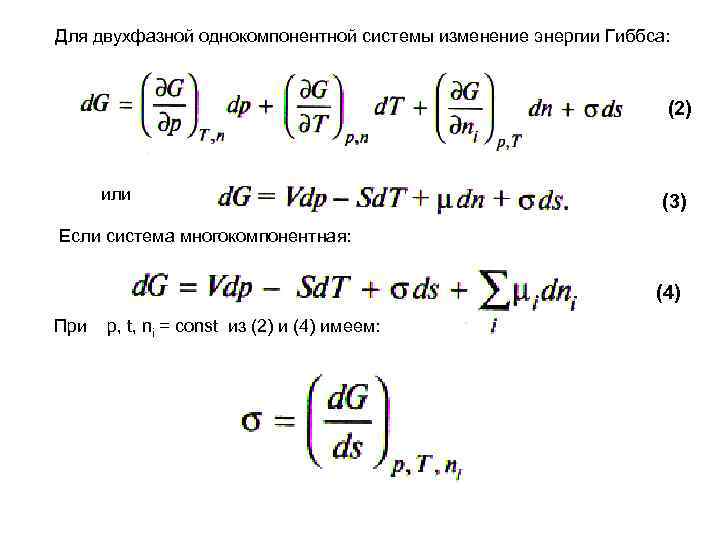



















поверхностное натяжение.ppt
- Количество слайдов: 37
 Лекция № 2 Поверхностное натяжение
Лекция № 2 Поверхностное натяжение
 Поверхностная энергия и поверхностное натяжение на границе раздела жидкость воздух
Поверхностная энергия и поверхностное натяжение на границе раздела жидкость воздух
 Дисперсная система Насыщенный пар Избыток свободной энергии, Fs 1 Жидкость 1 Взаимодействия: Диполь-дипольные Индукционные Дисперсионные Fсист = Fж + Fн. п. + Fs Водородные связи……
Дисперсная система Насыщенный пар Избыток свободной энергии, Fs 1 Жидкость 1 Взаимодействия: Диполь-дипольные Индукционные Дисперсионные Fсист = Fж + Fн. п. + Fs Водородные связи……
 ПРИМЕРЫ ДЕЙСТВИЯ СИЛЫ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ Водомерка Игла на поверхности воды P = m g = σ l, где m – масса объекта, g – ускорение силы тяжести, σ – поверхностное натяжение воды, l – суммарный периметр контакта с поверхностью воды.
ПРИМЕРЫ ДЕЙСТВИЯ СИЛЫ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ Водомерка Игла на поверхности воды P = m g = σ l, где m – масса объекта, g – ускорение силы тяжести, σ – поверхностное натяжение воды, l – суммарный периметр контакта с поверхностью воды.
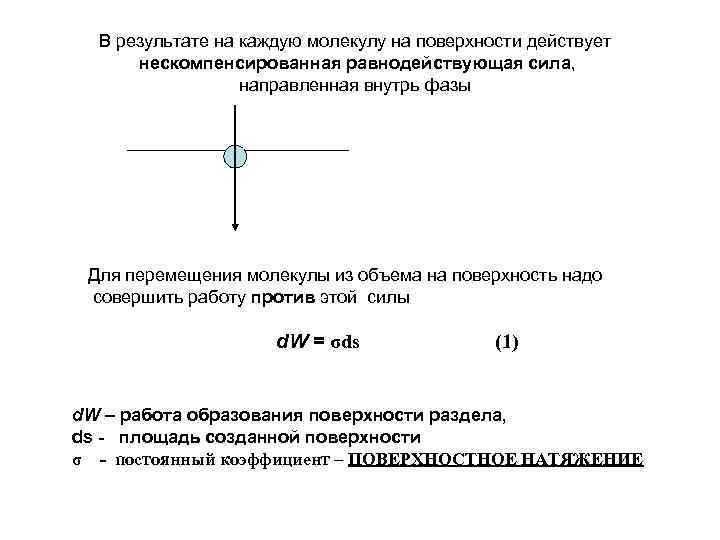
 В результате на каждую молекулу на поверхности действует нескомпенсированная равнодействующая сила, направленная внутрь фазы Для перемещения молекулы из объема на поверхность надо совершить работу против этой силы d. W = σds (1) d. W – работа образования поверхности раздела, ds - площадь созданной поверхности σ - постоянный коэффициент – ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ
В результате на каждую молекулу на поверхности действует нескомпенсированная равнодействующая сила, направленная внутрь фазы Для перемещения молекулы из объема на поверхность надо совершить работу против этой силы d. W = σds (1) d. W – работа образования поверхности раздела, ds - площадь созданной поверхности σ - постоянный коэффициент – ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ
 Поверхностное натяжение (σ) – равно работе образования единицы площади поверхности в обратимом изотермическом процессе [Дж/м 2]
Поверхностное натяжение (σ) – равно работе образования единицы площади поверхности в обратимом изотермическом процессе [Дж/м 2]
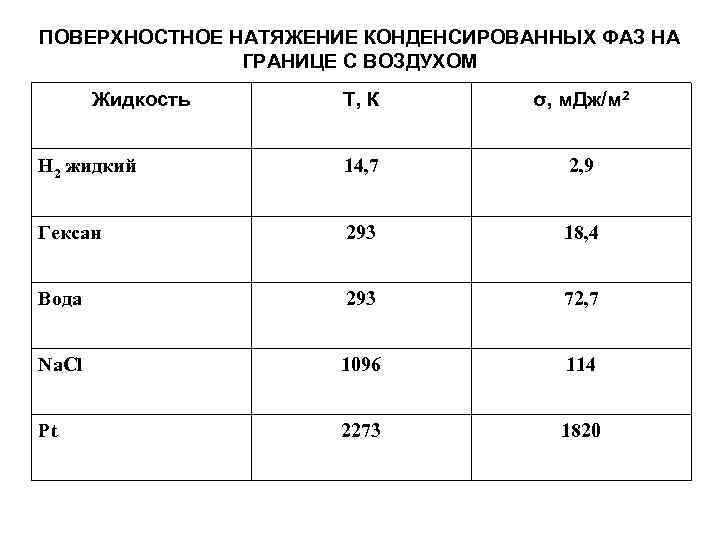
 ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ КОНДЕНСИРОВАННЫХ ФАЗ НА ГРАНИЦЕ С ВОЗДУХОМ Жидкость Т, К σ, м. Дж/м 2 Н 2 жидкий 14, 7 2, 9 Гексан 293 18, 4 Вода 293 72, 7 Na. Cl 1096 114 Pt 2273 1820
ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ КОНДЕНСИРОВАННЫХ ФАЗ НА ГРАНИЦЕ С ВОЗДУХОМ Жидкость Т, К σ, м. Дж/м 2 Н 2 жидкий 14, 7 2, 9 Гексан 293 18, 4 Вода 293 72, 7 Na. Cl 1096 114 Pt 2273 1820
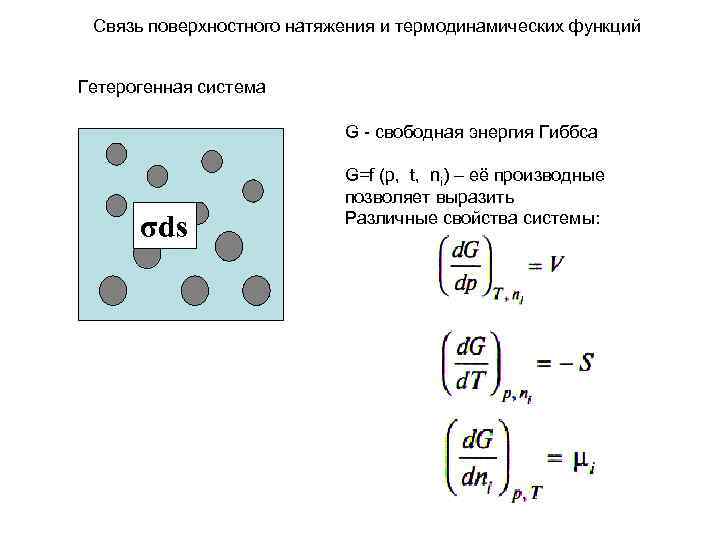
 Связь поверхностного натяжения и термодинамических функций Гетерогенная система G - свободная энергия Гиббса G=f (p, t, ni) – её производные позволяет выразить σds Различные свойства системы:
Связь поверхностного натяжения и термодинамических функций Гетерогенная система G - свободная энергия Гиббса G=f (p, t, ni) – её производные позволяет выразить σds Различные свойства системы:
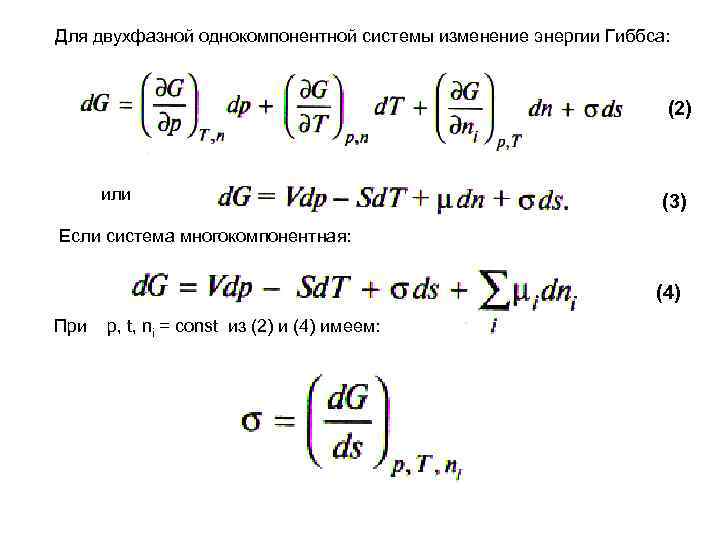 Для двухфазной однокомпонентной системы изменение энергии Гиббса: (2) или (3) Если система многокомпонентная: (4) При р, t, ni = const из (2) и (4) имеем:
Для двухфазной однокомпонентной системы изменение энергии Гиббса: (2) или (3) Если система многокомпонентная: (4) При р, t, ni = const из (2) и (4) имеем:
 Поверхностное натяжение – есть частная производная от свободной энергии Гиббса по площади межфазной поверхности при постоянстве температуры давления и числа молей компонентов
Поверхностное натяжение – есть частная производная от свободной энергии Гиббса по площади межфазной поверхности при постоянстве температуры давления и числа молей компонентов
 Аналогичные уравнения для гетерогенной системы можно записать для других термодинамических функций: Свободной энергии Гельмгольца: F= f (V, T, ni) Внутренней энергии: U = f (S, V, ni) Энтальпии: H = f (S, p, n i) (6) (7) (8)
Аналогичные уравнения для гетерогенной системы можно записать для других термодинамических функций: Свободной энергии Гельмгольца: F= f (V, T, ni) Внутренней энергии: U = f (S, V, ni) Энтальпии: H = f (S, p, n i) (6) (7) (8)
 По аналогии со свободной энергией Гиббса (при постоянстве соответствующих параметров) получаем: Поверхностное натяжение определяется частной производной от любого термодинамического потенциала по площади межфазной поверхности при постоянстве соответствующих параметров.
По аналогии со свободной энергией Гиббса (при постоянстве соответствующих параметров) получаем: Поверхностное натяжение определяется частной производной от любого термодинамического потенциала по площади межфазной поверхности при постоянстве соответствующих параметров.
 Силовой подход к поверхностному натяжению Поверхностное натяжение это сила, стремящаяся уменьшить площадь поверхности, которая действует тангенциально (по касательной) к этой поверхности на единицу длины её контура
Силовой подход к поверхностному натяжению Поверхностное натяжение это сила, стремящаяся уменьшить площадь поверхности, которая действует тангенциально (по касательной) к этой поверхности на единицу длины её контура
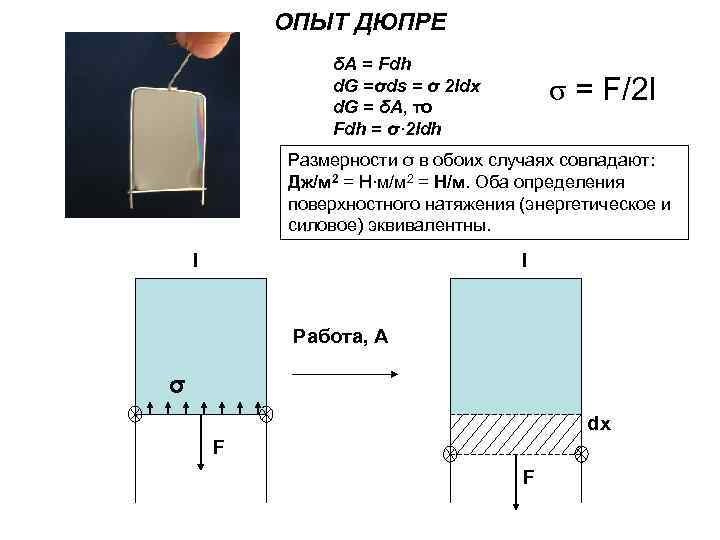
 ОПЫТ ДЮПРЕ δА = Fdh d. G =σds = σ 2 ldx d. G = δА, то σ = F/2 l Fdh = σ· 2 ldh Размерности σ в обоих случаях совпадают: Дж/м 2 = Н∙м/м 2 = Н/м. Оба определения поверхностного натяжения (энергетическое и силовое) эквивалентны. l Работа, А σ dх F F
ОПЫТ ДЮПРЕ δА = Fdh d. G =σds = σ 2 ldx d. G = δА, то σ = F/2 l Fdh = σ· 2 ldh Размерности σ в обоих случаях совпадают: Дж/м 2 = Н∙м/м 2 = Н/м. Оба определения поверхностного натяжения (энергетическое и силовое) эквивалентны. l Работа, А σ dх F F
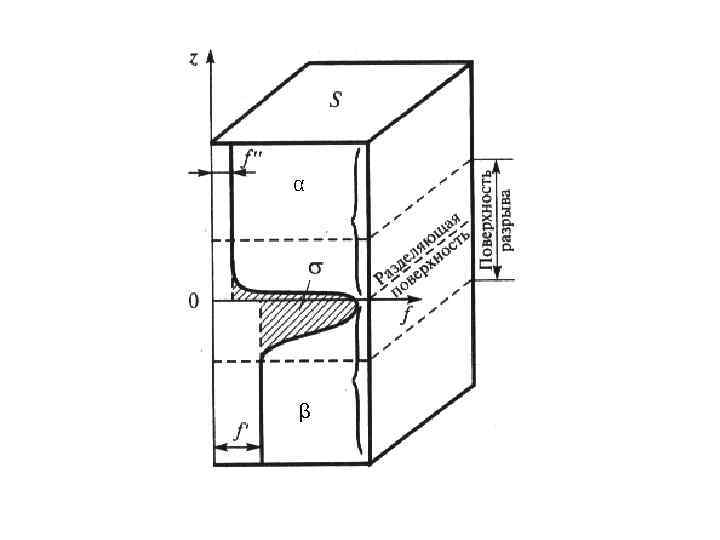
 Термодинамические свойства поверхности. Метод избыточных величин Гиббса Фаза α Поверхностный слой δ «поверхность разрыва» Фаза β Изменение термодинамических параметров (энергия, плотность……. ) 2 подхода термодинамики поверхностных явлений: Метод Гиббса Метод слоя конечной толщины
Термодинамические свойства поверхности. Метод избыточных величин Гиббса Фаза α Поверхностный слой δ «поверхность разрыва» Фаза β Изменение термодинамических параметров (энергия, плотность……. ) 2 подхода термодинамики поверхностных явлений: Метод Гиббса Метод слоя конечной толщины
 Для решения проблемы о СТРУКТУРЕ и ТОЛЩИНЕ поверхностного слоя Гиббс ввел понятия: 1) Идеализированной системы 2) Геометрической разделяющей поверхности (ГРП) 3) Поверхностных избытков экстенсивных термодинамических параметров: - Свободной энергии Гиббса Gs - Cсвободной энергии Гельмгольца Fs - Внутренней энергии Us - Энтальпии Hs - Энтропии Ss Метод Гиббса основан на сравнении РЕАЛЬНОЙ и ИДЕАЛИЗИРОВАННОЙ СИСТЕМЫ
Для решения проблемы о СТРУКТУРЕ и ТОЛЩИНЕ поверхностного слоя Гиббс ввел понятия: 1) Идеализированной системы 2) Геометрической разделяющей поверхности (ГРП) 3) Поверхностных избытков экстенсивных термодинамических параметров: - Свободной энергии Гиббса Gs - Cсвободной энергии Гельмгольца Fs - Внутренней энергии Us - Энтальпии Hs - Энтропии Ss Метод Гиббса основан на сравнении РЕАЛЬНОЙ и ИДЕАЛИЗИРОВАННОЙ СИСТЕМЫ
 Поверхностные избытки термодинамических свойств – есть разность между свойствами реальной и идеализированной систем. (9)
Поверхностные избытки термодинамических свойств – есть разность между свойствами реальной и идеализированной систем. (9)
 Удельные (отнесенные к единице площади поверхности s) избытки термодинамических функций:
Удельные (отнесенные к единице площади поверхности s) избытки термодинамических функций:
 Избыток вещества в поверхностном слое: (10) Адсорбция – удельная величина поверхностного избытка вещества (11)
Избыток вещества в поверхностном слое: (10) Адсорбция – удельная величина поверхностного избытка вещества (11)
 α β
α β
 Свободная энергия реальной системы: (12) Свободная энергия идеализированной системы: (13)
Свободная энергия реальной системы: (12) Свободная энергия идеализированной системы: (13)
 Избыточная ПОВЕРХНОСТНАЯ свободная энергия : Соответствует площади заштрихованного «языка» Важно! Fs – Определяется выбором положения ГРП Необходимо обосновать выбор ГРП.
Избыточная ПОВЕРХНОСТНАЯ свободная энергия : Соответствует площади заштрихованного «языка» Важно! Fs – Определяется выбором положения ГРП Необходимо обосновать выбор ГРП.
 Количество вещества в реальной системе: (15) Количество вещества в идеализ. системе: (16) Избыточное число молей : (17) ГРП – эквимолекулярна при ns=0 , т. е. отсутствует автоадсорбция компонента
Количество вещества в реальной системе: (15) Количество вещества в идеализ. системе: (16) Избыточное число молей : (17) ГРП – эквимолекулярна при ns=0 , т. е. отсутствует автоадсорбция компонента
 Докажем, что только для эквимолекулярной поверхности поверхностное натяжение равно удельной избыточной поверхностной энергии Величина d. F для реальной многокомпонентной гетерогенной системы : (6) Аналогично для гомогенных фаз идеализированной системы: (18) (19) В соответствии с определением гиббсовских избытков из уравнения (6) можно вычесть уравнения (18) и (19), учесть равенство химических потенциалов и давлений для плоской границы раздела фаз при равновесии, равенство объемов реальной и идеализированной систем и получить в итоге уравнение для избытка свободной поверхностной энергии: (20)
Докажем, что только для эквимолекулярной поверхности поверхностное натяжение равно удельной избыточной поверхностной энергии Величина d. F для реальной многокомпонентной гетерогенной системы : (6) Аналогично для гомогенных фаз идеализированной системы: (18) (19) В соответствии с определением гиббсовских избытков из уравнения (6) можно вычесть уравнения (18) и (19), учесть равенство химических потенциалов и давлений для плоской границы раздела фаз при равновесии, равенство объемов реальной и идеализированной систем и получить в итоге уравнение для избытка свободной поверхностной энергии: (20)
 Для однокомпонентной системы (i=1) при изотермических условиях уравнение (20) упрощается: (21) Для эквимолекулярной поверхности dns=0, это приводит к простому результату: И для однородной в тангенциальном направлении поверхности: (22) Следовательно, только для эквимолекулярной поверхности поверхностное натяжение равно удельной избыточной поверхностной энергии, т. е. сгущению поверхностной энергии
Для однокомпонентной системы (i=1) при изотермических условиях уравнение (20) упрощается: (21) Для эквимолекулярной поверхности dns=0, это приводит к простому результату: И для однородной в тангенциальном направлении поверхности: (22) Следовательно, только для эквимолекулярной поверхности поверхностное натяжение равно удельной избыточной поверхностной энергии, т. е. сгущению поверхностной энергии
 Фундаментальные уравнения для поверхностных функций Поверхностный избыток внутренней энергии: (23) Для эквимолекулярной поверхности и одного компонента: (24) Из (24) получаем уравнения для удельных избытков термодинамических функций (сгущений): (25) (26) Уравнение Гиббса- Гельмгольца
Фундаментальные уравнения для поверхностных функций Поверхностный избыток внутренней энергии: (23) Для эквимолекулярной поверхности и одного компонента: (24) Из (24) получаем уравнения для удельных избытков термодинамических функций (сгущений): (25) (26) Уравнение Гиббса- Гельмгольца
 Связь между сгущением энтропии в поверхностном слое и поверхностном натяжением Интегрируя уравнение (23) (при T и Г=const): (27) Продифференцируем уравнение (27): (28) Приравнивая правые части уравнений (28) и (23) получаем уравнение Гиббса-Дюгема (аналог) для поверхности: (29) А на единицу площади поверхности получаем: (30) Для однокомпонентной жидкости и эквимолекулярной ГРП (Г 1=0): (31) И если подставить (31) в (26) получаем:
Связь между сгущением энтропии в поверхностном слое и поверхностном натяжением Интегрируя уравнение (23) (при T и Г=const): (27) Продифференцируем уравнение (27): (28) Приравнивая правые части уравнений (28) и (23) получаем уравнение Гиббса-Дюгема (аналог) для поверхности: (29) А на единицу площади поверхности получаем: (30) Для однокомпонентной жидкости и эквимолекулярной ГРП (Г 1=0): (31) И если подставить (31) в (26) получаем:
 ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ВЕЛИЧИНУ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ
ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ВЕЛИЧИНУ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ
 1. ХИМИЧЕСКАЯ ПРИРОДА КОНДЕНСИРОВАННОЙ ФАЗЫ ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ КОНДЕНСИРОВАННЫХ ФАЗ НА ГРАНИЦЕ С ВОЗДУХОМ Жидкость Т, К σ, м. Дж/м 2 Н 2 жидкий 14, 7 2, 9 Гексан 293 18, 4 Вода 293 72, 7 Na. Cl 1096 114 Pt 2273 1820
1. ХИМИЧЕСКАЯ ПРИРОДА КОНДЕНСИРОВАННОЙ ФАЗЫ ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ КОНДЕНСИРОВАННЫХ ФАЗ НА ГРАНИЦЕ С ВОЗДУХОМ Жидкость Т, К σ, м. Дж/м 2 Н 2 жидкий 14, 7 2, 9 Гексан 293 18, 4 Вода 293 72, 7 Na. Cl 1096 114 Pt 2273 1820
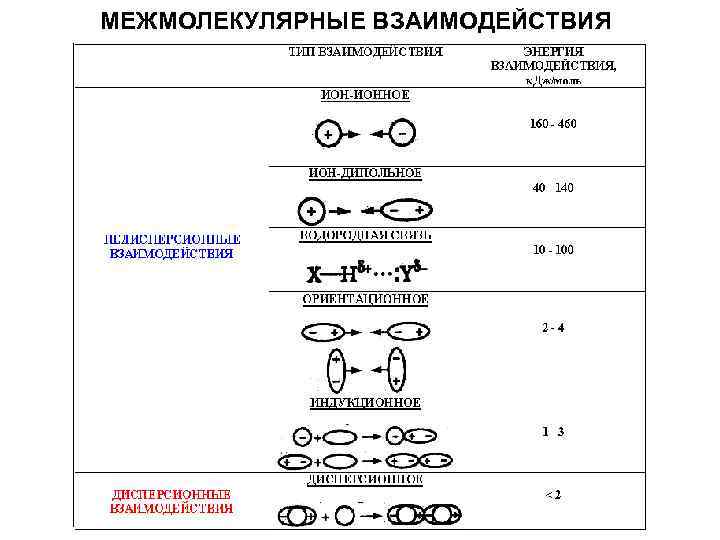
 МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ
МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ
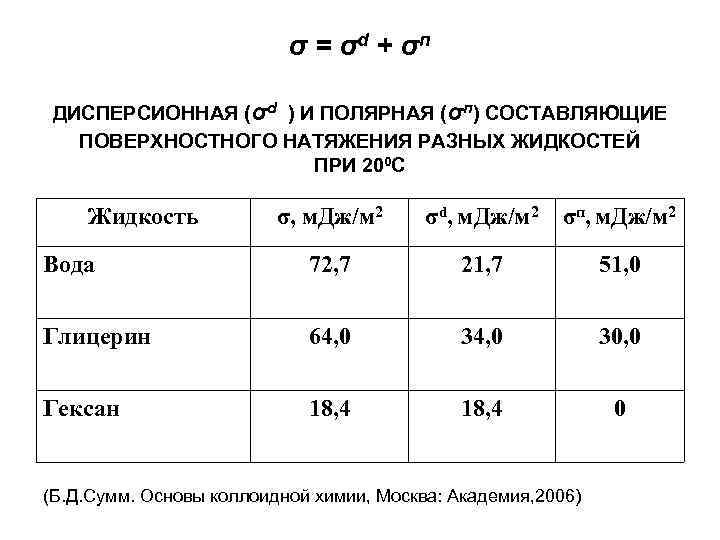
 σ = σd + σп ДИСПЕРСИОННАЯ (σd ) И ПОЛЯРНАЯ (σп) СОСТАВЛЯЮЩИЕ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ РАЗНЫХ ЖИДКОСТЕЙ ПРИ 200 С Жидкость σ, м. Дж/м 2 σd, м. Дж/м 2 σп, м. Дж/м 2 Вода 72, 7 21, 7 51, 0 Глицерин 64, 0 34, 0 30, 0 Гексан 18, 4 0 (Б. Д. Сумм. Основы коллоидной химии, Москва: Академия, 2006)
σ = σd + σп ДИСПЕРСИОННАЯ (σd ) И ПОЛЯРНАЯ (σп) СОСТАВЛЯЮЩИЕ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ РАЗНЫХ ЖИДКОСТЕЙ ПРИ 200 С Жидкость σ, м. Дж/м 2 σd, м. Дж/м 2 σп, м. Дж/м 2 Вода 72, 7 21, 7 51, 0 Глицерин 64, 0 34, 0 30, 0 Гексан 18, 4 0 (Б. Д. Сумм. Основы коллоидной химии, Москва: Академия, 2006)
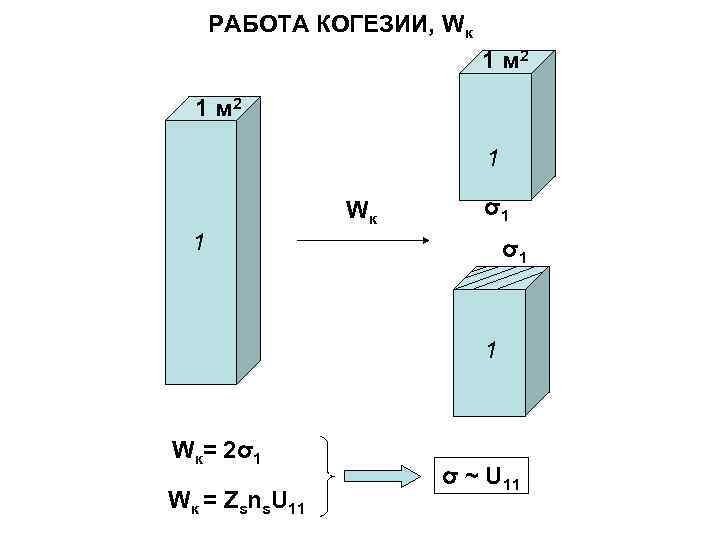
 РАБОТА КОГЕЗИИ, Wк 1 м 2 1 Wк σ1 1 σ1 1 Wк= 2σ1 σ ~ U 11 Wк = Zsns. U 11
РАБОТА КОГЕЗИИ, Wк 1 м 2 1 Wк σ1 1 σ1 1 Wк= 2σ1 σ ~ U 11 Wк = Zsns. U 11
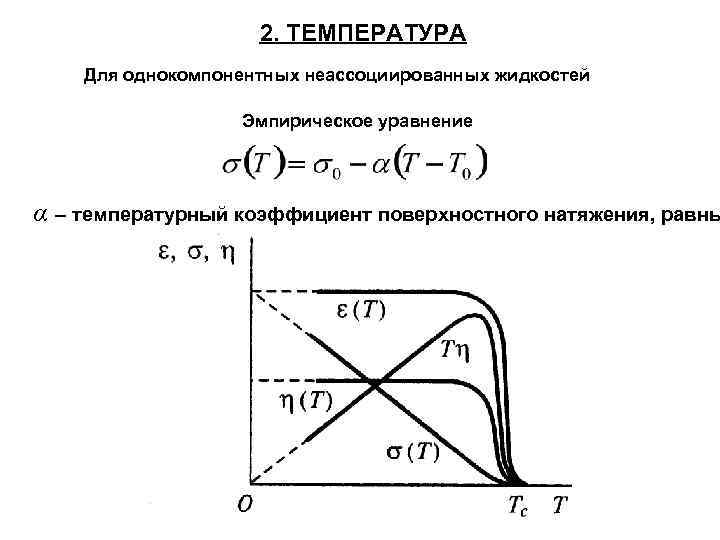
 2. ТЕМПЕРАТУРА Для однокомпонентных неассоциированных жидкостей Эмпирическое уравнение α – температурный коэффициент поверхностного натяжения, равны
2. ТЕМПЕРАТУРА Для однокомпонентных неассоциированных жидкостей Эмпирическое уравнение α – температурный коэффициент поверхностного натяжения, равны
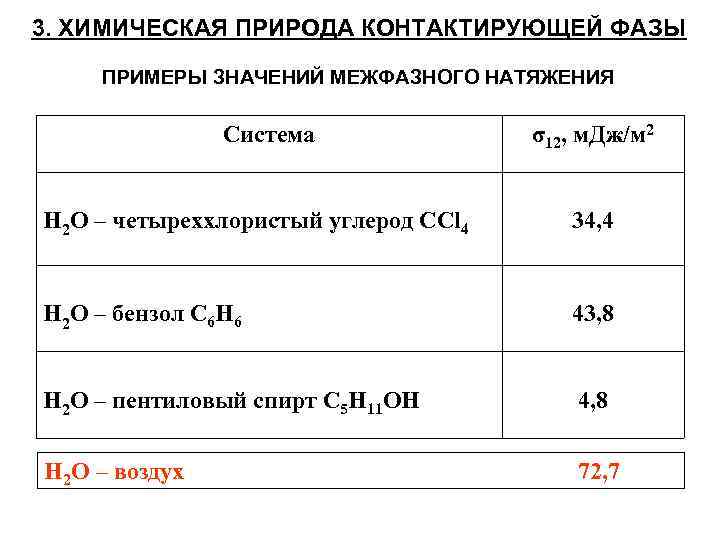
 3. ХИМИЧЕСКАЯ ПРИРОДА КОНТАКТИРУЮЩЕЙ ФАЗЫ ПРИМЕРЫ ЗНАЧЕНИЙ МЕЖФАЗНОГО НАТЯЖЕНИЯ Система σ12, м. Дж/м 2 Н 2 О – четыреххлористый углерод СCl 4 34, 4 Н 2 О – бензол C 6 H 6 43, 8 Н 2 О – пентиловый спирт C 5 H 11 OH 4, 8 Н 2 О – воздух 72, 7
3. ХИМИЧЕСКАЯ ПРИРОДА КОНТАКТИРУЮЩЕЙ ФАЗЫ ПРИМЕРЫ ЗНАЧЕНИЙ МЕЖФАЗНОГО НАТЯЖЕНИЯ Система σ12, м. Дж/м 2 Н 2 О – четыреххлористый углерод СCl 4 34, 4 Н 2 О – бензол C 6 H 6 43, 8 Н 2 О – пентиловый спирт C 5 H 11 OH 4, 8 Н 2 О – воздух 72, 7
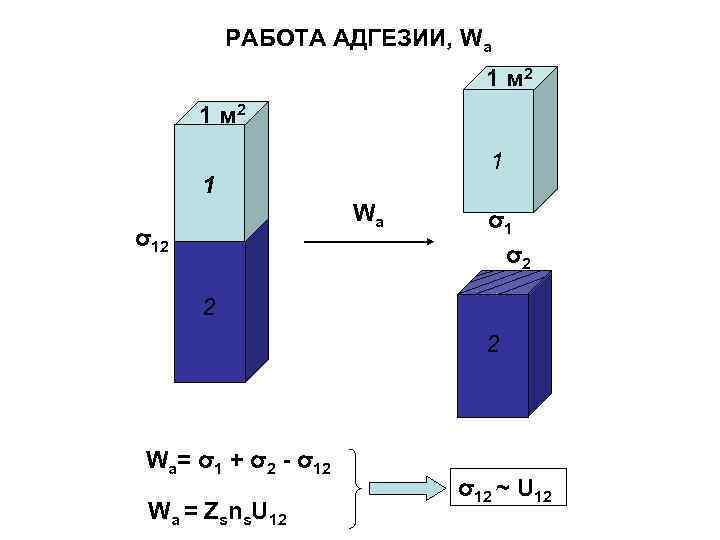
 РАБОТА АДГЕЗИИ, Wa 1 м 2 1 1 Wа σ1 σ12 σ2 2 2 Wа= σ1 + σ2 - σ12 σ12 ~ U 12 Wа = Zsns. U 12
РАБОТА АДГЕЗИИ, Wa 1 м 2 1 1 Wа σ1 σ12 σ2 2 2 Wа= σ1 + σ2 - σ12 σ12 ~ U 12 Wа = Zsns. U 12
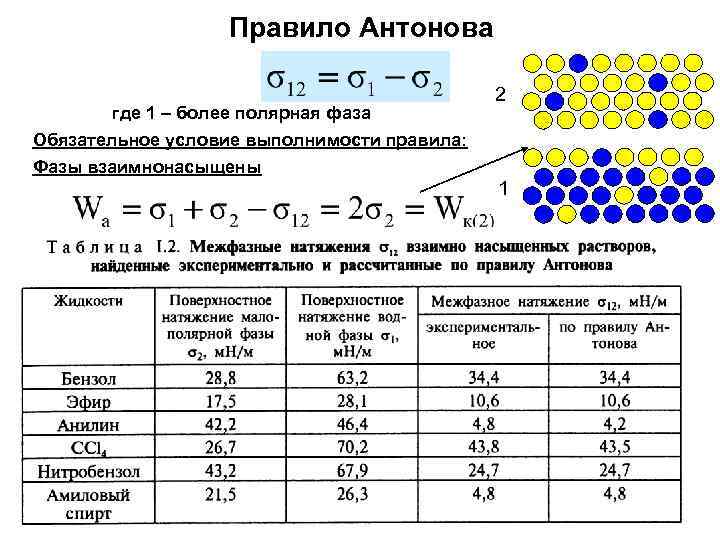
 Правило Антонова 2 где 1 – более полярная фаза Обязательное условие выполнимости правила: Фазы взаимнонасыщены 1
Правило Антонова 2 где 1 – более полярная фаза Обязательное условие выполнимости правила: Фазы взаимнонасыщены 1
 4. ПРИМЕСИ
4. ПРИМЕСИ

