молекулярная физика.ppt
- Количество слайдов: 55
 Лекция № 2. Основы молекулярной физики и термодинамики 1. 2. 3. 4. 5. 6. План: Статистический и термодинамический методы исследования Молекулярно кинетическая теория идеальных газов Основное уравнение молекулярно кинетической теории идеальных газов Закон Максвелла для распределения молекул идеального газа по скоростям и Барометрическая формула. Распределение Больцмана энергиям Первое начало термодинамики. Применение первого начала термодинамики к изопроцессам Второе начало термодинамики. Цикл Карно
Лекция № 2. Основы молекулярной физики и термодинамики 1. 2. 3. 4. 5. 6. План: Статистический и термодинамический методы исследования Молекулярно кинетическая теория идеальных газов Основное уравнение молекулярно кинетической теории идеальных газов Закон Максвелла для распределения молекул идеального газа по скоростям и Барометрическая формула. Распределение Больцмана энергиям Первое начало термодинамики. Применение первого начала термодинамики к изопроцессам Второе начало термодинамики. Цикл Карно
 1. Статистический и термодинамический методы исследования Молекулярная физика (МФ) и термодинамика разделы физики, в которых изучаются макроскопические процессы в телах, связанные с огромным числом содержащихся в телах атомов и молекул. Для исследования этих процессов применяют 2 метода: статистический и термодинамический. Процессы, изучаемые МФ, являются результатом совокупного действия огромного числа молекул. Законы поведения огромного числа молекул, являясь статистическими закономерностями, изучаются с помощью статистического метода.
1. Статистический и термодинамический методы исследования Молекулярная физика (МФ) и термодинамика разделы физики, в которых изучаются макроскопические процессы в телах, связанные с огромным числом содержащихся в телах атомов и молекул. Для исследования этих процессов применяют 2 метода: статистический и термодинамический. Процессы, изучаемые МФ, являются результатом совокупного действия огромного числа молекул. Законы поведения огромного числа молекул, являясь статистическими закономерностями, изучаются с помощью статистического метода.
 Молекулярная физика — раздел физики, изучающий строение и свойства вещества исходя из молекулярно кинетических представлений, основывающихся на том, что все тела состоят из молекул, находящихся в непрерывном хаотическом движении. Термодинамика — раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, и процессы перехода между этими состояниями. Термодинамика имеет дело с термодинамической системой — совокупностью макроскопических тел, которые взаимодействуют и обмениваются энергией как между собой, так и с другими телами (внешней средой). Основа термодинамического метода — определение состояния термодинамической системы. Состояние системы задается параметрами состояния — совокупностью физических величин, характеризующих свойства термодинамической системы (температуру, давление и объем)
Молекулярная физика — раздел физики, изучающий строение и свойства вещества исходя из молекулярно кинетических представлений, основывающихся на том, что все тела состоят из молекул, находящихся в непрерывном хаотическом движении. Термодинамика — раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, и процессы перехода между этими состояниями. Термодинамика имеет дело с термодинамической системой — совокупностью макроскопических тел, которые взаимодействуют и обмениваются энергией как между собой, так и с другими телами (внешней средой). Основа термодинамического метода — определение состояния термодинамической системы. Состояние системы задается параметрами состояния — совокупностью физических величин, характеризующих свойства термодинамической системы (температуру, давление и объем)
 2. Молекулярно-кинетическая теория идеальных газов В МКТ пользуются моделью идеального газа, согласно которой: Ø собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда; Ø между молекулами газа отсутствуют силы взаимодействия; Ø столкновения молекул газа между собой и со стенками сосуда абсолютно упругие. Опытным путем, еще до появления МКТ, был установлен целый ряд законов, описывающих поведение идеальных газов. Закон Бойля - Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
2. Молекулярно-кинетическая теория идеальных газов В МКТ пользуются моделью идеального газа, согласно которой: Ø собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда; Ø между молекулами газа отсутствуют силы взаимодействия; Ø столкновения молекул газа между собой и со стенками сосуда абсолютно упругие. Опытным путем, еще до появления МКТ, был установлен целый ряд законов, описывающих поведение идеальных газов. Закон Бойля - Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
 Закон Гей-Люссака: объем данной массы газа при постоянном давлении изменяется линейно с температурой: Закон Шарля: давление данной массы газа при постоянном объеме изменяется линейно с температурой: Вводя в эти формулы термодинамическую температуру, законам Гей Люссака и Шарля соответственно можно придать более удобный вид:
Закон Гей-Люссака: объем данной массы газа при постоянном давлении изменяется линейно с температурой: Закон Шарля: давление данной массы газа при постоянном объеме изменяется линейно с температурой: Вводя в эти формулы термодинамическую температуру, законам Гей Люссака и Шарля соответственно можно придать более удобный вид:
 Закон Авогадро: моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы. При нормальных условиях этот объем равен По определению, в одном моле различных веществ содержится одно и то же число молекул, называемое постоянной Авогадро: Закон Дальтона: давление смеси идеальных газов равно сумме парциаль ных давлений входящих в нее газов, т. е. где парциальные давления, которые оказывали бы газы смеси, если бы они одни занимали объем, равный объему смеси при той же температуре.
Закон Авогадро: моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы. При нормальных условиях этот объем равен По определению, в одном моле различных веществ содержится одно и то же число молекул, называемое постоянной Авогадро: Закон Дальтона: давление смеси идеальных газов равно сумме парциаль ных давлений входящих в нее газов, т. е. где парциальные давления, которые оказывали бы газы смеси, если бы они одни занимали объем, равный объему смеси при той же температуре.
 Уравнение Клапейрона - Менделеева Французский физик и инженер Б. Клапейрон вывел уравнение состояния идеального газа, объединив законы Бойля Мариотта и Гей Люссака. Русский ученый Д. И. Менделеев объединил уравнение Клапейрона с законом Авогадро, отнеся уравнение к одному молю, использовав молярный объем , . универсальная газовая постоянная Данному уравнению удовлетворяет лишь идеальный газ, и оно является уравнением состояния идеального газа, называемым также уравнением Клапейрона — Менделеева.
Уравнение Клапейрона - Менделеева Французский физик и инженер Б. Клапейрон вывел уравнение состояния идеального газа, объединив законы Бойля Мариотта и Гей Люссака. Русский ученый Д. И. Менделеев объединил уравнение Клапейрона с законом Авогадро, отнеся уравнение к одному молю, использовав молярный объем , . универсальная газовая постоянная Данному уравнению удовлетворяет лишь идеальный газ, и оно является уравнением состояния идеального газа, называемым также уравнением Клапейрона — Менделеева.
 От уравнения для моля газа можно перейти к уравнению Клапейрона Менделеева для произвольной массы газа. Часто пользуются несколько иной формой уравнения состояния идеального газа, вводя постоянную Больцмана: , тогда , где n – концентрация молекул (число молекул в единицу объема)
От уравнения для моля газа можно перейти к уравнению Клапейрона Менделеева для произвольной массы газа. Часто пользуются несколько иной формой уравнения состояния идеального газа, вводя постоянную Больцмана: , тогда , где n – концентрация молекул (число молекул в единицу объема)
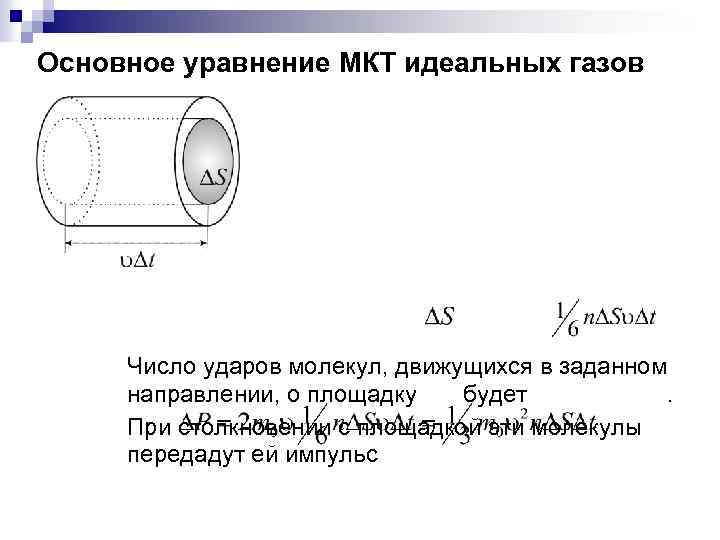 Основное уравнение МКТ идеальных газов Число ударов молекул, движущихся в заданном направлении, о площадку будет. При столкновении с площадкой эти молекулы передадут ей импульс
Основное уравнение МКТ идеальных газов Число ударов молекул, движущихся в заданном направлении, о площадку будет. При столкновении с площадкой эти молекулы передадут ей импульс
 Давление газа, оказываемое им на стенку сосуда, Если газ в объеме содержит молекул, движущихся со скоростями , то целесообразно рассматривать среднюю квадратичную скорость характеризующую всю совокупность молекул газа Уравнение (1) с учетом (2) примет вид основное уравнение МКТ идеальных газов
Давление газа, оказываемое им на стенку сосуда, Если газ в объеме содержит молекул, движущихся со скоростями , то целесообразно рассматривать среднюю квадратичную скорость характеризующую всю совокупность молекул газа Уравнение (1) с учетом (2) примет вид основное уравнение МКТ идеальных газов
 Учитывая, что , получим: или где Е суммарная кинетическая энергия поступательного движения всех молекул газа
Учитывая, что , получим: или где Е суммарная кинетическая энергия поступательного движения всех молекул газа
 4. Закон Максвелла для распределения молекул идеального газа по скоростям При выводе закона распределения молекул по скоростям Максвелл предполагал, что газ состоит из очень большого числа тождественных молекул, находящихся в состоянии беспорядочного теплового движения при одинаковой температуре. Предполагалось также, что силовые поля на газ не действуют. Закон Максвелла описывается некоторой функцией называемой функцией распределения молекул по скоростям.
4. Закон Максвелла для распределения молекул идеального газа по скоростям При выводе закона распределения молекул по скоростям Максвелл предполагал, что газ состоит из очень большого числа тождественных молекул, находящихся в состоянии беспорядочного теплового движения при одинаковой температуре. Предполагалось также, что силовые поля на газ не действуют. Закон Максвелла описывается некоторой функцией называемой функцией распределения молекул по скоростям.
 Если разбить диапазон скоростей молекул на малые интервалы, равные , то на каждый интервал скорости будет приходиться некоторое число молекул , имеющих скорость, заключенную в этом интервале. определяет относительное число молекул , скорости которых лежат в интервале от т. е. до ,
Если разбить диапазон скоростей молекул на малые интервалы, равные , то на каждый интервал скорости будет приходиться некоторое число молекул , имеющих скорость, заключенную в этом интервале. определяет относительное число молекул , скорости которых лежат в интервале от т. е. до ,
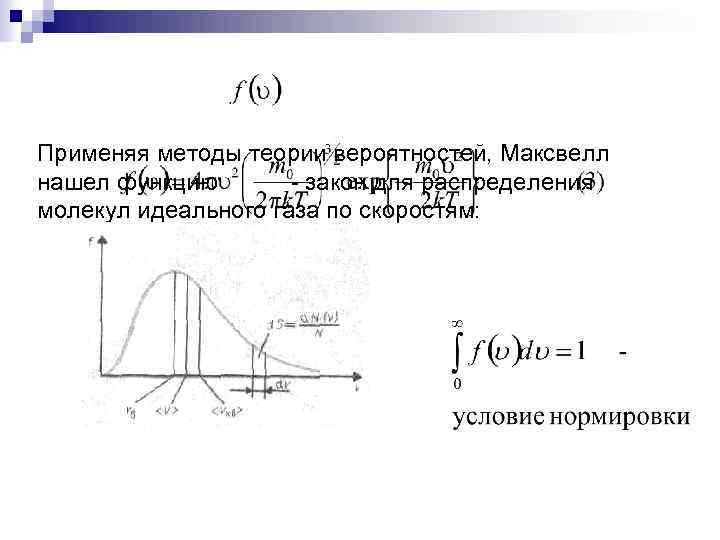 Применяя методы теории вероятностей, Максвелл нашел функцию закон для распределения молекул идеального газа по скоростям:
Применяя методы теории вероятностей, Максвелл нашел функцию закон для распределения молекул идеального газа по скоростям:
 Скорость, при которой молекул идеального газа, обладает значением называется наиболее вероятной скоростью. Найдем : Возможно:
Скорость, при которой молекул идеального газа, обладает значением называется наиболее вероятной скоростью. Найдем : Возможно:
 Средняя скорость молекулы (средняя арифметическая скорость) определяется по формуле: Подставляя (3) в (5) и интегрируя получаем: Средняя квадратичная определяется по формуле: скорость молекулы Подставляя (3) в (7) и интегрируя получаем:
Средняя скорость молекулы (средняя арифметическая скорость) определяется по формуле: Подставляя (3) в (5) и интегрируя получаем: Средняя квадратичная определяется по формуле: скорость молекулы Подставляя (3) в (7) и интегрируя получаем:
 Исходя из распределения молекул по скоростям можно найти распределение молекул газа по значениям кинетической энергии. Для этого в выражении (3) перейдем от переменной к переменной Подставив в (3) Т. О. получена , функция (9) распределения молекул по энергиями теплового движения
Исходя из распределения молекул по скоростям можно найти распределение молекул газа по значениям кинетической энергии. Для этого в выражении (3) перейдем от переменной к переменной Подставив в (3) Т. О. получена , функция (9) распределения молекул по энергиями теплового движения
 Средняя кинетическая энергия молекулы идеального газа определяется из условия: Средняя кинетическая энергия поступательного движения одной молекулы идеального газа пропорциональна термодинамической температуре и зависит только от нее.
Средняя кинетическая энергия молекулы идеального газа определяется из условия: Средняя кинетическая энергия поступательного движения одной молекулы идеального газа пропорциональна термодинамической температуре и зависит только от нее.
 Из выражения (10) следует, что при т. е. при 0 К прекращается поступательное движение молекул газа, а следовательно, его давление равно нулю. Т. О. , термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа и формула (10) раскрывает молекулярно кинетическое толкование температуры.
Из выражения (10) следует, что при т. е. при 0 К прекращается поступательное движение молекул газа, а следовательно, его давление равно нулю. Т. О. , термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа и формула (10) раскрывает молекулярно кинетическое толкование температуры.
 Если атмосферное давление на высоте равно , то на высоте оно равно (при ). Разность и равна весу газа, заключенного в объеме цилиндра высотой с основанием площадью, равной единице площади: где плотность газа на высоте h, Следовательно: Из уравнения состояния идеального газа: подставляя в (11) получим: или:
Если атмосферное давление на высоте равно , то на высоте оно равно (при ). Разность и равна весу газа, заключенного в объеме цилиндра высотой с основанием площадью, равной единице площади: где плотность газа на высоте h, Следовательно: Из уравнения состояния идеального газа: подставляя в (11) получим: или:
 С изменением высоты от изменяется от до до давление Выражение (12) называется барометрической формулой, выражение позволяет найти атмосферное давление в зависимости от высоты или, измерив давление, найти высоту.
С изменением высоты от изменяется от до до давление Выражение (12) называется барометрической формулой, выражение позволяет найти атмосферное давление в зависимости от высоты или, измерив давление, найти высоту.
 Выражение (13) можно преобразовать, воспользовавшись равенством: или: где – масса молекулы, – постоянная Больцмана Выражение (14) называется распределением Больцмана во внешнем потенциальном поле. Из него следует, что при постоянной температуре плотность газа больше там, где меньше потенциальная энергия его молекул.
Выражение (13) можно преобразовать, воспользовавшись равенством: или: где – масса молекулы, – постоянная Больцмана Выражение (14) называется распределением Больцмана во внешнем потенциальном поле. Из него следует, что при постоянной температуре плотность газа больше там, где меньше потенциальная энергия его молекул.
 Среднее число столкновений и средняя длина свободного пробега молекул Между двумя последовательными столкновениями молекулы проходят некоторый путь, называемый длиной свободного пробега. Минимальное расстояние, на которое сближаются при столкновении центры двух молекул, называется эффективным диаметром молекулы.
Среднее число столкновений и средняя длина свободного пробега молекул Между двумя последовательными столкновениями молекулы проходят некоторый путь, называемый длиной свободного пробега. Минимальное расстояние, на которое сближаются при столкновении центры двух молекул, называется эффективным диаметром молекулы.
 средняя длина свободного пробега: средняя скорость молекулы, число соударений в единицу времени Расчеты показывают, что концентрация и эффективный диаметр молекул соответственно средняя длина свободного пробега молекул:
средняя длина свободного пробега: средняя скорость молекулы, число соударений в единицу времени Расчеты показывают, что концентрация и эффективный диаметр молекул соответственно средняя длина свободного пробега молекул:
 Важной характеристикой термодинамической системы является ее внутренняя энергия — энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов и т. д. ) и энергия взаимодействия этих частиц. Внутренняя энергия — однозначная функция термодинамического состояния системы, в каждом состоянии система обладает вполне определенной внутренней энергией (она не зависит от того, как система пришла в данное состояние). Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю (молекулы между собой не взаимодействуют), то внутренняя энергия, отнесенная к одному молю газа, будет равна сумме кинетических энергий молекул: Внутренняя энергия для произвольной массы газа
Важной характеристикой термодинамической системы является ее внутренняя энергия — энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов и т. д. ) и энергия взаимодействия этих частиц. Внутренняя энергия — однозначная функция термодинамического состояния системы, в каждом состоянии система обладает вполне определенной внутренней энергией (она не зависит от того, как система пришла в данное состояние). Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю (молекулы между собой не взаимодействуют), то внутренняя энергия, отнесенная к одному молю газа, будет равна сумме кинетических энергий молекул: Внутренняя энергия для произвольной массы газа
 Первое начало термодинамики Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией , получила некоторое количество теплоты и, перейдя в новое состояние, характеризующееся внутренней энергией , совершила работу над внешней средой, т. е. против внешних сил. В соответствии с законом сохранения энергии при любом способе перехода системы из первого состояния во второе изменение внутренней энергии будет одинаковым и равным разности между количеством теплоты , полученным системой, и работой , совершенной системой против внешних сил: (15)
Первое начало термодинамики Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией , получила некоторое количество теплоты и, перейдя в новое состояние, характеризующееся внутренней энергией , совершила работу над внешней средой, т. е. против внешних сил. В соответствии с законом сохранения энергии при любом способе перехода системы из первого состояния во второе изменение внутренней энергии будет одинаковым и равным разности между количеством теплоты , полученным системой, и работой , совершенной системой против внешних сил: (15)
 Уравнение (15) выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил. В дифференциальной форме уравнение имеет вид: , (16) где — бесконечно малое изменение внутренней энергии системы, — элементарная работа, — бесконечно малое количество теплоты. Работа газа при изменении его объема
Уравнение (15) выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил. В дифференциальной форме уравнение имеет вид: , (16) где — бесконечно малое изменение внутренней энергии системы, — элементарная работа, — бесконечно малое количество теплоты. Работа газа при изменении его объема
 Работа газа при изменении его объема Рассмотрим, газ, находящийся под поршнем в цилиндрическом сосуде (см. рис). Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние dl, то производит над ним работу где площадь поршня, изменение объема системы. ТО Полную работу , совершаемую газом при изменении его объема от до , найдем
Работа газа при изменении его объема Рассмотрим, газ, находящийся под поршнем в цилиндрическом сосуде (см. рис). Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние dl, то производит над ним работу где площадь поршня, изменение объема системы. ТО Полную работу , совершаемую газом при изменении его объема от до , найдем
 Теплоемкость Удельная теплоемкость вещества величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К: Молярная теплоемкость величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К: Запишем выражение первого начала термодинамики (17) Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:
Теплоемкость Удельная теплоемкость вещества величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К: Молярная теплоемкость величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К: Запишем выражение первого начала термодинамики (17) Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:
 Если газ нагревается при постоянном давлении, то выражение (17) можно записать в виде (18) Выражение (18) называется уравнением Майера; оно показывает, что всегда больше на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа.
Если газ нагревается при постоянном давлении, то выражение (17) можно записать в виде (18) Выражение (18) называется уравнением Майера; оно показывает, что всегда больше на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа.
 Применение первого начала термодинамики к изопроцессам Изохорный процесс при изохорном процессе газ не совершает работы над внешними телами, т. е. Внутренняя энергия для произвольной массы газа: (19) (20) Изобарный процесс При изобарном процессе работа газа при расширении объема
Применение первого начала термодинамики к изопроцессам Изохорный процесс при изохорном процессе газ не совершает работы над внешними телами, т. е. Внутренняя энергия для произвольной массы газа: (19) (20) Изобарный процесс При изобарном процессе работа газа при расширении объема
 используя уравнение Клапейрона Менделеева для выбранных нами двух состояний, находим изменение объема Тогда выражение для работы изобарного расширения (21) физический смысл газовой постоянной: численно равна работе изобарного расширения 1 моля идеального газа при нагревании его на 1 К.
используя уравнение Клапейрона Менделеева для выбранных нами двух состояний, находим изменение объема Тогда выражение для работы изобарного расширения (21) физический смысл газовой постоянной: численно равна работе изобарного расширения 1 моля идеального газа при нагревании его на 1 К.
 В изобарном процессе при сообщении газу массой от количества теплоты его внутренняя энергия возрастает на величину (22) (23) (24) Изотермический процесс (25) из первого начала термодинамики
В изобарном процессе при сообщении газу массой от количества теплоты его внутренняя энергия возрастает на величину (22) (23) (24) Изотермический процесс (25) из первого начала термодинамики
 все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил: (26) для того чтобы при работе расширения температура не изменялась (не уменьшалась), к газу в течение изотермического процесса необходимо подводить количество теплоты, равное внешней работе расширения Адиабатическим называется процесс, при котором отсутствует теплообмен между системой и окружающей средой. Из I го начала термодинамики внешняя работа совершается за счет изменения внутренней энергии системы.
все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил: (26) для того чтобы при работе расширения температура не изменялась (не уменьшалась), к газу в течение изотермического процесса необходимо подводить количество теплоты, равное внешней работе расширения Адиабатическим называется процесс, при котором отсутствует теплообмен между системой и окружающей средой. Из I го начала термодинамики внешняя работа совершается за счет изменения внутренней энергии системы.
 (27) (28) разделим (28) на (27) Учтем, что
(27) (28) разделим (28) на (27) Учтем, что
 Интегрируя и потенцируя, получаем: (29) уравнение адиабатического процесса, его называют уравнением Пуассона
Интегрируя и потенцируя, получаем: (29) уравнение адиабатического процесса, его называют уравнением Пуассона
 показатель адиабаты (коэффициент Пуассона) число степеней свободы Работа, совершаемая газом при адиабатическом расширении (30) (31)
показатель адиабаты (коэффициент Пуассона) число степеней свободы Работа, совершаемая газом при адиабатическом расширении (30) (31)
 Работа, совершаемая газом при адиабатическом расширении меньше, чем при изотермическом (при адиабатическом расширении происходит охлаждение газа, тогда как при изотермическом — температура поддерживается постоянной за счет притока извне эквивалентного количества теплоты).
Работа, совершаемая газом при адиабатическом расширении меньше, чем при изотермическом (при адиабатическом расширении происходит охлаждение газа, тогда как при изотермическом — температура поддерживается постоянной за счет притока извне эквивалентного количества теплоты).
 Цикл. Обратимые и необратимые процессы. Энтропия. Второе начало термодинамики. Круговой процесс (цикл) процесс, при котором система, пройдя через ряд состояний, возвращается в исходное состояние цикл прямой цикл обратный
Цикл. Обратимые и необратимые процессы. Энтропия. Второе начало термодинамики. Круговой процесс (цикл) процесс, при котором система, пройдя через ряд состояний, возвращается в исходное состояние цикл прямой цикл обратный
 Прямой цикл используется в тепловых двигателях (периодически действующих двигателях, совершающих работу за счет полученной извне теплоты); обратный цикл в холодильных машинах (периодически действующих установках, в которых за счет работы внешних сил теплота переносится к телу с более высокой температурой) В результате кругового процесса система возвращается в исходное состояние и, полное изменение внутренней энергии газа равно нулю
Прямой цикл используется в тепловых двигателях (периодически действующих двигателях, совершающих работу за счет полученной извне теплоты); обратный цикл в холодильных машинах (периодически действующих установках, в которых за счет работы внешних сил теплота переносится к телу с более высокой температурой) В результате кругового процесса система возвращается в исходное состояние и, полное изменение внутренней энергии газа равно нулю
 первое начало термодинамики для кругового процесса т. е. работа, совершаемая за цикл, равна количеству полученной извне теплоты в результате кругового процесса система может как получать, так и отдавать тепло где соответственно количество теплоты, полученное и отданное системой КПД полезного действия для цикла (32)
первое начало термодинамики для кругового процесса т. е. работа, совершаемая за цикл, равна количеству полученной извне теплоты в результате кругового процесса система может как получать, так и отдавать тепло где соответственно количество теплоты, полученное и отданное системой КПД полезного действия для цикла (32)
 Термодинамический процесс обратимый, если он может происходить как в прямом, так и в обратном направлении; если такой процесс происходит сначала в прямом, а затем в обратном направлении и система возвращается в исходное состояние, то в окружающей среде и в этой системе не происходит никаких изменений. Любой процесс, не удовлетворяющий этим условиям, является необратимым.
Термодинамический процесс обратимый, если он может происходить как в прямом, так и в обратном направлении; если такой процесс происходит сначала в прямом, а затем в обратном направлении и система возвращается в исходное состояние, то в окружающей среде и в этой системе не происходит никаких изменений. Любой процесс, не удовлетворяющий этим условиям, является необратимым.
 Энтропия приведенным количеством теплоты называют отношение теплоты, полученной телом в изотермическом процессе, к температуре теплоотдающего тела Приведенное кол во теплоты, сообщаемое телу В любом обратимом круговом процессе приведенное количество теплоты, сообщаемое телу равно нулю: (33) (34)
Энтропия приведенным количеством теплоты называют отношение теплоты, полученной телом в изотермическом процессе, к температуре теплоотдающего тела Приведенное кол во теплоты, сообщаемое телу В любом обратимом круговом процессе приведенное количество теплоты, сообщаемое телу равно нулю: (33) (34)
 функция, определяется только состоянием системы и не зависит от пути, по которому система пришла в это состояние. для обратимых процессов изменение энтропии (35) энтропия системы, совершающей необратимый цикл, возрастает: (36) Выражения (35) и (36) справедливы для замкнутых систем, в незамкнутых системах энтропия может вести себя любым образом. (37) неравенство Клаузиуса
функция, определяется только состоянием системы и не зависит от пути, по которому система пришла в это состояние. для обратимых процессов изменение энтропии (35) энтропия системы, совершающей необратимый цикл, возрастает: (36) Выражения (35) и (36) справедливы для замкнутых систем, в незамкнутых системах энтропия может вести себя любым образом. (37) неравенство Клаузиуса
 Если система совершает равновесный переход из состояния 1 в состояние 2, то, изменение энтропии (38) Физический смысл имеет разность энтропии. Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропии тел, образующих в систему.
Если система совершает равновесный переход из состояния 1 в состояние 2, то, изменение энтропии (38) Физический смысл имеет разность энтропии. Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропии тел, образующих в систему.
 в статистической физике, связывается с термодинамической вероятностью состояния системы Термодинамическая вероятность состояния системы — это число способов, которыми может быть реализовано данное состояние макроскопической системы (число микросостояний, осуществляющих данное макросостояние) Согласно Больцману (1872) постоянная Больцмана (39) Формула Больцмана дает энтропии статистическое толкование: энтропия является мерой неупорядоченности системы
в статистической физике, связывается с термодинамической вероятностью состояния системы Термодинамическая вероятность состояния системы — это число способов, которыми может быть реализовано данное состояние макроскопической системы (число микросостояний, осуществляющих данное макросостояние) Согласно Больцману (1872) постоянная Больцмана (39) Формула Больцмана дает энтропии статистическое толкование: энтропия является мерой неупорядоченности системы
 2 -е начало термодинамики Появление 2 го начала термодинамики рассматривают как необходимость дать ответ на вопрос, какие процессы в природе возможны, а какие нет, и определяет направление развития процессов. Используя понятие энтропии и неравенство Клаузиуса 2 е начало термодинамики формулируют как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает. 1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу; 2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
2 -е начало термодинамики Появление 2 го начала термодинамики рассматривают как необходимость дать ответ на вопрос, какие процессы в природе возможны, а какие нет, и определяет направление развития процессов. Используя понятие энтропии и неравенство Клаузиуса 2 е начало термодинамики формулируют как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает. 1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу; 2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
 Первые два начала термодинамики дополняются третьим началом термодинамики теоремой Нернста Планка: энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Тепловые двигатели. Цикл Карно. Из формулировки второго начала термодинамики, что невозможен вечный двигатель второго рода — периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты.
Первые два начала термодинамики дополняются третьим началом термодинамики теоремой Нернста Планка: энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Тепловые двигатели. Цикл Карно. Из формулировки второго начала термодинамики, что невозможен вечный двигатель второго рода — периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты.
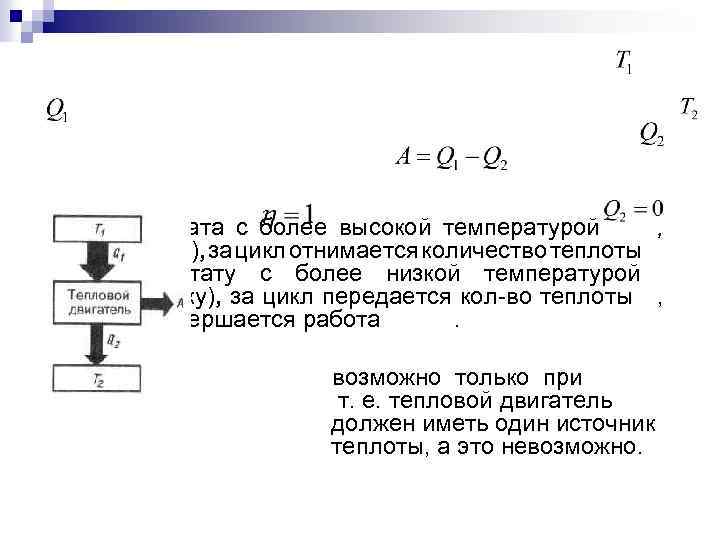 От термостата с более высокой температурой , (нагревателя), за цикл отнимается количество теплоты , а термостату с более низкой температурой (холодильнику), за цикл передается кол во теплоты , при этом совершается работа. возможно только при т. е. тепловой двигатель должен иметь один источник теплоты, а это невозможно.
От термостата с более высокой температурой , (нагревателя), за цикл отнимается количество теплоты , а термостату с более низкой температурой (холодильнику), за цикл передается кол во теплоты , при этом совершается работа. возможно только при т. е. тепловой двигатель должен иметь один источник теплоты, а это невозможно.
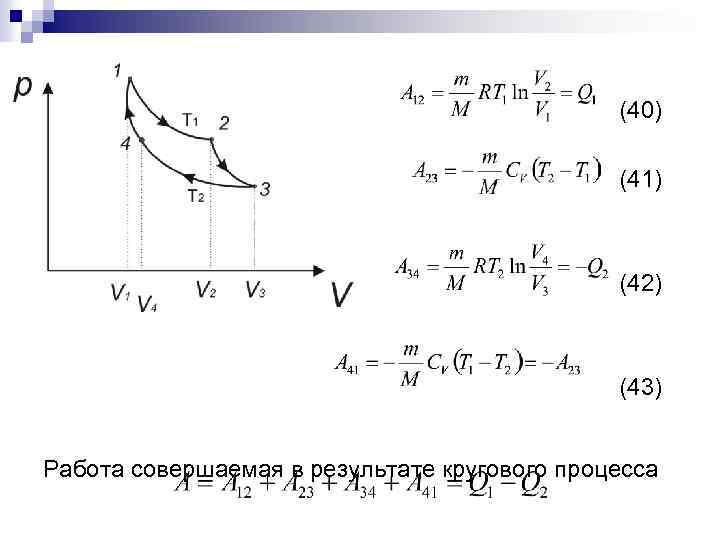 (40) (41) (42) (43) Работа совершаемая в результате кругового процесса
(40) (41) (42) (43) Работа совершаемая в результате кругового процесса
 КПД цикла согласно (32) Применяя уравнения адиабат 2 3 и 4 1: Подставляя (40) и (42) в (32) получаем
КПД цикла согласно (32) Применяя уравнения адиабат 2 3 и 4 1: Подставляя (40) и (42) в (32) получаем
 Подставляя (40) и (42) в (32) получаем (44) для цикла Карно КПД определяется только температурами нагревателя и холодильника.
Подставляя (40) и (42) в (32) получаем (44) для цикла Карно КПД определяется только температурами нагревателя и холодильника.
 Реальные газы, уравнение Ван-дер-Ваальса При рассмотрении реальных газов , свойства которых зависят от взаимодействия молекул, учитывают силы межмолекулярного взаимодействия, которые называются короткодействующими. Для реальных газов необходимо учитывать размеры молекул и их взаимодействие друг с другом, поэтому модель идеального газа и уравнение Клапейрона Менделеева описывающее идеальный газ, для реальных газов непригодны.
Реальные газы, уравнение Ван-дер-Ваальса При рассмотрении реальных газов , свойства которых зависят от взаимодействия молекул, учитывают силы межмолекулярного взаимодействия, которые называются короткодействующими. Для реальных газов необходимо учитывать размеры молекул и их взаимодействие друг с другом, поэтому модель идеального газа и уравнение Клапейрона Менделеева описывающее идеальный газ, для реальных газов непригодны.
 Учитывая собственный объем молекул и сил межмолекулярного взаимодействия, голландский физик Ван дер Ваальса вывел уравнения состояния реального газа. 1. Учет собственного объема молекул. Наличие сил отталкивания, которые противодействуют проникновению в занятый молекулой объем других молекул, сводится к тому, что фактический свободный объем, в котором могут двигаться молеку лы реального газа, будет меньше объема.
Учитывая собственный объем молекул и сил межмолекулярного взаимодействия, голландский физик Ван дер Ваальса вывел уравнения состояния реального газа. 1. Учет собственного объема молекул. Наличие сил отталкивания, которые противодействуют проникновению в занятый молекулой объем других молекул, сводится к тому, что фактический свободный объем, в котором могут двигаться молеку лы реального газа, будет меньше объема.
 2. Учет притяжения молекул. Действие сил притяжения газа приводит к появлению дополнительного давления на газ, называемого внутренним давлением. Вводя эти поправки, получим уравнение Ван дер Ваальса уравнение состояния реальных газов: (45) внутреннее давление, обусловленное силами притяжения между молекулами поправка на собственный объем молекул учитывающая действие сил отталкивания между молекулами
2. Учет притяжения молекул. Действие сил притяжения газа приводит к появлению дополнительного давления на газ, называемого внутренним давлением. Вводя эти поправки, получим уравнение Ван дер Ваальса уравнение состояния реальных газов: (45) внутреннее давление, обусловленное силами притяжения между молекулами поправка на собственный объем молекул учитывающая действие сил отталкивания между молекулами


