Лекция_N2_2013.ppt
- Количество слайдов: 46
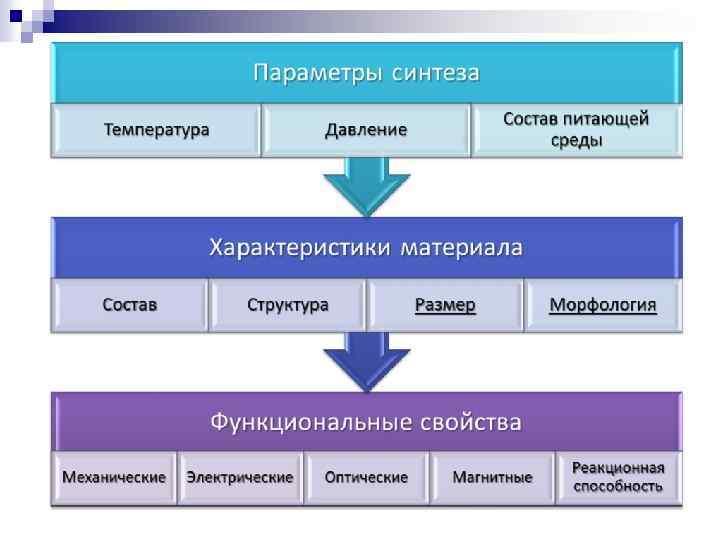
 Лекция 2. • Основные классы химических соединений. Типы химической связи. Кислотные и основные центры. • Химические реакции: окислениявосстановления, кислотно-основные, гидролиз, разложение. Классификация методов синтеза по фазовым состояниям исходных реагентов и продуктов реакции. 1
Лекция 2. • Основные классы химических соединений. Типы химической связи. Кислотные и основные центры. • Химические реакции: окислениявосстановления, кислотно-основные, гидролиз, разложение. Классификация методов синтеза по фазовым состояниям исходных реагентов и продуктов реакции. 1

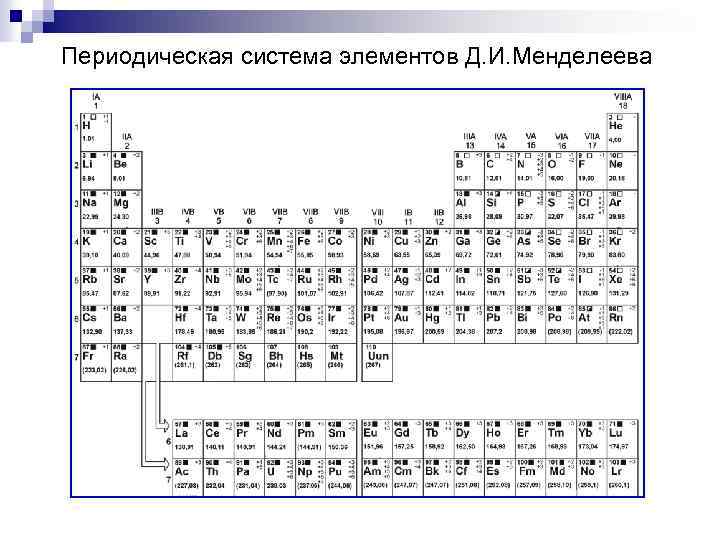 Периодическая система элементов Д. И. Менделеева
Периодическая система элементов Д. И. Менделеева

 Химические формулы. 1. Молекулярные формулы - состав 2. Графические формулы – последовательность связей атомов, кратность связи 3. Электронные формулы – наличие неспаренных электронов и свободных электронных пар 4. Структурные формулы – углы, расстояния 5. Другие формулы – наличие функциональных групп 6
Химические формулы. 1. Молекулярные формулы - состав 2. Графические формулы – последовательность связей атомов, кратность связи 3. Электронные формулы – наличие неспаренных электронов и свободных электронных пар 4. Структурные формулы – углы, расстояния 5. Другие формулы – наличие функциональных групп 6
 Молекулярные формулы 7
Молекулярные формулы 7
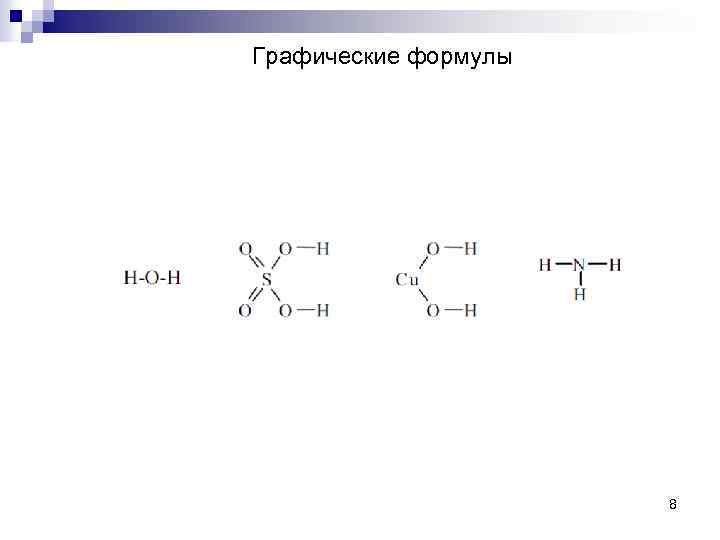 Графические формулы 8
Графические формулы 8
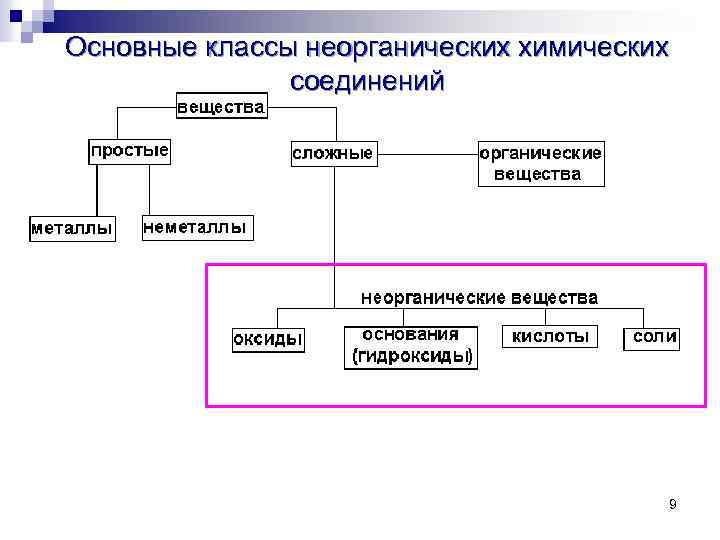 Основные классы неорганических химических соединений 9
Основные классы неорганических химических соединений 9
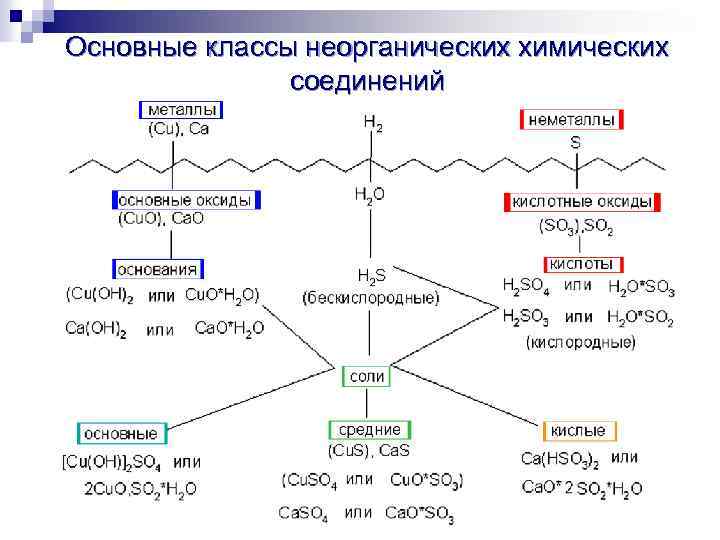 Основные классы неорганических химических соединений 10
Основные классы неорганических химических соединений 10
 ОКСИДЫ – соединения с кислородом Степень окисления кислорода = -2 11
ОКСИДЫ – соединения с кислородом Степень окисления кислорода = -2 11
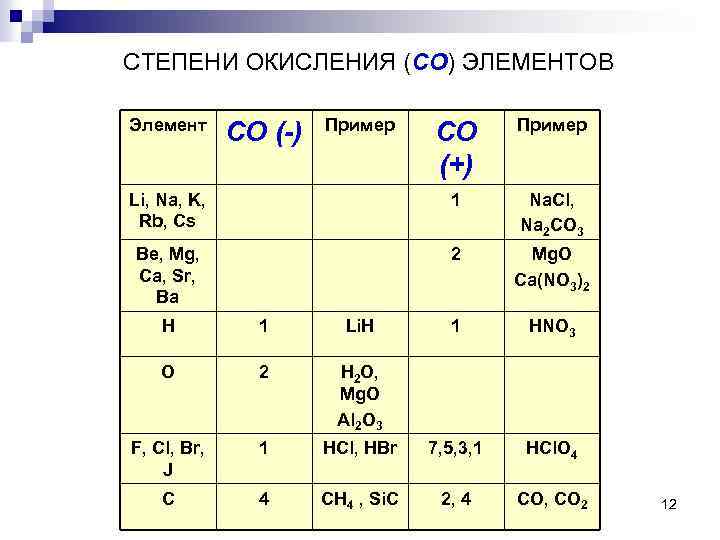 СТЕПЕНИ ОКИСЛЕНИЯ (СО) ЭЛЕМЕНТОВ Элемент СО (+) Пример Li, Na, K, Rb, Cs 1 Na. Cl, Na 2 CO 3 Be, Mg, Ca, Sr, Ba 2 Mg. O Ca(NO 3)2 1 HNO 3 СО (-) Пример H 1 Li. H O 2 H 2 O, Mg. O Al 2 O 3 F, Cl, Br, J 1 HCl, HBr 7, 5, 3, 1 HCl. O 4 CH 4 , Si. C 2, 4 CO, CO 2 12
СТЕПЕНИ ОКИСЛЕНИЯ (СО) ЭЛЕМЕНТОВ Элемент СО (+) Пример Li, Na, K, Rb, Cs 1 Na. Cl, Na 2 CO 3 Be, Mg, Ca, Sr, Ba 2 Mg. O Ca(NO 3)2 1 HNO 3 СО (-) Пример H 1 Li. H O 2 H 2 O, Mg. O Al 2 O 3 F, Cl, Br, J 1 HCl, HBr 7, 5, 3, 1 HCl. O 4 CH 4 , Si. C 2, 4 CO, CO 2 12
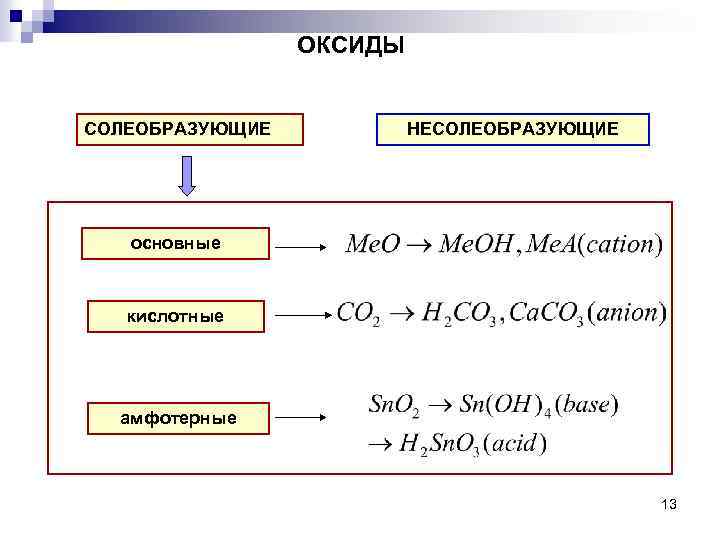 ОКСИДЫ СОЛЕОБРАЗУЮЩИЕ НЕСОЛЕОБРАЗУЮЩИЕ основные кислотные амфотерные 13
ОКСИДЫ СОЛЕОБРАЗУЮЩИЕ НЕСОЛЕОБРАЗУЮЩИЕ основные кислотные амфотерные 13
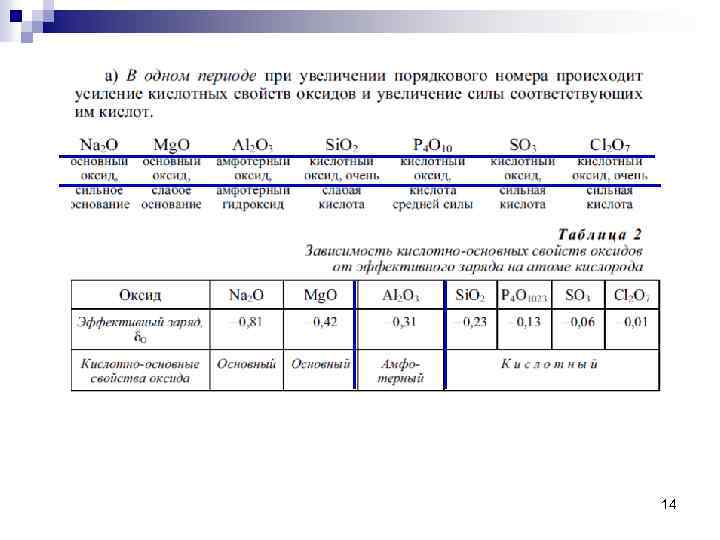 14
14
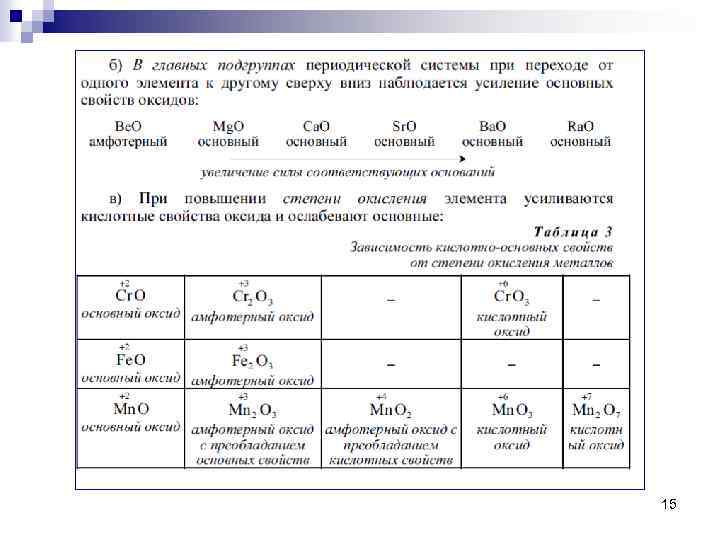 15
15
 ОСНОВНЫЕ ОКСИДЫ 16
ОСНОВНЫЕ ОКСИДЫ 16
 Химические свойства основных оксидов 17
Химические свойства основных оксидов 17
 КИСЛОТНЫЕ ОКСИДЫ 18
КИСЛОТНЫЕ ОКСИДЫ 18
 19
19
 20
20
 21
21
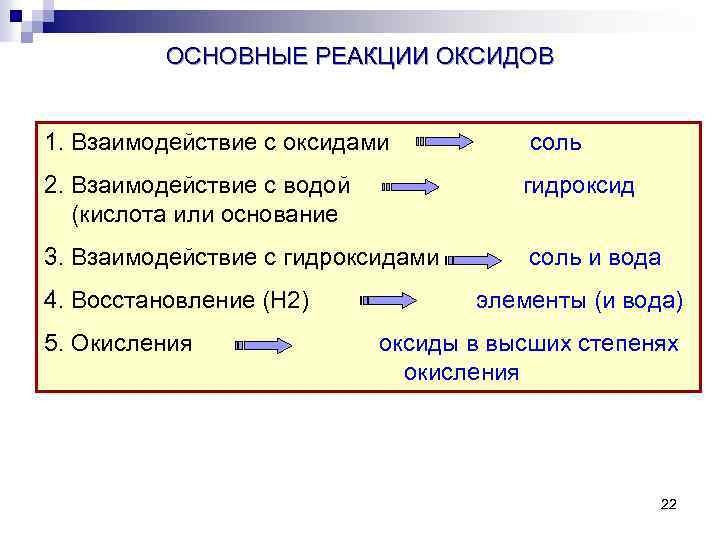 ОСНОВНЫЕ РЕАКЦИИ ОКСИДОВ 1. Взаимодействие с оксидами соль 2. Взаимодействие с водой (кислота или основание гидроксид 3. Взаимодействие с гидроксидами соль и вода 4. Восстановление (Н 2) 5. Окисления элементы (и вода) оксиды в высших степенях окисления 22
ОСНОВНЫЕ РЕАКЦИИ ОКСИДОВ 1. Взаимодействие с оксидами соль 2. Взаимодействие с водой (кислота или основание гидроксид 3. Взаимодействие с гидроксидами соль и вода 4. Восстановление (Н 2) 5. Окисления элементы (и вода) оксиды в высших степенях окисления 22
 Кислоты и Основания 1. Электролитическая теория (С. Аррениус) 2. Протонная (И. Брэнстэд и Т. Лоури) 3. Электронная (Г. Льюис) 23
Кислоты и Основания 1. Электролитическая теория (С. Аррениус) 2. Протонная (И. Брэнстэд и Т. Лоури) 3. Электронная (Г. Льюис) 23
 Электролитическая теория Кислота HCl = H+ + Cl- Основание KOH = K+ + OH- Амфотерное H 2 O = H+ + OH- 24
Электролитическая теория Кислота HCl = H+ + Cl- Основание KOH = K+ + OH- Амфотерное H 2 O = H+ + OH- 24
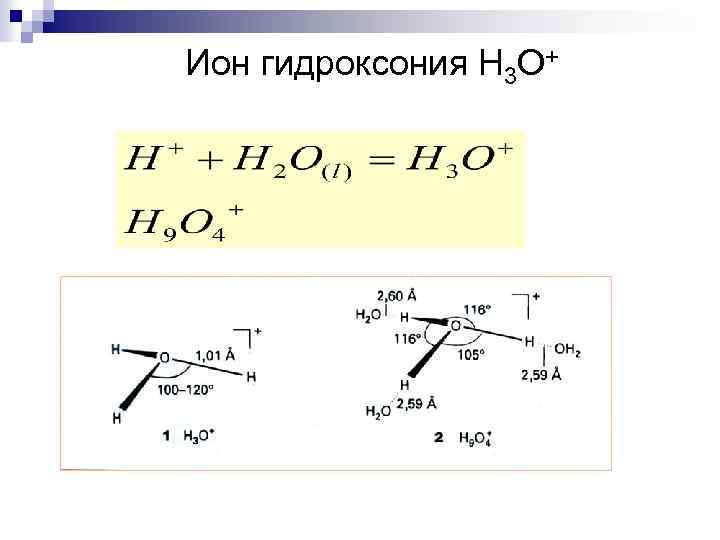 Ион гидроксония H 3 O+
Ион гидроксония H 3 O+
 Влияние полярного растворителя Диссоциация Сольватация Взаимодействие – водородные связи
Влияние полярного растворителя Диссоциация Сольватация Взаимодействие – водородные связи
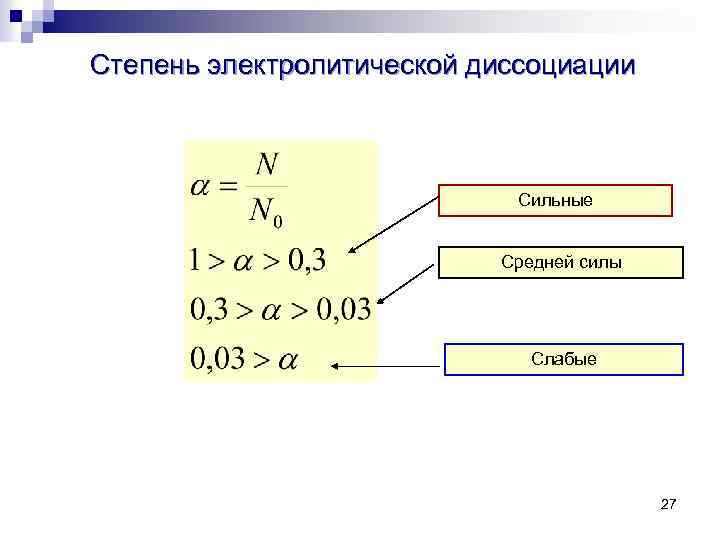 Степень электролитической диссоциации Сильные Средней силы Слабые 27
Степень электролитической диссоциации Сильные Средней силы Слабые 27
 КИСЛОТЫ И ОСНОВАНИЯ КИСЛОТНОСТЬ по Бренстеду : Донор протона (Н+) – кислота Акцептор протона - основание
КИСЛОТЫ И ОСНОВАНИЯ КИСЛОТНОСТЬ по Бренстеду : Донор протона (Н+) – кислота Акцептор протона - основание
 Равновесие в растворе кислота 1 +основание 2 кислота 2 + основание 1
Равновесие в растворе кислота 1 +основание 2 кислота 2 + основание 1
 Равновесие в растворе, ионное произведение воды
Равновесие в растворе, ионное произведение воды
 Нейтральный водный раствор p. H = p(OH)=7 Щелочной водный раствор p. H >7> p(OH) Кислый водный раствор p. H <7< p(OH) 31
Нейтральный водный раствор p. H = p(OH)=7 Щелочной водный раствор p. H >7> p(OH) Кислый водный раствор p. H <7< p(OH) 31
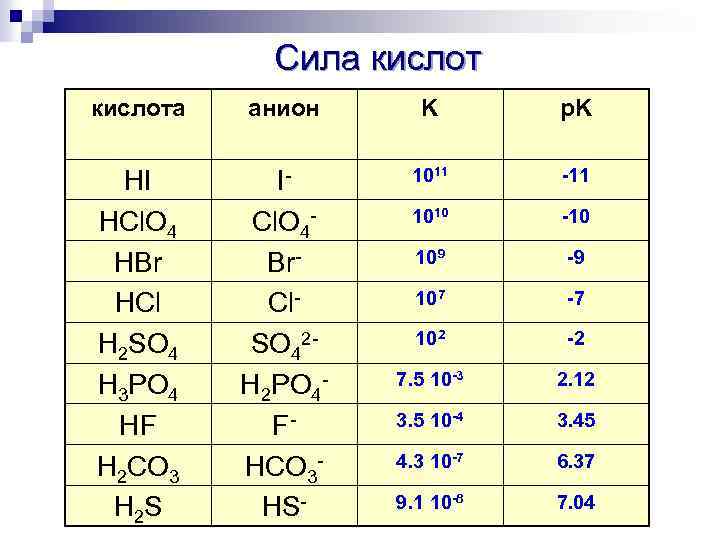 Сила кислота анион K р. K HI HCl. O 4 HBr HCl H 2 SO 4 H 3 PO 4 HF H 2 CO 3 H 2 S ICl. O 4 Br. Cl. SO 42 H 2 PO 4 FHCO 3 HS- 1011 -11 1010 -10 109 -9 107 -7 102 -2 7. 5 10 -3 2. 12 3. 5 10 -4 3. 45 4. 3 10 -7 6. 37 9. 1 10 -8 7. 04
Сила кислота анион K р. K HI HCl. O 4 HBr HCl H 2 SO 4 H 3 PO 4 HF H 2 CO 3 H 2 S ICl. O 4 Br. Cl. SO 42 H 2 PO 4 FHCO 3 HS- 1011 -11 1010 -10 109 -9 107 -7 102 -2 7. 5 10 -3 2. 12 3. 5 10 -4 3. 45 4. 3 10 -7 6. 37 9. 1 10 -8 7. 04
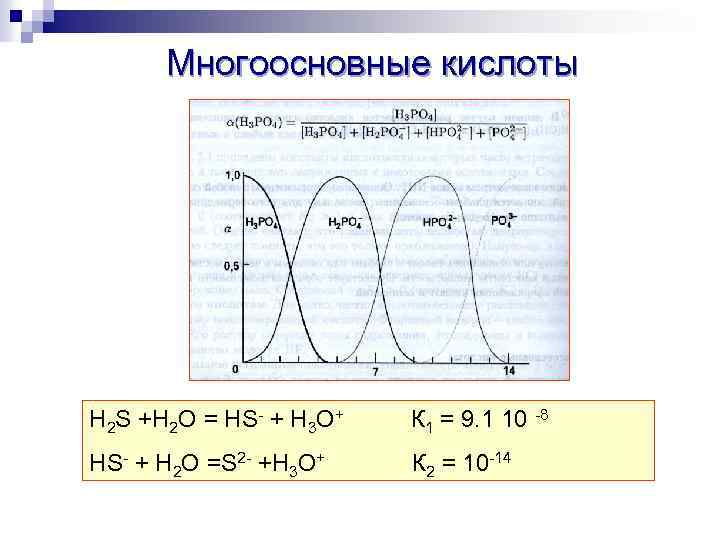 Многоосновные кислоты H 2 S +H 2 O = HS- + H 3 O+ К 1 = 9. 1 10 -8 HS- + H 2 O =S 2 - +H 3 O+ К 2 = 10 -14
Многоосновные кислоты H 2 S +H 2 O = HS- + H 3 O+ К 1 = 9. 1 10 -8 HS- + H 2 O =S 2 - +H 3 O+ К 2 = 10 -14
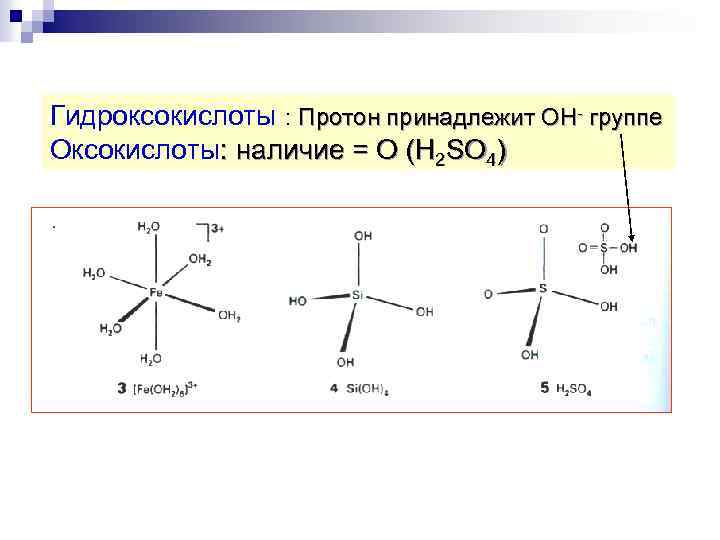 Гидроксокислоты : Протон принадлежит ОН- группе Оксокислоты: наличие = О (Н 2 SO 4)
Гидроксокислоты : Протон принадлежит ОН- группе Оксокислоты: наличие = О (Н 2 SO 4)
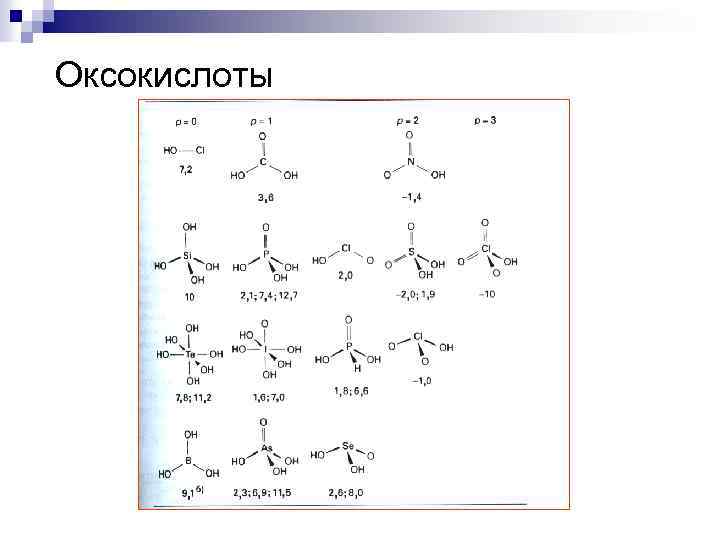 Оксокислоты
Оксокислоты
 Электронная теория (Г. Льюис) Кислота – принимает электронную пару Основание- отдает электронную пару Кислота Льюиса обладает низкой по энергии свободной молекулярной орбиталью BF 3, Zn. Cl 2, Fe. Cl 3, Sn. Cl 4 Основание Льюиса обладает высокой по энергии заполненной молекулярной орбиталью Амины RNH 2, R 2 NH, R 3 N 36
Электронная теория (Г. Льюис) Кислота – принимает электронную пару Основание- отдает электронную пару Кислота Льюиса обладает низкой по энергии свободной молекулярной орбиталью BF 3, Zn. Cl 2, Fe. Cl 3, Sn. Cl 4 Основание Льюиса обладает высокой по энергии заполненной молекулярной орбиталью Амины RNH 2, R 2 NH, R 3 N 36
 Реакции в растворах Гетерогенное равновесие ПР Условие выпадения осадка
Реакции в растворах Гетерогенное равновесие ПР Условие выпадения осадка
 Произведение растворимости
Произведение растворимости
 Гидролиз растворимых солей Соли слабой кислоты Силикаты : Na 2 Si. O 3, Как нейтрализовать OH- ?
Гидролиз растворимых солей Соли слабой кислоты Силикаты : Na 2 Si. O 3, Как нейтрализовать OH- ?
 Гидролиз растворимых солей Соли слабого основания Хлориды, нитраты: Fe. Cl 3 Как нейтрализовать H+ ?
Гидролиз растворимых солей Соли слабого основания Хлориды, нитраты: Fe. Cl 3 Как нейтрализовать H+ ?
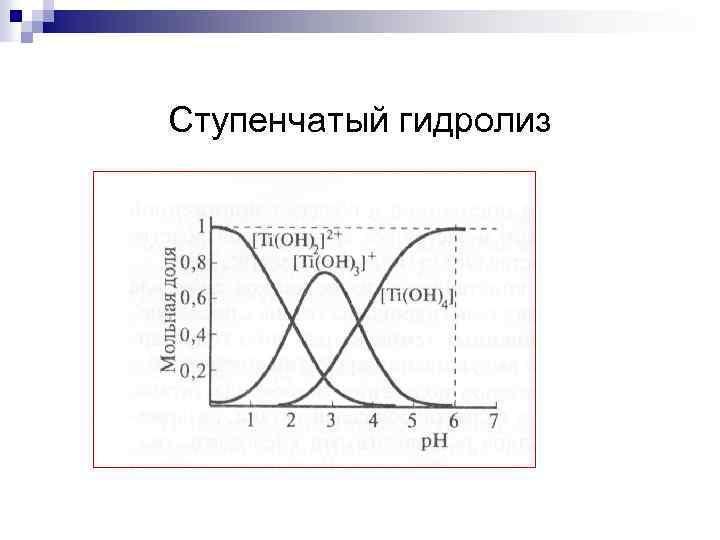 Ступенчатый гидролиз
Ступенчатый гидролиз
 42
42
 43
43
 44
44
 45
45
 46
46


