lektsia_2_-_1_kurs.pptx
- Количество слайдов: 26

Лекция 2 Образование дисперсных систем
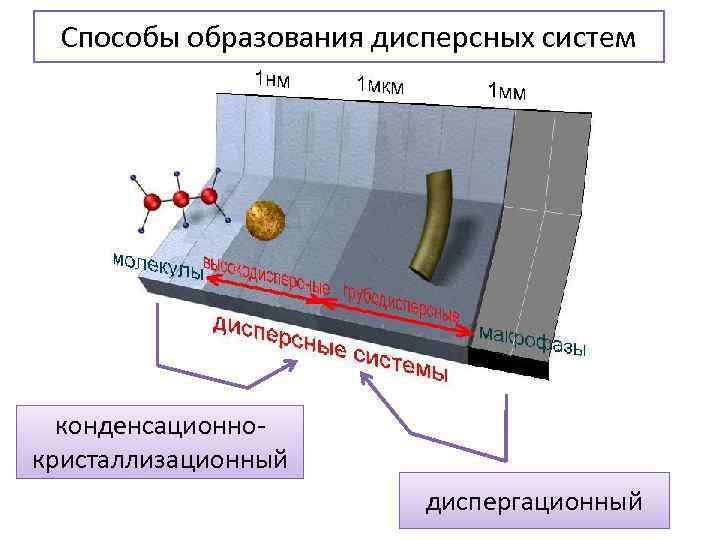
Способы образования дисперсных систем конденсационнокристаллизационный диспергационный
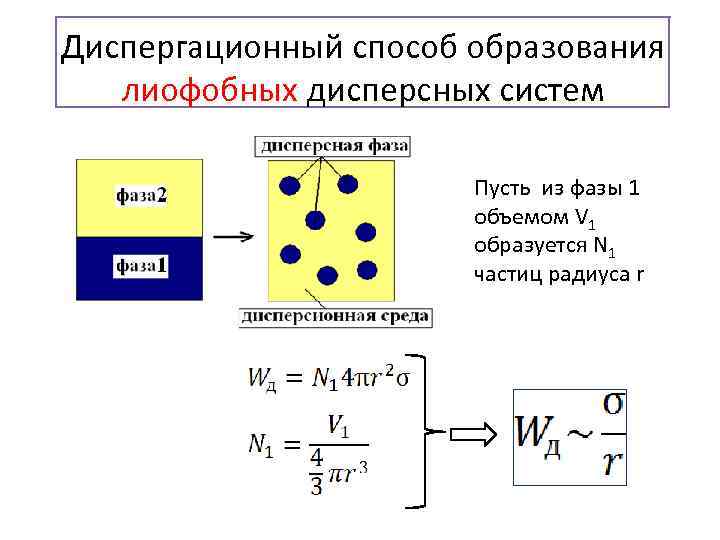
Диспергационный способ образования лиофобных дисперсных систем Пусть из фазы 1 объемом V 1 образуется N 1 частиц радиуса r
![Р [Н/м 2] – прочность твердого тела (сила, необходимая для разрыва столбика единичного сечения) Р [Н/м 2] – прочность твердого тела (сила, необходимая для разрыва столбика единичного сечения)](https://present5.com/presentation/17579586_74569001/image-4.jpg)
Р [Н/м 2] – прочность твердого тела (сила, необходимая для разрыва столбика единичного сечения) формула Гриффитса Е – модуль упругости, l. С – размер критической трещины
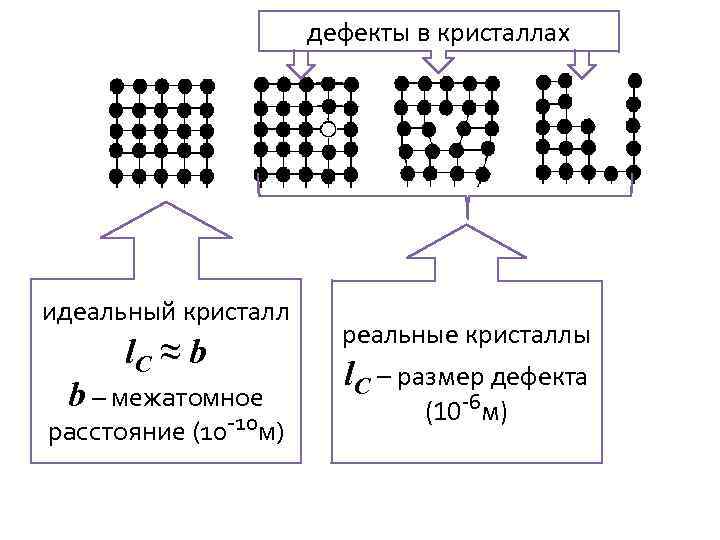
дефекты в кристаллах идеальный кристалл l. С ≈ b b – межатомное расстояние (10 -10 м) реальные кристаллы l. С – размер дефекта (10 -6 м)
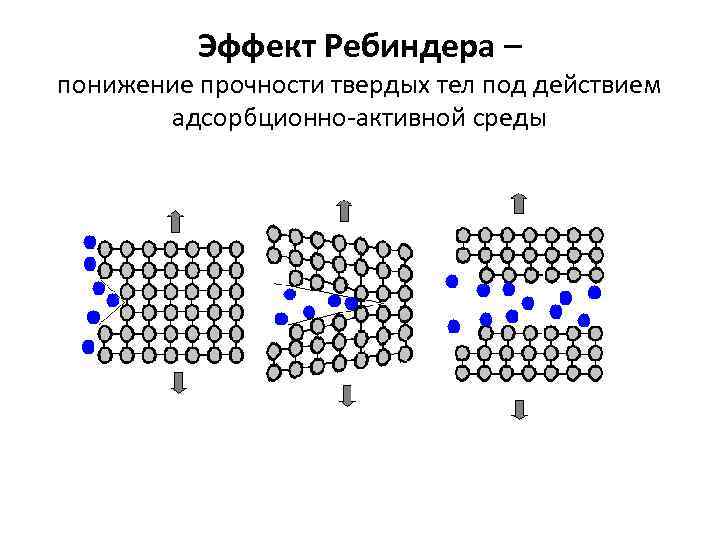
Эффект Ребиндера – понижение прочности твердых тел под действием адсорбционно-активной среды

Условия проявления эффекта Ребиндера - родственность твердого тела и жидкой среды - одновременное действие среды и нагрузки - реальная структура твердого тела (наличие дефектов)

Действие ртути на цинк
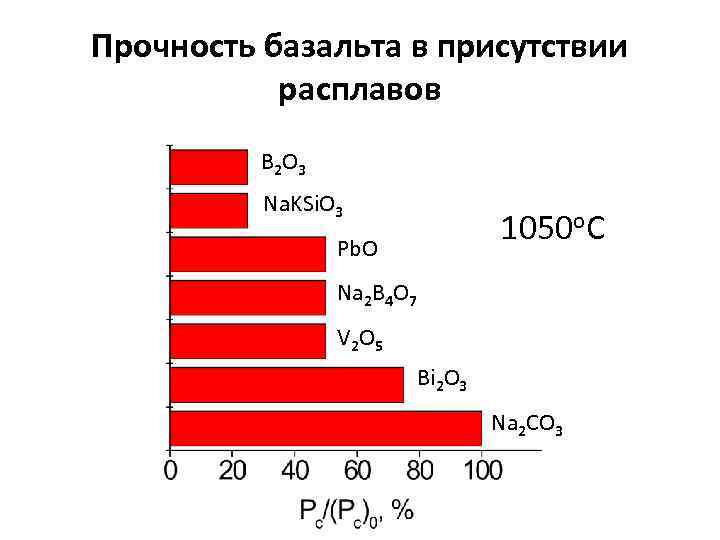
Прочность базальта в присутствии расплавов B 2 O 3 Na. KSi. O 3 1050 o. C Pb. O Na 2 B 4 O 7 V 2 O 5 Bi 2 O 3 Na 2 CO 3

Значение эффекта Ребиндера в геологии - эрозия горных пород - физико-химическая геомеханика (воздействие водных растворов и магматических расплавов на твердую породу при одновременном действии механической нагрузки) Вулканическая деятельность Выветривание Образование разломов
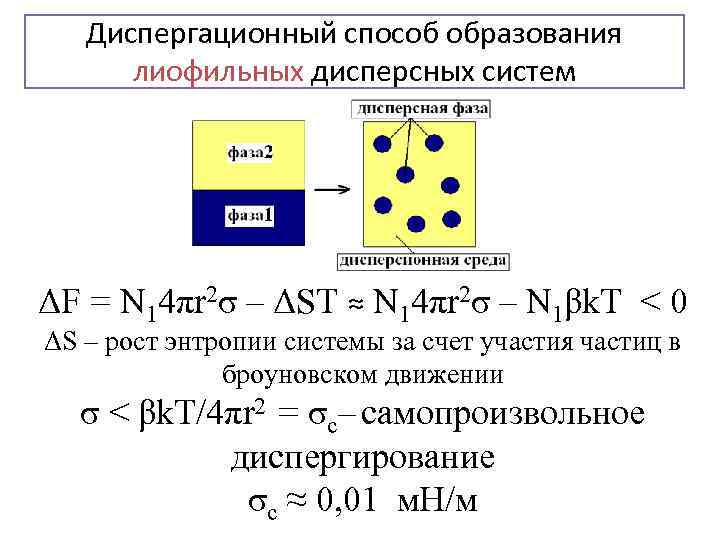
Диспергационный способ образования лиофильных дисперсных систем ΔF = N 14πr 2σ – ΔST ≈ N 14πr 2σ – N 1βk. T < 0 ΔS – рост энтропии системы за счет участия частиц в броуновском движении σ < βk. T/4πr 2 = σc– самопроизвольное диспергирование σc ≈ 0, 01 м. Н/м
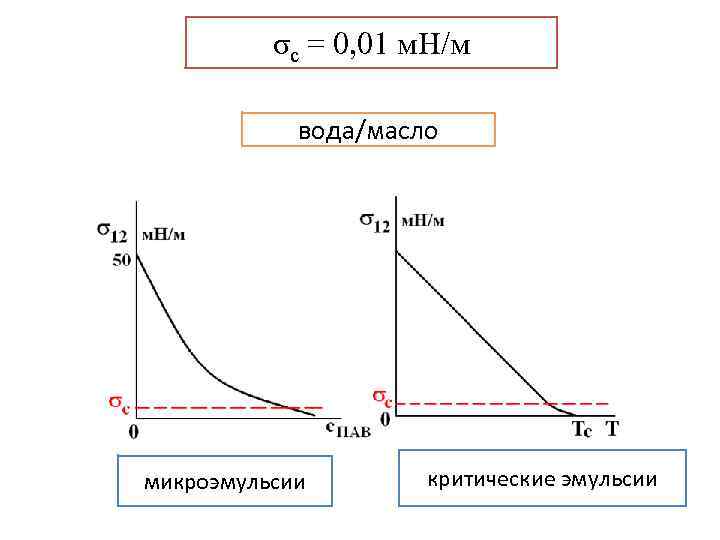
σc = 0, 01 м. Н/м вода/масло микроэмульсии критические эмульсии
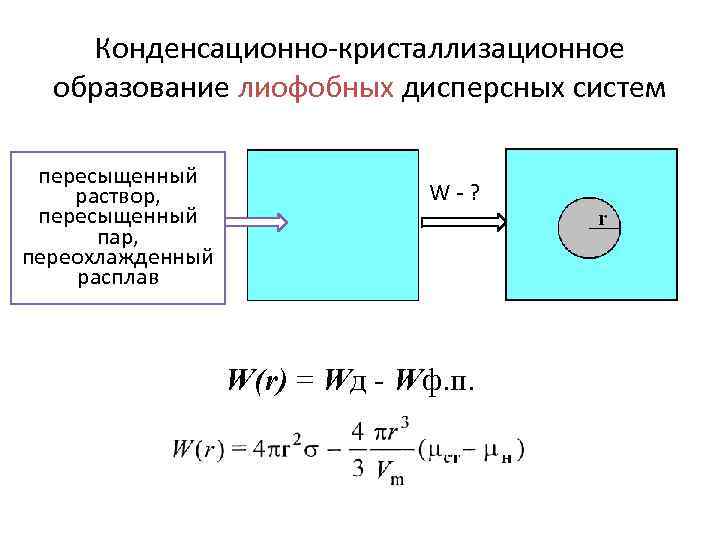
Конденсационно-кристаллизационное образование лиофобных дисперсных систем пересыщенный раствор, пересыщенный пар, переохлажденный расплав W-? W(r) = Wд - Wф. п.


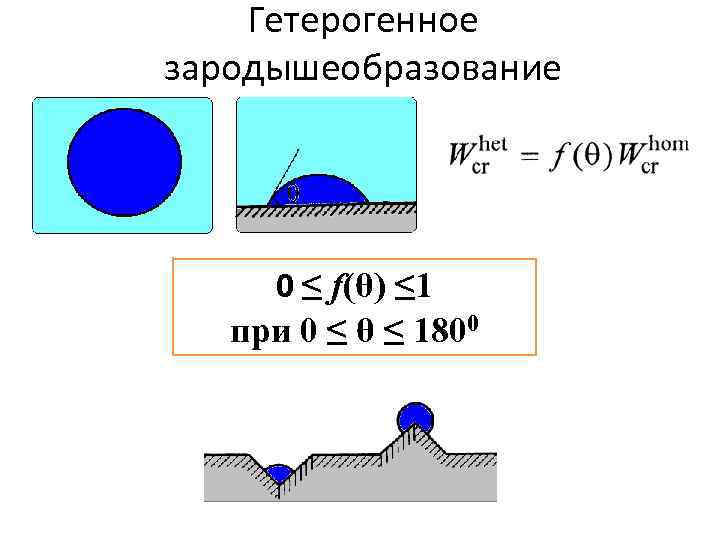
Гетерогенное зародышеобразование 0 ≤ f(θ) ≤ 1 при 0 ≤ θ ≤ 1800
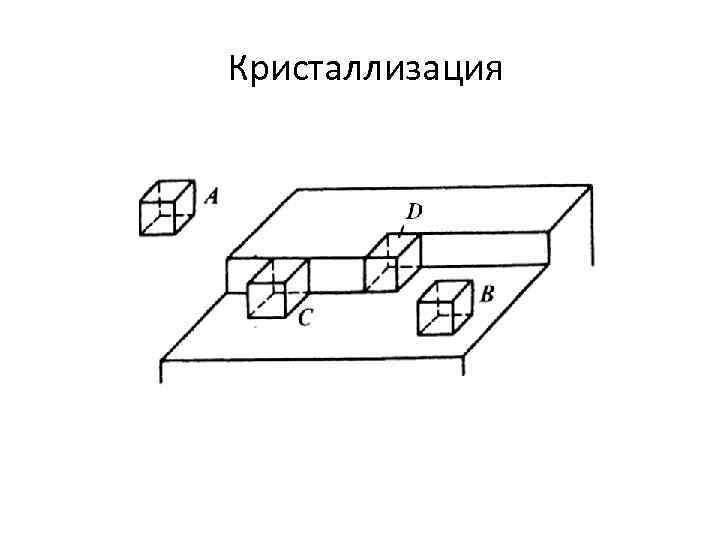
Кристаллизация

Образование лиофобных ДС Образование плохорастворимых солей: сульфидных руд (Ag, Zn, Hg, As, Ni) барита Ba. Cl 2 + Na 2 SO 4 → Ba. SO 4 ↓ + Na. Cl Образование золей в гидротермальных водах Fe(HCO 3)2 + O 2 + H 2 O → Fe(OH)3 ↓+ CO 2 H 2 S + O 2 → S ↓ + H 2 O Образование тумана, облаков (конденсация из пара) Образование поликристаллов при кристаллизации из расплавов (из магмы)
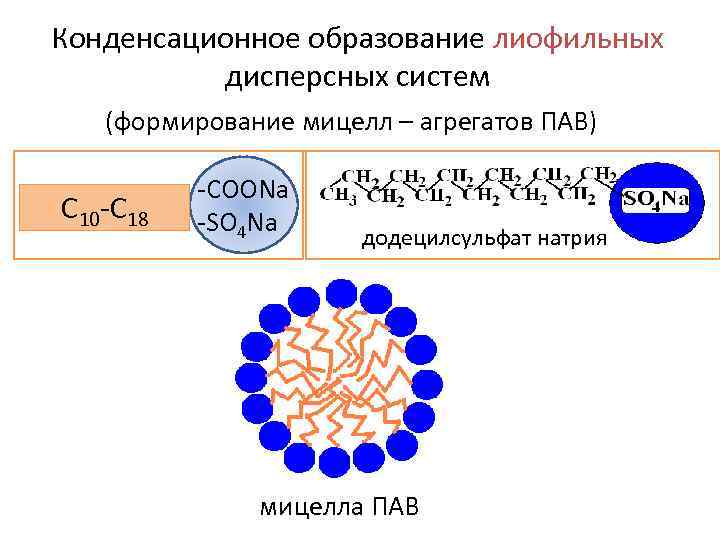
Конденсационное образование лиофильных дисперсных систем (формирование мицелл – агрегатов ПАВ) С 10 -С 18 -COONa -SO 4 Na додецилсульфат натрия мицелла ПАВ
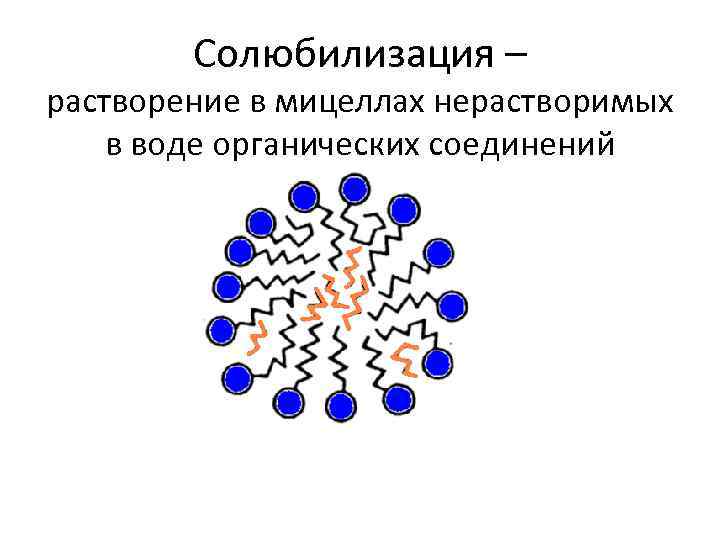
Солюбилизация – растворение в мицеллах нерастворимых в воде органических соединений
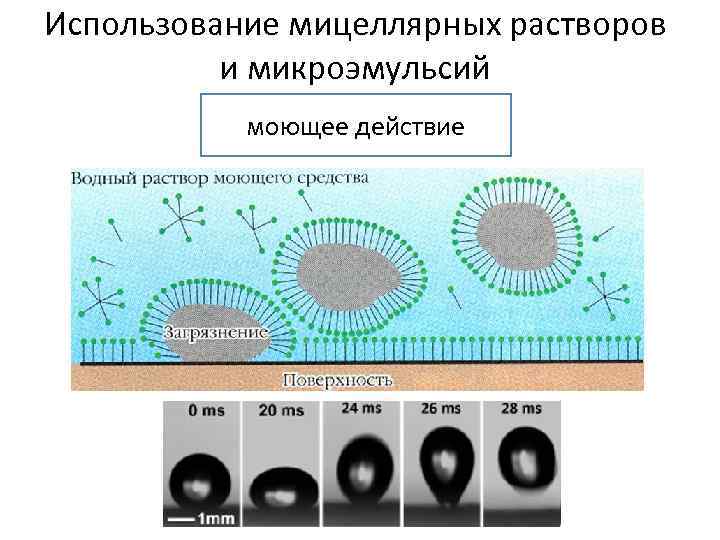
Использование мицеллярных растворов и микроэмульсий моющее действие
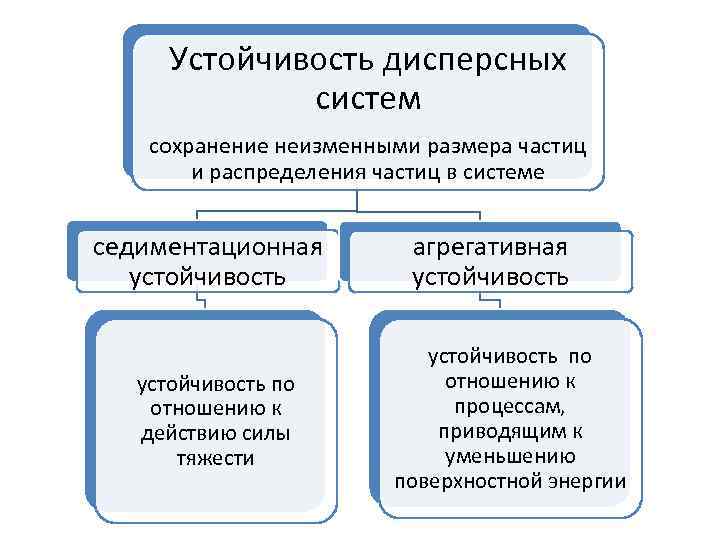
Устойчивость дисперсных систем сохранение неизменными размера частиц и распределения частиц в системе седиментационная устойчивость по отношению к действию силы тяжести агрегативная устойчивость по отношению к процессам, приводящим к уменьшению поверхностной энергии
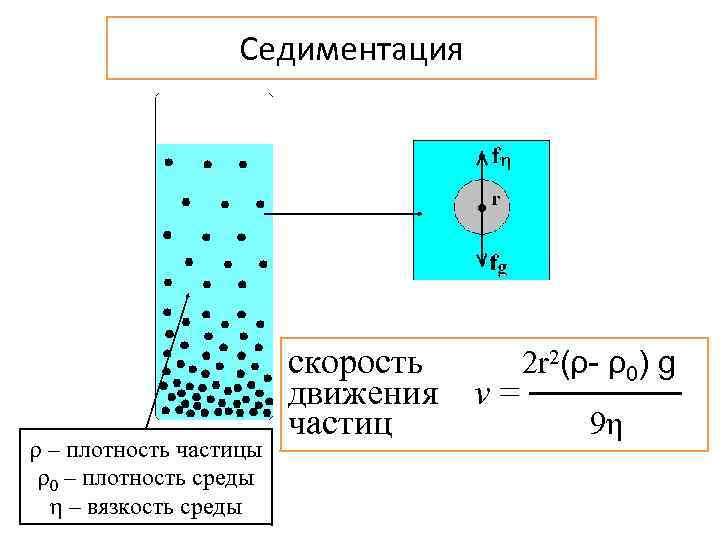
Седиментация ρ – плотность частицы ρ0 – плотность среды η – вязкость среды скорость движения частиц 2 r 2(ρ- ρ0) g v = ────── 9η
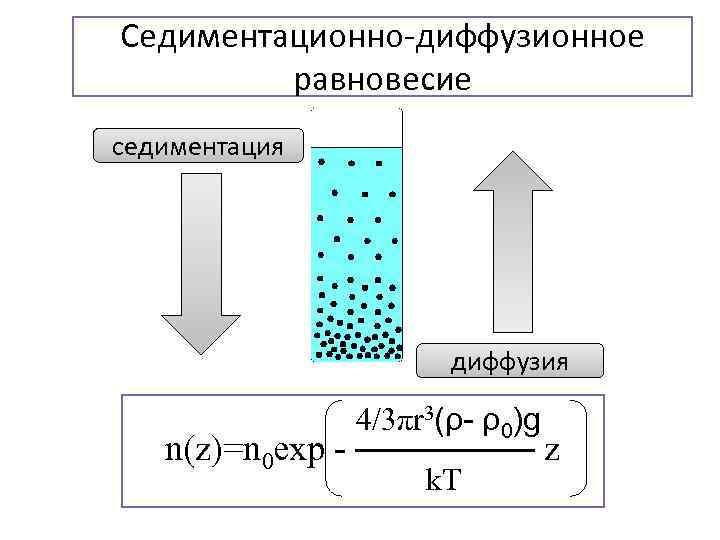
Седиментационно-диффузионное равновесие седиментация диффузия 4/3πr 3(ρ- ρ0)g n(z)=n 0 exp - ————— z k. T
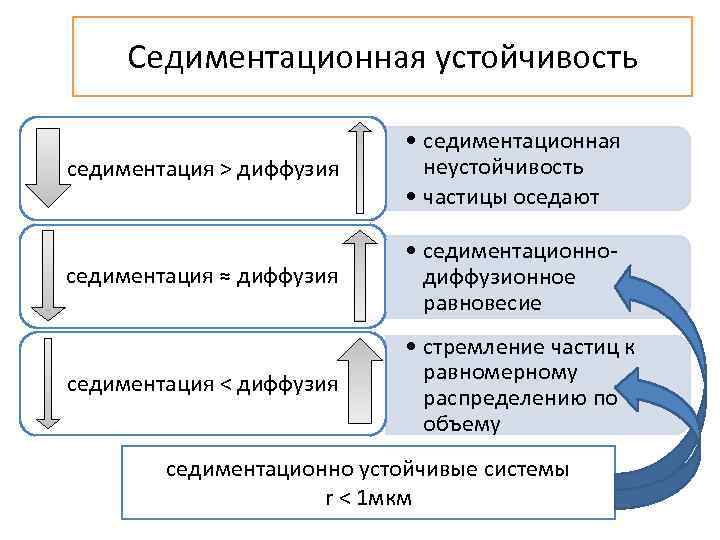
Седиментационная устойчивость седиментация > диффузия • седиментационная неустойчивость • частицы оседают седиментация ≈ диффузия • седиментационнодиффузионное равновесие седиментация < диффузия • стремление частиц к равномерному распределению по объему седиментационно устойчивые системы r < 1 мкм
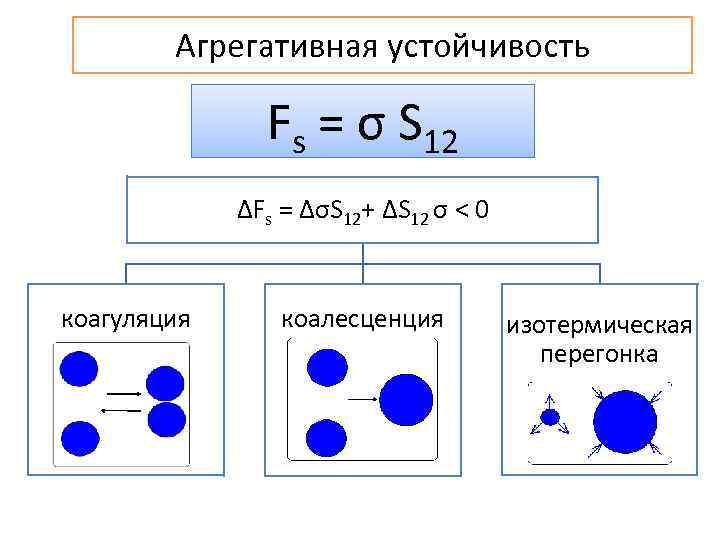
Агрегативная устойчивость Fs = σ S 12 ΔFs = ΔσS 12+ ΔS 12 σ < 0 коагуляция коалесценция изотермическая перегонка
lektsia_2_-_1_kurs.pptx