Презентация_Лекция_02_Белки.ppt
- Количество слайдов: 21

Лекция 2 Конформация белков: принципы формирования 1. Связи, определяющие конформацию белковых молекул l ковалентные связи: l пептидная дисульфидная l нековалентные взаимодействия: l ионные взаимодействия водородная связь гидрофобные взаимодействия ван-дер-ваальсовы взаимодействия l l 2. Уровни пространственной организации белковых молекул l первичная структура белков l вторичная структура белков l третичная структура белков l четвертичная структура белков
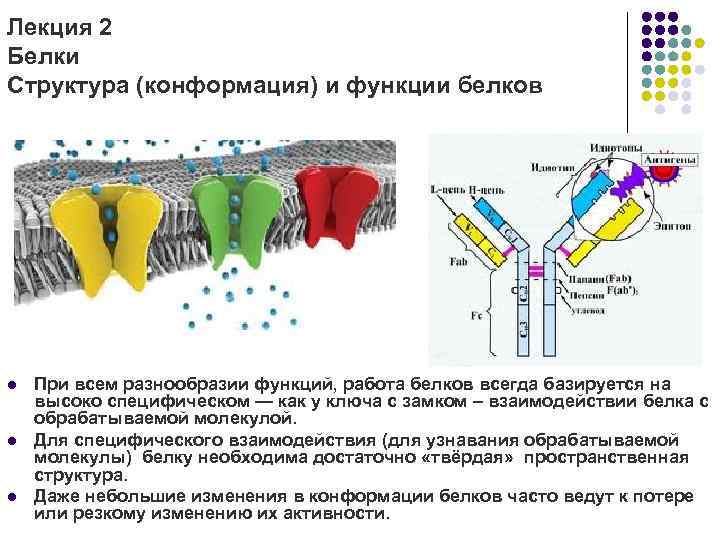
Лекция 2 Белки Структура (конформация) и функции белков l l l При всем разнообразии функций, работа белков всегда базируется на высоко специфическом — как у ключа с замком – взаимодействии белка с обрабатываемой молекулой. Для специфического взаимодействия (для узнавания обрабатываемой молекулы) белку необходима достаточно «твёрдая» пространственная структура. Даже небольшие изменения в конформации белков часто ведут к потере или резкому изменению их активности.
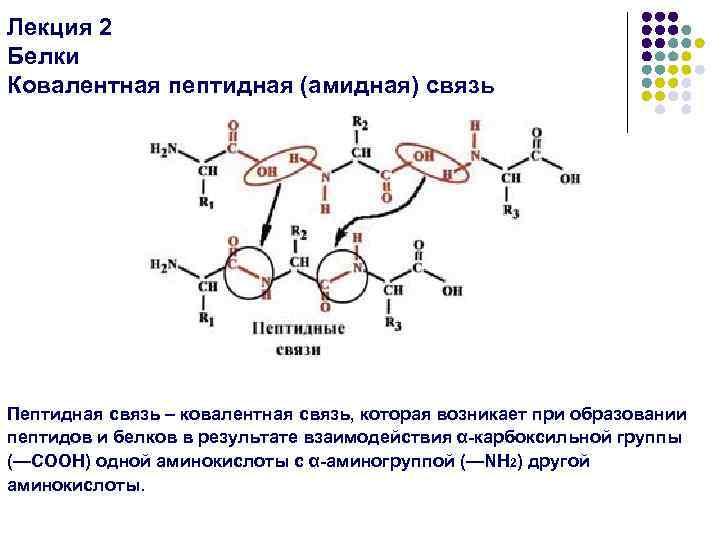
Лекция 2 Белки Ковалентная пептидная (амидная) связь Пептидная связь – ковалентная связь, которая возникает при образовании пептидов и белков в результате взаимодействия α-карбоксильной группы (—СООН) одной аминокислоты с α-аминогруппой (—NH 2) другой аминокислоты.
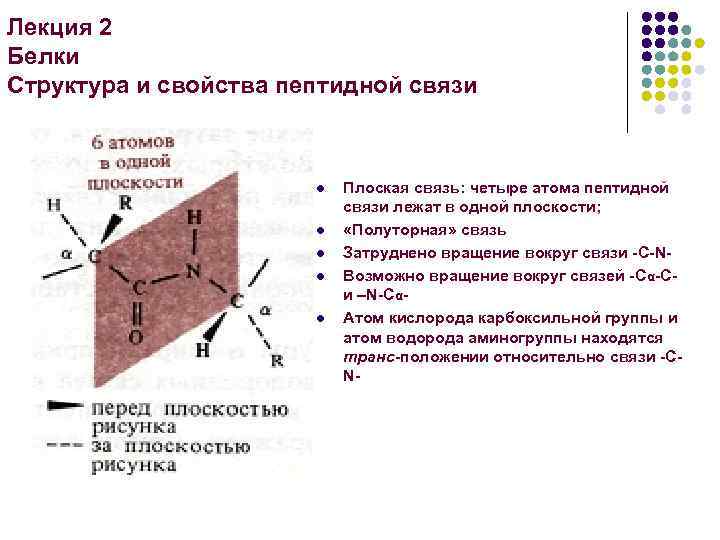
Лекция 2 Белки Структура и свойства пептидной связи l l l Плоская связь: четыре атома пептидной связи лежат в одной плоскости; «Полуторная» связь Затруднено вращение вокруг связи -С-NВозможно вращение вокруг связей -Cα-Cи –N-СαАтом кислорода карбоксильной группы и атом водорода аминогруппы находятся транс-положении относительно связи -CN-
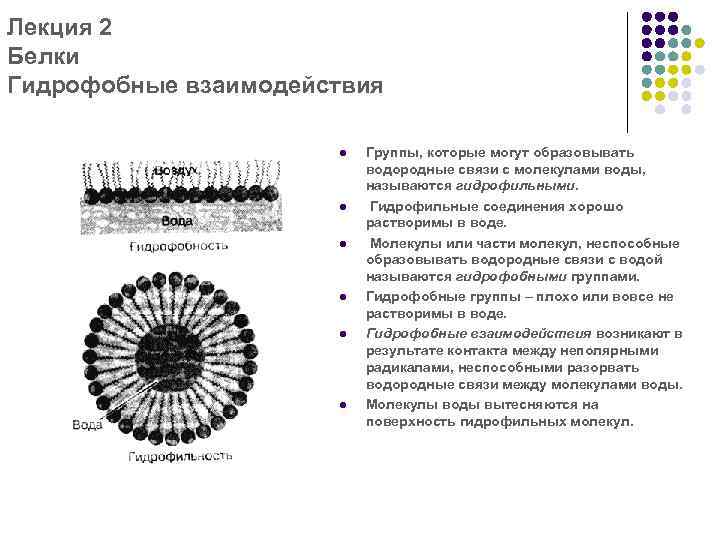
Лекция 2 Белки Гидрофобные взаимодействия l l l Группы, которые могут образовывать водородные связи с молекулами воды, называются гидрофильными. Гидрофильные соединения хорошо растворимы в воде. Молекулы или части молекул, неспособные образовывать водородные связи с водой называются гидрофобными группами. Гидрофобные группы – плохо или вовсе не растворимы в воде. Гидрофобные взаимодействия возникают в результате контакта между неполярными радикалами, неспособными разорвать водородные связи между молекулами воды. Молекулы воды вытесняются на поверхность гидрофильных молекул.
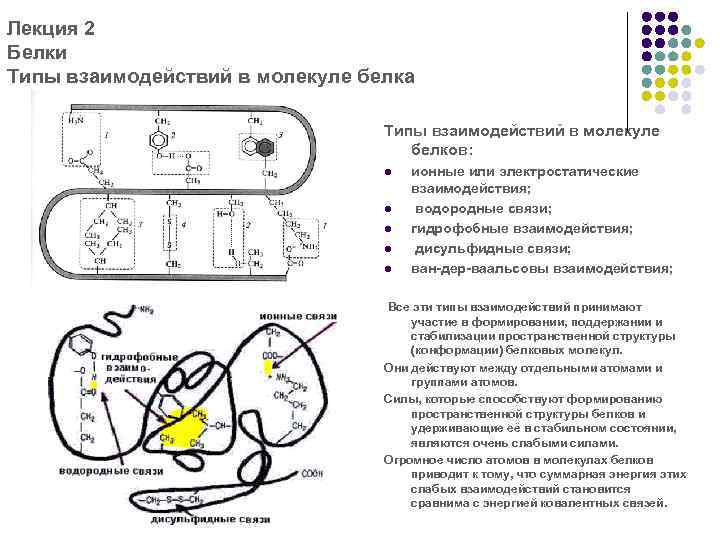
Лекция 2 Белки Типы взаимодействий в молекуле белка Типы взаимодействий в молекуле белков: l l l ионные или электростатические взаимодействия; водородные связи; гидрофобные взаимодействия; дисульфидные связи; ван-дер-ваальсовы взаимодействия; Все эти типы взаимодействий принимают участие в формировании, поддержании и стабилизации пространственной структуры (конформации) белковых молекул. Они действуют между отдельными атомами и группами атомов. Силы, которые способствуют формированию пространственной структуры белков и удерживающие её в стабильном состоянии, являются очень слабыми силами. Огромное число атомов в молекулах белков приводит к тому, что суммарная энергия этих слабых взаимодействий становится сравнима с энергией ковалентных связей.
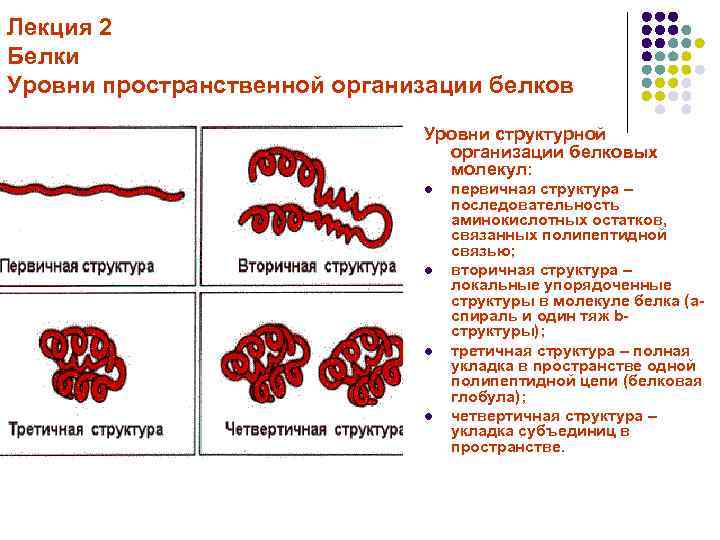
Лекция 2 Белки Уровни пространственной организации белков Уровни структурной организации белковых молекул: l l первичная структура – последовательность аминокислотных остатков, связанных полипептидной связью; вторичная структура – локальные упорядоченные структуры в молекуле белка (aспираль и один тяж bструктуры); третичная структура – полная укладка в пространстве одной полипептидной цепи (белковая глобула); четвертичная структура – укладка субъединиц в пространстве.
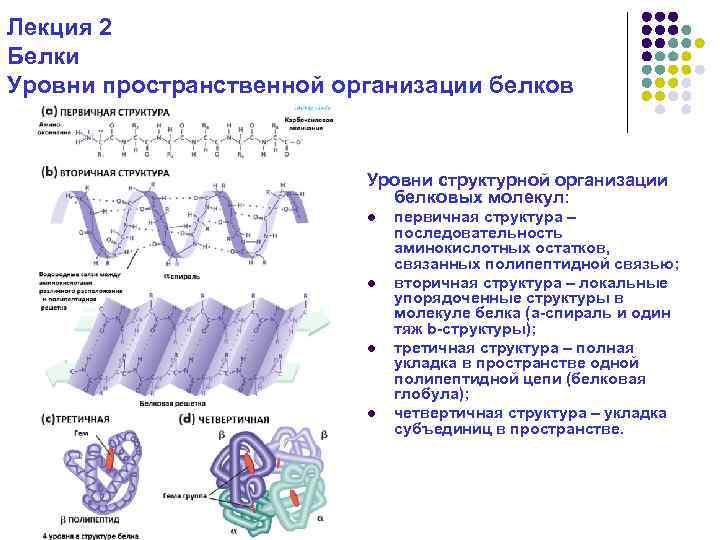
Лекция 2 Белки Уровни пространственной организации белков Уровни структурной организации белковых молекул: l l первичная структура – последовательность аминокислотных остатков, связанных полипептидной связью; вторичная структура – локальные упорядоченные структуры в молекуле белка (a-спираль и один тяж b-структуры); третичная структура – полная укладка в пространстве одной полипептидной цепи (белковая глобула); четвертичная структура – укладка субъединиц в пространстве.
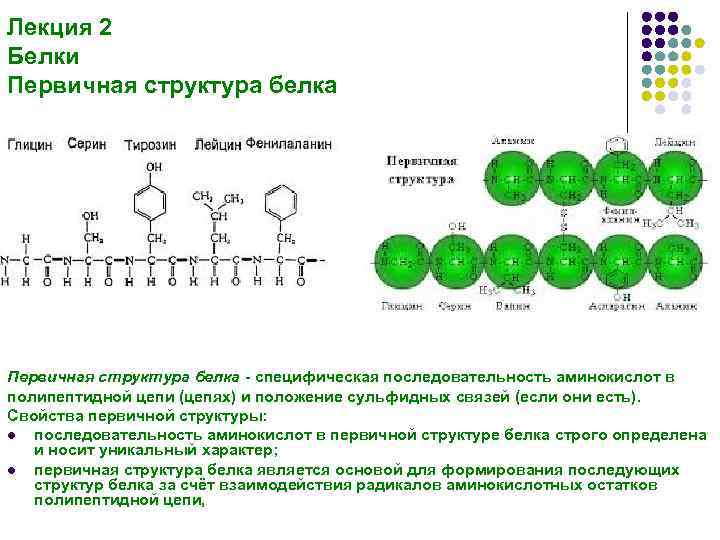
Лекция 2 Белки Первичная структура белка - специфическая последовательность аминокислот в полипептидной цепи (цепях) и положение сульфидных связей (если они есть). Свойства первичной структуры: l последовательность аминокислот в первичной структуре белка строго определена и носит уникальный характер; l первичная структура белка является основой для формирования последующих структур белка за счёт взаимодействия радикалов аминокислотных остатков полипептидной цепи,
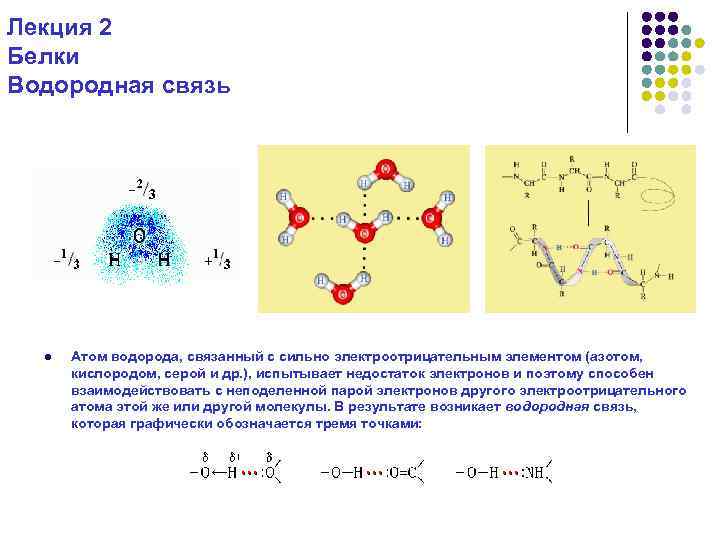
Лекция 2 Белки Водородная связь l Атом водорода, связанный с сильно электроотрицательным элементом (азотом, кислородом, серой и др. ), испытывает недостаток электронов и поэтому способен взаимодействовать с неподеленной парой электронов другого электроотрицательного атома этой же или другой молекулы. В результате возникает водородная связь, которая графически обозначается тремя точками:
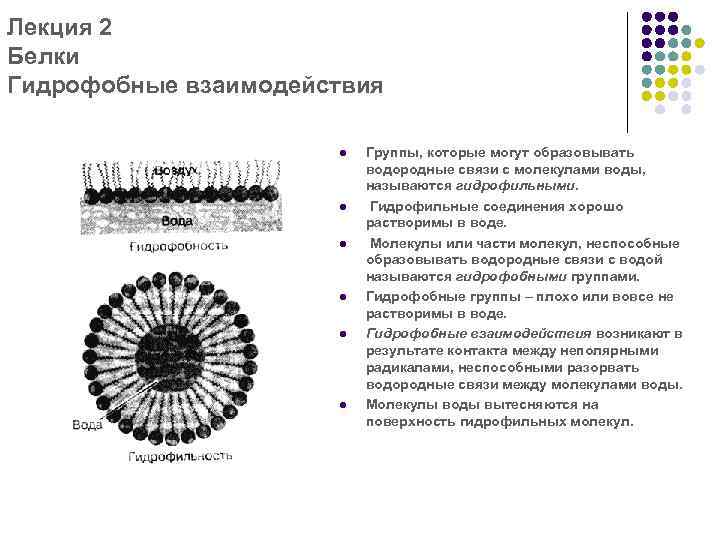
Лекция 2 Белки Гидрофобные взаимодействия l l l Группы, которые могут образовывать водородные связи с молекулами воды, называются гидрофильными. Гидрофильные соединения хорошо растворимы в воде. Молекулы или части молекул, неспособные образовывать водородные связи с водой называются гидрофобными группами. Гидрофобные группы – плохо или вовсе не растворимы в воде. Гидрофобные взаимодействия возникают в результате контакта между неполярными радикалами, неспособными разорвать водородные связи между молекулами воды. Молекулы воды вытесняются на поверхность гидрофильных молекул.

Лекция 2 Белки Типы взаимодействий в молекуле белка Типы взаимодействий в молекуле белков: l l l ионные или электростатические взаимодействия; водородные связи; гидрофобные взаимодействия; дисульфидные связи; ван-дер-ваальсовы взаимодействия; Все эти типы взаимодействий принимают участие в формировании, поддержании и стабилизации пространственной структуры (конформации) белковых молекул. Они действуют между отдельными атомами и группами атомов. Силы, которые способствуют формированию пространственной структуры белков и удерживающие её в стабильном состоянии, являются очень слабыми силами. Огромное число атомов в молекулах белков приводит к тому, что суммарная энергия этих слабых взаимодействий становится сравнима с энергией ковалентных связей.
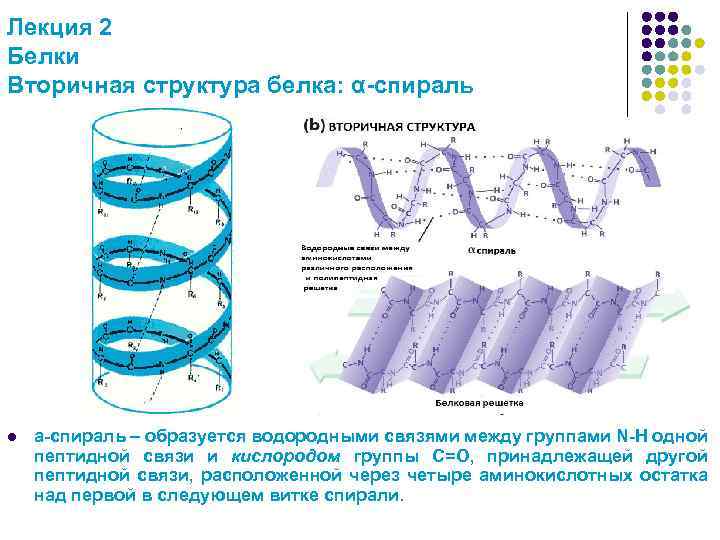
Лекция 2 Белки Вторичная структура белка: α-спираль l a-спираль – образуется водородными связями между группами N-H одной пептидной связи и кислородом группы С=О, принадлежащей другой пептидной связи, расположенной через четыре аминокислотных остатка над первой в следующем витке спирали.

Лекция 2 Белки Третичная структура: ленточная модель В ленточной модели третичной структуры белка: l красным цветом изображены α-спирали; l жёлтым цветом изображены β -складки; l серым цветом изображены неструктурированные участки полипептидной цепи.
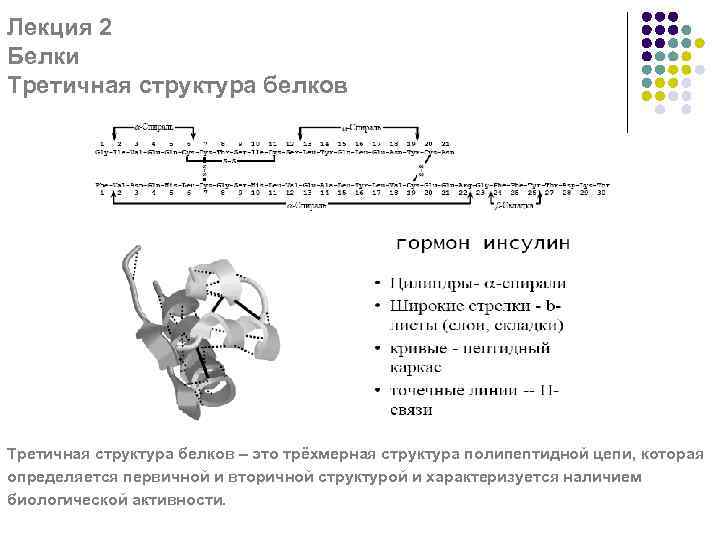
Лекция 2 Белки Третичная структура белков – это трёхмерная структура полипептидной цепи, которая определяется первичной и вторичной структурой и характеризуется наличием биологической активности.
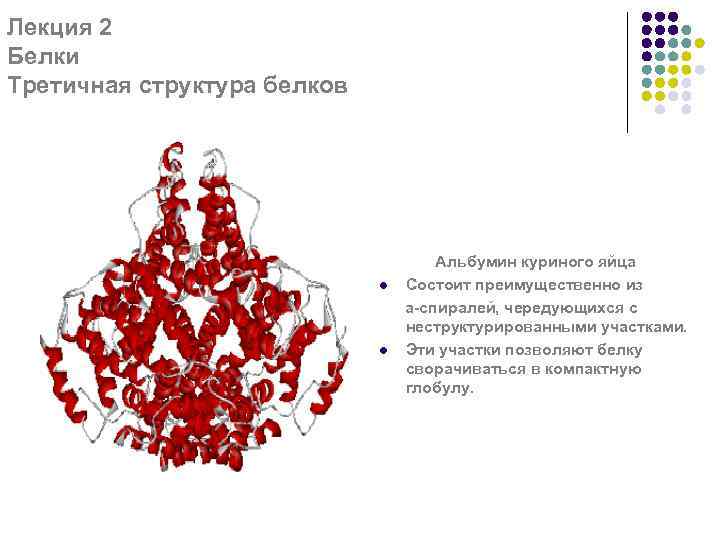
Лекция 2 Белки Третичная структура белков l l Альбумин куриного яйца Состоит преимущественно из a-спиралей, чередующихся с неструктурированными участками. Эти участки позволяют белку сворачиваться в компактную глобулу.
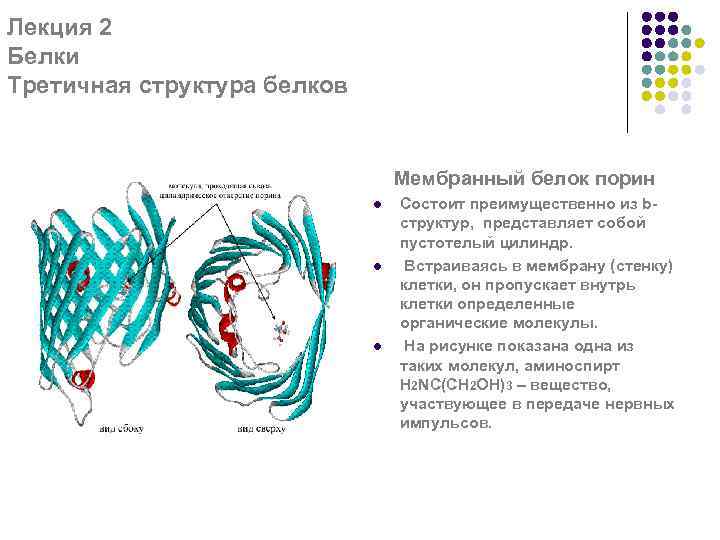
Лекция 2 Белки Третичная структура белков Мембранный белок порин l l l Состоит преимущественно из bструктур, представляет собой пустотелый цилиндр. Встраиваясь в мембрану (стенку) клетки, он пропускает внутрь клетки определенные органические молекулы. На рисунке показана одна из таких молекул, аминоспирт H 2 NC(CH 2 OH)3 – вещество, участвующее в передаче нервных импульсов.
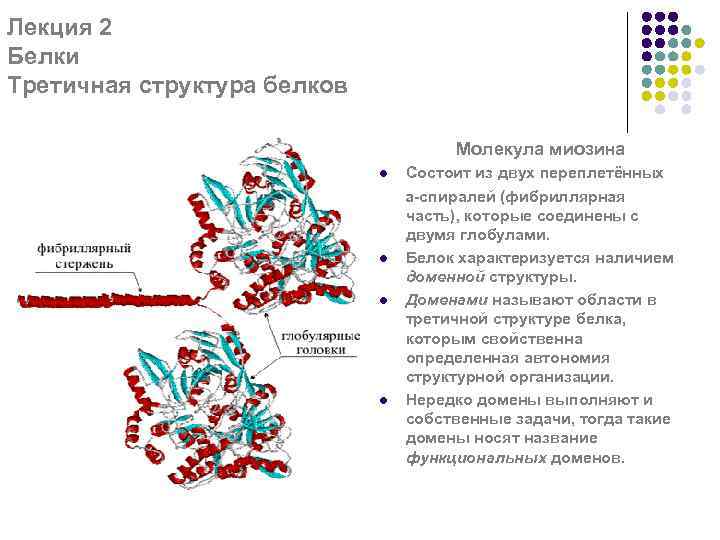
Лекция 2 Белки Третичная структура белков Молекула миозина l l Состоит из двух переплетённых a-спиралей (фибриллярная часть), которые соединены с двумя глобулами. Белок характеризуется наличием доменной структуры. Доменами называют области в третичной структуре белка, которым свойственна определенная автономия структурной организации. Нередко домены выполняют и собственные задачи, тогда такие домены носят название функциональных доменов.

Лекция 2 Белки Четвертичная структура белков l Четвертичная структура - способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой или разной третичной структурой. l Взаимодействие полипептидных цепей при формировании четвертичной структуры происходит за счет образования водородных и ионных связей, а также гидрофобных взаимодействий. l Каждая отдельно взятая полипептидная цепь, получившая название протомера или субъединицы, чаще всего не обладает биологической активностью. l Биологическая активность проявляется только при четвертичной структуры. белка наличии
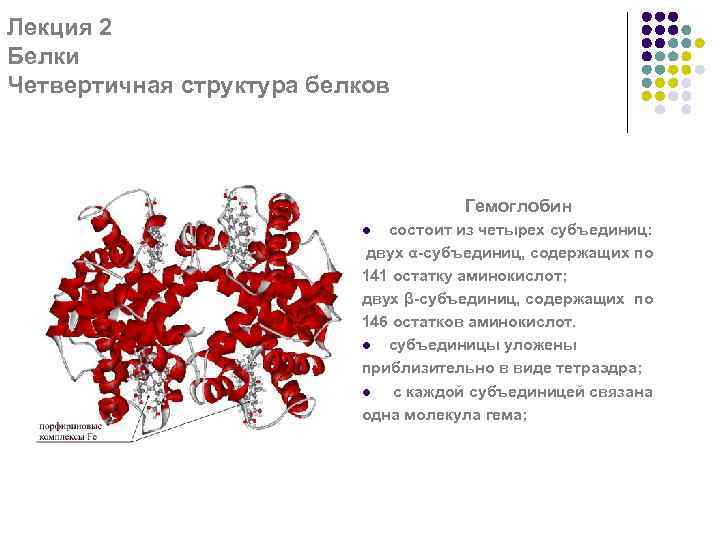
Лекция 2 Белки Четвертичная структура белков Гемоглобин состоит из четырех субъединиц: двух α-субъединиц, содержащих по 141 остатку аминокислот; двух β-субъединиц, содержащих по 146 остатков аминокислот. l субъединицы уложены приблизительно в виде тетраэдра; l с каждой субъединицей связана одна молекула гема; l

Лекция 2 Белки Четвертичная структура белков Образование четвертичной структуры молекулы белка ферритина Третичная структура каждой из субъединиц ферритина представляет собой структуру из 4 -х параллельно уложенных цепей. При объединении субъединиц в единый ансамбль образуется четвертичная структура, в которую может входить до 24 молекул ферритина.
Презентация_Лекция_02_Белки.ppt