ORGAN_HIMIYa_LYeKTsIYa_2.pptx
- Количество слайдов: 22
 Лекция № 2 Изомерия органических соединений. Изомерия – это явление при которой, вещества имеют одинаковый количественный состав, молекулярную массу, но отличаются химическим строением или пространственным расположением атомов или групп атомов. Изомерия делится на два основных вида: 1) Структурную изомерию 2) Пространственную изомерию или стереометрию. Структурная изомерия включает в себя следующие виды изомерии: 1) изомерия углеродной цепи а) н-бутан б) изобутан
Лекция № 2 Изомерия органических соединений. Изомерия – это явление при которой, вещества имеют одинаковый количественный состав, молекулярную массу, но отличаются химическим строением или пространственным расположением атомов или групп атомов. Изомерия делится на два основных вида: 1) Структурную изомерию 2) Пространственную изомерию или стереометрию. Структурная изомерия включает в себя следующие виды изомерии: 1) изомерия углеродной цепи а) н-бутан б) изобутан
 2) Изомерия положения кратных связей а) пентен-1 СН 3 – СН 2 – СН = СН 2 б) пентен-2 СН 3 – СН 2 – СН = СН – СН 3 3) Изомерия положения функциональных групп. а) пропанол-1 СН 3 – СН 2 – ОН б)пропанол-2 СН 3 – СН 3 4) Межклассовая изомерия ОН При этом, одной и той же имперической формуле соответствуют представители разных классов органических соединений. С 2 Н 6 О а) диметиловый эфир H 3 С-О-СН 3 б) этанол СН 3 – СН 2 – ОН Пространственная или стереоизомерия, включает следующие виды изомерии: 1)Конформационная изомерия 2) Энантиомерия (оптическая изомерия) 3) Диастереомерия а) σ-диастереомерия б) π-диастереомерия
2) Изомерия положения кратных связей а) пентен-1 СН 3 – СН 2 – СН = СН 2 б) пентен-2 СН 3 – СН 2 – СН = СН – СН 3 3) Изомерия положения функциональных групп. а) пропанол-1 СН 3 – СН 2 – ОН б)пропанол-2 СН 3 – СН 3 4) Межклассовая изомерия ОН При этом, одной и той же имперической формуле соответствуют представители разных классов органических соединений. С 2 Н 6 О а) диметиловый эфир H 3 С-О-СН 3 б) этанол СН 3 – СН 2 – ОН Пространственная или стереоизомерия, включает следующие виды изомерии: 1)Конформационная изомерия 2) Энантиомерия (оптическая изомерия) 3) Диастереомерия а) σ-диастереомерия б) π-диастереомерия
 Этантиомерия(оптическая изомерия) возможна у любых органических соединений, содержащих ассиметрический атом углерода. Ассиметричесим – называется атом углерода, соединенный с четырьмя различными атомами или группами атомов. Пр: молочная кислота СООН Н-С-ОН СН 3 Молекулы веществ, содержащих ассиметричный атом углерода, называются хиральными, а сам ассиметричный атом углерода, находящийся в состоянии sp 3 -гибридизации, называется хиральным центром.
Этантиомерия(оптическая изомерия) возможна у любых органических соединений, содержащих ассиметрический атом углерода. Ассиметричесим – называется атом углерода, соединенный с четырьмя различными атомами или группами атомов. Пр: молочная кислота СООН Н-С-ОН СН 3 Молекулы веществ, содержащих ассиметричный атом углерода, называются хиральными, а сам ассиметричный атом углерода, находящийся в состоянии sp 3 -гибридизации, называется хиральным центром.
 Хиральные молекулы не содержат элементов симметрии и относятся между собой как предмет и несовместимое с ним зеркальное изображение. Этантиометрия – вид стереизомерии, при котором стереоизомеры называемые этантиомерами, относятся между собой, как предмет и несовместимое с ним зеркальное изображение. СООН НО Н СН 3 D(-) молочная L(+) молочная кислота Для обозначения внешней конфронтации энантиомеров вводится система D и L стереохимической номенклатуры.
Хиральные молекулы не содержат элементов симметрии и относятся между собой как предмет и несовместимое с ним зеркальное изображение. Этантиометрия – вид стереизомерии, при котором стереоизомеры называемые этантиомерами, относятся между собой, как предмет и несовместимое с ним зеркальное изображение. СООН НО Н СН 3 D(-) молочная L(+) молочная кислота Для обозначения внешней конфронтации энантиомеров вводится система D и L стереохимической номенклатуры.
 D – формула – это энантиомер, в котором заместитель, соединенный с хиральным центром, записывается справа по отношению к углеродной цепи, L – формула – слева Это характерно для энантиомеров с одним хиральным центром. Энантиомеры обладают оптической активностью. Они способны вращать плоскость поляризации света. Оптическая активность энантиомеров определяется на приборе – поляриметре, в котором луч света пройдя через специальную призму, колеблется только в данной плоскости и становится плоскополяризованным
D – формула – это энантиомер, в котором заместитель, соединенный с хиральным центром, записывается справа по отношению к углеродной цепи, L – формула – слева Это характерно для энантиомеров с одним хиральным центром. Энантиомеры обладают оптической активностью. Они способны вращать плоскость поляризации света. Оптическая активность энантиомеров определяется на приборе – поляриметре, в котором луч света пройдя через специальную призму, колеблется только в данной плоскости и становится плоскополяризованным
 Энантиомеры отклоняют такой луч либо в лево, либо в право. α α У энантиомеров угол вращения плоскости поляризации света но направления света противоположное. Один энантиомер левовращающий знак “-”, а другой правовращающий, знак “+” У молочной кислоты D(-), α= -2, 60 L(+), α= +2, 6 при 250 С в 2, 5 в водном растворе. Знак вращения плоскости поляризации не связан с принадлежностью к D или L ряду, он определяется экспериментально.
Энантиомеры отклоняют такой луч либо в лево, либо в право. α α У энантиомеров угол вращения плоскости поляризации света но направления света противоположное. Один энантиомер левовращающий знак “-”, а другой правовращающий, знак “+” У молочной кислоты D(-), α= -2, 60 L(+), α= +2, 6 при 250 С в 2, 5 в водном растворе. Знак вращения плоскости поляризации не связан с принадлежностью к D или L ряду, он определяется экспериментально.
 Энантиомеры сходны между собой но химически и физически свойствами, НО отличается по оптическим свойствам, они являются оптическими антиподами. Смесь разных количеств энантиомеров, называется рацелат, он не обладает оптической активностью. Многие биологически важные соединения содержат два и более центра хиральности. Количество стереоизомеров для них рассчитывается по формуле: α = 2 n , где n число хиральных центров. Пример: CH 2 OH-CHOH-C=О n=2 ; Z=22=4 Н 2, 3, 4 -тригидрооксибутаналь
Энантиомеры сходны между собой но химически и физически свойствами, НО отличается по оптическим свойствам, они являются оптическими антиподами. Смесь разных количеств энантиомеров, называется рацелат, он не обладает оптической активностью. Многие биологически важные соединения содержат два и более центра хиральности. Количество стереоизомеров для них рассчитывается по формуле: α = 2 n , где n число хиральных центров. Пример: CH 2 OH-CHOH-C=О n=2 ; Z=22=4 Н 2, 3, 4 -тригидрооксибутаналь
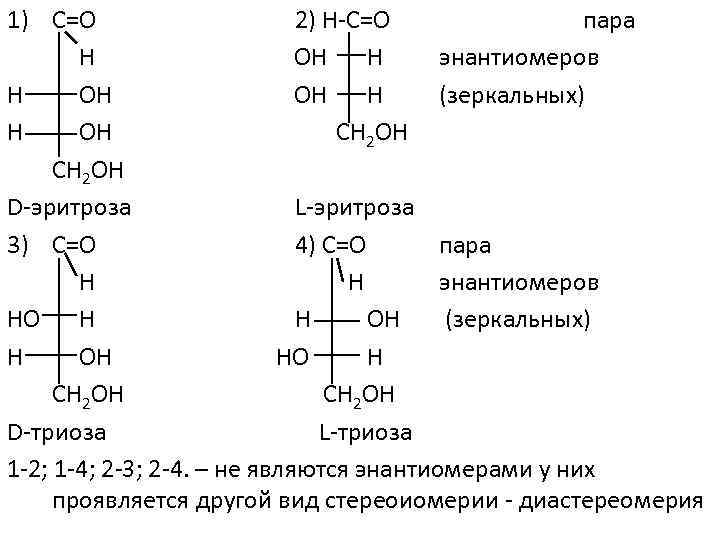 1) C=O 2) Н-C=О пара H OH H энантиомеров H OH OH H (зеркальных) H OH CH 2 OH D-эритроза L-эритроза 3) C=O 4) C=O пара H H энантиомеров НО H H OH (зеркальных) H OH HO H CH 2 OH D-триоза L-триоза 1 -2; 1 -4; 2 -3; 2 -4. – не являются энантиомерами у них проявляется другой вид стереоиомерии - диастереомерия
1) C=O 2) Н-C=О пара H OH H энантиомеров H OH OH H (зеркальных) H OH CH 2 OH D-эритроза L-эритроза 3) C=O 4) C=O пара H H энантиомеров НО H H OH (зеркальных) H OH HO H CH 2 OH D-триоза L-триоза 1 -2; 1 -4; 2 -3; 2 -4. – не являются энантиомерами у них проявляется другой вид стереоиомерии - диастереомерия
 Диастериомеры – это стереоизомеры, которые не являются энантиомерами. У выше перечисленных пар стереоизомеров веществ проявляется в виде σ – стереоизомерии, т. к заместители связаны с хиральными центрами σ – связями. Стереоизомеры, у которых заместители соединены с хиральными центрами, располагающимися по одну сторону от углеродной цепи, называются эритроформа, а по разные стороны – троеформа. Пр. : пара σ – диастереомеров С=O С=О H H HO H H OH CH 2 OH Эритроформа трео – форма
Диастериомеры – это стереоизомеры, которые не являются энантиомерами. У выше перечисленных пар стереоизомеров веществ проявляется в виде σ – стереоизомерии, т. к заместители связаны с хиральными центрами σ – связями. Стереоизомеры, у которых заместители соединены с хиральными центрами, располагающимися по одну сторону от углеродной цепи, называются эритроформа, а по разные стороны – троеформа. Пр. : пара σ – диастереомеров С=O С=О H H HO H H OH CH 2 OH Эритроформа трео – форма
 У σ – диастереомеров конформация (1)одного хирального центра одинакова, а(2) вторая – противоположна. Понятие диастериомерия и σ – диастериомерии взаимно исключается, если пара стериомеров является эномтиомерами, то они не будут σ – диастериамерами и наоборот. π – диастериамерия – это вид стериоидиомерии, при котором стериоизомеры отличаются друг от друга пространственным расположением одинаковых заместителей относительно плоскости π – связи. Пр. : бутадиенова кислота O=C-CH=CH-C=O HO OH
У σ – диастереомеров конформация (1)одного хирального центра одинакова, а(2) вторая – противоположна. Понятие диастериомерия и σ – диастериомерии взаимно исключается, если пара стериомеров является эномтиомерами, то они не будут σ – диастериамерами и наоборот. π – диастериамерия – это вид стериоидиомерии, при котором стериоизомеры отличаются друг от друга пространственным расположением одинаковых заместителей относительно плоскости π – связи. Пр. : бутадиенова кислота O=C-CH=CH-C=O HO OH
 H-C-COOH малеиновая кислота цис – π – диастериомер Н-С-СООН фумаровая кислота НООС-С-С транс – π – диастериомер Транс π – диастериомеры более стабильны, поэтому более распространены в природе в частности фумаровая кислота в организме является промежуточным продуктом обмена углеводов в анаэробных условиях.
H-C-COOH малеиновая кислота цис – π – диастериомер Н-С-СООН фумаровая кислота НООС-С-С транс – π – диастериомер Транс π – диастериомеры более стабильны, поэтому более распространены в природе в частности фумаровая кислота в организме является промежуточным продуктом обмена углеводов в анаэробных условиях.
 Кислотные свойства органических соединений. Большинство органических соединений можно рассматривать как кислоты, т. к в их молекулах имеются связи атомов водорода с атомами: С, О, N, S. Органические кислоты классифицируют по кислотным центрам на: С-Н; О-Н; N-H; S-H, кислоты Кислотный центр – это элемент и связанный с ним атом водорода. На кислотные свойства органических соединений оказывает влияние стабильность аниона, образующегося при отщеплении протона H+. НА= H++ АЧем стабильней анион тем сильнее кислота.
Кислотные свойства органических соединений. Большинство органических соединений можно рассматривать как кислоты, т. к в их молекулах имеются связи атомов водорода с атомами: С, О, N, S. Органические кислоты классифицируют по кислотным центрам на: С-Н; О-Н; N-H; S-H, кислоты Кислотный центр – это элемент и связанный с ним атом водорода. На кислотные свойства органических соединений оказывает влияние стабильность аниона, образующегося при отщеплении протона H+. НА= H++ АЧем стабильней анион тем сильнее кислота.
 На стабильность аниона оказывает влияние следующие факторы: 1) Электроотрицательность элемента в кислотном центре Пр. : СН 3 -СН 2 -ОН Этанол Pka =18 СН 3 -СН 2 -HNH этанамин Pka =30 Чем ниже показатель константы кислотности, тем сильнее кислота. Как видно из величины Pka этанол проявляет более выраженные кислотные свойства по сравнению с этанамином т. к образующиеся при отщеплении протона от этанола, алкоксидион СН 3 -СН 2 -О- будет обладать более высокой стабильностью, по сравнению с алкиламидионом СН 3 -СН 2 -HN- , т. к в алкоксидионе более Э. О.
На стабильность аниона оказывает влияние следующие факторы: 1) Электроотрицательность элемента в кислотном центре Пр. : СН 3 -СН 2 -ОН Этанол Pka =18 СН 3 -СН 2 -HNH этанамин Pka =30 Чем ниже показатель константы кислотности, тем сильнее кислота. Как видно из величины Pka этанол проявляет более выраженные кислотные свойства по сравнению с этанамином т. к образующиеся при отщеплении протона от этанола, алкоксидион СН 3 -СН 2 -О- будет обладать более высокой стабильностью, по сравнению с алкиламидионом СН 3 -СН 2 -HN- , т. к в алкоксидионе более Э. О.
 Кислород способен в гораздо большей степени нести отрицательный заряд по сравнению с атомами азота, в алкиламидионе СН 3 -СН 2 -HN-. 2) Поляризуемость элемента в кислотном центре СН 3 -СН 2 -ОН СН 3 -СН 2 -SH Этанол этантиол Pka =18 Pka =10, 5
Кислород способен в гораздо большей степени нести отрицательный заряд по сравнению с атомами азота, в алкиламидионе СН 3 -СН 2 -HN-. 2) Поляризуемость элемента в кислотном центре СН 3 -СН 2 -ОН СН 3 -СН 2 -SH Этанол этантиол Pka =18 Pka =10, 5
 Как видно из величины Pka этантиол проявляет более выраженные кислотные свойства по сравнению с этанолом, т. к. в данном случае преобладает не Э. О. , а фактор поляризуемости, поскольку элементы кислотных центров О и S, находятся в разных периодах. Поляризуемость атома – это мера смещения, рассредоточения электронного облака атома, под действием внешнего электрического поля. Поляризуемость атома возрастает с увеличением числа электронов и энергетических уровней. Атом серы более поляризуем по сравнению с атомом кислорода т. к. в атоме серы имеется
Как видно из величины Pka этантиол проявляет более выраженные кислотные свойства по сравнению с этанолом, т. к. в данном случае преобладает не Э. О. , а фактор поляризуемости, поскольку элементы кислотных центров О и S, находятся в разных периодах. Поляризуемость атома – это мера смещения, рассредоточения электронного облака атома, под действием внешнего электрического поля. Поляризуемость атома возрастает с увеличением числа электронов и энергетических уровней. Атом серы более поляризуем по сравнению с атомом кислорода т. к. в атоме серы имеется
 три энергетических уровня, а в атоме кислорода – два. Образующиеся при отщеплении протона, меркоксид ионы CH 3 - CH 2 - S- будут обладать более высокой стабильностью, по сравнению с алкоксид ионами CH 3 CH 2 - O-, т. к. в связи более высокой полярностью атома серы, отрицательный заряд в меркоктидионе будет делокализован гораздо в большем объеме. II. Стабилизация иона за счет сопряжения. CH 3 - CH 2 – OH C 6 H 5 – OH Этанол Фенол Pka = 18 Pka = 9, 9
три энергетических уровня, а в атоме кислорода – два. Образующиеся при отщеплении протона, меркоксид ионы CH 3 - CH 2 - S- будут обладать более высокой стабильностью, по сравнению с алкоксид ионами CH 3 CH 2 - O-, т. к. в связи более высокой полярностью атома серы, отрицательный заряд в меркоктидионе будет делокализован гораздо в большем объеме. II. Стабилизация иона за счет сопряжения. CH 3 - CH 2 – OH C 6 H 5 – OH Этанол Фенол Pka = 18 Pka = 9, 9
 Как видно из величины Pka фенол проявляет более выраженные кислотные свойста, по сравнению с этанолом. Для объяснения этого факта рассмторим влияние электронных эффектов заместителей в молекулах данных соединений. σ+ σ+ σ– CH 3 - CH 2 – OH - ОН (- I, Э. А. ). В молекуле этанола, под влиянием Э. А. заместителя ОН – группы, электронная плотность смещена к заместителю и повышена на атоме О. Образующийся алкоксидион CH 3 - CH 2 - O- будет обладать низкой стабильностью, т. к. отрицательный заряд в этом атоме практически не делокализован по всему объему,
Как видно из величины Pka фенол проявляет более выраженные кислотные свойста, по сравнению с этанолом. Для объяснения этого факта рассмторим влияние электронных эффектов заместителей в молекулах данных соединений. σ+ σ+ σ– CH 3 - CH 2 – OH - ОН (- I, Э. А. ). В молекуле этанола, под влиянием Э. А. заместителя ОН – группы, электронная плотность смещена к заместителю и повышена на атоме О. Образующийся алкоксидион CH 3 - CH 2 - O- будет обладать низкой стабильностью, т. к. отрицательный заряд в этом атоме практически не делокализован по всему объему,
 а сосредоточен на атоме кислорода, поэтому этанол проявляет слабовыраженные кислотные свойства. Например: фенол - ОН (- I, + M, σ– σ– + M>> - I >> Э. Д. ). σ– Молекула фенола является сопряженной системой, электронная плотность смещена от заместителя и делокализована по ароматическому кольцу. Образующийся при отщеплении протона от фенола феноксид ион C 6 H 5 - O- ,
а сосредоточен на атоме кислорода, поэтому этанол проявляет слабовыраженные кислотные свойства. Например: фенол - ОН (- I, + M, σ– σ– + M>> - I >> Э. Д. ). σ– Молекула фенола является сопряженной системой, электронная плотность смещена от заместителя и делокализована по ароматическому кольцу. Образующийся при отщеплении протона от фенола феноксид ион C 6 H 5 - O- ,
 являясь сопряженной системой, будет обладать более высокой стабильностью, по сравнению с алкоксидионом CH 3 - CH 2 - O- , который не является сопряженной системой. А следовательно образование сопряженной системы способствует делокализации отрицательного заряда в атоме, что повышает его способность и усиливает кислотные свойства веществ. III. Влияние радикала на стабильность аниона. При одинаковых кислотных центрах, появление в радикале электронноакцепторных заместителей (Э. А. ) спосбствует делокализации отрицательного заряда в анионе, что повышает его стабильность и усиливает кислотные свойства веществ.
являясь сопряженной системой, будет обладать более высокой стабильностью, по сравнению с алкоксидионом CH 3 - CH 2 - O- , который не является сопряженной системой. А следовательно образование сопряженной системы способствует делокализации отрицательного заряда в атоме, что повышает его способность и усиливает кислотные свойства веществ. III. Влияние радикала на стабильность аниона. При одинаковых кислотных центрах, появление в радикале электронноакцепторных заместителей (Э. А. ) спосбствует делокализации отрицательного заряда в анионе, что повышает его стабильность и усиливает кислотные свойства веществ.
 Сравним кислотные свойства этих веществ. Пропановая кислота CH 3 - CH 2 – СООН Pka = 4, 90 Молочная кислота CH 3 - CH – СООН ОН Pka = 3, 83 Как видно из величин Pk молочная кислота является более сильной кислотой, по сравнению с пропионовой кислотой т. к. наличие в радикале этой кислоты ЭА заместителя, - ОН группы способствует делокализации отрицательного заряда в лактат анионе.
Сравним кислотные свойства этих веществ. Пропановая кислота CH 3 - CH 2 – СООН Pka = 4, 90 Молочная кислота CH 3 - CH – СООН ОН Pka = 3, 83 Как видно из величин Pk молочная кислота является более сильной кислотой, по сравнению с пропионовой кислотой т. к. наличие в радикале этой кислоты ЭА заместителя, - ОН группы способствует делокализации отрицательного заряда в лактат анионе.
 CH 3 - CH – С О - , ОН О что способствует повышению его стабильности и усилению кислотных свойств, по сравнению с анионом CH 3 - CH 2 - СОO- , радикал которого не содержит такого заместителя. IV. Влияниерастворителя на стабильность аниона. (Сальватационные эффекты). В водных растворах анионы гидратированы, они окружены водными или гидратными оболочками, что повышает их стабильность и усиливает кислотные свойства веществ.
CH 3 - CH – С О - , ОН О что способствует повышению его стабильности и усилению кислотных свойств, по сравнению с анионом CH 3 - CH 2 - СОO- , радикал которого не содержит такого заместителя. IV. Влияниерастворителя на стабильность аниона. (Сальватационные эффекты). В водных растворах анионы гидратированы, они окружены водными или гидратными оболочками, что повышает их стабильность и усиливает кислотные свойства веществ.
 Чем меньше радиус аниона, тем он больше гидротирован, и стабилен, а следовательно, будут выше кислотные свойства соответствующего органического соединения. Например: Муравьиная к-та Уксусная к-та Пропиановая к-та НСООН CH 3 - CH 2 СООН Pka = 3, 70 Pka = 4, 76 Pka = 4, 90 Как видно из величин Pk в этом ряду кислот, наиболее сильной, является муравьиная кислота, т. к. образующийся при диссоциации этой кислоты формиат ион НСОO- имеет малые размеры и будет наиболее гидротирован, по сравнению с ацетанионом CH 3 СОO- и пропионатом CH 3 - CH 2 СОO-.
Чем меньше радиус аниона, тем он больше гидротирован, и стабилен, а следовательно, будут выше кислотные свойства соответствующего органического соединения. Например: Муравьиная к-та Уксусная к-та Пропиановая к-та НСООН CH 3 - CH 2 СООН Pka = 3, 70 Pka = 4, 76 Pka = 4, 90 Как видно из величин Pk в этом ряду кислот, наиболее сильной, является муравьиная кислота, т. к. образующийся при диссоциации этой кислоты формиат ион НСОO- имеет малые размеры и будет наиболее гидротирован, по сравнению с ацетанионом CH 3 СОO- и пропионатом CH 3 - CH 2 СОO-.


