Лекция 2. Гетерогенные реакции в растворах электролитов Растворимость




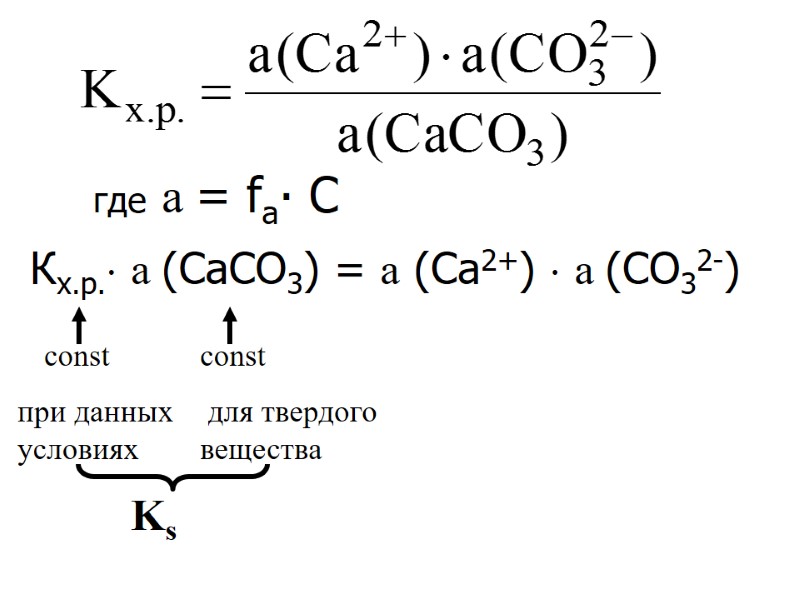










![[ Ag (NH3)2] внутренняя сфера внешняя сфера комплексообразователь лиганды (от лат. ligare – связывать, [ Ag (NH3)2] внутренняя сфера внешняя сфера комплексообразователь лиганды (от лат. ligare – связывать,](https://present5.com/presentacii-2/20171208\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy_20.jpg)








![Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2](https://present5.com/presentacii-2/20171208\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy_39.jpg)
![Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4](https://present5.com/presentacii-2/20171208\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy_40.jpg)
21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt
- Количество слайдов: 40
 Лекция 2. Гетерогенные реакции в растворах электролитов
Лекция 2. Гетерогенные реакции в растворах электролитов
 Растворимость – свойство вещества растворяться в воде или другом растворителе. Выражается константой растворимости (Ks), который показывает, какая масса вещества может раствориться в 100 г растворителя при данной температуре. Мерой растворимости (S) вещества при данных условиях является его содержание в насыщенном растворе.
Растворимость – свойство вещества растворяться в воде или другом растворителе. Выражается константой растворимости (Ks), который показывает, какая масса вещества может раствориться в 100 г растворителя при данной температуре. Мерой растворимости (S) вещества при данных условиях является его содержание в насыщенном растворе.
 СаСО3 Са2+ + СО32- При равновесии: Vраств. = Vосажд. растворение осаждение тв. фаза жидкая фаза Константа растворимости (Кs)
СаСО3 Са2+ + СО32- При равновесии: Vраств. = Vосажд. растворение осаждение тв. фаза жидкая фаза Константа растворимости (Кs)
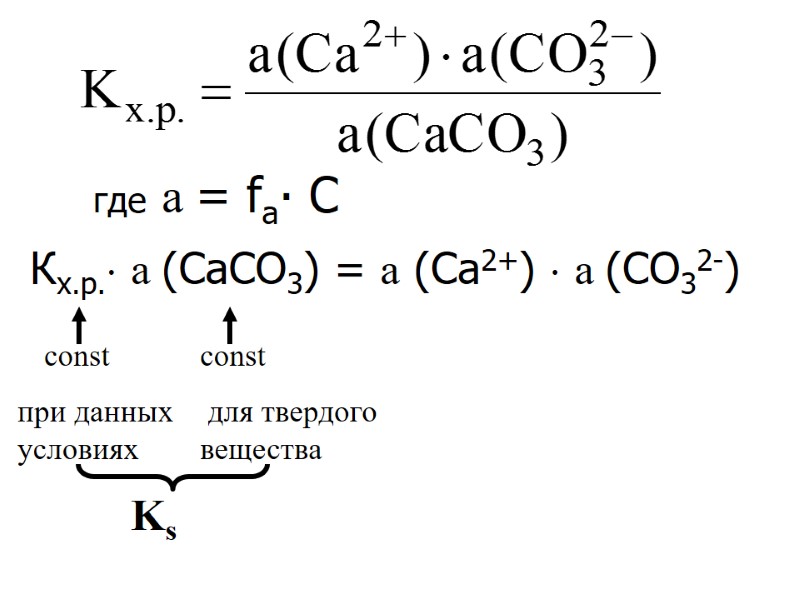 где а = fа∙ С Кх.р. а (CaСО3) = а (Са2+) а (СО32-) Ks соnst при данных условиях const для твердого вещества
где а = fа∙ С Кх.р. а (CaСО3) = а (Са2+) а (СО32-) Ks соnst при данных условиях const для твердого вещества
 Ks = а (Са2+) ∙ а (СО32-) Ks - константа растворимости Ks или ПР (произведение растворимости), справочные величины для разбавленных растворов fa→1 и а → С Ks = С(Са2+) ∙ С(СО32-) или Ks = [Са2+] ∙ [СО32-]
Ks = а (Са2+) ∙ а (СО32-) Ks - константа растворимости Ks или ПР (произведение растворимости), справочные величины для разбавленных растворов fa→1 и а → С Ks = С(Са2+) ∙ С(СО32-) или Ks = [Са2+] ∙ [СО32-]
 Ks = Cх(М+) ∙ Cy(А‾) Ks = C3 (Ca2+) ∙ C2 (PO43-) Например, Ca3(PO4)2 3Ca2+ + 2PO43- Для электролитов состава МхАy
Ks = Cх(М+) ∙ Cy(А‾) Ks = C3 (Ca2+) ∙ C2 (PO43-) Например, Ca3(PO4)2 3Ca2+ + 2PO43- Для электролитов состава МхАy
 Зная Ks можно рассчитать равновесную концентрацию вещества в насыщенном растворе, т.е. растворимость (S) общий вид для электролита типа AmBn mA n+ + nB m‾ Пример: Ca3(PO4)2 3Са 2+ + 2РО43-
Зная Ks можно рассчитать равновесную концентрацию вещества в насыщенном растворе, т.е. растворимость (S) общий вид для электролита типа AmBn mA n+ + nB m‾ Пример: Ca3(PO4)2 3Са 2+ + 2РО43-
 Условия образования и растворения осадков
Условия образования и растворения осадков
 CaSO4 Ca2+ + SO42‾ 1) В равновесии Vраств.=Vосажд С (Ca2+) ∙ С (SO42-) = Ks растворение осаждение 2) Увеличение [С] ионов => равновесие, т.е. выпадает осадок. С (Ca2+) ∙ С (SO42-) > Ks 3) С (Ca2+) ∙ С (SO42-) < Ks - условие растворения осадка - условие образования осадка ↓
CaSO4 Ca2+ + SO42‾ 1) В равновесии Vраств.=Vосажд С (Ca2+) ∙ С (SO42-) = Ks растворение осаждение 2) Увеличение [С] ионов => равновесие, т.е. выпадает осадок. С (Ca2+) ∙ С (SO42-) > Ks 3) С (Ca2+) ∙ С (SO42-) < Ks - условие растворения осадка - условие образования осадка ↓
 Конкурирующие гетерогенные равновесия
Конкурирующие гетерогенные равновесия
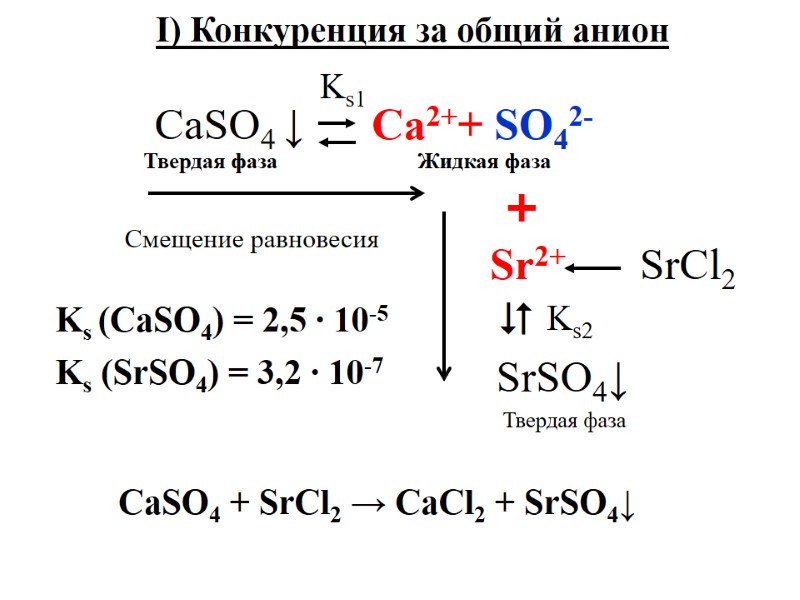
 Ks (CaSO4) = 2,5 ∙ 10-5 Ks (SrSO4) = 3,2 ∙ 10-7 I) Конкуренция за общий анион CaSO4 + SrCl2 → CaCl2 + SrSO4↓
Ks (CaSO4) = 2,5 ∙ 10-5 Ks (SrSO4) = 3,2 ∙ 10-7 I) Конкуренция за общий анион CaSO4 + SrCl2 → CaCl2 + SrSO4↓
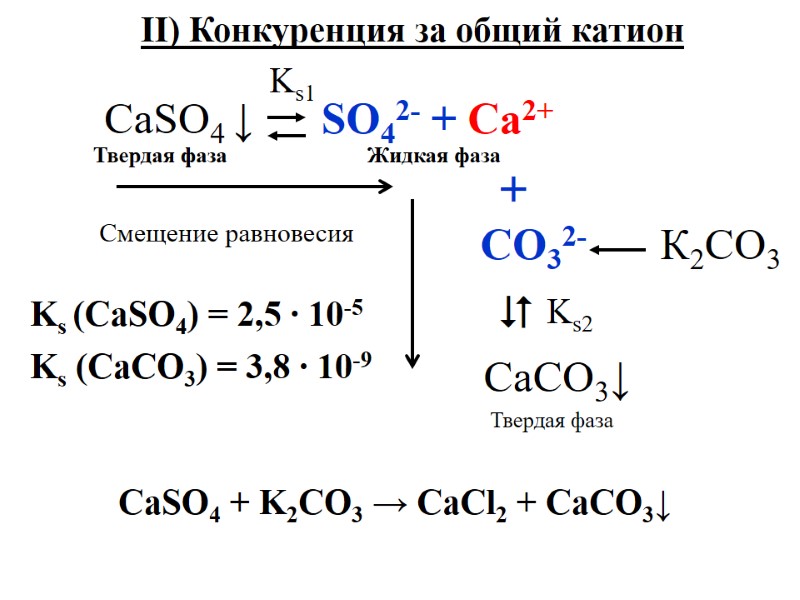
 Ks (CaSO4) = 2,5 ∙ 10-5 Ks (CaCO3) = 3,8 ∙ 10-9 II) Конкуренция за общий катион Смещение равновесия + CО32- К2CO3 CaSO4 + K2CO3 → CaCl2 + CaCO3↓
Ks (CaSO4) = 2,5 ∙ 10-5 Ks (CaCO3) = 3,8 ∙ 10-9 II) Конкуренция за общий катион Смещение равновесия + CО32- К2CO3 CaSO4 + K2CO3 → CaCl2 + CaCO3↓
 Гетерогенные процессы в живых организмах Далее происходит депротонирование Жидкая фаза – кровь Са2+, НРО42-, Н2РО4-, ОН- , НСО3-, лактаты, белки 2Са2++ 3СаНРО4 + 4ОН- Ca5(PO4)3ОН + 3H2O Ks (Ca(Н2РO4)2 = 1,0 ∙ 10-3 Ks (CaНРO4) = 2,7 ∙ 10-7 Са2+ + НРО42- → СаНРО4 гидроксиапатит Кs = 1,6 ∙ 10-58 рН крови (7,4)
Гетерогенные процессы в живых организмах Далее происходит депротонирование Жидкая фаза – кровь Са2+, НРО42-, Н2РО4-, ОН- , НСО3-, лактаты, белки 2Са2++ 3СаНРО4 + 4ОН- Ca5(PO4)3ОН + 3H2O Ks (Ca(Н2РO4)2 = 1,0 ∙ 10-3 Ks (CaНРO4) = 2,7 ∙ 10-7 Са2+ + НРО42- → СаНРО4 гидроксиапатит Кs = 1,6 ∙ 10-58 рН крови (7,4)
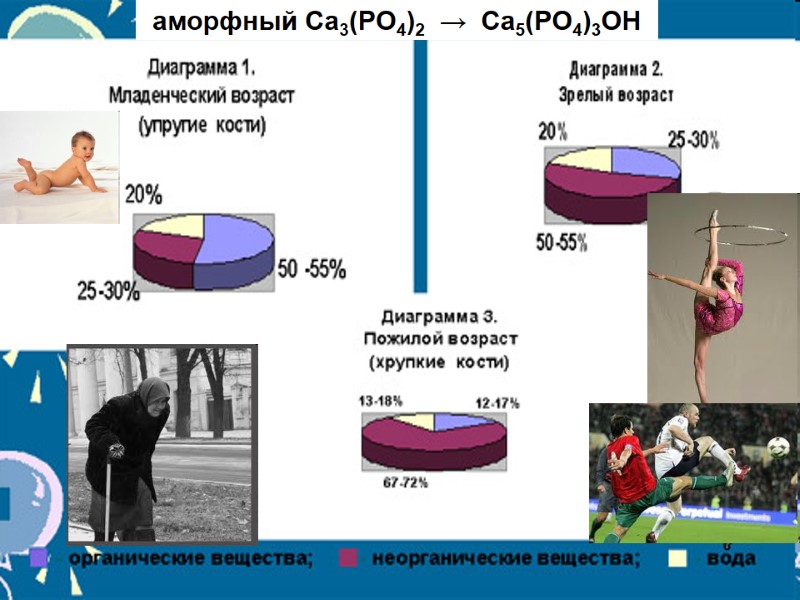
 аморфный Ca3(PO4)2 → Ca5(PO4)3OH
аморфный Ca3(PO4)2 → Ca5(PO4)3OH

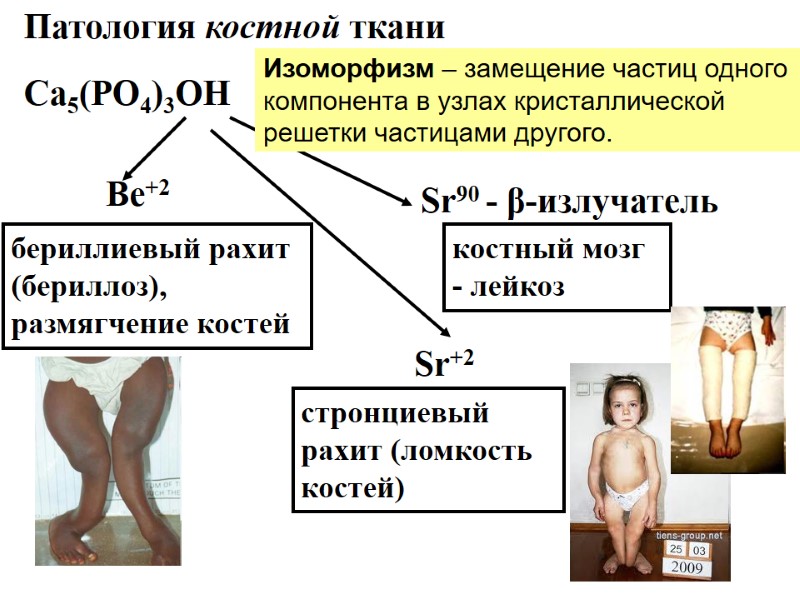
 Патология костной ткани Са5(РО4)3ОН Ве+2 Sr+2 Sr90 - β-излучатель бериллиевый рахит (бериллоз), размягчение костей стронциевый рахит (ломкость костей) костный мозг - лейкоз Изоморфизм – замещение частиц одного компонента в узлах кристаллической решетки частицами другого.
Патология костной ткани Са5(РО4)3ОН Ве+2 Sr+2 Sr90 - β-излучатель бериллиевый рахит (бериллоз), размягчение костей стронциевый рахит (ломкость костей) костный мозг - лейкоз Изоморфизм – замещение частиц одного компонента в узлах кристаллической решетки частицами другого.
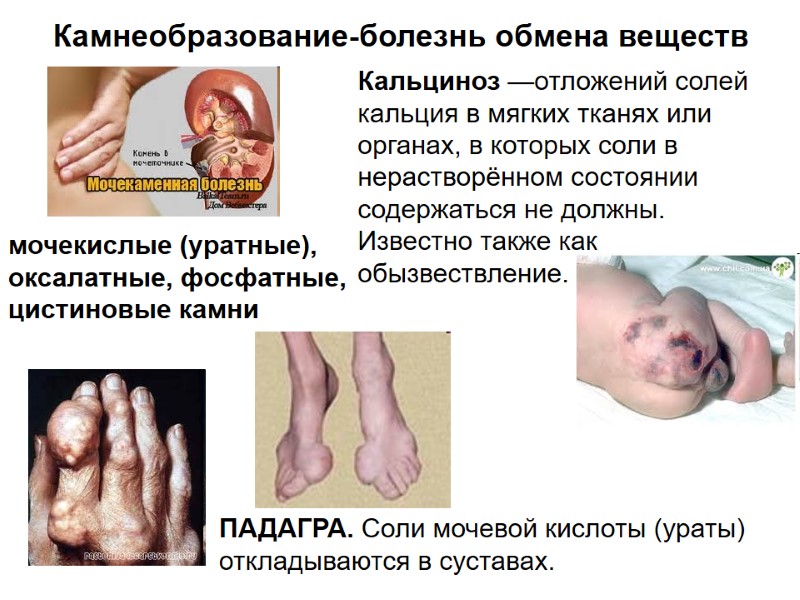
 Камнеобразование-болезнь обмена веществ ПАДАГРА. Соли мочевой кислоты (ураты) откладываются в суставах. мочекислые (уратные), оксалатные, фосфатные, цистиновые камни Кальциноз —отложений солей кальция в мягких тканях или органах, в которых соли в нерастворённом состоянии содержаться не должны. Известно также как обызвествление.
Камнеобразование-болезнь обмена веществ ПАДАГРА. Соли мочевой кислоты (ураты) откладываются в суставах. мочекислые (уратные), оксалатные, фосфатные, цистиновые камни Кальциноз —отложений солей кальция в мягких тканях или органах, в которых соли в нерастворённом состоянии содержаться не должны. Известно также как обызвествление.
 Лигандообменные равновесия и процессы
Лигандообменные равновесия и процессы
 Координационная теория, предложенная в 1893 году А. Вернером и дополненная Л.А.Чугаевым. Лев Александрович Чугаев (1873-1922) Альфред Вернер (1866-1919)
Координационная теория, предложенная в 1893 году А. Вернером и дополненная Л.А.Чугаевым. Лев Александрович Чугаев (1873-1922) Альфред Вернер (1866-1919)
![>[ Ag (NH3)2] внутренняя сфера внешняя сфера комплексообразователь лиганды (от лат. ligare – связывать, >[ Ag (NH3)2] внутренняя сфера внешняя сфера комплексообразователь лиганды (от лат. ligare – связывать,](https://present5.com/presentacii-2/20171208\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy_20.jpg) [ Ag (NH3)2] внутренняя сфера внешняя сфера комплексообразователь лиганды (от лат. ligare – связывать, соединять) Комплексные соединения – устойчивые химические соединения сложного состава, в которых хотя бы одна связь, образована по донорно-акцепторному механизму. Cl координационное число
[ Ag (NH3)2] внутренняя сфера внешняя сфера комплексообразователь лиганды (от лат. ligare – связывать, соединять) Комплексные соединения – устойчивые химические соединения сложного состава, в которых хотя бы одна связь, образована по донорно-акцепторному механизму. Cl координационное число

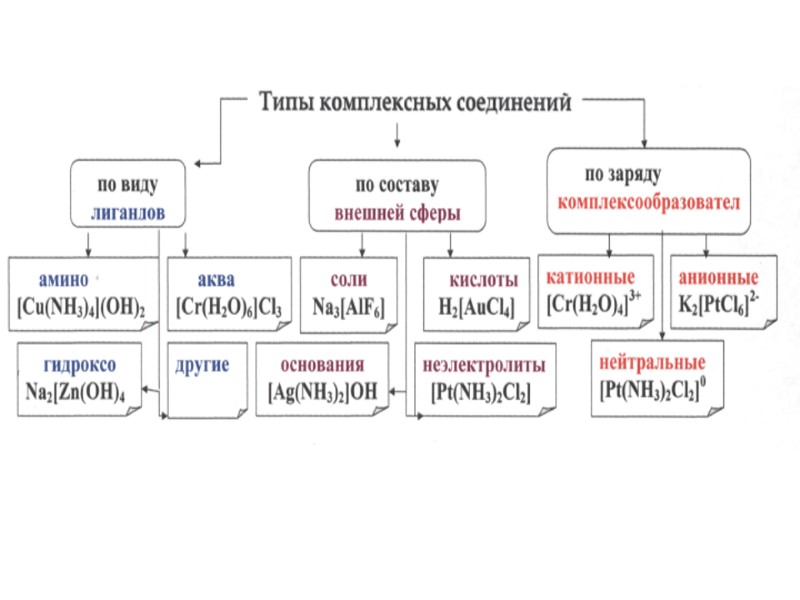
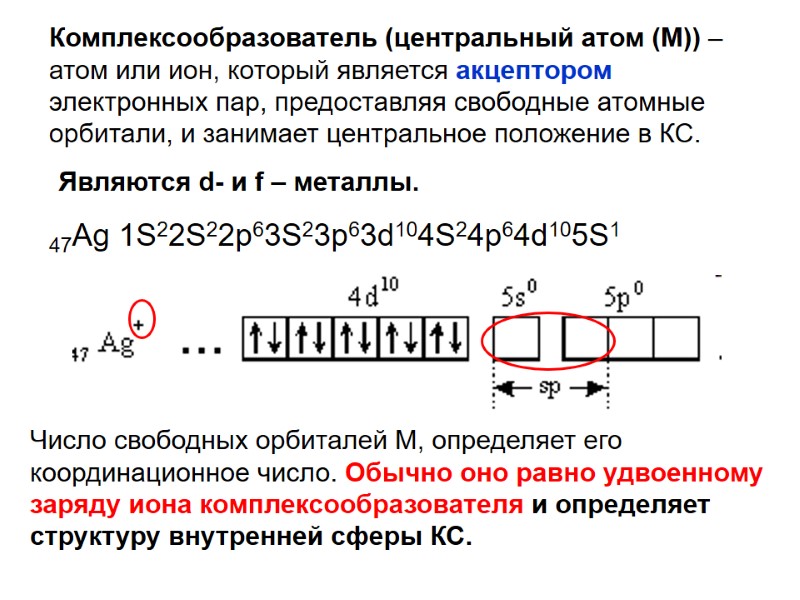
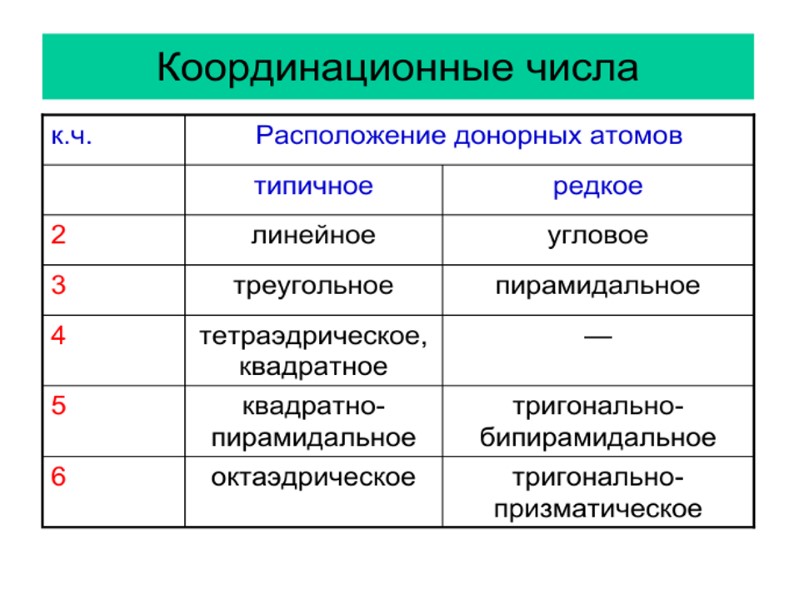
 Комплексообразователь (центральный атом (М)) – атом или ион, который является акцептором электронных пар, предоставляя свободные атомные орбитали, и занимает центральное положение в КС. 47Ag 1S22S22p63S23p63d104S24p64d105S1 Являются d- и f – металлы. Число свободных орбиталей М, определяет его координационное число. Обычно оно равно удвоенному заряду иона комплексообразователя и определяет структуру внутренней сферы КС.
Комплексообразователь (центральный атом (М)) – атом или ион, который является акцептором электронных пар, предоставляя свободные атомные орбитали, и занимает центральное положение в КС. 47Ag 1S22S22p63S23p63d104S24p64d105S1 Являются d- и f – металлы. Число свободных орбиталей М, определяет его координационное число. Обычно оно равно удвоенному заряду иона комплексообразователя и определяет структуру внутренней сферы КС.

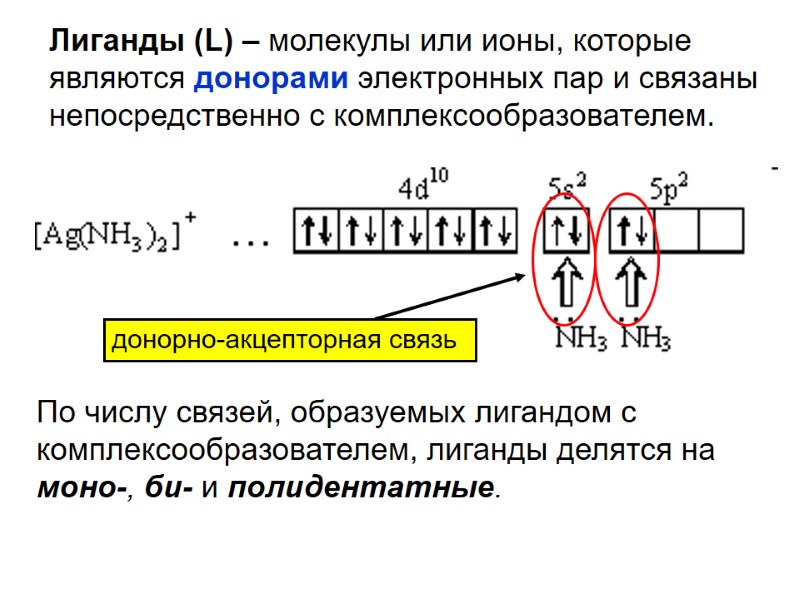
 Лиганды (L) – молекулы или ионы, которые являются донорами электронных пар и связаны непосредственно с комплексообразователем. По числу связей, образуемых лигандом с комплексообразователем, лиганды делятся на моно-, би- и полидентатные. донорно-акцепторная связь
Лиганды (L) – молекулы или ионы, которые являются донорами электронных пар и связаны непосредственно с комплексообразователем. По числу связей, образуемых лигандом с комплексообразователем, лиганды делятся на моно-, би- и полидентатные. донорно-акцепторная связь
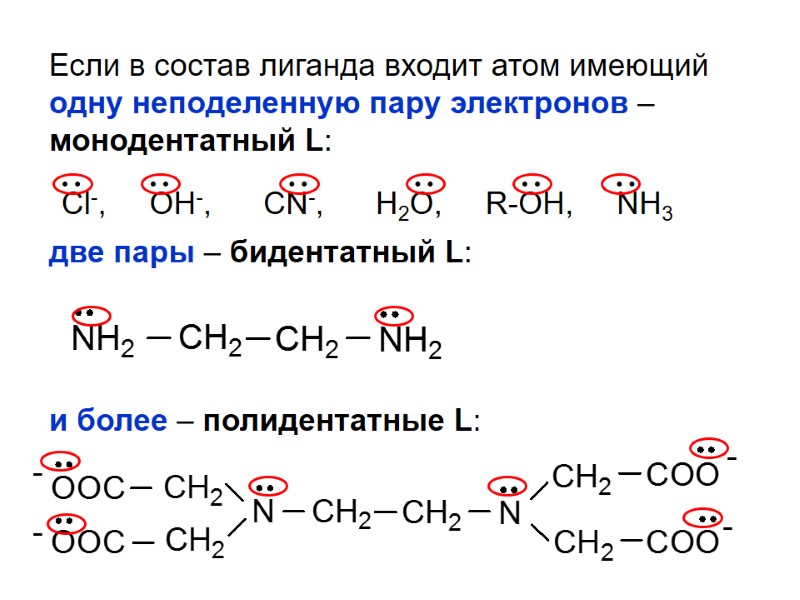
 Если в состав лиганда входит атом имеющий одну неподеленную пару электронов – монодентатный L: две пары – бидентатный L: и более – полидентатные L: Cl-, OH-, CN-, H2O, R-OH, NH3 • • • • • • • • • • • •
Если в состав лиганда входит атом имеющий одну неподеленную пару электронов – монодентатный L: две пары – бидентатный L: и более – полидентатные L: Cl-, OH-, CN-, H2O, R-OH, NH3 • • • • • • • • • • • •
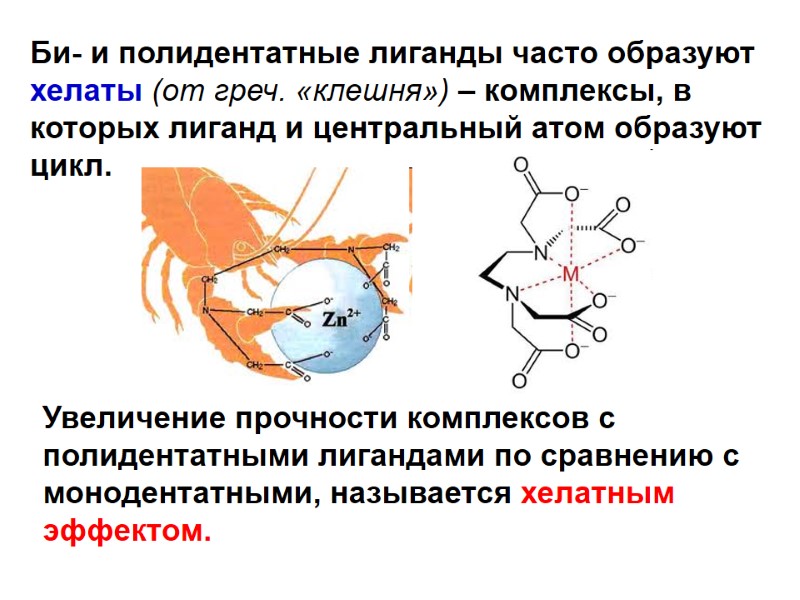
 Би- и полидентатные лиганды часто образуют хелаты (от греч. «клешня») – комплексы, в которых лиганд и центральный атом образуют цикл. Увеличение прочности комплексов с полидентатными лигандами по сравнению с монодентатными, называется хелатным эффектом.
Би- и полидентатные лиганды часто образуют хелаты (от греч. «клешня») – комплексы, в которых лиганд и центральный атом образуют цикл. Увеличение прочности комплексов с полидентатными лигандами по сравнению с монодентатными, называется хелатным эффектом.
 Эффективность донорно-акцепторного взаимодействия L и M (прочность связи) определяется их поляризуемостью. Чем меньше радиус и число электронов у частицы, тем менее поляризуема («жесткие»), наоборот – «мягкие».
Эффективность донорно-акцепторного взаимодействия L и M (прочность связи) определяется их поляризуемостью. Чем меньше радиус и число электронов у частицы, тем менее поляризуема («жесткие»), наоборот – «мягкие».
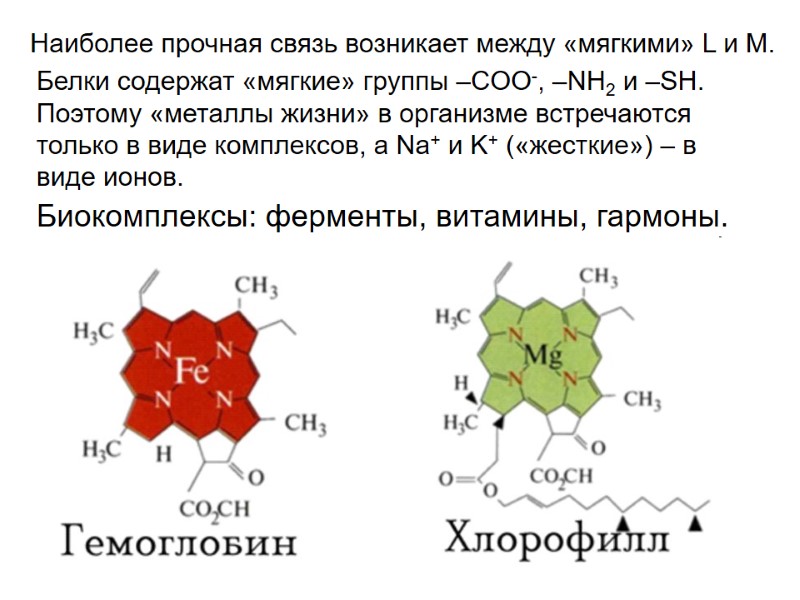
 Наиболее прочная связь возникает между «мягкими» L и M. Белки содержат «мягкие» группы –COO-, –NH2 и –SH. Поэтому «металлы жизни» в организме встречаются только в виде комплексов, а Na+ и K+ («жесткие») – в виде ионов. Биокомплексы: ферменты, витамины, гармоны.
Наиболее прочная связь возникает между «мягкими» L и M. Белки содержат «мягкие» группы –COO-, –NH2 и –SH. Поэтому «металлы жизни» в организме встречаются только в виде комплексов, а Na+ и K+ («жесткие») – в виде ионов. Биокомплексы: ферменты, витамины, гармоны.
 Очень «мягкие»: Cd2+, Pb2+, Hg2+, сильно токсичны, т.к. образуют прочные комплексы с белком (особенно содержащие группу – SH), нарушая обмен веществ, вызывая появление опухолей, мутагенез. Тиоловые яды
Очень «мягкие»: Cd2+, Pb2+, Hg2+, сильно токсичны, т.к. образуют прочные комплексы с белком (особенно содержащие группу – SH), нарушая обмен веществ, вызывая появление опухолей, мутагенез. Тиоловые яды
 Детоксикацию организма от металлов токсикантов проводят при помощи лиганд-препаратов на основе полидентатных L – хелатотератия. Принципы хелатотерапии: 1) детоксикант (антидот) должен эффективно связывать ионы-токсиканты; образующееся соединение должно быть прочнее, чем те, которые существовали в организме; 2) антидот не должен разрушать жизненно необходимые КС; соединение детоксиканта с биометаллами должно быть менее прочным, чем существующее в организме.
Детоксикацию организма от металлов токсикантов проводят при помощи лиганд-препаратов на основе полидентатных L – хелатотератия. Принципы хелатотерапии: 1) детоксикант (антидот) должен эффективно связывать ионы-токсиканты; образующееся соединение должно быть прочнее, чем те, которые существовали в организме; 2) антидот не должен разрушать жизненно необходимые КС; соединение детоксиканта с биометаллами должно быть менее прочным, чем существующее в организме.
 Диссоциация комплексных соединений Первичная диссоциация комплексных соединений - это распад КС в растворе на ионы внешней и внутренней сфер подобно cильным электролитам, так как эти ионы связаны ионными (электростатическими) силами. Вторичная диссоциация комплексного соединения – это распад внутренней сферы на составляющие ее компоненты. Этот процесс протекает по типу слабых электролитов, так как частицы внутренней сферы связаны ковалентной связью.
Диссоциация комплексных соединений Первичная диссоциация комплексных соединений - это распад КС в растворе на ионы внешней и внутренней сфер подобно cильным электролитам, так как эти ионы связаны ионными (электростатическими) силами. Вторичная диссоциация комплексного соединения – это распад внутренней сферы на составляющие ее компоненты. Этот процесс протекает по типу слабых электролитов, так как частицы внутренней сферы связаны ковалентной связью.
 Устойчивость комплексных соединений Для качественной характеристики устойчивости КС используют: 1) константу нестойкости комплекса (Кнест). Чем меньше значение Кн, тем более устойчивым является КС. 2) константу устойчивости (Kуст) - величина, обратная Кн. . Чем больше значение Куст, тем более устойчивый комплекс.
Устойчивость комплексных соединений Для качественной характеристики устойчивости КС используют: 1) константу нестойкости комплекса (Кнест). Чем меньше значение Кн, тем более устойчивым является КС. 2) константу устойчивости (Kуст) - величина, обратная Кн. . Чем больше значение Куст, тем более устойчивый комплекс.
 Эффективными препаратами для хелатотерапии являются: этилендиаминтетрауксусная кислота сукцимер БАЛ
Эффективными препаратами для хелатотерапии являются: этилендиаминтетрауксусная кислота сукцимер БАЛ
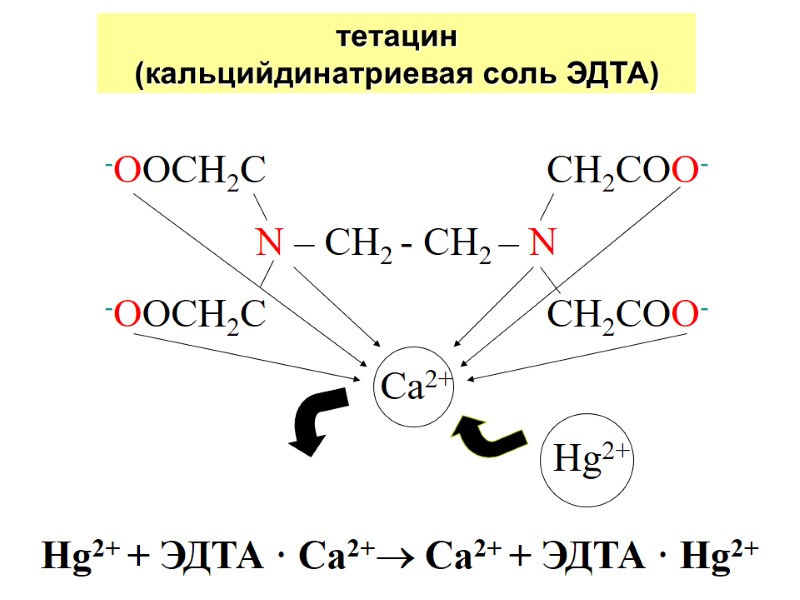
 тетацин (кальцийдинатриевая соль ЭДТА) -OOCH2C CH2COO- N – CH2 - CH2 – N -OOCH2C CH2COO- Сa2+ Hg2+ Hg2+ + ЭДТА · Ca2+ Ca2+ + ЭДТА · Hg2+
тетацин (кальцийдинатриевая соль ЭДТА) -OOCH2C CH2COO- N – CH2 - CH2 – N -OOCH2C CH2COO- Сa2+ Hg2+ Hg2+ + ЭДТА · Ca2+ Ca2+ + ЭДТА · Hg2+
 отравление ртутью отравление мышьяком
отравление ртутью отравление мышьяком


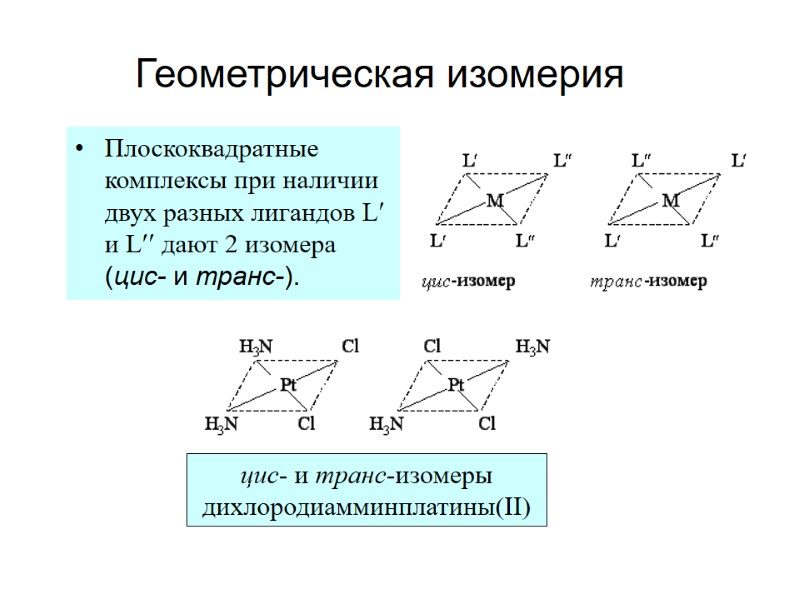
 Геометрическая изомерия Плоскоквадратные комплексы при наличии двух разных лигандов L и L дают 2 изомера (цис- и транс-).
Геометрическая изомерия Плоскоквадратные комплексы при наличии двух разных лигандов L и L дают 2 изомера (цис- и транс-).
![>Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 >Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2](https://present5.com/presentacii-2/20171208\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy_39.jpg) Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 [Co(NH3)5I]SO4 [Co(NH3)5SO4]I 1 Cl–; H2O (AgCl) 2 Cl– (2 AgCl) SO42– (BaSO4) I– (AgI)
Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 [Co(NH3)5I]SO4 [Co(NH3)5SO4]I 1 Cl–; H2O (AgCl) 2 Cl– (2 AgCl) SO42– (BaSO4) I– (AgI)
![>Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 >Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4](https://present5.com/presentacii-2/20171208\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy.ppt\21342-2_geterogennye_i_ligandoobmennye_ravnovesia_i_protsessy_40.jpg) Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 pH 7 pH 7 Координационные изомеры [Cr(NH3)4(NCS)2][Cr(NH3)2(NCS)4] [Cr(NH3)6][Cr(NCS)6]
Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 pH 7 pH 7 Координационные изомеры [Cr(NH3)4(NCS)2][Cr(NH3)2(NCS)4] [Cr(NH3)6][Cr(NCS)6]

