Лекция 2_литые_мет.pptx
- Количество слайдов: 27
 Лекция 2 «Формирование структуры литых металлов» 1
Лекция 2 «Формирование структуры литых металлов» 1
 Любое вещество может находиться в трех агрегатных состояниях: Твердом Жидком Газообразном Переход металла из жидкого состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. 2
Любое вещество может находиться в трех агрегатных состояниях: Твердом Жидком Газообразном Переход металла из жидкого состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. 2
 Кристаллы могут зарождаться самопроизвольно – самопроизвольная кристаллизация. Или расти на имеющихся готовых центрах кристаллизации – несамопроизвольная кристаллизация. Самопроизвольная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшением свободной энергии или термодинамического потенциала. 3
Кристаллы могут зарождаться самопроизвольно – самопроизвольная кристаллизация. Или расти на имеющихся готовых центрах кристаллизации – несамопроизвольная кристаллизация. Самопроизвольная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшением свободной энергии или термодинамического потенциала. 3
 Чем объяснить существование при одних температурах жидкого, а при других температурах твердого состояния и почему превращение происходит при строго определенных температурах? В природе все самопроизвольно протекающие процессы, а, следовательно, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии. Это можно пояснить примером: Тяжелый шарик из положения 1 стремиться попасть в более устойчивое положение 2, т. к. в положении 2 потенциальная энергия меньше, чем в положении 1. 4
Чем объяснить существование при одних температурах жидкого, а при других температурах твердого состояния и почему превращение происходит при строго определенных температурах? В природе все самопроизвольно протекающие процессы, а, следовательно, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии. Это можно пояснить примером: Тяжелый шарик из положения 1 стремиться попасть в более устойчивое положение 2, т. к. в положении 2 потенциальная энергия меньше, чем в положении 1. 4
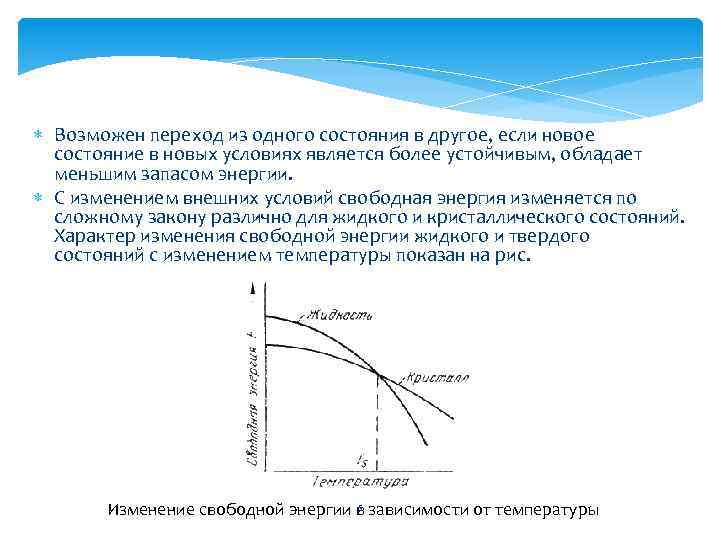 Возможен переход из одного состояния в другое, если новое состояние в новых условиях является более устойчивым, обладает меньшим запасом энергии. С изменением внешних условий свободная энергия изменяется по сложному закону различно для жидкого и кристаллического состояний. Характер изменения свободной энергии жидкого и твердого состояний с изменением температуры показан на рис. 5 Изменение свободной энергии в зависимости от температуры
Возможен переход из одного состояния в другое, если новое состояние в новых условиях является более устойчивым, обладает меньшим запасом энергии. С изменением внешних условий свободная энергия изменяется по сложному закону различно для жидкого и кристаллического состояний. Характер изменения свободной энергии жидкого и твердого состояний с изменением температуры показан на рис. 5 Изменение свободной энергии в зависимости от температуры
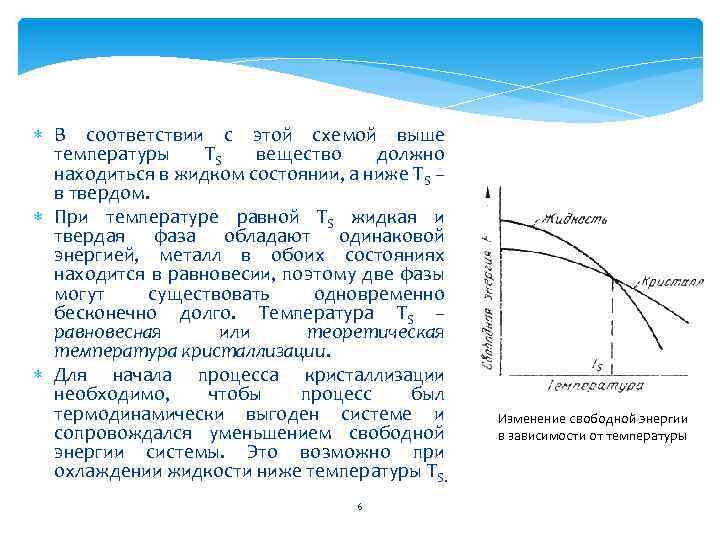 В соответствии с этой схемой выше температуры ТS вещество должно находиться в жидком состоянии, а ниже ТS – в твердом. При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго. Температура ТS – равновесная или теоретическая температура кристаллизации. Для начала процесса кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Это возможно при охлаждении жидкости ниже температуры ТS. 6 Изменение свободной энергии в зависимости от температуры
В соответствии с этой схемой выше температуры ТS вещество должно находиться в жидком состоянии, а ниже ТS – в твердом. При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго. Температура ТS – равновесная или теоретическая температура кристаллизации. Для начала процесса кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Это возможно при охлаждении жидкости ниже температуры ТS. 6 Изменение свободной энергии в зависимости от температуры
 Температура, при которой практически начинается кристаллизация называется фактической температурой кристаллизации. Охлаждение жидкости ниже равновесной температуры кристаллизации называется переохлаждением, которое характеризуется степенью переохлаждения. 7
Температура, при которой практически начинается кристаллизация называется фактической температурой кристаллизации. Охлаждение жидкости ниже равновесной температуры кристаллизации называется переохлаждением, которое характеризуется степенью переохлаждения. 7
 Процесс перехода металла из жидкого состояния в твердое можно изобразить графически в координатах температура – время по так называемым кривым охлаждения 8
Процесс перехода металла из жидкого состояния в твердое можно изобразить графически в координатах температура – время по так называемым кривым охлаждения 8
 Кривая охлаждения имеет следующий вид: 9
Кривая охлаждения имеет следующий вид: 9
 Д. К. Чернов, изучая структуру литой стали указал, что процесс кристаллизации состоит из двух элементарных процессов: зарождения мельчайших зародышей или центров кристаллизации роста кристаллов из этих центров Этот процесс можно изучать с помощью рассмотрения моделей (схем), что успешно применялось Миркиным И. Л. 10
Д. К. Чернов, изучая структуру литой стали указал, что процесс кристаллизации состоит из двух элементарных процессов: зарождения мельчайших зародышей или центров кристаллизации роста кристаллов из этих центров Этот процесс можно изучать с помощью рассмотрения моделей (схем), что успешно применялось Миркиным И. Л. 10
 Предположим, что на некоторой площади за 1 сек возникает 5 центров кристаллизации, которые растут с определенной скоростью. К концу 1 -ой сек образовалось 5 зародышей, к концу «-й они выросли и возникло еще 5 зародышей, к концу 2 -й они выросли и так далее. Так в результате возникновения зародышей и их роста происходит процесс кристаллизации. 11
Предположим, что на некоторой площади за 1 сек возникает 5 центров кристаллизации, которые растут с определенной скоростью. К концу 1 -ой сек образовалось 5 зародышей, к концу «-й они выросли и возникло еще 5 зародышей, к концу 2 -й они выросли и так далее. Так в результате возникновения зародышей и их роста происходит процесс кристаллизации. 11
 При образовании кристаллы растут свободно, они могут иметь геометрически правильную форму. При столкновении же растущих кристаллов их правильная форма нарушается. В результате этого при после затвердевания кристаллы имеют неправильную форму, их называют кристаллитами или зернами. 12
При образовании кристаллы растут свободно, они могут иметь геометрически правильную форму. При столкновении же растущих кристаллов их правильная форма нарушается. В результате этого при после затвердевания кристаллы имеют неправильную форму, их называют кристаллитами или зернами. 12
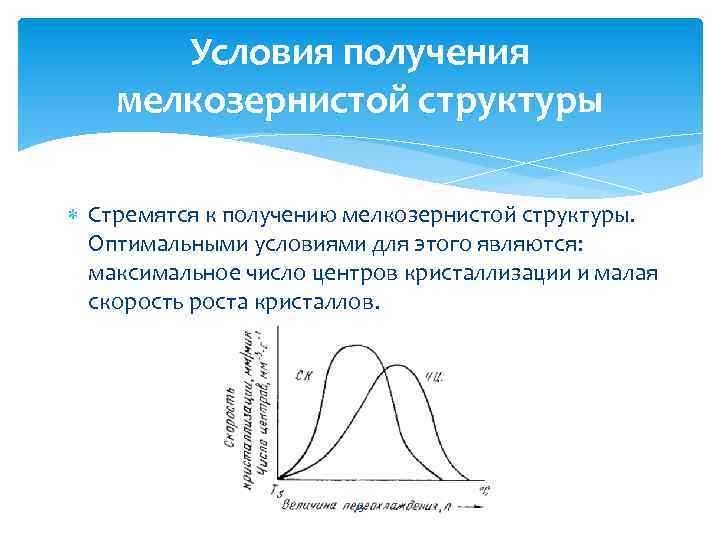 Условия получения мелкозернистой структуры Стремятся к получению мелкозернистой структуры. Оптимальными условиями для этого являются: максимальное число центров кристаллизации и малая скорость роста кристаллов. 13
Условия получения мелкозернистой структуры Стремятся к получению мелкозернистой структуры. Оптимальными условиями для этого являются: максимальное число центров кристаллизации и малая скорость роста кристаллов. 13
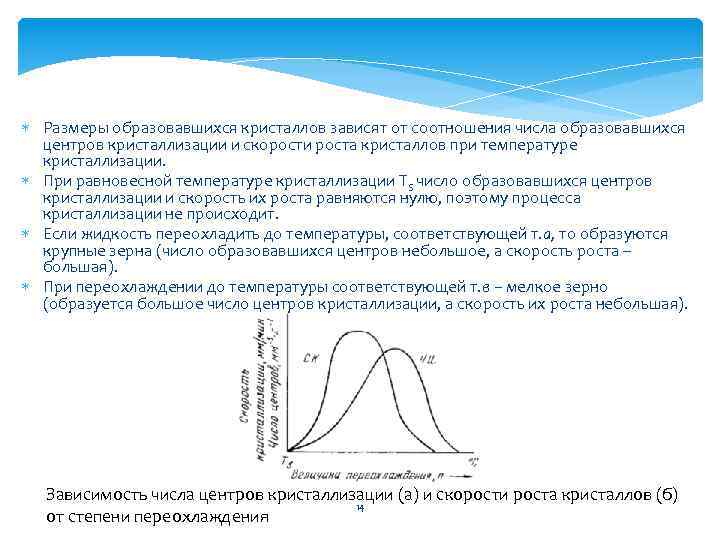 Размеры образовавшихся кристаллов зависят от соотношения числа образовавшихся центров кристаллизации и скорости роста кристаллов при температуре кристаллизации. При равновесной температуре кристаллизации ТS число образовавшихся центров кристаллизации и скорость их роста равняются нулю, поэтому процесса кристаллизации не происходит. Если жидкость переохладить до температуры, соответствующей т. а, то образуются крупные зерна (число образовавшихся центров небольшое, а скорость роста – большая). При переохлаждении до температуры соответствующей т. в – мелкое зерно (образуется большое число центров кристаллизации, а скорость их роста небольшая). Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) 14 от степени переохлаждения
Размеры образовавшихся кристаллов зависят от соотношения числа образовавшихся центров кристаллизации и скорости роста кристаллов при температуре кристаллизации. При равновесной температуре кристаллизации ТS число образовавшихся центров кристаллизации и скорость их роста равняются нулю, поэтому процесса кристаллизации не происходит. Если жидкость переохладить до температуры, соответствующей т. а, то образуются крупные зерна (число образовавшихся центров небольшое, а скорость роста – большая). При переохлаждении до температуры соответствующей т. в – мелкое зерно (образуется большое число центров кристаллизации, а скорость их роста небольшая). Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) 14 от степени переохлаждения
 Размер зерен при кристаллизации зависит и от числа частичек нерастворимых примесей, которые играют роль готовых центров кристаллизации – оксиды, нитриды, сульфиды. Чем больше частичек, тем мельче зерна закристаллизовавшегося металла. Стенки изложниц имеют неровности, шероховатости, которые увеличивают скорость кристаллизации. Мелкозернистую структуру можно получить в результате модифицирования, когда в жидкие металлы добавляются посторонние вещества – модификаторы 15
Размер зерен при кристаллизации зависит и от числа частичек нерастворимых примесей, которые играют роль готовых центров кристаллизации – оксиды, нитриды, сульфиды. Чем больше частичек, тем мельче зерна закристаллизовавшегося металла. Стенки изложниц имеют неровности, шероховатости, которые увеличивают скорость кристаллизации. Мелкозернистую структуру можно получить в результате модифицирования, когда в жидкие металлы добавляются посторонние вещества – модификаторы 15
 По механизму воздействия различают: Вещества не растворяющиеся в жидком металле – выступают в качестве дополнительных центров кристаллизации. Поверхностно - активные вещества, которые растворяются в металле, и, осаждаясь на поверхности растущих кристаллов, препятствуют их росту. 16
По механизму воздействия различают: Вещества не растворяющиеся в жидком металле – выступают в качестве дополнительных центров кристаллизации. Поверхностно - активные вещества, которые растворяются в металле, и, осаждаясь на поверхности растущих кристаллов, препятствуют их росту. 16
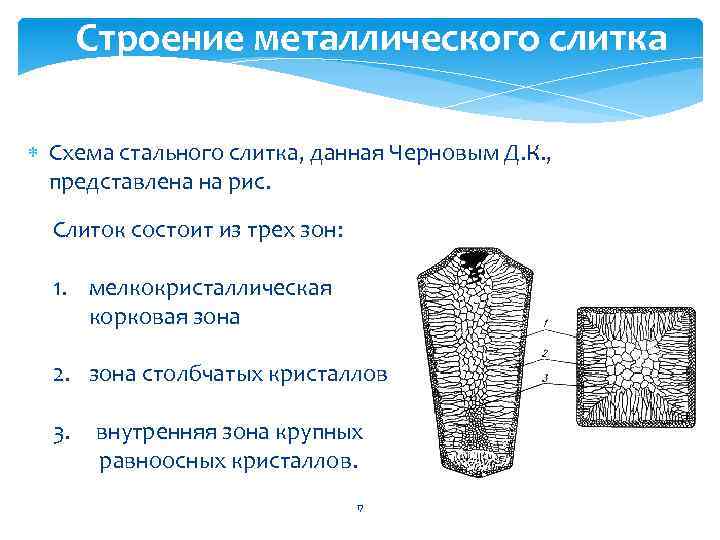 Строение металлического слитка Схема стального слитка, данная Черновым Д. К. , представлена на рис. Слиток состоит из трех зон: 1. мелкокристаллическая корковая зона 2. зона столбчатых кристаллов 3. внутренняя зона крупных равноосных кристаллов. 17
Строение металлического слитка Схема стального слитка, данная Черновым Д. К. , представлена на рис. Слиток состоит из трех зон: 1. мелкокристаллическая корковая зона 2. зона столбчатых кристаллов 3. внутренняя зона крупных равноосных кристаллов. 17
 Кристаллизация корковой зоны идет в условиях максимального переохлаждения. Скорость кристаллизации определяется большим числом центров кристаллизации. Образуется мелкозернистая структура. Жидкий металл под корковой зоной находится в условиях меньшего переохлаждения. Число центров ограничено и процесс кристаллизации реализуется за счет их интенсивного роста до большого размера. 18
Кристаллизация корковой зоны идет в условиях максимального переохлаждения. Скорость кристаллизации определяется большим числом центров кристаллизации. Образуется мелкозернистая структура. Жидкий металл под корковой зоной находится в условиях меньшего переохлаждения. Число центров ограничено и процесс кристаллизации реализуется за счет их интенсивного роста до большого размера. 18
 Дендрит Рост кристаллов во второй зоне имеет направленный характер. Они растут перпендикулярно стенкам изложницы, образуются древовидные кристаллы – дендриты. Растут дендриты с направлением, близким к направлению теплоотвода. 19
Дендрит Рост кристаллов во второй зоне имеет направленный характер. Они растут перпендикулярно стенкам изложницы, образуются древовидные кристаллы – дендриты. Растут дендриты с направлением, близким к направлению теплоотвода. 19
 Дендрит Так как теплоотвод от незакристаллизовавшегося металла в середине слитка в разные стороны выравнивается, то в центральной зоне образуются крупные дендриты со случайной ориентацией. Зоны столбчатых кристаллов в процессе кристаллизации стыкуются, это явление называется транскристаллизацией. Для малопластичных металлов и для сталей это явление нежелательное, так как при последующей прокатке, ковке могут образовываться трещины в зоне стыка. В верхней части слитка образуется усадочная раковина, которая подлежит отрезке и переплавке, так как металл более рыхлый. 20
Дендрит Так как теплоотвод от незакристаллизовавшегося металла в середине слитка в разные стороны выравнивается, то в центральной зоне образуются крупные дендриты со случайной ориентацией. Зоны столбчатых кристаллов в процессе кристаллизации стыкуются, это явление называется транскристаллизацией. Для малопластичных металлов и для сталей это явление нежелательное, так как при последующей прокатке, ковке могут образовываться трещины в зоне стыка. В верхней части слитка образуется усадочная раковина, которая подлежит отрезке и переплавке, так как металл более рыхлый. 20
 ПРЕВРАЩЕНИЯ В ТВЕРДОМ СОСТОЯНИИ Атомы элемента могут образовывать любую кристаллическую решетку. Однако устойчивым, а, следовательно, и реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии. Так, вольфрам, хром и др имеют ОЦК решетку, медь, серебро и др. – ГЦК. Однако в ряде случаев при изменении температуры может оказаться, что для того же металла более устойчивой будет другая решетка, чем была при другой температуре. 21
ПРЕВРАЩЕНИЯ В ТВЕРДОМ СОСТОЯНИИ Атомы элемента могут образовывать любую кристаллическую решетку. Однако устойчивым, а, следовательно, и реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии. Так, вольфрам, хром и др имеют ОЦК решетку, медь, серебро и др. – ГЦК. Однако в ряде случаев при изменении температуры может оказаться, что для того же металла более устойчивой будет другая решетка, чем была при другой температуре. 21
 Существование одного металла в нескольких кристаллических формах называется ПОЛИМОРФИЗМОМ или АЛЛОТРОПИЕЙ. Аллотропические формы обозначают буквами греческого алфавита. Превращение одной аллотропической формы в другую при нагреве чистого металла сопровождается поглощением тепла и происходит при постоянной температуре – горизонтальный участок на термической кривой. Такие металлы как железо, кобальт, олово, марганец, титан и др. имеют полиморфные превращения. 22
Существование одного металла в нескольких кристаллических формах называется ПОЛИМОРФИЗМОМ или АЛЛОТРОПИЕЙ. Аллотропические формы обозначают буквами греческого алфавита. Превращение одной аллотропической формы в другую при нагреве чистого металла сопровождается поглощением тепла и происходит при постоянной температуре – горизонтальный участок на термической кривой. Такие металлы как железо, кобальт, олово, марганец, титан и др. имеют полиморфные превращения. 22
 ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Постоянная температура при кристаллизации или, что тоже самое – наличие площадки на кривой охлаждения, объясняется, доказывается важнейшим физико-химическим законом, так называемым, правилом фаз или законом Гиббса. 23
ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Постоянная температура при кристаллизации или, что тоже самое – наличие площадки на кривой охлаждения, объясняется, доказывается важнейшим физико-химическим законом, так называемым, правилом фаз или законом Гиббса. 23
 ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Правило фаз – это закон, выражающий соотношение между числом фаз Ф, числом компонентов К, внешних переменных В и числом степеней свободы для равновесной температуры. Чтобы успешно пользоваться этим правилом необходимо дать понятия этим величинам. 24
ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Правило фаз – это закон, выражающий соотношение между числом фаз Ф, числом компонентов К, внешних переменных В и числом степеней свободы для равновесной температуры. Чтобы успешно пользоваться этим правилом необходимо дать понятия этим величинам. 24
 ПРАВИЛО ФАЗ или ЗАКОН ГИББСА ФАЗА – это однородная часть системы, ограниченная от другой части системы поверхностью раздела при переходе через которую свойства изменяются скачкообразно. КОМПОНЕНТАМИ системы называют химические соединения или элементы, из которых может быть образована любая система. Это может быть один металл или элементы сплава. ЧИСЛОМ СТЕПЕНЕЙ СВОБОДЫ – или ВАРИАНТНОСТЬЮ СИСТЕМЫ называют количество факторов ( концентрация, температура, давление), которые можно произвольно изменять без изменения числа фаз системы. 25
ПРАВИЛО ФАЗ или ЗАКОН ГИББСА ФАЗА – это однородная часть системы, ограниченная от другой части системы поверхностью раздела при переходе через которую свойства изменяются скачкообразно. КОМПОНЕНТАМИ системы называют химические соединения или элементы, из которых может быть образована любая система. Это может быть один металл или элементы сплава. ЧИСЛОМ СТЕПЕНЕЙ СВОБОДЫ – или ВАРИАНТНОСТЬЮ СИСТЕМЫ называют количество факторов ( концентрация, температура, давление), которые можно произвольно изменять без изменения числа фаз системы. 25
 ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Математически выражение правила фаз имеет вид: С = К - Ф + 1 , где К – количество компонентов, образующих систему Ф- число фаз в системе В – число внешних переменных Применяя правило фаз к металлам, можно во многих случаях принять изменяющимся только один внешний фактор – температуру, т. к. давление мало влияет на фазовое равновесие сплавов в твердом и жидком состояниях. Тогда правило фаз примет вид: С=К–Ф+1 26
ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Математически выражение правила фаз имеет вид: С = К - Ф + 1 , где К – количество компонентов, образующих систему Ф- число фаз в системе В – число внешних переменных Применяя правило фаз к металлам, можно во многих случаях принять изменяющимся только один внешний фактор – температуру, т. к. давление мало влияет на фазовое равновесие сплавов в твердом и жидком состояниях. Тогда правило фаз примет вид: С=К–Ф+1 26
 ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Математически - степень свободы – это разность между числом переменных и уравнений, в которые входят эти переменные Если С =0, то такое равновесие называется НОНВАРИАНТНЫМ. При нонвариантном равновесии сплав из данного числа фаз может существовать только в совершенно определенных условиях - при постоянной температуре. На кривой охлаждения – площадка. Если С = 1, то система называется МОНОВАРИАНТНОЙ, система находится не в равновесии, следовательно, температура меняется – на кривой перегиб 27
ПРАВИЛО ФАЗ или ЗАКОН ГИББСА Математически - степень свободы – это разность между числом переменных и уравнений, в которые входят эти переменные Если С =0, то такое равновесие называется НОНВАРИАНТНЫМ. При нонвариантном равновесии сплав из данного числа фаз может существовать только в совершенно определенных условиях - при постоянной температуре. На кривой охлаждения – площадка. Если С = 1, то система называется МОНОВАРИАНТНОЙ, система находится не в равновесии, следовательно, температура меняется – на кривой перегиб 27


