лек 2 2014.ppt
- Количество слайдов: 46

Лекция 2 Электронная микроскопия Подготовка образцов для исследования методами световой и электронной микроскопии

Макрообъекты Клеточная форма жизни
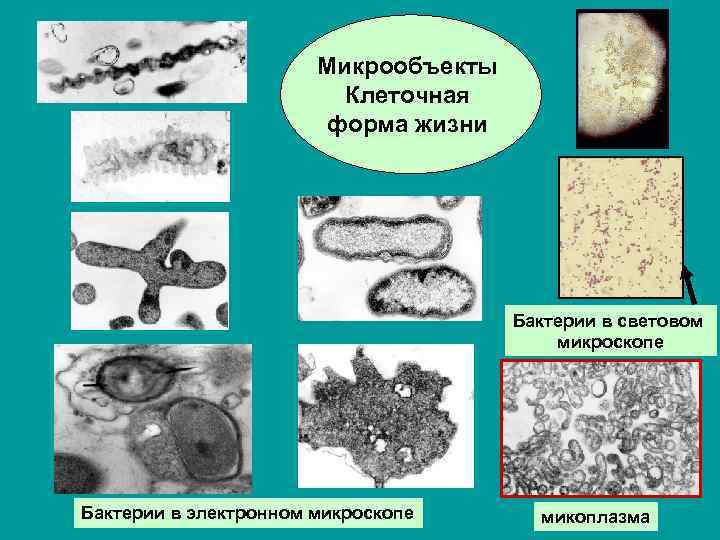
Микрообъекты Клеточная форма жизни Бактерии в световом микроскопе Бактерии в электронном микроскопе микоплазма
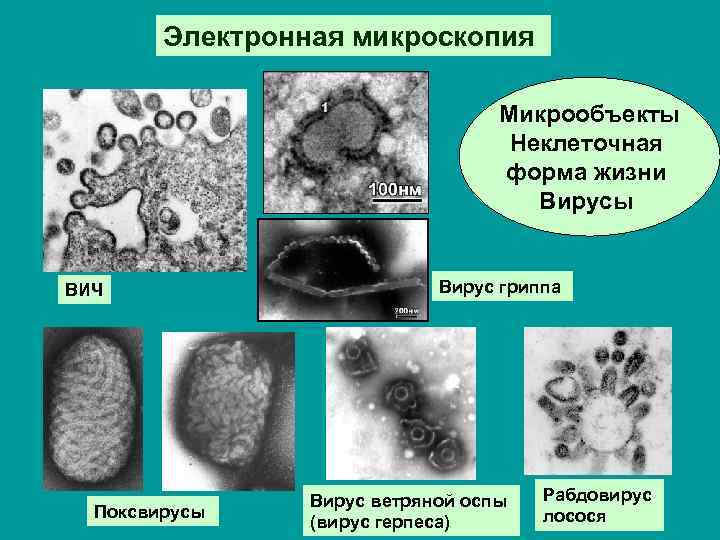
Электронная микроскопия Микрообъекты Неклеточная форма жизни Вирусы ВИЧ Поксвирусы Вирус гриппа Вирус ветряной оспы (вирус герпеса) Рабдовирус лосося
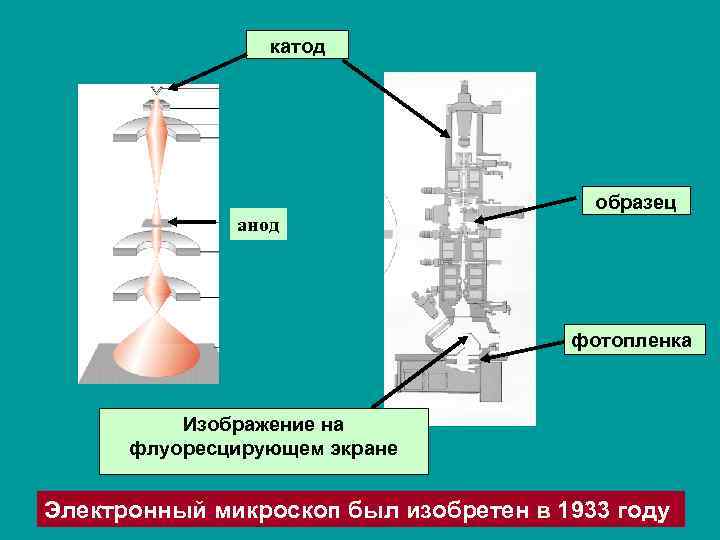
катод анод образец фотопленка Изображение на флуоресцирующем экране Электронный микроскоп был изобретен в 1933 году

Первый ЭМ фирмы Джеол (Jeol) 1948 г.

Первый ЭМ фирмы Филлипс Phillips, Нидерланды 1949


Современные просвечивающие электронные микроскопы H-7650 120 k. V Hitachi 200 k. V FEI

Современные просвечивающие электронные микроскопы Jem 1400 120 k. V Jeol Jem 2100 200 k. V Jeol

Jeol 1 000 V Университет Токио

Современные растровые электронные микроскопы Окись меди JSM 6390 Jeol Яблоко
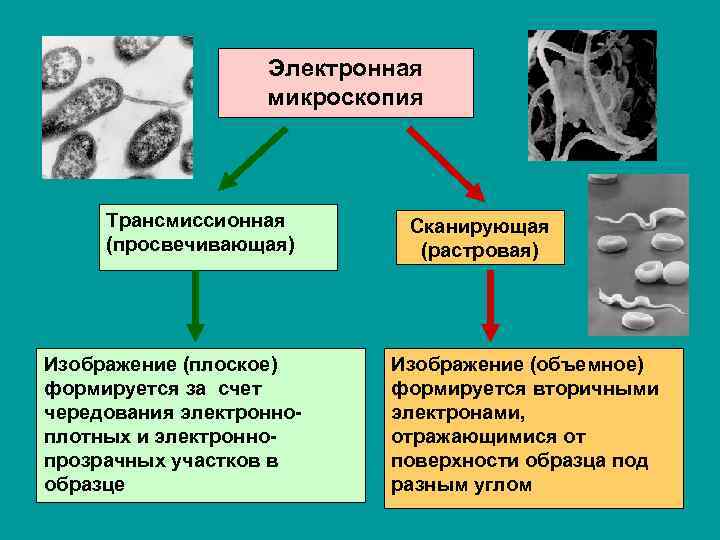
Электронная микроскопия Трансмиссионная (просвечивающая) Изображение (плоское) формируется за счет чередования электронноплотных и электроннопрозрачных участков в образце Сканирующая (растровая) Изображение (объемное) формируется вторичными электронами, отражающимися от поверхности образца под разным углом
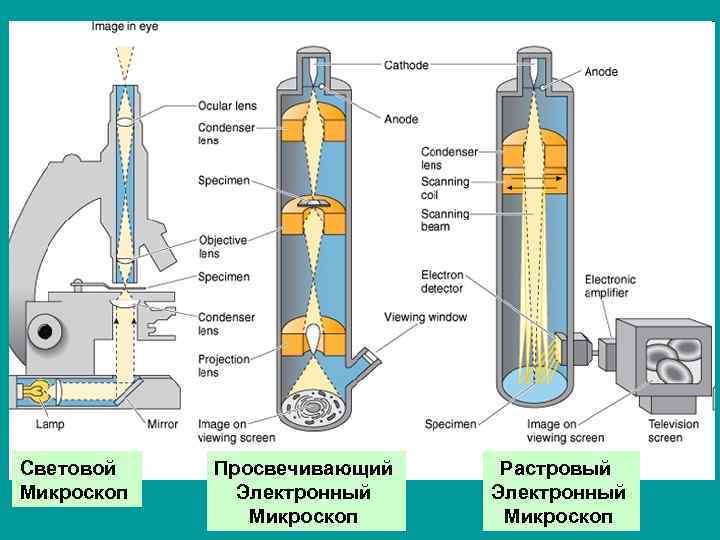
Световой Микроскоп Просвечивающий Электронный Микроскоп Растровый Электронный Микроскоп
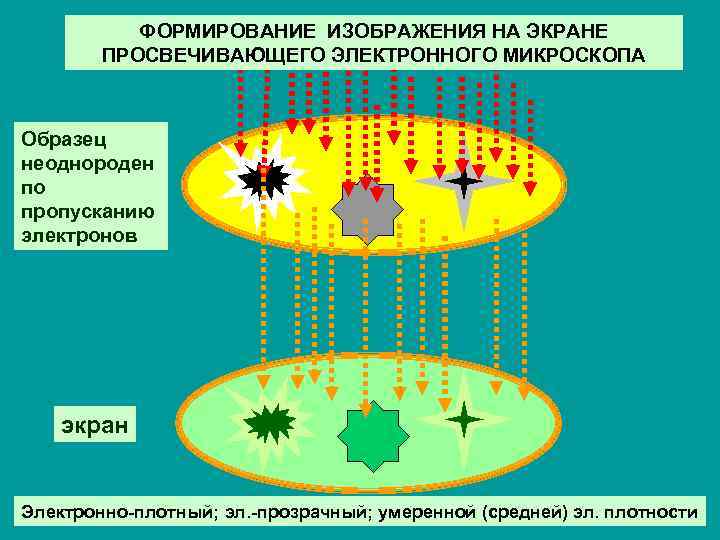
ФОРМИРОВАНИЕ ИЗОБРАЖЕНИЯ НА ЭКРАНЕ ПРОСВЕЧИВАЮЩЕГО ЭЛЕКТРОННОГО МИКРОСКОПА Образец неоднороден по пропусканию электронов экран Электронно-плотный; эл. -прозрачный; умеренной (средней) эл. плотности

Наночастицы золота в суспензии 50 nm 5 nm 200 nm 500 nm 10 nm 200 nm 50 nm НЧЗ, покрытые ПЭГ 100 nm 200 nm

Требования к образцам для электронно-микроскопического исследования: устойчивость к воздействию вакуума, температуры и электронного луча; оптимальная толщина; неоднородность химического состава и присутствие атомов тяжелых элементов; контраст Все эти требования достаточно легко реализуются для «неживых» материалов (кристаллы, пленки, порошки и т. п. ) БИОЛОГИЧЕСКИЕ ОБЪЕКТЫ? ?
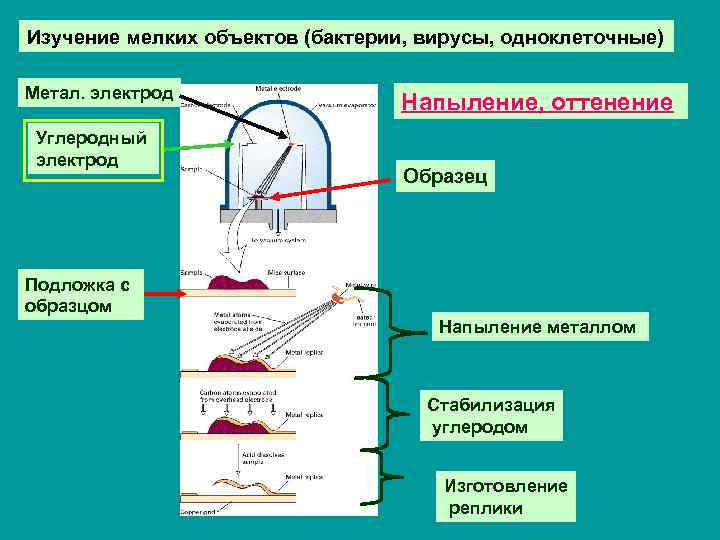
Изучение мелких объектов (бактерии, вирусы, одноклеточные) Метал. электрод Углеродный электрод Напыление, оттенение Образец Подложка с образцом Напыление металлом Стабилизация углеродом Изготовление реплики

ДНК, напыление
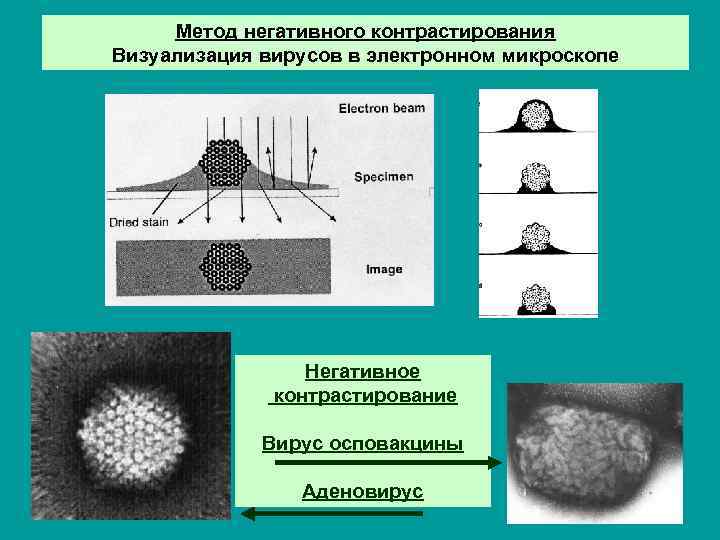
Метод негативного контрастирования Визуализация вирусов в электронном микроскопе Негативное контрастирование Вирус осповакцины Аденовирус

Метод негативного контрастирования Применяется - для быстрой диагностики (идентификации) вирусов - для изучения состава вирусных суспензий - для определения концентрации вирионов в суспензии (физический титр) - для индикации бактериальных клеток и изучения их поверхности Позволяет - изучить форму и размеры вирусных частиц - изучить строение поверхности вирусных частиц Достоинства метода - быстрота и относительная простота Требования к препаратам - концентрация не ниже 10 6 - 10 7 частиц в мл - чистота

ОСНОВНЫЕ ЭТАПЫ ИССЛЕДОВАНИЯ - подготовка сеточек с подложкой - нанесение суспензии вируса (бактерий, наночастиц, липосом и т. п. ) на сеточку, экспозиция - экспозиция сеточки с контрастирующим веществом (уранилацетат, фосфорновольфрамовая кислота и др. ) - просмотр сеточки в электронном микроскопе

Бактериофаги Вирусы в фекалиях детей Парвовирус собак Вирус паралича пчел
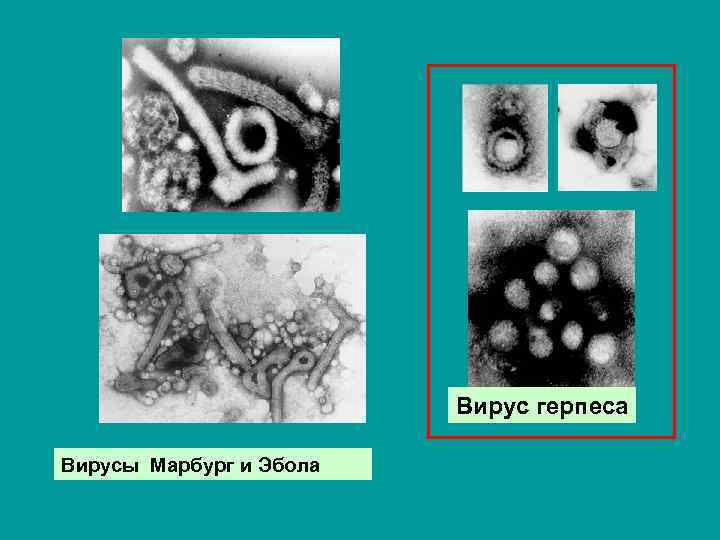
Вирус герпеса Вирусы Марбург и Эбола
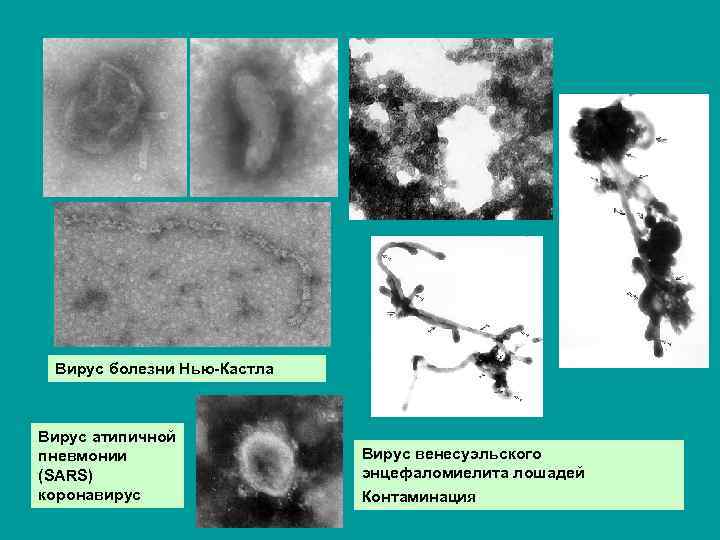
Вирус болезни Нью-Кастла Вирус атипичной пневмонии (SARS) коронавирус Вирус венесуэльского энцефаломиелита лошадей Контаминация
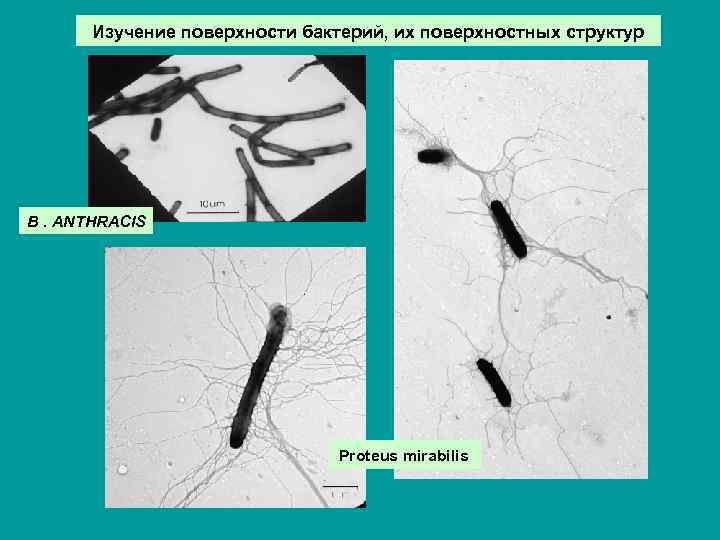
Изучение поверхности бактерий, их поверхностных структур B. ANTHRACIS Proteus mirabilis

Мелкие (нанообъекты) могут быть визуализированы в электронном микроскопе методами негативного контрастирования и напыления-оттенения металлом КЛЕТКИ? ОРГАНЫ? ? образцы для электронно-микроскопического исследования должны быть устойчивы к воздействию вакуума, температуры и электронного луча Пропускать электроны и быть неоднородными по электронной плотности Метод ультратонких срезов Возник на базе знаний о приготовлении парафиновых срезов для световой микроскопии

I. Фиксация клеток и тканей Молекулы фиксатора «сшивают» молекулы клеток Сохранность структуры Альдегидные фиксаторы Формальдегид и глутаровый альдегид Промышленный формалин = 40% насыщенный р-р формальдегида На практике его принимают за 100% формалин Стандартный фиксатор для световой микроскопии: 10% формалин (4% в действительности) Параформ (порошок) – смесь полимеров формальдегида, при нагревании до +80 о. С при р. Н выше 7 распадается на мономеры Условия фиксации должны быть максимально приближены к условиям существования живых клеток и тканей Процесс фиксации должен опережать аутолиз

Условия фиксации Важно: - р. Н фиксатора (7, 2 – 7, 4) - температура (4 – 8 о С) - величина образца - время фиксации - буферная емкость раствора, осмолярность - размеры кусочков (осадков) не более 1 х1 х1 -2 см для ЭМ Фосфатный буфер Какодилатный буфер Растворы для культивирования клеток (Хенкса и т. п. ) Для электронной микроскопии: - Параформальдегид 0, 5 – 4% - Глутаровый альдегид 0, 5 – 2, 5% - Четырехокись осмия 1 %

II. Обезвоживание образцов «Проводка образцов» III. Заливка в парафин или синтетические среды Задача – сделать материал пригодным для изготовления достаточно тонких срезов, для окрашивания и просмотра в световом или электронном микроскопе Обезвоживание – замена воды в образцах на органический растворитель В световой микроскопии: Этиловый спирт Изопропиловый спирт Ксилол Синтетические растворители (фирменные названия) Конечный растворитель должен растворять парафин Пропитка – смесь парафина и конечного растворителя

Обработка образцов для изучения методом ультратонких срезов Проводка: - обезвоживание в ацетоне или пропиленоксиде, плотно закрывающаяся посуда - пропитка в смеси ацетон-смола - заливка в смолу - пропитка в смоле - полимеризация Эпон, аралдит (эпоксидные смолы) самые широко используемые среды для заливки Требуют полного обезвоживания Водорастворимые среды для заливки

Автоматы для гистологической проводки Обезвоживание Пропитка Автоматы для гистологической проводки карусельного типа Автоматы для большого количества образцов
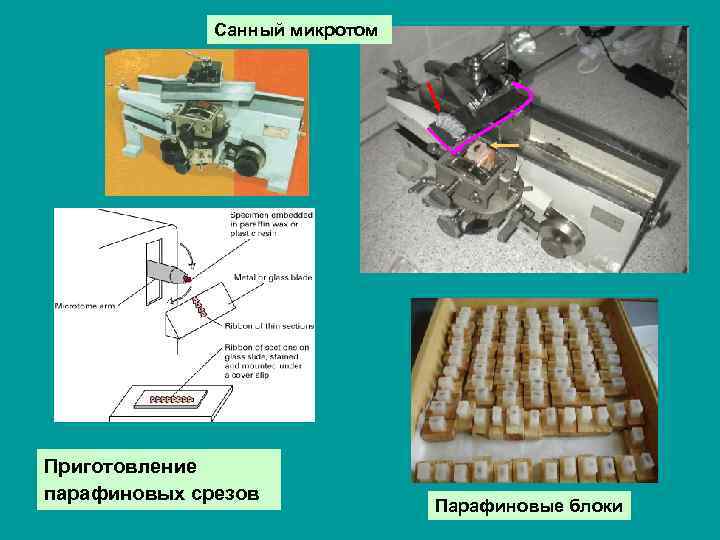
Санный микротом Приготовление парафиновых срезов Парафиновые блоки

Микротомы для приготовления гистологических срезов Ротационные микротомы Микротом с системой переноса срезов Автоматизированные микротомы

Окрашивание парафиновых срезов Депарафинирование срезов Окрашивание Приготовление постоянных препаратов Автомат для окрашивания парафиновых срезов LEICA ST 5020 Универсальный роботизированный мультистейнер
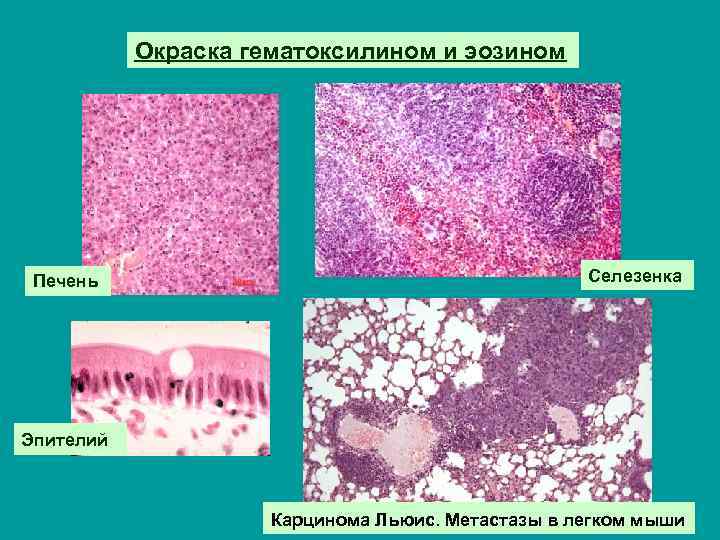
Окраска гематоксилином и эозином Печень Селезенка Эпителий Карцинома Льюис. Метастазы в легком мыши
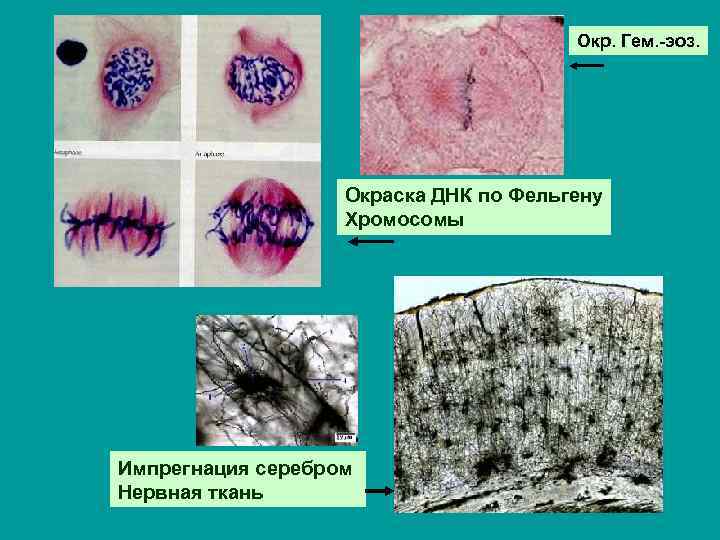
Окр. Гем. -эоз. Окраска ДНК по Фельгену Хромосомы Импрегнация серебром Нервная ткань

МЕТОД УЛЬТРАТОНКИХ СРЕЗОВ Увидеть вирус осповакцины в электронном микроскопе удалось в конце 30 -х годов. Первая фотография клетки, полученная с помощью ЭМ, была сделана в 1945 г. К. Р. Портером, А. Клодом и Э. Ф. Фулламом. Совершенствование методов электронной микроскопии: - Сохранения структуры объектов: фиксация, обезвоживание, заливочные среды - Разработка метода ультратонких срезов - Улучшение качества изображения и фотографий

МЕТОД УЛЬТРАТОНКИХ СРЕЗОВ ОСНОВНЫЕ ЭТАПЫ ИССЛЕДОВАНИЯ - фиксация образцов - дофиксация четырехокисью осмия, обезвоживание и заключение образцов в заливочные среды - приготовление полу- и ультратонких срезов - контрастирование ультратонких срезов - изучение срезов в электронном микроскопе, фотосъемка - изготовление фотоотпечатков, анализ результатов

Машина для изготовления ножей Ультратом (ультрамикротом)

Изготовление ультратонких срезов Обычно срезы имеют толщину 50 -70 нм

МЕТОД УЛЬТРАТОНКИХ СРЕЗОВ Применяется для исследования культур клеток, бактерий, тканей и органов животных и человека Метод позволяет: - изучать строение клеток и тканей в норме и при патологии - изучать размножение вирусов и бактерий - изучать изменения структуры клеток в разных экспериментальных условиях и при различных воздействиях - идентифицировать зараженные клетки в организме - контролировать контаминацию культур клеток
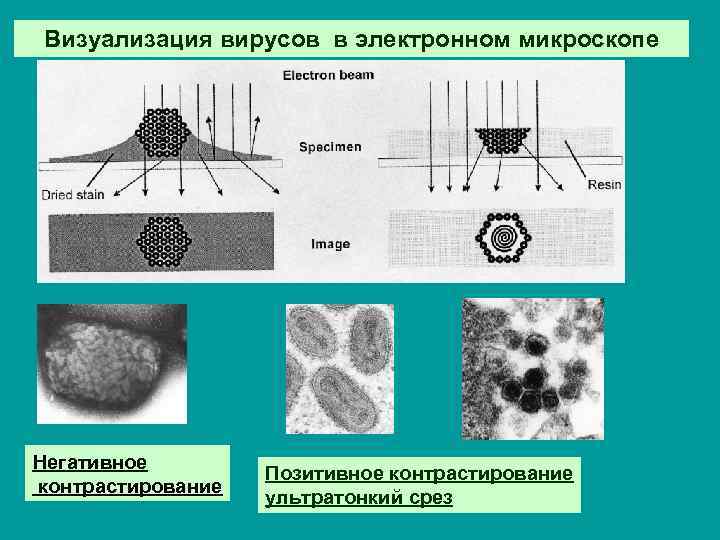
Визуализация вирусов в электронном микроскопе Негативное контрастирование Позитивное контрастирование ультратонкий срез
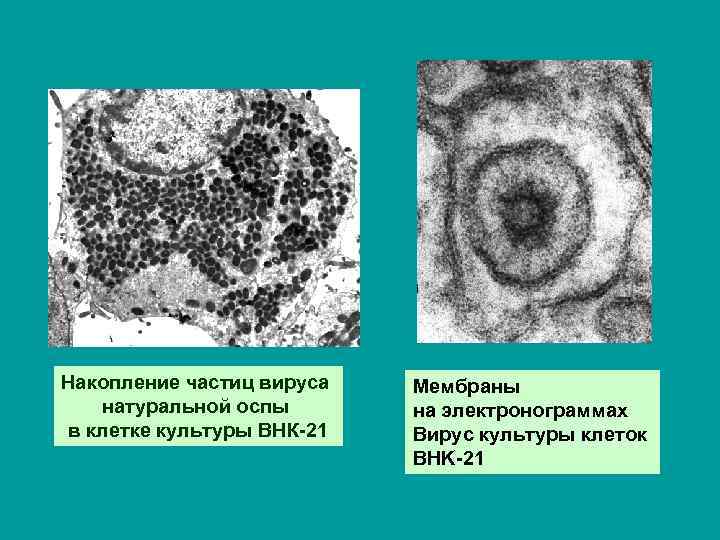
Накопление частиц вируса натуральной оспы в клетке культуры ВНК-21 Мембраны на электронограммах Вирус культуры клеток BHK-21
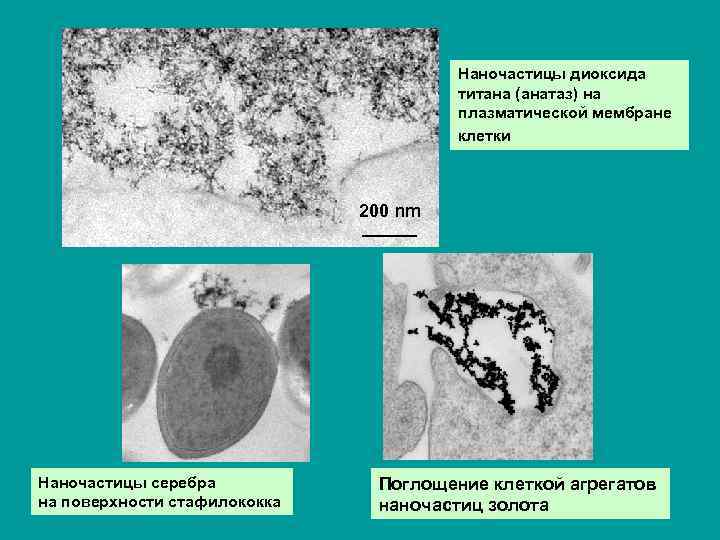
Наночастицы диоксида титана (анатаз) на плазматической мембране клетки 200 nm Наночастицы серебра на поверхности стафилококка Поглощение клеткой агрегатов наночастиц золота
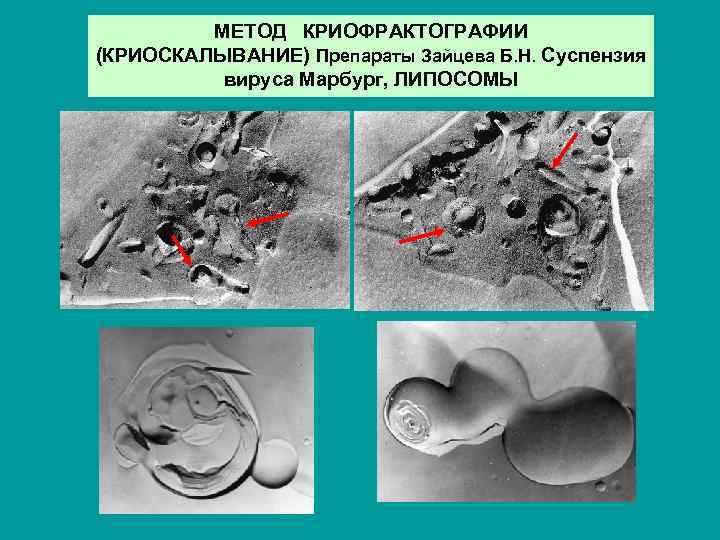
МЕТОД КРИОФРАКТОГРАФИИ (КРИОСКАЛЫВАНИЕ) Препараты Зайцева Б. Н. Суспензия вируса Марбург, ЛИПОСОМЫ
лек 2 2014.ppt