Lektsia_2.ppt
- Количество слайдов: 31

Лекция 2. Белки, часть 2. Ферменты

Классификация простых белков по растворимости • Альбумины содержатся в белке яйца, сыворотке крови (М. м. до 70 к. Да) • Глобулины содержатся в сыворотке крови, в гомогенатах мышечной ткани (М. м. от 70 до 40000 к. Да) • Гистоны – основа хромосом яйцеклеток и соматических клеток • Протамины – основа хромосом сперматозоидов • Глутелины – белки семян злаков (дефицитен по метионину) • Проламины – белки семян злаков (много пролина) • Склеропротеины – фибрилярные белки
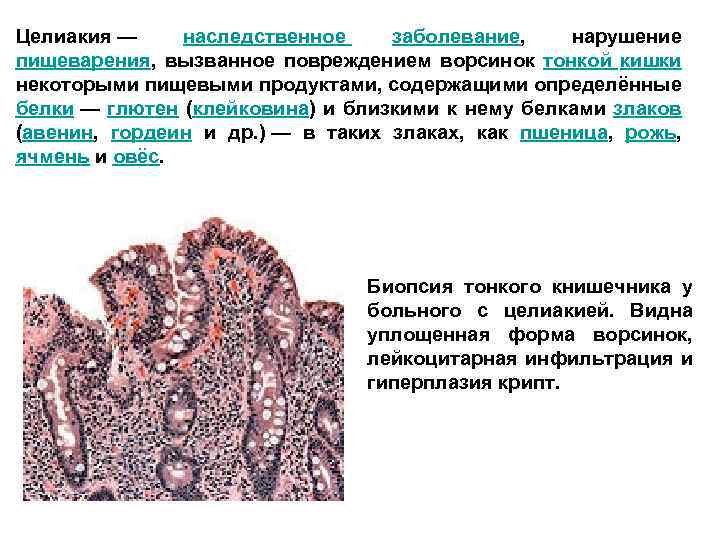
Целиакия — наследственное заболевание, нарушение пищеварения, вызванное повреждением ворсинок тонкой кишки некоторыми пищевыми продуктами, содержащими определённые белки — глютен (клейковина) и близкими к нему белками злаков (авенин, гордеин и др. ) — в таких злаках, как пшеница, рожь, ячмень и овёс. Биопсия тонкого книшечника у больного с целиакией. Видна уплощенная форма ворсинок, лейкоцитарная инфильтрация и гиперплазия крипт.

Свойства белков • • • Взаимодействие белков с лигандами Денатурация Высаливание Изменение суммарного заряда молекул в соответствии с р. Н Гидролиз кислотный, щелочной, ферментативный Белки – это коллоиды
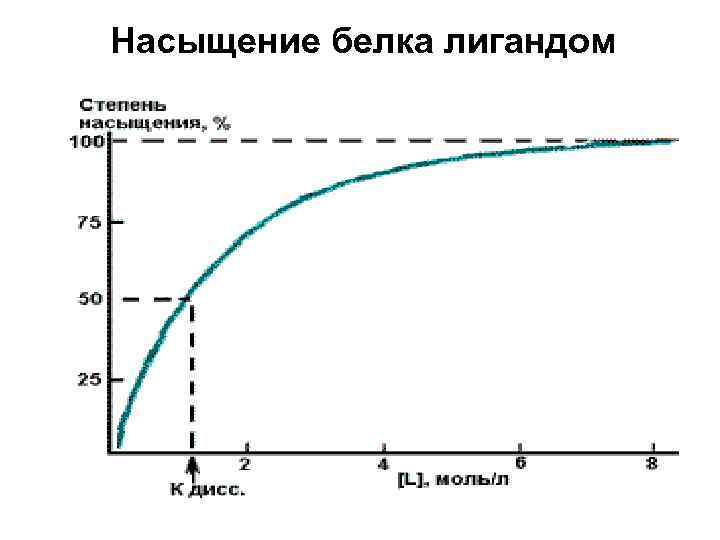
Насыщение белка лигандом
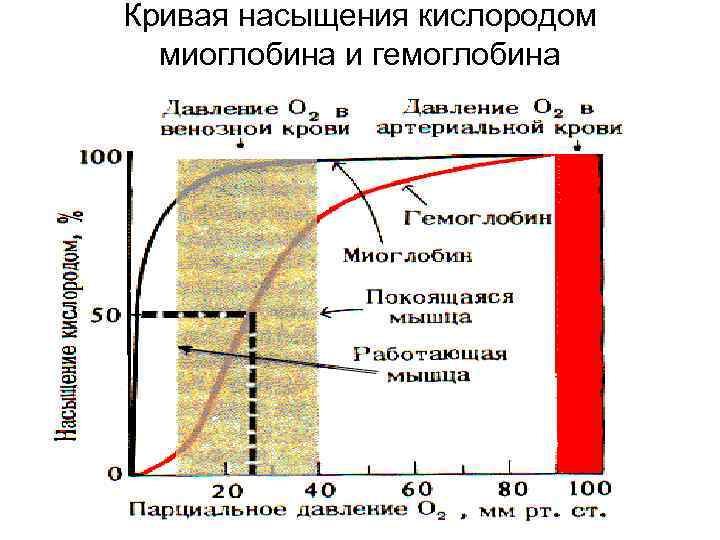
Кривая насыщения кислородом миоглобина и гемоглобина
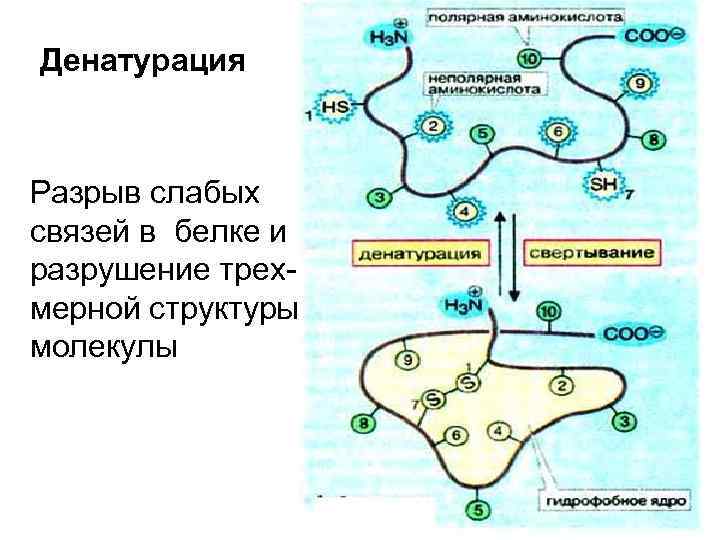
Денатурация Разрыв слабых связей в белке и разрушение трехмерной структуры молекулы
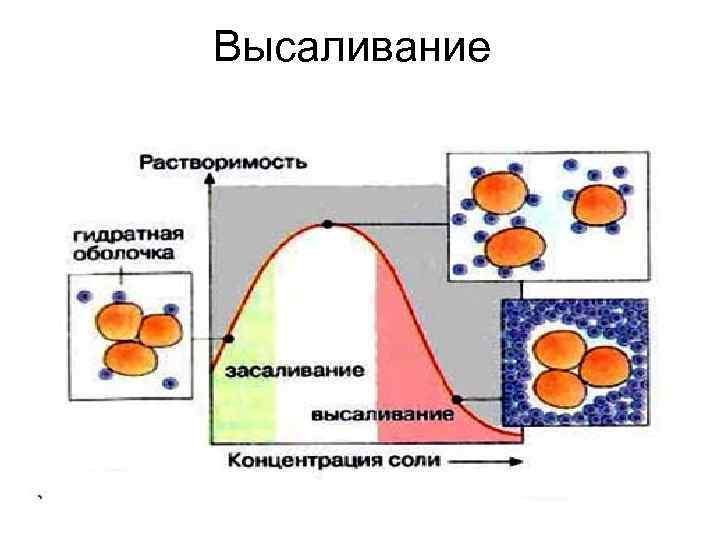
Высаливание
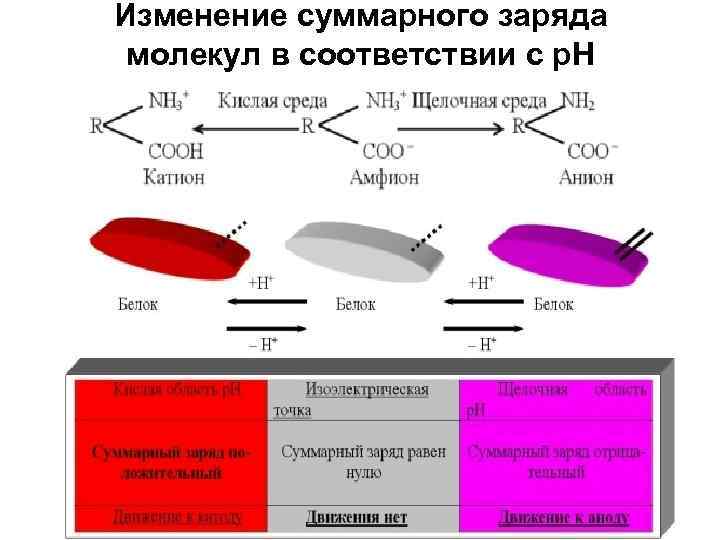
Изменение суммарного заряда молекул в соответствии с р. Н
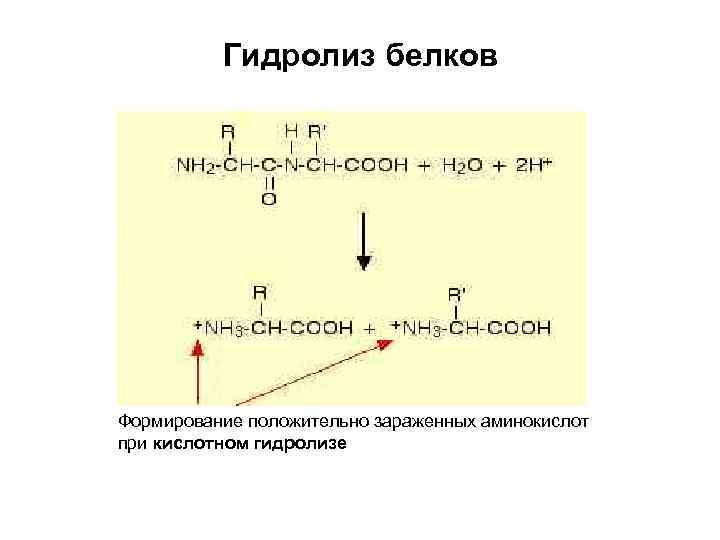
Гидролиз белков Формирование положительно зараженных аминокислот при кислотном гидролизе

Коллоидные свойства белков Диализ – очистка белковых растворов от низкомолекулярных соединений Размер белковых молекул лежит в пределах 1 мкм до 1 нм и, следовательно, они являются коллоидными частицами, которые в воде образуют коллоидные растворы. Эти растворы характеризуются высокой вязкостью, способностью рассеивать лучи видимого света, не проходят сквозь полупроницаемые мембраны.

Методы обнаружения, идентификации белков и оценки их аминокислотного состава • Химические методы. Качественные и количественные реакции на аминокислоты и белки • Физико-химические методы: – Электрофорез; – Хроматография; – Спектрометрия; – Иммуноферментные методы (ИФА)

Исследование белкового обмена • Общий белок крови и мочи • Альбумин сыворотки крови • Белковый спектр сыворотки или плазмы крови • Тимоловая проба • Остаточный азот сыворотке крови и моче : – Мочевина; – Креатинин; – Мочевая кислота; – Аммиак; – Оксид азота.
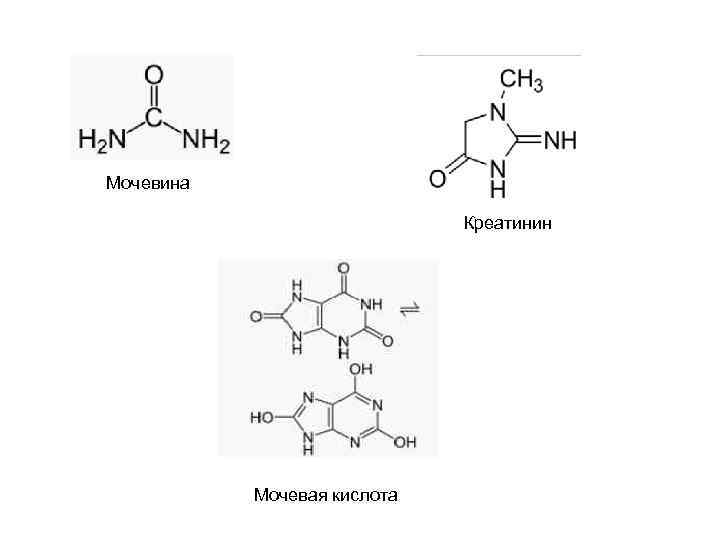
Мочевина Креатинин Мочевая кислота

Ферменты, часть 1 от лат. fermentum – брожение или закваска от греч. enzyme – внутри закваски

Ферменты – это органические вещества белковой природы, которые синтезируются в клетках и во много раз ускоряют протекающие в них реакции, не подвергаясь при этом химическим превращениям. Практически все биохимические реакции катализируются ферментами.

Свойства ферментов Все ферменты – это белки и свойства белков являются свойствами ферментов. Кроме того, ферменты имеют уникальные свойства: • высокую эффективность действия; • специфичность действия; • способность к регуляции. • изменением эффективности в соответствии с условиями среды, т. е. скорость ферментативных реакций существенно зависит от температуры и р. Н.
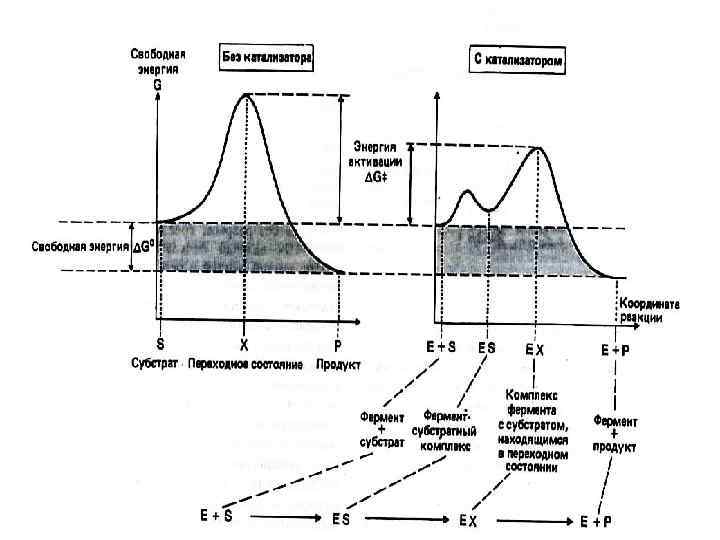

Зависимость скорости ферментативных реакций от р. Н 1 — пепсин, 2 — рибонуклеаза, 3 — аргиназа Единица скорости ферментативной реакции 1 МЕ (международная единица). Это такое количество фермента, которое катализирует превращение 1 мк. М субстрата в продукт за 1 минуту в оптимальных условиях.
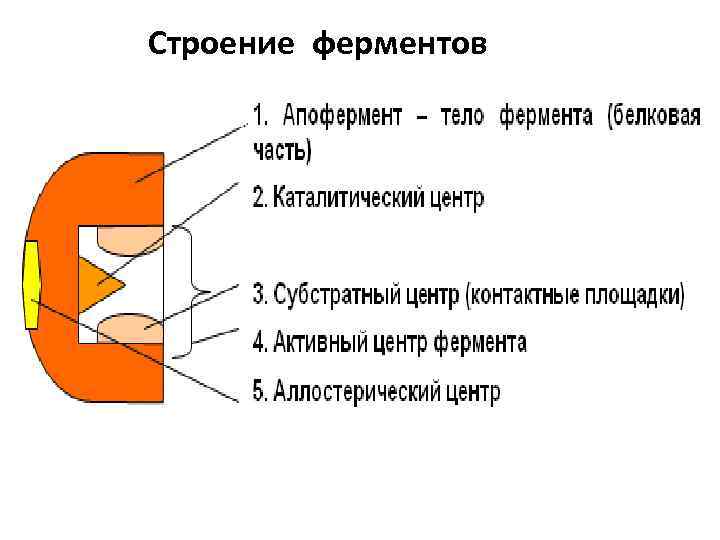
Строение ферментов
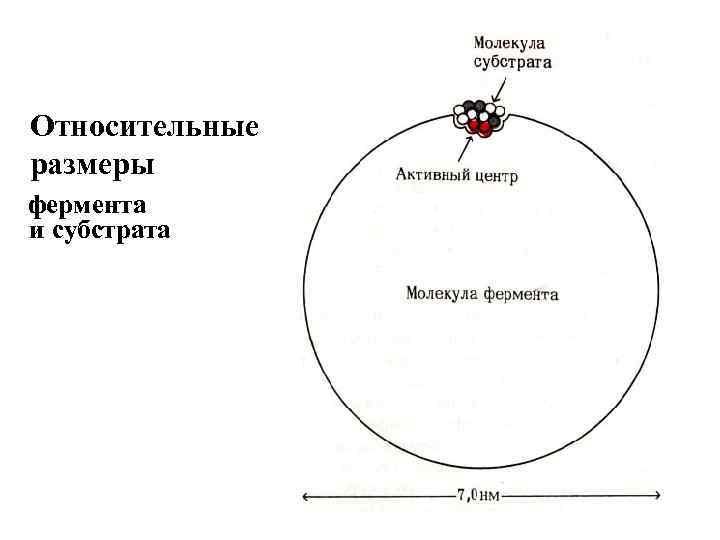
Относительные размеры фермента и субстрата

Простой фермент имеет только белковую часть. Сложный фермент (Холофермент ) = Апофермент + кофермент или кофактор (белок) (небелковая часть) Кофактор сидит в ферменте. Кофермент циркулирует от одного фермента к другому.

Простой фермент имеет только белковую часть. Сложный фермент (Холофермент ) = Апофермент + кофермент или кофактор (белок) (небелковая часть) Кофактор сидит в ферменте. Кофермент циркулирует от одного фермента к другому.

Ферменты и их кофакторы Фермент Цитохромоксидаза, каталаза, пероксидаза Алкогольдегидрогеназа, DNA-полимераза Гексокиназа, глюкозо-6 -фосфатаза Ион металла Fe 2+, Fe 3+ Zn 2+ Mg 2+ Уреаза Ni 2+ Нитратредуктаза Mo Глутатионпероксидаза Se
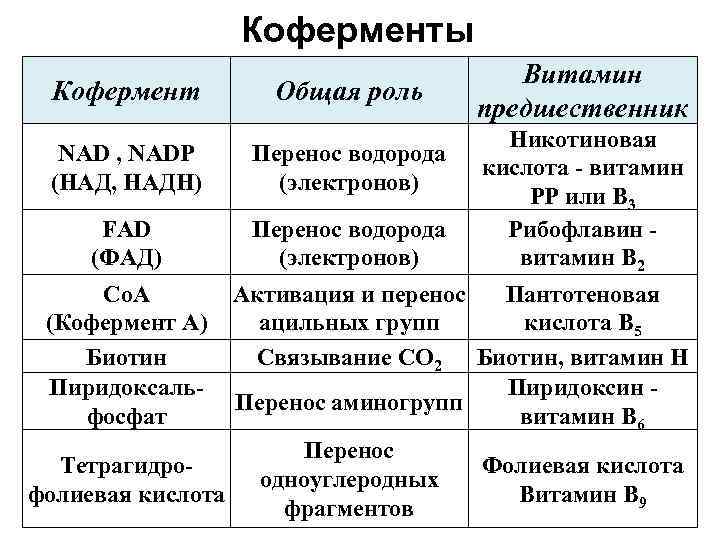
Коферменты Кофермент Общая роль NAD , NADP (НАД, НАДН) Перенос водорода (электронов) FAD (ФАД) Перенос водорода (электронов) Co. A (Кофермент А) Биотин Пиридоксальфосфат Витамин предшественник Никотиновая кислота - витамин РР или В 3 Рибофлавин витамин В 2 Активация и перенос Пантотеновая ацильных групп кислота В 5 Связывание СО 2 Биотин, витамин Н Пиридоксин Перенос аминогрупп витамин В 6 Перенос Тетрагидро. Фолиевая кислота одноуглеродных фолиевая кислота Витамин В 9 фрагментов
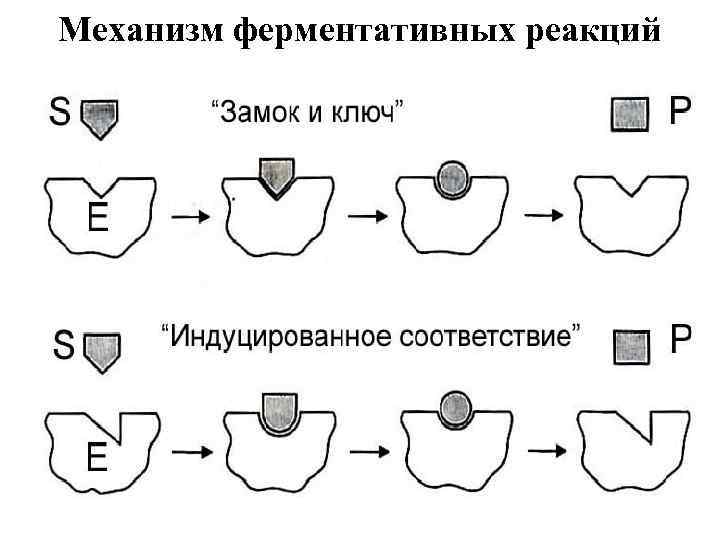
Механизм ферментативных реакций
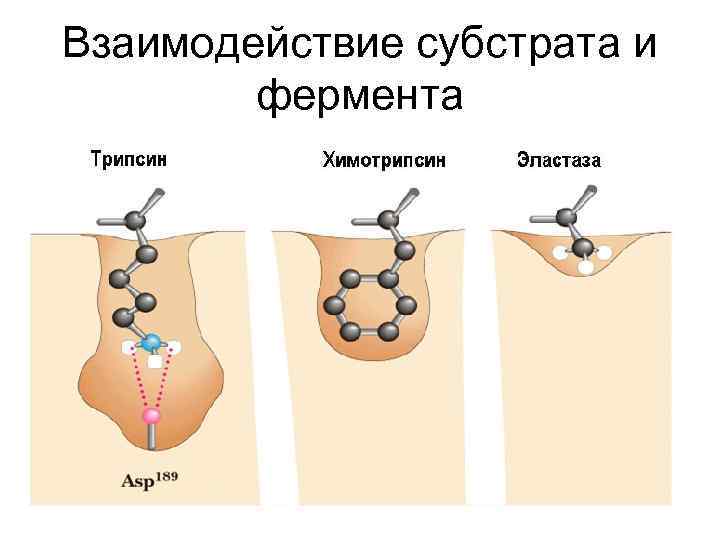
Взаимодействие субстрата и фермента

Ингибиторы ферментов По характеру действия ингибиторы могут быть обратимыми и необратимыми. В основе этого деления лежит прочность соединения ингибитора с ферментом. Необратимый ингибитор модифицирует молекулу фермента, в результате чего фермент полностью теряет свою активность, например, тяжелые металлы и мышьяк, или диизопропилфторфосфат. Обратимые ингибиторы подразделяются на конкурентные, неконкурентные и бесконкурентные. Конкурентный ингибитор конкурирует с субстратом за связывание с активным центром. Неконкурентный ингибитор связывается не с активным центром, а в каким либо иным участком фермента. Бесконкурентный ингибитор — это молекула, которая связывается только с фермент субстратным комп лексом и не может связаться со свободным ферментом.
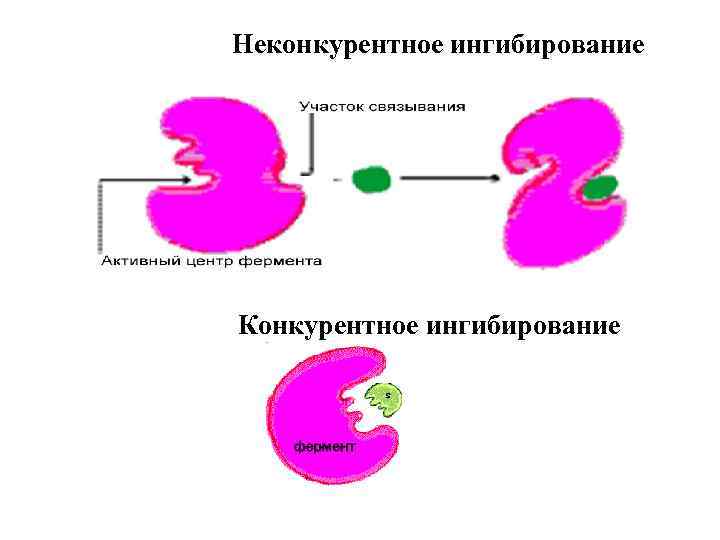
Неконкурентное ингибирование Конкурентное ингибирование
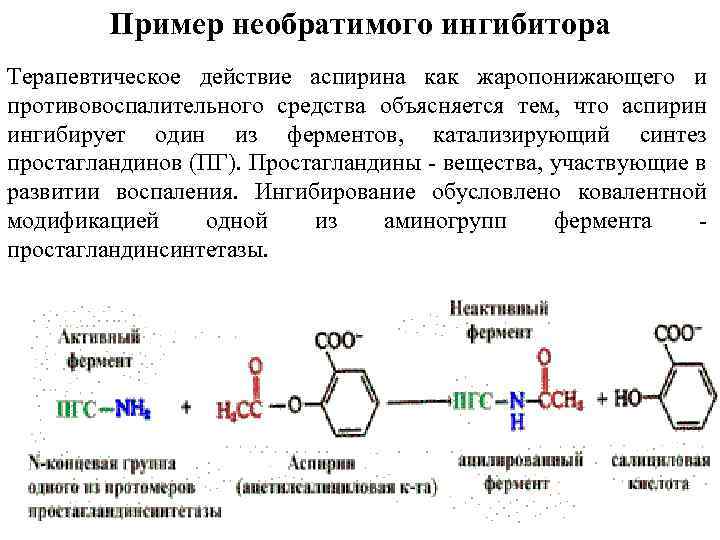
Пример необратимого ингибитора Терапевтическое действие аспирина как жаропонижающего и противовоспалительного средства объясняется тем, что аспирин ингибирует один из ферментов, катализирующий синтез простагландинов (ПГ). Простагландины вещества, участвующие в развитии воспаления. Ингибирование обусловлено ковалентной модификацией одной из аминогрупп фермента простагландинсинтетазы.
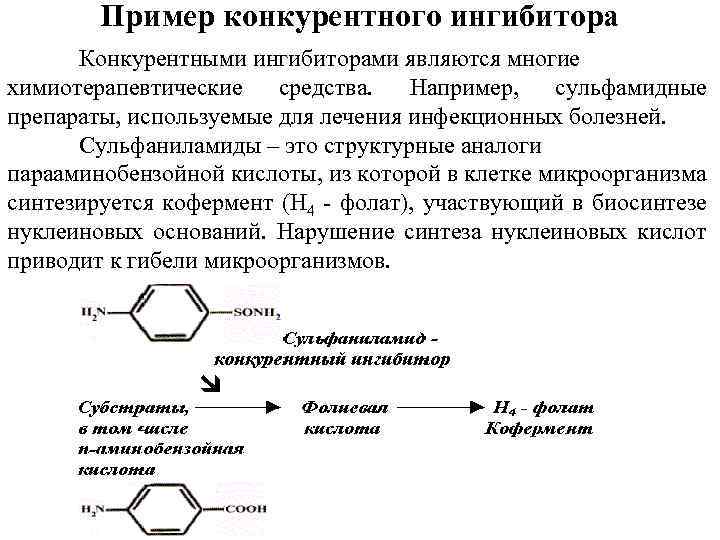
Пример конкурентного ингибитора Конкурентными ингибиторами являются многие химиотерапевтические средства. Например, сульфамидные препараты, используемые для лечения инфекционных болезней. Сульфаниламиды – это структурные аналоги парааминобензойной кислоты, из которой в клетке микроорганизма синтезируется кофермент (Н 4 фолат), участвующий в биосинтезе нуклеиновых оснований. Нарушение синтеза нуклеиновых кислот приводит к гибели микроорганизмов.
Lektsia_2.ppt