лекция 2 алканы алкены.ppt
- Количество слайдов: 31
 Лекция 2 Алканы и Алкены
Лекция 2 Алканы и Алкены
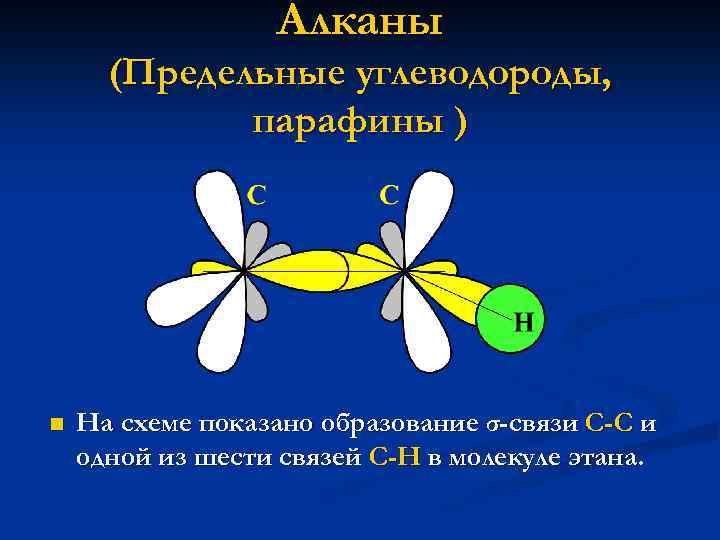 Алканы (Предельные углеводороды, парафины ) n На схеме показано образование σ-связи С-С и одной из шести связей С-Н в молекуле этана.
Алканы (Предельные углеводороды, парафины ) n На схеме показано образование σ-связи С-С и одной из шести связей С-Н в молекуле этана.
 Гомологический ряд n n Гомологический ряд - набор органических соединений отличающихся на группу -СН 2 -. Эта группа называется гомологической разницей. Общая брутто формула для алканов Сn. H 2 n+2 где n – целое положительное число. Систематические названия алканов строятся следующим образом: [Числительное][ан] мет ан (С 1), эт ан (С 2)пропн (С 3), бутан (С 4) пент (С 5) и ан ан а т. д.
Гомологический ряд n n Гомологический ряд - набор органических соединений отличающихся на группу -СН 2 -. Эта группа называется гомологической разницей. Общая брутто формула для алканов Сn. H 2 n+2 где n – целое положительное число. Систематические названия алканов строятся следующим образом: [Числительное][ан] мет ан (С 1), эт ан (С 2)пропн (С 3), бутан (С 4) пент (С 5) и ан ан а т. д.
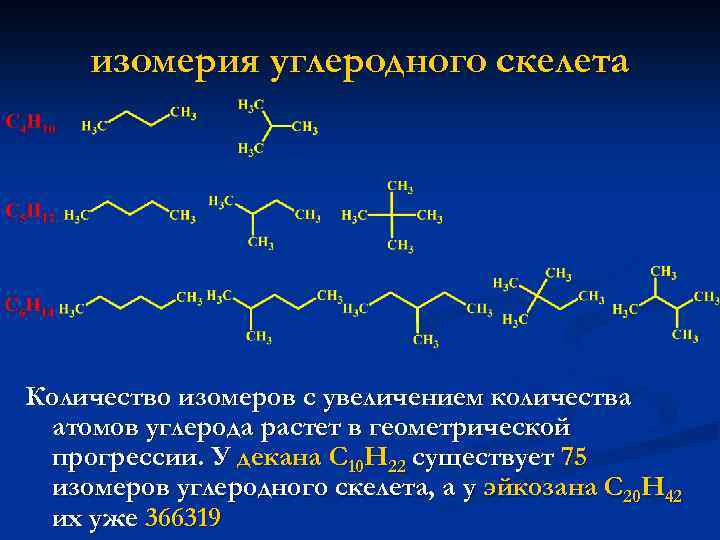 изомерия углеродного скелета Количество изомеров с увеличением количества атомов углерода растет в геометрической прогрессии. У декана С 10 Н 22 существует 75 изомеров углеродного скелета, а у эйкозана С 20 Н 42 их уже 366319
изомерия углеродного скелета Количество изомеров с увеличением количества атомов углерода растет в геометрической прогрессии. У декана С 10 Н 22 существует 75 изомеров углеродного скелета, а у эйкозана С 20 Н 42 их уже 366319
 Химические свойства алканов n Химические свойства алканов обусловлены в первую очередь высокой прочностью одинарной углеродной (83 ккал/моль) и углеродводородной (99 ккал/моль) связи.
Химические свойства алканов n Химические свойства алканов обусловлены в первую очередь высокой прочностью одинарной углеродной (83 ккал/моль) и углеродводородной (99 ккал/моль) связи.
 радикальное замещение (SR) Механизм радикального замещения цепной, радикал, генерируемый на стадии зарождения цепи, после ряда превращений снова высвобождается для следующего цикла. n На одну, полученную на стадии зарождения цепи, новую радикальную частицу образуется несколько сотен (иногда тысяч) молекул продукта реакции. n
радикальное замещение (SR) Механизм радикального замещения цепной, радикал, генерируемый на стадии зарождения цепи, после ряда превращений снова высвобождается для следующего цикла. n На одну, полученную на стадии зарождения цепи, новую радикальную частицу образуется несколько сотен (иногда тысяч) молекул продукта реакции. n
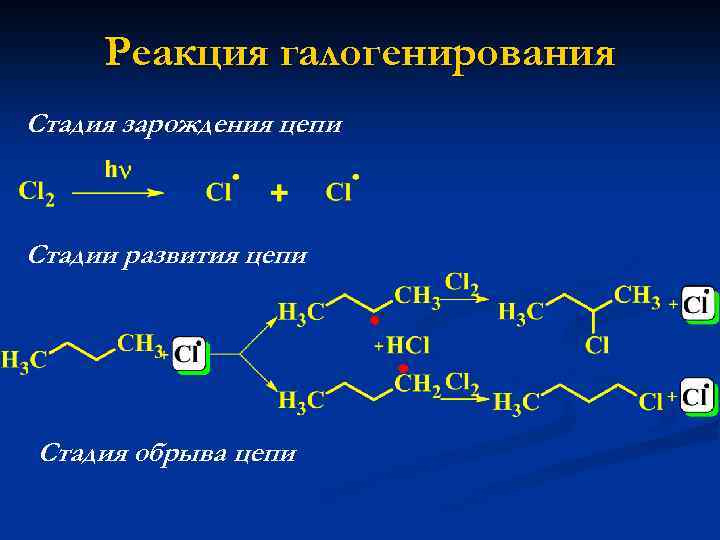 Реакция галогенирования Стадия зарождения цепи Стадии развития цепи Стадия обрыва цепи
Реакция галогенирования Стадия зарождения цепи Стадии развития цепи Стадия обрыва цепи
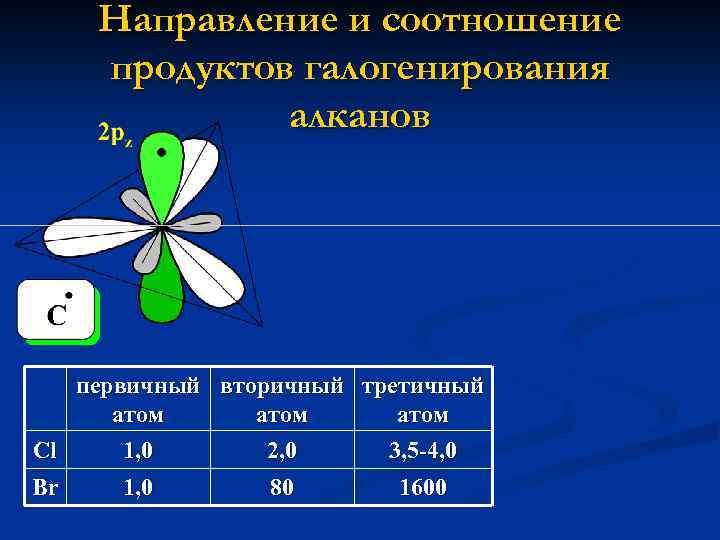 Направление и соотношение продуктов галогенирования алканов первичный вторичный третичный атом Cl 1, 0 2, 0 3, 5 -4, 0 Br 1, 0 80 1600
Направление и соотношение продуктов галогенирования алканов первичный вторичный третичный атом Cl 1, 0 2, 0 3, 5 -4, 0 Br 1, 0 80 1600
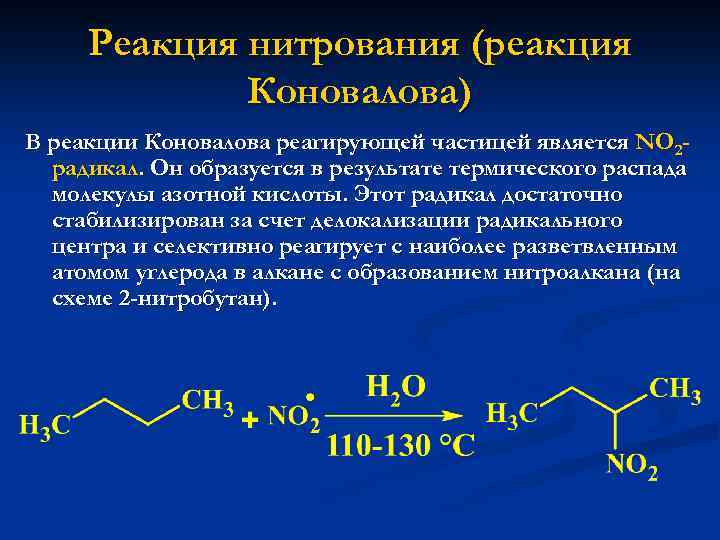 Реакция нитрования (реакция Коновалова) В реакции Коновалова реагирующей частицей является NO 2 радикал. Он образуется в результате термического распада молекулы азотной кислоты. Этот радикал достаточно стабилизирован за счет делокализации радикального центра и селективно реагирует с наиболее разветвленным атомом углерода в алкане с образованием нитроалкана (на схеме 2 -нитробутан).
Реакция нитрования (реакция Коновалова) В реакции Коновалова реагирующей частицей является NO 2 радикал. Он образуется в результате термического распада молекулы азотной кислоты. Этот радикал достаточно стабилизирован за счет делокализации радикального центра и селективно реагирует с наиболее разветвленным атомом углерода в алкане с образованием нитроалкана (на схеме 2 -нитробутан).
 Сульфохлорирование Сульфохлориды по этой схеме синтезируют в промышленности в больших количествах. Они являются исходными для производства синтетических моющих средств и других ПАВ (поверхностно активных веществ).
Сульфохлорирование Сульфохлориды по этой схеме синтезируют в промышленности в больших количествах. Они являются исходными для производства синтетических моющих средств и других ПАВ (поверхностно активных веществ).
 Алкены (олефины)
Алкены (олефины)
 Номенклатура: Названия строятся аналогично алканам, окончание –ЕН. После окончания цифрой указывается положение двойной связи в цепи с учетом нумерации. пример: СН 3 -СН=СН-СН 2 -СН 3 пентен-2
Номенклатура: Названия строятся аналогично алканам, окончание –ЕН. После окончания цифрой указывается положение двойной связи в цепи с учетом нумерации. пример: СН 3 -СН=СН-СН 2 -СН 3 пентен-2
 Методы получения алкенов n 1. Реакция элиминирования (Е) n а) элиминирование галогеноводородов из алкилгалогенидов протекает под действием органических или неорганических оснований (KOH, Na. OH, t-Bu. OK и т. п. ) в неводных полярных средах (например, в спирте). Водород, как правило, уходит от того атома углерода, где образуется наиболее стабильный карбоанион. n б) Элиминирование двух атомов галогенов расположенных у соседних атомов углерода (так называемых вицинальных ) протекает под действием активных двухвалентных металлов (Zn, Mg). n в) Элиминирование воды из спиртов протекает под действием водоотнимающих (дегидратирующих) средств – Al 2 O 3 H 2 SO 4 H 3 PO 4. Закономерности отщепления похожи на случай с элиминированием галогеноводородов. n г) Дегидрирование насыщенных углеводородов крекинг нефти) и (включая частичное гидрирование ацетиленовых углеводородов (алкинов).
Методы получения алкенов n 1. Реакция элиминирования (Е) n а) элиминирование галогеноводородов из алкилгалогенидов протекает под действием органических или неорганических оснований (KOH, Na. OH, t-Bu. OK и т. п. ) в неводных полярных средах (например, в спирте). Водород, как правило, уходит от того атома углерода, где образуется наиболее стабильный карбоанион. n б) Элиминирование двух атомов галогенов расположенных у соседних атомов углерода (так называемых вицинальных ) протекает под действием активных двухвалентных металлов (Zn, Mg). n в) Элиминирование воды из спиртов протекает под действием водоотнимающих (дегидратирующих) средств – Al 2 O 3 H 2 SO 4 H 3 PO 4. Закономерности отщепления похожи на случай с элиминированием галогеноводородов. n г) Дегидрирование насыщенных углеводородов крекинг нефти) и (включая частичное гидрирование ацетиленовых углеводородов (алкинов).
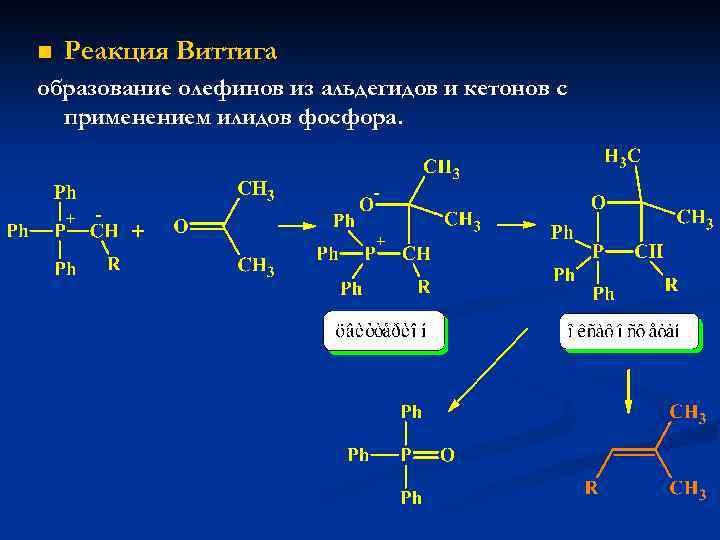 n Реакция Виттига образование олефинов из альдегидов и кетонов с применением илидов фосфора.
n Реакция Виттига образование олефинов из альдегидов и кетонов с применением илидов фосфора.
 Химические свойства алкенов n Химические свойства алкенов в большой степени связаны с наличием в их составе кратной связи. Прочность π-связи (145 -88=57 ккал/моль) меньше чем σ-связи. Поэтому, многие реакции с участием олефинов протекают по механизму присоединения с разрывом π-связи и образованием двух σсвязей.
Химические свойства алкенов n Химические свойства алкенов в большой степени связаны с наличием в их составе кратной связи. Прочность π-связи (145 -88=57 ккал/моль) меньше чем σ-связи. Поэтому, многие реакции с участием олефинов протекают по механизму присоединения с разрывом π-связи и образованием двух σсвязей.
 Реакция электрофильного присоединения (Ad. E) Богатые электронной плотностью πорбитали удалены от оси связи и легко доступны для взаимодействия. n Основным типом атакующей частицы будет электрофил. n n Электрофил представляет собой положительно заряженный ион (катион) или положительный конец диполя.
Реакция электрофильного присоединения (Ad. E) Богатые электронной плотностью πорбитали удалены от оси связи и легко доступны для взаимодействия. n Основным типом атакующей частицы будет электрофил. n n Электрофил представляет собой положительно заряженный ион (катион) или положительный конец диполя.
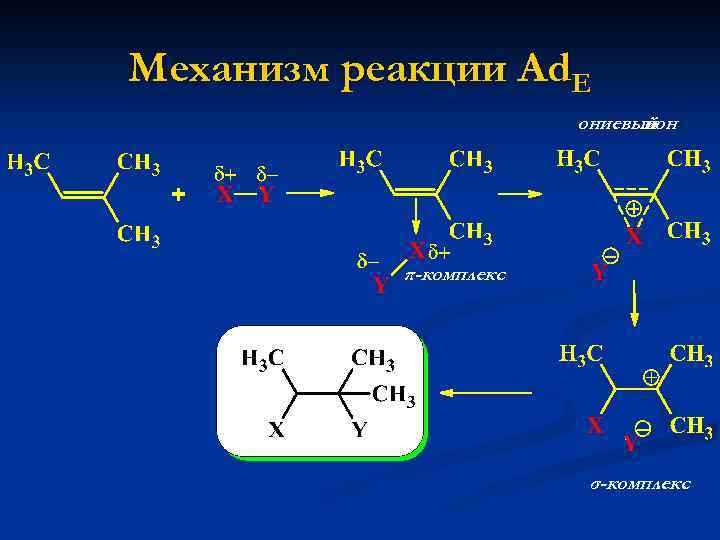 Механизм реакции Ad. E ониевый ион π-комплекс σ-комплекс
Механизм реакции Ad. E ониевый ион π-комплекс σ-комплекс
 n n Селективность Ad. E правило Марковникова Правило Марковникова в современном толковании Селективность электрофильного присоединения по кратной связи обусловлена раскрытием цикла ониевого иона с образованием σ-комплекса, содержащего наиболее стабилизированный (устойчивый) карбокатион. Электронное строение карбокатиона аналогично углеродному радикалу, с той только разницей, что на негибридизованной р-орбитали располагается катионный центр (формально, пустая электронная орбиталь).
n n Селективность Ad. E правило Марковникова Правило Марковникова в современном толковании Селективность электрофильного присоединения по кратной связи обусловлена раскрытием цикла ониевого иона с образованием σ-комплекса, содержащего наиболее стабилизированный (устойчивый) карбокатион. Электронное строение карбокатиона аналогично углеродному радикалу, с той только разницей, что на негибридизованной р-орбитали располагается катионный центр (формально, пустая электронная орбиталь).
 n n По механизму Ad. E присоединяются галогеноводороды (X=H, Y=Hal) с образованием алкилгалогенидов, галогены (X=Y=Cl, Br) с образованием вицинальных дигалогенидов, вода (X=H, Y=OH) с образованием спиртов, спирты (X=H, Y=OR) с образованием простых эфиров и многие другие реагенты. Электрофильное присоединение, как правило, д только один продукт – по правилу Марковникова.
n n По механизму Ad. E присоединяются галогеноводороды (X=H, Y=Hal) с образованием алкилгалогенидов, галогены (X=Y=Cl, Br) с образованием вицинальных дигалогенидов, вода (X=H, Y=OH) с образованием спиртов, спирты (X=H, Y=OR) с образованием простых эфиров и многие другие реагенты. Электрофильное присоединение, как правило, д только один продукт – по правилу Марковникова.
 Стабильность карбокатионов n n Стабильность карбокатионов (как и радикалов) связана с “индуктивным (I)” и “мезомерным (M)” электронными эффектами заместителей при катионном центре. Наличие соседних групп, проявляющих положительные электронные эффекты, стабилизирует карбокатионный центр за счет подачи электронной плотности и делокализации положительного заряда. Группы, проявляющие отрицательные электронные эффекты, наоборот, дестабилизируют катионный центр.
Стабильность карбокатионов n n Стабильность карбокатионов (как и радикалов) связана с “индуктивным (I)” и “мезомерным (M)” электронными эффектами заместителей при катионном центре. Наличие соседних групп, проявляющих положительные электронные эффекты, стабилизирует карбокатионный центр за счет подачи электронной плотности и делокализации положительного заряда. Группы, проявляющие отрицательные электронные эффекты, наоборот, дестабилизируют катионный центр.
 (I) индуктивный эффект n Электронное влияние, распространяющееся по σсвязи и связанное с разницей в электроотрицательности рассматриваемого атома углерода и атома (или группы атомов) заместителя. n Прямыми стрелками указывается направление смещения электронной плотности по σ-связи.
(I) индуктивный эффект n Электронное влияние, распространяющееся по σсвязи и связанное с разницей в электроотрицательности рассматриваемого атома углерода и атома (или группы атомов) заместителя. n Прямыми стрелками указывается направление смещения электронной плотности по σ-связи.
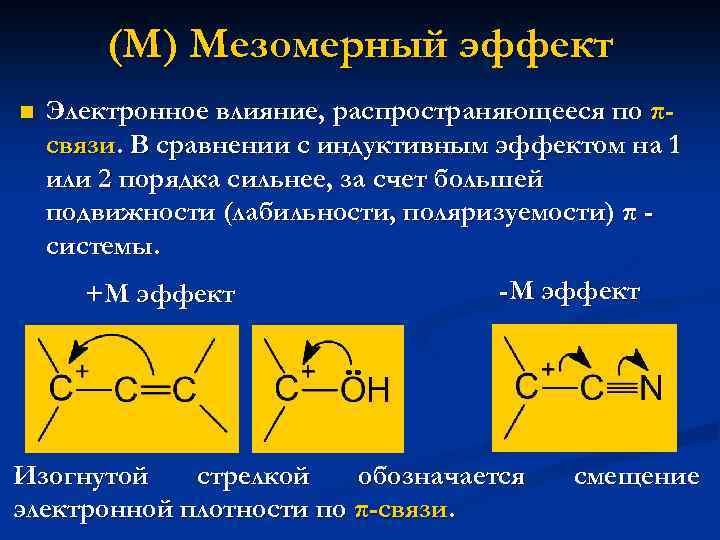 (М) Мезомерный эффект n Электронное влияние, распространяющееся по πсвязи. В сравнении с индуктивным эффектом на 1 или 2 порядка сильнее, за счет большей подвижности (лабильности, поляризуемости) π системы. +М эффект -М эффект Изогнутой стрелкой обозначается электронной плотности по π-связи. смещение
(М) Мезомерный эффект n Электронное влияние, распространяющееся по πсвязи. В сравнении с индуктивным эффектом на 1 или 2 порядка сильнее, за счет большей подвижности (лабильности, поляризуемости) π системы. +М эффект -М эффект Изогнутой стрелкой обозначается электронной плотности по π-связи. смещение
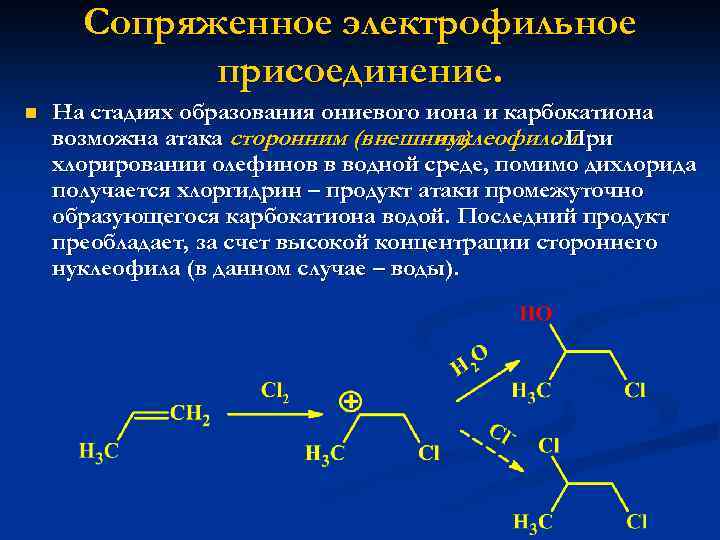 Сопряженное электрофильное присоединение. n На стадиях образования ониевого иона и карбокатиона возможна атака сторонним (внешним) нуклеофилом. При хлорировании олефинов в водной среде, помимо дихлорида получается хлоргидрин – продукт атаки промежуточно образующегося карбокатиона водой. Последний продукт преобладает, за счет высокой концентрации стороннего нуклеофила (в данном случае – воды).
Сопряженное электрофильное присоединение. n На стадиях образования ониевого иона и карбокатиона возможна атака сторонним (внешним) нуклеофилом. При хлорировании олефинов в водной среде, помимо дихлорида получается хлоргидрин – продукт атаки промежуточно образующегося карбокатиона водой. Последний продукт преобладает, за счет высокой концентрации стороннего нуклеофила (в данном случае – воды).
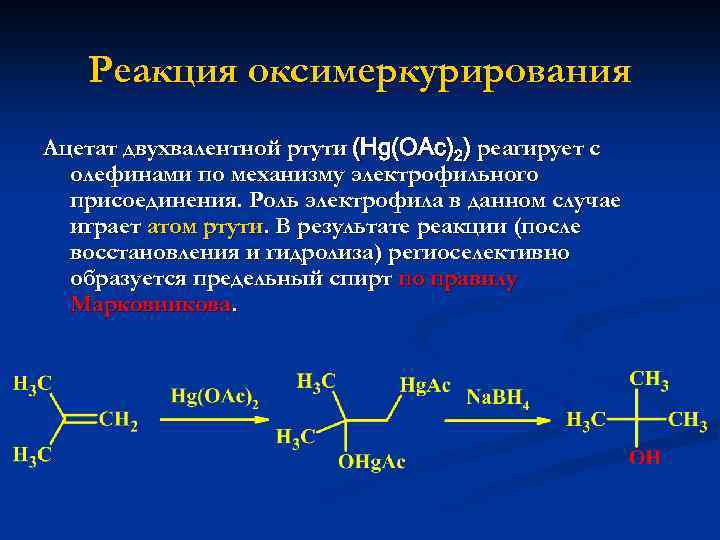 Реакция оксимеркурирования Ацетат двухвалентной ртути (Hg(OAc)2) реагирует с олефинами по механизму электрофильного присоединения. Роль электрофила в данном случае играет атом ртути. В результате реакции (после восстановления и гидролиза) региоселективно образуется предельный спирт по правилу Марковникова.
Реакция оксимеркурирования Ацетат двухвалентной ртути (Hg(OAc)2) реагирует с олефинами по механизму электрофильного присоединения. Роль электрофила в данном случае играет атом ртути. В результате реакции (после восстановления и гидролиза) региоселективно образуется предельный спирт по правилу Марковникова.
 Реакция гидроборирования Соединения содержащие связь В-Н способны присоединяться по кратной связи с образованием борорганических соединений. Окислительный гидролиз этих производных (водная Н 2 О 2) приводит к образованию предельных спиртов. Присоединение протекает против правила Марковникова (Получается наименее разветвленный карбинол).
Реакция гидроборирования Соединения содержащие связь В-Н способны присоединяться по кратной связи с образованием борорганических соединений. Окислительный гидролиз этих производных (водная Н 2 О 2) приводит к образованию предельных спиртов. Присоединение протекает против правила Марковникова (Получается наименее разветвленный карбинол).
 Реакция свободнорадикального присоединения (Ad. R) n n n Присоединение бромистого водорода к олефинам в присутствии пероксидов приводит к образованию продукта против правила Марковникова ( «Антимарковниковское присоединение» ). Под действием пероксида, связь H-Br в молекуле бромистого водорода подвергается гомолитическому разрыву и образуется бром-радикал. Радикальные частицы проявляют свойства электрофилов и поэтому способны атаковать кратную связь алкена. В данном случае первым присоединяется бром-радикал (устойчивость образующегося промежуточного радикала подч тем же правилам, что карбокатионато, формально, и ), бромоводород присоединяется против правила Марковникова, хотя механизм взаимодействия, в общем, очень близок.
Реакция свободнорадикального присоединения (Ad. R) n n n Присоединение бромистого водорода к олефинам в присутствии пероксидов приводит к образованию продукта против правила Марковникова ( «Антимарковниковское присоединение» ). Под действием пероксида, связь H-Br в молекуле бромистого водорода подвергается гомолитическому разрыву и образуется бром-радикал. Радикальные частицы проявляют свойства электрофилов и поэтому способны атаковать кратную связь алкена. В данном случае первым присоединяется бром-радикал (устойчивость образующегося промежуточного радикала подч тем же правилам, что карбокатионато, формально, и ), бромоводород присоединяется против правила Марковникова, хотя механизм взаимодействия, в общем, очень близок.
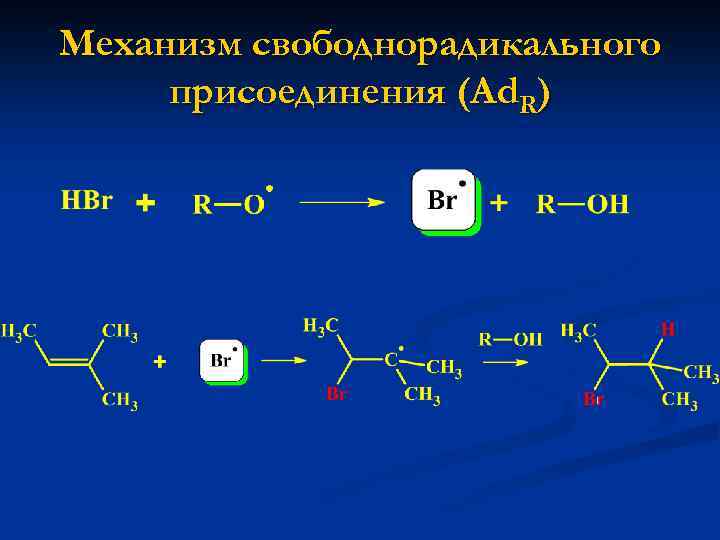 Механизм свободнорадикального присоединения (Ad. R)
Механизм свободнорадикального присоединения (Ad. R)
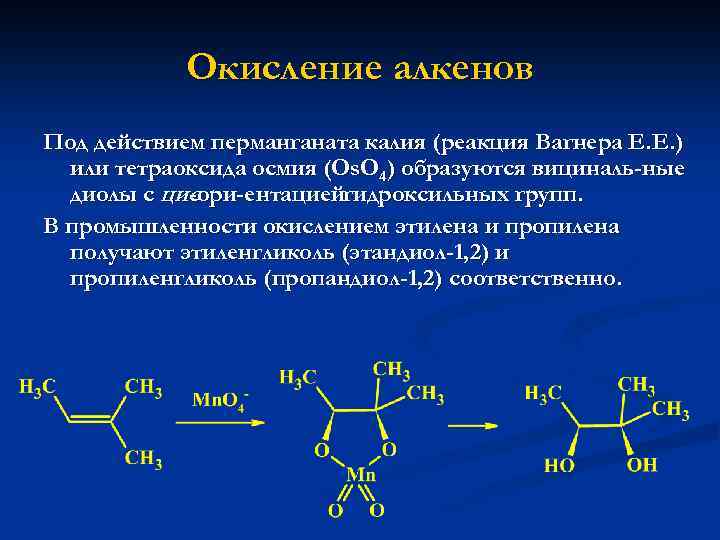 Окисление алкенов Под действием перманганата калия (реакция Вагнера Е. Е. ) или тетраоксида осмия (Os. O 4) образуются вициналь ные диолы с цисори ентациейгидроксильных групп. -ори ентацией В промышленности окислением этилена и пропилена получают этиленгликоль (этандиол-1, 2) и пропиленгликоль (пропандиол-1, 2) соответственно.
Окисление алкенов Под действием перманганата калия (реакция Вагнера Е. Е. ) или тетраоксида осмия (Os. O 4) образуются вициналь ные диолы с цисори ентациейгидроксильных групп. -ори ентацией В промышленности окислением этилена и пропилена получают этиленгликоль (этандиол-1, 2) и пропиленгликоль (пропандиол-1, 2) соответственно.
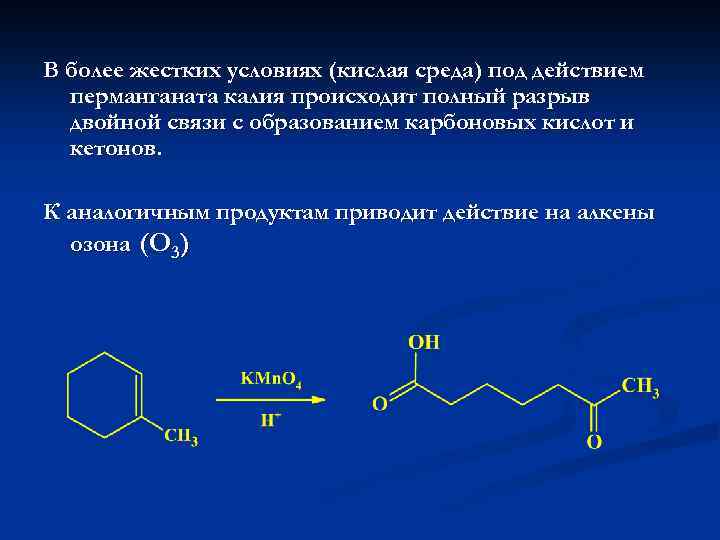 В более жестких условиях (кислая среда) под действием перманганата калия происходит полный разрыв двойной связи с образованием карбоновых кислот и кетонов. К аналогичным продуктам приводит действие на алкены озона (О 3)
В более жестких условиях (кислая среда) под действием перманганата калия происходит полный разрыв двойной связи с образованием карбоновых кислот и кетонов. К аналогичным продуктам приводит действие на алкены озона (О 3)
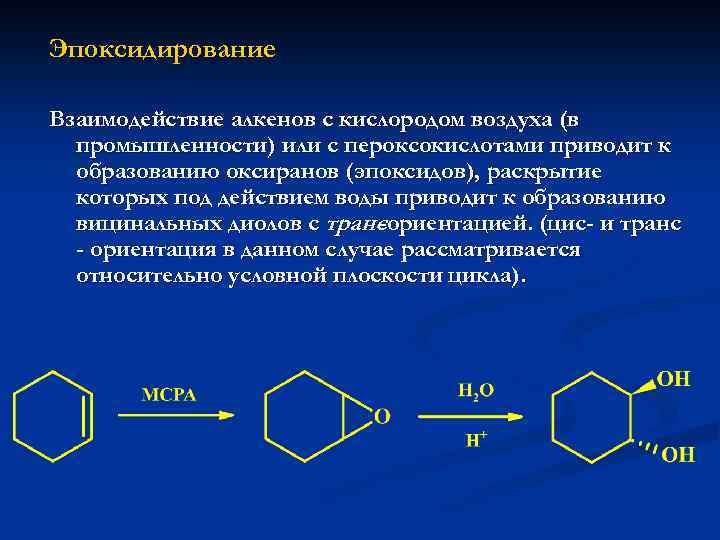 Эпоксидирование Взаимодействие алкенов с кислородом воздуха (в промышленности) или с пероксокислотами приводит к образованию оксиранов (эпоксидов), раскрытие которых под действием воды приводит к образованию вицинальных диолов с транс -ориентацией. (цис- и транс - ориентация в данном случае рассматривается относительно условной плоскости цикла).
Эпоксидирование Взаимодействие алкенов с кислородом воздуха (в промышленности) или с пероксокислотами приводит к образованию оксиранов (эпоксидов), раскрытие которых под действием воды приводит к образованию вицинальных диолов с транс -ориентацией. (цис- и транс - ориентация в данном случае рассматривается относительно условной плоскости цикла).
![[2+2]-Циклоприсоединение n n Многие олефины способны вступать в реакцию [2+2]циклоприсоединения друг с другом или [2+2]-Циклоприсоединение n n Многие олефины способны вступать в реакцию [2+2]циклоприсоединения друг с другом или](https://present5.com/presentation/142257568_437577253/image-31.jpg) [2+2]-Циклоприсоединение n n Многие олефины способны вступать в реакцию [2+2]циклоприсоединения друг с другом или сами с собой. Под действием света (как правило УФ) из двух молекул алкена образуется фрагмент циклобутана Этот процесс используют не только как один из немногих удобных методов сборки циклобутанового ядра.
[2+2]-Циклоприсоединение n n Многие олефины способны вступать в реакцию [2+2]циклоприсоединения друг с другом или сами с собой. Под действием света (как правило УФ) из двух молекул алкена образуется фрагмент циклобутана Этот процесс используют не только как один из немногих удобных методов сборки циклобутанового ядра.


