Презентация_Лекция_02а_Белки.ppt
- Количество слайдов: 15

Лекция 2 а Белки 1. Физико-химические свойства белков l l l кислотно-основные свойства белков растворимость белков денатурация белков 2. Классификация белков l l фибриллярные и глобулярные белки простые и сложные белки 3. Функции белков

Лекция 2 а Белки Кислотно-основные свойства белков l Подобно аминокислотам, белки сочетают в себе, как основные, так и кислотные свойства, т. е. являются амфотерными веществами. l Амфотерные свойства белковых молекул обусловлены наличием в их структуре заряженных функциональных групп: l - отрицательно заряженных остатков глутаминовой и аспарагиновой кислот; - положительно заряженных остатков аргинина, лизина и гистидина; –NH 2 и –COOH группы на концах каждой полипептидной цепи белка. l l

Лекция 2 а Белки Растворимость белков 1. Каждый белок обладает определённой растворимостью, зависящей от природы самого белка и состава растворителя. 2. Растворимость белка зависит от: а) аминокислотного состава, который определяет заряд белковой молекулы: чем больше белок содержит полярных и заряженных аминокислотных радикалов, тем выше его растворимость; б) наличие гидратного слоя (полярные и заряженные радикалы аминокислот связывают диполи воды, которые и образуют вокруг молекулы белка гидратный слой). 3. Добавление к водному раствору белка водоотнимающих веществ (спирт, ацетон) вызывает разрушение гидратного слоя и белок выпадает в осадок.
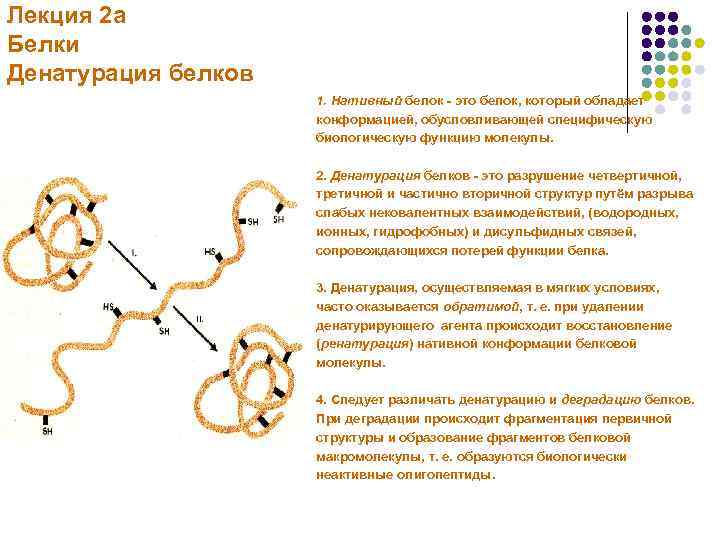
Лекция 2 а Белки Денатурация белков 1. Нативный белок - это белок, который обладает конформацией, обусловливающей специфическую биологическую функцию молекулы. 2. Денатурация белков - это разрушение четвертичной, третичной и частично вторичной структур путём разрыва слабых нековалентных взаимодействий, (водородных, ионных, гидрофобных) и дисульфидных связей, сопровождающихся потерей функции белка. 3. Денатурация, осуществляемая в мягких условиях, часто оказывается обратимой, т. е. при удалении денатурирующего агента происходит восстановление (ренатурация) нативной конформации белковой молекулы. 4. Следует различать денатурацию и деградацию белков. При деградации происходит фрагментация первичной структуры и образование фрагментов белковой макромолекулы, т. е. образуются биологически неактивные олигопептиды.
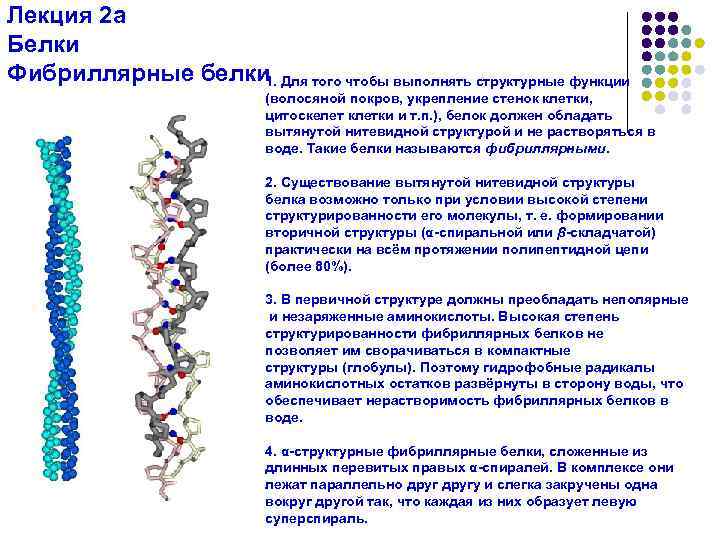
Лекция 2 а Белки Фибриллярные белки Для того чтобы выполнять структурные функции 1. (волосяной покров, укрепление стенок клетки, цитоскелет клетки и т. п. ), белок должен обладать вытянутой нитевидной структурой и не растворяться в воде. Такие белки называются фибриллярными. 2. Существование вытянутой нитевидной структуры белка возможно только при условии высокой степени структурированности его молекулы, т. е. формировании вторичной структуры (α-спиральной или β-складчатой) практически на всём протяжении полипептидной цепи (более 80%). 3. В первичной структуре должны преобладать неполярные и незаряженные аминокислоты. Высокая степень структурированности фибриллярных белков не позволяет им сворачиваться в компактные структуры (глобулы). Поэтому гидрофобные радикалы аминокислотных остатков развёрнуты в сторону воды, что обеспечивает нерастворимость фибриллярных белков в воде. 4. α-структурные фибриллярные белки, сложенные из длинных перевитых правых α-спиралей. В комплексе они лежат параллельно другу и слегка закручены одна вокруг другой так, что каждая из них образует левую суперспираль.
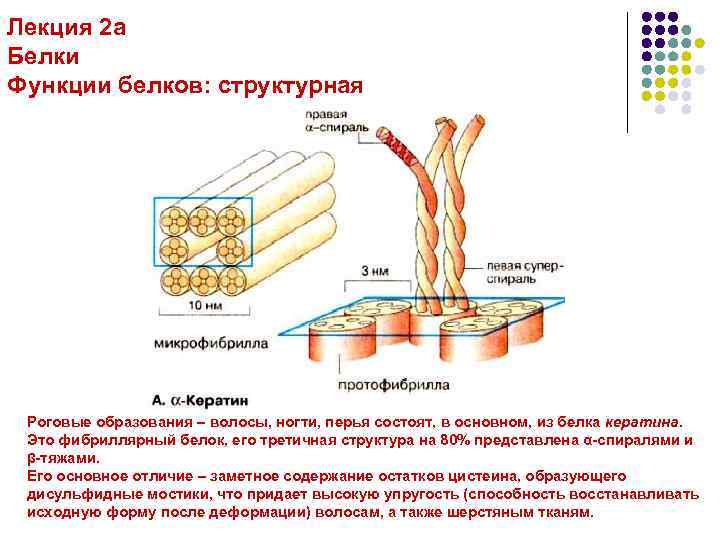
Лекция 2 а Белки Функции белков: структурная Роговые образования – волосы, ногти, перья состоят, в основном, из белка кератина. Это фибриллярный белок, его третичная структура на 80% представлена α-спиралями и β-тяжами. Его основное отличие – заметное содержание остатков цистеина, образующего дисульфидные мостики, что придает высокую упругость (способность восстанавливать исходную форму после деформации) волосам, а также шерстяным тканям.

Лекция 2 а Белки Фибриллярные белки: коллаген Надмолекулярная структура фибриллярного белка коллагена 1. Молекула коллагена построена из трёх полипептидных цепей. 2. Каждая полипептидная цепь содержит около 1000 аминокислотных остатков (35% - глицин, 21% - пролин или оксипролин, 11% - аланин. 3. Каждая полипептидная цепь имеет конформацию плотной (3 аминокислотных остатка на виток) левозакрученной спирали (спирализация 1 -го порядка). 4. Эти три спирали перевиты друг с другом, в результате чего образуется тройная суперспираль коллагена (спирализация 2 -го порядка), которая принципиально отличается от α‑спирали. Это очень слабо закрученная (один оборот на 1000 Å) правая спираль. 5. Между спиралями 1 -го порядка за счёт пептидных групп образуются водородные связи. 6. На примере коллагена можно видеть, что в образовании фибриллярных белков могут участвовать как α-спирали, так и β-структуры.

Лекция 2 а Белки Глобулярные белки: рибонуклеаза А 1. Для осуществления каталитической (ферментативной) функции белок должен связываться с трехмерным субстратом, т. е. место связывания в молекуле белка, должно быть трехмерным. Это возможно только при условии, что сам белок имеет трехмерную третичную (глобулярную) структуру. Структура рибонуклеазы А представлена одной цепью, содержащей 128 аминокислотных остатков), и построена преимущественно из b-слоёв. Основные принципы формирования третичной структуры: S–S-мостики (4 мостика) вместе с большим числом водородных связей (72 связи) служат каркасом молекулы и скрепляют структуру в плотную глобулу. 2. Глобулярная структура обеспечивает растворимость белков в воде, так как большинство реакций протекает в цитоплазме клетки. Действительно, гидрофобные радикалы аминокислотных остатков могут быть спрятаны внутрь глобулы, а в воду экспонированы гидрофильные остатки. 3. Для обеспечения компактной трехмерной структуры белок должен обладать элементами вторичной структуры небольшой протяженности, соединенных неструктурированными участками полипептидной цепи. Эти участки позволяют белку сворачиваться в компактную глобулу.
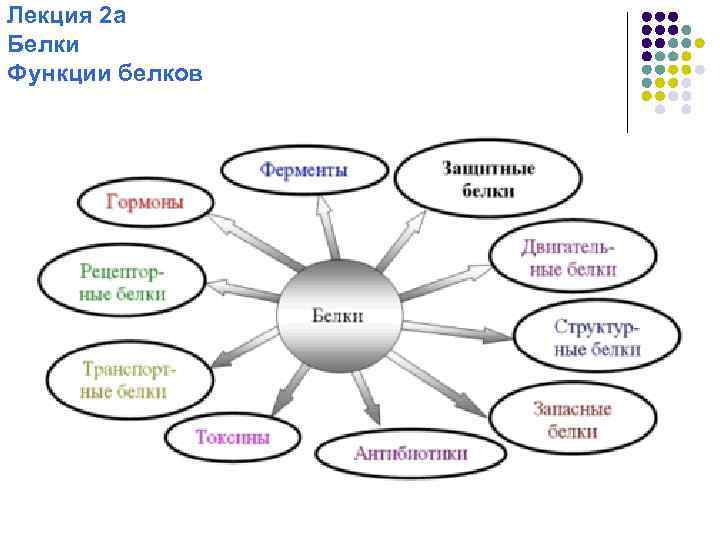
Лекция 2 а Белки Функции белков

Лекция 2 а Белки Функции белков: запасающая Структура альбумина куриного яйца Простыми белками называются белки, которые при гидролизе дают только аминокислоты. Пример простого белка глобулярной структуры – альбумин куриного яйца. Выполняет запасающую (питательную) функцию. Полимерная цепь альбумина собрана, в основном, из аланина, аспаргиновой кислоты, глицина, и цистеина, чередующихся в определенном порядке. Благодаря повышенному содержанию аспарагиновой кислоты, этот белок хорошо растворим в воде. Третичная структура содержит α-спирали, соединенные одиночными цепями.
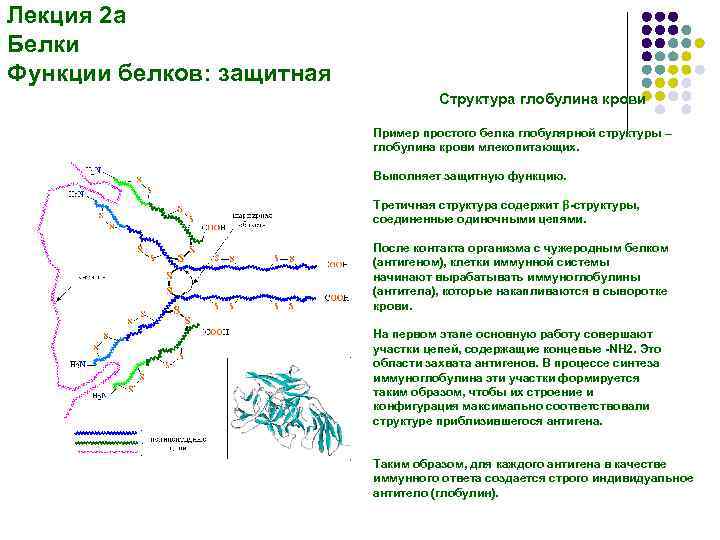
Лекция 2 а Белки Функции белков: защитная Структура глобулина крови Пример простого белка глобулярной структуры – глобулина крови млекопитающих. Выполняет защитную функцию. Третичная структура содержит β-структуры, соединенные одиночными цепями. После контакта организма с чужеродным белком (антигеном), клетки иммунной системы начинают вырабатывать иммуноглобулины (антитела), которые накапливаются в сыворотке крови. На первом этапе основную работу совершают участки цепей, содержащие концевые -NH 2. Это области захвата антигенов. В процессе синтеза иммуноглобулина эти участки формируется таким образом, чтобы их строение и конфигурация максимально соответствовали структуре приблизившегося антигена. Таким образом, для каждого антигена в качестве иммунного ответа создается строго индивидуальное антитело (глобулин).
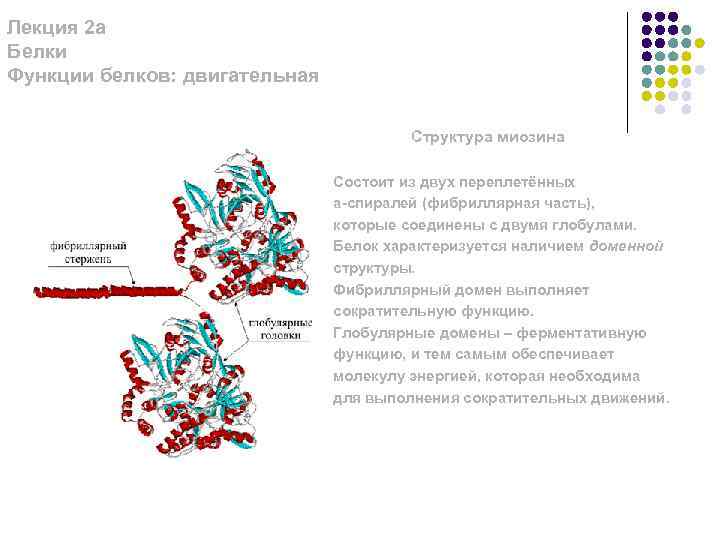
Лекция 2 а Белки Функции белков: двигательная Структура миозина Состоит из двух переплетённых a-спиралей (фибриллярная часть), которые соединены с двумя глобулами. Белок характеризуется наличием доменной структуры. Фибриллярный домен выполняет сократительную функцию. Глобулярные домены – ферментативную функцию, и тем самым обеспечивает молекулу энергией, которая необходима для выполнения сократительных движений.
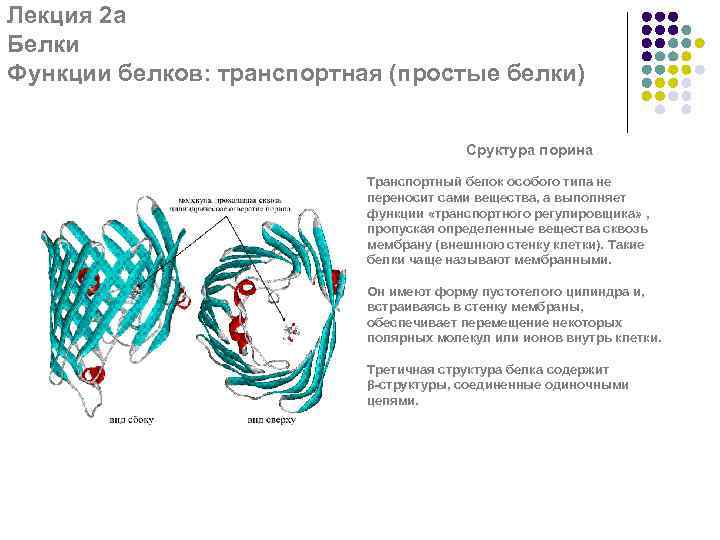
Лекция 2 а Белки Функции белков: транспортная (простые белки) Сруктура порина Транспортный белок особого типа не переносит сами вещества, а выполняет функции «транспортного регулировщика» , пропуская определенные вещества сквозь мембрану (внешнюю стенку клетки). Такие белки чаще называют мембранными. Он имеют форму пустотелого цилиндра и, встраиваясь в стенку мембраны, обеспечивает перемещение некоторых полярных молекул или ионов внутрь клетки. Третичная структура белка содержит β-структуры, соединенные одиночными цепями.

Лекция 2 а Белки Функция белков: транспортная (сложные белки) Структура гемоглобина Состоит из четырех субъединиц: двух α-субъединиц, содержащих по 141 остатку аминокислот; двух β-субъединиц, содержащих по 146 остатков аминокислот. Субъединицы уложены приблизительно в виде тетраэдра. С каждой субъединицей связана одна молекула гема. Гем представляет собой плоскую структуру, состоящую их четырёх пиррольных колец, в центре координации которых находится атом железа. Атом Fe связан в порфирине с двумя атомами N химическими связями, и с двумя другими – координационными связями (обозначены пунктиром). Основное «достоинство» гемоглобина состоит в том, что присоединение кислорода и последующее его отщепление при передаче различным тканям и органам проходит быстро. Вторая функция гемоглобина – перенос выдыхаемого СО 2, но в процессе временного связывания углекислоты участвует не атом железа, а -NH 2 группы белка.
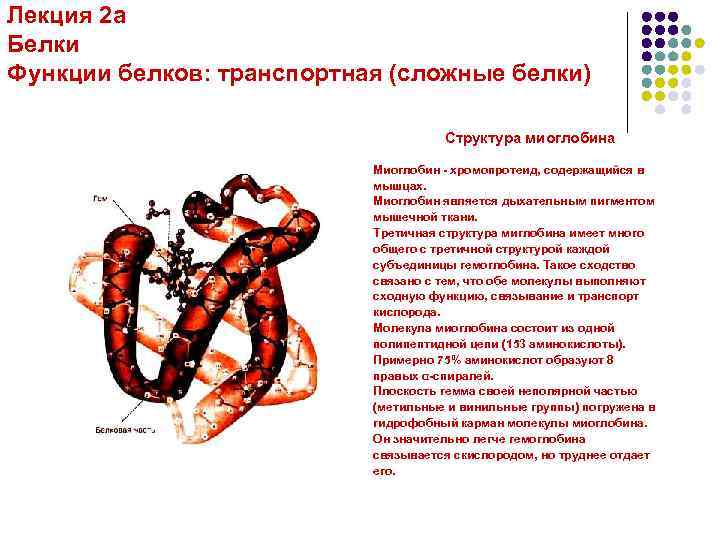
Лекция 2 а Белки Функции белков: транспортная (сложные белки) Структура миоглобина Миоглобин - хромопротеид, содержащийся в мышцах. Миоглобин является дыхательным пигментом мышечной ткани. Третичная структура миглобина имеет много общего с третичной структурой каждой субъединицы гемоглобина. Такое сходство связано с тем, что обе молекулы выполняют сходную функцию, связывание и транспорт кислорода. Молекула миоглобина состоит из одной полипептидной цепи (153 аминокислоты). Примерно 75% аминокислот образуют 8 правых α-спиралей. Плоскость гемма своей неполярной частью (метильные и винильные группы) погружена в гидрофобный карман молекулы миоглобина. Он значительно легче гемоглобина связывается скислородом, но труднее отдает его.
Презентация_Лекция_02а_Белки.ppt