Л_02+03-SPA-Основные характеристики кат-ров.ppt
- Количество слайдов: 56
 Лекция 2 -3 3. Основные характеристики катализатора. Их зависимость от метода его приготовления. 3. 1. Удельная каталитическая активность однофазных и многофазных катализаторов 3. 2. Селективность 3. 3. Текстурные характеристики катализатора 3. 3. 1. Пористая структура катализатора и кинетика реакций 3. 3. 2. Основные механизмы изменения удельной поверхности и пористости 3. 4. Механическая прочность катализатора 3. 5. Устойчивость катализатора к дезактивации 3. 5. 1. Термическая стабильность. Текстурные и структурные промоторы 3. 5. 2. Устойчивость к каталитическим ядам 3. 6. Гидродинамические характеристики катализатора
Лекция 2 -3 3. Основные характеристики катализатора. Их зависимость от метода его приготовления. 3. 1. Удельная каталитическая активность однофазных и многофазных катализаторов 3. 2. Селективность 3. 3. Текстурные характеристики катализатора 3. 3. 1. Пористая структура катализатора и кинетика реакций 3. 3. 2. Основные механизмы изменения удельной поверхности и пористости 3. 4. Механическая прочность катализатора 3. 5. Устойчивость катализатора к дезактивации 3. 5. 1. Термическая стабильность. Текстурные и структурные промоторы 3. 5. 2. Устойчивость к каталитическим ядам 3. 6. Гидродинамические характеристики катализатора
 Требования к свойствам катализаторов § Эффективный промышленный катализатор должен обладать следующими характеристиками: Высокой каталитической активностью и селективностью § Достаточно развитой удельной поверхностью § Оптимальной пористой структурой, обеспечивающей максимальное § Достаточной механической прочностью использование внутренней поверхности § Высокой термической стабильностью, в значительной степени определяющей срок службы катализатора § Устойчивостью к каталитическим ядам и другим химическим воздействиям, вызывающим § Оптимальными гидродинамическими дезактивацию характеристиками § Низкой себестоимостью (в совокупности с затратами на технологическое оформление
Требования к свойствам катализаторов § Эффективный промышленный катализатор должен обладать следующими характеристиками: Высокой каталитической активностью и селективностью § Достаточно развитой удельной поверхностью § Оптимальной пористой структурой, обеспечивающей максимальное § Достаточной механической прочностью использование внутренней поверхности § Высокой термической стабильностью, в значительной степени определяющей срок службы катализатора § Устойчивостью к каталитическим ядам и другим химическим воздействиям, вызывающим § Оптимальными гидродинамическими дезактивацию характеристиками § Низкой себестоимостью (в совокупности с затратами на технологическое оформление
 При разработке теории приготовления катализатора необходимо ответить на вопросы: § какие особенности катализатора, кроме химического состава, предопределяют его эксплуатационные качества, § каковы оптимальные значения этих характеристик (или оптимальное сочетание их значений), необходимые для достижения высокой эффективности катализатора в данной реакции, § каким образом можно варьировать эти свойства катализатора в ходе его приготовления для достижения их оптимальных значений
При разработке теории приготовления катализатора необходимо ответить на вопросы: § какие особенности катализатора, кроме химического состава, предопределяют его эксплуатационные качества, § каковы оптимальные значения этих характеристик (или оптимальное сочетание их значений), необходимые для достижения высокой эффективности катализатора в данной реакции, § каким образом можно варьировать эти свойства катализатора в ходе его приготовления для достижения их оптимальных значений
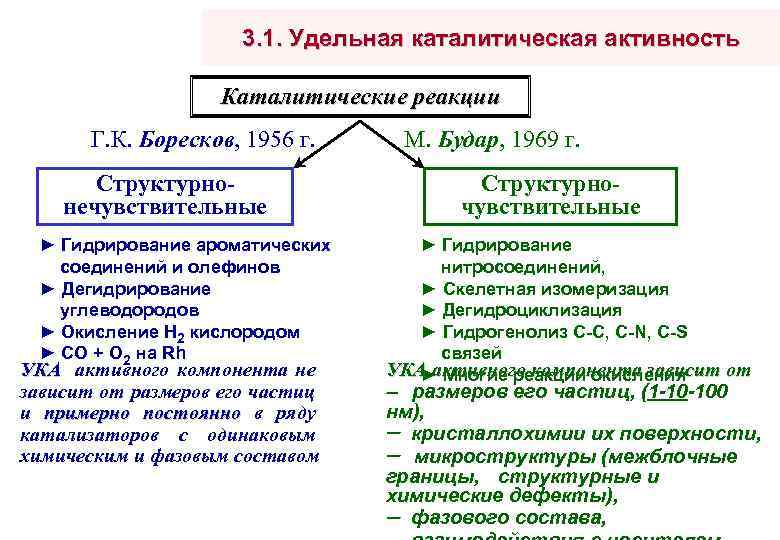 3. 1. Удельная каталитическая активность Каталитические реакции Г. К. Боресков, 1956 г. Структурнонечувствительные ► Гидрирование ароматических соединений и олефинов ► Дегидрирование углеводородов ► Окисление H 2 кислородом ► CO + O 2 на Rh УКА активного компонента не зависит от размеров его частиц и примерно постоянно в ряду катализаторов с одинаковым химическим и фазовым составом М. Будар, 1969 г. Структурночувствительные ► Гидрирование нитросоединений, ► Скелетная изомеризация ► Дегидроциклизация ► Гидрогенолиз C-C, C-N, C-S связей УКА активного компонента зависит от ► Многие реакции окисления размеров его частиц, (1 -10 -100 нм), кристаллохимии их поверхности, микроструктуры (межблочные границы, структурные и химические дефекты), фазового состава,
3. 1. Удельная каталитическая активность Каталитические реакции Г. К. Боресков, 1956 г. Структурнонечувствительные ► Гидрирование ароматических соединений и олефинов ► Дегидрирование углеводородов ► Окисление H 2 кислородом ► CO + O 2 на Rh УКА активного компонента не зависит от размеров его частиц и примерно постоянно в ряду катализаторов с одинаковым химическим и фазовым составом М. Будар, 1969 г. Структурночувствительные ► Гидрирование нитросоединений, ► Скелетная изомеризация ► Дегидроциклизация ► Гидрогенолиз C-C, C-N, C-S связей УКА активного компонента зависит от ► Многие реакции окисления размеров его частиц, (1 -10 -100 нм), кристаллохимии их поверхности, микроструктуры (межблочные границы, структурные и химические дефекты), фазового состава,
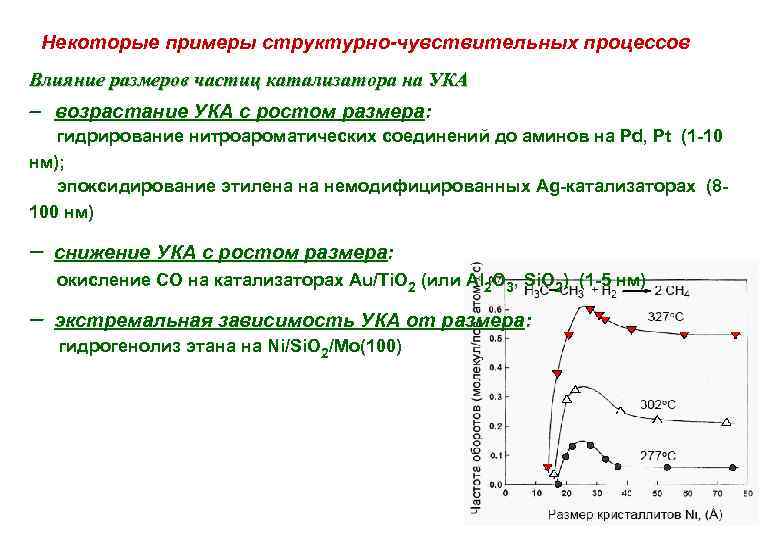 Некоторые примеры структурно-чувствительных процессов Влияние размеров частиц катализатора на УКА возрастание УКА с ростом размера: гидрирование нитроароматических соединений до аминов на Pd, Pt (1 -10 нм); эпоксидирование этилена на немодифицированных Ag-катализаторах (8100 нм) снижение УКА с ростом размера: окисление CO на катализаторах Au/Ti. O 2 (или Al 2 O 3, Si. O 2) (1 -5 нм) экстремальная зависимость УКА от размера: гидрогенолиз этана на Ni/Si. O 2/Mo(100)
Некоторые примеры структурно-чувствительных процессов Влияние размеров частиц катализатора на УКА возрастание УКА с ростом размера: гидрирование нитроароматических соединений до аминов на Pd, Pt (1 -10 нм); эпоксидирование этилена на немодифицированных Ag-катализаторах (8100 нм) снижение УКА с ростом размера: окисление CO на катализаторах Au/Ti. O 2 (или Al 2 O 3, Si. O 2) (1 -5 нм) экстремальная зависимость УКА от размера: гидрогенолиз этана на Ni/Si. O 2/Mo(100)
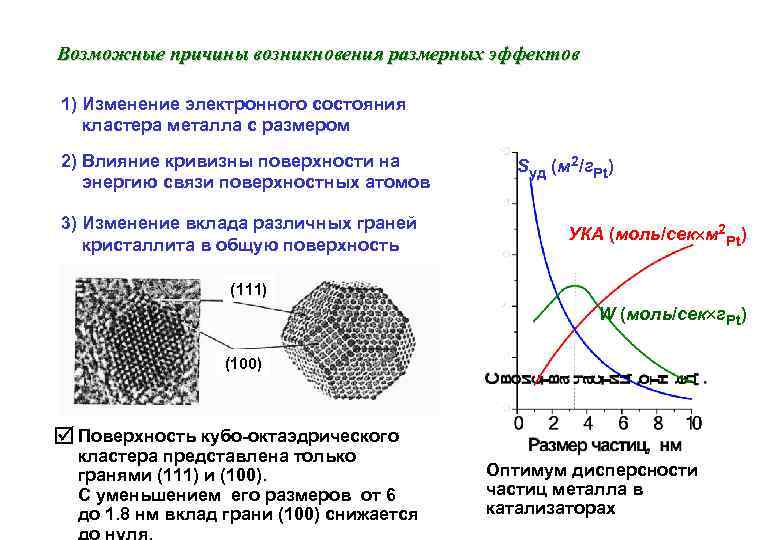 Возможные причины возникновения размерных эффектов 1) Изменение электронного состояния кластера металла с размером 2) Влияние кривизны поверхности на энергию связи поверхностных атомов 3) Изменение вклада различных граней кристаллита в общую поверхность Sуд (м 2/г. Pt) УКА (моль/сек м 2 Pt) (111) W (моль/сек г. Pt) (100) Поверхность кубо-октаэдрического кластера представлена только гранями (111) и (100). С уменьшением его размеров от 6 до 1. 8 нм вклад грани (100) снижается до нуля. Оптимум дисперсности частиц металла в катализаторах
Возможные причины возникновения размерных эффектов 1) Изменение электронного состояния кластера металла с размером 2) Влияние кривизны поверхности на энергию связи поверхностных атомов 3) Изменение вклада различных граней кристаллита в общую поверхность Sуд (м 2/г. Pt) УКА (моль/сек м 2 Pt) (111) W (моль/сек г. Pt) (100) Поверхность кубо-октаэдрического кластера представлена только гранями (111) и (100). С уменьшением его размеров от 6 до 1. 8 нм вклад грани (100) снижается до нуля. Оптимум дисперсности частиц металла в катализаторах
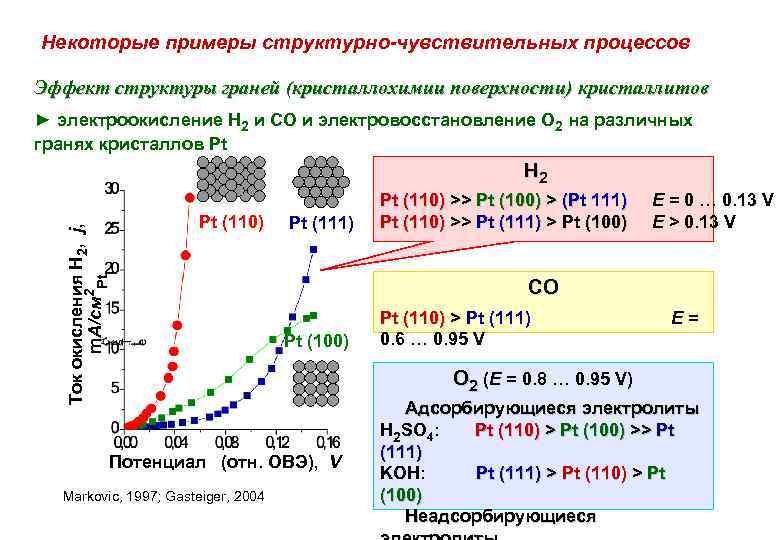 Некоторые примеры структурно-чувствительных процессов Эффект структуры граней (кристаллохимии поверхности) кристаллитов ► электроокисление H 2 и СО и электровосстановление О 2 на различных гранях кристаллов Pt Ток окисления Н 2, j, m. А/см 2 Pt H 2 Pt (110) Pt (111) CO Pt (100) Потенциал (отн. ОВЭ), V Markovic, 1997; Gasteiger, 2004 Pt (110) >> Pt (100) > (Pt 111) E = 0 … 0. 13 V Pt (110) >> Pt (111) > Pt (100) E > 0. 13 V Pt (110) > Pt (111) 0. 6 … 0. 95 V E = O 2 (E = 0. 8 … 0. 95 V) Адсорбирующиеся электролиты H 2 SO 4: Pt (110) > Pt (100) >> Pt (111) KOH: Pt (111) > Pt (110) > Pt (100) Неадсорбирующиеся
Некоторые примеры структурно-чувствительных процессов Эффект структуры граней (кристаллохимии поверхности) кристаллитов ► электроокисление H 2 и СО и электровосстановление О 2 на различных гранях кристаллов Pt Ток окисления Н 2, j, m. А/см 2 Pt H 2 Pt (110) Pt (111) CO Pt (100) Потенциал (отн. ОВЭ), V Markovic, 1997; Gasteiger, 2004 Pt (110) >> Pt (100) > (Pt 111) E = 0 … 0. 13 V Pt (110) >> Pt (111) > Pt (100) E > 0. 13 V Pt (110) > Pt (111) 0. 6 … 0. 95 V E = O 2 (E = 0. 8 … 0. 95 V) Адсорбирующиеся электролиты H 2 SO 4: Pt (110) > Pt (100) >> Pt (111) KOH: Pt (111) > Pt (110) > Pt (100) Неадсорбирующиеся
 Некоторые примеры структурно-чувствительных процессов Эффект структуры граней (кристаллохимии поверхности) кристаллитов ► синтез NH 3 из N 2 + H 2 на железном катализаторе: УКА граней кристаллов Fe падает в ряду Fe(111) > Fe(100) > Fe(110) с различием примерно на порядок между соседними членами ряда Практически невозможно получать промышленные катализаторы с однородной в кристаллохимическом отношении поверхностью активного компонента вследствие – равновесного распределения различного типа граней в кристаллитах, – реконструкции поверхности кристаллитов в реакционных условиях (термический отжиг, химическое взаимодействие с адсорбатами)
Некоторые примеры структурно-чувствительных процессов Эффект структуры граней (кристаллохимии поверхности) кристаллитов ► синтез NH 3 из N 2 + H 2 на железном катализаторе: УКА граней кристаллов Fe падает в ряду Fe(111) > Fe(100) > Fe(110) с различием примерно на порядок между соседними членами ряда Практически невозможно получать промышленные катализаторы с однородной в кристаллохимическом отношении поверхностью активного компонента вследствие – равновесного распределения различного типа граней в кристаллитах, – реконструкции поверхности кристаллитов в реакционных условиях (термический отжиг, химическое взаимодействие с адсорбатами)
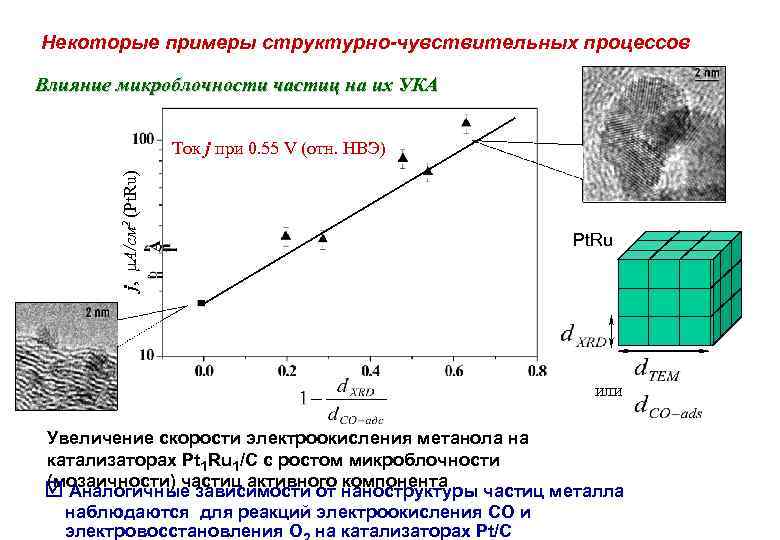 Некоторые примеры структурно-чувствительных процессов Влияние микроблочности частиц на их УКА j, А/см 2 (Pt. Ru) Ток j при 0. 55 V (отн. НВЭ) Pt. Ru или Увеличение скорости электроокисления метанола на катализаторах Pt 1 Ru 1/C с ростом микроблочности (мозаичности) частиц активного компонента Аналогичные зависимости от наноструктуры частиц металла наблюдаются для реакций электроокисления CO и электровосстановления O на катализаторах Pt/C
Некоторые примеры структурно-чувствительных процессов Влияние микроблочности частиц на их УКА j, А/см 2 (Pt. Ru) Ток j при 0. 55 V (отн. НВЭ) Pt. Ru или Увеличение скорости электроокисления метанола на катализаторах Pt 1 Ru 1/C с ростом микроблочности (мозаичности) частиц активного компонента Аналогичные зависимости от наноструктуры частиц металла наблюдаются для реакций электроокисления CO и электровосстановления O на катализаторах Pt/C
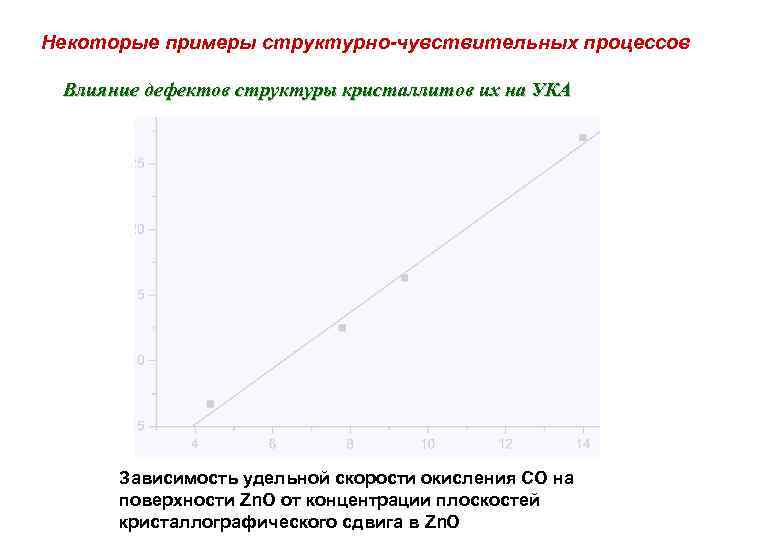 Некоторые примеры структурно-чувствительных процессов Влияние дефектов структуры кристаллитов их на УКА Зависимость удельной скорости окисления СО на поверхности Zn. O от концентрации плоскостей кристаллографического сдвига в Zn. O
Некоторые примеры структурно-чувствительных процессов Влияние дефектов структуры кристаллитов их на УКА Зависимость удельной скорости окисления СО на поверхности Zn. O от концентрации плоскостей кристаллографического сдвига в Zn. O
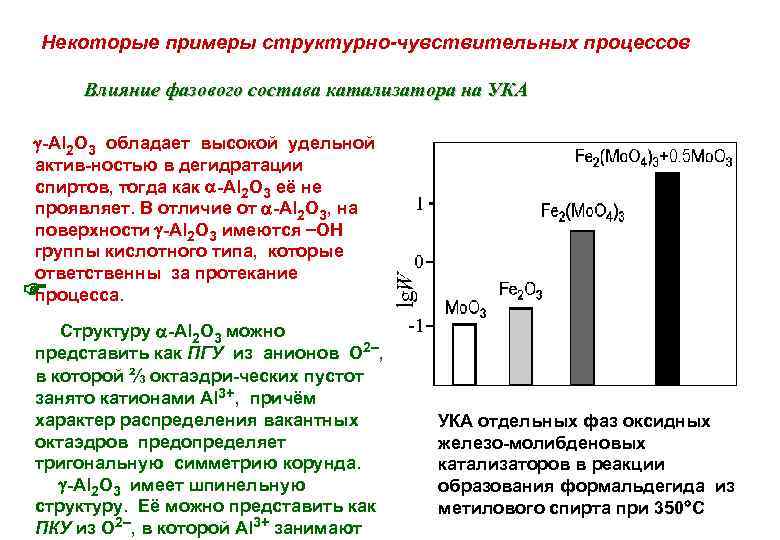 Некоторые примеры структурно-чувствительных процессов Влияние фазового состава катализатора на УКА -Al 2 O 3 обладает высокой удельной актив-ностью в дегидратации спиртов, тогда как -Al 2 O 3 её не проявляет. В отличие от -Al 2 O 3, на поверхности -Al 2 O 3 имеются OH группы кислотного типа, которые ответственны за протекание процесса. Структуру -Al 2 O 3 можно представить как ПГУ из анионов О 2 , в которой ⅔ октаэдри-ческих пустот занято катионами Al 3+, причём характер распределения вакантных октаэдров предопределяет тригональную симметрию корунда. -Al 2 O 3 имеет шпинельную структуру. Её можно представить как ПКУ из О 2 , в которой Al 3+ занимают УКА отдельных фаз оксидных железо-молибденовых катализаторов в реакции образования формальдегида из метилового спирта при 350 С
Некоторые примеры структурно-чувствительных процессов Влияние фазового состава катализатора на УКА -Al 2 O 3 обладает высокой удельной актив-ностью в дегидратации спиртов, тогда как -Al 2 O 3 её не проявляет. В отличие от -Al 2 O 3, на поверхности -Al 2 O 3 имеются OH группы кислотного типа, которые ответственны за протекание процесса. Структуру -Al 2 O 3 можно представить как ПГУ из анионов О 2 , в которой ⅔ октаэдри-ческих пустот занято катионами Al 3+, причём характер распределения вакантных октаэдров предопределяет тригональную симметрию корунда. -Al 2 O 3 имеет шпинельную структуру. Её можно представить как ПКУ из О 2 , в которой Al 3+ занимают УКА отдельных фаз оксидных железо-молибденовых катализаторов в реакции образования формальдегида из метилового спирта при 350 С
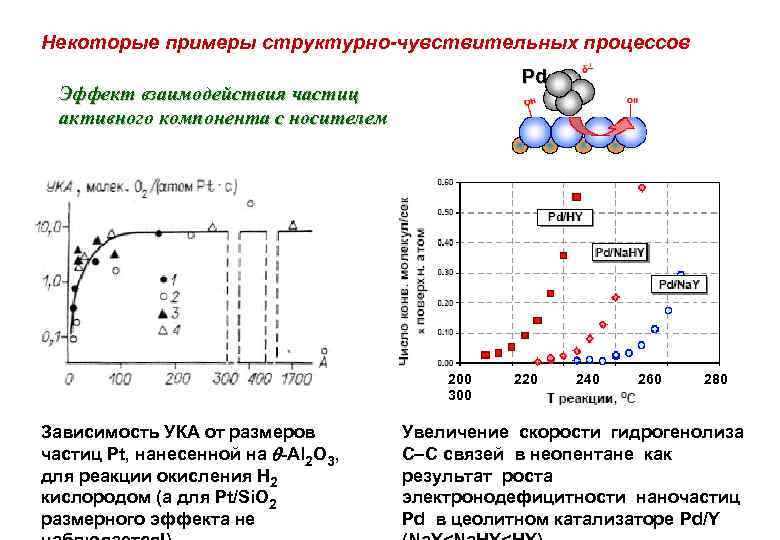 Некоторые примеры структурно-чувствительных процессов Эффект взаимодействия частиц активного компонента с носителем Pd 200 220 240 260 280 300 Зависимость УКА от размеров частиц Pt, нанесенной на -Al 2 O 3, для реакции окисления H 2 кислородом (а для Pt/Si. O 2 размерного эффекта не Увеличение скорости гидрогенолиза С С связей в неопентане как результат роста электронодефицитности наночастиц Pd в цеолитном катализаторе Pd/Y
Некоторые примеры структурно-чувствительных процессов Эффект взаимодействия частиц активного компонента с носителем Pd 200 220 240 260 280 300 Зависимость УКА от размеров частиц Pt, нанесенной на -Al 2 O 3, для реакции окисления H 2 кислородом (а для Pt/Si. O 2 размерного эффекта не Увеличение скорости гидрогенолиза С С связей в неопентане как результат роста электронодефицитности наночастиц Pd в цеолитном катализаторе Pd/Y
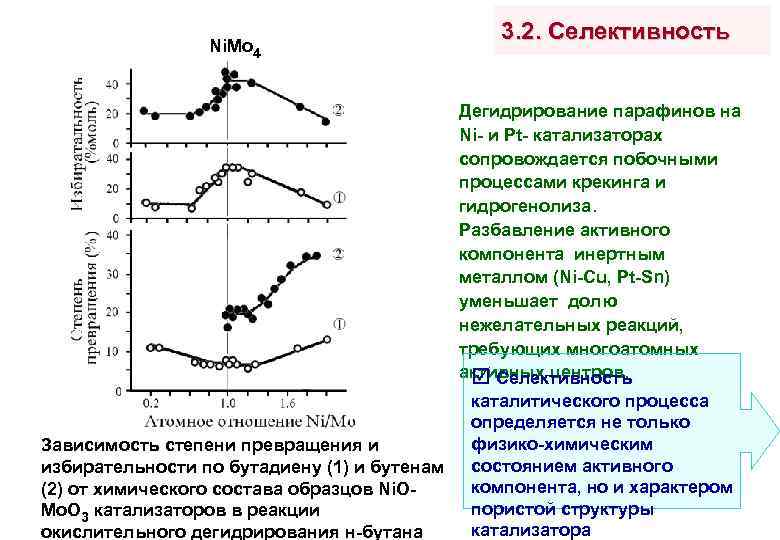 Ni. Mo 4 3. 2. Селективность Дегидрирование парафинов на Ni- и Pt- катализаторах сопровождается побочными процессами крекинга и гидрогенолиза. Разбавление активного компонента инертным металлом (Ni-Cu, Pt-Sn) уменьшает долю нежелательных реакций, требующих многоатомных активных центров. Селективность каталитического процесса определяется не только физико-химическим Зависимость степени превращения и избирательности по бутадиену (1) и бутенам состоянием активного компонента, но и характером (2) от химического состава образцов Ni. Oпористой структуры Mo. O 3 катализаторов в реакции катализатора окислительного дегидрирования н-бутана
Ni. Mo 4 3. 2. Селективность Дегидрирование парафинов на Ni- и Pt- катализаторах сопровождается побочными процессами крекинга и гидрогенолиза. Разбавление активного компонента инертным металлом (Ni-Cu, Pt-Sn) уменьшает долю нежелательных реакций, требующих многоатомных активных центров. Селективность каталитического процесса определяется не только физико-химическим Зависимость степени превращения и избирательности по бутадиену (1) и бутенам состоянием активного компонента, но и характером (2) от химического состава образцов Ni. Oпористой структуры Mo. O 3 катализаторов в реакции катализатора окислительного дегидрирования н-бутана
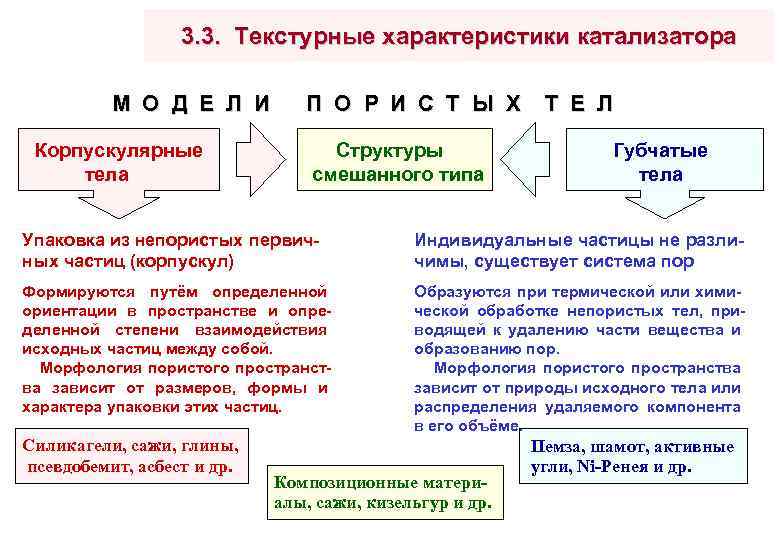 3. 3. Текстурные характеристики катализатора М О Д Е Л И П О Р И С Т Ы Х Т Е Л Корпускулярные тела Структуры Губчатые смешанного типа тела Упаковка из непористых первичных частиц (корпускул) Индивидуальные частицы не различимы, существует система пор Формируются путём определенной ориентации в пространстве и определенной степени взаимодействия исходных частиц между собой. Морфология пористого пространства зависит от размеров, формы и характера упаковки этих частиц. Образуются при термической или хими- ческой обработке непористых тел, приводящей к удалению части вещества и образованию пор. Морфология пористого пространства зависит от природы исходного тела или распределения удаляемого компонента в его объёме. Силикагели, сажи, глины, псевдобемит, асбест и др. Композиционные материалы, сажи, кизельгур и др. Пемза, шамот, активные угли, Ni-Ренея и др.
3. 3. Текстурные характеристики катализатора М О Д Е Л И П О Р И С Т Ы Х Т Е Л Корпускулярные тела Структуры Губчатые смешанного типа тела Упаковка из непористых первичных частиц (корпускул) Индивидуальные частицы не различимы, существует система пор Формируются путём определенной ориентации в пространстве и определенной степени взаимодействия исходных частиц между собой. Морфология пористого пространства зависит от размеров, формы и характера упаковки этих частиц. Образуются при термической или хими- ческой обработке непористых тел, приводящей к удалению части вещества и образованию пор. Морфология пористого пространства зависит от природы исходного тела или распределения удаляемого компонента в его объёме. Силикагели, сажи, глины, псевдобемит, асбест и др. Композиционные материалы, сажи, кизельгур и др. Пемза, шамот, активные угли, Ni-Ренея и др.
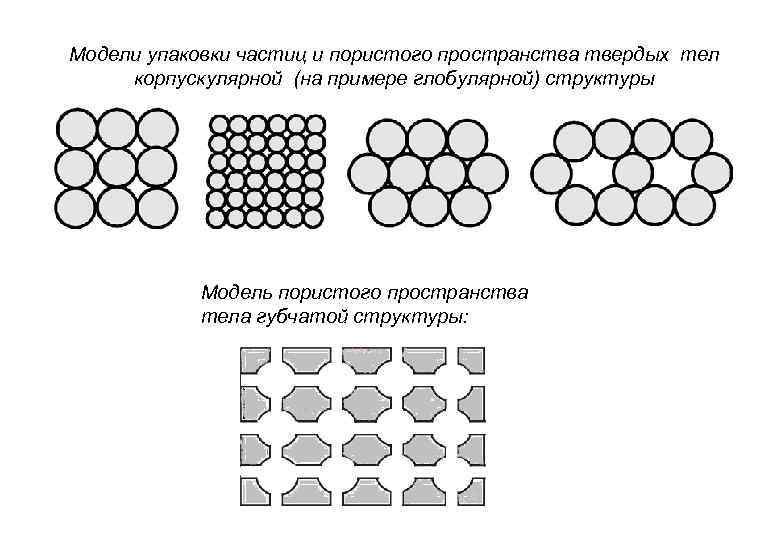 Модели упаковки частиц и пористого пространства твердых тел корпускулярной (на примере глобулярной) структуры Модель пористого пространства тела губчатой структуры:
Модели упаковки частиц и пористого пространства твердых тел корпускулярной (на примере глобулярной) структуры Модель пористого пространства тела губчатой структуры:
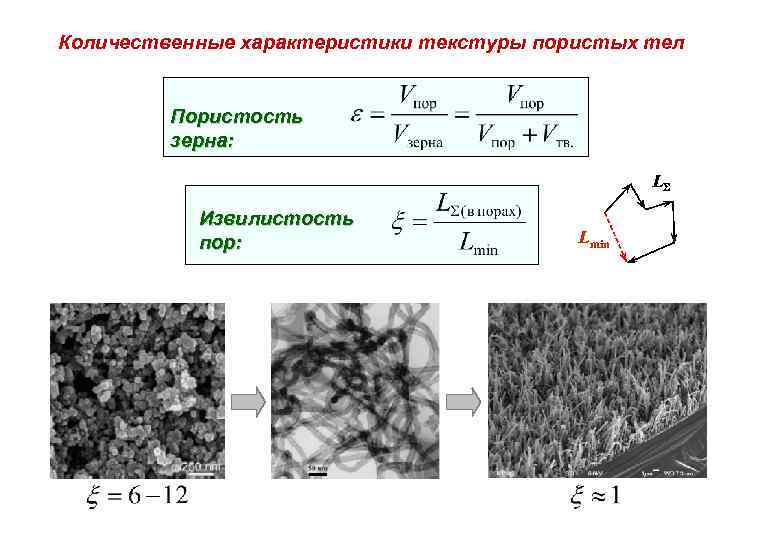 Количественные характеристики текстуры пористых тел Пористость зерна: L Извилистость пор: Lmin
Количественные характеристики текстуры пористых тел Пористость зерна: L Извилистость пор: Lmin
 Количественные характеристики текстуры пористых тел Средний пор: размер Классификация пор (по М. М. Дубинину): Механизм диффузии молекул газов в порах при н. у. : микропоры (менее 1. 5 фольмеровская нм) мезопоры (1. 5 – 100 нм) макропоры (более 100 Dфольм. << нм) молекулярная Dкнудс. <
Количественные характеристики текстуры пористых тел Средний пор: размер Классификация пор (по М. М. Дубинину): Механизм диффузии молекул газов в порах при н. у. : микропоры (менее 1. 5 фольмеровская нм) мезопоры (1. 5 – 100 нм) макропоры (более 100 Dфольм. << нм) молекулярная Dкнудс. <
 Величина внутренней поверхности пористого тела поверхности корпускулярной модели равна сумме поверхностей отдельных корпускул, из которых состоит это тело, за вычетом площади мест контакта этих корпускул между собой. Для монодисперсных частиц: где N – число частиц, S – поверхность отдельной частицы, n – число контактов. Удельная поверхность (при условии n. Sконт. ~ 0): поверхность [м 2/м 3] или [м 2/г] Для частиц произвольной формы: [м 2/м 3] или [м 2/г] где плотность вещества частицы, V и L соответственно, объём и размер частицы, kч коэффициент, зависящий от формы частиц.
Величина внутренней поверхности пористого тела поверхности корпускулярной модели равна сумме поверхностей отдельных корпускул, из которых состоит это тело, за вычетом площади мест контакта этих корпускул между собой. Для монодисперсных частиц: где N – число частиц, S – поверхность отдельной частицы, n – число контактов. Удельная поверхность (при условии n. Sконт. ~ 0): поверхность [м 2/м 3] или [м 2/г] Для частиц произвольной формы: [м 2/м 3] или [м 2/г] где плотность вещества частицы, V и L соответственно, объём и размер частицы, kч коэффициент, зависящий от формы частиц.
 3. 3. 1. Пористая структура катализатора и кинетика реакций ► Wmax – максимальная (т. е. в отсутствие диффузионного торможения) скорость реакции на зерне катализатора, является функцией W(Ci) от концентраций реагентов в каталитической системе ► является функцией от безразмерного параметра Ψ, определяемого через отношение Wmax к скорости диффузии реагента, массоперенос которого тормозит реакцию (критерий Тиле): В случае <<1 : Эффективный коэффициент диффузии: Размер зерна катализатора: пластин а цилиндр ша р
3. 3. 1. Пористая структура катализатора и кинетика реакций ► Wmax – максимальная (т. е. в отсутствие диффузионного торможения) скорость реакции на зерне катализатора, является функцией W(Ci) от концентраций реагентов в каталитической системе ► является функцией от безразмерного параметра Ψ, определяемого через отношение Wmax к скорости диффузии реагента, массоперенос которого тормозит реакцию (критерий Тиле): В случае <<1 : Эффективный коэффициент диффузии: Размер зерна катализатора: пластин а цилиндр ша р
 Оптимальная пористая структура катализатора ► Для реакций, протекающих с малой скоростью или при повышенных скоростью давлениях, когда скорость массопереноса значительно выше скорости давлениях реакции (Wдиф. > Wреак. ), оптимальной является однородная тонкопористая структура с размером пор 1 -10 нм. ► Для быстрых реакций (Wдиф. < Wреак. ) требуются поры с размерами порядка 100 нм, поэтому оптимальна бидисперсная структура гранул. Модели моно- (а) и бидисперсной (б) структуры гранулы катализатора
Оптимальная пористая структура катализатора ► Для реакций, протекающих с малой скоростью или при повышенных скоростью давлениях, когда скорость массопереноса значительно выше скорости давлениях реакции (Wдиф. > Wреак. ), оптимальной является однородная тонкопористая структура с размером пор 1 -10 нм. ► Для быстрых реакций (Wдиф. < Wреак. ) требуются поры с размерами порядка 100 нм, поэтому оптимальна бидисперсная структура гранул. Модели моно- (а) и бидисперсной (б) структуры гранулы катализатора
 Увеличение скорости реакции вследствие перехода от моно- к бидисперсной структуре гранул катализатора составляет: D 1 и 1 коэффициент диффузии молекул реагента и пористость для первичных зёрен, D 2 и 2 коэффициент диффузии молекул реагента и пористость для вторичных зёрен. Наиболее выгодная доля свободного объёма между вторичными частицами 2 = 0. 5. При этом скорость реакции, протекающей при атмосферном давлении, при переходе к бидисперсной структуре зёрен катализатора может увеличиться в 5 -8 раз.
Увеличение скорости реакции вследствие перехода от моно- к бидисперсной структуре гранул катализатора составляет: D 1 и 1 коэффициент диффузии молекул реагента и пористость для первичных зёрен, D 2 и 2 коэффициент диффузии молекул реагента и пористость для вторичных зёрен. Наиболее выгодная доля свободного объёма между вторичными частицами 2 = 0. 5. При этом скорость реакции, протекающей при атмосферном давлении, при переходе к бидисперсной структуре зёрен катализатора может увеличиться в 5 -8 раз.
 Селективность катализатора и характер его пористой структуры Оптимальная пористая структура катализатора необходима и для его высокой селективности при осуществлении многомаршрутных процессов. 1) Параллельные реакции: реакции ► диффузионное торможение может как снижать, так и повышать селективность. Если реакция получения целевого продукта B имеет первый порядок, а для побочной реакции порядок больше единицы, то в области внутренней диффузии наряду с уменьшением общей скорости будет возрастать селективность по B.
Селективность катализатора и характер его пористой структуры Оптимальная пористая структура катализатора необходима и для его высокой селективности при осуществлении многомаршрутных процессов. 1) Параллельные реакции: реакции ► диффузионное торможение может как снижать, так и повышать селективность. Если реакция получения целевого продукта B имеет первый порядок, а для побочной реакции порядок больше единицы, то в области внутренней диффузии наряду с уменьшением общей скорости будет возрастать селективность по B.
 2) Последовательные реакции: реакции ► если полезный продукт является промежуточным (В), диффузионное торможение всегда снижает селективность. Переход к бидисперсным структурам в этом случае позволяет повышать селективность. Вывод: Требования к пористой структуре оптимального катализатора определяются схемой протекания многомаршрутного каталитического процесса и кинетическими параметрами каждой реакции, а также особенностями массопереноса реагирующих веществ в порах
2) Последовательные реакции: реакции ► если полезный продукт является промежуточным (В), диффузионное торможение всегда снижает селективность. Переход к бидисперсным структурам в этом случае позволяет повышать селективность. Вывод: Требования к пористой структуре оптимального катализатора определяются схемой протекания многомаршрутного каталитического процесса и кинетическими параметрами каждой реакции, а также особенностями массопереноса реагирующих веществ в порах
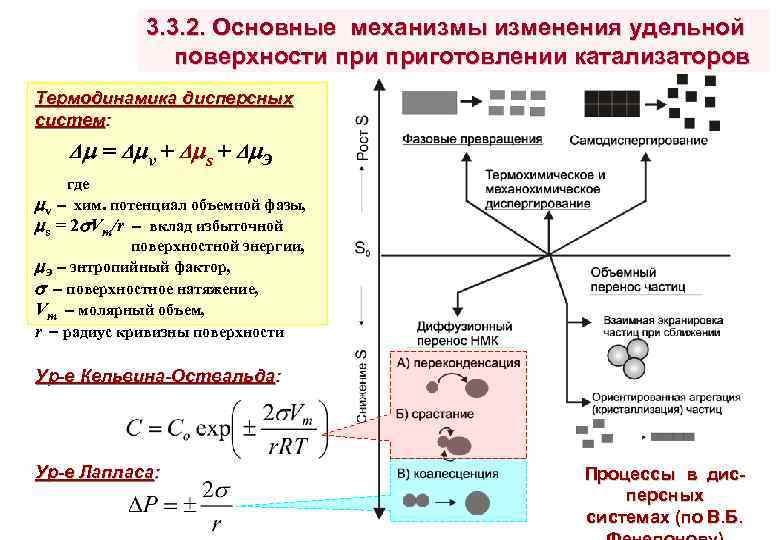 3. 3. 2. Основные механизмы изменения удельной поверхности приготовлении катализаторов Термодинамика дисперсных систем: = v + s + Э где v хим. потенциал объемной фазы, s = 2 Vm/r вклад избыточной поверхностной энергии, Э энтропийный фактор, поверхностное натяжение, Vm молярный объем, r радиус кривизны поверхности Ур-е Кельвина-Оствальда: Ур-е Лапласа: Процессы в дисперсных системах (по В. Б.
3. 3. 2. Основные механизмы изменения удельной поверхности приготовлении катализаторов Термодинамика дисперсных систем: = v + s + Э где v хим. потенциал объемной фазы, s = 2 Vm/r вклад избыточной поверхностной энергии, Э энтропийный фактор, поверхностное натяжение, Vm молярный объем, r радиус кривизны поверхности Ур-е Кельвина-Оствальда: Ур-е Лапласа: Процессы в дисперсных системах (по В. Б.
 Задачи НОПК в области управления текстурными свойствами катализатора · Проблема управления величиной удельной поверхности катализатора корпускулярной структуры сводится к раскрытию механизмов и закономерностей формирования дисперсных частиц и на основе этих знаний – к целенаправленному регулированию их размера; · При создании оптимальной пористой структуры помимо управления размером первичных частиц задача сводится к раскрытию закономерностей формирования их формы и характера упаковки, а также к поиску путей управления этими процессами.
Задачи НОПК в области управления текстурными свойствами катализатора · Проблема управления величиной удельной поверхности катализатора корпускулярной структуры сводится к раскрытию механизмов и закономерностей формирования дисперсных частиц и на основе этих знаний – к целенаправленному регулированию их размера; · При создании оптимальной пористой структуры помимо управления размером первичных частиц задача сводится к раскрытию закономерностей формирования их формы и характера упаковки, а также к поиску путей управления этими процессами.
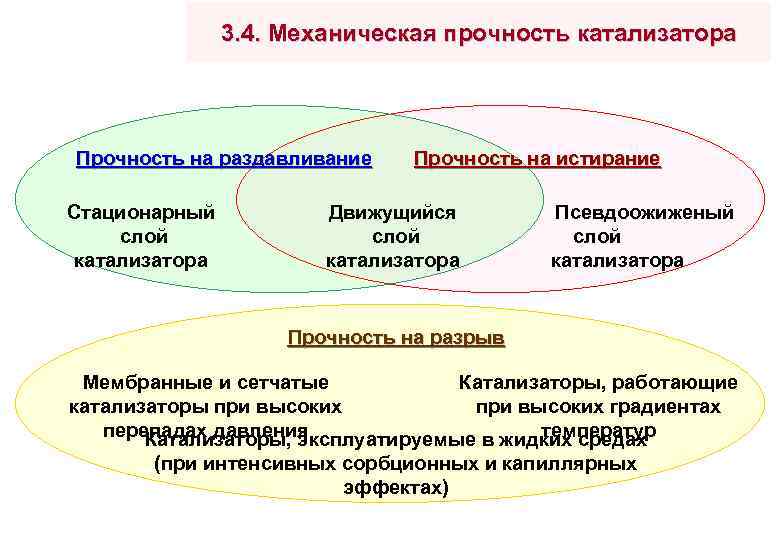 3. 4. Механическая прочность катализатора Прочность на раздавливание Стационарный слой катализатора Прочность на истирание Движущийся слой катализатора Псевдоожиженый слой катализатора Прочность на разрыв Мембранные и сетчатые Катализаторы, работающие катализаторы при высоких градиентах перепадах давления температур Катализаторы, эксплуатируемые в жидких средах (при интенсивных сорбционных и капиллярных эффектах)
3. 4. Механическая прочность катализатора Прочность на раздавливание Стационарный слой катализатора Прочность на истирание Движущийся слой катализатора Псевдоожиженый слой катализатора Прочность на разрыв Мембранные и сетчатые Катализаторы, работающие катализаторы при высоких градиентах перепадах давления температур Катализаторы, эксплуатируемые в жидких средах (при интенсивных сорбционных и капиллярных эффектах)
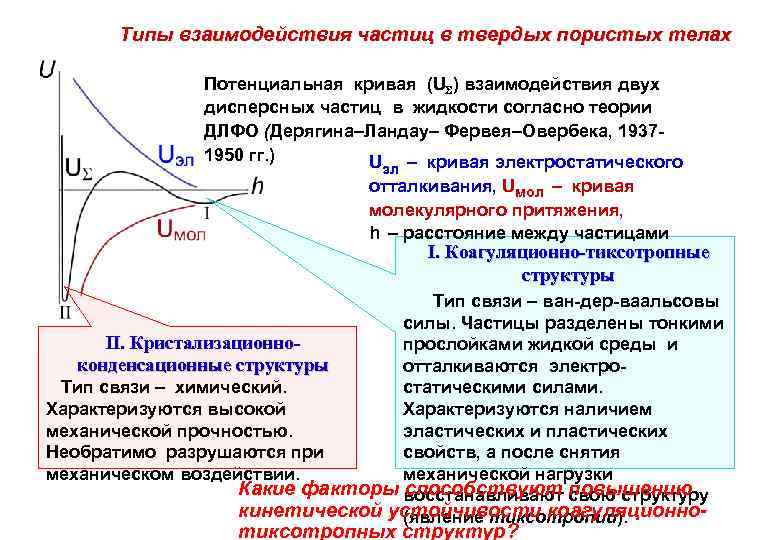 Типы взаимодействия частиц в твердых пористых телах Потенциальная кривая (U ) взаимодействия двух дисперсных частиц в жидкости согласно теории ДЛФО (Дерягина–Ландау– Фервея–Овербека, 19371950 гг. ) U – кривая электростатического эл отталкивания, Uмол – кривая молекулярного притяжения, h – расстояние между частицами I. Коагуляционно-тиксотропные структуры Тип связи – ван-дер-ваальсовы силы. Частицы разделены тонкими II. Кристализационнопрослойками жидкой среды и конденсационные структуры отталкиваются электростатическими силами. Тип связи – химический. Характеризуются наличием Характеризуются высокой эластических и пластических механической прочностью. свойств, а после снятия Необратимо разрушаются при механической нагрузки механическом воздействии. Какие факторы восстанавливают свою структуру способствуют повышению кинетической устойчивости коагуляционно(явление тиксотропии). тиксотропных структур?
Типы взаимодействия частиц в твердых пористых телах Потенциальная кривая (U ) взаимодействия двух дисперсных частиц в жидкости согласно теории ДЛФО (Дерягина–Ландау– Фервея–Овербека, 19371950 гг. ) U – кривая электростатического эл отталкивания, Uмол – кривая молекулярного притяжения, h – расстояние между частицами I. Коагуляционно-тиксотропные структуры Тип связи – ван-дер-ваальсовы силы. Частицы разделены тонкими II. Кристализационнопрослойками жидкой среды и конденсационные структуры отталкиваются электростатическими силами. Тип связи – химический. Характеризуются наличием Характеризуются высокой эластических и пластических механической прочностью. свойств, а после снятия Необратимо разрушаются при механической нагрузки механическом воздействии. Какие факторы восстанавливают свою структуру способствуют повышению кинетической устойчивости коагуляционно(явление тиксотропии). тиксотропных структур?
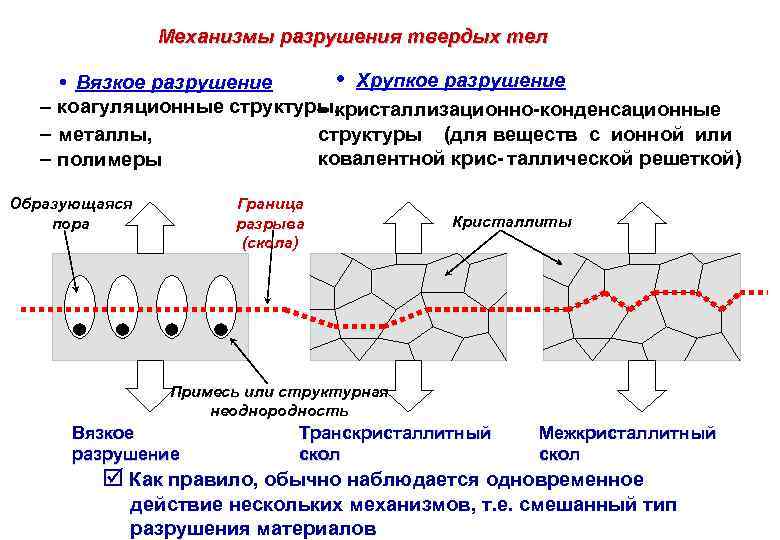 Механизмы разрушения твердых тел • Хрупкое разрушение • Вязкое разрушение коагуляционные структуры, кристаллизационно-конденсационные металлы, структуры (для веществ с ионной или ковалентной крис- таллической решеткой) полимеры Образующаяся пора Граница разрыва (скола) Кристаллиты Примесь или структурная неоднородность Вязкое разрушение Транскристаллитный скол Межкристаллитный скол Как правило, обычно наблюдается одновременное действие нескольких механизмов, т. е. смешанный тип разрушения материалов
Механизмы разрушения твердых тел • Хрупкое разрушение • Вязкое разрушение коагуляционные структуры, кристаллизационно-конденсационные металлы, структуры (для веществ с ионной или ковалентной крис- таллической решеткой) полимеры Образующаяся пора Граница разрыва (скола) Кристаллиты Примесь или структурная неоднородность Вязкое разрушение Транскристаллитный скол Межкристаллитный скол Как правило, обычно наблюдается одновременное действие нескольких механизмов, т. е. смешанный тип разрушения материалов
 Пористые тела. Основные положения теории Ребиндера - Щукина о прочности пористых тел • прочность твердого тела определяется не столько прочностью частиц, его образующих, сколько прочностью индивидуальных контактов между ними и числом этих контактов; • число контактов в единице объёма тела обусловлено размером частиц и способом их упаковки, т. е. тесно связано с пористостью и распределением пор по размерам; • крупные поры не только уменьшают общую поверхность контактов, они таят опасность как концентраторы напряжений (трещины) и поэтому особенно резко понижают прочность; • пористые тела в зависимости от способа их формирования характеризуются определенным распределением макро- и микроскопических внутренних напряжений, которые разрывают часть контактов на последующих стадиях обработки, а также снижают прочность в процессе эксплуатации
Пористые тела. Основные положения теории Ребиндера - Щукина о прочности пористых тел • прочность твердого тела определяется не столько прочностью частиц, его образующих, сколько прочностью индивидуальных контактов между ними и числом этих контактов; • число контактов в единице объёма тела обусловлено размером частиц и способом их упаковки, т. е. тесно связано с пористостью и распределением пор по размерам; • крупные поры не только уменьшают общую поверхность контактов, они таят опасность как концентраторы напряжений (трещины) и поэтому особенно резко понижают прочность; • пористые тела в зависимости от способа их формирования характеризуются определенным распределением макро- и микроскопических внутренних напряжений, которые разрывают часть контактов на последующих стадиях обработки, а также снижают прочность в процессе эксплуатации
 Природа сил, совместное действие которых может вызвать разрушение пористых тел Снаружи • Внешняя механическая нагрузка В твердом теле • Остаточные внутренние напряжения (предыстория материала!!!) • Поверхностное натяжение • Локальные различия в коэффициентах термического расширения В порах твердого тела • Капиллярное давление жидкости (наличие газов в порах!!!) • Расклинивающее давление жидкости в порах как суперпозиция разнонаправленных сил: молекулярных (ван-дер-ваальсовы силы), молекулярных электростатических (взаимодействие ДЭС стенок пор), электростатических структурных (изменение структуры растворителя в узких структурных порах), адсорбционных (из-за неравномерного распределение адсорбционных адсорбата в пленке),
Природа сил, совместное действие которых может вызвать разрушение пористых тел Снаружи • Внешняя механическая нагрузка В твердом теле • Остаточные внутренние напряжения (предыстория материала!!!) • Поверхностное натяжение • Локальные различия в коэффициентах термического расширения В порах твердого тела • Капиллярное давление жидкости (наличие газов в порах!!!) • Расклинивающее давление жидкости в порах как суперпозиция разнонаправленных сил: молекулярных (ван-дер-ваальсовы силы), молекулярных электростатических (взаимодействие ДЭС стенок пор), электростатических структурных (изменение структуры растворителя в узких структурных порах), адсорбционных (из-за неравномерного распределение адсорбционных адсорбата в пленке),
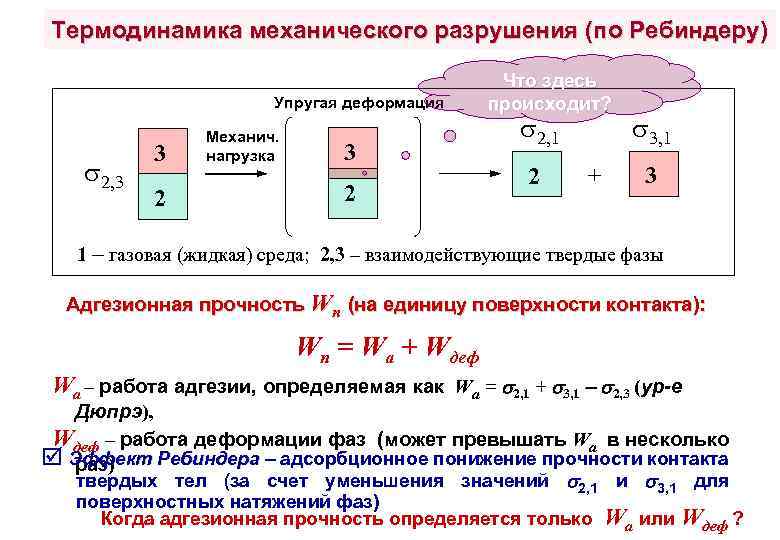 Термодинамика механического разрушения (по Ребиндеру) Упругая деформация 2, 3 3 2 Механич. нагрузка 3 2 Что здесь происходит? 2, 1 2 + 3, 1 3 1 – газовая (жидкая) среда; 2, 3 – взаимодействующие твердые фазы Адгезионная прочность Wп (на единицу поверхности контакта): Wп = Wа + Wдеф Wа – работа адгезии, определяемая как Wa = 2, 1 + 3, 1 2, 3 (ур-е Дюпрэ), Wдеф – работа деформации фаз (может превышать Wа в несколько Эффект Ребиндера – адсорбционное понижение прочности контакта Ребиндера раз) твердых тел (за счет уменьшения значений 2, 1 и 3, 1 для поверхностных натяжений фаз) Когда адгезионная прочность определяется только Wа или Wдеф ?
Термодинамика механического разрушения (по Ребиндеру) Упругая деформация 2, 3 3 2 Механич. нагрузка 3 2 Что здесь происходит? 2, 1 2 + 3, 1 3 1 – газовая (жидкая) среда; 2, 3 – взаимодействующие твердые фазы Адгезионная прочность Wп (на единицу поверхности контакта): Wп = Wа + Wдеф Wа – работа адгезии, определяемая как Wa = 2, 1 + 3, 1 2, 3 (ур-е Дюпрэ), Wдеф – работа деформации фаз (может превышать Wа в несколько Эффект Ребиндера – адсорбционное понижение прочности контакта Ребиндера раз) твердых тел (за счет уменьшения значений 2, 1 и 3, 1 для поверхностных натяжений фаз) Когда адгезионная прочность определяется только Wа или Wдеф ?
 Работа разрушения однофазной системы: Wп = Wк + Wдеф = S + k. V S – приращение поверхности в процессе разрушения тела, k – работа объёмного деформирования единицы объёма тела, V – объём тела Так как V R 3 (R линейный размер тела), а S R 2, то Wп = k 1 R 2 + k 2 R 3 k 1 и k 2 – коэффициенты пропорциональности Работа диспергирования определяется, главным образом, ► для массивных тел работой упругого и пластического деформи Wп k 2 R 3 (т. к. R 2 << R 3) ► для дисперсных тел работой образования новой поверхности (работой Wk по преодолению когезионных сил): Wп k 1 R 2 (т. к. R 2 >> R 3)
Работа разрушения однофазной системы: Wп = Wк + Wдеф = S + k. V S – приращение поверхности в процессе разрушения тела, k – работа объёмного деформирования единицы объёма тела, V – объём тела Так как V R 3 (R линейный размер тела), а S R 2, то Wп = k 1 R 2 + k 2 R 3 k 1 и k 2 – коэффициенты пропорциональности Работа диспергирования определяется, главным образом, ► для массивных тел работой упругого и пластического деформи Wп k 2 R 3 (т. к. R 2 << R 3) ► для дисперсных тел работой образования новой поверхности (работой Wk по преодолению когезионных сил): Wп k 1 R 2 (т. к. R 2 >> R 3)
 Способы повышения механической прочности твердых тел и контактов между ними Условие высокой механической прочности твердых тел или контактов между ними – эффективное торможение движущихся дислокаций и рассеяние поля напряжений во фронте распространения трещины за счет дислокаций (упрочнение пропорционально за счет дислокаций квадратному корню из общей плотности дислокаций), при образовании твердых растворов (повышение предела при образовании твердых растворов текучести при добавке легирующих элементов аддитивно и тем больше, чем сильнее их отличие в атомном радиусе или валентности от элементов матрицы), за счет межкристаллитных границ; за счет межкристаллитных границ посредством создания текстуры (т. е. регулярной упаковки из посредством создания текстуры кристаллитов, образующих тело); за счет фазовых превращений (вкрапление кристаллитов за счет фазовых превращений новых фаз); путём создания композиционных материалов, содержащих второй компонент в виде плёнок между частицами матрицы, в
Способы повышения механической прочности твердых тел и контактов между ними Условие высокой механической прочности твердых тел или контактов между ними – эффективное торможение движущихся дислокаций и рассеяние поля напряжений во фронте распространения трещины за счет дислокаций (упрочнение пропорционально за счет дислокаций квадратному корню из общей плотности дислокаций), при образовании твердых растворов (повышение предела при образовании твердых растворов текучести при добавке легирующих элементов аддитивно и тем больше, чем сильнее их отличие в атомном радиусе или валентности от элементов матрицы), за счет межкристаллитных границ; за счет межкристаллитных границ посредством создания текстуры (т. е. регулярной упаковки из посредством создания текстуры кристаллитов, образующих тело); за счет фазовых превращений (вкрапление кристаллитов за счет фазовых превращений новых фаз); путём создания композиционных материалов, содержащих второй компонент в виде плёнок между частицами матрицы, в
 3. 5. Устойчивость катализатора к дезактивации Дезактивация – явление снижения активности и селективности катализатора в процессе его эксплуатации Основные причины: ► изменение химического и фазового состава катализатора ► изменение текстуры зёрен катализатора ► изменение субструктурных свойств активного компонента Основные факторы, обуславливающие дезактивацию: • высокая температура, • наличие каталитических ядов в реакционной смеси, • образование побочных высокомолекулярных продуктов реакции, которые блокируют поверхность катализатора
3. 5. Устойчивость катализатора к дезактивации Дезактивация – явление снижения активности и селективности катализатора в процессе его эксплуатации Основные причины: ► изменение химического и фазового состава катализатора ► изменение текстуры зёрен катализатора ► изменение субструктурных свойств активного компонента Основные факторы, обуславливающие дезактивацию: • высокая температура, • наличие каталитических ядов в реакционной смеси, • образование побочных высокомолекулярных продуктов реакции, которые блокируют поверхность катализатора
 3. 5. 1. Термическая стабильность катализатора. Текстурные и структурные промоторы Эффекты температуры: • Изменение фазового состава катализатора: полиморфные превращения, твердофазное взаимодействие компонентов • Изменение химического состава поверхности активного компонента: выход объёмных примесей на поверхность, миграция поверхностных компонентов в объём катализатора, удаление компонентов катализатора с продуктами реакции • Рекристаллизация частиц активного компонента: изменение формы и размеров частиц (редиспергирование или спекание), изменение их субструктуры (отжиг дефектов, межкристаллитных границ и др. ), Изменение микроструктуры (т. е. реконструкция) поверхности • уменьшение удельной поверхности и объёма пор вследствие увеличения активного компонента кристаллитов их среднего размера (спекание) • Изменение характера их взаимодействия с носителем • Механическое разрушение частиц катализатора
3. 5. 1. Термическая стабильность катализатора. Текстурные и структурные промоторы Эффекты температуры: • Изменение фазового состава катализатора: полиморфные превращения, твердофазное взаимодействие компонентов • Изменение химического состава поверхности активного компонента: выход объёмных примесей на поверхность, миграция поверхностных компонентов в объём катализатора, удаление компонентов катализатора с продуктами реакции • Рекристаллизация частиц активного компонента: изменение формы и размеров частиц (редиспергирование или спекание), изменение их субструктуры (отжиг дефектов, межкристаллитных границ и др. ), Изменение микроструктуры (т. е. реконструкция) поверхности • уменьшение удельной поверхности и объёма пор вследствие увеличения активного компонента кристаллитов их среднего размера (спекание) • Изменение характера их взаимодействия с носителем • Механическое разрушение частиц катализатора
 Общие способы повышения термической стабильности катализаторов: • Предварительная стабилизирующая термообработка катализатора: определение устойчивости фаз, входящих в состав катализатора, и в соответствии с этим – выбор оптимального режима его термообработки • Введение специальных добавок (или промоторов), препятствующих спеканию активного компонента: текстурные промоторы структурные промоторы Текстурные промоторы Структурные промоторы физически препятствуют спеканию кристаллитов активного компонента. Это относительно тугоплавкие инертные вещества (Al 2 O 3, Zr. O 2, Ce. O 2, Cr 2 O 3, La 2 O 3, Mg. O, Ti. O 2 и С) в виде высокодисперсных частиц изменяют химический состав активного компо-нента. В отличие от текстурных промоторов, они влияют на адсорб-цию реагентов и кажущуюся энергию активации каталитического процесса Выбор того или иного типа промоторов зависит, в первую очередь, от природы процессов массопереноса, определяющих скорость спекания катализатора
Общие способы повышения термической стабильности катализаторов: • Предварительная стабилизирующая термообработка катализатора: определение устойчивости фаз, входящих в состав катализатора, и в соответствии с этим – выбор оптимального режима его термообработки • Введение специальных добавок (или промоторов), препятствующих спеканию активного компонента: текстурные промоторы структурные промоторы Текстурные промоторы Структурные промоторы физически препятствуют спеканию кристаллитов активного компонента. Это относительно тугоплавкие инертные вещества (Al 2 O 3, Zr. O 2, Ce. O 2, Cr 2 O 3, La 2 O 3, Mg. O, Ti. O 2 и С) в виде высокодисперсных частиц изменяют химический состав активного компо-нента. В отличие от текстурных промоторов, они влияют на адсорб-цию реагентов и кажущуюся энергию активации каталитического процесса Выбор того или иного типа промоторов зависит, в первую очередь, от природы процессов массопереноса, определяющих скорость спекания катализатора
 Спекание массивных и нанесенных катализаторов Механизм переноса материала Ключевые факторы процесса ► Миграция устойчивых многоатомных образований (сложных ионов, класте- ров или наночастиц по поверхности твердого тела) ► Миграция отдельных атомов, Состав газовой (жидкой) фазы, природа поверхностных примесей, микрострук-тура поверхности тв. тела, реакционная способность Энергия связи атомов и ионов кластеров и частиц в крис-таллической структуре простых ионов или вакансий по поверхности (модель Оствальда) в объёме твердого тела, примеси T >TH (Хюттига темп. ~ 0. 3 Tпл) T >TT (Таммана темп. ~ 0. 5 Tпл для металлов, ~ 0. 8 Tпл для ► Перенос вещества через газовую Tисп /растворимость/ элементов оксидов) /жидкую/ среду структу-ры катализатора, а также продуктов их реакций с компонентами газа (жидкости) или собственными примесями ► Вязкое T Tпл , течение давление
Спекание массивных и нанесенных катализаторов Механизм переноса материала Ключевые факторы процесса ► Миграция устойчивых многоатомных образований (сложных ионов, класте- ров или наночастиц по поверхности твердого тела) ► Миграция отдельных атомов, Состав газовой (жидкой) фазы, природа поверхностных примесей, микрострук-тура поверхности тв. тела, реакционная способность Энергия связи атомов и ионов кластеров и частиц в крис-таллической структуре простых ионов или вакансий по поверхности (модель Оствальда) в объёме твердого тела, примеси T >TH (Хюттига темп. ~ 0. 3 Tпл) T >TT (Таммана темп. ~ 0. 5 Tпл для металлов, ~ 0. 8 Tпл для ► Перенос вещества через газовую Tисп /растворимость/ элементов оксидов) /жидкую/ среду структу-ры катализатора, а также продуктов их реакций с компонентами газа (жидкости) или собственными примесями ► Вязкое T Tпл , течение давление
 Спекание массивных катализаторов
Спекание массивных катализаторов
 Кинетика спекания пористых систем Механизм переноса материала Миграция отдельных атомов, простых ионов или вакансий по поверхности или в объёме твердого тела Перенос через газовую (или жидкую) среду Вязкое течение Lзерна, Vпор, Rпор, Sпор однородного состава Кинетические закономерности Lзерна, Vпор~ const, Rпор , Sпор Удельная поверхность: S и S 0 – текущее и начальное значения, – время, k, n – константы Объё м пор: пор Относитель ная усадка тела: тела
Кинетика спекания пористых систем Механизм переноса материала Миграция отдельных атомов, простых ионов или вакансий по поверхности или в объёме твердого тела Перенос через газовую (или жидкую) среду Вязкое течение Lзерна, Vпор, Rпор, Sпор однородного состава Кинетические закономерности Lзерна, Vпор~ const, Rпор , Sпор Удельная поверхность: S и S 0 – текущее и начальное значения, – время, k, n – константы Объё м пор: пор Относитель ная усадка тела: тела
 Кинетика рекристаллизации систем неоднородного состава Изменение размеров кристаллитов при рекристаллизации поликристаллических тел: тел где D и D 0 – текущее и начальное значение размера кристаллитов спекающегося компонента Рекристаллизация практически прекращается при: при где d, – размер и объёмная доля тугоплавких включений (или пор)
Кинетика рекристаллизации систем неоднородного состава Изменение размеров кристаллитов при рекристаллизации поликристаллических тел: тел где D и D 0 – текущее и начальное значение размера кристаллитов спекающегося компонента Рекристаллизация практически прекращается при: при где d, – размер и объёмная доля тугоплавких включений (или пор)
 Влияние добавок (примесей) на спекание массивных катализаторов Вид добавки или примеси Эффекты Несовпадение зарядов катионов: ► Образующие твердые растворы, т. е. полностью растворимые в появле- ние вакансий в катионной или анионной подрешётке оксида кристалли-ческой решетке рост спекаемости. основного вещества Совпадение зарядов катионов: (на примере оксидных систем) уменьше-ние параметра решетки из-за разницы в радиусах падение скорости спекания, и наоборот (для кубической Ускоряют спекание вследствие ► Нерастворимые, но решетки). интенси-фикации процессов легкоплавкие, или дающие массопереноса через жидкую расплав эвтектики при взаи- среду модействии с основным веществом Замедляют спекание, стерически ► Тугоплавкие, инертные по затрудняя слияние частиц отношению к основному основного вещества веществу ► Химически взаимодействующие Ускоряют или замедляют спекание в зави-симости от природы с ос- новным веществом с образующегося соединения образованием новых соединений
Влияние добавок (примесей) на спекание массивных катализаторов Вид добавки или примеси Эффекты Несовпадение зарядов катионов: ► Образующие твердые растворы, т. е. полностью растворимые в появле- ние вакансий в катионной или анионной подрешётке оксида кристалли-ческой решетке рост спекаемости. основного вещества Совпадение зарядов катионов: (на примере оксидных систем) уменьше-ние параметра решетки из-за разницы в радиусах падение скорости спекания, и наоборот (для кубической Ускоряют спекание вследствие ► Нерастворимые, но решетки). интенси-фикации процессов легкоплавкие, или дающие массопереноса через жидкую расплав эвтектики при взаи- среду модействии с основным веществом Замедляют спекание, стерически ► Тугоплавкие, инертные по затрудняя слияние частиц отношению к основному основного вещества веществу ► Химически взаимодействующие Ускоряют или замедляют спекание в зави-симости от природы с ос- новным веществом с образующегося соединения образованием новых соединений
 Спекание нанесенных катализаторов
Спекание нанесенных катализаторов
 Кинетика спекания нанесенных катализаторов Механизм переноса материала Миграция наночастиц катализатора по поверхности носителя Распределение частиц по размерам Лог-нормальное распределение, “хвост” Отрыв атомов (или простых ионов) от нано-частиц и их миграция по поверхности носителя Перенос компонентов катализатора через газовую (или жидкую) среду “Хвост” вперёд Общее кинетическое уравнение для удельной поверхности: S и S 0 – текущее и начальное значения, – время, k, n – константы
Кинетика спекания нанесенных катализаторов Механизм переноса материала Миграция наночастиц катализатора по поверхности носителя Распределение частиц по размерам Лог-нормальное распределение, “хвост” Отрыв атомов (или простых ионов) от нано-частиц и их миграция по поверхности носителя Перенос компонентов катализатора через газовую (или жидкую) среду “Хвост” вперёд Общее кинетическое уравнение для удельной поверхности: S и S 0 – текущее и начальное значения, – время, k, n – константы
 Способы повышения устойчивости катализаторов к спеканию нанесенных При приготовлении нанесенных катализаторов нужно обеспечивать протекание тех физико-химических процессов, которые способствуют достижению высокой прочности связи частиц активного компонента с носителем, что затрудняет их спекание путём миграции и слияния 2, 1 2 3, 1 + 3 3 2 2, 3 1 - газовая (жидкая) среда; 2, 3 – взаимодействующие твердые фазы Работа Wa образования контакта сечением S (уравнение Дюпрэ): Wa = ( 2, 1 + 3, 1 2, 3)S Условие высокой прочности связи между фазами 2 и 3: площадь контакта S и поверхностные натяжения 2, 1 и 3, 1 – велики, тогда как 2, 3 – малó
Способы повышения устойчивости катализаторов к спеканию нанесенных При приготовлении нанесенных катализаторов нужно обеспечивать протекание тех физико-химических процессов, которые способствуют достижению высокой прочности связи частиц активного компонента с носителем, что затрудняет их спекание путём миграции и слияния 2, 1 2 3, 1 + 3 3 2 2, 3 1 - газовая (жидкая) среда; 2, 3 – взаимодействующие твердые фазы Работа Wa образования контакта сечением S (уравнение Дюпрэ): Wa = ( 2, 1 + 3, 1 2, 3)S Условие высокой прочности связи между фазами 2 и 3: площадь контакта S и поверхностные натяжения 2, 1 и 3, 1 – велики, тогда как 2, 3 – малó
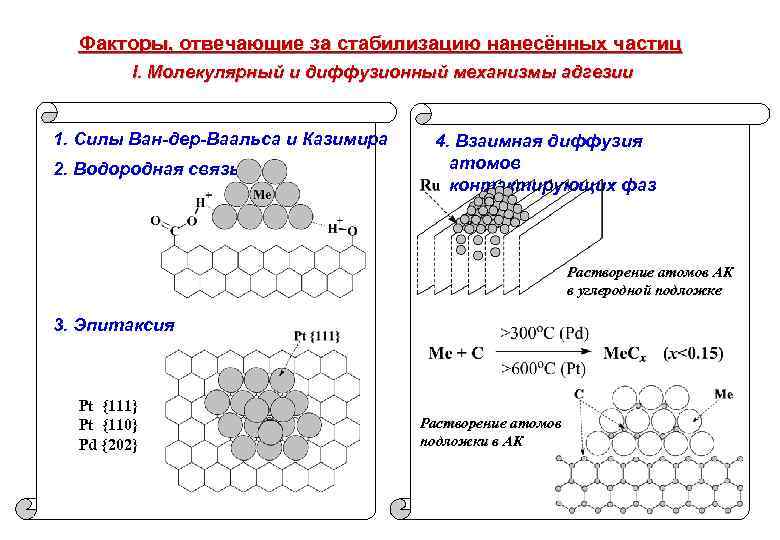 Факторы, отвечающие за стабилизацию нанесённых частиц I. Молекулярный и диффузионный механизмы адгезии 1. Силы Ван-дер-Ваальса и Казимира 2. Водородная связь 4. Взаимная диффузия атомов контактирующих фаз Растворение атомов АК в углеродной подложке 3. Эпитаксия Pt {111} Pt {110} Pd {202} Растворение атомов подложки в АК
Факторы, отвечающие за стабилизацию нанесённых частиц I. Молекулярный и диффузионный механизмы адгезии 1. Силы Ван-дер-Ваальса и Казимира 2. Водородная связь 4. Взаимная диффузия атомов контактирующих фаз Растворение атомов АК в углеродной подложке 3. Эпитаксия Pt {111} Pt {110} Pd {202} Растворение атомов подложки в АК
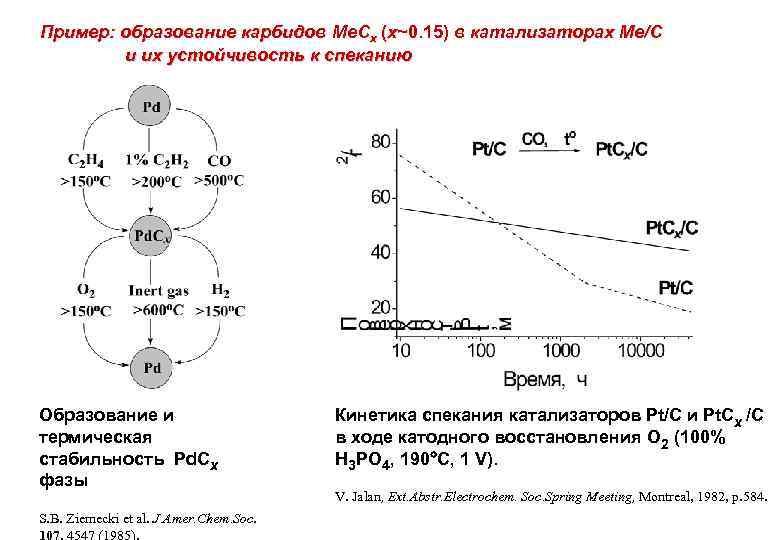 Пример: образование карбидов Me. Cx (х~0. 15) в катализаторах Me/C и их устойчивость к спеканию Образование и термическая стабильность Pd. Cx фазы S. B. Ziemecki et al. J. Amer. Chem. Soc. 107, 4547 (1985). Кинетика спекания катализаторов Pt/C и Pt. Cx /C в ходе катодного восстановления O 2 (100% H 3 PO 4, 190 C, 1 V). V. Jalan, Ext. Abstr. Electrochem. Soc. Spring Meeting, Montreal, 1982, p. 584.
Пример: образование карбидов Me. Cx (х~0. 15) в катализаторах Me/C и их устойчивость к спеканию Образование и термическая стабильность Pd. Cx фазы S. B. Ziemecki et al. J. Amer. Chem. Soc. 107, 4547 (1985). Кинетика спекания катализаторов Pt/C и Pt. Cx /C в ходе катодного восстановления O 2 (100% H 3 PO 4, 190 C, 1 V). V. Jalan, Ext. Abstr. Electrochem. Soc. Spring Meeting, Montreal, 1982, p. 584.
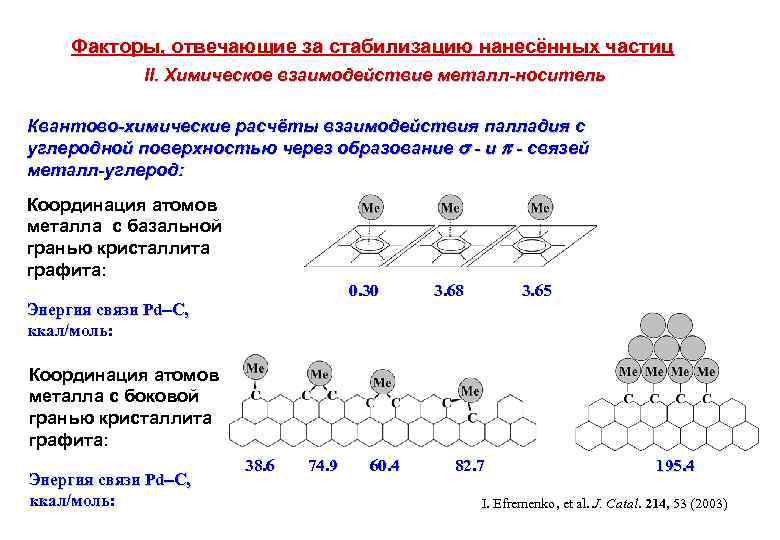 Факторы, отвечающие за стабилизацию нанесённых частиц II. Химическое взаимодействие металл-носитель Квантово-химические расчёты взаимодействия палладия с углеродной поверхностью через образование - и - связей металл-углерод: Координация атомов металла с базальной гранью кристаллита графита: 0. 30 Энергия связи Pd C, ккал/моль: 3. 68 3. 65 Координация атомов металла с боковой гранью кристаллита графита: Энергия связи Pd C, ккал/моль: 38. 6 74. 9 60. 4 82. 7 195. 4 I. Efremenko, et al. J. Catal. 214, 53 (2003)
Факторы, отвечающие за стабилизацию нанесённых частиц II. Химическое взаимодействие металл-носитель Квантово-химические расчёты взаимодействия палладия с углеродной поверхностью через образование - и - связей металл-углерод: Координация атомов металла с базальной гранью кристаллита графита: 0. 30 Энергия связи Pd C, ккал/моль: 3. 68 3. 65 Координация атомов металла с боковой гранью кристаллита графита: Энергия связи Pd C, ккал/моль: 38. 6 74. 9 60. 4 82. 7 195. 4 I. Efremenko, et al. J. Catal. 214, 53 (2003)
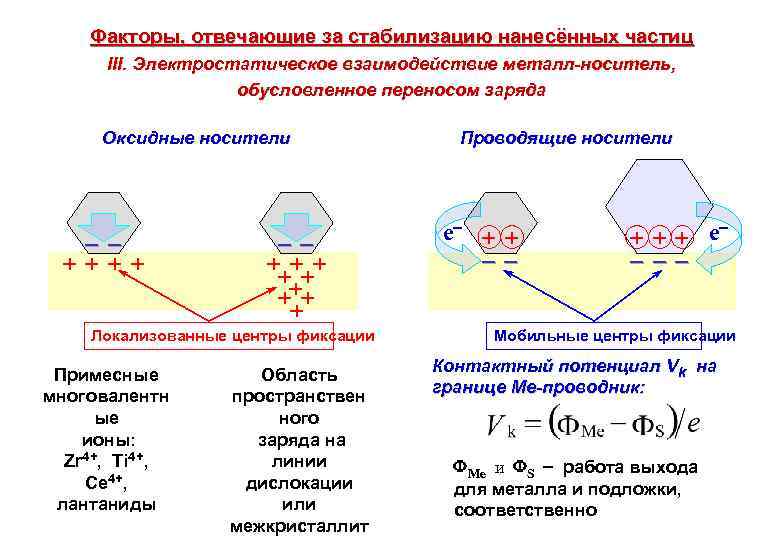 Факторы, отвечающие за стабилизацию нанесённых частиц III. Электростатическое взаимодействие металл-носитель, обусловленное переносом заряда Оксидные носители ++++ +++ ++ + Локализованные центры фиксации Примесные многовалентн ые ионы: Zr 4+, Ti 4+, Ce 4+, лантаниды Область пространствен ного заряда на линии дислокации или межкристаллит Проводящие носители e + + +++ e Мобильные центры фиксации Контактный потенциал Vk на границе Me-проводник: Me и S работа выхода для металла и подложки, соответственно
Факторы, отвечающие за стабилизацию нанесённых частиц III. Электростатическое взаимодействие металл-носитель, обусловленное переносом заряда Оксидные носители ++++ +++ ++ + Локализованные центры фиксации Примесные многовалентн ые ионы: Zr 4+, Ti 4+, Ce 4+, лантаниды Область пространствен ного заряда на линии дислокации или межкристаллит Проводящие носители e + + +++ e Мобильные центры фиксации Контактный потенциал Vk на границе Me-проводник: Me и S работа выхода для металла и подложки, соответственно
 Величина работы выхода зависит от: • микроструктуры вещества, • кристаллохимии поверхности, • наличия объёмных или поверхностных примесей, • размера кристаллитов: (для сферических частиц) r радиус частицы (нм), , константы: ~ 0. 2 - 0. 3 нм, / ~ 1 нм 1 Работа выхода, (e. V), для металлов и углей
Величина работы выхода зависит от: • микроструктуры вещества, • кристаллохимии поверхности, • наличия объёмных или поверхностных примесей, • размера кристаллитов: (для сферических частиц) r радиус частицы (нм), , константы: ~ 0. 2 - 0. 3 нм, / ~ 1 нм 1 Работа выхода, (e. V), для металлов и углей
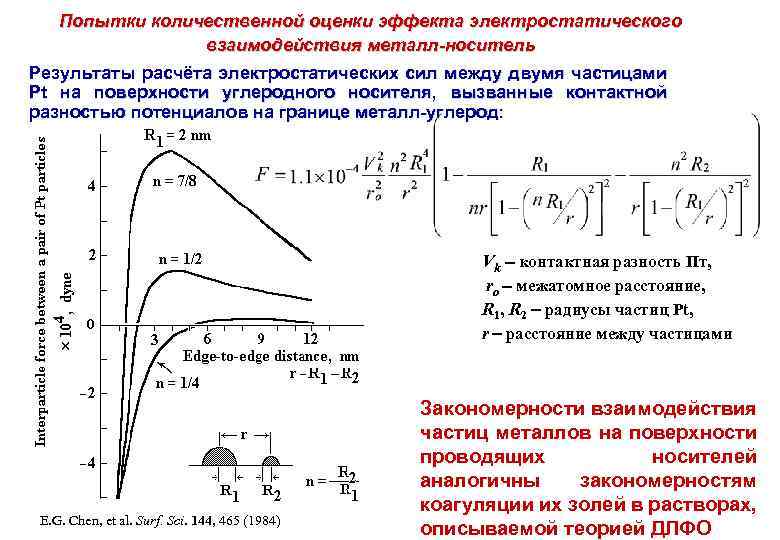 Попытки количественной оценки эффекта электростатического взаимодействия металл-носитель Результаты расчёта электростатических сил между двумя частицами Pt на поверхности углеродного носителя, вызванные контактной разностью потенциалов на границе металл-углерод: Vk контактная разность Пт, ro межатомное расстояние, R 1, R 2 радиусы частиц Pt, r расстояние между частицами E. G. Chen, et al. Surf. Sci. 144, 465 (1984) Закономерности взаимодействия частиц металлов на поверхности проводящих носителей аналогичны закономерностям коагуляции их золей в растворах, описываемой теорией ДЛФО
Попытки количественной оценки эффекта электростатического взаимодействия металл-носитель Результаты расчёта электростатических сил между двумя частицами Pt на поверхности углеродного носителя, вызванные контактной разностью потенциалов на границе металл-углерод: Vk контактная разность Пт, ro межатомное расстояние, R 1, R 2 радиусы частиц Pt, r расстояние между частицами E. G. Chen, et al. Surf. Sci. 144, 465 (1984) Закономерности взаимодействия частиц металлов на поверхности проводящих носителей аналогичны закономерностям коагуляции их золей в растворах, описываемой теорией ДЛФО
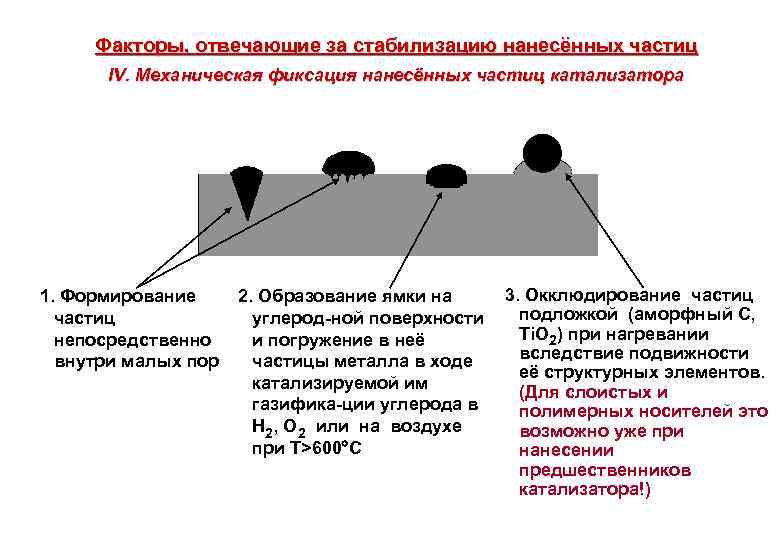 Факторы, отвечающие за стабилизацию нанесённых частиц IV. Механическая фиксация нанесённых частиц катализатора 1. Формирование частиц непосредственно внутри малых пор 3. Окклюдирование частиц 2. Образование ямки на подложкой (аморфный С, углерод-ной поверхности Ti. O 2) при нагревании и погружение в неё вследствие подвижности частицы металла в ходе её структурных элементов. катализируемой им (Для слоистых и газифика-ции углерода в полимерных носителей это H 2, O 2 или на воздухе возможно уже при T>600 C нанесении предшественников катализатора!)
Факторы, отвечающие за стабилизацию нанесённых частиц IV. Механическая фиксация нанесённых частиц катализатора 1. Формирование частиц непосредственно внутри малых пор 3. Окклюдирование частиц 2. Образование ямки на подложкой (аморфный С, углерод-ной поверхности Ti. O 2) при нагревании и погружение в неё вследствие подвижности частицы металла в ходе её структурных элементов. катализируемой им (Для слоистых и газифика-ции углерода в полимерных носителей это H 2, O 2 или на воздухе возможно уже при T>600 C нанесении предшественников катализатора!)
 Выводы: для достижения высокой устойчивости нанесенных катализаторов к спеканию требуется использование тугоплавких носителей (большое 2, 1) или повышение температуры плавления частиц катализатора (большое 3, 1) уменьшение межфазного натяжения 2, 3 посредством: эпитаксиального и химического взаимодействия, диффузии атомов одного из компонентов вглубь решётки друго создания разности потенциалов на границе раздела фаз, образования донорно-акцепторных связей с кислотными (льюи или бренстедовскими) поверхностными центрами носителя увеличение поверхности S контакта фаз за счет: локализации частиц в малых порах носителя, создания микрошероховатости поверхности носителя увеличение протяженности путей миграции частиц и атомов активного компонента: высокая удельная поверхность носителя, высокая концентрация протяжённых дефектов на носителе узкое распределение нанесённых частиц по размерам
Выводы: для достижения высокой устойчивости нанесенных катализаторов к спеканию требуется использование тугоплавких носителей (большое 2, 1) или повышение температуры плавления частиц катализатора (большое 3, 1) уменьшение межфазного натяжения 2, 3 посредством: эпитаксиального и химического взаимодействия, диффузии атомов одного из компонентов вглубь решётки друго создания разности потенциалов на границе раздела фаз, образования донорно-акцепторных связей с кислотными (льюи или бренстедовскими) поверхностными центрами носителя увеличение поверхности S контакта фаз за счет: локализации частиц в малых порах носителя, создания микрошероховатости поверхности носителя увеличение протяженности путей миграции частиц и атомов активного компонента: высокая удельная поверхность носителя, высокая концентрация протяжённых дефектов на носителе узкое распределение нанесённых частиц по размерам
 3. 5. 2. Устойчивость к каталитическим ядам Контактные яды уменьшают общую активность (Sуд ), изменяют Еакт и селективность катализатора вследствие химического взаимодействия с ним Необратимо сорбирующиеся КАТАЛИТИЧЕСКИЕ ЯДЫ Обратимо сорбирующиеся Способы борьбы с ядами: • Предварительное извлечение ядов из реакционной смеси • Изменение условий (Р, Т) проведения каталитического процесса • Периодическая химическая регенерация катализатора Приёмы повышения устойчивости катализаторов к ядам: • Использование носителей с высоким сродством поверхности к яду, • Повышение дисперсности частиц активного компонента, • Адекватное распределение активного компонента в порах носителя, • Использование структурных промоторов
3. 5. 2. Устойчивость к каталитическим ядам Контактные яды уменьшают общую активность (Sуд ), изменяют Еакт и селективность катализатора вследствие химического взаимодействия с ним Необратимо сорбирующиеся КАТАЛИТИЧЕСКИЕ ЯДЫ Обратимо сорбирующиеся Способы борьбы с ядами: • Предварительное извлечение ядов из реакционной смеси • Изменение условий (Р, Т) проведения каталитического процесса • Периодическая химическая регенерация катализатора Приёмы повышения устойчивости катализаторов к ядам: • Использование носителей с высоким сродством поверхности к яду, • Повышение дисперсности частиц активного компонента, • Адекватное распределение активного компонента в порах носителя, • Использование структурных промоторов
 Устойчивость активного компонента к блокировке Блокировка поверхности активного компонента происходит из-за отложения высокомолекулярных продуктов (кокс, полимеры) вследствие побочных каталитических реакций или использования органических предшественников уже при синтезе катализатора. Уменьшает общую активность (Sуд ), но обычно не изменяет Еакт. Устранение эффекта блокировки: • Химическая модификация поверхности катализатора для подавления центров, ответственных за побочные процессы, • Периодическое выжигание углеродистых отложений В случае полимерных или слоистых носителей блокировка частиц нанесенного активного компонента может быть вызвана набуханием носителя (т. е. изменением структуры его пористого пространства) в реакционной непосредственно при или среде синтезе этих катализаторов
Устойчивость активного компонента к блокировке Блокировка поверхности активного компонента происходит из-за отложения высокомолекулярных продуктов (кокс, полимеры) вследствие побочных каталитических реакций или использования органических предшественников уже при синтезе катализатора. Уменьшает общую активность (Sуд ), но обычно не изменяет Еакт. Устранение эффекта блокировки: • Химическая модификация поверхности катализатора для подавления центров, ответственных за побочные процессы, • Периодическое выжигание углеродистых отложений В случае полимерных или слоистых носителей блокировка частиц нанесенного активного компонента может быть вызвана набуханием носителя (т. е. изменением структуры его пористого пространства) в реакционной непосредственно при или среде синтезе этих катализаторов
 3. 6. Гидродинамические характеристики катализаторов Гидродинамические характеристики катализаторного слоя определяются размером и формой его зерен, которые задаются при их формовании: P гидравлическое сопротивление слоя катализатора высотой Н, G, массовая скорость и удельная масса реакционной смеси, соответственно, доля свободного объема между зёрнами в слое, Ф фактор формы частиц (наименьший для сферических частиц), n показатель степени, r приведенный радиус зерна (r = занимаемый объём / внешняя поверхность), f коэффициент гидравлического сопротивления, значение которого зависит от критерия Рейнольдса (Re): при Re <30 при Re = 30 -7000 Ламинарное течение Турбулентное течение
3. 6. Гидродинамические характеристики катализаторов Гидродинамические характеристики катализаторного слоя определяются размером и формой его зерен, которые задаются при их формовании: P гидравлическое сопротивление слоя катализатора высотой Н, G, массовая скорость и удельная масса реакционной смеси, соответственно, доля свободного объема между зёрнами в слое, Ф фактор формы частиц (наименьший для сферических частиц), n показатель степени, r приведенный радиус зерна (r = занимаемый объём / внешняя поверхность), f коэффициент гидравлического сопротивления, значение которого зависит от критерия Рейнольдса (Re): при Re <30 при Re = 30 -7000 Ламинарное течение Турбулентное течение
 Примеры носителей и катализаторов различной формы Выбор формы зерна – это компромисс между стремлением не превысить давление, но уменьшить диффузионное торможение, а для процессов, протекающих в кинетическом режиме, – увеличить производительность единицы объёма реактора. Оптимальные размер и форма зёрен катализатора отвечают протеканию каталитического процесса в переходной области, т. е. на границе между кинетическим и диффузионным режимом
Примеры носителей и катализаторов различной формы Выбор формы зерна – это компромисс между стремлением не превысить давление, но уменьшить диффузионное торможение, а для процессов, протекающих в кинетическом режиме, – увеличить производительность единицы объёма реактора. Оптимальные размер и форма зёрен катализатора отвечают протеканию каталитического процесса в переходной области, т. е. на границе между кинетическим и диффузионным режимом


