lektsia_2_16-17_fermenty (1).ppt
- Количество слайдов: 146

Лекция № 2 16 17 учебный год ТЕМА: Ферменты. Общие свойства ферментов Классификация ферментов Гидролазы, основные представители. Примененеие гидролаз в медицине

Цель l Дать представление о ферментах, как о биологических катализаторах белковой природы. l Ознакомить с классификацией ферментов. l Рассмотреть класс гидролаз, их основные представители в пищеварительных соках, их значение и применение в медицине

ПЛАН ЛЕКЦИИ l Ферменты, понятие l Общие свойства ферментов и классификация ферментов l Гидролазы, основные представители. Применение гидролаз в медицине

Ферменты l Ферменты это специализированные белки, образующиеся в клетках и способные ускорять химические процессы, l т. е. ферменты биологические катализаторы.

l Термин «фермент» произошел от лат. «fermentum» закваска, бродило. l Был предложен голландским ученым Ван Гельмонтом в начале XVII века.

l Долгое время многие ученые продолжали считать ферменты, выделяемые клетками, чем то принципиально отличным от внутриклеточных ферментов, для которых было предложено особое название «энзимы» l В англоязычной литературе употребляется термин «энзим» от греч. «en zyme» – в закваске.

Сходство ферментов и неорганических катализаторов: катализируют только энергетически возможные реакции; l не изменяют равновесия в обратимых реакциях; l не изменяют направление реакции; l не расходуются в результате реакции. l

Отличия между ферментами и неорганическими катализаторами l l l Ферменты имеют более сложное химическое строение Ферменты обладают высокой мощностью действия; Ферменты обладают специфичностью Ферменты это вещества с регулируемой активностью; Ферменты действуют в мягких условиях
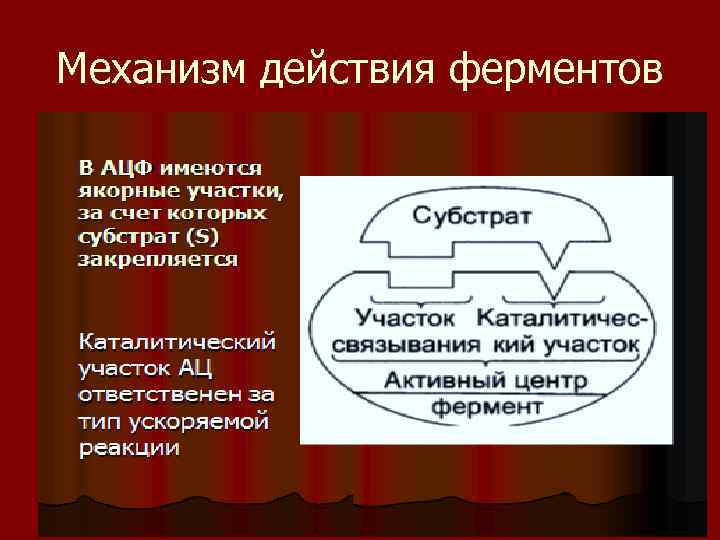
Механизм действия ферментов

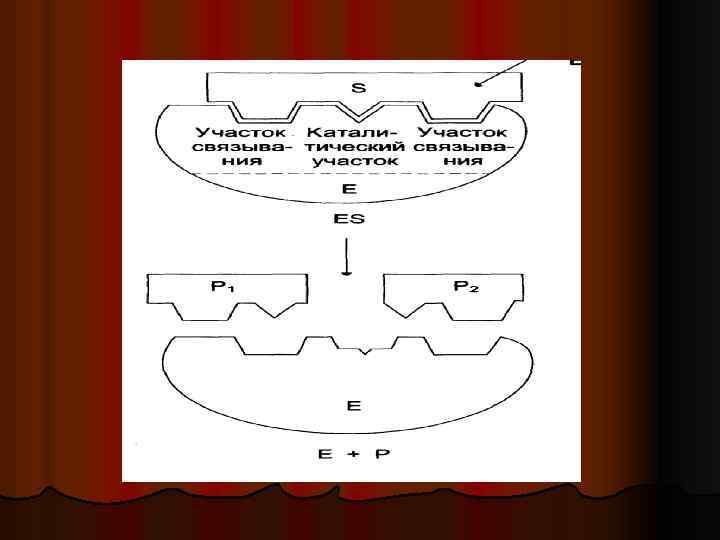
Первая стадия l фермент отличается от белка наличием активного центра (АЦФ участка, с помощью которого фермент соединяется с субстратом и ускоряет реакцию. Долгое время считали, что между ферментом и субстратом имеется точное соответствие ( «ключ к замку» ). Однако сейчас принято считать, что АЦ фермента приспосабливается к субстрату в ходе реакции (теория вынужденного соответствия).

Первая стадия l 1 этап сближение и ориентации субстрата относительно активного центра фермента l Е+S Е S l Е – фермент l S субстрат

Вторая стадия l 2 этап образование ЕS комплекса в результате индуцированного взаимодействия l. Е +S ЕS
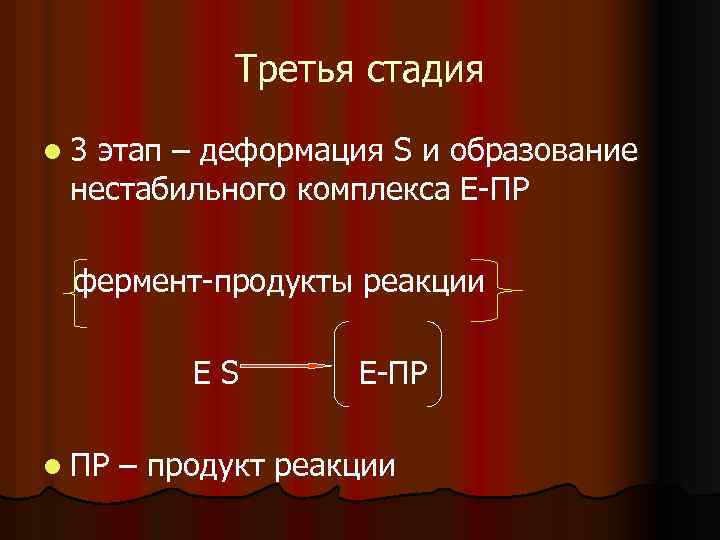
Третья стадия l 3 этап – деформация S и образование нестабильного комплекса Е ПР фермент продукты реакции ЕS l ПР Е ПР – продукт реакции

Вторая стадия l функционально активные группы АЦ фермента действуют на субстрат, дестабилизируя связи в нем, вызывая изменение конфигурации субстрата, поляризацию его молекулы, растяжение связей и т. д. Это приводит к химическому преобразованию субстрата (т. е. к протеканию реакции) и образованию продуктов реакции, которые некоторое время находятся в связи с ферментом
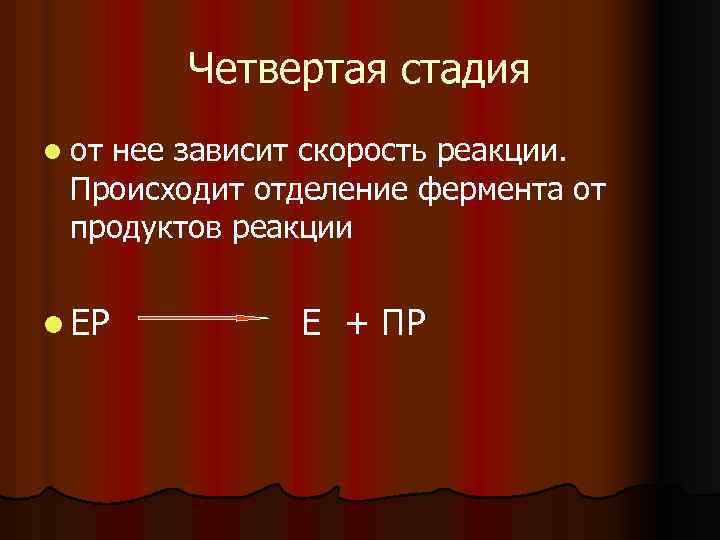
Четвертая стадия l от нее зависит скорость реакции. Происходит отделение фермента от продуктов реакции l ЕР Е + ПР

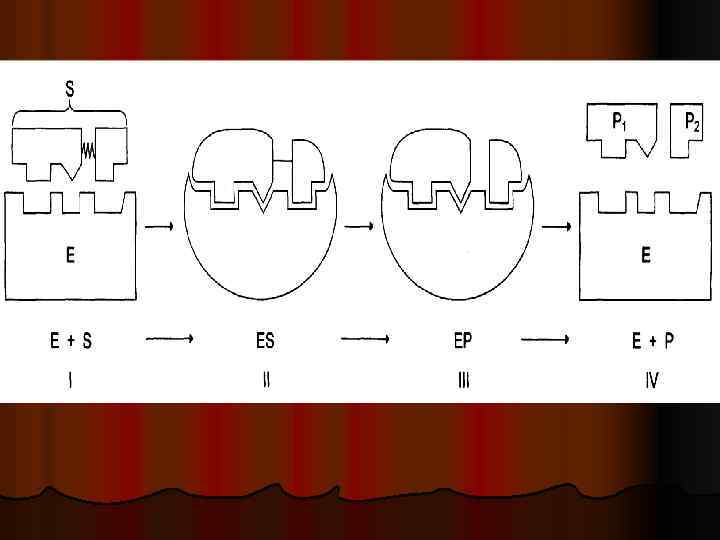

Этапы ферментативного катализа l 1 этап сближение и ориентации субстрата относительно активного центра фермента l 2 этап образование ЕS комплекса в результате индуцированного взаимодействия

l 3 этап – деформация S и образование нестабильного комплекса Е ПР l 4 этап – распад комплекса с освобождением продуктов реакции из активного центра фермента и освобождением фермента

l l l Любая химическая реакция происходит при столкновении молекул реагирующих веществ. Движение молекул реагирующих веществ в системе зависит от наличия свободной потенциальной энергии. Для протекания химической реакции необходимо, чтобы молекулы исходных веществ достигли переходного состояния, т. е. чтобы реагирующие молекулы имели достаточно энергии для преодоления энергетического барьера. Энергетический барьер – это минимальное количество энергии, необходимое для того, чтобы все молекулы стали реакционно способными. Разность значений свободной энергии исходного продукта (субстрата) и энергии, которая потребуется для того, чтобы субстрат перешел в переходное состояние, соответствует свободной энергии активации. Скорость любой химической реакции пропорциональна концентрации молекул, находящихся в переходном состоянии.

l Все катализаторы, в т. ч. ферменты понижают энергетический барьер реакции (снижают энергию активации), что делает возможным более быстрое протекание реакции.

Общие свойства ферментов

l 1. Ферменты – это вещества белковой природы, поэтому они обладают всеми свойствами, характерными для белков

l 2. имеют сложное химическое строение. l Различают ферменты протеины однокомпонентные ферменты l. И ферменты протеиды – двукомпонентные ферменты

Однокомпонентные ферменты l Специфические простые белки. l Каталитическая активность зависит от наличия активного центра (АЦ) l АЦ имеет два участка: каталитический и субстратный l У некоторых ферментов имеется так называемый аллостерический центр, участвующий в регуляции АЦ


Активный центр фермента (АЦФ) l Это уникальная для каждого Фермента совокупность функциональных групп АК остатков (сер. , цис. , гис. И др) расположенных на поверхности ферментов и строго ориентированных в пространстве за счет третичной и иногда четвертичной структуры Ф.

Ферменты протеиды (двукомпонентные) (холоферменты) l Состоят из белковой части – апофермент l И вещества небелковой природы – кофермент l Роль коферментов выполняют производные различных витаминов, металлы (железо, медь)

l Апофермент обуславливает субстратную специфичность фермента (на что действует фермент) l Кофермент – обеспечивает специфичность действия фермента, тип реакции, которую ведет фермент

l Двукомпонентные ферменты могут иметь несколько молекулярных форм, которые называются изоферментами

Изоферменты — молекулярные формы ферментов, катализирующие одну и ту же реакцию с одним и тем же субстратом, но в различных условиях. l Они различаются по строению апофермента, по физико химическим свойствам, по сродству апофермента к субстрату l Коферменты изоферментов одинаковы, поэтому биологическое действие изоферментов одинаково. Различия проявляются в аминокислотном составе полипептидных цепей, вследствие этого изоферменты имеют различную молекулярную массу, различный по величине заряд и легко разделяются при электрофорезе. l

Лактатдегидрогеназа (ЛДГ) l l l ускоряет реакцию дегидрирования молочной кислоты, имеет пять изоферментов, которые отличаются соотношением различных по строению полипептидных цепей, но имеют одинаковый кофермент — НАД. В состав апофермента ЛДГ входят четыре полипептидные цепи. Различают Н цепи (heart сердце) и М цепи (muscle мышцы). Изоферменты ЛДГ отличаются соотношением входящих в их состав цепей.
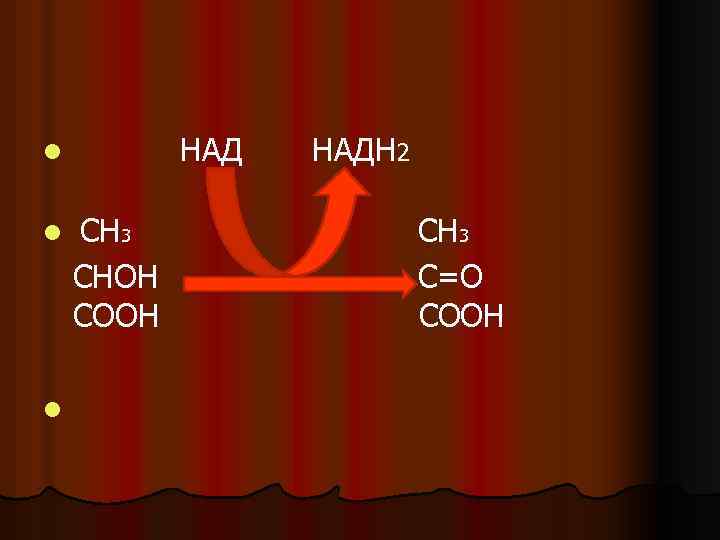
НАД l l l СН 3 СНОН СООН НАДН 2 СН 3 С=О СООН

l Изоф Типы пп цепей l ЛДГ 1 4 цепи Н типа l ЛДГ 2 3 цепи Н типа и 1 цепь М типа l ЛДГ 3 2 цепи Н типа 2 цепи М типа l ЛДГ 4 – 1 цепь Н типа 3 цепи М типа l ЛДГ 5 4 цепи М типа

Место нахождения l ЛДГ 1 в сердце; l ЛДГ 2 в основном, в сердце, почках l ЛДГ 3 в легких l ЛДГ 4, в печени, мышцах l ЛДГ 5 в печени
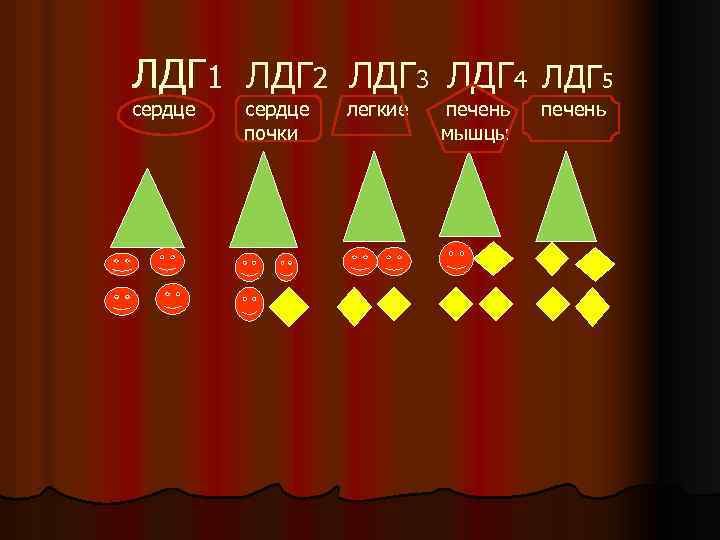
ЛДГ 1 ЛДГ 2 ЛДГ 3 ЛДГ 4 сердце почки легкие печень мышцы ЛДГ 5 печень

l Изоферменты позволяют лучше приспособиться к изменению внешних и внутренних факторов l и ведут одну и ту же реакцию в различных метаболических условиях: l при различной концентрации субстрата и продуктов реакции, l разных значениях р. Н, l имеют разную чувствительность к ингибиторам.

3. Ферменты обладают специфичностью действия l способны избирательно действовать на определенный субстрат и ускорять определенную химическую реакцию. l Таким образом, различают; субстратную специфичность и специфичность действия. l По степени проявления субстратная специфичность разделяется на абсолютную и относительную.
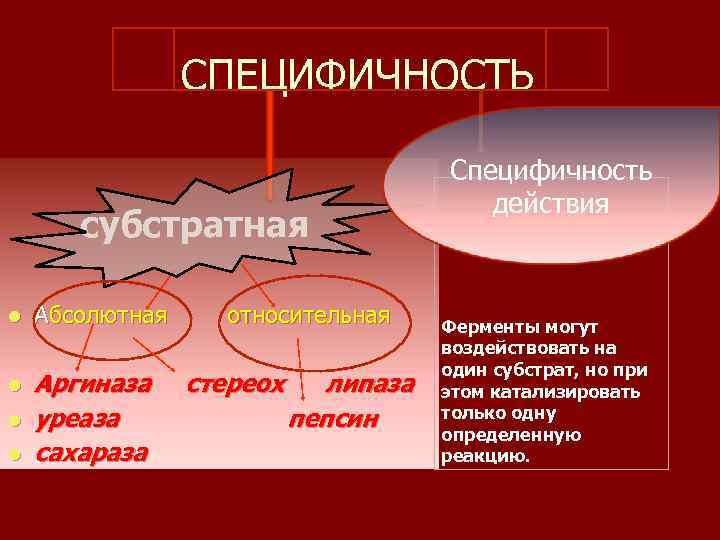
СПЕЦИФИЧНОСТЬ субстратная l Абсолютная l Аргиназа стереох липаза уреаза пепсин сахараза l l относительная Специфичность действия Ферменты могут воздействовать на один субстрат, но при этом катализировать только одну определенную реакцию.

При абсолютной (индивидуальной) специфичности фермент воздействует на один единственный субстрат. Примером может служить специфичность аргиназы, расщепляющей только аргинин; l уреазы, катализирующей превращения только мочевины; l сахаразы, гидролизующей только сахарозу. l

аргиназа l Аргинин орнитин +мочевина l сахараза l Сахароза глюкоза + фруктоза l

Стереохимическая субстратная специфичность — — высшее проявление абсолютной субстратной специфичности. Фермент катализирует превращение только одного из возможных стереоизомеров субстрата. Например, есть оксидазы L аминокислот и оксидазы Д аминокислот. l Фумараза действует только на фумаровую кислоту (транс изомер) и не оказывает действия на малеиновую кислоту (цис форма l

Специфичность действия - это способность ферментов производить с субстратом лишь одно из возможных химических превращений. Ферменты могут воздействовать на один субстрат, но при этом катализировать только одну определенную реакцию. l Примером может служить мультиферментный пируватдегидрогеназный комплекс, субстратом этого комплекса является пировиноградная кислота. l Ферменты, входящие в этот комплекс, выполняют каждый свою функцию — декарбоксилаза отщепляет СО 2, дегидрогеназы дегидрируют субстрат и т. д. l
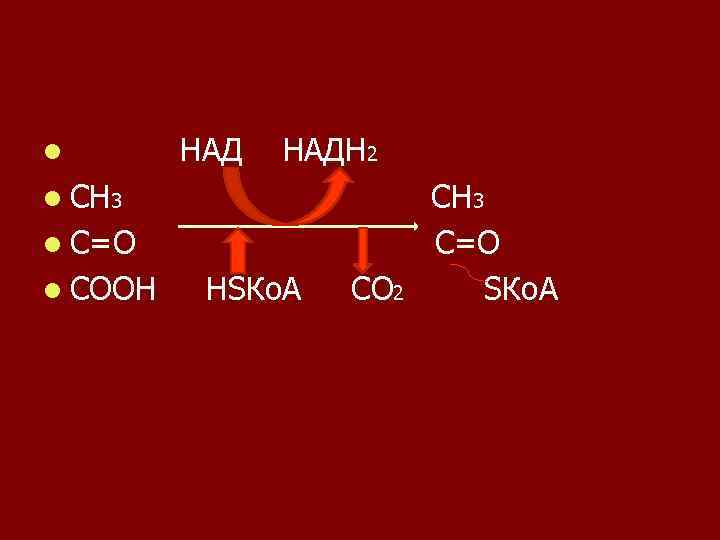
l НАДН 2 l СН 3 l С=О l СООН НSКо. А СО 2 СН 3 С=О SКо. А

Относительная (групповая) специфичность. Фермент, обладающий таким видом субстратной специфичности, может оказывать воздействие на группу сходных субстратов, имеющих одинаковый тип связи. l Например, липаза расщепляет сложноэфирные связи в липидах; l пепсин и трипсин расщепляют пептидные связи в белках. l
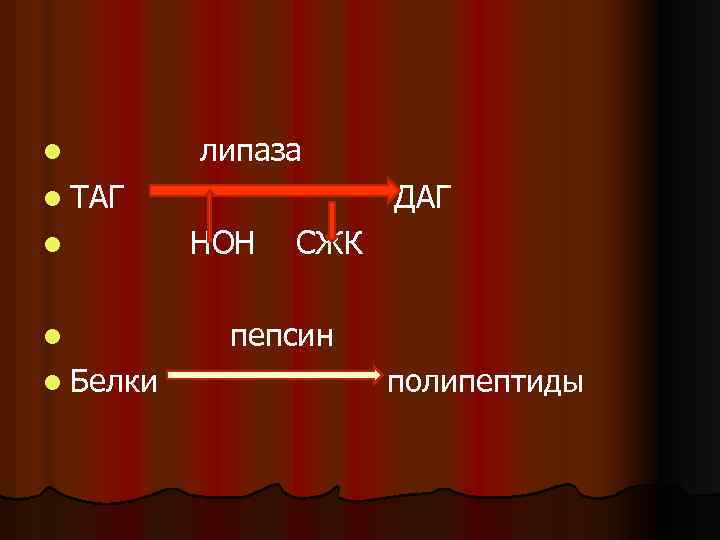
l липаза l ТАГ l l l Белки ДАГ НОН СЖК пепсин полипептиды

4. Ферменты обладают большой мощностью действия. l Большинство реакций, катализируемых ферментами, протекают в 10 100 раз быстрее, чем некатализируемые реакции. Подсчитано, что каждая молекула фермента способна ежесекундно превращать от 100 до 1000 молекул субстрата.

l Для характеристики мощности действия ферментов введено понятие катал — число молекул субстрата, подвергающееся воздействию одной молекулы фермента l в течение 1 минуты. l

l Мощность большинства ферментов равна 1000 каталов, l мощность действия каталазы — 1. 000 каталов, l амилазы — 240 000, а ацетилхолинэстеразы более 1. 000. l Высокая мощность действия ферментов обусловливает высокую скорость химических процессов в организме.

l 5. Ферменты не входят в состав конечных продуктов, катализируемых ими реакций l 6. Ферменты – это катализаторы с регулируемой активностью

Факторы, влияющие на активность ферментов Ферменттің белсенділігіне әсер ететін факторлар

Влияние р. Н среды l Оптимум l l р. Н = 4 7 1, 5 – 2, 0 8, 0 9, 0 ИЭТ ИЭН ИЭС ИЭЖ
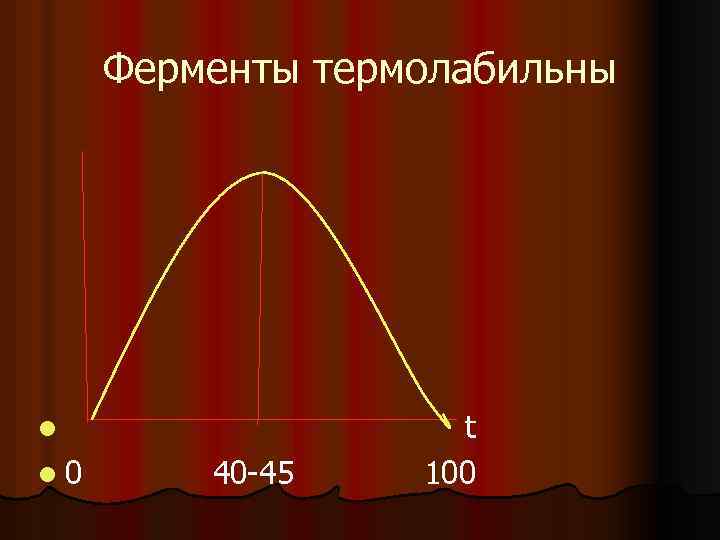
Ферменты термолабильны l l 0 40 45 t 100
l обратимая l Инактивация l необратимая
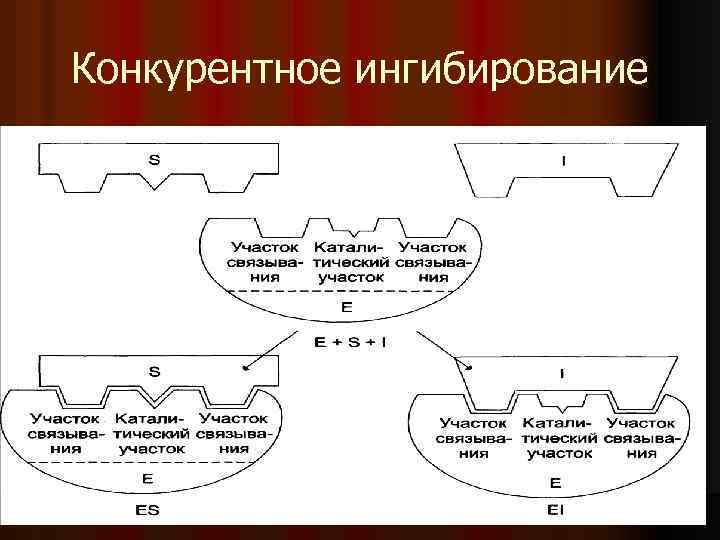
Конкурентное ингибирование
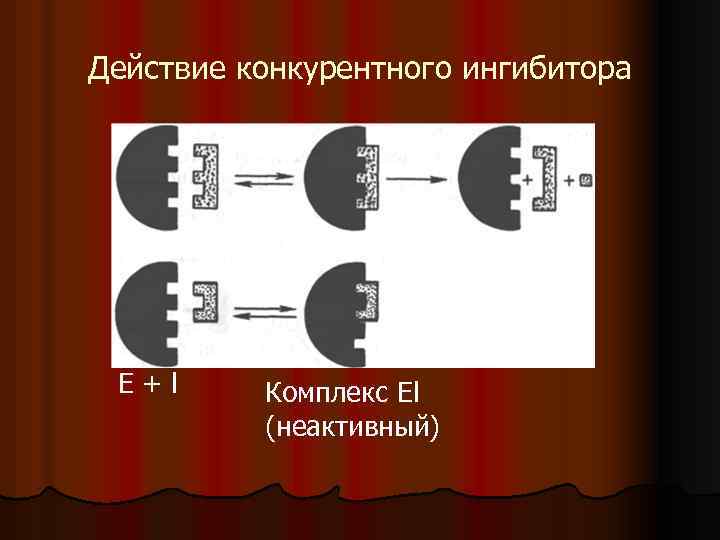
Действие конкурентного ингибитора E+l Комплекс El (неактивный)
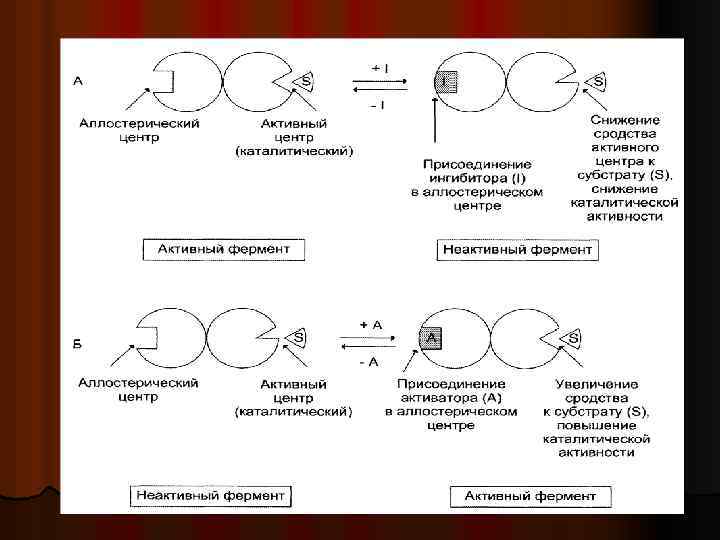
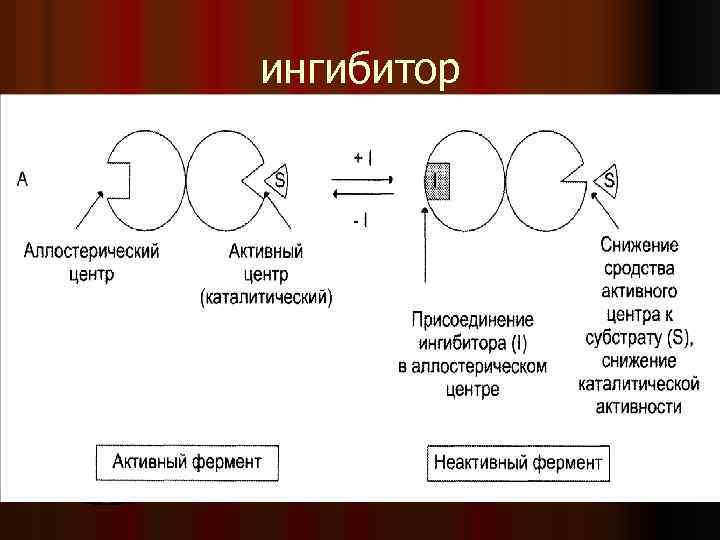
ингибитор
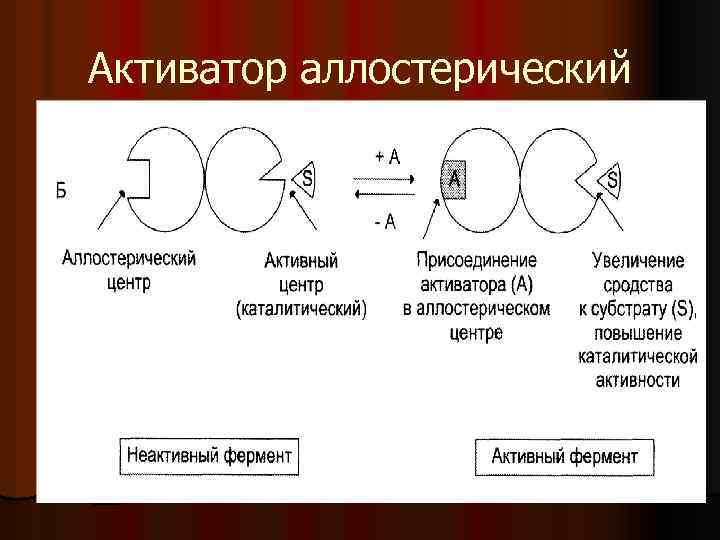
Активатор аллостерический
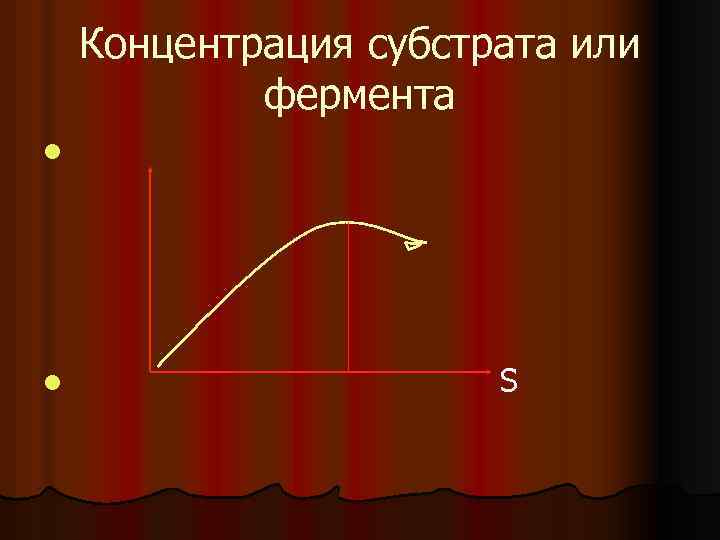
Концентрация субстрата или фермента l l S


l 1 класс Оксидоредуктазы l 2 класс Трансферазы l 3 класс Гидролазы l 4 класс Лиазы. l 5 класс Изомеразы – l 6 класс Лигазы или синтетазы – ускоряют процесс синтеза с использованием энергии АТФ

Номенклатура и классификация ферментов l класс l подкласс, l подподкласс, lв каждом подподклассе обозначен порядковый номер представителя.

l Поэтому для каждого фермента существует шифр, состоящий из 4 цифр – первая показывает номер класса, l вторая – номер подкласса, l третья – номер подподкласса, l четвертая – место фермента в подподклассе.

Шифр для липазы поджелудочной железы – 3. 1. 1. 3. , это означает, что липаза п/ж относится к гидролазам, (третий класс, т. е. ускоряет гидролиз), l к первому подклассу – эстеразам (т. е. ускоряет гидролиз сложно эфирных связей), l к первому подподклассу (т. е. ускоряет гидролиз сложно эфирных связей, образованных карбоновыми кислотами), место в подподклассе – третье. l l

1 класс Оксидоредуктазы l– ускоряют окислительно восстановительные реакции.
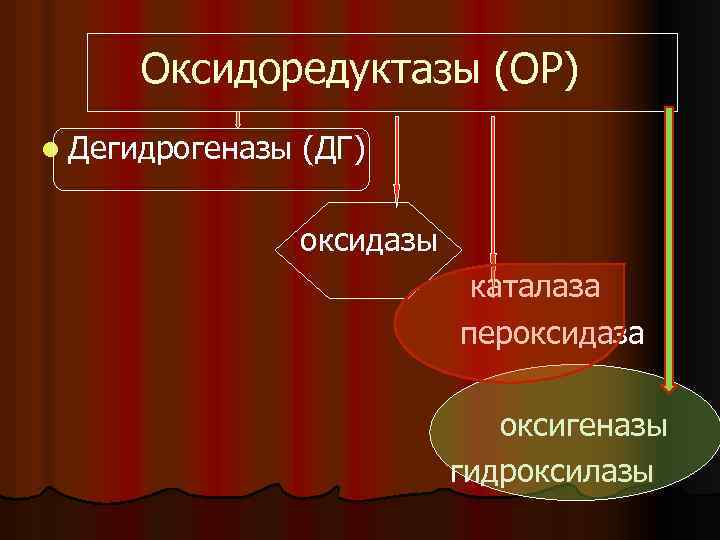
Оксидоредуктазы (ОР) l Дегидрогеназы (ДГ) оксидазы каталаза пероксидаза оксигеназы гидроксилазы
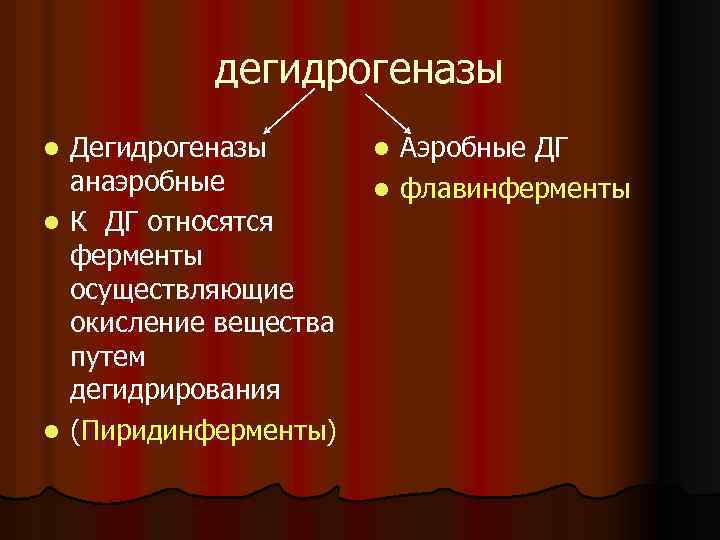
дегидрогеназы l l l Дегидрогеназы анаэробные К ДГ относятся ферменты осуществляющие окисление вещества путем дегидрирования (Пиридинферменты) Аэробные ДГ l флавинферменты l

оксидазы l Цитохромы ЦХ (гемсодержащие гемопротеиды). l ЦХ служат переносчиками электронов

гидропероксидазы l Каталаза и пероксидаза l Катализируют реакции разложения перекиси водорода

оксигеназы l Гидроксилазы и оксигеназы l Способствуют окислению субстрата, включая в его молекулу кислород l Гидроксилазы включают атом кислорода l Оксигеназы способствуют включению молекулы О 2 , вызывая окислительное расщепление двойной связи С=С

Второй класс трансферазы l 2 класс Трансферазы – катализируют перенос атомов или группы атомов от одного вещества на другое.

гидролазы l 3 класс Гидролазы – катализируют распад сложных веществ на более простые с участием воды.

лиазы l 4 класс Лиазы – катализируют распад или синтез веществ без участия воды.

изомеразы l 5 класс Изомеразы – катализируют процесс изомеризации.

Лигазы или синтетазы l 6 класс Лигазы или синтетазы – ускоряют процесс синтеза с использованием энергии АТФ

гидролазы

l Гидролазы - ферменты, широко распространенные в природе, встречаются в клетках и пищеварительных соках. Почти все гидролазы ЖКТ однокомпонентные ферменты.

l. В клетках гидролазы находятся в особых органеллах – лизосомах и потому называются лизосомальными ферментами.

ГИДРОЛАЗЫ (3 класс). Эстеразы гликозидазы l l пептид l гидролазы l l
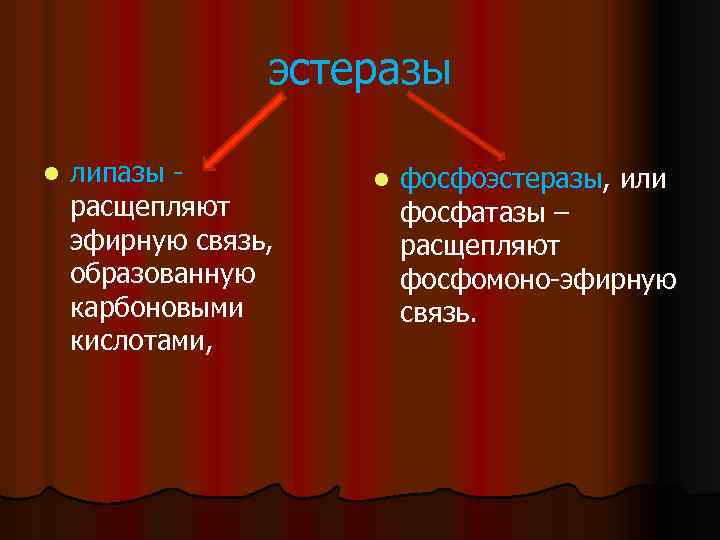
эстеразы l липазы расщепляют эфирную связь, образованную карбоновыми кислотами, l фосфоэстеразы, или фосфатазы – расщепляют фосфомоно эфирную связь.

Представители липаз l 1. липаза желудочного сока. Фермент мало активен у взрослых, активен у детей раннего возраста. р. Н среды желудка в раннем детском возрасте соответствует опт. р. Н этого фермента. Во взрослом организме липаза желудочного сока неактивна. Липаза жел. сока расщепляет только эмульгированные жиры молока.

l l l l липаза поджелудочной железы вырабатывается в неактивном состоянии, активируется желчными кислотами и их солями. Липазы желудочного и поджелудочного соков ускоряют реакции гидролиза ТАГов. 3. липаза кишечного сока образуется в небольших количествах в активном виде, ускоряет гидролиз бетта МАГов ТАГ ДАГ β МАГ НОН СЖК

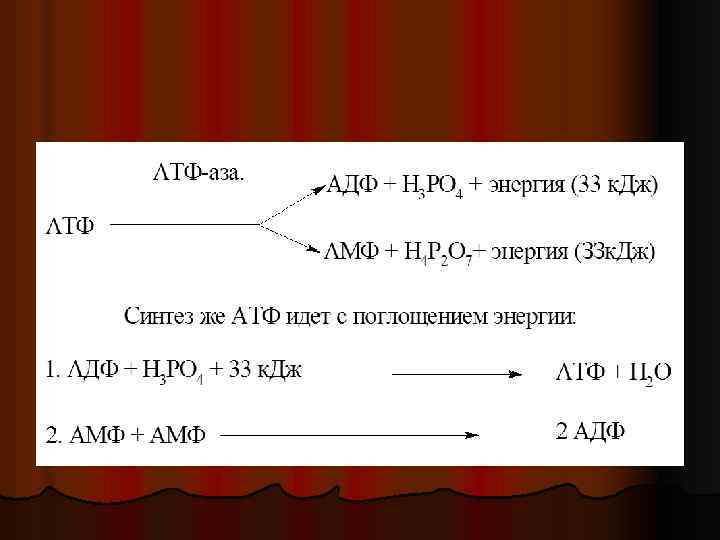
Фосфоэстеразы (или фосфатаз Ø расщепляют фосфомоноэфирную связь. l Субстратами для этих ферментов являются эфиры фосфорной кислоты. Ø АТФ аза.
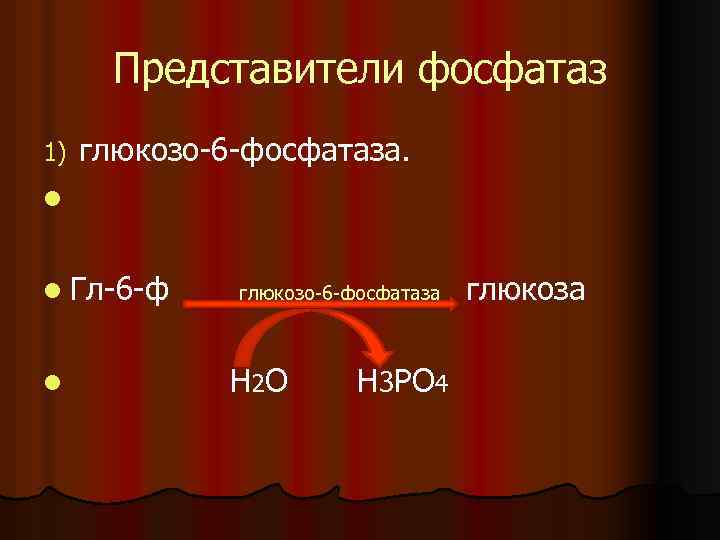
Представители фосфатаз 1) глюкозо 6 фосфатаза. l l Гл 6 ф l глюкозо 6 фосфатаза Н 2 О Н 3 РО 4 глюкоза

гликозидазы l Однокомпонентные ферменты l гликозидазы ведут гидролиз гликозидных связей, действуя на полисахариды и дисахариды

l Представители. 1) амилаза. В организме человека имеется альфа и гамма амилаза. Альфа амилаза содержится в слюне, поджелудочном соке, в клетках соединительной ткани. Субстратами альфа амилазы являются крахмал и гликоген, фермент расщепляет их до мальтозы. Под действием гамма амилазы, которая находится только в печени, гликоген расщепляется до глюкозы. 2) мальтаза встречается в клетках и кишечном соке. Фермент расщепляет мальтозу до 2 глюкоз. 3) лактаза находится в клетках грудной железы, кишечном соке. Расщепляет лактозу до бета галактозы и глюкозы 3) сахараза находится в кишечном соке, расщепляет сахарозу до глюкозы и фруктозы, в желудочном соке нет гликозидаз.
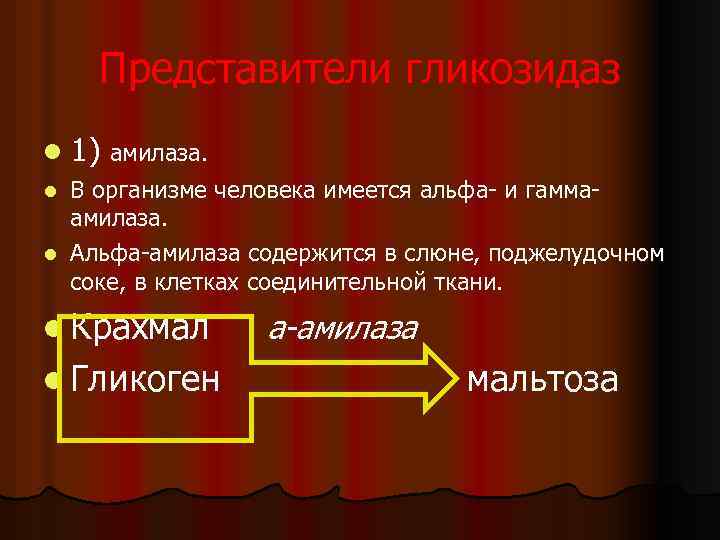
Представители гликозидаз l 1) амилаза. В организме человека имеется альфа и гамма амилаза. l Альфа амилаза содержится в слюне, поджелудочном соке, в клетках соединительной ткани. l l Крахмал l Гликоген a-амилаза мальтоза
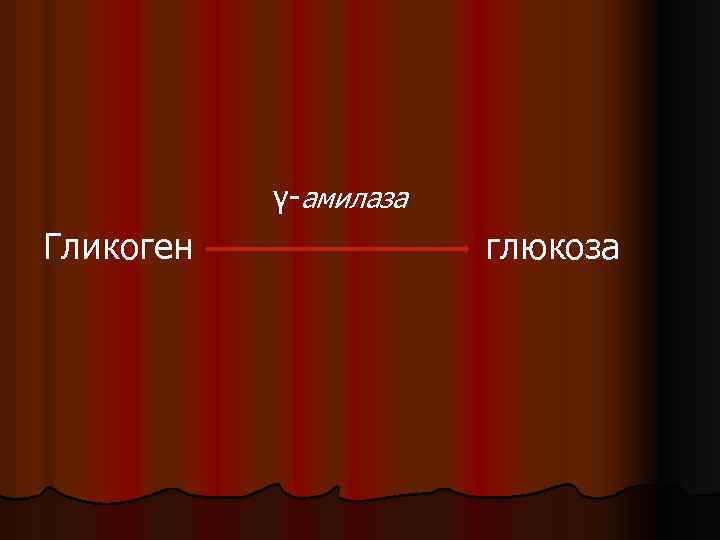
γ амилаза Гликоген глюкоза

l мальтаза встречается в клетках и кишечном соке. l l Мальтоза мальтаза 2 Глюкозы

лактаза l Лактоза l лактаза глю+гал находится в клетках грудной железы, кишечном соке.

Лактоза лактаза глю+гал лактаза находится в клетках грудной железы, кишечном соке.

Сахароза сахараза l сахараза ГЛЮ+ФРУК находится в кишечном соке, расщепляет сахарозу до глюкозы и фруктозы

в желудочном соке нет гликозидаз нет! l.

ПЕПТИДГИДРОЛАЗЫ, ПЕПТИДАЗЫ ведут гидролиз пептидных связей
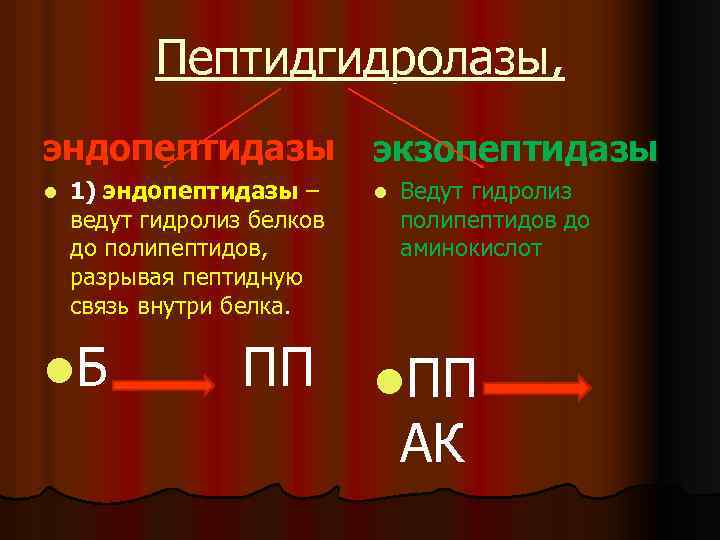
Пептидгидролазы, эндопептидазы l 1) эндопептидазы – ведут гидролиз белков до полипептидов, разрывая пептидную связь внутри белка. l. Б ПП экзопептидазы l Ведут гидролиз полипептидов до аминокислот l. ПП АК

ЭНДОПЕПТИДАЗЫ пепсин выделяется главными клетками желудка в неактивном состоянии в 1) виде пепсиногена. Под действием соляной кислоты и в результате аутокатализа (под действием пепсина) пепсиноген превращается в пепсин. Оптимум р. Н пепсина от 1, 5 до 2, 0, что соответствует р. Н желудочного сока взрослого организма.
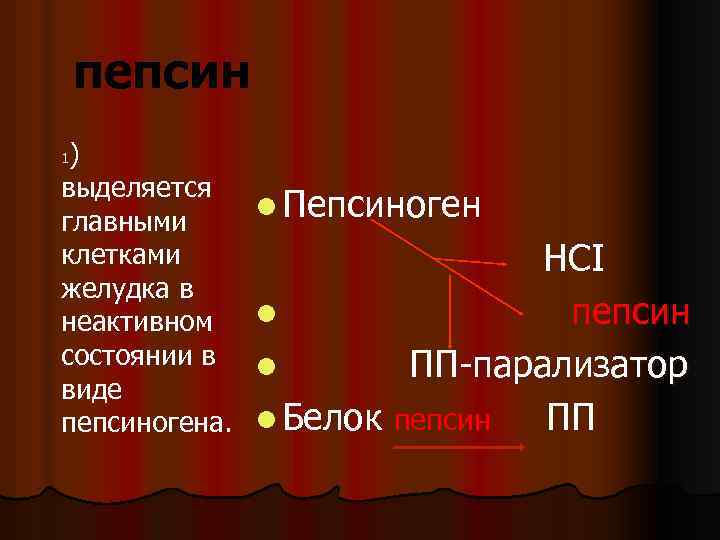
пепсин ) выделяется главными клетками желудка в неактивном состоянии в виде пепсиногена. 1 l Пепсиноген НСI l пепсин l ПП парализатор l Белок пепсин ПП
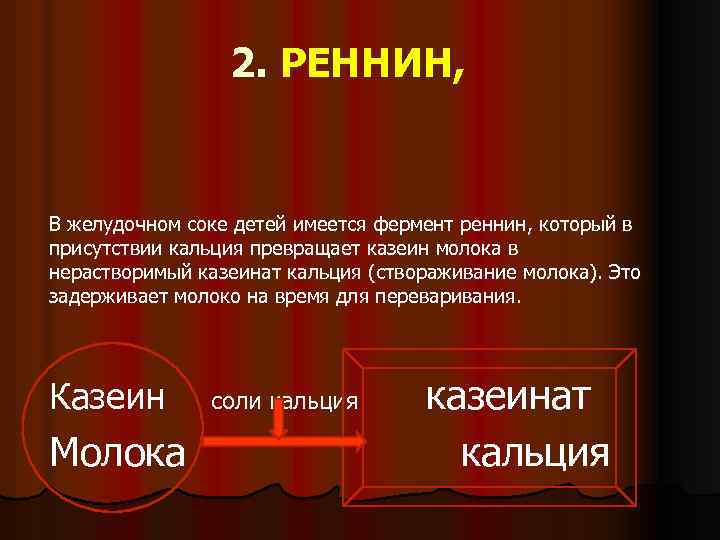
2. РЕННИН, В желудочном соке детей имеется фермент реннин, который в присутствии кальция превращает казеин молока в нерастворимый казеинат кальция (створаживание молока). Это задерживает молоко на время для переваривания. Казеин Молока соли кальция казеинат кальция

трипсин l трипсин образуется в поджелудочной железе в виде трипсиногена и активируется при помощи энтеропептидазы и путем аутокатализа (при действии самого трипсина). Энтеропептидаза отщепляет концевой гексапептид от трипсиногена в кишечнике, превращая трипсиноген в трипсин оптимум р. Н трипсина от 8 до 9, что соответствует р. Н кишечника
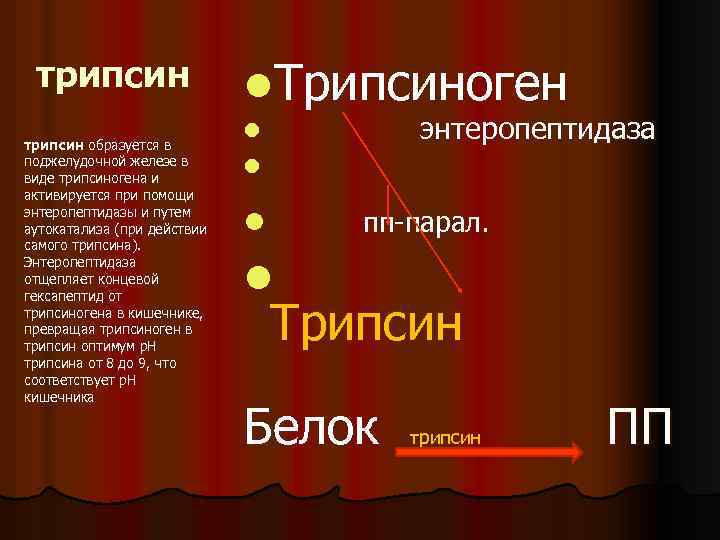
трипсин образуется в поджелудочной железе в виде трипсиногена и активируется при помощи энтеропептидазы и путем аутокатализа (при действии самого трипсина). Энтеропептидаза отщепляет концевой гексапептид от трипсиногена в кишечнике, превращая трипсиноген в трипсин оптимум р. Н трипсина от 8 до 9, что соответствует р. Н кишечника l. Трипсиноген энтеропептидаза l l пп парал. l l Трипсин Белок трипсин ПП

Энтеропептидаза l Встречается в 12 перстной кишке и поджелудочной железе. Фактор, активирующий трипсин. l Фермент действует на трипсиноген, отщепляя от его N конца являющийся специфическим ингибитором гексапептид, и превращает в активный трипсин.

химотрипсин l химотрипсин образуется в поджелудочной железе в виде химотрипсиногена (245 аминокислотных остатков) и активируется при помощи трипсина, который последовательно отщепляет концевые дипептиды от химотрипсиногена в кишечнике, превращая химотрипсиноген в химотрипсины различной степени активности. Оптимум р. Н химотрипсинов от 8 до 9.

l. Химотрипсиноген трипсин полипептид парализатор химотрипси l н l. Белок химотрипсин ПП l НОН

Эластаза l Образуется в поджелудочной железе в виде проэластазы, под действием трипсина активируется, l. Проэластаза трипсин эластаза l гидролизует эластин, разрывая пептидные связи образованные аланином, лейцином, изолейцином и

Экзопептидазы — ферменты, ведущие гидролиз пептидной связи в полипептидах разной сложности, разрушая их до отдельных аминокислот.

экзопептидазы аминопептидазы l Аминопептидазы — по химической природе напоминающие α глобулины белки. Их активаторами явля ются различные металлы Mn 2+, Mg 2+, Zn 2+. Причем для различных представителей аминопептидаз активаторами яв ляются различные металлы. Содержатся в клетках и кишеч ном соке. Катализируют разрыв пептидной связи у N концевой аминокислоты, отщепляя эту аминокислоту от полипептида. карбоксипептидазы l Карбоксипептидазы — протеиды, двухкомпонентные ферменты, В состав кофермента которых входит прочно связанный цинк. Содержатся в клетках, соке поджелудочной железы. Образуется в поджелудочной железе в неактивной форме в виде прокарбоксипептидазы. В кишечнике под действием трипсина путем отщепления полипептида образуется активный фермент.
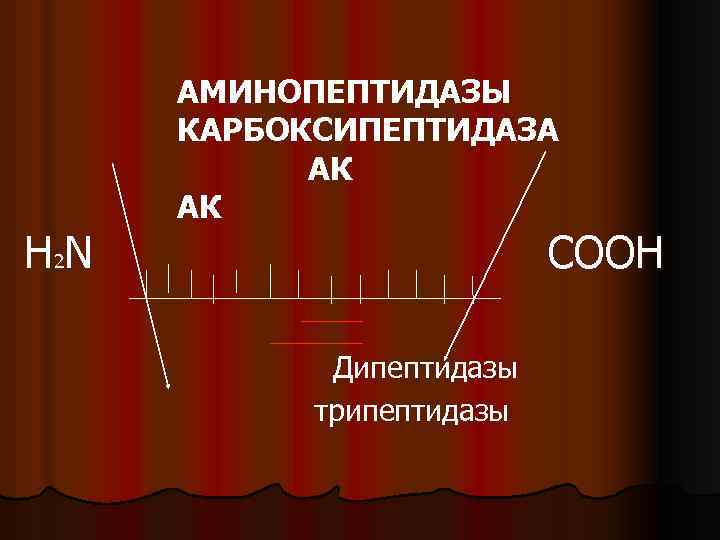
Н 2 N АМИНОПЕПТИДАЗЫ КАРБОКСИПЕПТИДАЗА АК АК СООН Дипептидазы трипептидазы

Лизосомальные ферменты выполняют защитную роль: под их влиянием чужеродные вещества, поступившие в клетку, а затем в лизосомы, подвергаются расщеплению. Расщепляются также вещества, неиспользованные организмом, поэтому лизосомальные ферменты называют клеточными санитарами. l При инфекционных заболеваниях, при воспалительных процессах, уменьшении р. Н, гипоксии мембраны лизосом становятся проницаемыми и гидролазы могут выходить из них, начиная переваривать собственную клетку, вызывая аутолиз клетки. Поэтому лизосомы называют клеточными самоубийцами. l

l дипептидазы Дипептидазы – ферменты, расщепляющие дипептиды до аминокислот. Содержатся в клетках и кишечном соке. l l трипептидазы

ПРИМЕНЕНИЕ ФЕРМЕНТОВ В МЕДИЦИНЕ ØФерментные препараты широко используют в медицине ØФерменты в медицинской практике используют в качестве диагностических (энзимодиагностика) терапевтических средств (энзимотерапия)

ПРИМЕНЕНИЕ ГИДРОЛАЗ В МЕДИЦИНЕ гидролазы используются для заместительной терапии. Пепсин, трипсин, панкреатин применяются при гастритах, при резекции желудка, когда вырабатывается недостаточное количество фермента; q

для растворения тромба при тромбофлебитах, инфаркте миокарда. Стрептокиназа предложена академиком Е. П. Чазовым для введения через катетер в сосуды сердца для растворения тромбов; q

для рассасывания гематом при операциях на лице, травмах (в виде таблеток, мази, содержащих гидролазы). q для рассасывания воспалительных экссудатов при вос палении легких, абсцессах легкого, плевритах, пиелонефритах. q в стоматологии при обработке десневых карманов при парадонтозе. q для лечения старости. q

Применение ферментов в медицине l Ферментные препараты широко используются в медицине: l Энзимодиагностика l Энзимотерапия l В качестве специфических реактивов для определения ряда веществ l В качестве лекарственных средств

Клиническое значение определения отдельных ферментов l Большинство ферментов находятся в клетках и их активность в сыворотке крови в норме минимальна. При разрушении клеток соответствующего органа ферменты попадают в кровь и это служит индикатором повреждения того или иного органа или ткани, так как определенные ферменты органоспецифичны

l. В этой связи наиболее значимыми для клиники являются представители класса гидролаз, трансфераз и ЛДГ. l Уровень активности альфа-амилазы в норме: в сыворотке 25 220 МЕ/л; в моче 10 490 МЕ/л. Увеличение активности данного фермента чаще связана с поражением поджелудочной железы (острый панкреатит), в меньшей мере слюнных желез (паротит).

l Уровень активности сывороточной альдолазы составляет 1 7, 5 ЕД/л (0, 0038 0, 020 мк. М/мин • мл). l Сывороточная альдолаза (фруктозо 1, 6 дифосфатаза) увеличивается в основном при заболеваниях скелетной мускулатуры (прогрессирующая мышечная дистрофия)

l ЩФ (щелочная фосфатаза) широко распространена в тканях человека, особенно в слизистой оболочке кишечника, остеобластах, стенках желчевыводящих путей, плаценте и лактирующей молочной железе. l Она катализирует отщепление фосфатов от их органических соединений, название получила в связи с тем, что оптимум р. Н лежит в щелочной среде (р. Н 8, 6 10, 1).

l Активность ЩФ повышается при холестазе (застое желчи), или механической желтухе, а также при заболеваниях костей

Кислая фосфатаза l Уровень активности КФ (кислая фосфатаза) в норме 0 6, 5 МЕ/л. Этот фермент содержится почти во всех органах и тканях человека, особенно в печени, костях, почках, предстательной железе, клетках крови.

l КФ (кислая фосфатаза) увеличивается в основном l при прогрессирующей болезни Педжета (заболевание костной системы) , l раке предстательной железы

l Аланинаминотрансфераза (АЛТ) l Аспартатаминотрансфераза (АСТ) l АЛТ и АСТ находятся во многих тканях, но больше всего их в сердце и печени.

l Активность данных ферментов повышается значительно при остром гепатите, некрозе печени, травматическом повреждении мышц и инфаркте миокарда.

l ГГТ находится в больших количествах в печени, почках, поджелудочной железе. l Этот фермент считается маркером l рака поджелудочной железы, l застоя желчи l и поражения почек

l Для клинической диагностики важно понятие «изоферменты» l Изоферменты – это множественные формы одного и того же фермента, которые ускоряют одну и ту же реакцию, действуют на один и тот же субстрат, но располагаются в разных органах и тканях.

l Изоферменты имеют одинаковое строение кофермента (небелковой части) и разное строение апофермента (белковой части), поэтому имеют разную молекулярную массу и величину заряда и легко делятся на фракции при электрофорезе. Так, ЛДГ имеет 5 изоферментов, КФК 3

l Креатинфосфотрансфераза, или креатинфосфокиназа (КФК) имеет 3 изофермента – l КФК 1 – в нервной ткани, l КФК 2 в сердце, l КФК 3 – в мышцах. l Если нет признаков повреждения мышц и нервной ткани, то повышение КФК характерно для инфаркта миокарда.

l ЛДГ 1 находится в сердце и эритроцитах; l ЛДГ 2 – в основном в почках; l ЛДГ 3 – в основном в легких; l ЛДГ 4 – в основном в печени, l ЛДГ 5 – в скелетных мышцах и печени. l Соответственно повышение той или иной фракции ЛДГ говорит о локализации повреждения

Клиническое значение определения отдельных ферментов l Большинство ферментов находятся в клетках и их активность в сыворотке крови в норме минимальна. При разрушении клеток соответствующего органа ферменты попадают в кровь и это служит индикатором повреждения того или иного органа или ткани, так как определенные ферменты органоспецифичны

l. В этой связи наиболее значимыми для клиники являются представители класса гидролаз, трансфераз и ЛДГ. l Уровень активности альфа-амилазы в норме: в сыворотке 25 220 МЕ/л; в моче 10 490 МЕ/л. Увеличение активности данного фермента чаще связана с поражением поджелудочной железы (острый панкреатит), в меньшей мере слюнных желез (паротит).

l Уровень активности сывороточной альдолазы составляет 1 7, 5 ЕД/л (0, 0038 0, 020 мк. М/мин • мл). Сывороточная альдолаза (фруктозо 1, 6 дифосфатаза) увеличивается в основном при заболеваниях скелетной мускулатуры (прогрессирующая мышечная дистрофия)

l ЩФ широко распространена в тканях человека, особенно в слизистой оболочке кишечника, остеобластах, стенках желчевыводящих путей, плаценте и лактирующей молочной железе. Она катализирует отщепление фосфатов от их органических соединений, название получила в связи с тем, что оптимум р. Н лежит в щелочной среде (р. Н 8, 6 10, 1).

l Активность ЩФ повышается при холестазе (застое желчи), или механической желтухе, а также при заболеваниях костей l Уровень активности КФ в норме 0 6, 5 МЕ/л. Этот фермент содержится почти во всех органах и тканях человека, особенно в печени, костях, почках, предстательной железе, клетках крови.

КФ увеличивается в основном при прогрессирующей болезни Педжета (заболевание костной системы) и раке предстательной железы

l АЛТ и АСТ находятся во многих тканях, но больше всего их в сердце и печени. l Активность данных ферментов повышается значительно при остром гепатите, некрозе печени, травматическом повреждении мышц и инфаркте миокарда.

l ГГТ находится в больших количествах в печени, почках, поджелудочной железе. Этот фермент считается маркером рака поджелудочной железы, застоя желчи и поражения почек

l Для клинической диагностики важно понятие «изоферменты» l Изоферменты – это множественные формы одного и того же фермента, которые ускоряют одну и ту же реакцию, действуют на один и тот же субстрат, но располагаются в разных органах и тканях.

l Креатинфосфотрансфераза, или креатинфосфокиназа (КФК) имеет 3 изофермента КФК 1 – в нервной ткани, КФК 2 в сердце, КФК 3 – в мышцах. Если нет признаков повреждения мышц и нервной ткани, то повышение КФК характерно для инфаркта миокарда.

l ЛДГ 1 находится в сердце и эритроцитах; l ЛДГ 2 – в основном в почках; l ЛДГ 3 – в основном в легких; l ЛДГ 4 – в основном в печени, l ЛДГ 5 – в скелетных мышцах и печени. l Соответственно повышение той или иной фракции ЛДГ говорит о локализации повреждения

l Изоферменты имеют одинаковое строение кофермента (небелковой части) и разное строение апофермента (белковой части), поэтому имеют разную молекулярную массу и величину заряда и легко делятся на фракции при электрофорезе. Так, ЛДГ имеет 5 изоферментов, КФК 3

Литература основная Основная: 1. Северин Е. С. «Биохимия» , М, : ГЭОТАРМЕДИА, 2013 l 2. Сеитов З. С. «Биохимия» , Алматы, 2012 г. l 3. Harper‘s Illusstrated Biochemistry, 29 е, 2012 l l

Дополнительная 1. Николаева А. Я «Биологическая химия» М. , 2004 2. Т. Т. Березов, Б. Ф. Коровкин «Биологическая химия» , 2002 г. 3. С. М. Плешкова, и др. Учебное пособие для самостоятельного изучения биохимии часть 1 «Белки. Биосинтез белков. Основы молекулярной генетики» , Алматы 2009 г. l 4. Р. Марри, Д. Греннер «Биохимия человека» , I II том, 1993 г. l l l

КОНТРОЛЬНЫЕ ВОПРОСЫ: 1. 2. 3. 4. 5. 6. 7. Что такое ферменты? Классификация и вид катализируемой реакции В чем заключается принцип номенклатуры ферментов На какие подклассы делятся гидролазы Назовите карбоэстеразы Назовите гликозидазы Назовите эндопептидазы
lektsia_2_16-17_fermenty (1).ppt