Аминокислоты новая.pptx
- Количество слайдов: 20
 ЛЕКЦИЯ № 19. ТЕМА: «АМИНОКИСЛОТЫ» . ПЛАН: 1. 2. 3. 4. 5. 6. Формулы и названия некоторых аминокислот, остатки которых входят в состав белков. Аминокислоты Физические свойства. Получение: Химические свойства. Применение: Аминокислоты – это производные углеводородов, содержащие аминогруппы О // ( — NH 2 ) и карбоксильные группы (— С ). ОН Их можно рассматривать как производные карбоновых кислот, у которых один или несколько атомов водорода замещены аминогруппами. Общая формула: (NH 2)m. R(COOH)n, где m или n чаще равны 1 или 2. Таким образом, аминокислоты являются соединениями со смешанными функциями. Названия аминокислотам по международной номенклатуре дают от названия соответствующих карбоновых кислот с добавлением приставки амино.
ЛЕКЦИЯ № 19. ТЕМА: «АМИНОКИСЛОТЫ» . ПЛАН: 1. 2. 3. 4. 5. 6. Формулы и названия некоторых аминокислот, остатки которых входят в состав белков. Аминокислоты Физические свойства. Получение: Химические свойства. Применение: Аминокислоты – это производные углеводородов, содержащие аминогруппы О // ( — NH 2 ) и карбоксильные группы (— С ). ОН Их можно рассматривать как производные карбоновых кислот, у которых один или несколько атомов водорода замещены аминогруппами. Общая формула: (NH 2)m. R(COOH)n, где m или n чаще равны 1 или 2. Таким образом, аминокислоты являются соединениями со смешанными функциями. Названия аминокислотам по международной номенклатуре дают от названия соответствующих карбоновых кислот с добавлением приставки амино.
 1. По числу функциональных групп: NH 2 / m=1 моноаминомонокарбоновые кислоты R n=1 COOH (NH 2)2 / m=2 диаминомонокарбоновые кислоты R n=1 COOH NH 2 / m=1 моноаминодикарбоновые кислоты R n=2 (COOH)2
1. По числу функциональных групп: NH 2 / m=1 моноаминомонокарбоновые кислоты R n=1 COOH (NH 2)2 / m=2 диаминомонокарбоновые кислоты R n=1 COOH NH 2 / m=1 моноаминодикарбоновые кислоты R n=2 (COOH)2
 1. По положению аминогруппы: О 4γ 3β 2α 1 // α-аминокислоты, например: СН 3—СН 2—СН—С │ NH 2 OH О γ β α // β-аминокислоты, например: СН 3—СН—СН 2—С │ NH 2 OH О γ β α // γ-аминокислоты, например: СН 2—СН 2—С │ NH 2 OH Остатки около 20 различных α- аминокислот входят в состав белков.
1. По положению аминогруппы: О 4γ 3β 2α 1 // α-аминокислоты, например: СН 3—СН 2—СН—С │ NH 2 OH О γ β α // β-аминокислоты, например: СН 3—СН—СН 2—С │ NH 2 OH О γ β α // γ-аминокислоты, например: СН 2—СН 2—С │ NH 2 OH Остатки около 20 различных α- аминокислот входят в состав белков.
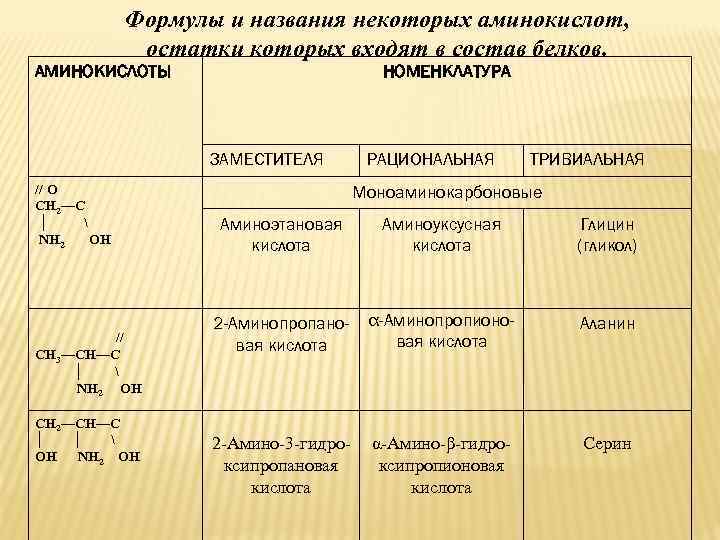 Формулы и названия некоторых аминокислот, остатки которых входят в состав белков. АМИНОКИСЛОТЫ НОМЕНКЛАТУРА ЗАМЕСТИТЕЛЯ // О СН 2—С │ NH 2 OH // СН 3—СН—С │ NH 2 OH СН 2—СН—С │ │ ОН NH 2 OH РАЦИОНАЛЬНАЯ ТРИВИАЛЬНАЯ Моноаминокарбоновые Аминоэтановая кислота Аминоуксусная кислота Глицин (гликол) 2 -Аминопропановая кислота α-Аминопропионовая кислота Аланин 2 -Амино-3 -гидроксипропановая кислота α-Амино-β-гидро- ксипропионовая кислота Серин
Формулы и названия некоторых аминокислот, остатки которых входят в состав белков. АМИНОКИСЛОТЫ НОМЕНКЛАТУРА ЗАМЕСТИТЕЛЯ // О СН 2—С │ NH 2 OH // СН 3—СН—С │ NH 2 OH СН 2—СН—С │ │ ОН NH 2 OH РАЦИОНАЛЬНАЯ ТРИВИАЛЬНАЯ Моноаминокарбоновые Аминоэтановая кислота Аминоуксусная кислота Глицин (гликол) 2 -Аминопропановая кислота α-Аминопропионовая кислота Аланин 2 -Амино-3 -гидроксипропановая кислота α-Амино-β-гидро- ксипропионовая кислота Серин
 О // СН 2—СН—С │ │ SH NH 2 OH О // СН 3—СН—СН—С │ │ СН 3 NH 2 OH О // СН 2—СН—С │ NH 2 OH О // СН 2—СН—С │ │ │ NH 2 OH │ ОН 2 -Амино-3 -меркаптопропановая кислота α-Амино-β-меркаптопропионовая кислота Цистеин 2 -Амино-3 -метилбутановая кислота α-Аминоизовалериановая кислота Валин 2 -Амино-3 фенилпропановая кислота α-Амино-βфенилпропионовая кислота Фенилаланин 2 -Амино-3(n-гидрокси-фенил)пропано-вая кислота α-Амино-β-(n-гидроксифенил)-пропионовая кислота Тирозин
О // СН 2—СН—С │ │ SH NH 2 OH О // СН 3—СН—СН—С │ │ СН 3 NH 2 OH О // СН 2—СН—С │ NH 2 OH О // СН 2—СН—С │ │ │ NH 2 OH │ ОН 2 -Амино-3 -меркаптопропановая кислота α-Амино-β-меркаптопропионовая кислота Цистеин 2 -Амино-3 -метилбутановая кислота α-Аминоизовалериановая кислота Валин 2 -Амино-3 фенилпропановая кислота α-Амино-βфенилпропионовая кислота Фенилаланин 2 -Амино-3(n-гидрокси-фенил)пропано-вая кислота α-Амино-β-(n-гидроксифенил)-пропионовая кислота Тирозин
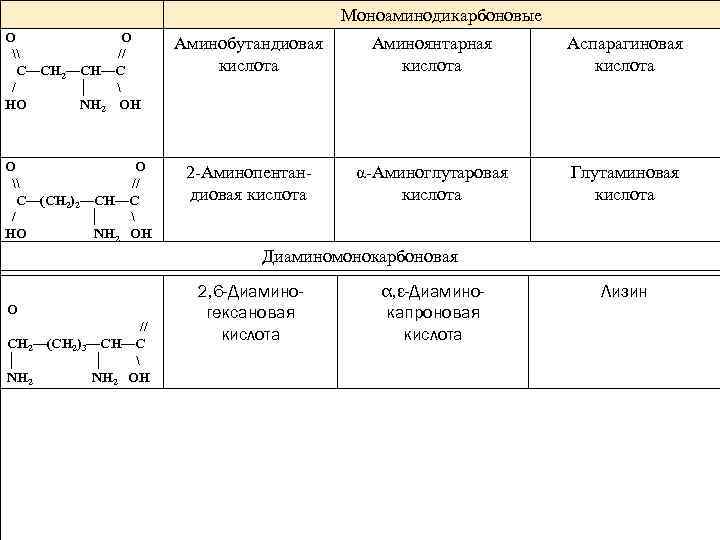 Моноаминодикарбоновые О О \ // С—СН 2—СН—С / │ НО NH 2 OH Аминобутандиовая кислота О О 2 -Аминопентан \ // диовая кислота С—(СН 2)2—СН—С / │ HO NH 2 OH Аминоянтарная кислота Аспарагиновая кислота α-Аминоглутаровая кислота Глутаминовая кислота Диаминомонокарбоновая 2, 6 -Диаминогексановая кислота О // СН 2—(СН 2)3—СН—С │ NH 2 OH α, ε-Диаминокапроновая кислота Лизин
Моноаминодикарбоновые О О \ // С—СН 2—СН—С / │ НО NH 2 OH Аминобутандиовая кислота О О 2 -Аминопентан \ // диовая кислота С—(СН 2)2—СН—С / │ HO NH 2 OH Аминоянтарная кислота Аспарагиновая кислота α-Аминоглутаровая кислота Глутаминовая кислота Диаминомонокарбоновая 2, 6 -Диаминогексановая кислота О // СН 2—(СН 2)3—СН—С │ NH 2 OH α, ε-Диаминокапроновая кислота Лизин
 Для аминокислот характерны следующие виды изомерии: 1. Изомерия положения аминогруппы. 2. Цис-, транс- изомерия. Для ароматических аминокислот характерна орто, мета и пара изомерия АМИНОКИСЛОТЫ ОРГАНИЗМА Заменимые Незаменимые Синтезируются в организме человека, Не синтезируются в организме человека, к ним относятся: глицин, аланин, глута- поступают с пищей. К ним относятся: миновая кислота, серин, аспарагиновая валин, лизин, фенилаланин и другие. кислота, тирозин, цистеин. Физические свойства. Аминокислоты – бесцветные кристаллические вещества, хорошо растворяются в воде, температура плавления 230º – 300º. Многие α-аминокислоты имеют сладкий вкус. Получение: 1. Гидролиз белков ( как конечные продукты гидролиза ). 2. Синтетический путь:
Для аминокислот характерны следующие виды изомерии: 1. Изомерия положения аминогруппы. 2. Цис-, транс- изомерия. Для ароматических аминокислот характерна орто, мета и пара изомерия АМИНОКИСЛОТЫ ОРГАНИЗМА Заменимые Незаменимые Синтезируются в организме человека, Не синтезируются в организме человека, к ним относятся: глицин, аланин, глута- поступают с пищей. К ним относятся: миновая кислота, серин, аспарагиновая валин, лизин, фенилаланин и другие. кислота, тирозин, цистеин. Физические свойства. Аминокислоты – бесцветные кристаллические вещества, хорошо растворяются в воде, температура плавления 230º – 300º. Многие α-аминокислоты имеют сладкий вкус. Получение: 1. Гидролиз белков ( как конечные продукты гидролиза ). 2. Синтетический путь:
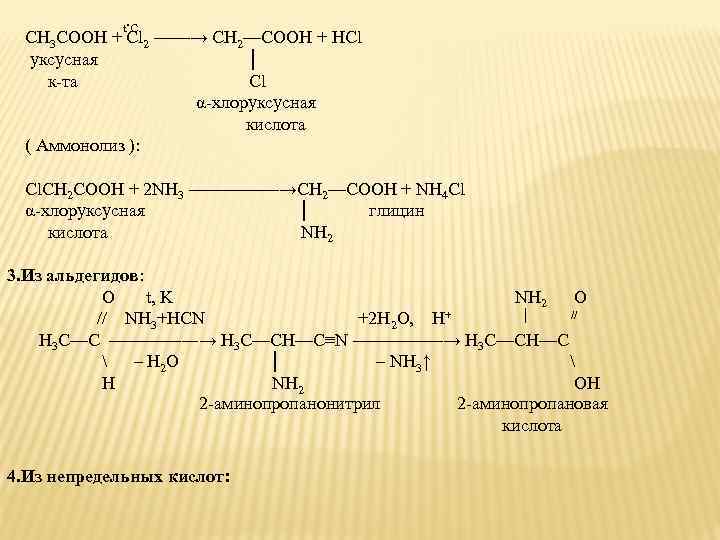 t˚C СН 3 СООН + Cl 2 ——→ CH 2—COOH + HCl уксусная │ к-та Cl α-хлоруксусная кислота ( Аммонолиз ): Cl. CH 2 COOH + 2 NH 3 —————→CH 2—COOH + NH 4 Cl α-хлоруксусная │ глицин кислота NH 2 3. Из альдегидов: O t, K NH 2 O // NH 3+HCN +2 H 2 O, H+ │ // H 3 C—C ————―→ H 3 C—CH—C≡N —————→ H 3 C—CH—C – H 2 O │ – NH 3↑ H NH 2 OH 2 -аминопропанонитрил 2 -аминопропановая кислота 4. Из непредельных кислот:
t˚C СН 3 СООН + Cl 2 ——→ CH 2—COOH + HCl уксусная │ к-та Cl α-хлоруксусная кислота ( Аммонолиз ): Cl. CH 2 COOH + 2 NH 3 —————→CH 2—COOH + NH 4 Cl α-хлоруксусная │ глицин кислота NH 2 3. Из альдегидов: O t, K NH 2 O // NH 3+HCN +2 H 2 O, H+ │ // H 3 C—C ————―→ H 3 C—CH—C≡N —————→ H 3 C—CH—C – H 2 O │ – NH 3↑ H NH 2 OH 2 -аминопропанонитрил 2 -аминопропановая кислота 4. Из непредельных кислот:
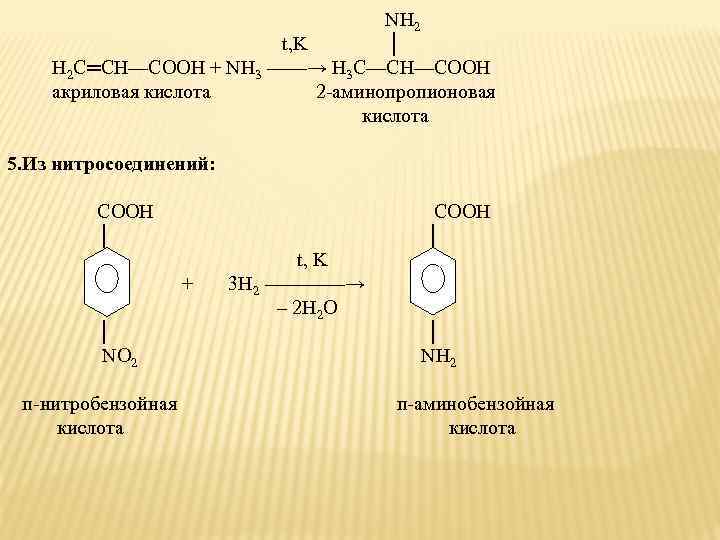 NH 2 t, K │ H 2 C═CH—COOH + NH 3 ——→ H 3 C—CH—COOH акриловая кислота 2 -аминопропионовая кислота 5. Из нитросоединений: СООН COOH │ t, K + 3 H 2 ————→ – 2 H 2 O │ NO 2 NH 2 п-нитробензойная п-аминобензойная кислота
NH 2 t, K │ H 2 C═CH—COOH + NH 3 ——→ H 3 C—CH—COOH акриловая кислота 2 -аминопропионовая кислота 5. Из нитросоединений: СООН COOH │ t, K + 3 H 2 ————→ – 2 H 2 O │ NO 2 NH 2 п-нитробензойная п-аминобензойная кислота
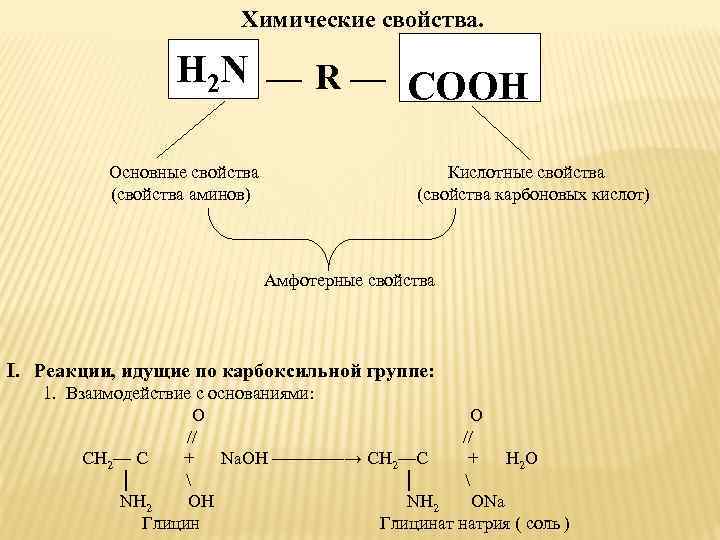 Химические свойства. Н 2 N — COOH R — Основные свойства Кислотные свойства (свойства аминов) (свойства карбоновых кислот) Амфотерные свойства I. Реакции, идущие по карбоксильной группе: 1. Взаимодействие с основаниями: О O // СН 2— С + Na. OH ————→ CH 2—C + H 2 O │ NH 2 OH NH 2 ONa Глицинат натрия ( соль )
Химические свойства. Н 2 N — COOH R — Основные свойства Кислотные свойства (свойства аминов) (свойства карбоновых кислот) Амфотерные свойства I. Реакции, идущие по карбоксильной группе: 1. Взаимодействие с основаниями: О O // СН 2— С + Na. OH ————→ CH 2—C + H 2 O │ NH 2 OH NH 2 ONa Глицинат натрия ( соль )
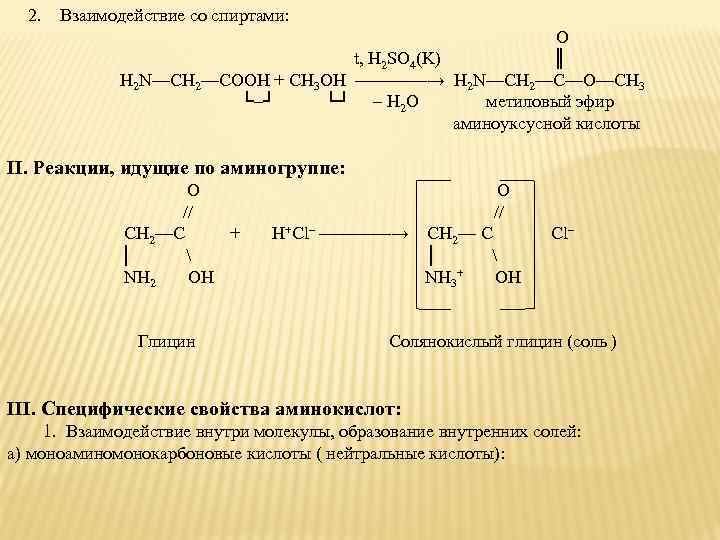 2. Взаимодействие со спиртами: O t, H 2 SO 4(K) ║ Н 2 N—CH 2—COOH + CH 3 OH ————→ H 2 N—CH 2—C—O—CH 3 └–┘ └┘ – H 2 O метиловый эфир аминоуксусной кислоты II. Реакции, идущие по аминогруппе: O // CH 2—C + H+Cl– ————→ CH 2— C Cl– │ NH 2 OH NH 3+ OH Глицин Солянокислый глицин (соль ) III. Специфические свойства аминокислот: 1. Взаимодействие внутри молекулы, образование внутренних солей: а) моноаминомонокарбоновые кислоты ( нейтральные кислоты):
2. Взаимодействие со спиртами: O t, H 2 SO 4(K) ║ Н 2 N—CH 2—COOH + CH 3 OH ————→ H 2 N—CH 2—C—O—CH 3 └–┘ └┘ – H 2 O метиловый эфир аминоуксусной кислоты II. Реакции, идущие по аминогруппе: O // CH 2—C + H+Cl– ————→ CH 2— C Cl– │ NH 2 OH NH 3+ OH Глицин Солянокислый глицин (соль ) III. Специфические свойства аминокислот: 1. Взаимодействие внутри молекулы, образование внутренних солей: а) моноаминомонокарбоновые кислоты ( нейтральные кислоты):
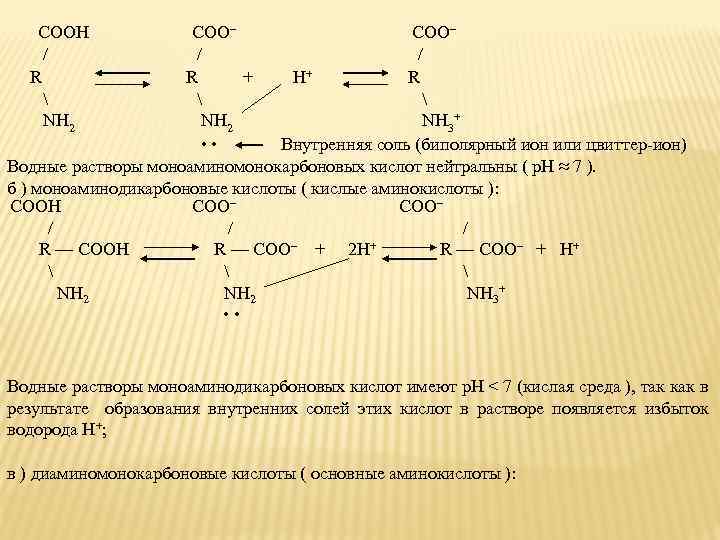 COOH COO– / / R R + H+ R NH 2 NH 3+ • • Внутренняя соль (биполярный ион или цвиттер-ион) Водные растворы моноаминомонокарбоновых кислот нейтральны ( р. Н ≈ 7 ). б ) моноаминодикарбоновые кислоты ( кислые аминокислоты ): COOH COO– / R — COOH R — COO– + 2 H+ R — COO– + H+ NH 2 NH 3+ • • Водные растворы моноаминодикарбоновых кислот имеют р. Н < 7 (кислая среда ), так как в результате образования внутренних солей этих кислот в растворе появляется избыток водорода Н+; в ) диаминомонокарбоновые кислоты ( основные аминокислоты ):
COOH COO– / / R R + H+ R NH 2 NH 3+ • • Внутренняя соль (биполярный ион или цвиттер-ион) Водные растворы моноаминомонокарбоновых кислот нейтральны ( р. Н ≈ 7 ). б ) моноаминодикарбоновые кислоты ( кислые аминокислоты ): COOH COO– / R — COOH R — COO– + 2 H+ R — COO– + H+ NH 2 NH 3+ • • Водные растворы моноаминодикарбоновых кислот имеют р. Н < 7 (кислая среда ), так как в результате образования внутренних солей этих кислот в растворе появляется избыток водорода Н+; в ) диаминомонокарбоновые кислоты ( основные аминокислоты ):
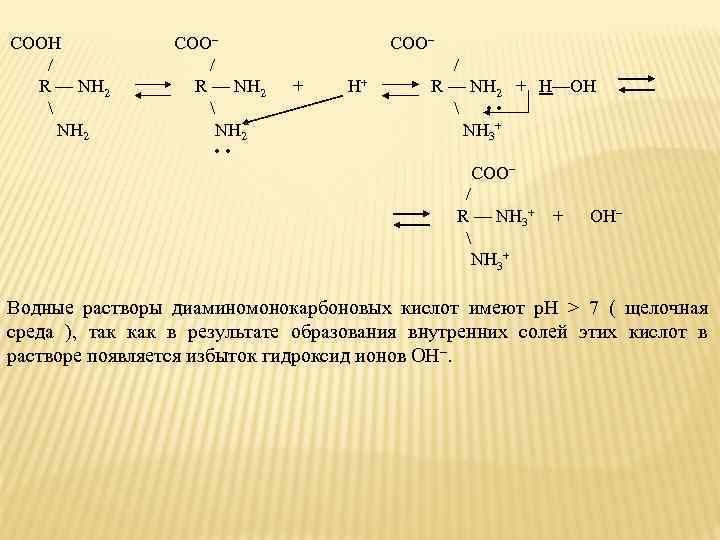 COOH COO– / R — NH 2 R — NH 2 + H+ R — NH 2 + H—OH • • NH 2 NH 3+ • • COO– / R — NH 3+ + OH– NH 3+ Водные растворы диаминомонокарбоновых кислот имеют р. Н > 7 ( щелочная среда ), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид ионов ОН–.
COOH COO– / R — NH 2 R — NH 2 + H+ R — NH 2 + H—OH • • NH 2 NH 3+ • • COO– / R — NH 3+ + OH– NH 3+ Водные растворы диаминомонокарбоновых кислот имеют р. Н > 7 ( щелочная среда ), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид ионов ОН–.
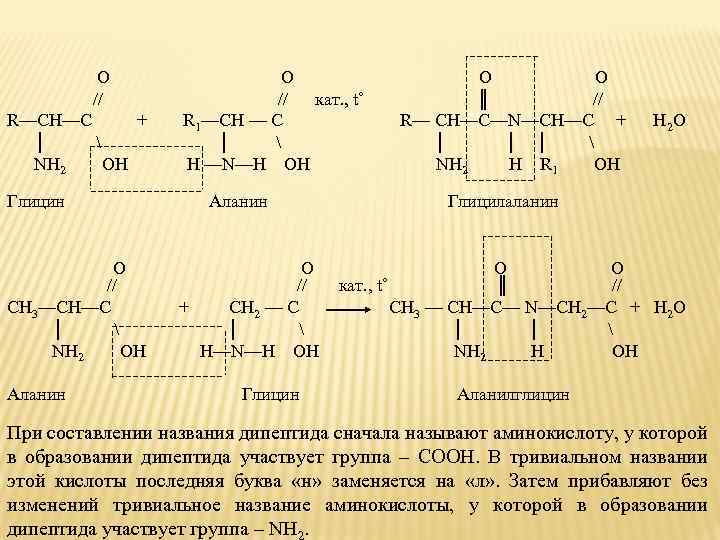 O О O // кат. , t˚ ║ // R—CH—C + R 1—CH — C R— CH—C—N—CH—C + H 2 O │ │ │ │ NH 2 OH H —N—H OH NH 2 H R 1 OH Глицин Аланин Глицилаланин O О O // кат. , t˚ ║ // СН 3—CH—C + CH 2 — C СН 3 — CH—C— N—CH 2—C + H 2 O │ │ │ NH 2 OH H—N—H OH NH 2 H OH Аланин Глицин Аланилглицин При составлении названия дипептида сначала называют аминокислоту, у которой в образовании дипептида участвует группа – СООН. В тривиальном названии этой кислоты последняя буква «н» заменяется на «л» . Затем прибавляют без изменений тривиальное название аминокислоты, у которой в образовании дипептида участвует группа – NH.
O О O // кат. , t˚ ║ // R—CH—C + R 1—CH — C R— CH—C—N—CH—C + H 2 O │ │ │ │ NH 2 OH H —N—H OH NH 2 H R 1 OH Глицин Аланин Глицилаланин O О O // кат. , t˚ ║ // СН 3—CH—C + CH 2 — C СН 3 — CH—C— N—CH 2—C + H 2 O │ │ │ NH 2 OH H—N—H OH NH 2 H OH Аланин Глицин Аланилглицин При составлении названия дипептида сначала называют аминокислоту, у которой в образовании дипептида участвует группа – СООН. В тривиальном названии этой кислоты последняя буква «н» заменяется на «л» . Затем прибавляют без изменений тривиальное название аминокислоты, у которой в образовании дипептида участвует группа – NH.
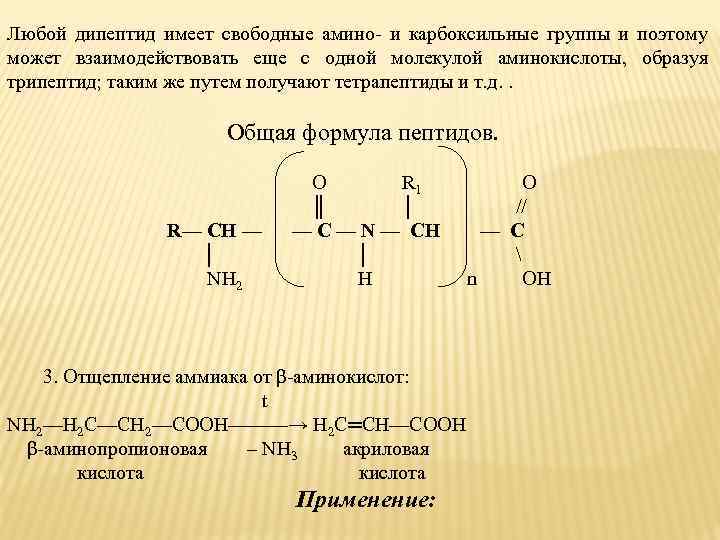 Любой дипептид имеет свободные амино- и карбоксильные группы и поэтому может взаимодействовать еще с одной молекулой аминокислоты, образуя трипептид; таким же путем получают тетрапептиды и т. д. . Общая формула пептидов. O R 1 O ║ │ // R— CH — — C — N — CH — C │ NH 2 H n OH 3. Отщепление аммиака от β-аминокислот: t NH 2—H 2 C—CH 2—COOH———→ H 2 C═CH—COOH β-аминопропионовая – NH 3 акриловая кислота Применение:
Любой дипептид имеет свободные амино- и карбоксильные группы и поэтому может взаимодействовать еще с одной молекулой аминокислоты, образуя трипептид; таким же путем получают тетрапептиды и т. д. . Общая формула пептидов. O R 1 O ║ │ // R— CH — — C — N — CH — C │ NH 2 H n OH 3. Отщепление аммиака от β-аминокислот: t NH 2—H 2 C—CH 2—COOH———→ H 2 C═CH—COOH β-аминопропионовая – NH 3 акриловая кислота Применение:
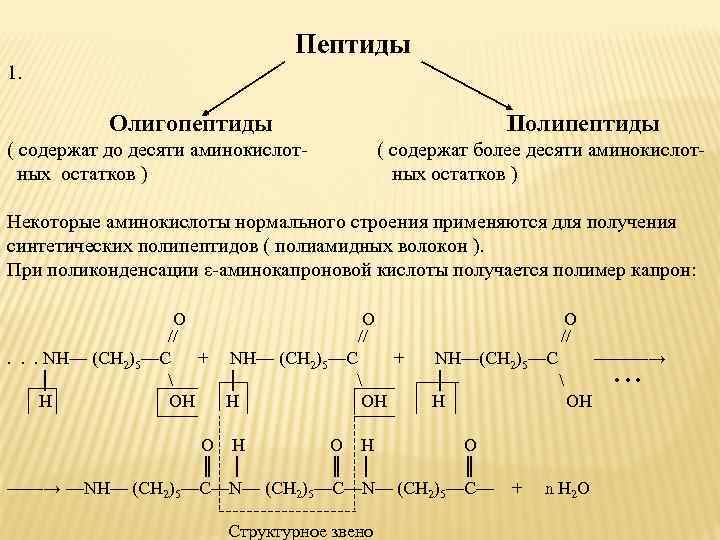 Пептиды 1. Олигопептиды Полипептиды ( содержат до десяти аминокислот- ( содержат более десяти аминокислот- ных остатков ) ных остатков ) Некоторые аминокислоты нормального строения применяются для получения синтетических полипептидов ( полиамидных волокон ). При поликонденсации ε-аминокапроновой кислоты получается полимер капрон: O O // // . . . NH— (CH 2)5—C + NH— (CH 2)5—C + NH—(CH 2)5—C ———→ │ • • • H OH H OH O H O ║ │ ║ ——→ —NH— (CH 2)5—C—N— (CH 2)5—C— + n H 2 O Структурное звено
Пептиды 1. Олигопептиды Полипептиды ( содержат до десяти аминокислот- ( содержат более десяти аминокислот- ных остатков ) ных остатков ) Некоторые аминокислоты нормального строения применяются для получения синтетических полипептидов ( полиамидных волокон ). При поликонденсации ε-аминокапроновой кислоты получается полимер капрон: O O // // . . . NH— (CH 2)5—C + NH— (CH 2)5—C + NH—(CH 2)5—C ———→ │ • • • H OH H OH O H O ║ │ ║ ——→ —NH— (CH 2)5—C—N— (CH 2)5—C— + n H 2 O Структурное звено
 Из капроновой смолы получают не только волокно, но и пластмассовые изделия. 2. 4 -аминобутановая кислота (γ-аминомасляная кислота) ГАМК. Используется в медицине под названием аминадон или гаминалон, применяется при психических заболеваниях, обладает ноотропным действием, т. е. влияет на процессы мышления. На основе ГАМК созданы многие ноотропные средства. 3. СООН │ NH 2 Парааминобензойная кислота (ПАБК) Сложные эфиры ПАБК – анестезин, новокаин, используется в качестве местных анестезирующих средств.
Из капроновой смолы получают не только волокно, но и пластмассовые изделия. 2. 4 -аминобутановая кислота (γ-аминомасляная кислота) ГАМК. Используется в медицине под названием аминадон или гаминалон, применяется при психических заболеваниях, обладает ноотропным действием, т. е. влияет на процессы мышления. На основе ГАМК созданы многие ноотропные средства. 3. СООН │ NH 2 Парааминобензойная кислота (ПАБК) Сложные эфиры ПАБК – анестезин, новокаин, используется в качестве местных анестезирующих средств.
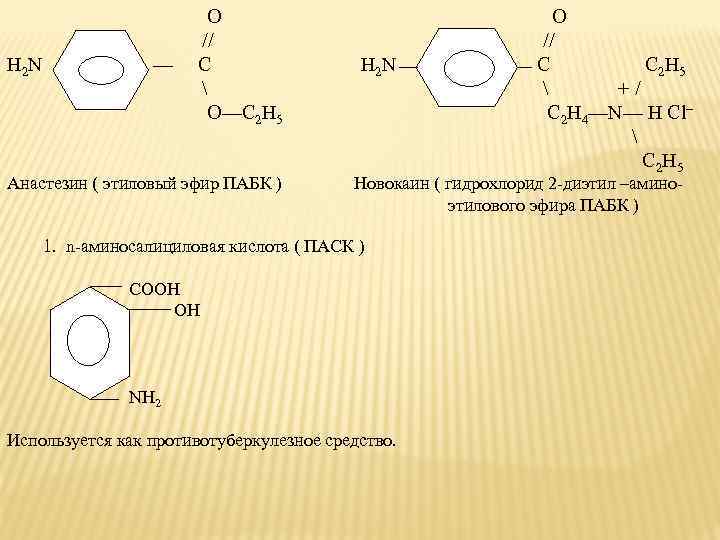 О // H 2 N — С H 2 N С C 2 H 5 + / О—С 2 Н 5 С 2 Н 4—N— H Cl– C 2 H 5 Анастезин ( этиловый эфир ПАБК ) Новокаин ( гидрохлорид 2 -диэтил –амино- этилового эфира ПАБК ) 1. n-аминосалициловая кислота ( ПАСК ) COOH OH NH 2 Используется как противотуберкулезное средство.
О // H 2 N — С H 2 N С C 2 H 5 + / О—С 2 Н 5 С 2 Н 4—N— H Cl– C 2 H 5 Анастезин ( этиловый эфир ПАБК ) Новокаин ( гидрохлорид 2 -диэтил –амино- этилового эфира ПАБК ) 1. n-аминосалициловая кислота ( ПАСК ) COOH OH NH 2 Используется как противотуберкулезное средство.
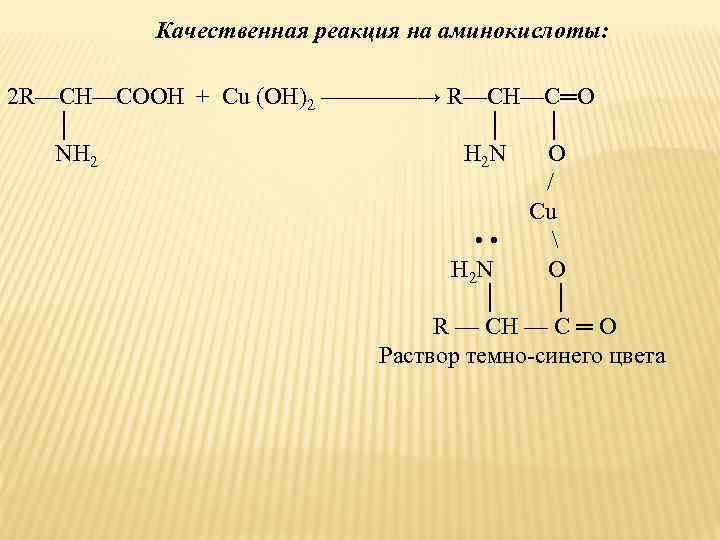 Качественная реакция на аминокислоты: 2 R—CH—COOH + Cu (OH)2 ————→ R—CH—C═O │ │ │ NH 2 H 2 N O / Cu • • H 2 N O │ R — CH — C ═ O Раствор темно-синего цвета
Качественная реакция на аминокислоты: 2 R—CH—COOH + Cu (OH)2 ————→ R—CH—C═O │ │ │ NH 2 H 2 N O / Cu • • H 2 N O │ R — CH — C ═ O Раствор темно-синего цвета
 ДОМАШНЕЕ ЗАДАНИЕ: Н. А. Тюкавкина. "Органическая химия", Москва, "Медицина, "1989 г. стр 284 -288 СОСТАВИЛА ПРЕПОДАВАТЕЛЬ: Томуль Т. В.
ДОМАШНЕЕ ЗАДАНИЕ: Н. А. Тюкавкина. "Органическая химия", Москва, "Медицина, "1989 г. стр 284 -288 СОСТАВИЛА ПРЕПОДАВАТЕЛЬ: Томуль Т. В.


