Лекция № 16 Лектор: доцент Самоданова Г. И.


















obmen_belkov-2.ppt
- Размер: 339.0 Кб
- Автор: Ульяна Смирнова
- Количество слайдов: 19
Описание презентации Лекция № 16 Лектор: доцент Самоданова Г. И. по слайдам
 Лекция № 16 Лектор: доцент Самоданова Г. И.
Лекция № 16 Лектор: доцент Самоданова Г. И.
 Биогенные амины (БА)- те амины , которые малыми дозами оказывают большой биологический эффект. R-CH-COOH R-CH 2 -NH 2 + CO 2 декарбоксилаза пф (БА) NH 2 аминомаслянная кислота. CH 2 -NH 2 (CH 2 ) 2 COOHДекарбоксилаза ПФ CO 2 COOH CHNH 2 (CH 2 ) 2 COOH (ГАМК)ГЛУ
Биогенные амины (БА)- те амины , которые малыми дозами оказывают большой биологический эффект. R-CH-COOH R-CH 2 -NH 2 + CO 2 декарбоксилаза пф (БА) NH 2 аминомаслянная кислота. CH 2 -NH 2 (CH 2 ) 2 COOHДекарбоксилаза ПФ CO 2 COOH CHNH 2 (CH 2 ) 2 COOH (ГАМК)ГЛУ
 ДАО(диаминооксидаза) , цитоплазма , ПФ , С u +2 МАО (моноаминооксидаза) , митохондрия , ФАДR-CH 2 -NH 2 + O 2 + H 2 O R-C-H + NH 3 + H 2 Oаминооксидаза. Способ инактвации биогенных аминов — окислительное дезаминирование. R-C-H R-C-OOH (органическая кислота)альдегид. ДГ O H 2 O HADH
ДАО(диаминооксидаза) , цитоплазма , ПФ , С u +2 МАО (моноаминооксидаза) , митохондрия , ФАДR-CH 2 -NH 2 + O 2 + H 2 O R-C-H + NH 3 + H 2 Oаминооксидаза. Способ инактвации биогенных аминов — окислительное дезаминирование. R-C-H R-C-OOH (органическая кислота)альдегид. ДГ O H 2 O HADH
 Янтарная кислота. CH 2 -NH 2 ФАД H 2 C-H HADH 2 С OOH CH 2 CH 2 COOH H 2 O NH 3 (ГАМК) CH 2 CH 2 COOH H 2 O янтарный полуальдегид Ц ткмао
Янтарная кислота. CH 2 -NH 2 ФАД H 2 C-H HADH 2 С OOH CH 2 CH 2 COOH H 2 O NH 3 (ГАМК) CH 2 CH 2 COOH H 2 O янтарный полуальдегид Ц ткмао
 HADH 2 HAD ДГ CH 2 -C=O NH H CH 2 -COOH NH Имидазол-уксусная кислота HN CH 2 -CH-COOH NH NH 2 N ГИС NHN CH 2 — NH 2 ГИСТАМИНдекарбоксилаза CO 2 NH 3 ДАО ПФ , С u +2 МОЧА
HADH 2 HAD ДГ CH 2 -C=O NH H CH 2 -COOH NH Имидазол-уксусная кислота HN CH 2 -CH-COOH NH NH 2 N ГИС NHN CH 2 — NH 2 ГИСТАМИНдекарбоксилаза CO 2 NH 3 ДАО ПФ , С u +2 МОЧА
 тетро- дегидро птеридинтриптофанмонооксидаза гидро- птеридин 5’ОКСИТРИПТОФАНNHOH CH 2 -CH-COOH NH 2 NH CH 2 -CH-COOH ТРИПТОФАН NHNH серотонин. HO CH 2 -CH-NH 2 декарбоксилаза С O
тетро- дегидро птеридинтриптофанмонооксидаза гидро- птеридин 5’ОКСИТРИПТОФАНNHOH CH 2 -CH-COOH NH 2 NH CH 2 -CH-COOH ТРИПТОФАН NHNH серотонин. HO CH 2 -CH-NH 2 декарбоксилаза С O
 норадреналин. CH 2 -CH-NH 2 фенилмоно оксигеназа ФЕН COOH HO CH 2 -CH-NH 2 COOH ДОФА НОHO CH 2 -CH-NH 2 COOH тирозинмоно оксигеназа ТИР OH CH 2 -CH-NH 2 HO ДОФАМИН C o
норадреналин. CH 2 -CH-NH 2 фенилмоно оксигеназа ФЕН COOH HO CH 2 -CH-NH 2 COOH ДОФА НОHO CH 2 -CH-NH 2 COOH тирозинмоно оксигеназа ТИР OH CH 2 -CH-NH 2 HO ДОФАМИН C o
 CH 2 -SH NH 2 -CH-COOH ЦИС NH 2 -CH 2 -SO 3 H ТАУРИНCH 2 -SO 2 H ЦИСТЕИН — СУЛЬФИНОВАЯ КИСЛОТАNH 2 — CH — COOH CH 2 -SO 3 H ЦИСТЕИНОВАЯ КИСЛОТА СО 2 NH 2 — CH — COOH
CH 2 -SH NH 2 -CH-COOH ЦИС NH 2 -CH 2 -SO 3 H ТАУРИНCH 2 -SO 2 H ЦИСТЕИН — СУЛЬФИНОВАЯ КИСЛОТАNH 2 — CH — COOH CH 2 -SO 3 H ЦИСТЕИНОВАЯ КИСЛОТА СО 2 NH 2 — CH — COOH
 Образование аммонийных солей синтез Нуклеотидов синтез заменимых аминокислот аминогексоз синтез аммониогенезсинтез мочевины Восстановительное аминирование кетокислот. ДЕЗАМИНИРОВАНИЕ : 1. Аминокислот тканей 2. Биогенных аминов 3. Пуринов 4. Пиримидинов 5. Аспарагина 6. Глютамина 7. г НИЕНИЕ В КИШЕЧНИКЕ
Образование аммонийных солей синтез Нуклеотидов синтез заменимых аминокислот аминогексоз синтез аммониогенезсинтез мочевины Восстановительное аминирование кетокислот. ДЕЗАМИНИРОВАНИЕ : 1. Аминокислот тканей 2. Биогенных аминов 3. Пуринов 4. Пиримидинов 5. Аспарагина 6. Глютамина 7. г НИЕНИЕ В КИШЕЧНИКЕ
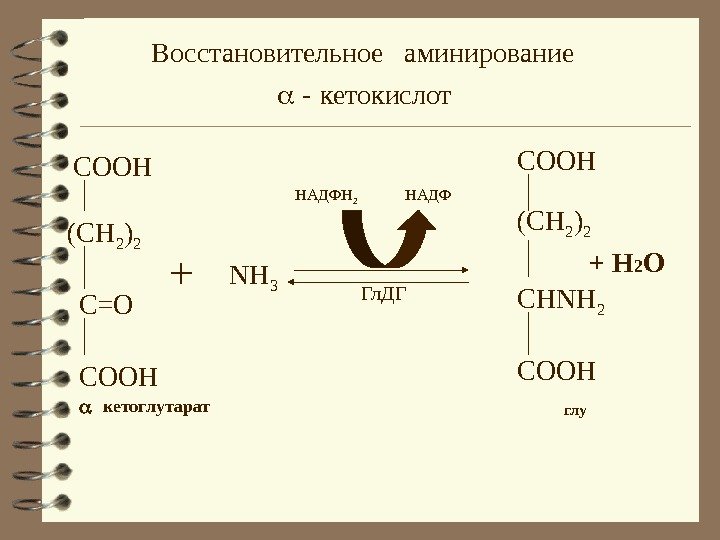
 Восстановительное аминирование кетокислот — COOH C=O COOH(CH 2 ) 2 + NH 3 кетоглутарат НАДФН 2 НАДФ Гл. ДГ COОН (CH 2 ) 2 CHNH 2 COOH + H 2 O глу
Восстановительное аминирование кетокислот — COOH C=O COOH(CH 2 ) 2 + NH 3 кетоглутарат НАДФН 2 НАДФ Гл. ДГ COОН (CH 2 ) 2 CHNH 2 COOH + H 2 O глу
 Образование глутамина (аспарагина) АТФ АДФ+ФН ГЛУТАМИНСИНТАЗА 1. Форма обезвреживания аммиака 2. Коллектор аммиака 3. Форма транспорта аммиака Основной путь выведения аммиака-мочевина. С OOH ( CH 2)2 CHNH 2 COOH + NH 3 глу CONH 2 (CH 2 ) 2 CHNH 2 COOH глн
Образование глутамина (аспарагина) АТФ АДФ+ФН ГЛУТАМИНСИНТАЗА 1. Форма обезвреживания аммиака 2. Коллектор аммиака 3. Форма транспорта аммиака Основной путь выведения аммиака-мочевина. С OOH ( CH 2)2 CHNH 2 COOH + NH 3 глу CONH 2 (CH 2 ) 2 CHNH 2 COOH глн
 Ненский , Салазкин , Кребс , Гензлейт Глутамин печень NH 4 + ГЛУ 1. Синтез карбомоилфосфата — активной формы NH 3 NH 4 +CO 2 NH 2 C O ~ P Oкарбомоилфосфатсинтаза МТХ Mg +22 АТФ 2 АДФ+ФН
Ненский , Салазкин , Кребс , Гензлейт Глутамин печень NH 4 + ГЛУ 1. Синтез карбомоилфосфата — активной формы NH 3 NH 4 +CO 2 NH 2 C O ~ P Oкарбомоилфосфатсинтаза МТХ Mg +22 АТФ 2 АДФ+ФН
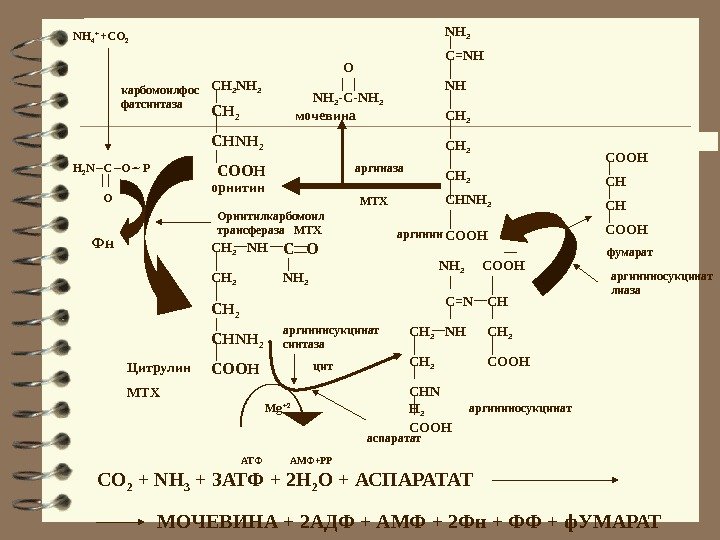
 H 2 N C O ~ P ONH 4 + +CO 2 карбомоилфос фатсинтаза Фн С H 2 NH 2 CHNH 2 COOH орнитин Орнитилкарбомоил трансфераза МТХ CH 2 NH CH 2 CHNH 2 COOHЦитрулин МТХ C O NH 2 аспаратат АТФ АМФ+РР Mg +2 аргининсукцинат синтаза CHNH 2 C=NH CH 2 NH COOHаргинин С O 2 + NH 3 + 3 АТФ + 2 H 2 O + АСПАРАТАТ МОЧЕВИНА + 2 АДФ + АМФ + 2 Фн + ФФ + ф. УМАРАТ фумарат. COOH CH CH COOH аргининосукцинат лиаза. NH 2 COOH C=N CH NH CH 2 CHN H 2 COOH аргининосукцинатцит аргиназа. NH 2 -C-NH 2 O мочевина МТХ
H 2 N C O ~ P ONH 4 + +CO 2 карбомоилфос фатсинтаза Фн С H 2 NH 2 CHNH 2 COOH орнитин Орнитилкарбомоил трансфераза МТХ CH 2 NH CH 2 CHNH 2 COOHЦитрулин МТХ C O NH 2 аспаратат АТФ АМФ+РР Mg +2 аргининсукцинат синтаза CHNH 2 C=NH CH 2 NH COOHаргинин С O 2 + NH 3 + 3 АТФ + 2 H 2 O + АСПАРАТАТ МОЧЕВИНА + 2 АДФ + АМФ + 2 Фн + ФФ + ф. УМАРАТ фумарат. COOH CH CH COOH аргининосукцинат лиаза. NH 2 COOH C=N CH NH CH 2 CHN H 2 COOH аргининосукцинатцит аргиназа. NH 2 -C-NH 2 O мочевина МТХ
 COOH CH 2 COOH МАЛАТCOOH CH CH COOH фумараза ФУМАРАТ H 2 O МАЛАТ ДГНАД НАДН 2 COOH CHNH 2 COOH АСПCOOH C=O CH 2 COOH оксалоацетат Ас. АТГЛУ — КЕТОГЛУ 3 АТФ аспаратат малат цтк оксалоацетат — кетоглутарат. NH 3 МОЧЕВИНА CO 2 фумарат. Орнитиновый цикл ГЛУ
COOH CH 2 COOH МАЛАТCOOH CH CH COOH фумараза ФУМАРАТ H 2 O МАЛАТ ДГНАД НАДН 2 COOH CHNH 2 COOH АСПCOOH C=O CH 2 COOH оксалоацетат Ас. АТГЛУ — КЕТОГЛУ 3 АТФ аспаратат малат цтк оксалоацетат — кетоглутарат. NH 3 МОЧЕВИНА CO 2 фумарат. Орнитиновый цикл ГЛУ
 О ОНОН ОННО CH 2 OH O НО ОН ОНОН СН 2 O ~ P ГЛЮКОЗА — 6 — ФОСФАТ O OH OHHO NH 2 CH 2 — O ~ P АТФ АДФ ГЛН ГЛУ Глюкозамин ( Галактозамин )ГК
О ОНОН ОННО CH 2 OH O НО ОН ОНОН СН 2 O ~ P ГЛЮКОЗА — 6 — ФОСФАТ O OH OHHO NH 2 CH 2 — O ~ P АТФ АДФ ГЛН ГЛУ Глюкозамин ( Галактозамин )ГК
 2 Трансаминирование Глу + — кето — кислота — кетоглу 3 Трансреанимирование 1 + 3 4 глутамин + кетокислота Глу + AK 5 Исходными для синтеза могут служить метаболиты распада углеводов , цикла Кребса , незаменимые аминокислот А) ПВК АЛА Б ) 3 — фосфоглицерат 3 — фосфосерин В) серин + ТГФК глицин + N 5 , N 10 , ТГФК Г) рибозо — 5 -фосфат фосфорибозил — пирофосфат гистидин Д) оксалоацетат + ГЛУ аспарагин + Е) незаменимые ФА + НАДФН 2 + О 2 ТИР + НАДФ + Н 2 О метионин цистеин орнитин аргинин Кетоглу + АК 1 Восстановительное аминирование — кетокислот — Кето — глу НАДФН 2 НАДФ NH 3 H 2 O ГЛУ Гл. ДГ
2 Трансаминирование Глу + — кето — кислота — кетоглу 3 Трансреанимирование 1 + 3 4 глутамин + кетокислота Глу + AK 5 Исходными для синтеза могут служить метаболиты распада углеводов , цикла Кребса , незаменимые аминокислот А) ПВК АЛА Б ) 3 — фосфоглицерат 3 — фосфосерин В) серин + ТГФК глицин + N 5 , N 10 , ТГФК Г) рибозо — 5 -фосфат фосфорибозил — пирофосфат гистидин Д) оксалоацетат + ГЛУ аспарагин + Е) незаменимые ФА + НАДФН 2 + О 2 ТИР + НАДФ + Н 2 О метионин цистеин орнитин аргинин Кетоглу + АК 1 Восстановительное аминирование — кетокислот — Кето — глу НАДФН 2 НАДФ NH 3 H 2 O ГЛУ Гл. ДГ
 Глицин — амидин — трансфераза + NH 2 COOH 1 В ПОЧКАХ глицин. NH 2 (CH 2 ) 3 C=NH CHNH 2 NH аргинин. COOH NH 2 C=NH NH CH 2 COOH + NH 2 (CH 2 ) 3 CHNH 2 COOH Гуанидин — уксусная кислота орнитин Гуанидин — уксусная кислота 2 В ПЕЧЕНИ NH 2 C=NH NH CH 2 COOH гуанидинацетатметилтрансфераза 3 — аденозил гомоцистеин 3 Аденозил метионин NH 2 C=NH N — CH 3 CH 2 COOH креатин
Глицин — амидин — трансфераза + NH 2 COOH 1 В ПОЧКАХ глицин. NH 2 (CH 2 ) 3 C=NH CHNH 2 NH аргинин. COOH NH 2 C=NH NH CH 2 COOH + NH 2 (CH 2 ) 3 CHNH 2 COOH Гуанидин — уксусная кислота орнитин Гуанидин — уксусная кислота 2 В ПЕЧЕНИ NH 2 C=NH NH CH 2 COOH гуанидинацетатметилтрансфераза 3 — аденозил гомоцистеин 3 Аденозил метионин NH 2 C=NH N — CH 3 CH 2 COOH креатин
 3 В МЫШЦАХ АТФ АДФ КФК В диагностике используются : 1) Определение креатина в моче при патологии мышц. 2) Определение креатинина в моче и крови (клиренс , проба Реберга , выделительгая функция почек. 3) Определение активности КФК и ее изоферментов в крови (диагностика ИМ) NH 2 C=NH N — CH 3 CH 2 COOH креатин ~P NH — P C=NH N — CH 3 CH 2 COOH моча. NH C=NH N — CH 3 CH 2 CO Креати-н ин Креатинфосфат — форма депонирования и транспорта энергии Фн
3 В МЫШЦАХ АТФ АДФ КФК В диагностике используются : 1) Определение креатина в моче при патологии мышц. 2) Определение креатинина в моче и крови (клиренс , проба Реберга , выделительгая функция почек. 3) Определение активности КФК и ее изоферментов в крови (диагностика ИМ) NH 2 C=NH N — CH 3 CH 2 COOH креатин ~P NH — P C=NH N — CH 3 CH 2 COOH моча. NH C=NH N — CH 3 CH 2 CO Креати-н ин Креатинфосфат — форма депонирования и транспорта энергии Фн
 Na. A Na + A — CO 2 + H 2 O H 2 CO 3 KА NH 3 ГЛУ ГЛНNH 3 NH 4 +H H + HCO 3 — HCO 3 Na + В результате в крови восстанавливается концентрация бикарбоната , а «расплатой» за этоявляется выведение протонов с мочей в виде аммонийных солей. Просвет дистального канальца клетка кровь. Аммониогенз протекает в почках и дистальном канальце , механизм поддержания постоянства р. Н МОЧАNH 4 A H + + HCO 3 — H 2 CO 3 p. H=p. K+lg [HCO 3 — ] [H 2 CO 3 ]
Na. A Na + A — CO 2 + H 2 O H 2 CO 3 KА NH 3 ГЛУ ГЛНNH 3 NH 4 +H H + HCO 3 — HCO 3 Na + В результате в крови восстанавливается концентрация бикарбоната , а «расплатой» за этоявляется выведение протонов с мочей в виде аммонийных солей. Просвет дистального канальца клетка кровь. Аммониогенз протекает в почках и дистальном канальце , механизм поддержания постоянства р. Н МОЧАNH 4 A H + + HCO 3 — H 2 CO 3 p. H=p. K+lg [HCO 3 — ] [H 2 CO 3 ]

