LEKTsIYa__15_po_monosakharidam_polnaya_s_pravkoy.ppt
- Количество слайдов: 37

ЛЕКЦИЯ № 15 УГЛЕВОДЫ МОНОЗЫ, БИОЗЫ

Углеводы чрезвычайно распространены в природе § В биосфере Земли на долю углеводов приходится до 50% биомассы. Углеводы образуются в результате фотосинтеза § СХЕМА ФОТОСИНТЕЗА § солнечная энергия § х. СО 2+у. Н 2 О → Сх(Н 2 О)y+ х. О 2

ОКИСЛЕНИЕ УГЛЕВОДОВ аэробный процесс Сх(Н 2 О)Y + х О 2 → х СО 2 + у Н 2 О + 38 АТФ Важнейшая биологическая роль углеводов – энергетическая О 2 + 2 е → 2 О 22 Н (от субстрата) – 2 e → 2 H+ О 2 - + 2 H+ → H 2 O Электронотранспортная цепь НАДН → Флавинадениндинклеотид (ФАДН) → Кофермент Q 10 → Цитохром b → Цитохром c → Цитохром a → O 2

Классификация углеводов УГЛЕВОДЫ Монозы биозы полиозы тетрозы Восстанавливающие пентозы Невосстанавливающие гексозы моногликаны гетерогликаны

Монозы –альдегидо- или кетоспирты

Число стереоизомеров зависит от числа хиральных центров и определяется по формуле N= 2 n, где n- число хиральных центров; у тетроз: N=22=4 (2 изомера из D-ряда, 2 -Lряда) у пентоз: N=23=8 (4 изомера D-ряда, 4 изомера-L-ряда) у гексоз: N=24=16 (8 изомеров D-ряда, 8 изомеров L-ряда)
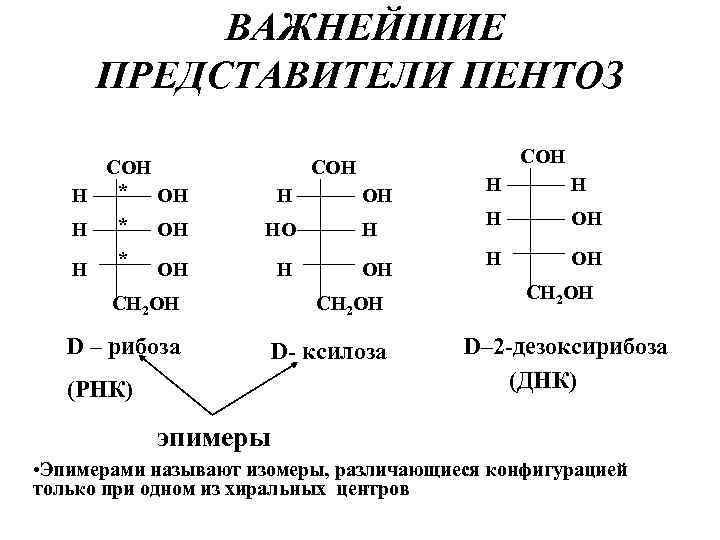
ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ ПЕНТОЗ СОН Н * СОН Н НО ОН Н ОН СН 2 ОН D – рибоза D- ксилоза (РНК) Н Н Н ОН СН 2 ОН D– 2 -дезоксирибоза (ДНК) эпимеры • Эпимерами называют изомеры, различающиеся конфигурацией только при одном из хиральных центров

ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ ГЕКСОЗ НО НО Н Н СОН * Н * ОН Н НО Н Н СН 2 ОН СОН * Н * ОН Н НО НО Н СН 2 ОН D- манноза D- глюкоза СОН * Н * ОН СН 2 ОН D- галактоза СН 2 ОН Н Н С * * * О Н ОН ОН СН 2 ОН D-фруктоза ЭПИМЕРЫ (различия у 2 атома углерода) ЭПИМЕРЫ (различия у 4 атома углерода). ДИАСТЕРЕОМЕРЫ

5 -гидрокси пентаналь Полуацеталь

ТАУТОМЕРИЯ МОНОЗ +δ Н НО Н Н О С -δ Н ОН ОН СН 2 ОН ОН Н С Н НО С ОН Н О ОН СН 2 ОН α, Д - глюкопираноза + Н НО Н Н О ОН СН 2 ОН β, Д-глюкопираноза

Происхождение названия циклических форм моноз фуран пиран В названии пятичленных циклов к родоначальному слову фуран или пиран добавляется суффикс обозначающий принадлежность к углеводам оза,

Наиболее общепринятой формой изображения циклических форм углеводов являются структуры Хеуорса

Формулы Хеуорса Гидроксильная группа при новом центре асимметрии является полуацетальной (помечена красным ). Этот гидроксил называют также гликозидным. Гликозидный гидроксил проявляет более высокую реакционную способность по сравнению с остальными гидроксилами в молекуле углеводов СН 2 ОН О Н Н ОН ОН α, Д - глюкопираноза О Н ОН ОН Н НО Н СН 2 ОН ОН Н НО β, Д - глюкопираноза

При замыкании пятичленного цикла из D-глюкозы образуется α-Д-глюкофураноза и β-Д- глюкофураноза +δ Н НО Н Н О С 4 -δ Н ОН ОН СН 2 ОН ОН Н С С Н НО ОН О Н ОН СН 2 ОН α, Д-глюкофураноза + Н НО Н Н ОН О Н ОН СН 2 ОН β, Д-глюкофураноза

Формулы Хеуорса СН 2 ОН НО Н СН 2 ОН Н О Н Н Н ОН ОН ОН α, Д - глюкофураноза НО Н Н ОН β, Д - глюкофураноза

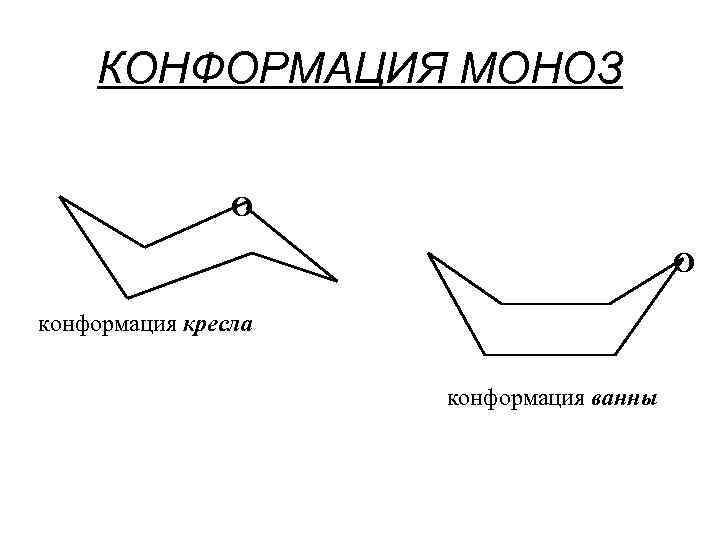
КОНФОРМАЦИЯ МОНОЗ О О конформация кресла конформация ванны
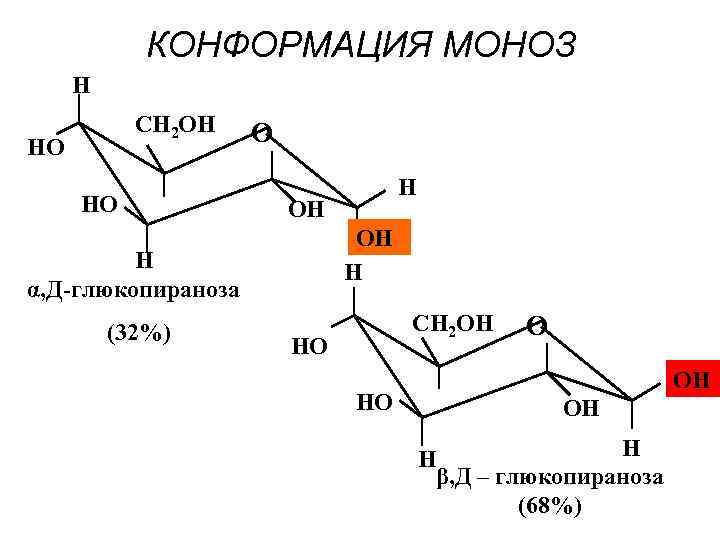
КОНФОРМАЦИЯ МОНОЗ Н СН 2 ОН НО НО О ОН ОН Н Н α, Д-глюкопираноза (32%) Н СН 2 ОН НО НО О ОН ОН Н Н β, Д – глюкопираноза (68%)

Взаимопревращение форм глюкозы друг в друга через образование линейной конформации носит название мутаротации:

Производные моносахаридов 1) АМИНОСАХАРА СОН Н НО NН 2 Н НО Н Н ОН ОН Н СН 2 ОН D-галактозамин Н НО NН – СН 3 Н О СН 2 ОН 2 -N- ацетил-D- глюкозамин

Производные моносахаридов 2) N-ацетилнейраминовая кислота (сиаловая кислота) – выстилает стенки сосудов. Сиаловая кислота препятствует отложению холестерина на стенках сосудов и образованию атеросклеротических бляшек СОН С СОН альдольная конденсация О СН 2 ——→ Н О +δ С -δ Н СН 3 –С - NН Н НО Н ОН СН 2 ОН N-ацетил-D-маннозамин С=О СН 2 Н – С - ОН Н 3 С –С - НN Н НО Н ОН ОН Н СН 2 ОН N-ацетилнейраминовая кислота

Производные моносахаридов Аскорбиновая кислота (витамин С) Синтез аскорбиновой кислоты -Н 2 О аскорбиновая кислота 2 -оксо – L- гулоновая кислота аскорбиновая кислота

Образование биоз Биозы довольно широко распространены в растительных и живых организмах. + + ά-D-глюкопираноза +Н 2 О ά-D-глюкопиранозил-1 -4 -ά-D-глюкопираноза (мальтоза) (ВОССТАНАВЛИВАЮЩАЯ БИОЗА)

Образование биоз с β-связью β –D-глюкопираноза ά-D-глюкопираноза +Н 2 О Β- D-глюкопиранозил-ά-D-глюкопираноза (целлобиоза) (ВОССТАНАВЛИВАЮЩАЯ БИОЗА)

Сравнительно редко встречается в свободном состоянии дисахарид целлобиоза, являющаяся структурной единицей целлюлозы:

Лактоза встречается чаще всего в молочной сыворотке, откуда получила свое тривиальное название. Женское молоко содержит до 8 % лактозы. Лактоза – восстанавливающая биоза

Очень широко в растительных материалах встречается и сахароза, соединение остатков глюкозы и фруктозы. Сахароза – невосстанавливающая биоза

Прочие дисахариды очень редки. К ним относятся невосстанавливающая биоза – трегалога. В ее структуре оба полуацетальных гидроксила у глюкозы заняты образованием гликозидной связи.

Еще более редкими являются трисахариды и тетрасахариды. Вообще, в природе олигосахариды (содержащие от 3 до 8 остатков моносахаров) практически не встречаются. В грибах и сахарной свекле присутствует трисахарид раффиноза:

Химические свойства моносахаридов 1. Реакции карбонильной группы Качественной реакцией на глюкозу является реакция «серебряного зеркала» (реакция Толленса): [Ag(NH 3)2]OH ─────→ 2 Ag + 3 NH 3 + H 2 O Глюконовая кислота D-глюкоза

Получение уроновых кислот Ферментативное окисление ↔ ↔ ─────→ Циклическая форма Dглюкуроновой D-глюкоза D-глюкуроновая кислота кислоты

Проба Троммера Сu(OH)2 ─────→ 2 D-глюкоза нагревание Хелатный комплекс, обладает свойствами окислителя ─────→ + Сu 2 O оксид меди (красный цвет) D-глюконовая кислота D

Реакция восстановления карбонильной группы моноз СН 2 ОH Н Ni, Pt, Pd (катализатор) D-глюкоза * Н Н ─────→ ОН НО Н 2 * * ОН Н * ОН СН 2 ОН D-сорбит

Реакция углеводов со спиртами Углеводы взаимодействуют со спиртами как в карбонильной, так и в полуацетальной форме C 2 H 5 OH ─────→ С 2 Н 5 OH ─────→ D-глюкоза Полуацеталь Ацеталь D-глюкозы

Реакции алкилирования по полуацетальному или гликозидному гидроксилу СН 2 ОН О Н ОН НО СН 3 ОН О Н НСl (газ) ОН ОН α, Д-глюкопираноза + Н 2 О ОН О-СН 3 НО ОН О-метил-α, Д-глюкопираноза

Реакции алкилирования по всем 5 гидроксильным группам СН 3 Cl + α, Д-глюкопираноза Н 2 О пента метил-α, Д-глюкопираноза Реакции ацилирования по всем 5 гидроксильным группам α, Д-глюкопираноза - Пента ацетил-α, Д-глюкопираноза

Реакции нуклеофильного присоединения по карбонильной группе моноз СN Н Н Н+ CN- C OН ОН Н ─────→ НО ОН СН 2 ОН D-глюкоза Гидроксинитрил D-глюкозы Глюкоза (40% раствор) используется для детоксикации организма, вызванного цианид-ионами, например, при употреблении ядер свежих абрикосовых косточек, содержащих НCN, при лечении нитропруссидом натрия Na 2 Fe(NO)(CN)5
LEKTsIYa__15_po_monosakharidam_polnaya_s_pravkoy.ppt