Обмен белков-1.ppt
- Количество слайдов: 22

Лекция № 15 ТЕМА: ОБМЕН ПРОСТЫХ БЕЛКОВ. ДЕЗАМИНИРОВАНИЕ И ТРАНСАМИНИРОВАНИЕ АМИНОКИСЛОТ Лектор: доцент

Сгорание 1 грамма белка - 16, 8 к. Дж энергии 8 дней безбелковой диеты - выделение азота - 53 мг/сут/кг 53*70=3. 71 г азота/сут 6. 25*3. 71=23. 2 г белка/сут - коэффициент изнашивания (Рубнера)

Азот вводимый в организм (пища) Азотистый = баланс Азот выводимый из организма (моча, кал, пот) N ввод > N вывод + Nввод < Nвывод - Nввод = Nвывод Азотистое равновесие

ЭНДО ЭКЗО Пепсин Желудочный сок реннин гастриксин трипсин химотрипсин Панкреатический сок эластаза карбоксипептидаза аминопептидаза Кишечный сок пептидазы
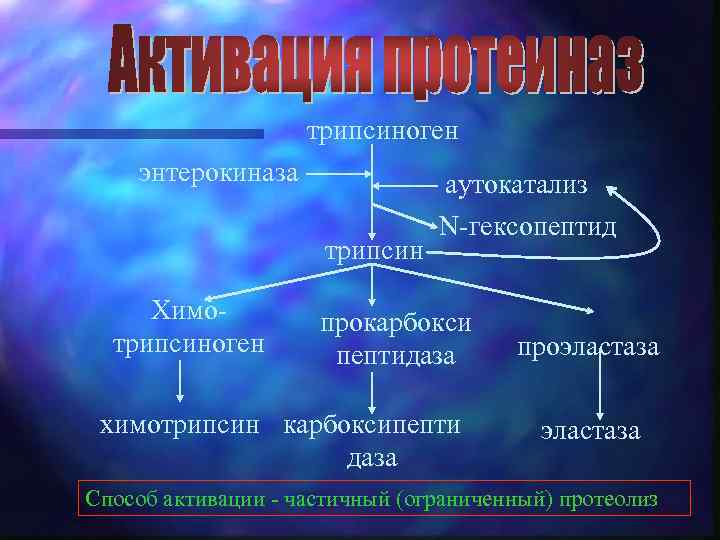
трипсиноген энтерокиназа трипсин Химотрипсиноген аутокатализ N-гексопептид прокарбокси пептидаза химотрипсин карбоксипепти даза проэластаза Способ активации - частичный (ограниченный) протеолиз

1. Активация пепсиногена 2. Создание р. Н оптимума для пепсина 3. Набухание и денатурация белков пищи 4. Бактерицидное действие 5. Стимуляция образования секретина
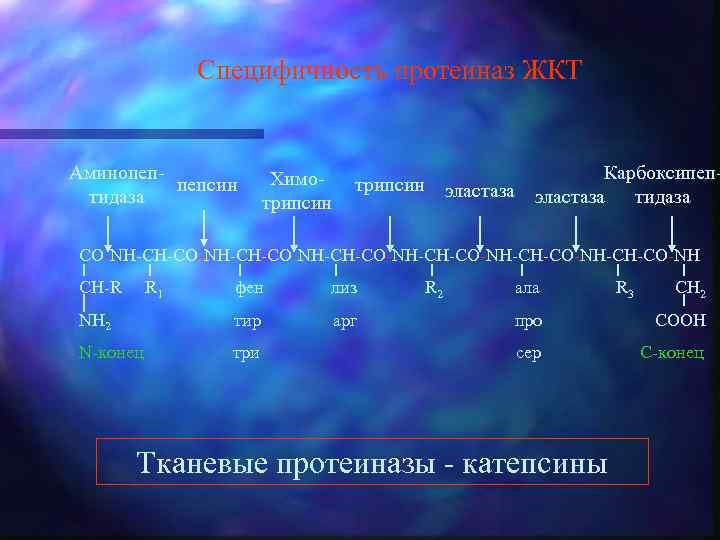
Специфичность протеиназ ЖКТ Аминопеппепсин тидаза Химотрипсин Карбоксипептрипсин эластаза тидаза CO-NH-CH-CO-NH-CH-CO-NH-CH-CO-NH CH-R R 1 фен лиз NH 2 тир арг N-конец три R 2 ала R 3 CH 2 про COOH сер C-конец Тканевые протеиназы - катепсины

а) NH 2 -CH-COOH (CH 2)4 NH 2 лиз H 2 N-CH 2 -CH 2 -NH 2 кадаверин CO 2 Орнитин путресцин CO 2 б) Серосодержащие H 2 S сероводород CO 2 CH 3 SH - метил CH 3 CH 2 SH - этил меркаптаны
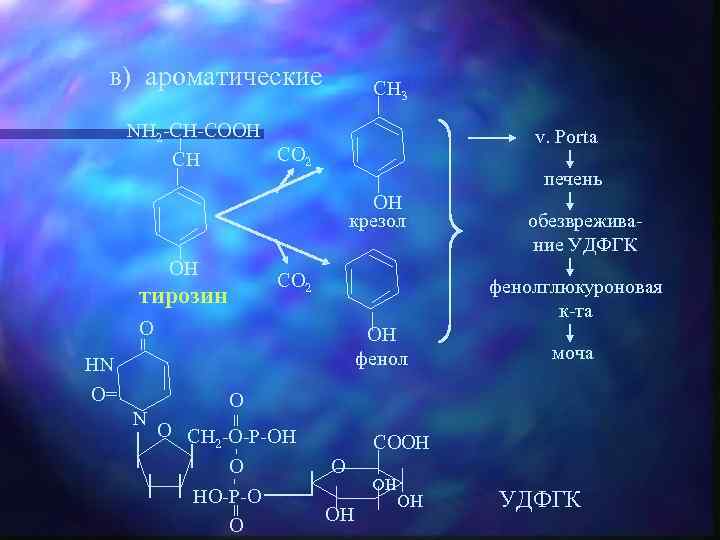
в) ароматические CH 3 NH 2 -CH-COOH CO 2 CH v. Porta печень OH крезол OH CO 2 тирозин фенолглюкуроновая к-та O OH фенол = = O CH -O-P-OH 2 COOH - N моча O O HO-P-O O = - HN O= обезвреживание УДФГК O OH OH OH УДФГК
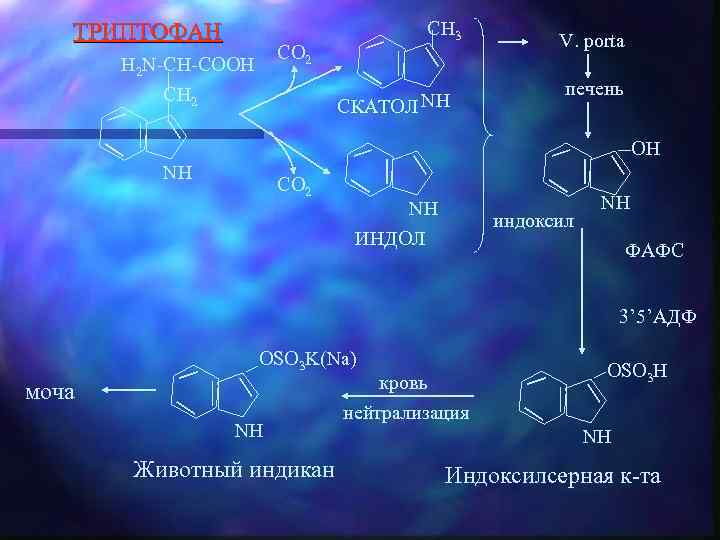
ТРИПТОФАН CH 3 CO 2 H 2 N-CH-COOH CH 2 СКАТОЛ NH V. porta печень OH NH CO 2 NH ИНДОЛ индоксил NH ФАФС 3’ 5’АДФ OSO 3 K(Na) моча NH Животный индикан кровь нейтрализация OSO 3 H NH Индоксилсерная к-та
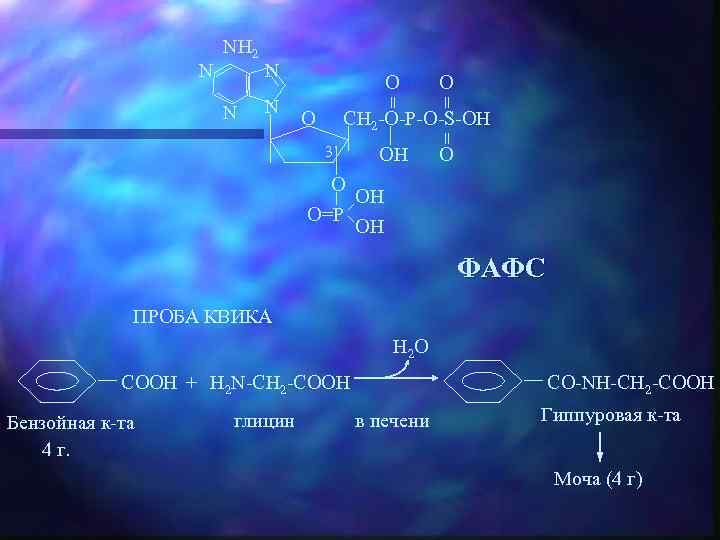
O OH = N O = N NH 2 CH 2 -O-P-O-S-OH O 3’ O O OH O=P OH ФАФС ПРОБА КВИКА H 2 O COOH + H 2 N-CH 2 -COOH Бензойная к-та 4 г. глицин CO-NH-CH 2 -COOH в печени Гиппуровая к-та Моча (4 г)
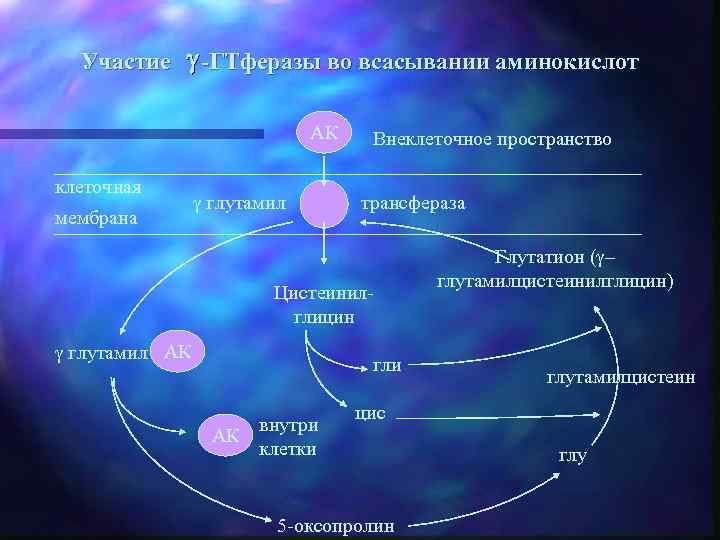
Участие -ГТферазы во всасывании аминокислот АК клеточная мембрана глутамил Внеклеточное пространство трансфераза Цистеинилглицин глутамил АК гли внутри АК клетки Глутатион ( – глутамилцистеинилглицин) глутамилцистеин цис 5 -оксопролин глу
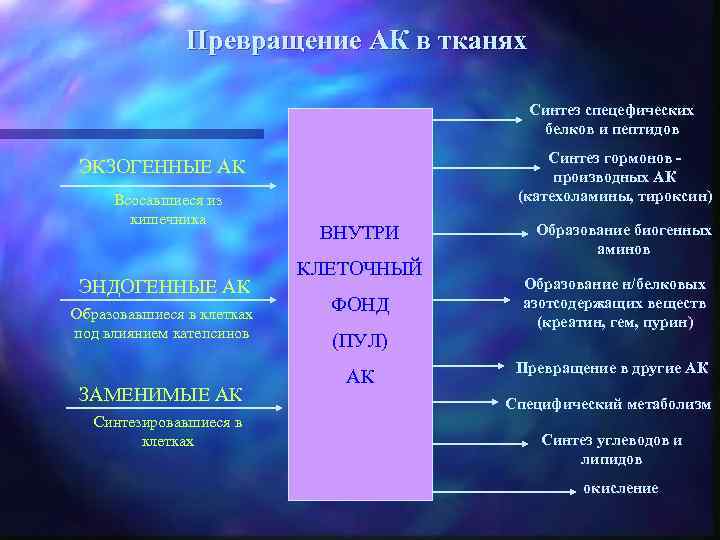
Превращение АК в тканях Синтез спецефических белков и пептидов Синтез гормонов производных АК (катехоламины, тироксин) ЭКЗОГЕННЫЕ АК Всосавшиеся из кишечника ЭНДОГЕННЫЕ АК Образовавшиеся в клетках под влиянием катепсинов ЗАМЕНИМЫЕ АК Синтезировавшиеся в клетках ВНУТРИ КЛЕТОЧНЫЙ ФОНД (ПУЛ) АК Образование биогенных аминов Образование н/белковых азотсодержащих веществ (креатин, гем, пурин) Превращение в другие АК Специфический метаболизм Синтез углеводов и липидов окисление
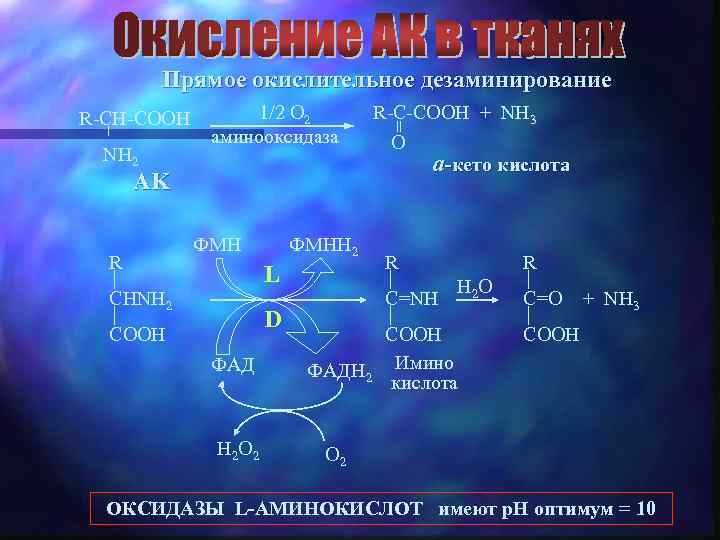
Прямое окислительное дезаминирование NH 2 1/2 O 2 аминооксидаза R-C-COOH + NH 3 = R-CH-COOH O AK R ФМНН 2 L CHNH 2 D COOH ФАД H 2 O 2 a-кето кислота R C=NH R H 2 O COOH ФАДН 2 Имино кислота C=O + NH 3 COOH O 2 ОКСИДАЗЫ L-АМИНОКИСЛОТ имеют p. H оптимум = 10

В физиологических условиях прямому окислительному дезаминированию подвергается только глутаминовая к-та COOH CHNH 2 CH 2 COOH глу НАД(Ф)Н 2 Глутаматдегидрогеназа (Гл. ДГ) COOH C=NH 2 C=O CH 2 Н 2 О CH 2 + NH 3 CH 2 COOH Имино к-та -кетоглу

R 1 R 2 CHNH 2 + COOH C=O COOH АК a - кето к-та Амино транс фераза ПФ (В 6) R 1 R 2 C=O + COOH CHNH 2 COOH a-кето к-та АК Механизм трансаминирования АК O CH -H 2 O = R 1 CH-NH 2 + COOH R 1 -кето C=O к-та COOH ПФ +H 2 O Пиридоксальфосфат +H 2 O NH 2 + Пиридок CH 2 самин фосфат ПФ R 1 CH-N=CH-ПФ COOH альдимин Шиффовы основания R 1 C=N-CH 2 -ПФ COOH кетимин
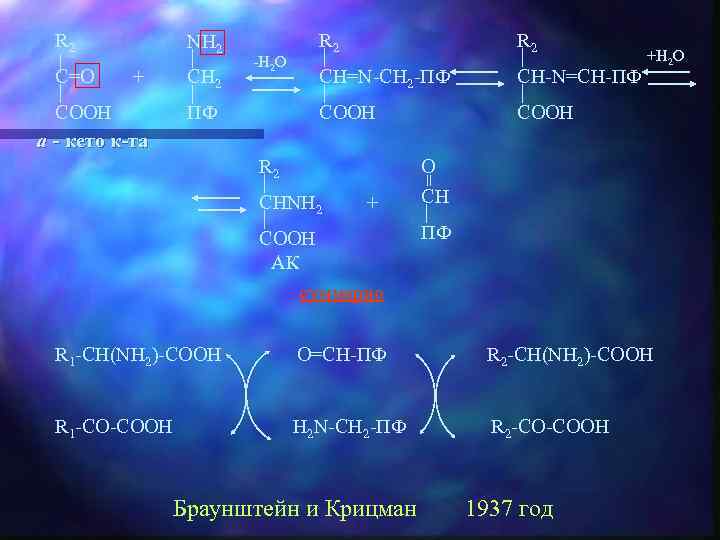
R 2 NH 2 + CH 2 COOH a - кето к-та ПФ C=O R 2 CH=N-CH 2 -ПФ CH-N=CH-ПФ COOH -H 2 O R 2 COOH O CH = R 2 +H 2 O CHNH 2 + COOH АК суммарно ПФ R 1 -CH(NH 2)-COOH O=CH-ПФ R 2 -CH(NH 2)-COOH R 1 -CO-COOH H 2 N-CH 2 -ПФ R 2 -CO-COOH Браунштейн и Крицман 1937 год

Из кето-кислот в реакциях трансаминирования чаще всего участвуют: ПВК, оксалоацетат, -кетоглутарат R CH 3 CHNH 2 + C=O COOH АК COOH ПВК R COOH CHNH 2 COOH АК R CHNH 2 + COOH АК Амино трансфераза ПФ R C=O CH 3 + COOH -кето к-та R Амино + трансфераза C=O CH 2 ПФ COOH Оксало -кето к-та COOH ацетат COOH R C=O Амино + трансфераза C=O (CH 2)2 кето ПФ глу COOH -кето к-та COOH + C=O CHNH 2 COOH ала COOH CHNH 2 COOH асп CHNH 2 (CH 2)2 COOH глу

Аланин и аспартат в свою очередь могут вступить в реакцию трансаминированияс -кетоглутаратом CH 3 CHNH 2 + COOH ала COOH CH 3 Ал. АТ C=O CH 2 C=O ПФ COOH CH 2 ПВК COOH -кето-глу COOH CHNH 2 C=O CH 2 COOH асп + CH 2 COOH -кето-глу + CHNH 2 CH 2 COOH глу COOH Ас. АТ ПФ CHNH 2 C=O CH 2 COOH оксалоацетат + CH 2 COOH глу

ЗНАЧЕНИЕ АМИНОТРАНСФЕРАЗ 1. Очень активные и распространенные в тканях ферменты, особенно Ас. АТ и Ал. АТ 2. В результате их действия образуются заменимые аминокислоты ала, асп, и особенно важно глутаминовая, единственная, которая подвергается прямому окислительному дезаминированию 3. Способ образования -кетокислот из АК без продукции аммиака 4. Определение активности Ас. АТ и Ал. АТ в крови имеет диагностическое значение: определяют отношение Ас. АТ/Ал. АТ=1. 33 у здоровых людей; при инфаркте оно увеличивается при гепатите - уменьшается

Все АК, кроме глутаминовой окисляются путем непрямого окислительного дезаминирования Непрямое окислительное дезаминирование = трансдезаминирование АК -кетокислота I трансаминирование -кетоглутарат L-глутамат II прямое окислительное дезаминирование глутамата H 2 O NH 3 Т. е. Непрямое окислительное дезаминирование проходит в 2 этапа: трансаминирование с выходом на глутаминовую к-ту и прямое окислительное дезаминирование глутаминовой кислоты. 1. 2.
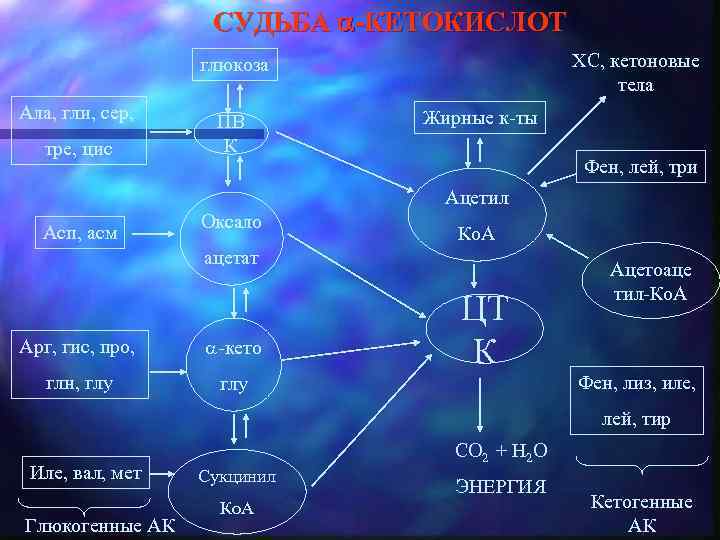
СУДЬБА -КЕТОКИСЛОТ ХС, кетоновые тела глюкоза Ала, гли, сер, тре, цис ПВ К Жирные к-ты Фен, лей, три Ацетил Асп, асм Оксало Ко. А ацетат Арг, гис, про, -кето глн, глу ЦТ К глу Ацетоаце тил-Ко. А Фен, лиз, иле, лей, тир Иле, вал, мет Глюкогенные АК CO 2 + H 2 O Сукцинил Ко. А ЭНЕРГИЯ Кетогенные АК
Обмен белков-1.ppt