Slayd_k_l_14.ppt
- Количество слайдов: 17

Лекция № 14 Химия неметаллов. Общая характеристика. продолжение
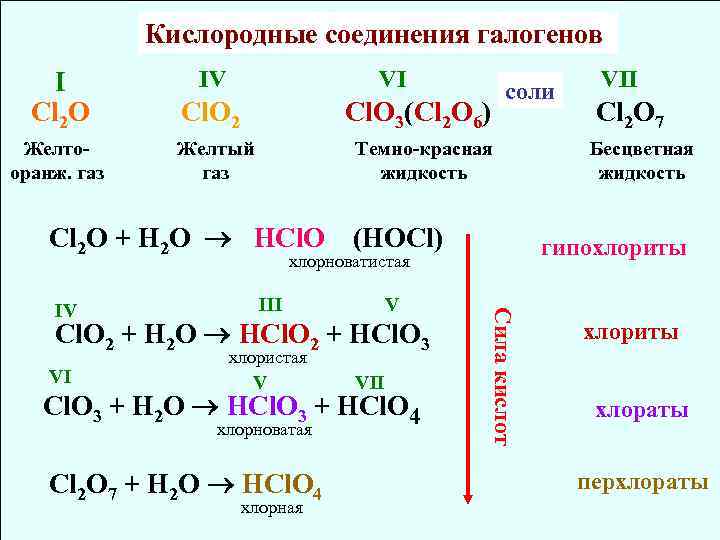
Кислородные соединения галогенов IV VI I Cl 2 O Cl. O 2 Cl. O 3(Cl 2 O 6) Желтооранж. газ Желтый газ Темно-красная жидкость Cl 2 O + H 2 O HCl. O соли (HOCl) V Cl. O 2 + H 2 O HCl. O 2 + HCl. O 3 VI хлористая V VII Cl. O 3 + H 2 O HCl. O 3 + HCl. O 4 хлорноватая Cl 2 O 7 + H 2 O HCl. O 4 хлорная Сила кислот III Cl 2 O 7 Бесцветная жидкость гипохлориты хлорноватистая IV VII хлориты хлораты перхлораты
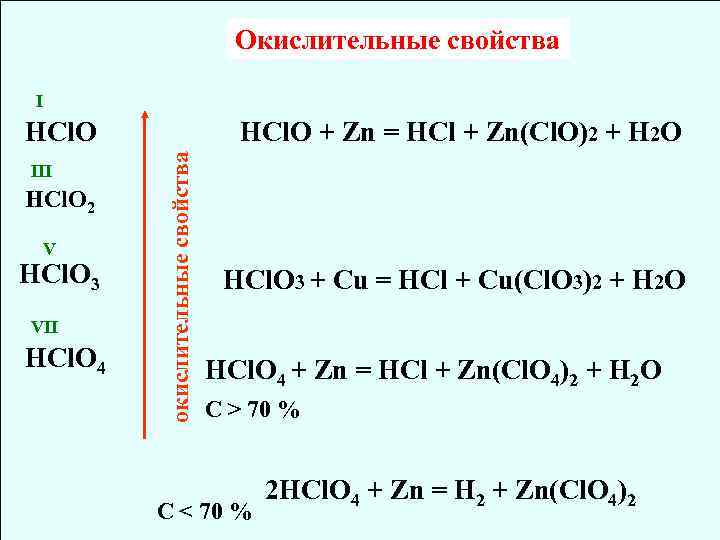
Окислительные свойства I III HCl. O 2 V HCl. O 3 VII HCl. O 4 HCl. O + Zn = HCl + Zn(Cl. O)2 + H 2 O окислительные свойства HCl. O 3 + Cu = HCl + Cu(Cl. O 3)2 + H 2 O HCl. O 4 + Zn = HCl + Zn(Cl. O 4)2 + H 2 O С > 70 % С < 70 % 2 HCl. O 4 + Zn = H 2 + Zn(Cl. O 4)2
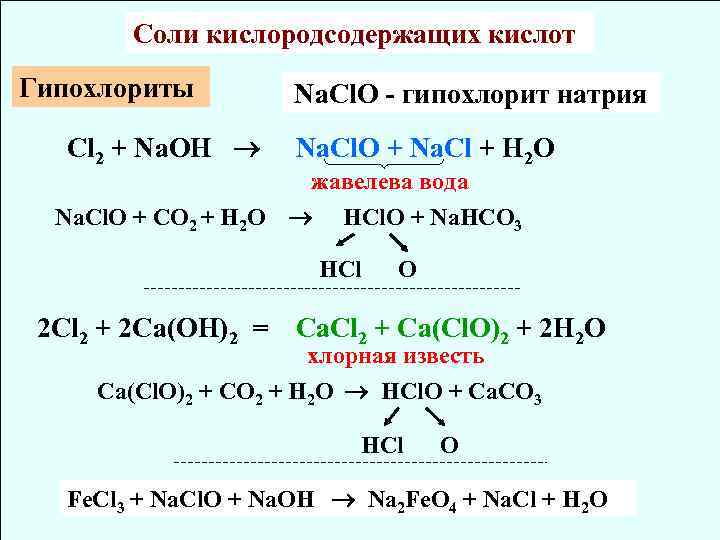
Cоли кислородсодержащих кислот Гипохлориты Cl 2 + Na. OH Na. Cl. O + CO 2 + H 2 O Na. Cl. O - гипохлорит натрия Na. Cl. O + Na. Cl + H 2 O жавелева вода HCl. O + Na. HCO 3 HCl 2 + 2 Ca(OH)2 = O Ca. Cl 2 + Ca(Cl. O)2 + 2 H 2 O хлорная известь Сa(Cl. O)2 + CO 2 + H 2 O HCl. O + Ca. CO 3 HCl O Fe. Cl 3 + Na. Cl. O + Na. OH Na 2 Fe. O 4 + Na. Cl + H 2 O
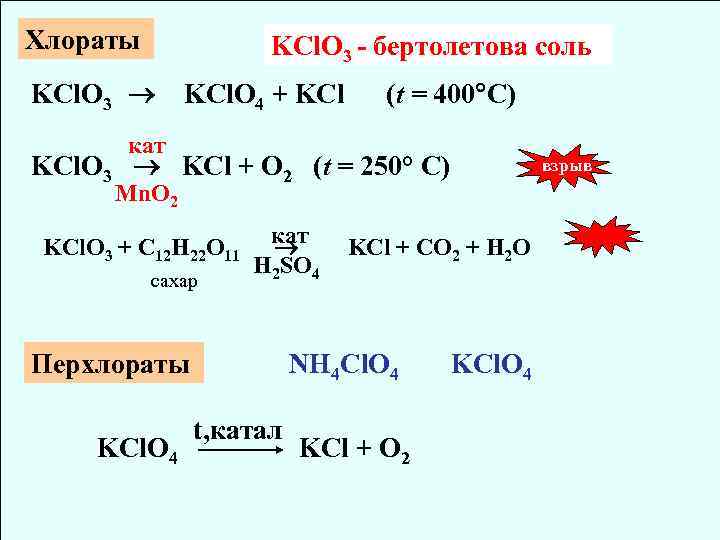
Хлораты KCl. O 3 - бертолетова соль KCl. O 3 KCl. O 4 + KCl (t = 400 C) кат KCl. O 3 KCl + O 2 (t = 250° C) взрыв Mn. O 2 KCl. O 3 + C 12 H 22 O 11 сахар кат H 2 SO 4 Перхлораты KCl. O 4 KCl + CO 2 + H 2 O NH 4 Cl. O 4 t, катал KCl + O 2 KCl. O 4

Кислородсодержащие кислоты брома и йода HBr. O 3 Бромноватая кислота - броматы HIO 3 Йодноватая кислота - йодаты KIO 3 + 3 Na 2 SO 3 KI + 3 Na 2 SO 4 KIO 3 +5 KI + 6 HCl 3 I 2 + 6 KCl + 3 H 2 O

Кислородные соединения халькогенов +IV SO 2 Se. O 2 Бесцв. газ Te. O 2 Бел. , тв. H 2 SO 3 Бел. , тв. H 2 Se. O 3 H 2 Te. O 3 SO 2 + n. H 2 O SO 2 · n. H 2 O (n=1 SO 2·H 2 O ≡ «H 2 SO 3 » ) SO 2·H 2 O H + + HSO 3 - KI ~ HSO 3 - H+ + SO 32 - + H 2 O HSO 3 + OH KII ~ 10 -8 Не выделена в свободном состоянии - SO 2 + Br 2 + H 2 O H 2 SO 4 + HBr SO 2 + H 2 S S + H 2 O 10 -2 Na 2 SO 3 + O 2 = Na 2 SO 4 Na 2 SO 3 Na 2 SO 4 + Na 2 S
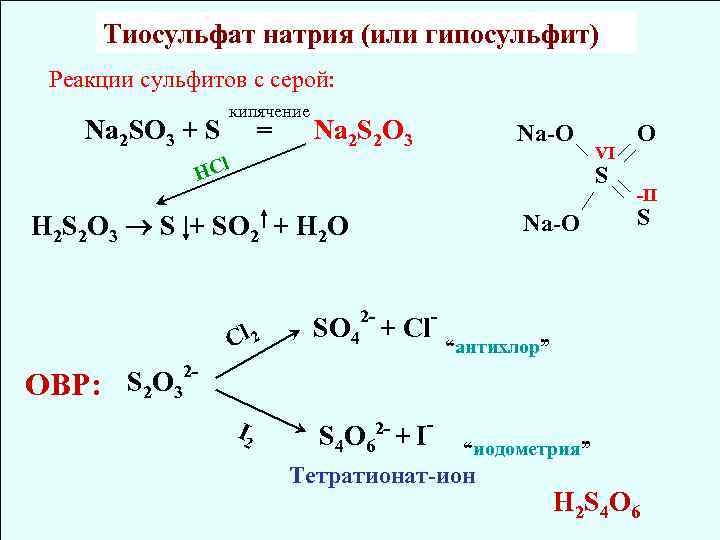
Тиосульфат натрия (или гипосульфит) Реакции сульфитов с серой: Na 2 SO 3 + S кипячение = Na 2 S 2 O 3 Na-O Cl VI S H H 2 S 2 O 3 S + SO 2 + H 2 O Na-O 2 - O -II S - Cl 2 SO 4 + Cl I 2 2 S 4 O 6 + I “антихлор” S 2 O 32 ОВР: “иодометрия” Тетратионат-ион H 2 S 4 O 6
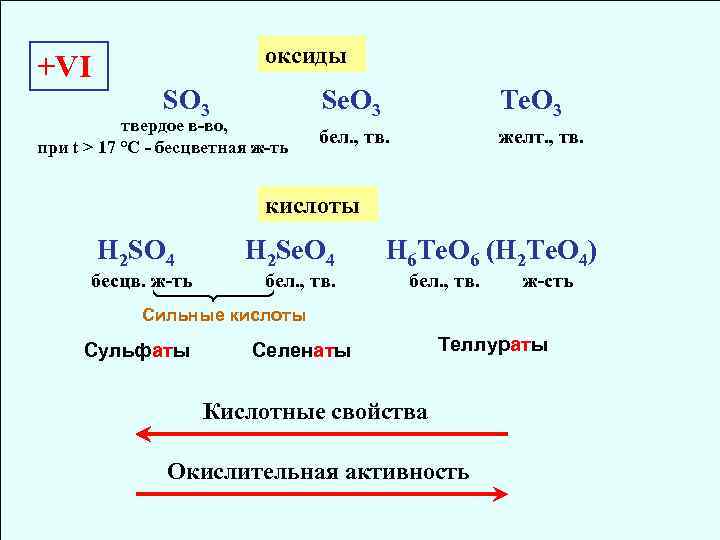
оксиды +VI SO 3 твердое в-во, при t > 17 °С - бесцветная ж-ть Se. O 3 Te. O 3 бел. , тв. желт. , тв. кислоты H 2 SO 4 H 2 Se. O 4 бесцв. ж-ть бел. , тв. H 6 Te. O 6 (H 2 Te. O 4) бел. , тв. ж-сть Сильные кислоты Сульфаты Селенаты Теллураты Кислотные свойства Окислительная активность
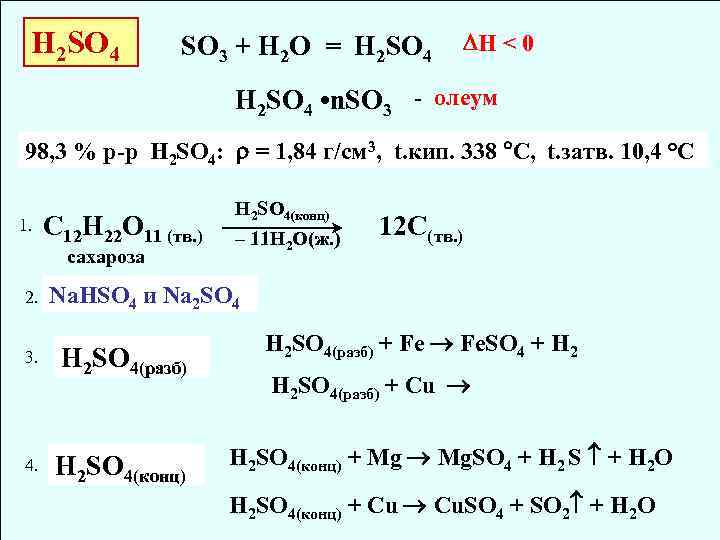
H 2 SO 4 SO 3 + H 2 O = H 2 SO 4 H < 0 H 2 SO 4 • n. SO 3 - олеум 98, 3 % р-р H 2 SO 4: = 1, 84 г/см 3, t. кип. 338 С, t. затв. 10, 4 °C 1. C 12 H 22 O 11 (тв. ) сахароза 2. 3. 4. H 2 SO 4(конц) – 11 H 2 O(ж. ) 12 С(тв. ) Na. HSO 4 и Na 2 SO 4 H 2 SO 4(разб) H 2 SO 4(конц) H 2 SO 4(разб) + Fe Fe. SO 4 + H 2 SO 4(разб) + Cu H 2 SO 4(конц) + Mg Mg. SO 4 + H 2 S + H 2 O H 2 SO 4(конц) + Cu Cu. SO 4 + SO 2 + H 2 O

Cоли серной кислоты Соли – сульфаты и гидросульфаты. Ba. SO 4, Sr. SO 4, Pb. SO 4 видио № 11 Имеют наибольшее практическое значение: Cu. SO 4 · 5 H 2 O - медный купорос Fe. SO 4 · 7 H 2 O - железный купорос Zn. SO 4 · 7 H 2 O I - цинковый купорос M MIII(SO 4)2 · n. H 2 O - фотография - медицина - крашение тканей - квасцы KAl(SO 4)2 · 12 H 2 O - алюмокалиевые квасцы - медицина - производство KCr(SO 4)2 · 12 H 2 O - хромокалиевые квасцы бумаги

Пиросерная (двусерная) кислота и ее соли H 2 SO 4·n. SO 3 - олеум K 2 S 2 O 7 >35°С 2 KHSO 4 SO 3 + H 2 SO 4 H 2 S 2 O 7 (H 2 SO 4 · SO 3 ) K 2 SO 4 + SO 3 до 240°С K 2 S 2 O 7 + H 2 SO 4 Пероксодисерная кислота и ее соли 2 H 2 SO 4 электролиз H 2 S 2 O 8 + H 2 SO 4 H+ + HSO 4 K 2 S 2 O 8 + KI = K 2 SO 4 + I 2 S 2 O 8 - + 2 e = 2 SO 422 I- - 2 e = I 2 полуреакция для окислителя полуреакция для восстановителя
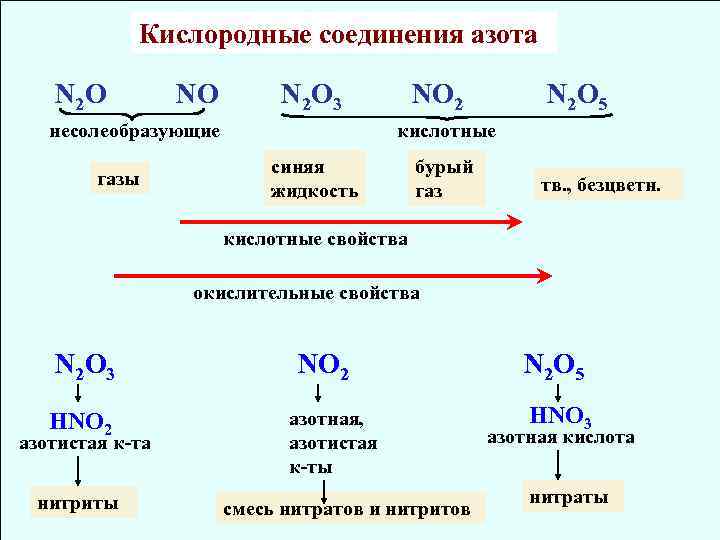
Кислородные соединения азота N 2 O NO N 2 O 3 несолеобразующие газы NO 2 N 2 O 5 кислотные синяя жидкость бурый газ тв. , безцветн. кислотные свойства окислительные свойства N 2 O 3 HNO 2 азотистая к-та нитриты NO 2 азотная, азотистая к-ты смесь нитратов и нитритов N 2 O 5 HNO 3 азотная кислота нитраты
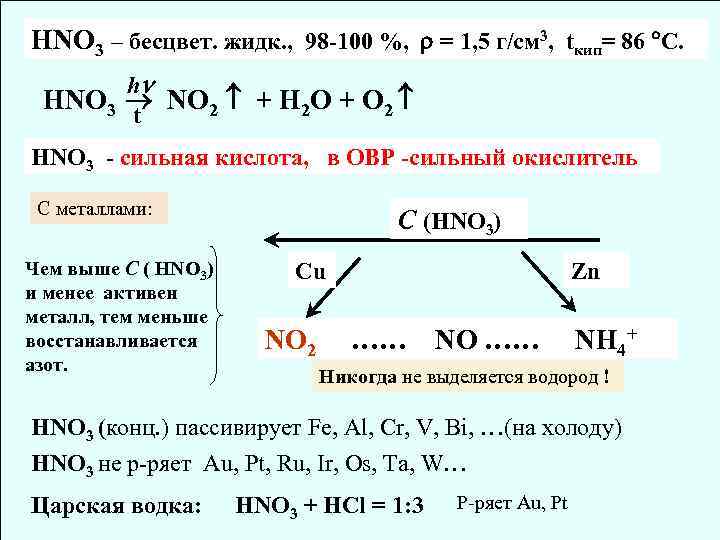
HNO 3 – бесцвет. жидк. , 98 -100 %, = 1, 5 г/см 3, tкип= 86 С. h HNO 3 NO 2 + H 2 O + O 2 t HNO 3 - сильная кислота, в ОВР -сильный окислитель C металлами: Чем выше C ( HNO 3) и менее активен металл, тем меньше восстанавливается азот. С (HNO 3) Cu NO 2 Zn …… NO …… NH 4+ Никогда не выделяется водород ! HNO 3 (конц. ) пассивирует Fe, Al, Cr, V, Bi, …(на холоду) HNO 3 не р-ряет Au, Pt, Ru, Ir, Os, Ta, W… Царская водка: HNO 3 + HCl = 1: 3 Р-ряет Au, Pt
![Au + HNO 3 + HCl H[Au. Cl 4] + NO + H 2 Au + HNO 3 + HCl H[Au. Cl 4] + NO + H 2](https://present5.com/presentation/140522884_167921906/image-15.jpg)
Au + HNO 3 + HCl H[Au. Cl 4] + NO + H 2 O C неметаллами: HNO 3 + S H 2 SO 4 + NO HNO 3 + P + H 2 O H 3 PO 4 + NO Нитраты: При нагревании разлагаются с выделение кислорода (О 2) Эл. -хим. ряд напряжений Меt. До Mg: От Mg до Сu : После Cu : Na. NO 3 Na. NO 2 + O 2 Pb(NO 3)2 Pb. O + NO 2 + O 2 Ag. NO 3 Ag + NO 2 +O 2 Нитраты натрия, калия, аммония, кальция - селитры в ОВР : Fe 2 O 3 + KNO 3 + KOH K 2 Fe. O 4 + KNO 2 + H 2 O

HNO 2 - азотистая кислота N 2 O 3 + H 2 O HNO 2 Разлагается: HNO 2 HNO 3 + NO + H 2 O Нитриты нестойкая, слабая к-та, сущ-ет в водном р-ре при низких тем-рах t = 3, 5 N 2 O 3 NO + NO 2 Хорошо растворимы в воде (кроме Ag. NO 2), ядовиты В ОВР – двойственная природа: Na. NO 2 + Na. Cl. O 3 Na. NO 3 + Na. Cl восстановитель Na. NO 2 + Na. I + H 2 SO 4 NO + I 2 + Na 2 SO 4 + H 2 O окислитель Реакции диспропорционирования: 3 HNO 2 HNO 3 + 2 NO + H 2 O

Термическое разложение нитритов: t - щелочных металлов: Li. NO 2 Li 2 O + NO + O 2 - других металлов: t Cd(NO 2)2 Cd. O + NO 2 t Ag. NO 2 Ag + NO 2 - благородных металлов: t - аммония: NH 4 NO 2 N 2 + H 2 O Нитриты натрия, калия находят применение в пищевой промышленности, в производстве красителей, в фотографии
Slayd_k_l_14.ppt