Clayd_k_l_13.ppt
- Количество слайдов: 44

Лекция № 13 Химия неметаллов. Общая характеристика. VIIA, VA подгруппы

VIIА подгруппа - галогены ns 2 np 5 Степени окисления Эл. строение rат ЭО -I F [He] 2 s 22 p 5 Cl [Ne] 3 s 23 p 5 Br [Ar] 3 d 104 s 24 p 5 - I, I, III, V, VII I [Kr] 4 d 105 s 25 p 5 - I, I, III, V, VII At [Xe] 4 f 145 d 106 s 26 p 5 - I, I, III, (IV), V, (VI), VII

VIА подгруппа - халькогены …ns 2 np 4 Эл. строение О S Se Te Po [He] [Ne] [Ar] [Kr] [Xe] Степени окисления 2 s 22 p 4 -II, (-I) 3 s 23 p 4 - II, (-I), IV, VI 3 d 104 s 24 p 4 4 d 105 s 25 p 4 4 f 145 d 106 s 26 p 4 II, IV rат ЭО
![VA подгруппа – подгруппа азота Степени окисления ns 2 np 3 N [He] 2 VA подгруппа – подгруппа азота Степени окисления ns 2 np 3 N [He] 2](https://present5.com/presentation/140522884_167921832/image-4.jpg)
VA подгруппа – подгруппа азота Степени окисления ns 2 np 3 N [He] 2 s 22 p 3 -III(-II, -I), I, III, IV, V P [Ne] 3 s 23 p 3 ЭО -III, (I), III, V As [Ar] 3 d 104 s 24 p 3 Sb [Kr] 4 d 105 s 25 p 3 Bi - III, V [Xe] 4 f 145 d 106 s 26 p 3 rат

Физические свойства галогенов F 2(г), Cl 2(г) Br 2(ж) I 2(к) I 2(г) Краснокоричневая жидкость с тяжелыми коричневыми парами Твердое вещество газы жёлтозелёного цвета Фтор – трудносжижаемый газ, t кип = -188 ºC Хлор – легко сжижается, t кип = -34 ºС t кип = - 59, 8°С Блестящие темнофиолетовые кристаллы

Физические свойства халькогенов Кислород O 2 - газ без запаха, без цвета жидкий кислород t кип = – 183°C Озон O 3 – бесцветный токсичный газ с характерным резким запахом
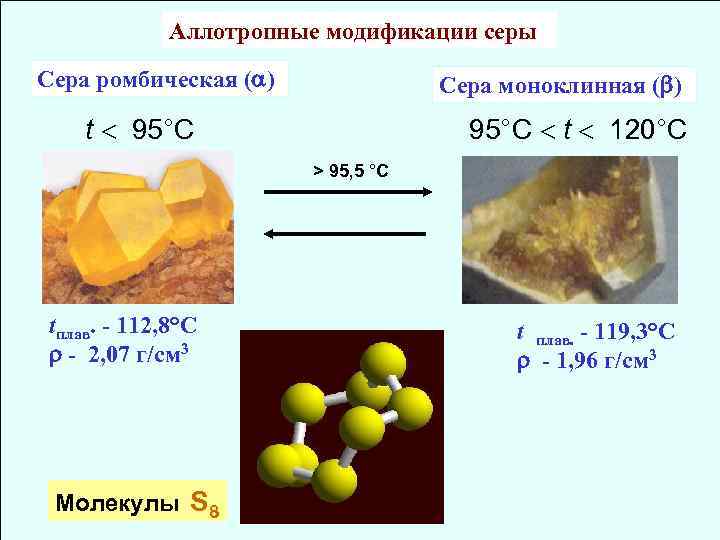
Аллотропные модификации серы Сера ромбическая ( ) Сера моноклинная ( ) t 95°C t 120°C > 95, 5 °C tплав. - 112, 8°С - 2, 07 г/см 3 Молекулы S 8 t плав. - 119, 3°C - 1, 96 г/см 3
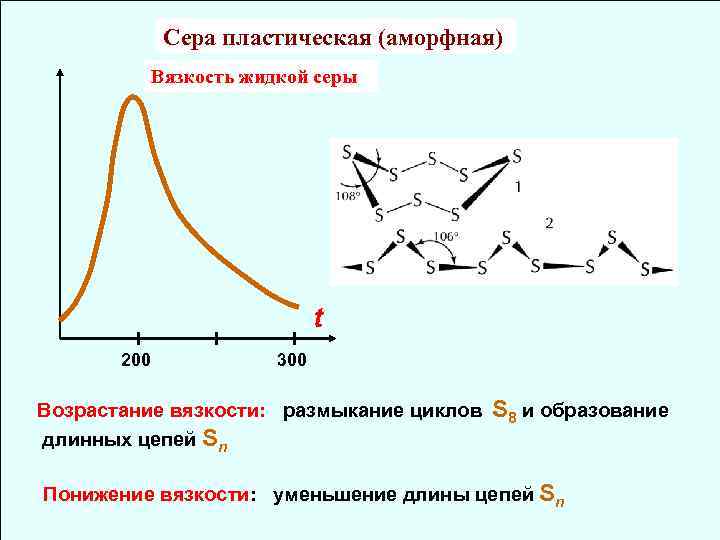
Сера пластическая (аморфная) Вязкость жидкой серы t 200 300 Возрастание вязкости: размыкание циклов длинных цепей Sn S 8 и образование Понижение вязкости: уменьшение длины цепей Sn

Физические свойства азота N 2 - газ 80 % (по объёму) N 2 в воздухе Na. NO 3 - чилийская селитра жидкий азот Tкип = – 196°C содержат в сосудах Дьюара

Химические свойства галогенов Все галогены - типичные окислители, их активность уменьшается при переходе от фтора к иоду C металлами: 2 Al + 3 F 2 2 Al. F 3 + Q 3 Cl 2 + 2 Al. Cl 3 + Q Br 2 + Al Al. Br 3 C неметаллами: F 2 + Si Si. F 4 H 2 + F 2 HF H 2 + Cl 2 2 HCl Взрыв ! Br 2 + H 2 2 HBr t – 200 -300 ºC I 2 + H 2 2 HI t – 500 -600 ºC Экзотерм.
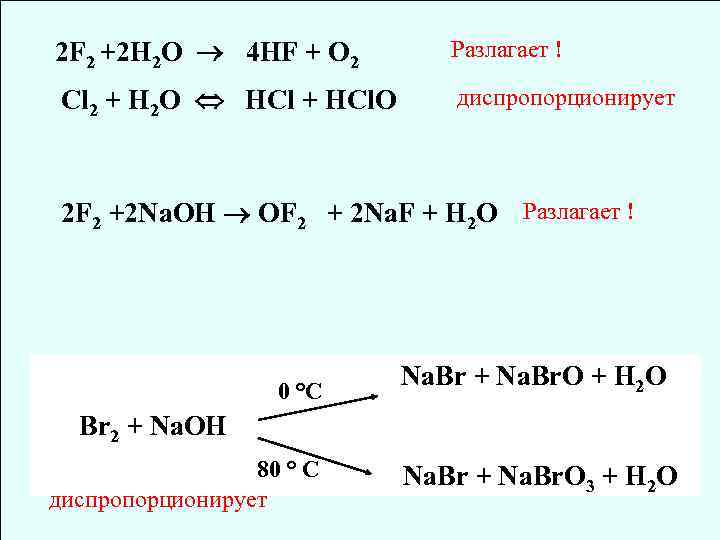
2 F 2 +2 H 2 O 4 HF + O 2 Разлагает ! Cl 2 + Н 2 О HCl + HCl. O диспропорционирует 2 F 2 +2 Na. OH OF 2 + 2 Na. F + H 2 O Разлагает ! 0 °C Na. Br + Na. Br. O + H 2 O Br 2 + Na. OH 80 ° C диспропорционирует Na. Br + Na. Br. O 3 + H 2 O
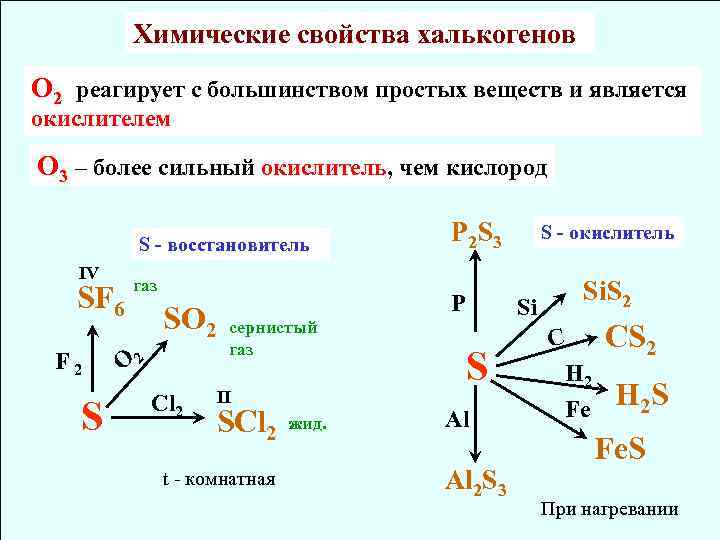
Химические свойства халькогенов O 2 реагирует с большинством простых веществ и является окислителем O 3 – более сильный окислитель, чем кислород S - восстановитель IV SF 6 F 2 S газ SО 2 Сl 2 P 2 S 3 P сернистый газ II SCl 2 t - комнатная жид. S - окислитель Si S Al Al 2 S 3 Si. S 2 C Н 2 Fe CS 2 H 2 S Fe. S При нагревании

Химические свойства азота : N N: Азот - активный неметалл и малоактивное простое вещество из-за высокой прочности тройной связи в молекуле АЗОТ – « безжизненный» N 2 + O 2 NO N 2 + H 2 NH 3 Li + N 2 Li 3 N N 2 + Na 3 N N 2 + Mg 3 N 2 + Al Al. N истинные нитриды Ti + N 2 Tix. Ny Zr + N 2 Zrx. Ny нитриды переменного состава тугоплавкие, коррозионностойкие материалы
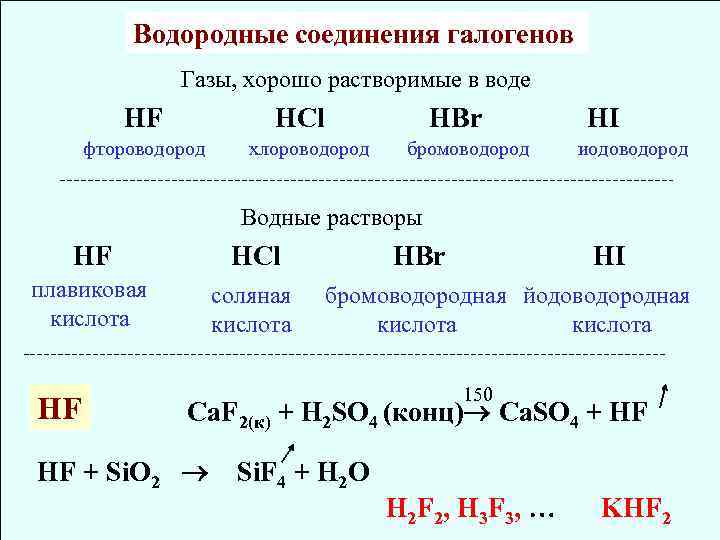
Водородные соединения галогенов Газы, хорошо растворимые в воде HF HCl фтороводород HBr хлороводород бромоводород HI иодоводород Водные растворы HF HCl плавиковая кислота соляная кислота HF HBr HI бромоводородная йодоводородная кислота 150 Сa. F 2(к) + H 2 SO 4 (конц) Ca. SO 4 + HF HF + Si. O 2 Si. F 4 + H 2 O H 2 F 2, H 3 F 3, KHF 2

HCl h H 2 + Cl 2 HCl (на свету) Na. Cl(тв. ) + H 2 SO 4(конц. ) = HCl ↑ + Na 2 SO 4 HCl конц. - сильнейший восстановитель HCl конц. + KMn. O 4 Cl 2 + HBr Растворимость HCl в воде велика, в 1 л воды при 25 ° С растворяется 426 л HCl. Максимальная концентрация кислоты составляет 35 -38 % HI HBr и HI – сильные кислоты. В ОВР являются восстановителями: 2 Cu 2+ + 4 Iˉ = 2 Cu. I + I 2 2 Iˉ + Br 2 = I 2 + 2 Brˉ + Cl 2 = Br 2 + 2 Clˉ

Cоли галогенов (галогениды) Большинство солей – хлоридов, бромидов и йодидов хорошо растворимы в воде, фториды хуже. Однако фторид серебра хорошо растворим. Ag. Cl Ag. Br Ag. I Ag. F белый кремовый бледножелтый растворим Cu. Cl белый Pb. Cl 2 белый Cu. I Pb. I 2 белый

Восстановительные свойства галогенид-ионов F- Cl- Br- I- восстановительные свойства F- - никогда не будет восстановителем Cl- - только в концентрированной HCl Br- - относительно слабый восстановитель I- - сильный восстановитель Na. Br + H 2 SO 4 Br 2 + SO 2 + Na 2 SO 4 + H 2 O Na. I+ H 2 SO 4 I 2 + H 2 S + Na 2 SO 4 + H 2 O
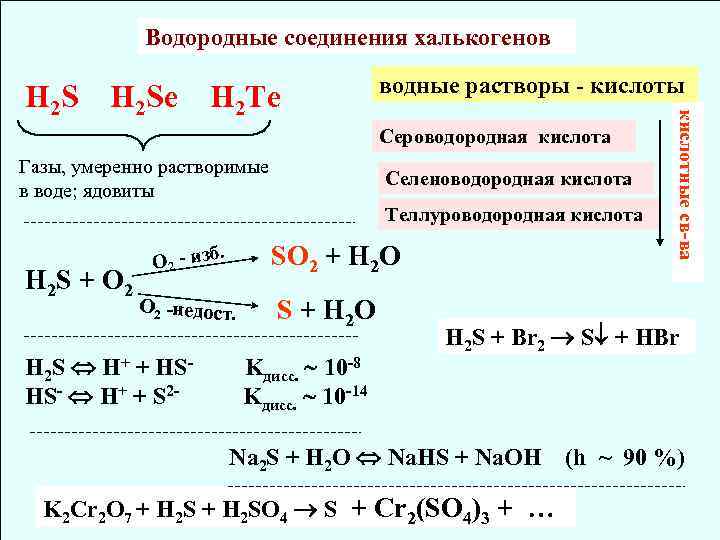
Водородные соединения халькогенов H 2 Se H 2 Te водные растворы - кислоты Сероводородная кислота Газы, умеренно растворимые в воде; ядовиты Селеноводородная кислота Теллуроводородная кислота H 2 S + O 2 - изб SO 2 + H 2 O . O 2 -недост. H 2 S H+ + HSHS- H+ + S 2 - S + H 2 O Kдисс. 10 -8 Kдисс. 10 -14 кислотные св-ва H 2 S + Br 2 S + HBr Na 2 S + H 2 O Na. HS + Na. OH (h ~ 90 %) K 2 Cr 2 O 7 + H 2 SO 4 S + Cr 2(SO 4)3 +

Cульфиды черные Pb. S, Сu. S, Fe. S, Ag 2 S, Hg. S желтые Cd. S, Sn. S 2 белы. Й Zn. S pозовый (телесный) Mn. S Полисульфиды Cульфиды – сильные восстановители Na 2 S + S = Na 2 S 2 дисульфид натрия ( Na 2 Sx ) x - от 2 до 9 Na — S — Na Fe. S 2

Аммиак (степень окисления азота -III) NH 3 Бесцветный газ с резким запахом (запах нашатыря), сжижается при -33, 4°С NH 4 Cl + Ca(OH)2 NH 3 + Ca. Cl 2 + H 2 O ( t = 200 C) При 20 ºС в 1 объеме Н 2 О - 700 объемов NH 3 ~ 25% р-р 10 %-ный раствор NH 3 – «нашатырный спирт» H 3 N HOH NH 3 • H 2 O водородная связь : NH 3 + H+ NH 4+ донорно-акцепторный механизм NH 3 + H 2 O NH 3 • H 2 O NH 4 OH NH 4+ + OHКдисс 10 -5 р. Н = 11, 8 слабое основание
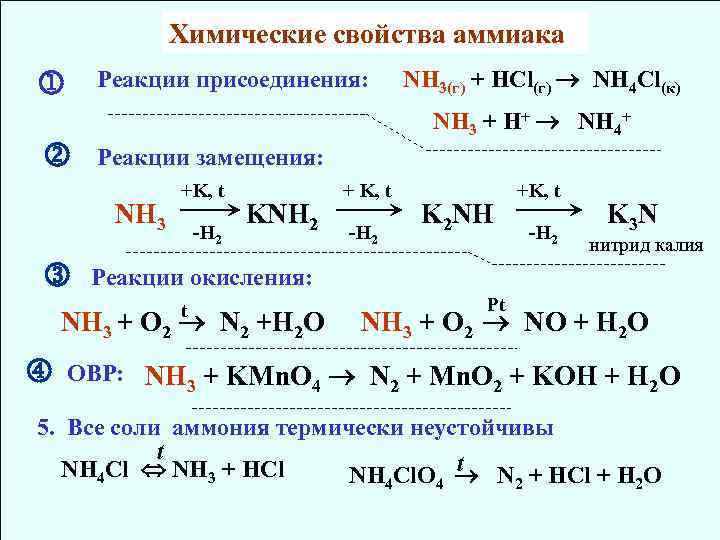
Химические свойства аммиака Реакции присоединения: NH 3(г) + HCl(г) NH 4 Cl(к) NH 3 + H+ NH 4+ Реакции замещения: NH 3 +K, t -H 2 KNH 2 -H 2 K 2 NH +K, t -H 2 K 3 N нитрид калия Реакции окисления: t NH 3 + O 2 N 2 +H 2 O + K, t Pt NH 3 + O 2 NO + H 2 O ОВР: NH 3 + KMn. O 4 N 2 + Mn. O 2 + KOH + H 2 O 5. Все соли аммония термически неустойчивы t t NH 4 Cl NH 3 + HCl NH 4 Cl. O 4 N 2 + HCl + H 2 O

Дополнительные материалы Лекция № 13 ХИМИЯ НЕМЕТАЛЛОВ ОБЩАЯ ХАРАКТЕРИСТИКА

Распространение в природе галогенов Cодержание в земной коре, % F флюорит Ca. F 2 криолит Na 3 Al. F 6 фторапатит Ca 5 F(PO 4)3 F Cl Br I 0, 03 0, 2 10 -4 10 -5 Сl сильвин KCl поваренная соль Na. Cl бишофит Mg. Cl 2 карналлит Mg. Cl 2 · KCl · 6 H 2 O At Br бромиды калия, натрия, магния содержатся в морской воде, в воде озер, в подземных рассолах I водоросли морской воды, подземные воды, соли иодаты, периодаты, сопутствующие другим минералам

ФЛЮОРИТ Ca. F 2

Минералы – хлориды Галит (Na. Cl) Сильвин (KCl)

Минералы, содержащие фтор Апатит Ca 5(PO 4)3 F, Cl Фосфорит

Распространение в природе халькогенов Содержание в земной коре, масс. % О S Se Te Po 47, 0 0, 05 10– 4 10– 7 10– 14

Кислород - самый распространённый элемент; - cоставляет 21 % земной атмосферы - входит в состав воды, оксидов кремния и алюминия; Озон - макс. содержание на высоте 25 км (озоновый слой). Сера - самородная сера; - минералы двух видов: сульфидные и сульфатные. - cера встречается в природном газе и сырой нефти

Основные минералы серы Fe. S 2 - пирит, а также железный или серный колчедан Pb. S - галенит или свинцовый блеск Zn. S - cфалерит или цинковая обманка Hg. S - киноварь Cu 2 S - халькозин Ni. S - миллерит Сu. Fe. S 2 - халькопирит или медный колчедан Ca. SO 4 2 H 2 O - гипс Ba. SO 4 - барит или тяжелый шпат Mg. SO 4 7 H 2 O - горькая или английская соль Селен и теллур - находятся в виде примесей в сульфидных рудах. Au 2 Te - калаверит или теллуристое золото

Природные соединения серы Сульфатная руда Гипс Ca. SO 4· 2 H 2 O Самородная сера Сульфидная руда Cu. Fe. S 2 Халькопирит (медный колчедан)

Методы получения
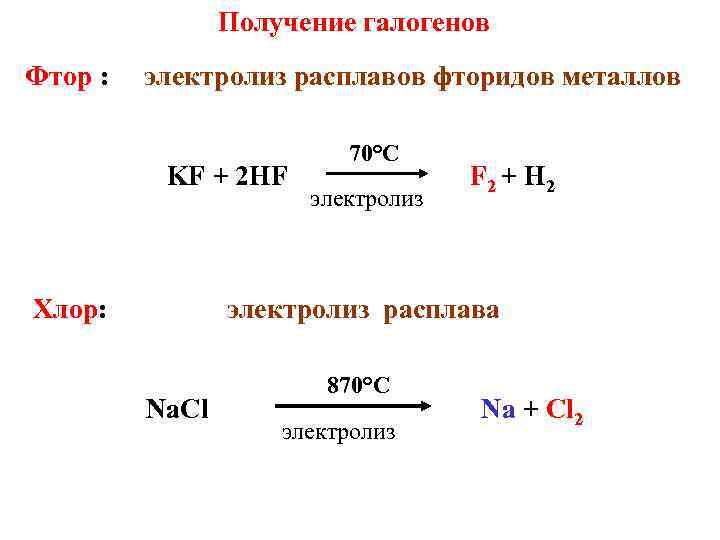
Получение галогенов Фтор : электролиз расплавов фторидов металлов KF + 2 HF Хлор: 70°C электролиз F 2 + H 2 электролиз расплава Na. Cl 870°С электролиз Na + Cl 2
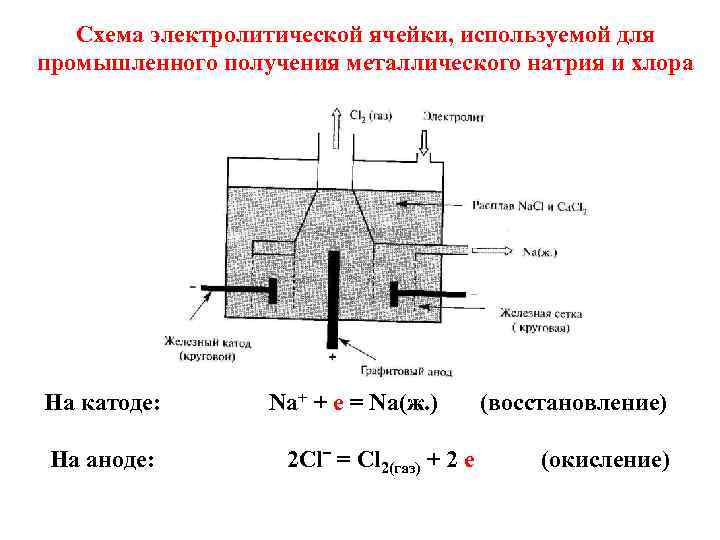
Cхема электролитической ячейки, используемой для промышленного получения металлического натрия и хлора На катоде: На аноде: Na+ + e = Na(ж. ) 2 Clˉ = Cl 2(газ) + 2 е (восстановление) (окисление)
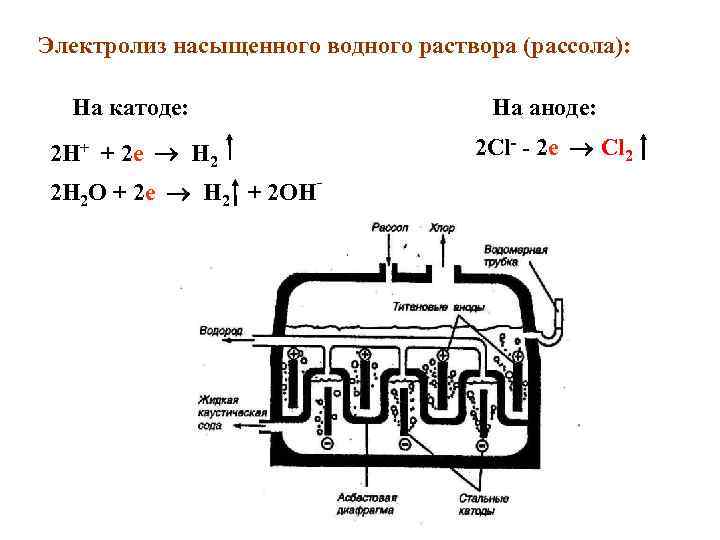
Электролиз насыщенного водного раствора (рассола): На катоде: 2 H+ + 2 e H 2 2 H 2 O + 2 e H 2 + 2 OHˉ На аноде: 2 Cl- - 2 e Cl 2

Cуммарная реакция 2 Na. Cl + 2 H 2 O электр. ток диафрагма H 2 + 2 Na. OH + Cl 2 продукты электролиза: хлор, водород, едкий натр (каустическая сода) В лаборатории его синтезируют по реакции: Мn. O 2 + 4 HCl = Mn. Cl 2 + 2 H 2 O Бром и иод получают, пропуская хлор через растворы бромидов и иодидов (используя морские и подземные буровые воды) 2 KBr + Cl 2 = Br 2 + 2 KCl 2 KI + Cl 2 = I 2 + 2 KCl
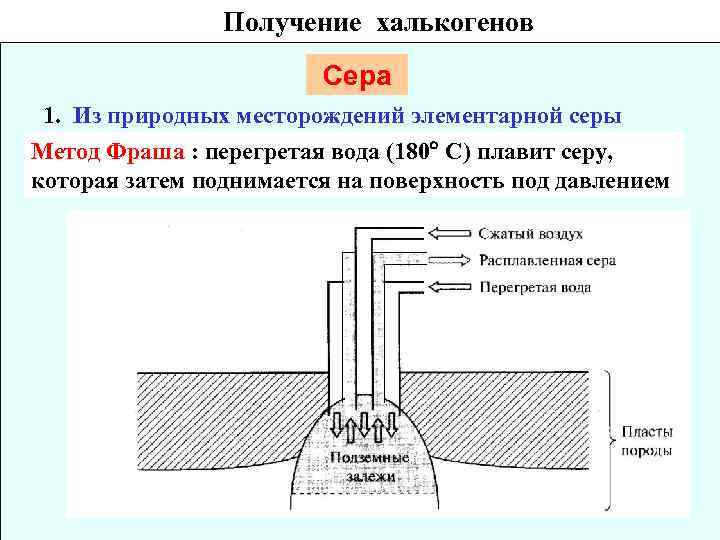
Получение халькогенов Сера 1. Из природных месторождений элементарной серы Метод Фраша : перегретая вода (180 С) плавит серу, которая затем поднимается на поверхность под давлением

2. Попутно из сульфидных руд. Важным источником получения серы служит железный колчедан (пирит) Fe. S 2 + H 2 SO 4 + O 2 t в автоклаве Cелен S + Fe 2(SO 4)3 + H 2 O Теллур Получают попутно из полупродуктов металлургии Pb, Cu, Ni Так, в производстве меди при электролитическом рафинировании в шламе накапливаются Se, Te, Ag, Au и др. элементы, откуда их извлекают.

ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ Fe. S 2 SO 3 H 2 SO 4 4 Fe. S 2+ 11 O 2= 2 Fe 2 O 3 + 8 SO 2 2 SO 2 + O 2 = 2 SO 3 + H 2 O = H 2 SO 4, ΔH < 0
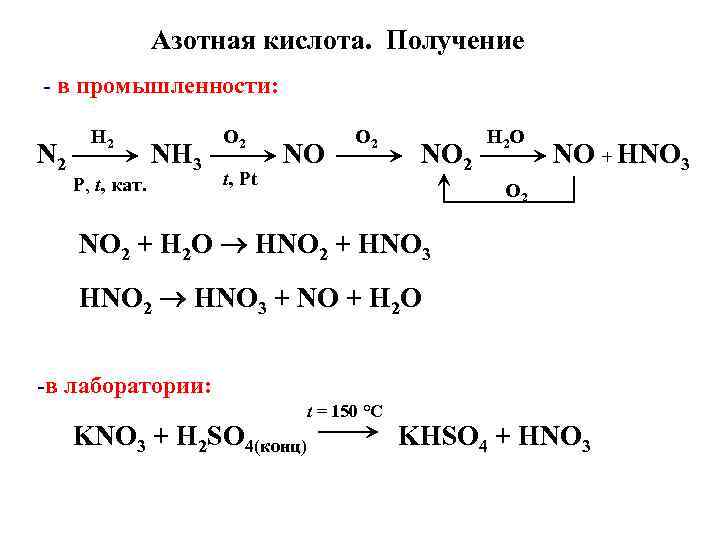
Азотная кислота. Получение - в промышленности: N 2 H 2 Р, t, кат. NH 3 O 2 t, Pt NO O 2 NO 2 H 2 O NO + HNO 3 O 2 NO 2 + H 2 O HNO 2 + HNO 3 HNO 2 HNO 3 + NO + H 2 O -в лаборатории: t = 150 °C KNO 3 + H 2 SO 4(конц) KHSO 4 + HNO 3

Области применения

Области применения галогенов F - металлургия Al, Be, Zr, Nb … - получение фторопластов, фреонов; - оптические материалы и волоконная оптика; - разделение изотопов урана в виде UF 6; Cl Br I - хлорная металлургия; - производство полимеров и растворителей; - синтез HCl; производство ПВХ - получение металлов высокой чистоты; - галогенные лампы; - медицина; фотография;

Области применения халькогенов S - производство серной кислоты - вулканизация каучука, органический синтез - производство спичек и черного пороха - сельское хозяйство - медицина Se - производство фотоэлементов и выпрямителей электрического тока, оптических приборов, в фотографии Те - добавка к сплавам

Основные области применения серной кислоты - производство неорганических кислот; - гидрометаллургия: производство цветных металлов; - травление металлов; - органический синтез; - производство взрывчатых веществ; - для очистки нефтепродуктов; - производство лекарственных препаратов и др.
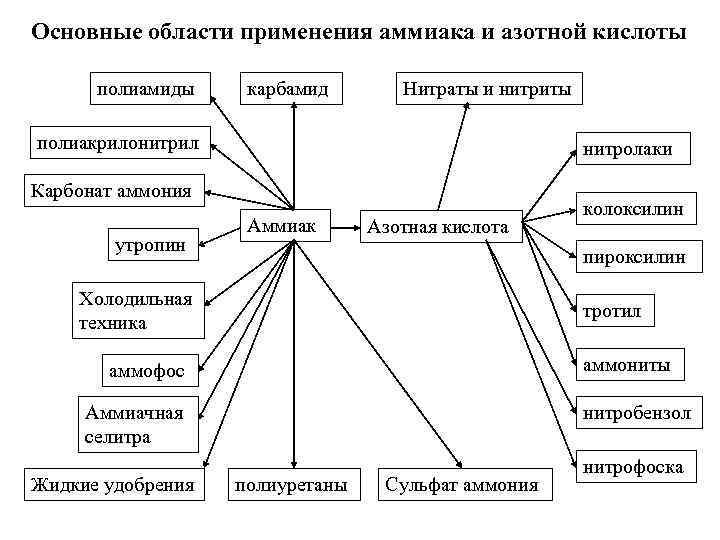
Основные области применения аммиака и азотной кислоты полиамиды карбамид Нитраты и нитриты полиакрилонитрил нитролаки Карбонат аммония утропин Аммиак Азотная кислота пироксилин Холодильная техника тротил аммониты аммофос Аммиачная селитра Жидкие удобрения колоксилин нитробензол полиуретаны Сульфат аммония нитрофоска
Clayd_k_l_13.ppt