Органич. реагенты в аналитике.pptx
- Количество слайдов: 41
 Лекция 13 ОРГАНИЧЕСКИЕ РЕАГЕНТЫ В АНАЛИТИЧЕСКОЙ ХИМИИ
Лекция 13 ОРГАНИЧЕСКИЕ РЕАГЕНТЫ В АНАЛИТИЧЕСКОЙ ХИМИИ
 План: 1. Реакции, основанные на образовании комплексных соединений металлов. 2. Реакции без участия комплексных соединений металлов. 3. Образование органических соединений, обладающих специфическими свойствами. Литература: Харитонов Ю. А. гл. 8, § 8. 1 -8. 3
План: 1. Реакции, основанные на образовании комплексных соединений металлов. 2. Реакции без участия комплексных соединений металлов. 3. Образование органических соединений, обладающих специфическими свойствами. Литература: Харитонов Ю. А. гл. 8, § 8. 1 -8. 3
 В качестве аналитических реагентов наряду с неорганическими широко используют органические соединения.
В качестве аналитических реагентов наряду с неорганическими широко используют органические соединения.
 ОРГАНИЧЕСКИЕ РЕАГЕНТЫ в аналитической химии (ОР), органические соединения различных классов, служащие для качественного обнаружения или количественного определения химических элементов.
ОРГАНИЧЕСКИЕ РЕАГЕНТЫ в аналитической химии (ОР), органические соединения различных классов, служащие для качественного обнаружения или количественного определения химических элементов.
 Органические соединения — класс химических соединений, в состав которых входит углерод.
Органические соединения — класс химических соединений, в состав которых входит углерод.
 Применение органических реагентов. Используя органические реагенты, можно выполнять реакцию различными методами и способами. Можно проводить реакцию в пробирке, на предметном стекле, на фильтровальной бумаге. Можно использовать капельный метод анализа, хроматографию, экстракцию, фотометрию, гравиметрию, титриметрию и др.
Применение органических реагентов. Используя органические реагенты, можно выполнять реакцию различными методами и способами. Можно проводить реакцию в пробирке, на предметном стекле, на фильтровальной бумаге. Можно использовать капельный метод анализа, хроматографию, экстракцию, фотометрию, гравиметрию, титриметрию и др.
 Преимущества органических реагентов перед неорганическими: образуются более чистые осадки, молекулярная масса продукта реакции с органическим реагентом выше, чем с неорганическим реагентом, образование малорастворимых осадков, высокая интенсивность окраски продукта реакции, многие комплексные соединения с органическими реагентами в воде не растворяются, что важно для использования в экстракции, изменяя р. Н, концентрацию, температуру и др. условия, можно повысить селективность определения.
Преимущества органических реагентов перед неорганическими: образуются более чистые осадки, молекулярная масса продукта реакции с органическим реагентом выше, чем с неорганическим реагентом, образование малорастворимых осадков, высокая интенсивность окраски продукта реакции, многие комплексные соединения с органическими реагентами в воде не растворяются, что важно для использования в экстракции, изменяя р. Н, концентрацию, температуру и др. условия, можно повысить селективность определения.
 Высокая чувствительность и избирательность органических реагентов в реакциях с ионами металлов способствовала их широкому применению в аналитической химии, но применение каждого органического реагента требует соблюдения определенных значений р. Н и соответствующего растворителя.
Высокая чувствительность и избирательность органических реагентов в реакциях с ионами металлов способствовала их широкому применению в аналитической химии, но применение каждого органического реагента требует соблюдения определенных значений р. Н и соответствующего растворителя.
 Механизм реакции с органическим реагентом Ионы металлов в водных растворах сами являются аквакомплексами, в которых нейтральные молекулы воды выполняют роль лиганда. Лиганд (донор) должен иметь хотя бы одну пару электронов, которую он может дать катиону металла (акцептору) на его вакантную орбиталь. Лиганды - органические реагенты - это обычно нейтральные молекулы с основными свойствами или в виде анионов.
Механизм реакции с органическим реагентом Ионы металлов в водных растворах сами являются аквакомплексами, в которых нейтральные молекулы воды выполняют роль лиганда. Лиганд (донор) должен иметь хотя бы одну пару электронов, которую он может дать катиону металла (акцептору) на его вакантную орбиталь. Лиганды - органические реагенты - это обычно нейтральные молекулы с основными свойствами или в виде анионов.
 Полифункциональный лиганд: Лиганд, имеющий несколько донорных атомов, через которые он может присоединяться к катиону металла, называется полифункциональным. При образовании комплексов с полифункциональными лигандами из гидратной оболочки катиона или из внутрисферного пространства комплексного акваиона вытесняется ровно столько молекул воды, сколько донорных атомов лиганда займут их места.
Полифункциональный лиганд: Лиганд, имеющий несколько донорных атомов, через которые он может присоединяться к катиону металла, называется полифункциональным. При образовании комплексов с полифункциональными лигандами из гидратной оболочки катиона или из внутрисферного пространства комплексного акваиона вытесняется ровно столько молекул воды, сколько донорных атомов лиганда займут их места.
 1. Реакции, основанные на образовании комплексных соединений металлов При таких аналитических реакциях преимущественно (хотя и не всегда) применяются циклообразующие лиганды, способные к построению хелатных комплексов, особенно внутрикомплексных соединений и комплексонатов металлов. Молекулы подобных лигандов должны содержать функциональные аналитические группы (ФАГ), способные образовы вать с атомами металлов комплексообразователей относительно прочные координационные связи, чаще всего устойчивые металлоциклы. В состав ФАГ могут входить группы ОН, SH, NН, С=О, C=S, гетероатомы азота и др.
1. Реакции, основанные на образовании комплексных соединений металлов При таких аналитических реакциях преимущественно (хотя и не всегда) применяются циклообразующие лиганды, способные к построению хелатных комплексов, особенно внутрикомплексных соединений и комплексонатов металлов. Молекулы подобных лигандов должны содержать функциональные аналитические группы (ФАГ), способные образовы вать с атомами металлов комплексообразователей относительно прочные координационные связи, чаще всего устойчивые металлоциклы. В состав ФАГ могут входить группы ОН, SH, NН, С=О, C=S, гетероатомы азота и др.
 Функционально-аналитичесекие группы (ФАГ) - это такие группы атомов, которые могут обеспечить механизм реакции. Например: карбоксильная группа СООН
Функционально-аналитичесекие группы (ФАГ) - это такие группы атомов, которые могут обеспечить механизм реакции. Например: карбоксильная группа СООН
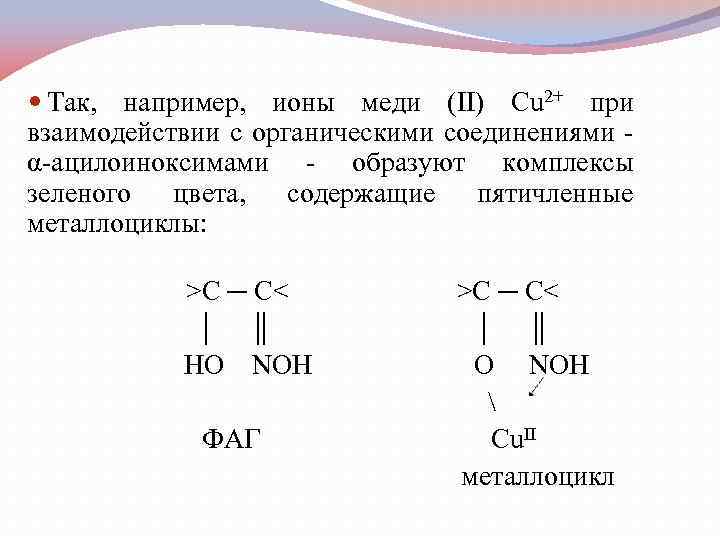 Так, например, ионы меди (II) Сu 2+ при взаимодействии с органическими соединениями α ацилоиноксимами образуют комплексы зеленого цвета, содержащие пятичленные металлоциклы: >C ─ C< │ ║ HO NOH O NOH ФАГ Cu. II металлоцикл
Так, например, ионы меди (II) Сu 2+ при взаимодействии с органическими соединениями α ацилоиноксимами образуют комплексы зеленого цвета, содержащие пятичленные металлоциклы: >C ─ C< │ ║ HO NOH O NOH ФАГ Cu. II металлоцикл
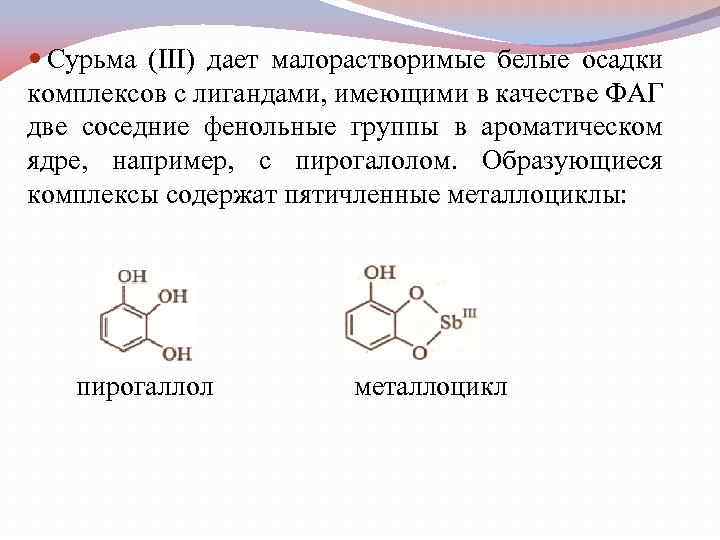 Сурьма (III) дает малорастворимые белыe осадки комплексов с лигандами, имеющими в качестве ФАГ две соседние фенольные группы в ароматическом ядре, например, с пирогалолом. Образующиеся комплексы содержат пятичленные металлоциклы: пирогаллол металлоцикл
Сурьма (III) дает малорастворимые белыe осадки комплексов с лигандами, имеющими в качестве ФАГ две соседние фенольные группы в ароматическом ядре, например, с пирогалолом. Образующиеся комплексы содержат пятичленные металлоциклы: пирогаллол металлоцикл
 Аналитико-активные группы (ААГ) - это такое сочетание атомов, которые, не изменяя механизма реакции, вызывают аналитический эффект. Аналитический эффект – изменение окраски, растворение или образование комплексного соединения.
Аналитико-активные группы (ААГ) - это такое сочетание атомов, которые, не изменяя механизма реакции, вызывают аналитический эффект. Аналитический эффект – изменение окраски, растворение или образование комплексного соединения.
 Функционально-аналитические группы, содержащие кислород, такие как: • гидроксидная группа -ОН, • карбонильная группа =С=О, • карбоксильная группа - СООН, • оксихиноидная группа, входят в реагенты, которые предпочтительны для катионов с электронной конфигурацией благородных газов: II A, III A группы. Например, катион Al 3+.
Функционально-аналитические группы, содержащие кислород, такие как: • гидроксидная группа -ОН, • карбонильная группа =С=О, • карбоксильная группа - СООН, • оксихиноидная группа, входят в реагенты, которые предпочтительны для катионов с электронной конфигурацией благородных газов: II A, III A группы. Например, катион Al 3+.
 Азотсодержащие реагенты • амино-группы -NH 2, =NH, =N- ; • третичный или циклический азот -N=; • азо-группа - N=N- ; • гидразо-группа =N-N=; • оксимная группа =C=NOH) образуют устойчивые комплексные соединения с катионами переходных металлов с частично заполненными d- и f- орбиталями ( Fe 2+, Fe 3+, Co 2+, Cr 3+, Mn 2+ и др. ).
Азотсодержащие реагенты • амино-группы -NH 2, =NH, =N- ; • третичный или циклический азот -N=; • азо-группа - N=N- ; • гидразо-группа =N-N=; • оксимная группа =C=NOH) образуют устойчивые комплексные соединения с катионами переходных металлов с частично заполненными d- и f- орбиталями ( Fe 2+, Fe 3+, Co 2+, Cr 3+, Mn 2+ и др. ).
 Реагенты, содержащие серу • меркапто-группа -SH; • тио-группа =C=S; и др. или сочетание этих группировок аминами, взаимодействуют легко с катионами с заполненными d-орбиталями ( Cu 2+, Zn 2+, Ag+) и с катионами, имеющими инертную пару S 2 электронов ( Sn 2+, Pb 2+)
Реагенты, содержащие серу • меркапто-группа -SH; • тио-группа =C=S; и др. или сочетание этих группировок аминами, взаимодействуют легко с катионами с заполненными d-орбиталями ( Cu 2+, Zn 2+, Ag+) и с катионами, имеющими инертную пару S 2 электронов ( Sn 2+, Pb 2+)
 Понятие о ФАГ и ААГ было введено Л. М. Кульбергом. К некоторым основным критериям применения внутрикомплексных соединений в химическом анализе относятся: а) малая растворимость комплексного соединения в тех случаях, когда их используют для осаждения ионов металлов из растворов; б) наличие интенсивной характерной окраски образующихся комплексов, если их используют для открытия или определения ионов металлов по окраске раствора; в) достаточно высокая устойчивость образующихся комплексов (большие значения констант устойчивости).
Понятие о ФАГ и ААГ было введено Л. М. Кульбергом. К некоторым основным критериям применения внутрикомплексных соединений в химическом анализе относятся: а) малая растворимость комплексного соединения в тех случаях, когда их используют для осаждения ионов металлов из растворов; б) наличие интенсивной характерной окраски образующихся комплексов, если их используют для открытия или определения ионов металлов по окраске раствора; в) достаточно высокая устойчивость образующихся комплексов (большие значения констант устойчивости).
 Для обеспечения этих критериев необходимо соблюдение следующих условий: 1) молекулы органических реагентов должны содержать ФАГ; 2) ФАГ должны иметь такую пространственную конфигурацию и взаимное расположение донорных атомов (азота, кислорода, серы, фосфора, мышьяка и др. ), чтобы могла реализоваться возможность образования наиболее устойчивых пяти и шестичленных металлоциклов; 3) молекула органического лиганда должна иметь, по возможности большую молекулярную массу это понижает погрешности определения металлов.
Для обеспечения этих критериев необходимо соблюдение следующих условий: 1) молекулы органических реагентов должны содержать ФАГ; 2) ФАГ должны иметь такую пространственную конфигурацию и взаимное расположение донорных атомов (азота, кислорода, серы, фосфора, мышьяка и др. ), чтобы могла реализоваться возможность образования наиболее устойчивых пяти и шестичленных металлоциклов; 3) молекула органического лиганда должна иметь, по возможности большую молекулярную массу это понижает погрешности определения металлов.
 На практике процессы комплексообразования часто сочетают с экстракцией. Некоторые органические реагенты позволяют открывать или определять целый ряд катионов. К числу таких органических реагентов относятся соединения группы арсеназо, содержащие мышьяк, азогруппы, SО 3 Н, ОН (арсеназо I, арсеназо III, полиарсеназо), например: арсеназо I арсеназо III
На практике процессы комплексообразования часто сочетают с экстракцией. Некоторые органические реагенты позволяют открывать или определять целый ряд катионов. К числу таких органических реагентов относятся соединения группы арсеназо, содержащие мышьяк, азогруппы, SО 3 Н, ОН (арсеназо I, арсеназо III, полиарсеназо), например: арсеназо I арсеназо III
 Так, с помощью арсеназо I можно определять уранилъную группу UO 22+, катионы кальция Са 2+, бериллия Ве 2+, меди Сu 2+, кобальта Со 2+, никеля Ni 2+, алюминия Al. З+, редкоземельных металлов, титан (III), цирконий (IV), торий (IV), вaнaдий (V), ниобий (V), тaнтaл (V), а также анионы F , BF 4. Арсеназо III позволяет определять катионы Ве 2+, Mg 2+, Са 2+, Zn 2+, Cd 2+, Hg 2+, Al. З+, Рb 2+, редкоземельных металлов, титан (IV), цирконий (IV), гафний (IV), торий (IV).
Так, с помощью арсеназо I можно определять уранилъную группу UO 22+, катионы кальция Са 2+, бериллия Ве 2+, меди Сu 2+, кобальта Со 2+, никеля Ni 2+, алюминия Al. З+, редкоземельных металлов, титан (III), цирконий (IV), торий (IV), вaнaдий (V), ниобий (V), тaнтaл (V), а также анионы F , BF 4. Арсеназо III позволяет определять катионы Ве 2+, Mg 2+, Са 2+, Zn 2+, Cd 2+, Hg 2+, Al. З+, Рb 2+, редкоземельных металлов, титан (IV), цирконий (IV), гафний (IV), торий (IV).
 К числу достаточно распространенных в химическом анализе относятся, например, такие органические реагенты, как дитизон, диметилглисим, 1 нитрозо 2 нафтол. Дuтизон, дифенилтиокарбазон S ║ С 6 Н 5 NН NН С N=N C 6 Н 5 (сокращенно H 2 Dz) впервые был предложен в качестве реагента на катионы цинка Zn 2+, с которыми он образует комплекс мaлинового цвета дитизонат цинка Zn(НDz)2, растворимый в хлороформе и в тетрахлориде углерода. Реакция весьма чувствительная: пре дел бнаружения т = о 0, 025 мкг, предельное разбавление Vlim = 104 мл/г. Дитизон используется также для определения Сu(II), Ag(I), Аu(III), Cd(II), Нg(II), In(III), Tl(I), Рb(II), Вi(III), Со(II), Ni(II), Pd(II), Pt(II) и некоторых других ионов.
К числу достаточно распространенных в химическом анализе относятся, например, такие органические реагенты, как дитизон, диметилглисим, 1 нитрозо 2 нафтол. Дuтизон, дифенилтиокарбазон S ║ С 6 Н 5 NН NН С N=N C 6 Н 5 (сокращенно H 2 Dz) впервые был предложен в качестве реагента на катионы цинка Zn 2+, с которыми он образует комплекс мaлинового цвета дитизонат цинка Zn(НDz)2, растворимый в хлороформе и в тетрахлориде углерода. Реакция весьма чувствительная: пре дел бнаружения т = о 0, 025 мкг, предельное разбавление Vlim = 104 мл/г. Дитизон используется также для определения Сu(II), Ag(I), Аu(III), Cd(II), Нg(II), In(III), Tl(I), Рb(II), Вi(III), Со(II), Ni(II), Pd(II), Pt(II) и некоторых других ионов.
 Дuметилглиокcuм реактив Чугаева) (диацетилдиоксим, СН 3 С=N ОН │ СН 3 С=N ОН это классический органический реагент, впервые предложенный, Л. А. Чугаевым в 1905 г. в качестве специфического се лективного реагента на никель. Ионы Ni 2+ образуют с диметилrлиоксимом в водной среде объемистый осадок красного цвета, малорастворимый в воде или в водном аммиаке, растворимый в минеральных кислотах. Реакция протекает по схеме:
Дuметилглиокcuм реактив Чугаева) (диацетилдиоксим, СН 3 С=N ОН │ СН 3 С=N ОН это классический органический реагент, впервые предложенный, Л. А. Чугаевым в 1905 г. в качестве специфического се лективного реагента на никель. Ионы Ni 2+ образуют с диметилrлиоксимом в водной среде объемистый осадок красного цвета, малорастворимый в воде или в водном аммиаке, растворимый в минеральных кислотах. Реакция протекает по схеме:
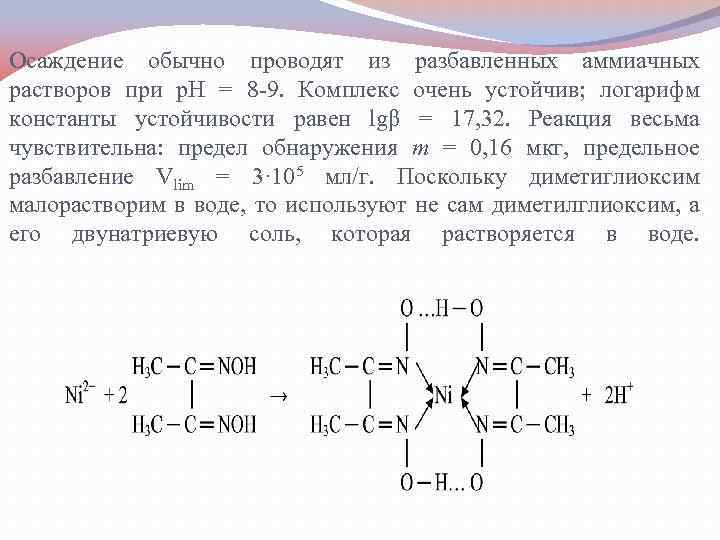 Осаждение обычно проводят из разбавленных аммиачных растворов при р. Н = 8 9. Комплекс очень устойчив; логарифм константы устойчивости равен lgβ = 17, 32. Реакция весьма чувствительна: предел обнаружения т = 0, 16 мкг, предельное разбавление Vlim = 3· 105 мл/г. Поскольку диметиглиоксим малорастворим в воде, то используют не сам диметилглиоксим, а его двунатриевую соль, которая растворяется в воде.
Осаждение обычно проводят из разбавленных аммиачных растворов при р. Н = 8 9. Комплекс очень устойчив; логарифм константы устойчивости равен lgβ = 17, 32. Реакция весьма чувствительна: предел обнаружения т = 0, 16 мкг, предельное разбавление Vlim = 3· 105 мл/г. Поскольку диметиглиоксим малорастворим в воде, то используют не сам диметилглиоксим, а его двунатриевую соль, которая растворяется в воде.
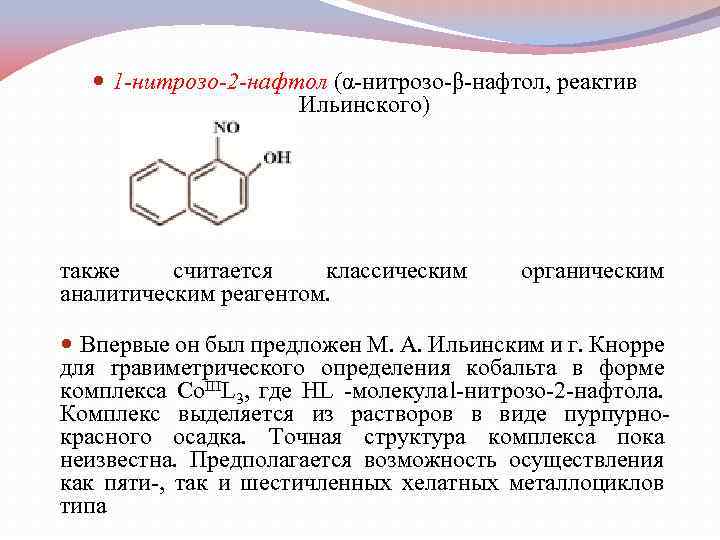 1 -нитрозо-2 -нафтол (α нитрозо β нафтол, реактив Ильинского) также считается классическим аналитическим реагентом. органическим Впервые он был предложен М. А. Ильинским и г. Кнорре для rpавиметрического определения кобальта в форме комплекса Со. IIIL 3, где НL молекула l нитрозо 2 нафтола. Комплекс выделяется из растворов в виде пурпурно красного осадка. Точная структура комплекса пока неизвестна. Предполагается возможность осyществления как пяти , так и шестичленных хелатных металлоциклов типа
1 -нитрозо-2 -нафтол (α нитрозо β нафтол, реактив Ильинского) также считается классическим аналитическим реагентом. органическим Впервые он был предложен М. А. Ильинским и г. Кнорре для rpавиметрического определения кобальта в форме комплекса Со. IIIL 3, где НL молекула l нитрозо 2 нафтола. Комплекс выделяется из растворов в виде пурпурно красного осадка. Точная структура комплекса пока неизвестна. Предполагается возможность осyществления как пяти , так и шестичленных хелатных металлоциклов типа
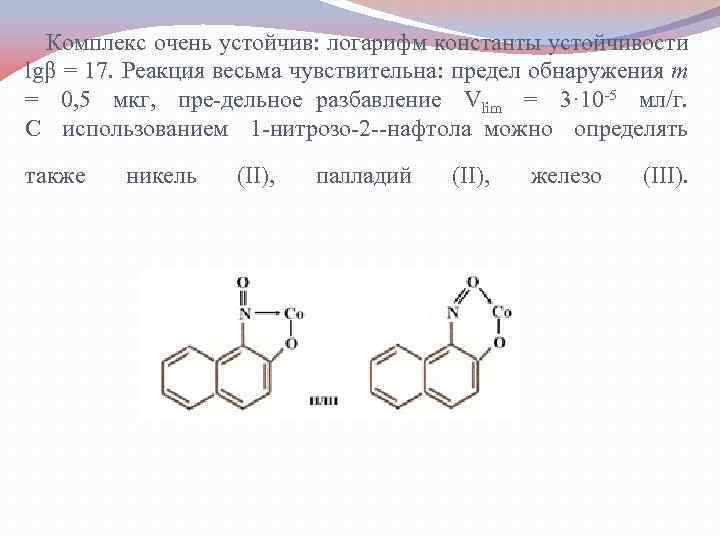 Комплекс очень устойчив: логарифм константы устойчивости lgβ = 17. Реакция весьма чувствительна: предел обнаружения т = 0, 5 мкг, пре дельное разбавление Vlim = 3· 10 5 мл/г. С использованием 1 нитрозо 2 нафтола можно определять также никель (II), паллaдий (II), железо (III).
Комплекс очень устойчив: логарифм константы устойчивости lgβ = 17. Реакция весьма чувствительна: предел обнаружения т = 0, 5 мкг, пре дельное разбавление Vlim = 3· 10 5 мл/г. С использованием 1 нитрозо 2 нафтола можно определять также никель (II), паллaдий (II), железо (III).
 2. Реакции без участия комплексных соединений металлов Образование окрашенных соединений с открываемыми веществами Дифениламин (C 6 Н 5)2 NН при реакциях в кислой среде с соединения ми, содержащими окислители (NO 2 , NO 3 , Br. O 3 , Сr. O 42 , Мn. O 4 , Fe 3+ и др. ), окрашивает растворы в синий цвет вследствие необратимого окис ления дифениламина в синий дифенилдифенохинондиимин. Эта реакция фармакопейная, используется для открытия нитратов и нитритов. С нитратами реакция протекает по схеме:
2. Реакции без участия комплексных соединений металлов Образование окрашенных соединений с открываемыми веществами Дифениламин (C 6 Н 5)2 NН при реакциях в кислой среде с соединения ми, содержащими окислители (NO 2 , NO 3 , Br. O 3 , Сr. O 42 , Мn. O 4 , Fe 3+ и др. ), окрашивает растворы в синий цвет вследствие необратимого окис ления дифениламина в синий дифенилдифенохинондиимин. Эта реакция фармакопейная, используется для открытия нитратов и нитритов. С нитратами реакция протекает по схеме:
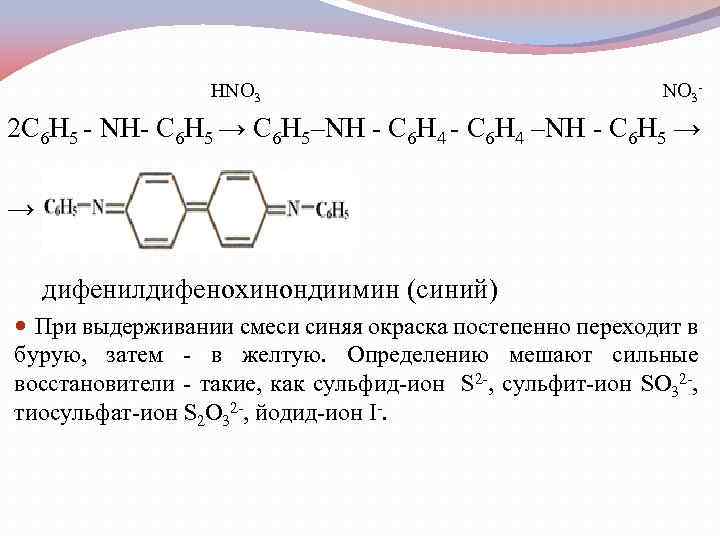 НNO 3 NO 3 2 С 6 Н 5 NН С 6 Н 5 → С 6 Н 5–NН С 6 Н 4 –NН С 6 Н 5 → → дифенилдифенохинондиимин (синий) При выдерживании смеси синяя окраска постепенно переходит в бурую, затем в желтую. Определению мешают сильные восстановители такие, как сульфид ион S 2 , сульфит ион SO 32 , тиосульфат ион S 2 O 32 , йодид ион I.
НNO 3 NO 3 2 С 6 Н 5 NН С 6 Н 5 → С 6 Н 5–NН С 6 Н 4 –NН С 6 Н 5 → → дифенилдифенохинондиимин (синий) При выдерживании смеси синяя окраска постепенно переходит в бурую, затем в желтую. Определению мешают сильные восстановители такие, как сульфид ион S 2 , сульфит ион SO 32 , тиосульфат ион S 2 O 32 , йодид ион I.
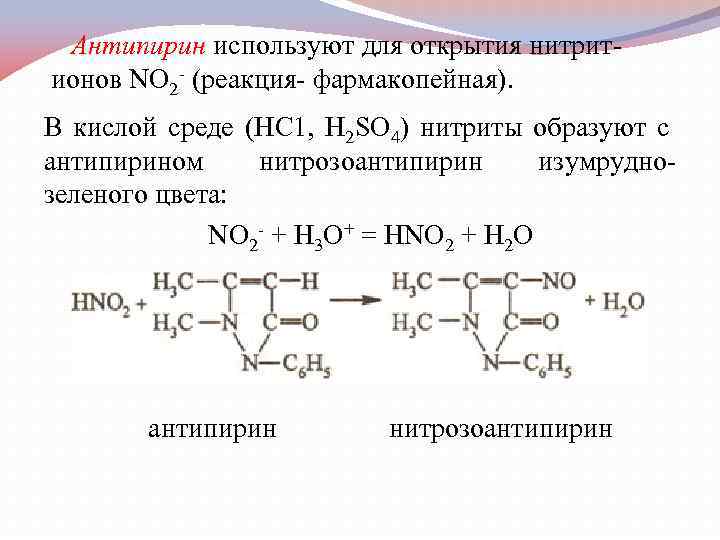 Антипирин используют для открытия нитрит ионов NO 2 (реакция фармакопейная). В кислой среде (НС 1, Н 2 SO 4) нитриты образуют с антипирином нитрозоантипирин изумрудно зеленого цвета: NO 2 + Н 3 О+ = НNO 2 + H 2 O антипирин нитрозоантипирин
Антипирин используют для открытия нитрит ионов NO 2 (реакция фармакопейная). В кислой среде (НС 1, Н 2 SO 4) нитриты образуют с антипирином нитрозоантипирин изумрудно зеленого цвета: NO 2 + Н 3 О+ = НNO 2 + H 2 O антипирин нитрозоантипирин
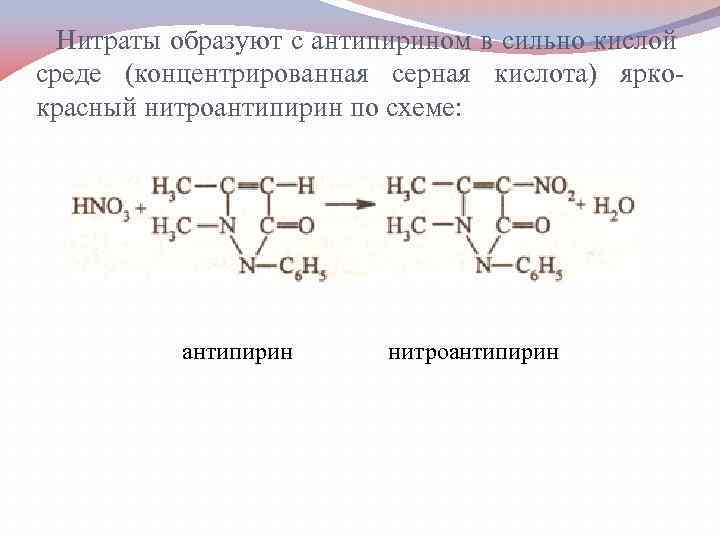 Нитраты образуют с антипирином в сильно кислой среде (концентрированная серная кислота) ярко красный нитроантипирин по схеме: антипирин нитроантипирин
Нитраты образуют с антипирином в сильно кислой среде (концентрированная серная кислота) ярко красный нитроантипирин по схеме: антипирин нитроантипирин
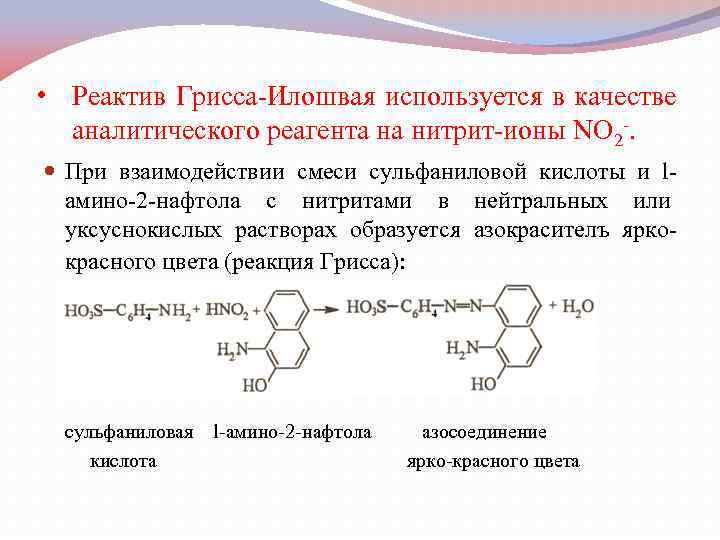 • Реактив Грисса Илошвая используется в качестве аналитического реагента на нитрит ионы NO 2. При взаимодействии смеси сульфаниловой кислоты и l амино 2 нафтола с нитритами в нейтральных или уксуснокислых растворах образуется азокрасителъ ярко красного цвета (реакция Грисса): сульфаниловая l амино 2 нафтола азосоединение кислота ярко красного цвета
• Реактив Грисса Илошвая используется в качестве аналитического реагента на нитрит ионы NO 2. При взаимодействии смеси сульфаниловой кислоты и l амино 2 нафтола с нитритами в нейтральных или уксуснокислых растворах образуется азокрасителъ ярко красного цвета (реакция Грисса): сульфаниловая l амино 2 нафтола азосоединение кислота ярко красного цвета
 Образование органических соединений, обладающих специфическими свойствами В ряде случаев в химическом анализе используют такие реакции с участием органических реагентов, в результате которых образуются продукты реакции, обладающие специфическими свойствами – запахом, окрашиванием пламени газовой горелки и т. д. Так, реакция образования сложных эфиров используется для открытия ацетат ионов СН 3 СОО , борат ионов BO 3 , В 4 О 7. Открытие ацетат ионов проводят в кислой среде. При этом ацетат ионы, присоединяя ион водорода, переходят в слабую уксусную кислоту. При реакции с этанолом уксусная кислота дает уксусноэтиловый эфир, обладающий характерным запахом: СН 3 СОО + Н 3 О+ = СН 3 СООН + Н 2 О СН 3 СООН + НОС 2 Н 5 = СНз. СООС 2 Н 5 + Н 2 О Реакция фармакопейная.
Образование органических соединений, обладающих специфическими свойствами В ряде случаев в химическом анализе используют такие реакции с участием органических реагентов, в результате которых образуются продукты реакции, обладающие специфическими свойствами – запахом, окрашиванием пламени газовой горелки и т. д. Так, реакция образования сложных эфиров используется для открытия ацетат ионов СН 3 СОО , борат ионов BO 3 , В 4 О 7. Открытие ацетат ионов проводят в кислой среде. При этом ацетат ионы, присоединяя ион водорода, переходят в слабую уксусную кислоту. При реакции с этанолом уксусная кислота дает уксусноэтиловый эфир, обладающий характерным запахом: СН 3 СОО + Н 3 О+ = СН 3 СООН + Н 2 О СН 3 СООН + НОС 2 Н 5 = СНз. СООС 2 Н 5 + Н 2 О Реакция фармакопейная.
 Образование органических соединений, обладающих специфическими свойствами Летучие сложные эфиры борной кислоты окрашивают пламя в зеленый цвет. В присутствии серной кислоты и этанола борат ионы образуют летучие сложные эфиры: В 4 О 7 + 2 Н+ + 5 Н 2 О = 4 Н 3 ВО 3 + ЗС 2 Н 5 ОН = В(ОС 2 Н 5)3 + ЗН 2 О При поднесении пламени к чашке или тиглю, в которых протекает эта реакция, продукты сгорания окрашивают пламя в зеленый цвет. Реакция фармакопейная.
Образование органических соединений, обладающих специфическими свойствами Летучие сложные эфиры борной кислоты окрашивают пламя в зеленый цвет. В присутствии серной кислоты и этанола борат ионы образуют летучие сложные эфиры: В 4 О 7 + 2 Н+ + 5 Н 2 О = 4 Н 3 ВО 3 + ЗС 2 Н 5 ОН = В(ОС 2 Н 5)3 + ЗН 2 О При поднесении пламени к чашке или тиглю, в которых протекает эта реакция, продукты сгорания окрашивают пламя в зеленый цвет. Реакция фармакопейная.
 Маскирование мешающих ионов
Маскирование мешающих ионов
 Органические реагенты используются для маскирования мешающих ионов. При этом они образуют устойчивые хелатные комплексы с мешающим ионом. Например, для маскирования Fe 3+, который мешает открытию многих ионов, используют из органических реагентов винную кислоту или лимонную кислоту.
Органические реагенты используются для маскирования мешающих ионов. При этом они образуют устойчивые хелатные комплексы с мешающим ионом. Например, для маскирования Fe 3+, который мешает открытию многих ионов, используют из органических реагентов винную кислоту или лимонную кислоту.
 ОТДЕЛЕНИЕ МЕШАЮЩИХ ИОНОВ Специфических органических реагентов, используемых для процессов отделения и разделения, очень немного. Как правило, эти реагенты участвуют в таких процессах отделения как: осаждение, хроматография, экстракция.
ОТДЕЛЕНИЕ МЕШАЮЩИХ ИОНОВ Специфических органических реагентов, используемых для процессов отделения и разделения, очень немного. Как правило, эти реагенты участвуют в таких процессах отделения как: осаждение, хроматография, экстракция.
 Экстракционное отделение мешающих ионов: Более эффективное отделение ( разделение ) достигается при использовании экстракции хелатов определяемых элементов, плохо растворимых в воде, но хорошо растворимых в органических растворителях. В качестве органических растворителей для экстракции хелатов используют (инертные) растворители: хлороформ CHCl 3 (трихлорметан), тетрахлоруглерод CCl 4 (тетрахлорметан); полярные растворители: метилизобутилкетон CH 3 -CO-CH(CH 3)-CH 2 -CH 3,
Экстракционное отделение мешающих ионов: Более эффективное отделение ( разделение ) достигается при использовании экстракции хелатов определяемых элементов, плохо растворимых в воде, но хорошо растворимых в органических растворителях. В качестве органических растворителей для экстракции хелатов используют (инертные) растворители: хлороформ CHCl 3 (трихлорметан), тетрахлоруглерод CCl 4 (тетрахлорметан); полярные растворители: метилизобутилкетон CH 3 -CO-CH(CH 3)-CH 2 -CH 3,
 Окраска хелатов: Окраска хелатов зависит от наличия групп - носителей цвета - хромофорных групп : = С =, =C=O, =C=S, =C=N-, -N=O, =C-C=C- К хромофорным группам относятся также группы атомов с тройной связью, однако она не имеет значения в химии хелатов. Группы - усилители цвета - ауксохромные группы ( -CH 3, -OH, -NH 2, -O- , -NHC 6 H 5).
Окраска хелатов: Окраска хелатов зависит от наличия групп - носителей цвета - хромофорных групп : = С =, =C=O, =C=S, =C=N-, -N=O, =C-C=C- К хромофорным группам относятся также группы атомов с тройной связью, однако она не имеет значения в химии хелатов. Группы - усилители цвета - ауксохромные группы ( -CH 3, -OH, -NH 2, -O- , -NHC 6 H 5).
 Во всех интенсивно окрашенных хелатах и в большинстве хелатообразующих реагентах имеется сопряженная - система, в которой - электроны делокализованы и не принадлежат более какой-либо одной связи.
Во всех интенсивно окрашенных хелатах и в большинстве хелатообразующих реагентах имеется сопряженная - система, в которой - электроны делокализованы и не принадлежат более какой-либо одной связи.
 Ко. Не. Ц…
Ко. Не. Ц…


