Общая химия.Лекция13.ppt
- Количество слайдов: 85
 Лекция 13 Комплексные соединения
Лекция 13 Комплексные соединения
 ПЛАН 13. 1 Основные понятия химии комплексных соединений(КС). 13. 2 Строение КС. 13. 3 Металло-лигандное равновесие в растворах. 13. 4 Биологическая роль КС.
ПЛАН 13. 1 Основные понятия химии комплексных соединений(КС). 13. 2 Строение КС. 13. 3 Металло-лигандное равновесие в растворах. 13. 4 Биологическая роль КС.
 13. 1 Комплексными (координационными) соединениями называют вещества, в структурных единицах которых число связей, образованных центральным атомом, превышает его высшую валентность.
13. 1 Комплексными (координационными) соединениями называют вещества, в структурных единицах которых число связей, образованных центральным атомом, превышает его высшую валентность.
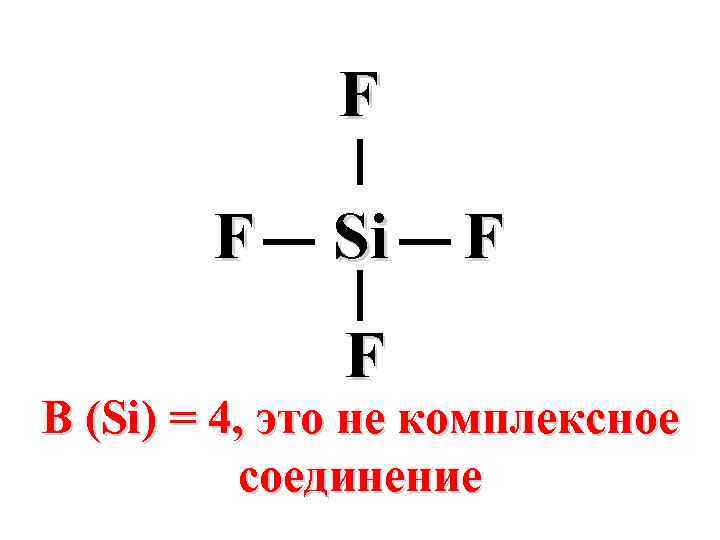 F F Si F F В (Si) = 4, это не комплексное соединение
F F Si F F В (Si) = 4, это не комплексное соединение
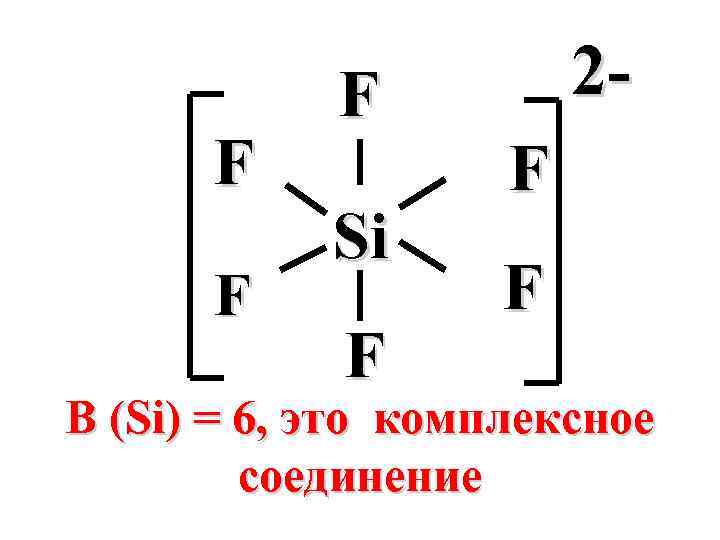 F F F Si F 2 F F В (Si) = 6, это комплексное соединение
F F F Si F 2 F F В (Si) = 6, это комплексное соединение
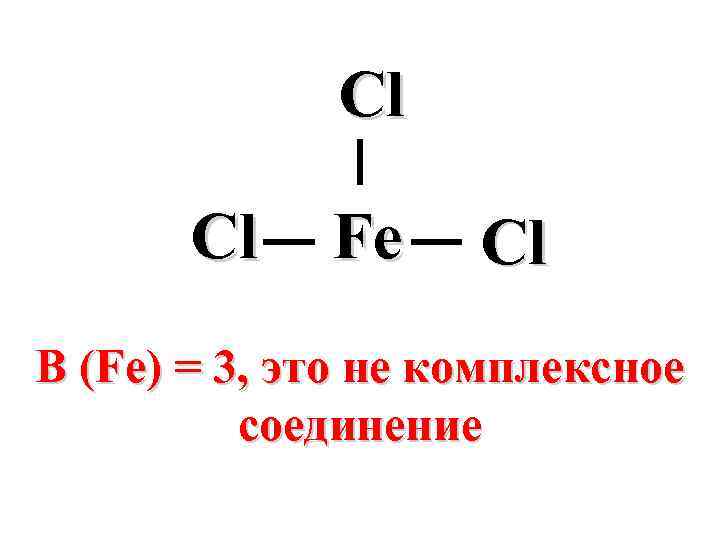 Cl Cl Fe Cl В (Fe) = 3, это не комплексное соединение
Cl Cl Fe Cl В (Fe) = 3, это не комплексное соединение
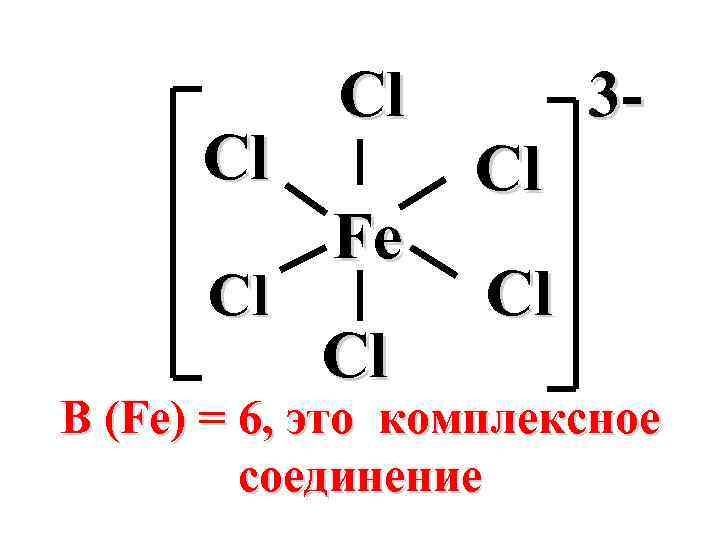 Cl Cl Cl Fe Cl Cl 3 - Cl В (Fe) = 6, это комплексное соединение
Cl Cl Cl Fe Cl Cl 3 - Cl В (Fe) = 6, это комплексное соединение
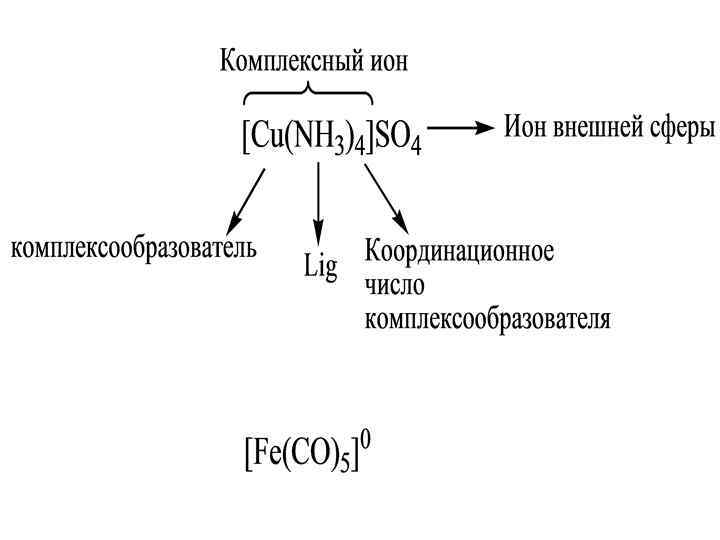
 Комплексные соединения состоят из: • комплексообразователей (Ме, реже неметаллы: Si, P и др. ); • лигандов (ионов или полярных молекул); • ионов внешней сферы (могут отсутствовать).
Комплексные соединения состоят из: • комплексообразователей (Ме, реже неметаллы: Si, P и др. ); • лигандов (ионов или полярных молекул); • ионов внешней сферы (могут отсутствовать).
 В природе комплексных соединений больше, чем простых. Их изучение началось ~ 200 лет назад. Первой теорией КС была теория А. Вернера (1893).
В природе комплексных соединений больше, чем простых. Их изучение началось ~ 200 лет назад. Первой теорией КС была теория А. Вернера (1893).
 Швейцарский химик, выдвинувший и развивший координационную теорию строения комплексных соединений. Лауреат Нобелевской премии 1913 г. Альфред Вернер 1866 -1919
Швейцарский химик, выдвинувший и развивший координационную теорию строения комплексных соединений. Лауреат Нобелевской премии 1913 г. Альфред Вернер 1866 -1919
 Важнейшей характеристикой комплексообразователя является его координационное число (к. ч. ), т. е. число связей, образованных им с лигандами.
Важнейшей характеристикой комплексообразователя является его координационное число (к. ч. ), т. е. число связей, образованных им с лигандами.
 Степень окисления Ме +1 +2 +3 +4 к. ч. 2 4, 6 6, 8
Степень окисления Ме +1 +2 +3 +4 к. ч. 2 4, 6 6, 8
 Важнейшей характеристикой лиганда является его дентантность – число связей, образованных с комплексообразователем.
Важнейшей характеристикой лиганда является его дентантность – число связей, образованных с комплексообразователем.
 Классификация лигандов • монодентантные лиганды: а) анионы: OH‾, F‾, Cl‾, Br‾, I‾, CNS‾, NO 2‾, NO 3‾; б) молекулы: NH 3, H 2 O, CO; +. в) катионы: NH 2 NH 3
Классификация лигандов • монодентантные лиганды: а) анионы: OH‾, F‾, Cl‾, Br‾, I‾, CNS‾, NO 2‾, NO 3‾; б) молекулы: NH 3, H 2 O, CO; +. в) катионы: NH 2 NH 3
 • бидентантные лиганды 2‾, а)анионы: SO 4 C 2 O 4 2‾; CO 3 б)молекулы: NH 2 – CH 2 – NH 2 (этилендиамин) NH 2 – COOH(глицин)
• бидентантные лиганды 2‾, а)анионы: SO 4 C 2 O 4 2‾; CO 3 б)молекулы: NH 2 – CH 2 – NH 2 (этилендиамин) NH 2 – COOH(глицин)
 • полидентантные лиганды. Важнейшими из них являются комплексоны – аминополикарбоновые кислоты и их соли.
• полидентантные лиганды. Важнейшими из них являются комплексоны – аминополикарбоновые кислоты и их соли.
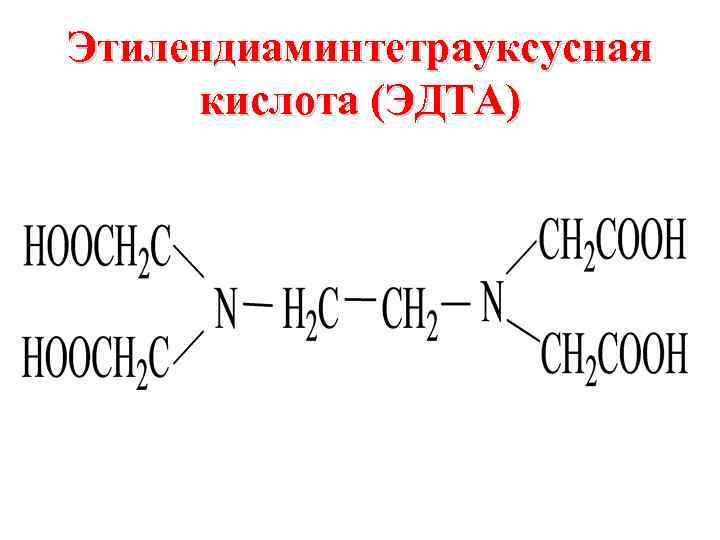 Этилендиаминтетрауксусная кислота (ЭДТА)
Этилендиаминтетрауксусная кислота (ЭДТА)
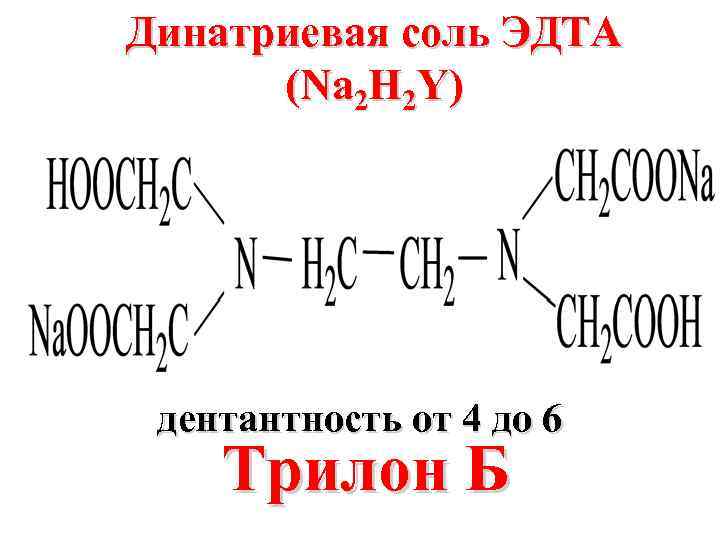 Динатриевая соль ЭДТА (Na 2 H 2 Y) дентантность от 4 до 6 Трилон Б
Динатриевая соль ЭДТА (Na 2 H 2 Y) дентантность от 4 до 6 Трилон Б
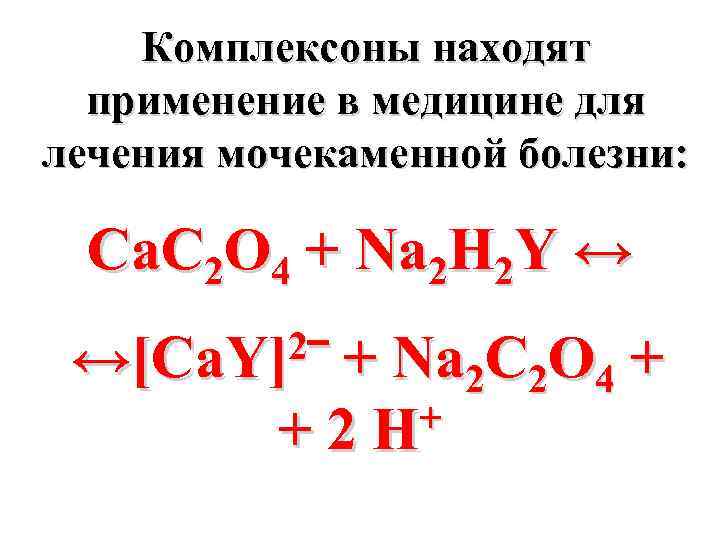 Комплексоны находят применение в медицине для лечения мочекаменной болезни: Ca. C 2 O 4 + Na 2 H 2 Y ↔ 2‾ ↔[Ca. Y] + Na 2 C 2 O 4 + + +2 H
Комплексоны находят применение в медицине для лечения мочекаменной болезни: Ca. C 2 O 4 + Na 2 H 2 Y ↔ 2‾ ↔[Ca. Y] + Na 2 C 2 O 4 + + +2 H
 Метод комплексонометрии является одним из методов объемного анализа, в основе которого лежит реакция комплексообразования: 2+ Me + Na 2 H 2 Y ↔ 2‾ + 2 Na+ + 2 H+ ↔Me. Y
Метод комплексонометрии является одним из методов объемного анализа, в основе которого лежит реакция комплексообразования: 2+ Me + Na 2 H 2 Y ↔ 2‾ + 2 Na+ + 2 H+ ↔Me. Y
 Метод комплексонометрии позволяет определять содержание катионов 2+, Mg 2+, Fe 2+, металлов Ca 3+ и др. в растворах и Fe биологических жидкостях.
Метод комплексонометрии позволяет определять содержание катионов 2+, Mg 2+, Fe 2+, металлов Ca 3+ и др. в растворах и Fe биологических жидкостях.
 Классификация комплексных соединений 1) по природе лигандов А)КС с монодентантными лигандами: • аммиакаты [Cu(NH 3)4]Cl 2 • аквакомплексы [Cu(H 2 O)4]SO 4 • гидроксокомплексы Na Al(OH)4 • ацидокомплексы Na Ag(CN)2 • со смешанными [Pt(NH 3)2 Cl 2 лигандами
Классификация комплексных соединений 1) по природе лигандов А)КС с монодентантными лигандами: • аммиакаты [Cu(NH 3)4]Cl 2 • аквакомплексы [Cu(H 2 O)4]SO 4 • гидроксокомплексы Na Al(OH)4 • ацидокомплексы Na Ag(CN)2 • со смешанными [Pt(NH 3)2 Cl 2 лигандами
 Б) КС с би- и полидентантными лигадами Особую группу составляют хелатные (клешневидные) комплексы, содержащие полидентантные лиганды, образующие замкнутые циклы
Б) КС с би- и полидентантными лигадами Особую группу составляют хелатные (клешневидные) комплексы, содержащие полидентантные лиганды, образующие замкнутые циклы
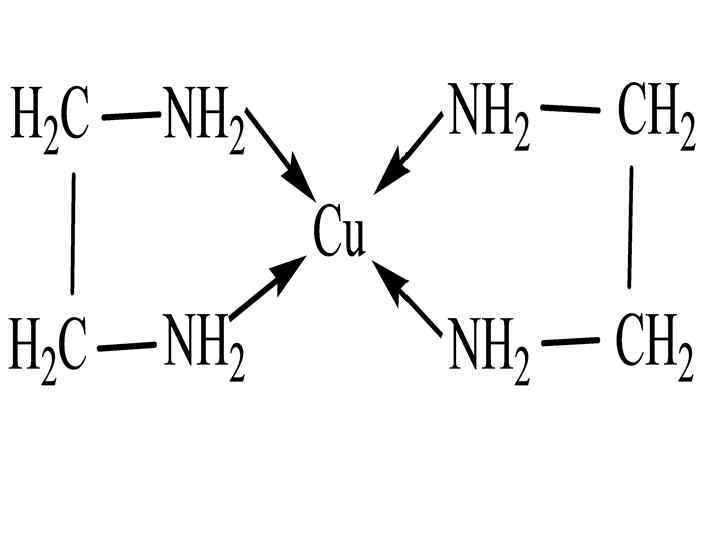
 Наиболее устойчивыми являются внутрикомплексные КС, в которых часть связей Me-Lig образованы по обменному, а часть – по донорно-акцепторному механизму
Наиболее устойчивыми являются внутрикомплексные КС, в которых часть связей Me-Lig образованы по обменному, а часть – по донорно-акцепторному механизму
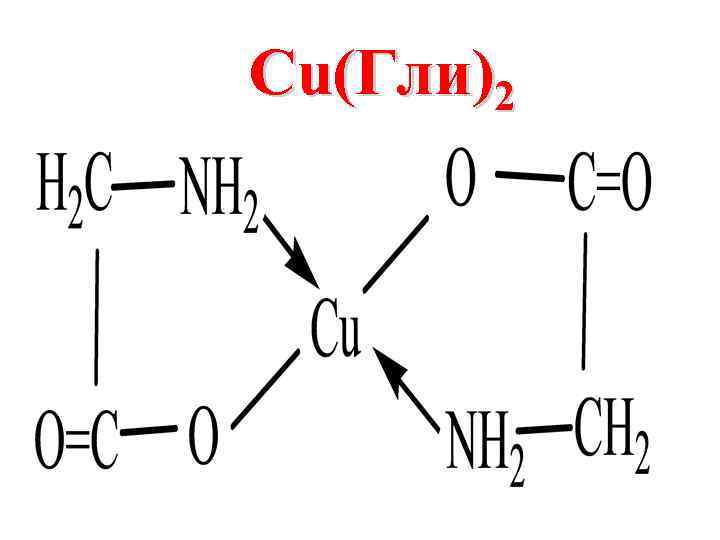 Сu(Гли)2
Сu(Гли)2
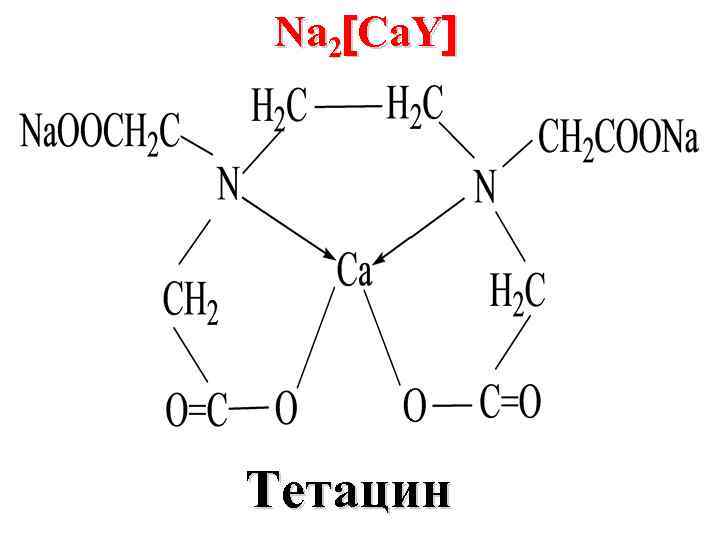 Na 2 Ca. Y Тетацин
Na 2 Ca. Y Тетацин
 Тетацин применяется в медицине как лекарственный препарат для детоксификации организма при отравлении тяжелыми металлами): Hg 2+ + [Ca. Y]2‾ ↔ Ca 2+ + [Hg. Y]2‾
Тетацин применяется в медицине как лекарственный препарат для детоксификации организма при отравлении тяжелыми металлами): Hg 2+ + [Ca. Y]2‾ ↔ Ca 2+ + [Hg. Y]2‾
 Классификация комплексных соединений 2) По скорости образования комплексов: лабильные инертные
Классификация комплексных соединений 2) По скорости образования комплексов: лабильные инертные
 НОМЕНКЛАТУРА КС (1960, ИЮПАК) 1) вначале называют катионы, затем анионы. Названия комплексных анионов заканчиваются суффиксом –ат;
НОМЕНКЛАТУРА КС (1960, ИЮПАК) 1) вначале называют катионы, затем анионы. Названия комплексных анионов заканчиваются суффиксом –ат;
 2) В комплексном ионе сначала называют лигандыанионы, затем лигандымолекулы, затем лигандыкатионы: NH 3 – аммин H 2 O – аква СО – карбонил
2) В комплексном ионе сначала называют лигандыанионы, затем лигандымолекулы, затем лигандыкатионы: NH 3 – аммин H 2 O – аква СО – карбонил
 Названия лигандов-анионов заканчиваются на – о: OH‾ –гидроксо CN‾ – циано NO 2‾ – нитро СNS‾ – родано NO 3‾ –нитрато SO 42‾ –сульфато Катион-лиганд гидразиниум + NH 2 NH 3
Названия лигандов-анионов заканчиваются на – о: OH‾ –гидроксо CN‾ – циано NO 2‾ – нитро СNS‾ – родано NO 3‾ –нитрато SO 42‾ –сульфато Катион-лиганд гидразиниум + NH 2 NH 3
 Названия некоторых комплексообразователей зависит от их положения в КС
Названия некоторых комплексообразователей зависит от их положения в КС
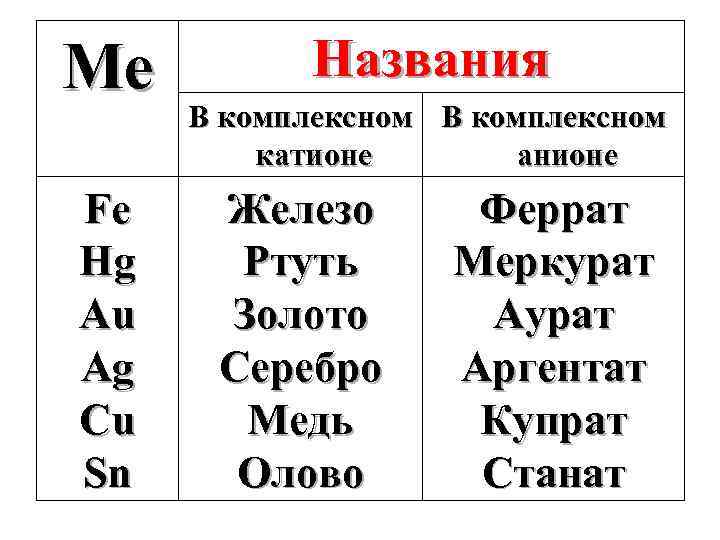 Ме Fe Hg Au Ag Cu Sn Названия В комплексном катионе анионе Железо Ртуть Золото Серебро Медь Олово Феррат Меркурат Аргентат Купрат Станат
Ме Fe Hg Au Ag Cu Sn Названия В комплексном катионе анионе Железо Ртуть Золото Серебро Медь Олово Феррат Меркурат Аргентат Купрат Станат
 Степень окисления комплексообразователя указывают, если у металла их несколько.
Степень окисления комплексообразователя указывают, если у металла их несколько.
![Na[Al(OH)4] натрий тетрагидроксоалюминат [Cu(NH 3)4]SO 4 тетраамминмедь(II) сульфат NH 4[Co(NH 3)2(NO 2)4] аммоний тетранитродиамминкобальтат(III) Na[Al(OH)4] натрий тетрагидроксоалюминат [Cu(NH 3)4]SO 4 тетраамминмедь(II) сульфат NH 4[Co(NH 3)2(NO 2)4] аммоний тетранитродиамминкобальтат(III)](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-37.jpg) Na[Al(OH)4] натрий тетрагидроксоалюминат [Cu(NH 3)4]SO 4 тетраамминмедь(II) сульфат NH 4[Co(NH 3)2(NO 2)4] аммоний тетранитродиамминкобальтат(III) [Pt(NH 3)2 Cl 2 дихлородиамминплатина
Na[Al(OH)4] натрий тетрагидроксоалюминат [Cu(NH 3)4]SO 4 тетраамминмедь(II) сульфат NH 4[Co(NH 3)2(NO 2)4] аммоний тетранитродиамминкобальтат(III) [Pt(NH 3)2 Cl 2 дихлородиамминплатина
 13. 2 Строение КС описывается либо в рамках метода ВС, либо с позиций теории кристаллического поля.
13. 2 Строение КС описывается либо в рамках метода ВС, либо с позиций теории кристаллического поля.
 С позиций метода ВС связи металл-лиганд являются ковалентными полярными, образованными по донорно-акцепторному механизму.
С позиций метода ВС связи металл-лиганд являются ковалентными полярными, образованными по донорно-акцепторному механизму.
 Лиганды выступают в роли доноров электронных пар, а комплексообразователи – в роли их акцепторов.
Лиганды выступают в роли доноров электронных пар, а комплексообразователи – в роли их акцепторов.
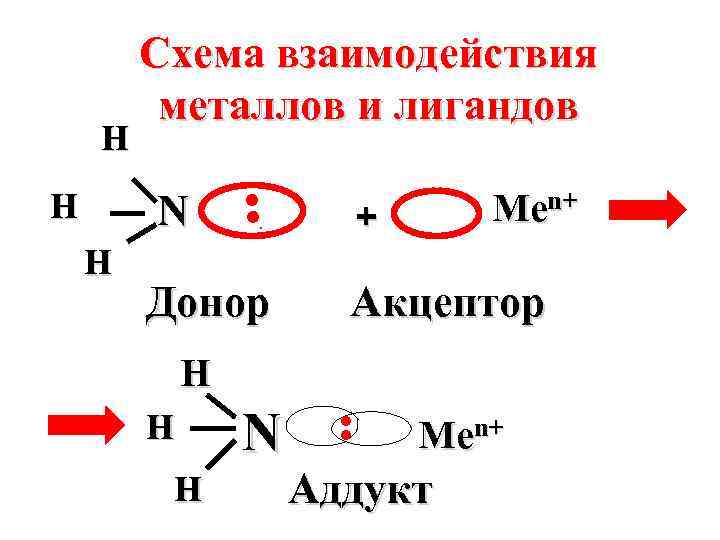 N H Донор Men+ + Акцептор H H H N ●● H Схема взаимодействия металлов и лигандов Men+ Аддукт
N H Донор Men+ + Акцептор H H H N ●● H Схема взаимодействия металлов и лигандов Men+ Аддукт
 Конфигурация комплексного иона определяется типом гибридизации АО комплексообразователя.
Конфигурация комплексного иона определяется типом гибридизации АО комплексообразователя.
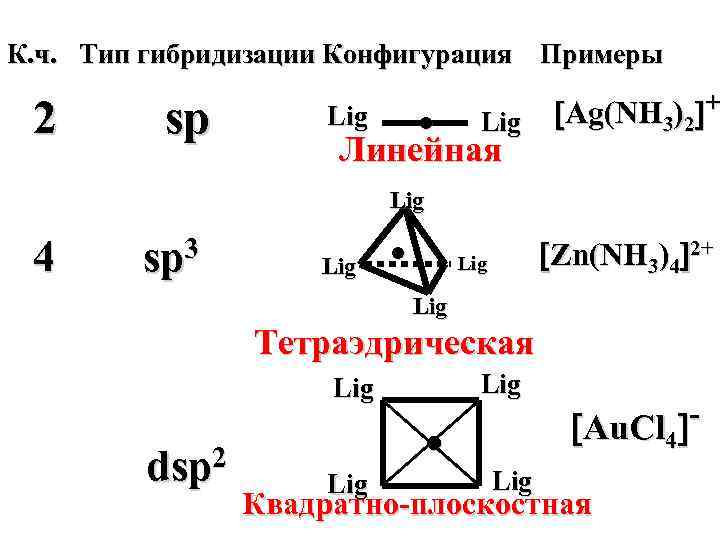 К. ч. Тип гибридизации Конфигурация Примеры 2 sp Lig ● Lig Линейная Ag(NH 3)2 + Lig 4 sp 3 Lig ● Zn(NH 3)4 2+ Lig Тетраэдрическая Lig dsp 2 ● Lig Au. Cl 4 - Квадратно-плоскостная
К. ч. Тип гибридизации Конфигурация Примеры 2 sp Lig ● Lig Линейная Ag(NH 3)2 + Lig 4 sp 3 Lig ● Zn(NH 3)4 2+ Lig Тетраэдрическая Lig dsp 2 ● Lig Au. Cl 4 - Квадратно-плоскостная
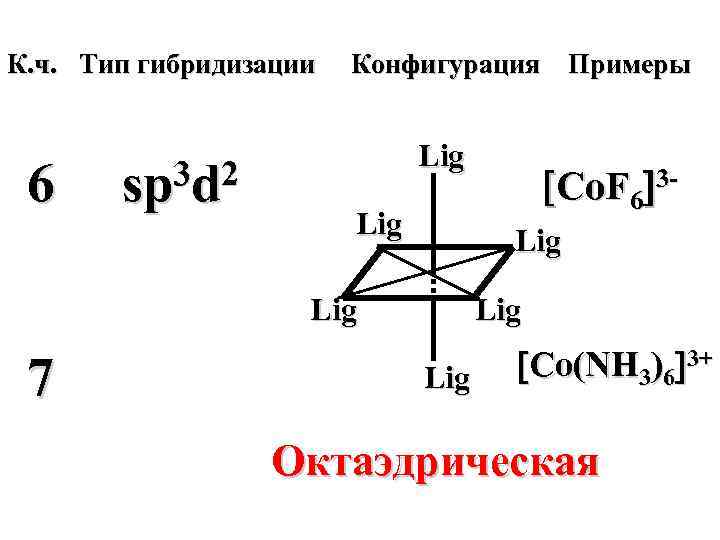 К. ч. Тип гибридизации 6 3 d 2 sp Конфигурация Примеры Lig Lig Lig 7 Co. F 6 3 - Lig Co(NH 3)6 3+ Октаэдрическая
К. ч. Тип гибридизации 6 3 d 2 sp Конфигурация Примеры Lig Lig Lig 7 Co. F 6 3 - Lig Co(NH 3)6 3+ Октаэдрическая
 Теория кристаллического поля исходит из того, что металлы и лиганды связаны между собой силами электростатического притяжения.
Теория кристаллического поля исходит из того, что металлы и лиганды связаны между собой силами электростатического притяжения.
 Эта теория рассматривает воздействие лигандов на d-орбитали ионакомплексообразователя.
Эта теория рассматривает воздействие лигандов на d-орбитали ионакомплексообразователя.
 Если катион металла находится в симметричном магнитном поле, его d -орбитали имеют одинаковый запас энергии (являются вырожденными).
Если катион металла находится в симметричном магнитном поле, его d -орбитали имеют одинаковый запас энергии (являются вырожденными).
 Если ион находится в октаэдрическом, тетраэдрическом или другом несимметричном поле лигандов, то происходит расщепление его d-подуровня.
Если ион находится в октаэдрическом, тетраэдрическом или другом несимметричном поле лигандов, то происходит расщепление его d-подуровня.
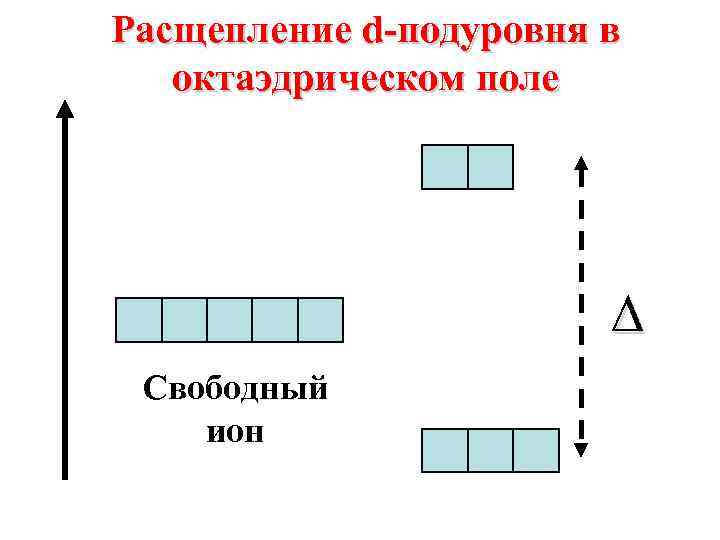 Расщепление d-подуровня в октаэдрическом поле ∆ Свободный ион
Расщепление d-подуровня в октаэдрическом поле ∆ Свободный ион
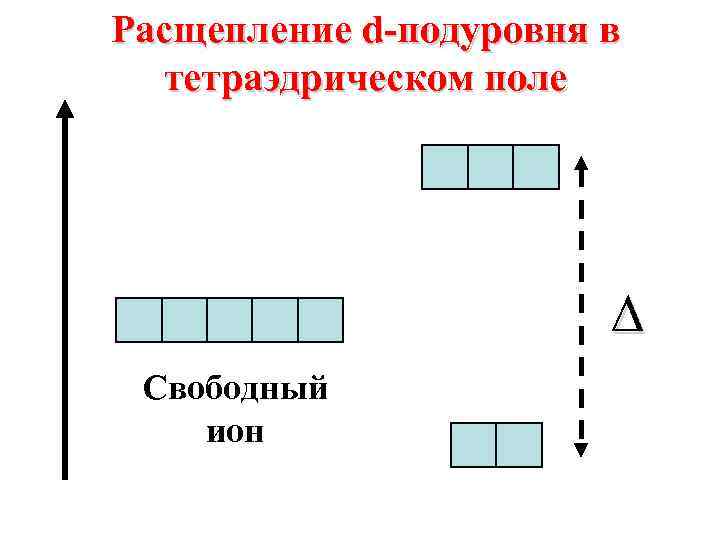 Расщепление d-подуровня в тетраэдрическом поле ∆ Свободный ион
Расщепление d-подуровня в тетраэдрическом поле ∆ Свободный ион
 Величина энергии расщепления (∆) зависит от конфигурации комплекса и природы лиганда.
Величина энергии расщепления (∆) зависит от конфигурации комплекса и природы лиганда.
 Спектрохимический ряд лигандов I‾, Cl‾, F‾, OH‾, H 2 O, CNS‾, NH 3, NO 2‾, CN‾ Слабые Lig Сильные Lig Увеличение энергии расщепления ∆
Спектрохимический ряд лигандов I‾, Cl‾, F‾, OH‾, H 2 O, CNS‾, NH 3, NO 2‾, CN‾ Слабые Lig Сильные Lig Увеличение энергии расщепления ∆
 В поле слабых лигандов энергия расщепления (∆) не велика, поэтому распределение электронов на d-орбиталях соответствует правилу Гунда
В поле слабых лигандов энергия расщепления (∆) не велика, поэтому распределение электронов на d-орбиталях соответствует правилу Гунда
 В поле сильных лигандов энергия расщепления (∆) имеет большое значение, в следствие чего первыми заполняются d-орбитали нижнего подуровня (распределение электронов происходит против правила Гунда).
В поле сильных лигандов энергия расщепления (∆) имеет большое значение, в следствие чего первыми заполняются d-орбитали нижнего подуровня (распределение электронов происходит против правила Гунда).
![Рассмотрим строение КС: х -1 3‾ [Fe. F 6] х -1 3‾ [Fe(CN)6] х– Рассмотрим строение КС: х -1 3‾ [Fe. F 6] х -1 3‾ [Fe(CN)6] х–](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-55.jpg) Рассмотрим строение КС: х -1 3‾ [Fe. F 6] х -1 3‾ [Fe(CN)6] х– 6=– 3 х=+3
Рассмотрим строение КС: х -1 3‾ [Fe. F 6] х -1 3‾ [Fe(CN)6] х– 6=– 3 х=+3
 Координационное 3+ число катиона Fe равно 6, так как он связан с шестью монодентантными лигандами
Координационное 3+ число катиона Fe равно 6, так как он связан с шестью монодентантными лигандами
 Электронная конфигурация атома и иона Fe 23 d 6 4 s 3+ Fe 03 d 5 4 s
Электронная конфигурация атома и иона Fe 23 d 6 4 s 3+ Fe 03 d 5 4 s
 Оба комплексных иона имеют октаэдрическую конфигурацию, что обуславливает одинаковый характер расщепления dорбиталей
Оба комплексных иона имеют октаэдрическую конфигурацию, что обуславливает одинаковый характер расщепления dорбиталей
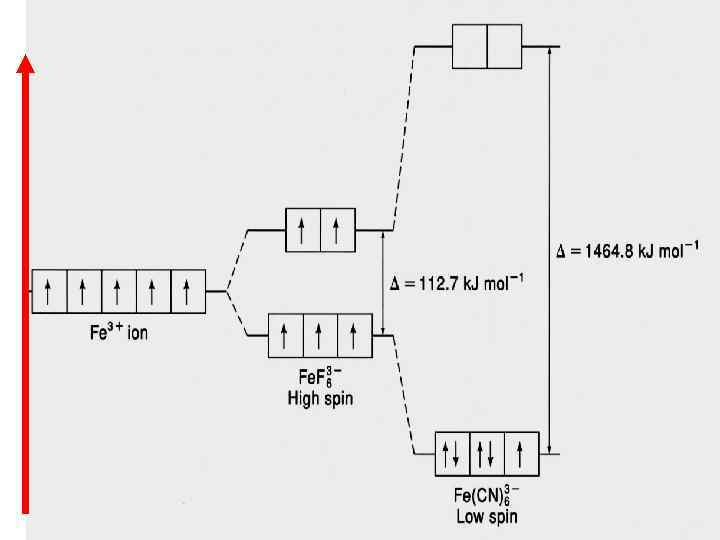
 - является «слабым F лигандом» (∆ = 112, 7 к. Дж/моль), поэтому распределение 3+ электронов катиона Fe происходит в соответствии с правилом Гунда
- является «слабым F лигандом» (∆ = 112, 7 к. Дж/моль), поэтому распределение 3+ электронов катиона Fe происходит в соответствии с правилом Гунда
 - является «сильным CN лигандом» (∆ = 1464, 8 к. Дж/моль), поэтому распределение 3+ электронов катиона Fe происходит против правила Гунда
- является «сильным CN лигандом» (∆ = 1464, 8 к. Дж/моль), поэтому распределение 3+ электронов катиона Fe происходит против правила Гунда
![3 Fe. F 6] Ион парамагнитен, так как содержит неспаренные электроны на внешнем уровне 3 Fe. F 6] Ион парамагнитен, так как содержит неспаренные электроны на внешнем уровне](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-62.jpg) 3 Fe. F 6] Ион парамагнитен, так как содержит неспаренные электроны на внешнем уровне (высокоспиновый комплекс).
3 Fe. F 6] Ион парамагнитен, так как содержит неспаренные электроны на внешнем уровне (высокоспиновый комплекс).
![3 Fe(СN)6] Ион диамагнитен, (низкоспиновый комплекс). 3 Fe(СN)6] Ион диамагнитен, (низкоспиновый комплекс).](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-63.jpg) 3 Fe(СN)6] Ион диамагнитен, (низкоспиновый комплекс).
3 Fe(СN)6] Ион диамагнитен, (низкоспиновый комплекс).
![13. 3 Комплексные соединения Электролиты Неэлектролиты [Pt(NH 3)2 Cl 2] Кислоты H 2[Pt. Cl 13. 3 Комплексные соединения Электролиты Неэлектролиты [Pt(NH 3)2 Cl 2] Кислоты H 2[Pt. Cl](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-64.jpg) 13. 3 Комплексные соединения Электролиты Неэлектролиты [Pt(NH 3)2 Cl 2] Кислоты H 2[Pt. Cl 4] Основания [Ag(NH 3)2]OH Соли K 4[Fe(CN)6]
13. 3 Комплексные соединения Электролиты Неэлектролиты [Pt(NH 3)2 Cl 2] Кислоты H 2[Pt. Cl 4] Основания [Ag(NH 3)2]OH Соли K 4[Fe(CN)6]
![Различают первичную (необратимую) диссоциацию: K 4[Fe(CN)6] → 4 K+ + [Fe(CN)6]4‾ и вторичную (обратимую) Различают первичную (необратимую) диссоциацию: K 4[Fe(CN)6] → 4 K+ + [Fe(CN)6]4‾ и вторичную (обратимую)](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-65.jpg) Различают первичную (необратимую) диссоциацию: K 4[Fe(CN)6] → 4 K+ + [Fe(CN)6]4‾ и вторичную (обратимую) диссоциацию КС: 4‾ [Fe(CN)6] ⇄ 2+ Fe + 6 CN‾
Различают первичную (необратимую) диссоциацию: K 4[Fe(CN)6] → 4 K+ + [Fe(CN)6]4‾ и вторичную (обратимую) диссоциацию КС: 4‾ [Fe(CN)6] ⇄ 2+ Fe + 6 CN‾
 Константа равновесия, описывающая вторичную диссоциацию КС, называется константой нестойкости (Кн): Кн
Константа равновесия, описывающая вторичную диссоциацию КС, называется константой нестойкости (Кн): Кн
![Чем меньше Кн, тем устойчивее комплексное соединение [Ag(NO 2)2]‾ [Ag(NH 3)2]+ [Ag(CN)2]‾ 1, 3∙ Чем меньше Кн, тем устойчивее комплексное соединение [Ag(NO 2)2]‾ [Ag(NH 3)2]+ [Ag(CN)2]‾ 1, 3∙](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-67.jpg) Чем меньше Кн, тем устойчивее комплексное соединение [Ag(NO 2)2]‾ [Ag(NH 3)2]+ [Ag(CN)2]‾ 1, 3∙ 10‾ 3 6, 8· 10‾ 8 1, 0∙ 10‾ 21 увеличение устойчивости КС
Чем меньше Кн, тем устойчивее комплексное соединение [Ag(NO 2)2]‾ [Ag(NH 3)2]+ [Ag(CN)2]‾ 1, 3∙ 10‾ 3 6, 8· 10‾ 8 1, 0∙ 10‾ 21 увеличение устойчивости КС
 Устойчивость комплексов можно охарактеризовать при помощи константы устойчивости (Ку): Ку = 1 Кн
Устойчивость комплексов можно охарактеризовать при помощи константы устойчивости (Ку): Ку = 1 Кн
 Причины устойчивости КС лежат в их строении: а) чем меньше ионный радиус комплексообразователя и больше его заряд, тем сильнее притяжение лигандов и устойчивее КС.
Причины устойчивости КС лежат в их строении: а) чем меньше ионный радиус комплексообразователя и больше его заряд, тем сильнее притяжение лигандов и устойчивее КС.
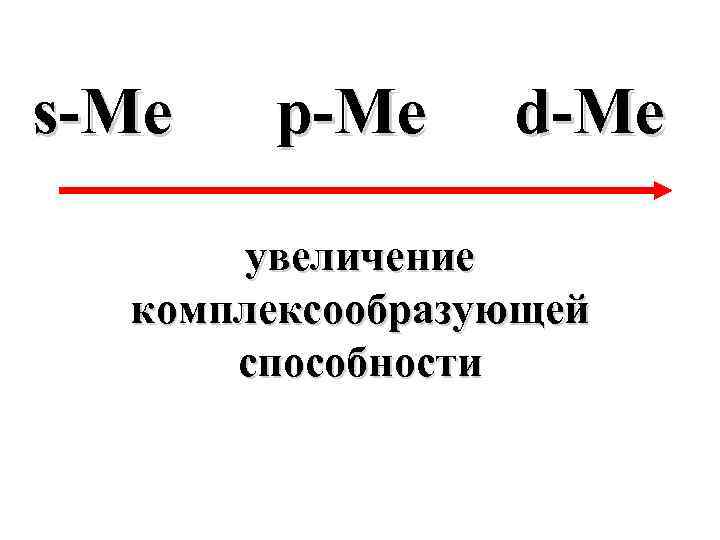 s-Me p-Me d-Me увеличение комплексообразующей способности
s-Me p-Me d-Me увеличение комплексообразующей способности
![б) чем выше дентантность лиганда, тем устойчивее КС: КC Кн 2+ 5 [Co(NH 3)4] б) чем выше дентантность лиганда, тем устойчивее КС: КC Кн 2+ 5 [Co(NH 3)4]](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-71.jpg) б) чем выше дентантность лиганда, тем устойчивее КС: КC Кн 2+ 5 [Co(NH 3)4] 1, 0· 10‾ 9 [Co(Гли)2] 3, 3∙ 10‾ 2‾ 16 [Co. Y] 1, 0∙ 10‾
б) чем выше дентантность лиганда, тем устойчивее КС: КC Кн 2+ 5 [Co(NH 3)4] 1, 0· 10‾ 9 [Co(Гли)2] 3, 3∙ 10‾ 2‾ 16 [Co. Y] 1, 0∙ 10‾
 Самыми устойчивыми комплексными соединениями являются хелатные КС. Это явление получило название эффекта хелатирования.
Самыми устойчивыми комплексными соединениями являются хелатные КС. Это явление получило название эффекта хелатирования.
 13. 4 В организме человека все металлы, кроме щелочных и, частично, щелочноземельных находятся в виде прочных хелатных КС с биолигандами: белками, аминокислотами, витаминами, гормонами и другими биоактивными соединениями.
13. 4 В организме человека все металлы, кроме щелочных и, частично, щелочноземельных находятся в виде прочных хелатных КС с биолигандами: белками, аминокислотами, витаминами, гормонами и другими биоактивными соединениями.
 Важнейшими являются комплексы с белками. К ним относятся многочисленные металлоферменты, а так же гемоглобин (комплекс железа с порфином), хлорофилл (комплекс магния).
Важнейшими являются комплексы с белками. К ним относятся многочисленные металлоферменты, а так же гемоглобин (комплекс железа с порфином), хлорофилл (комплекс магния).
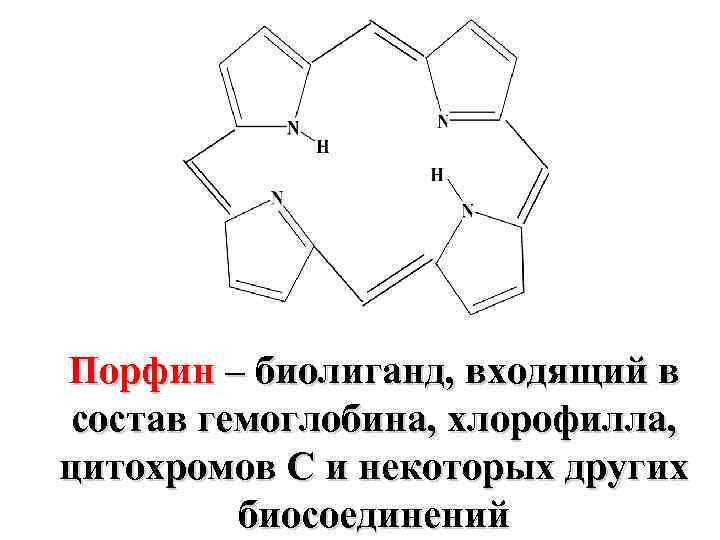 Порфин – биолиганд, входящий в состав гемоглобина, хлорофилла, цитохромов С и некоторых других биосоединений
Порфин – биолиганд, входящий в состав гемоглобина, хлорофилла, цитохромов С и некоторых других биосоединений
 Сбалансированные потоки металлов и лигандов в биосистемах обуславливают металло-лигандный гомеостаз.
Сбалансированные потоки металлов и лигандов в биосистемах обуславливают металло-лигандный гомеостаз.
 Его нарушение приводит к различным заболеваниям: При недостатке железа – анемия, при его избытке – сидероз.
Его нарушение приводит к различным заболеваниям: При недостатке железа – анемия, при его избытке – сидероз.
 По данным ВОЗ дефицит железа в организме человека является одной из наиболее серьезных проблем современности. На земном шаре от дефицита железа страдает 4 -5 миллиардов человек (66 -80% населения Земли). Недостаток железа - один из десяти глобальных факторов риска, являющийся причиной смерти 800 000 человек в год.
По данным ВОЗ дефицит железа в организме человека является одной из наиболее серьезных проблем современности. На земном шаре от дефицита железа страдает 4 -5 миллиардов человек (66 -80% населения Земли). Недостаток железа - один из десяти глобальных факторов риска, являющийся причиной смерти 800 000 человек в год.
 Недостаток кальция приводит к остеопорозу, а его избыток в организме человека способствует развитию катаракты, атеросклероза, а также обызвествлению костной ткани.
Недостаток кальция приводит к остеопорозу, а его избыток в организме человека способствует развитию катаракты, атеросклероза, а также обызвествлению костной ткани.
 Для коррекции металлолигандного гомеостаза используются: • комплексоны, связывающие токсичные металлы, и выводящие их из организма человека;
Для коррекции металлолигандного гомеостаза используются: • комплексоны, связывающие токсичные металлы, и выводящие их из организма человека;
 • комплексные соединения: А)комплексы Pt – противоопухолевые препараты, например, соль Пейроне [Pt(NH 3)2 Cl 2] (синтезирована в 1850, используется как препарат с 1969 года);
• комплексные соединения: А)комплексы Pt – противоопухолевые препараты, например, соль Пейроне [Pt(NH 3)2 Cl 2] (синтезирована в 1850, используется как препарат с 1969 года);
![Б) комплексы Au – лечение артритов и туберкулеза: Na 3[Au(S 2 O 3)2]; B)тетацин–при Б) комплексы Au – лечение артритов и туберкулеза: Na 3[Au(S 2 O 3)2]; B)тетацин–при](https://present5.com/presentation/3/-57947089_217556891.pdf-img/-57947089_217556891.pdf-82.jpg) Б) комплексы Au – лечение артритов и туберкулеза: Na 3[Au(S 2 O 3)2]; B)тетацин–при отравлениях тяжелыми Ме.
Б) комплексы Au – лечение артритов и туберкулеза: Na 3[Au(S 2 O 3)2]; B)тетацин–при отравлениях тяжелыми Ме.
 Строение, свойства и биологическая роль КС металлов с биолигандами является объектом изучения бионеорганической химии, возникшей в середине 50 -х годов, на стыке неорганической химии, биологии и медицины.
Строение, свойства и биологическая роль КС металлов с биолигандами является объектом изучения бионеорганической химии, возникшей в середине 50 -х годов, на стыке неорганической химии, биологии и медицины.
 Достижения бионеорганики широко внедряются в медицину.
Достижения бионеорганики широко внедряются в медицину.
 Благодарим за внимание!!!
Благодарим за внимание!!!


