Слайд_к_л_12.ppt
- Количество слайдов: 31

Лекция № 12 Химия элементов VI B подгруппы Cr, Mo, W
H Li He Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti Cu Zn Ga Ge Rb Sr Y Ag Cd In Cs Ba La Au Hg Tl Fr Ra V Cr As Se Mn Br Zr Nb Mo Sn Sb Hf Ta Pb Bi Te W Po Tc I Re At Fe Co Ni Kr Ru Rh Pd Xe Os Rn Ir Pt
![Общая характеристика элементов VIB подгруппы Эл. cтроение Cr [Ar] 3 d 54 s 1 Общая характеристика элементов VIB подгруппы Эл. cтроение Cr [Ar] 3 d 54 s 1](https://present5.com/presentation/3/26150394_165586596.pdf-img/26150394_165586596.pdf-3.jpg)
Общая характеристика элементов VIB подгруппы Эл. cтроение Cr [Ar] 3 d 54 s 1 Mo [Kr] 4 d 55 s 1 W [Xe] 4 f 145 d 46 s 2 rат, нм 0, 126 0, 137 СО II, III, VI (IV, V), VI r Mo ≈ r W как следствие лантаноидного сжатия Склонность к проявлению высшей СО растёт Убывание кислотных свойств (H 2 Cr. O 4 и H 2 Mo. O 4) Активные комплексообразователи (изополи- и гетерополисоединения)
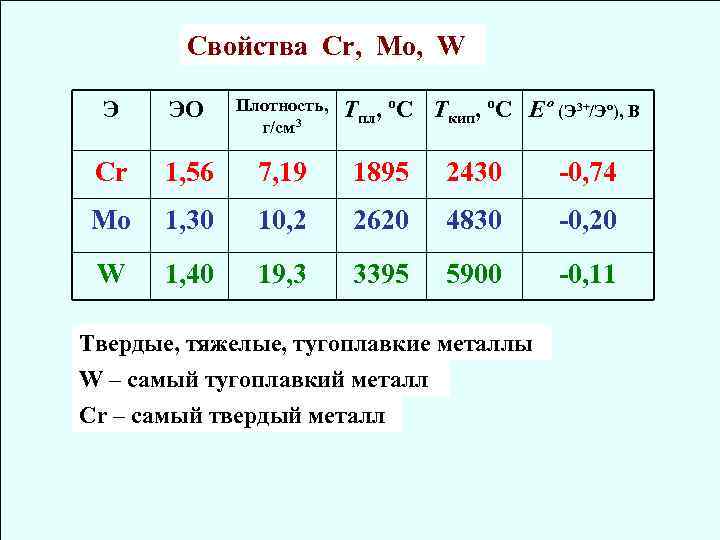
Cвойства Cr, Mo, W Э ЭО Плотность, г/см 3 Cr 1, 56 7, 19 1895 2430 -0, 74 Mo 1, 30 10, 2 2620 4830 -0, 20 W 1, 40 19, 3 3395 5900 -0, 11 Tпл, ºC Tкип, ºC Еº (Э 3+/Эº), B Твердые, тяжелые, тугоплавкие металлы W – самый тугоплавкий металл Сr – самый твердый металл
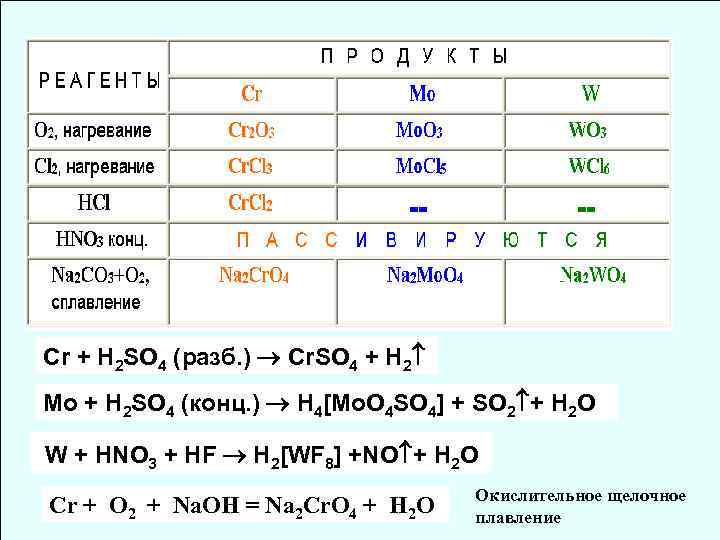
Cr + H 2 SO 4 (разб. ) Сr. SO 4 + H 2 Mo + H 2 SO 4 (конц. ) H 4[Mo. O 4 SO 4] + SO 2 + H 2 O W + HNO 3 + HF H 2[WF 8] +NO + H 2 O Cr + O 2 + Na. OH = Na 2 Cr. O 4 + H 2 O Окислительное щелочное плавление
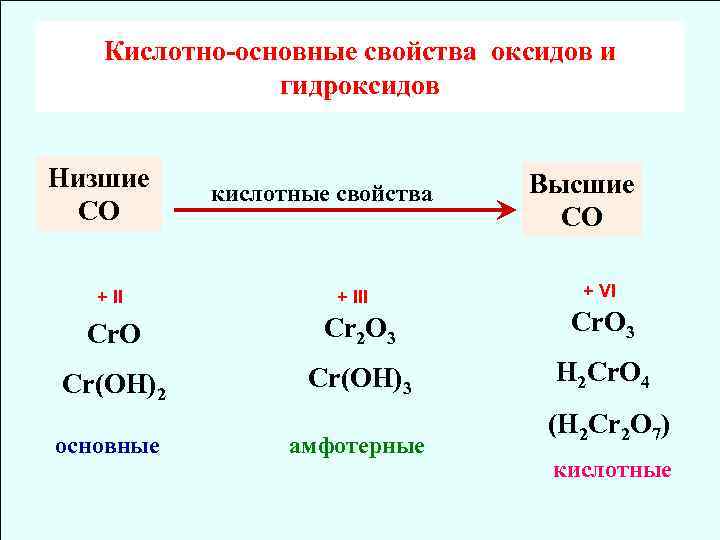
Кислотно-основные свойcтва оксидов и гидроксидов Низшие СО + II кислотные свойства + III Высшие СО + VI Cr. O Cr 2 O 3 Cr(OH)2 Cr(OH)3 H 2 Cr. O 4 основные амфотерные (H 2 Cr 2 O 7) кислотные
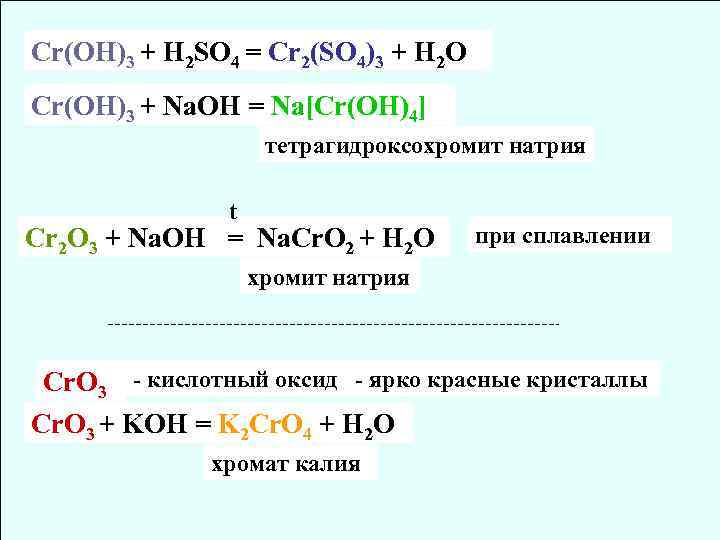
Cr(OH)3 + H 2 SO 4 = Cr 2(SO 4)3 + H 2 O Cr(OH)3 + Na. OH = Na[Cr(OH)4] тетрагидроксохромит натрия t Cr 2 O 3 + Na. OH = Na. Cr. O 2 + H 2 O при сплавлении хромит натрия Сr. O 3 - кислотный оксид - ярко красные кристаллы Cr. O 3 + KOH = K 2 Cr. O 4 + H 2 O хромат калия

+VI Соединения Cr, Mo, W K 2 Cr 2 O 7 + H 2 SO 4 (конц. ) Cr. O 3 + K 2 SO 4 + H 2 O cильный окислитель Cr. O 3 Cr 2 O 3 + O 2 (T > 400 °C) Cr. O 3 + Н 2 О H 2 Cr. O 4 Pb. Cr. O 4, Ba. Cr. O 4, Ag 2 Cr. O 4 Хорошо р-римы хроматы щелочных металлов и аммония
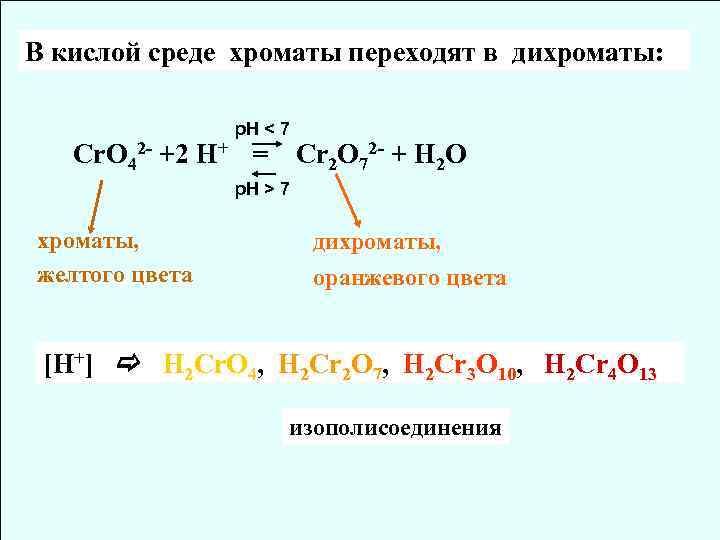
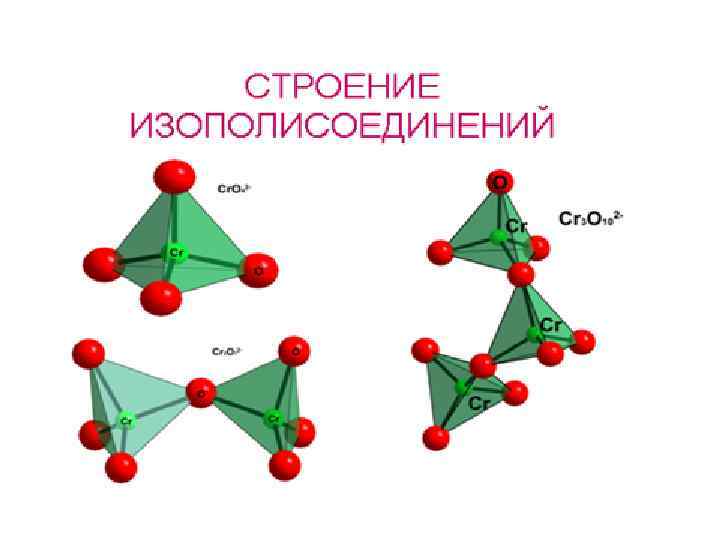
В кислой среде хроматы переходят в дихроматы: p. H < 7 Сr. O 42 - +2 H+ = Cr 2 O 72 - + H 2 O p. H > 7 хроматы, желтого цвета дихроматы, оранжевого цвета [H+] H 2 Cr. O 4, H 2 Cr 2 O 7, H 2 Cr 3 O 10, H 2 Cr 4 O 13 изополисоединения

Дихроматы - сильные окислители: K 2 Cr 2 O 7 + KI + H 2 SO 4 = I 2 + Cr 2(SO 4)3 + K 2 SO 4 +H 2 O K 2 Cr 2 O 7 + HCl (конц. ) Сr. Cl 3 + Cl 2 + KCl + H 2 O Самостоятельно закончите данное уравнение, подобрав коэффициенты с применением метода полуреакций
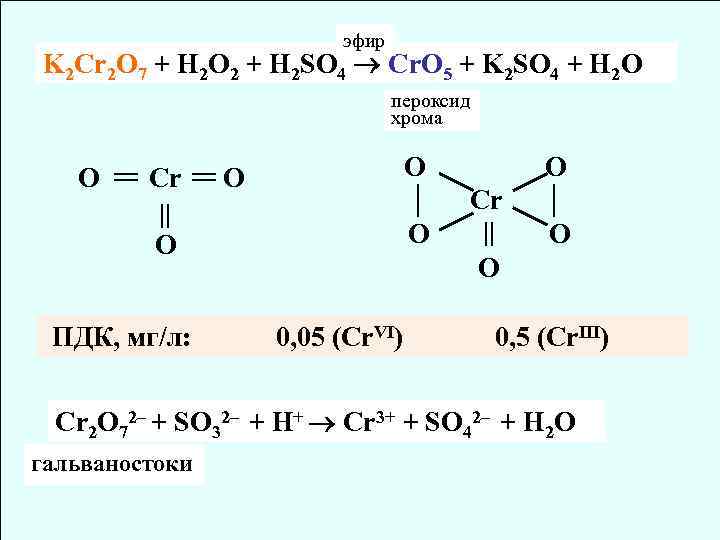
эфир K 2 Cr 2 O 7 + H 2 O 2 + H 2 SO 4 Cr. O 5 + K 2 SO 4 + H 2 O пероксид хрома O Cr O │ O O O ПДК, мг/л: Cr O │ O O 0, 05 (Cr. VI) 0, 5 (Cr. III) Cr 2 O 72– + SO 32– + H+ Cr 3+ + SO 42– + H 2 O гальваностоки
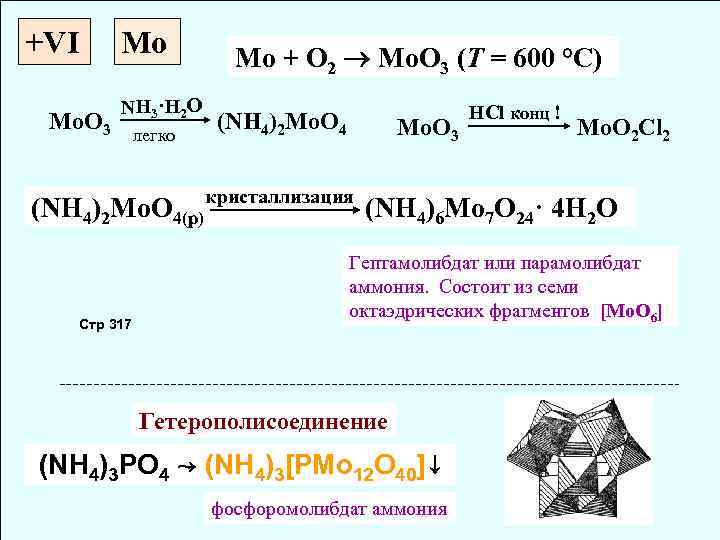
+VI Mo Mo. O 3 NH 3·H 2 O легко (NH 4)2 Mo. O 4(p) Стр 317 Mo + O 2 Mo. O 3 (T = 600 °C) (NH 4)2 Mo. O 4 Mo. O 3 кристаллизация HCl конц ! Mo. O 2 Cl 2 (NH 4)6 Mo 7 O 24· 4 H 2 O Гептамолибдат или парамолибдат аммония. Cостоит из семи октаэдрических фрагментов [Mo. O 6] Гетерополисоединение (NH 4)3 PO 4 ↝ (NH 4)3[PMo 12 O 40]↓ фосфоромолибдат аммония
![Вольфрам. Изополисоединения. Гетерополисоединения. [H 2 W 12 O 42]10 - - паравольфрамат Б-ион [W Вольфрам. Изополисоединения. Гетерополисоединения. [H 2 W 12 O 42]10 - - паравольфрамат Б-ион [W](https://present5.com/presentation/3/26150394_165586596.pdf-img/26150394_165586596.pdf-14.jpg)
Вольфрам. Изополисоединения. Гетерополисоединения. [H 2 W 12 O 42]10 - - паравольфрамат Б-ион [W 7 O 24]6 - - паравольфрамат А-ион [H 2 W 12 O 42]6 - - метавольфрамат-ион Молибденовые и вольфрамовые сини Zn VI V Na 2 Mo. O 4 — 3 Mo. O 3 • Mo 2 O 5 • H 2 O H+ (W 5 O 14) Mo 4 O 11, Mo 8 O 23, Mo 9 O 26, W 18 O 49, W 20 O 58, W 24 O 70 и т. д.

+III (NH 4)2 Cr 2 O 7 Cr 2 O 3 + N 2 + H 2 O (T = 180 °C)
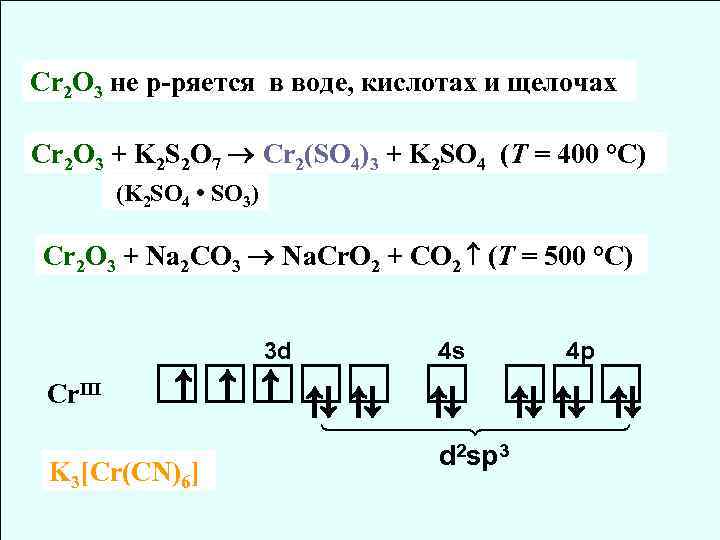
Cr 2 O 3 не р-ряется в воде, кислотах и щелочах Cr 2 O 3 + K 2 S 2 O 7 Cr 2(SO 4)3 + K 2 SO 4 (T = 400 °C) (K 2 SO 4 • SO 3) Cr 2 O 3 + Na 2 CO 3 Na. Cr. O 2 + CO 2 (T = 500 °C) 3 d Cr. III 4 s 4 p ↑↑↑ ⇅⇅ ⇅ K 3[Cr(CN)6] d 2 sp 3
![p. H Условно: [Cr(H 2 O)6]3+ [Cr(H 2 O)5 OH]2+ …… [Cr(H 2 O)3(OH)3]0 p. H Условно: [Cr(H 2 O)6]3+ [Cr(H 2 O)5 OH]2+ …… [Cr(H 2 O)3(OH)3]0](https://present5.com/presentation/3/26150394_165586596.pdf-img/26150394_165586596.pdf-17.jpg)
p. H Условно: [Cr(H 2 O)6]3+ [Cr(H 2 O)5 OH]2+ …… [Cr(H 2 O)3(OH)3]0 [Cr(H 2 O)2(OH)4]– …… [Cr(OH)6]3– Cr 3+ Cr. OH 2+ Cr(OH)3 [Cr(OH)4]– [Cr(OH)6]3–
![HCl Cr. Cl 3 Сr(OH)3 KOH K[Cr(OH)4] K 3[Cr(OH)6] S 2– H 2 S HCl Cr. Cl 3 Сr(OH)3 KOH K[Cr(OH)4] K 3[Cr(OH)6] S 2– H 2 S](https://present5.com/presentation/3/26150394_165586596.pdf-img/26150394_165586596.pdf-18.jpg)
HCl Cr. Cl 3 Сr(OH)3 KOH K[Cr(OH)4] K 3[Cr(OH)6] S 2– H 2 S Cr 3+ + CO 32– + H 2 O Cr(OH)3 + CO 2 SO 32– SO 2 [Cr(OH)6]3– + Br 2 + OH– Cr. O 42– + Br– + H 2 O
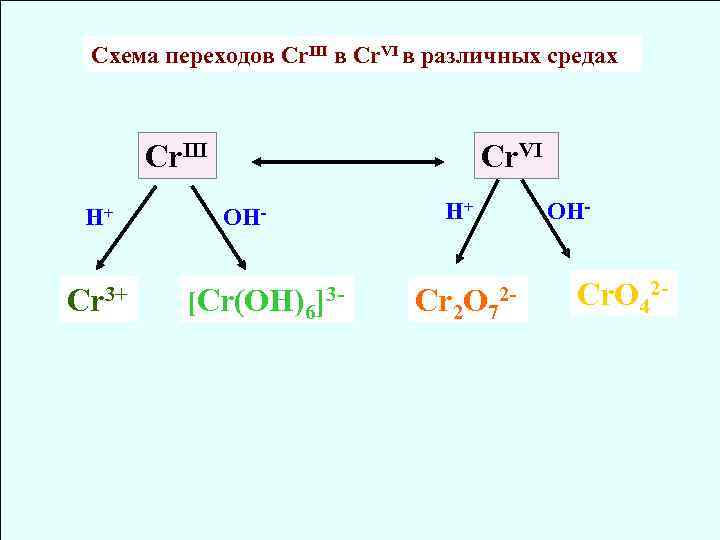
Схема переходов Cr. III в Cr. VI в различных средах Cr. III H+ Cr 3+ Cr. VI H+ OH- [Cr(OH)6 ]3 - Cr 2 O 72 - OH- Cr. O 42 -

+II Cr + HCl Cr. Cl 2 + H 2 H+ Cr. Cl 3 + Zn Cr. Cl 2 + Zn. Cl 2 Cr 3+ + e ⇄ Cr 2+, φ°= – 0, 41 B Соединения Cr(II) — сильные восстановители Cr. Cl 2 + H 2 O Cr. OHCl 2 + H 2 Cr 2+ + 2 OH– = Cr(OH)2 + H 2 O + O 2 = Cr(OH)3

Получение хрома из оксида осуществляют методом алюмотермического восстановления Cr. O 3 + Al t Cr + Al 2 O 3 Основная область применения хрома – легирование железа для получения нержавеющей стали Более подробное описание способов получения хрома и молибдена вы можете найти в дополнительных материалах к лекции № 12 на сайте кафедры

Дополнительный материал к лекции № 12 Хром, молибден, вольфрам* *Производство вольфрама описано в дополнительных материалах к лекции № 5.

Хром Основная область применения хрома – это легирование сталей и сплавов. Стали, содержащие хром, подразделяются на хромистые, хромоникелевые (пластичные, коррозионноустойчивые); нержавеющие; инструментальные; жаростойкие и жаропрочные. Также на основе добавок хрома получают термостойкие материалы, керметы. В металлургии для получения легированных сталей более выгодно использовать не чистый металл (Cr), а его сплав с железом, так называемый феррохром, поскольку ферросплавы значительно дешевле металлов и имеют более низкую температуру плавления.

Получение феррохрома Для выплавки феррохрома применяют хромовую руду – хромистый железняк (Fe. O · Cr 2 O 3), в котором содержание Cr 2 O 3 доходит до 62 %, остальное - Fe. O, Mg. O, Al 2 O 3, Si. O 2. Для выплавки углеродистого феррохрома в качестве восстановителя применяют коксик (С), для получения феррохрома с пониженным содержанием углерода восстановление ведут кремнием или алюминием. В процессе плавки руды идет восстановление хрома, железа, кремния. 1/3 Cr 2 O 3 + C = 2/3 Cr + CO - Q 1/3 Cr 2 O 3 + 9/7 C = 2/21 Cr 7 C 3 + CO - Q карбид хрома Температура плавки – 1600 -1800 ºС. Железо также восстанавливается углеродом и растворяется в карбиде хрома.

Содержание углерода в феррохроме может достигать 8 % - это так называемый высокоуглеродистый феррохром. В процессе плавки частично восстанавливается кремний, так что содержание кремния в феррохроме доходит до 2 -5 %. В феррохром переходит также часть фосфора и серы, вносимых с шихтой. Восстановительные ферросплавные печи представляют собой мощные электродуговые печи сталеплавильного типа. Они работают в непрерывном режиме. Общий вид ферросплавной печи приведен в доп. материалах лекции № 20. Для получения феррохрома с пониженным содержанием углерода (средне-, мало- и безуглеродистый феррохром) применяют силикотермический и алюмотермический способы, а также продувку кислородом жидкого углеродистого феррохрома с последующим вакуумированием.

При силикотермическом способе хромовую руду восстанавливают кремнием по реакциям: 2/3 Cr 2 O 3 + Si = 4/3 Cr + Si. O 2 2 Fe. O + Si = 2 Fe + Si. O 2 Одновременно протекают реакции восстановления карбидов хрома и железа: (Cr, Fe)х. Су + х. Si = х(Cr, Fe) Si + у. С При алюмотермическом способе оксид хрома восстанавливают алюминиевой крупкой по реакции: Cr 2 O 3 + 2 Al = 2 Cr + Al 2 O 3 Обезуглероживание продувкой кислородом и вакуумированием ведут в конвертере. Вначале жидкий феррохром продувают кислородом при нормальном давлении, а затем при пониженном давлении (в вакууме). Таким образом, cредне- и малоуглеродистый феррохром содержит соответственно 1 - 4 и 0, 2 - 0, 5 % C, безуглеродистый феррохром содержит 0, 02 - 0, 1 % C.

Получение хрома Получение металлического хрома из природного хромистого железняка осуществляют в несколько стадий. Первая стадия– окислительное плавление хромита в щелочной среде. 4 Fe. Cr 2 O 4 + 8 Na 2 CO 3 + 7 O 2 8 Na 2 Cr. O 4 + 2 Fe 2 O 3 + 8 CO 2 t Вторая стадия – растворение полученного спека в кислой среде. При этом происходит перевод хромата в дихромат, а железо в форме частично гидратированного оксида остается в осадке. 2 Na 2 Cr. O 4 + 2 H 2 SO 4 = Na 2 Cr 2 O 7 + 2 Na. HSO 4 + H 2 O Третья стадия – восстановление хрома (VI) до хрома (III) (до Cr 2 O 3). t Na 2 Cr 2 O 7 + 2 C Cr 2 O 3 + Na 2 CO 3 + CO

Металлический хром получают электролизом растворов солей хрома (III) или алюмотермическим восстановлением Cr 2 O 3 + 2 Al = Al 2 O 3 + 2 Cr Полученный «технически чистый» хром дополнительно очищают перегонкой в вакууме или электролитическим путем.

Молибденит (Mo. S 2) – наиболее распространенный и промышленно важный минерал молибдена. После обогащения молибденовых руд концентрат содержит до 70 % Mo. S 2. Краткая технологическая схема получения молибдена 1. Окислительный обжиг молибденитовых концентратов Mo. S 2 + 3, 5 O 2 500 -600 ºC Mo. O 3 + 2 SO 2 Обжиг проводят в многоподовых печах или в печах кипящего слоя. 2. Возгонка триоксида молибдена Возгонка или испарение Mo. O 3 осуществляется с целью очистки триоксида молибдена. Температура возгонки – 900 -1100 ºС. Возогнанный триоксид (огарок) имеет высокую чистоту (99, 975 % Mо. О 3). Аппарат для возгонки – электрические печи непрерывного действия с вращающимся кольцевым подом.

3. Выщелачивание. Огарок выщелачивают раствором аммиака. Выщелачивание проводят в стальных реакторах, на холоду или при температуре 50 -70 ºС, концентрация раствора аммиака – 8 -10 %. Образуется раствор парамолибдата аммония. 7 Mo. O 3 + 6 NH 3 + 3 H 2 O = (NH 4)6 Mo 7 O 24 4. Нейтрализация раствора Раствор парамолибдата аммония нейтрализуют соляной кислотой до р. Н = 2 -3 и выделяют осадок молибденовой кислоты. (NH 4)6 Mo 7 O 24 + 6 HCl + 4 H 2 O = 7 H 2 Mo. O 4 + 6 NH 4 Cl 5. Термическое разложение молибденовой кислоты Термолиз молибденовой кислоты протекает при температуре 450 -500 ºС в барабанных печах непрерывного действия. H 2 Mo. O 4 Mo. O 3 + H 2 O Mo. O 3 - порошок бледно-зеленого цвета

6. Получение порошков молибдена. Наиболее распространен в промышленной практике способ восстановления Mo. O 3 водородом. Mo. O 3 + 3 H 2 Mo + 3 H 2 O Реакция протекает в две стадии. Вторую стадию ведут при температуре 900 -1100 ºС. Молибден получают в виде порошка, который затем превращают в компактный металл методом порошковой металлургии.
Слайд_к_л_12.ppt