Лекция 12.pptx
- Количество слайдов: 66
 Лекция 12 Митоз Клеточный цикл Апоптоз
Лекция 12 Митоз Клеточный цикл Апоптоз
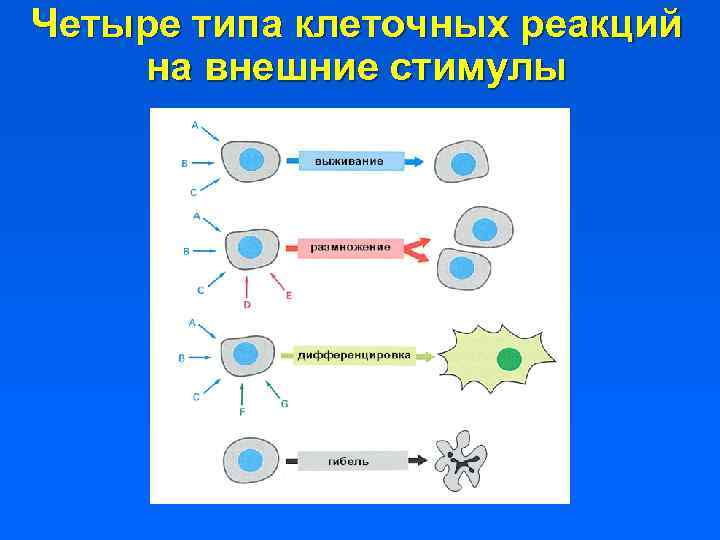 Четыре типа клеточных реакций на внешние стимулы
Четыре типа клеточных реакций на внешние стимулы
 Митоз и цитокинез Митоз – часть клеточного цикла, в которой происходит разделение ядра и расхождение удвоившейся ДНК. Расхождение молекул ядерной ДНК у эукариот всегда происходит через конденсацию хроматина с формированием компактных хромосом и с помощью специализированного аппарата – веретена деления. Как правило, митоз сопровождается разделением тела клетки – цитокинезом. Митоз без цитокинеза приводит к возникновению двуядерной клетки. Механизмы, обеспечивающие расхождение хромосом (кариокинез) и цитокинез различны.
Митоз и цитокинез Митоз – часть клеточного цикла, в которой происходит разделение ядра и расхождение удвоившейся ДНК. Расхождение молекул ядерной ДНК у эукариот всегда происходит через конденсацию хроматина с формированием компактных хромосом и с помощью специализированного аппарата – веретена деления. Как правило, митоз сопровождается разделением тела клетки – цитокинезом. Митоз без цитокинеза приводит к возникновению двуядерной клетки. Механизмы, обеспечивающие расхождение хромосом (кариокинез) и цитокинез различны.
 Основные события митоза Профаза – конденсация хромосом, формирование звезд в цитоплазме (только у животных). Прометафаза – разрушение ядерной оболочки, формирование митотического аппарата (пучков МТ и кинетохоров) и начало движения хромосом. Метафаза – формирование пластинки из кинетохоров на экваторе и натяжение кинетохорных пучков МТ. Анафаза – расхождение хромосом и полюсов, формирование перетяжки (фрагмопласта). Телофаза – деконденсация хромосом, сокращение перетяжки (рост фрагмопласта), восстановление ядерной оболочки.
Основные события митоза Профаза – конденсация хромосом, формирование звезд в цитоплазме (только у животных). Прометафаза – разрушение ядерной оболочки, формирование митотического аппарата (пучков МТ и кинетохоров) и начало движения хромосом. Метафаза – формирование пластинки из кинетохоров на экваторе и натяжение кинетохорных пучков МТ. Анафаза – расхождение хромосом и полюсов, формирование перетяжки (фрагмопласта). Телофаза – деконденсация хромосом, сокращение перетяжки (рост фрагмопласта), восстановление ядерной оболочки.
 Фазы митоза – схема
Фазы митоза – схема
 Параметры митоза Общая продолжительность: 10 мин. – 3 часа. Относительная продолжительность фаз митоза в животной клетке (общее время 70 -90 мин. ): профаза – 15 -30 мин. , прометафаза – 10 -15 мин. , метафаза – 20 мин. , анафаза – 6 -8 мин. , телофаза – 1520 мин. Скорость расхождения хромосом – около 1 мкм/мин. Скорость расхождения полюсов – 0, 5 мкм/мин. Начало цитокинеза – в анафазе. Завершение цитокинеза – после окончания телофазы.
Параметры митоза Общая продолжительность: 10 мин. – 3 часа. Относительная продолжительность фаз митоза в животной клетке (общее время 70 -90 мин. ): профаза – 15 -30 мин. , прометафаза – 10 -15 мин. , метафаза – 20 мин. , анафаза – 6 -8 мин. , телофаза – 1520 мин. Скорость расхождения хромосом – около 1 мкм/мин. Скорость расхождения полюсов – 0, 5 мкм/мин. Начало цитокинеза – в анафазе. Завершение цитокинеза – после окончания телофазы.
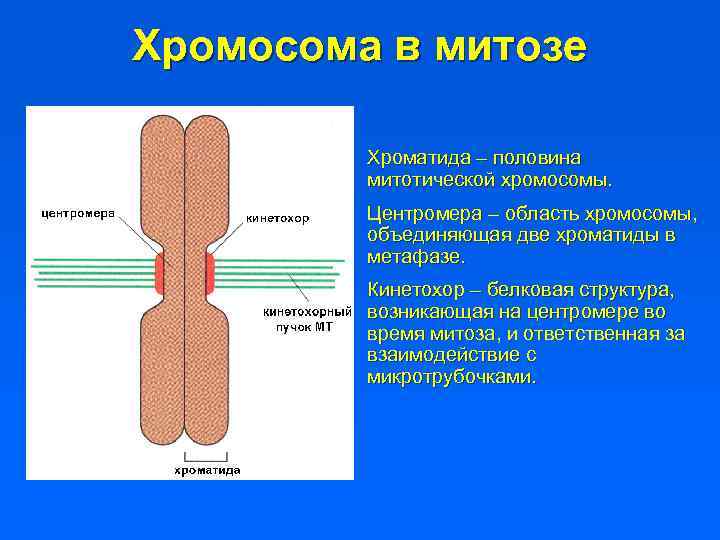 Хромосома в митозе Хроматида – половина митотической хромосомы. Центромера – область хромосомы, объединяющая две хроматиды в метафазе. Кинетохор – белковая структура, возникающая на центромере во время митоза, и ответственная за взаимодействие с микротрубочками.
Хромосома в митозе Хроматида – половина митотической хромосомы. Центромера – область хромосомы, объединяющая две хроматиды в метафазе. Кинетохор – белковая структура, возникающая на центромере во время митоза, и ответственная за взаимодействие с микротрубочками.
 Центромера и кинетохор Центромера – специальная область хромосомы (первичная перетяжка), которая существует постоянно, и наследуется (эпигенетически) в ряду клеточных поколений. Наследование центромеры обеспечивает модифицированный гистон Н 3 - белок CENP-A, который садится на центромерную ДНК в процессе репликации в S-фазе. Центромерный хроматин устойчив к деконденсации, и ДНК в нем метилирована. Кинетохор – структура, образующаяся на центромере во время деления. Кинетохор возникает в профазе и исчезает в телофазе митоза. Он содержит внутреннюю часть (связанную с центромерой) и лабильную наружную часть, взаимодействующую с микротрубочками. Кинетохор обеспечивает движение хромосом во время деления. Механизмы взаимодействия кинетохора с микротрубочками и развиваемые им усилия закономерно изменяются по фазам митоза.
Центромера и кинетохор Центромера – специальная область хромосомы (первичная перетяжка), которая существует постоянно, и наследуется (эпигенетически) в ряду клеточных поколений. Наследование центромеры обеспечивает модифицированный гистон Н 3 - белок CENP-A, который садится на центромерную ДНК в процессе репликации в S-фазе. Центромерный хроматин устойчив к деконденсации, и ДНК в нем метилирована. Кинетохор – структура, образующаяся на центромере во время деления. Кинетохор возникает в профазе и исчезает в телофазе митоза. Он содержит внутреннюю часть (связанную с центромерой) и лабильную наружную часть, взаимодействующую с микротрубочками. Кинетохор обеспечивает движение хромосом во время деления. Механизмы взаимодействия кинетохора с микротрубочками и развиваемые им усилия закономерно изменяются по фазам митоза.
 Кинетохор хромосомы Общий вид кинетохора в анафазе. Хромосома следует за пучком разбирающихся микротрубочек.
Кинетохор хромосомы Общий вид кинетохора в анафазе. Хромосома следует за пучком разбирающихся микротрубочек.
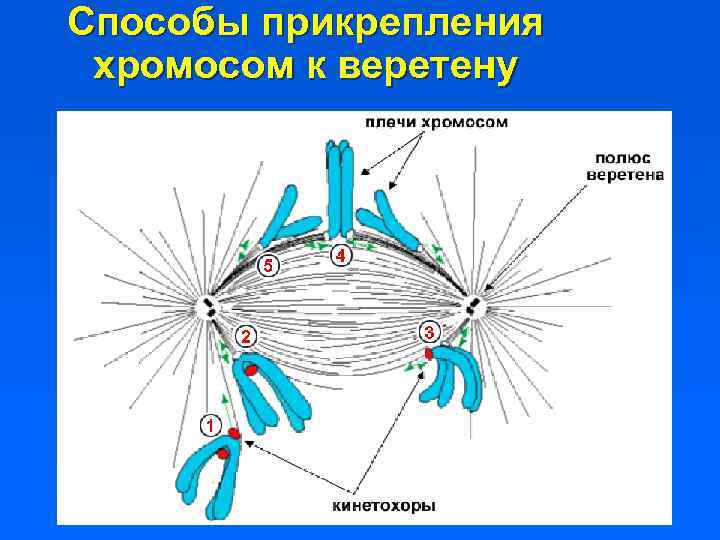 Способы прикрепления хромосом к веретену
Способы прикрепления хромосом к веретену
 Поведение кинетохора при формировании веретена 1 -3 - Одиночная МТ достигает сферической «короны» кинетохора и обеспечивает подтягивание хромосомы к полюсу (динеинзависимый процесс) 4 -5 – Кинетохор перестраивается, и, двигаясь вдоль детирозилированных МТ, хромосома уходит от полюса (мотор CENP-E/kinesin 7) 6 – Кинетохор становится плоским и закрепляется на плюс-концах пучка МТ. Устанавливается связь противоположных кинетохоров с противоположными полюсами.
Поведение кинетохора при формировании веретена 1 -3 - Одиночная МТ достигает сферической «короны» кинетохора и обеспечивает подтягивание хромосомы к полюсу (динеинзависимый процесс) 4 -5 – Кинетохор перестраивается, и, двигаясь вдоль детирозилированных МТ, хромосома уходит от полюса (мотор CENP-E/kinesin 7) 6 – Кинетохор становится плоским и закрепляется на плюс-концах пучка МТ. Устанавливается связь противоположных кинетохоров с противоположными полюсами.
 Движение хромосом в митозе Прометафаза ранняя – хромосомы поодиночке подтягиваются к полюсам за счет скольжения кинетохоров вдоль отдельных микротрубочек (с помощью динеина). Прометафаза поздняя – кинетохоры перестраиваются, и хромосомы отталкиваются от полюсов за счет роста плюс концов микротрубочек, прикрепившихся к плоскому кинетохору. Метафаза ранняя – колебание хромосом за счет роста и укорочения пучков микротрубочек, отходящих от противоположных кинетохоров. Метафаза поздняя – начало растяжения кинетохоров хромосом. Анафаза А – расхождение хромосом к полюсам за счет укорочения плюс концов прикрепленных к кинетохорам микротрубочек. Анафаза Б – одновременное расхождение хромосом и полюсов за счет удлинения межполюсных микротрубочек.
Движение хромосом в митозе Прометафаза ранняя – хромосомы поодиночке подтягиваются к полюсам за счет скольжения кинетохоров вдоль отдельных микротрубочек (с помощью динеина). Прометафаза поздняя – кинетохоры перестраиваются, и хромосомы отталкиваются от полюсов за счет роста плюс концов микротрубочек, прикрепившихся к плоскому кинетохору. Метафаза ранняя – колебание хромосом за счет роста и укорочения пучков микротрубочек, отходящих от противоположных кинетохоров. Метафаза поздняя – начало растяжения кинетохоров хромосом. Анафаза А – расхождение хромосом к полюсам за счет укорочения плюс концов прикрепленных к кинетохорам микротрубочек. Анафаза Б – одновременное расхождение хромосом и полюсов за счет удлинения межполюсных микротрубочек.
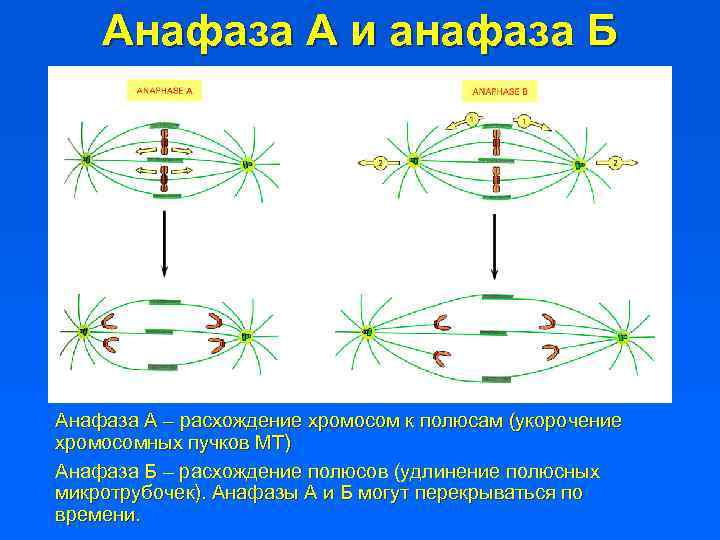 Анафаза А и анафаза Б Анафаза А – расхождение хромосом к полюсам (укорочение хромосомных пучков МТ) Анафаза Б – расхождение полюсов (удлинение полюсных микротрубочек). Анафазы А и Б могут перекрываться по времени.
Анафаза А и анафаза Б Анафаза А – расхождение хромосом к полюсам (укорочение хромосомных пучков МТ) Анафаза Б – расхождение полюсов (удлинение полюсных микротрубочек). Анафазы А и Б могут перекрываться по времени.
 Механизм расхождения хромосом в анафазе Процесс расхождения хромосом тщательно регулируется клеткой – любое экспериментальное вмешательство его только тормозит или подавляет. Основная модель – скольжение адапторных комплексов, прикрепленных к кинетохорам вдоль микротрубочек при их деполимеризации. Источник энергии – энергия, запасенная в структуре полимеризованной микротрубочки при гидролизе ГТФ.
Механизм расхождения хромосом в анафазе Процесс расхождения хромосом тщательно регулируется клеткой – любое экспериментальное вмешательство его только тормозит или подавляет. Основная модель – скольжение адапторных комплексов, прикрепленных к кинетохорам вдоль микротрубочек при их деполимеризации. Источник энергии – энергия, запасенная в структуре полимеризованной микротрубочки при гидролизе ГТФ.
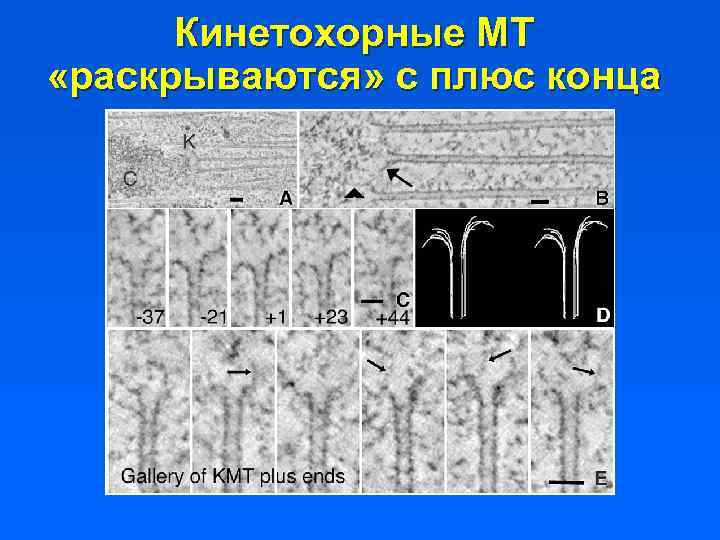 Кинетохорные МТ «раскрываются» с плюс конца
Кинетохорные МТ «раскрываются» с плюс конца
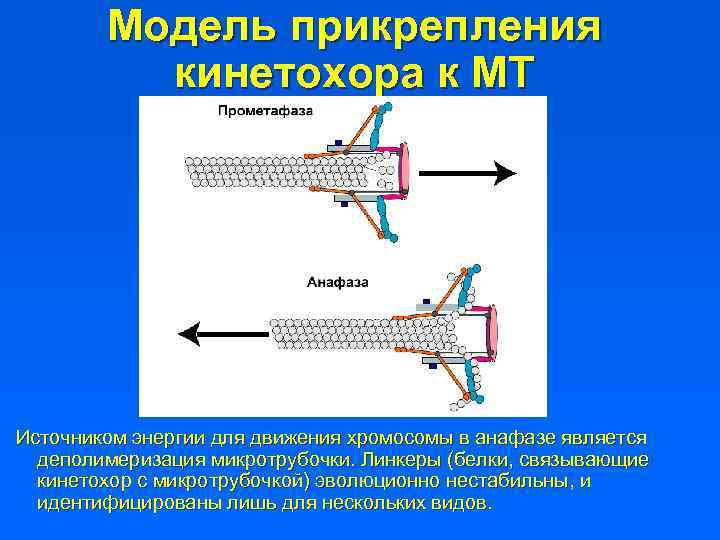 Модель прикрепления кинетохора к МТ Источником энергии для движения хромосомы в анафазе является деполимеризация микротрубочки. Линкеры (белки, связывающие кинетохор с микротрубочкой) эволюционно нестабильны, и идентифицированы лишь для нескольких видов.
Модель прикрепления кинетохора к МТ Источником энергии для движения хромосомы в анафазе является деполимеризация микротрубочки. Линкеры (белки, связывающие кинетохор с микротрубочкой) эволюционно нестабильны, и идентифицированы лишь для нескольких видов.
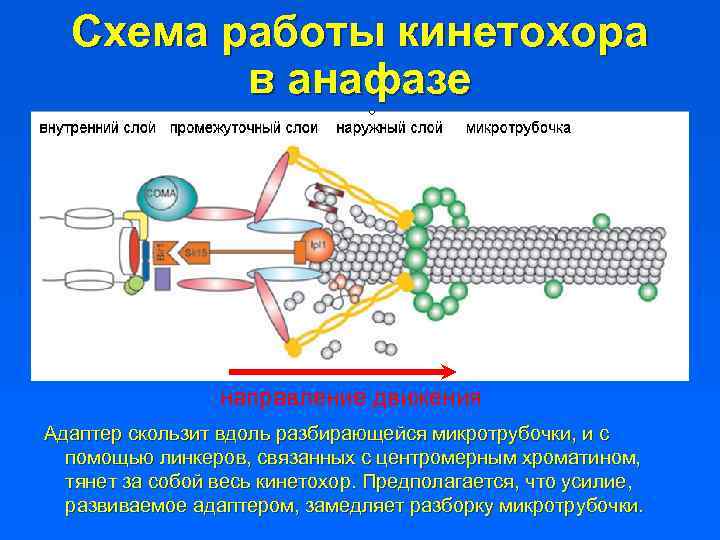 Схема работы кинетохора в анафазе направление движения Адаптер скользит вдоль разбирающейся микротрубочки, и с помощью линкеров, связанных с центромерным хроматином, тянет за собой весь кинетохор. Предполагается, что усилие, развиваемое адаптером, замедляет разборку микротрубочки.
Схема работы кинетохора в анафазе направление движения Адаптер скользит вдоль разбирающейся микротрубочки, и с помощью линкеров, связанных с центромерным хроматином, тянет за собой весь кинетохор. Предполагается, что усилие, развиваемое адаптером, замедляет разборку микротрубочки.
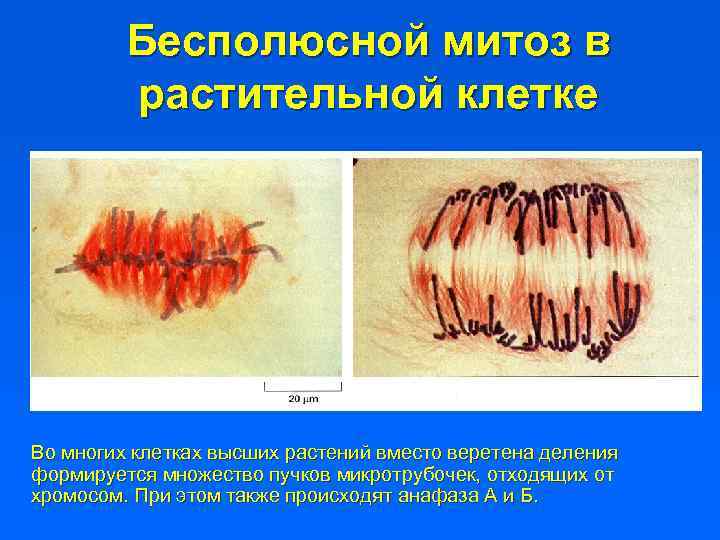 Бесполюсной митоз в растительной клетке Во многих клетках высших растений вместо веретена деления формируется множество пучков микротрубочек, отходящих от хромосом. При этом также происходят анафаза А и Б.
Бесполюсной митоз в растительной клетке Во многих клетках высших растений вместо веретена деления формируется множество пучков микротрубочек, отходящих от хромосом. При этом также происходят анафаза А и Б.
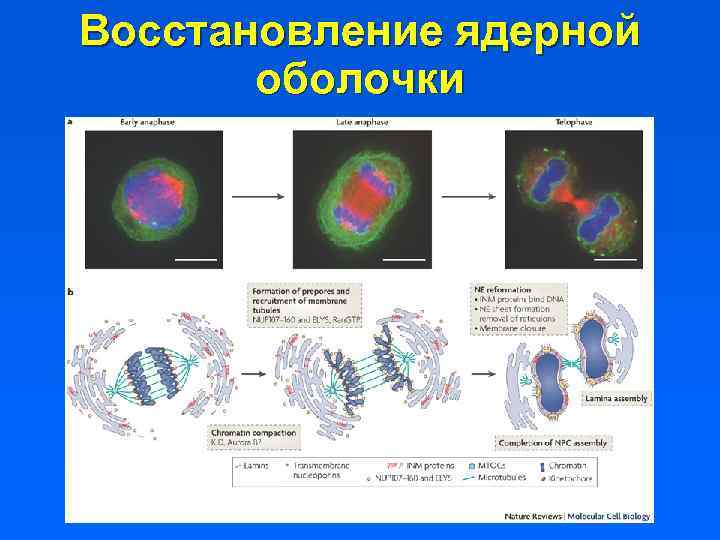 Восстановление ядерной оболочки
Восстановление ядерной оболочки
 Ингибирование митоза Остановка митоза происходит почти всегда на стадии прометафазы – метафазы. Остановка в прометафазе – ингибиторы динеина и кинезинов, а также полное разрушение веретена деления. Ингибиторы транспорта по микротрубочкам – ванадат, специфические антитела, и проч. Достаточное условие ингибирования митоза – частичное подавление динамической нестабильности микротрубочек (достигается при наномолярных концентрациях ингибиторов). Остановка происходит на стадии метафазы. Ингибиторы динамики МТ (микротрубочковые яды) – колхицин, нокодазол, винбластин, таксол и др.
Ингибирование митоза Остановка митоза происходит почти всегда на стадии прометафазы – метафазы. Остановка в прометафазе – ингибиторы динеина и кинезинов, а также полное разрушение веретена деления. Ингибиторы транспорта по микротрубочкам – ванадат, специфические антитела, и проч. Достаточное условие ингибирования митоза – частичное подавление динамической нестабильности микротрубочек (достигается при наномолярных концентрациях ингибиторов). Остановка происходит на стадии метафазы. Ингибиторы динамики МТ (микротрубочковые яды) – колхицин, нокодазол, винбластин, таксол и др.
 Патология митоза Нерасхождение хромосом (К-митоз) – результат стабилизиации микротрубочек или разрушения веретена колхицином и др. ядами. Формирование многополюсного веретена деления – как правило, обратимый процесс, но изредка заканчивается расхождением хромосом на три группы. Формирование однополюсного веретена – необратимое нарушение веретена деления, расхождения хромосом при этом не происходит.
Патология митоза Нерасхождение хромосом (К-митоз) – результат стабилизиации микротрубочек или разрушения веретена колхицином и др. ядами. Формирование многополюсного веретена деления – как правило, обратимый процесс, но изредка заканчивается расхождением хромосом на три группы. Формирование однополюсного веретена – необратимое нарушение веретена деления, расхождения хромосом при этом не происходит.
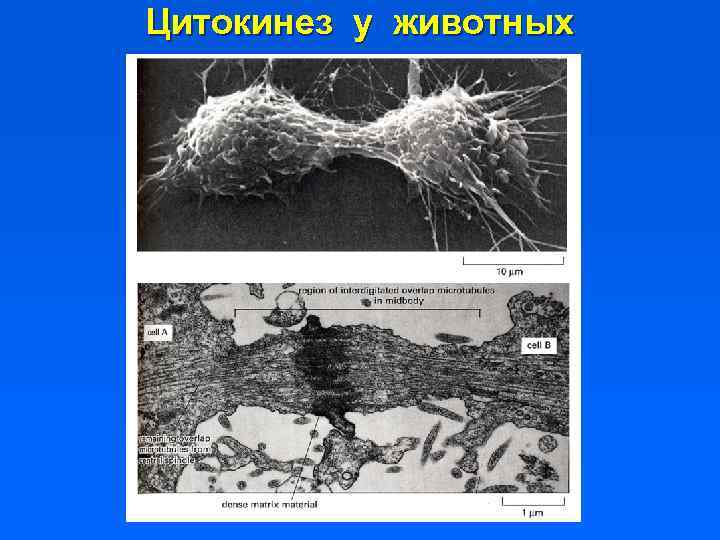 Цитокинез у животных
Цитокинез у животных
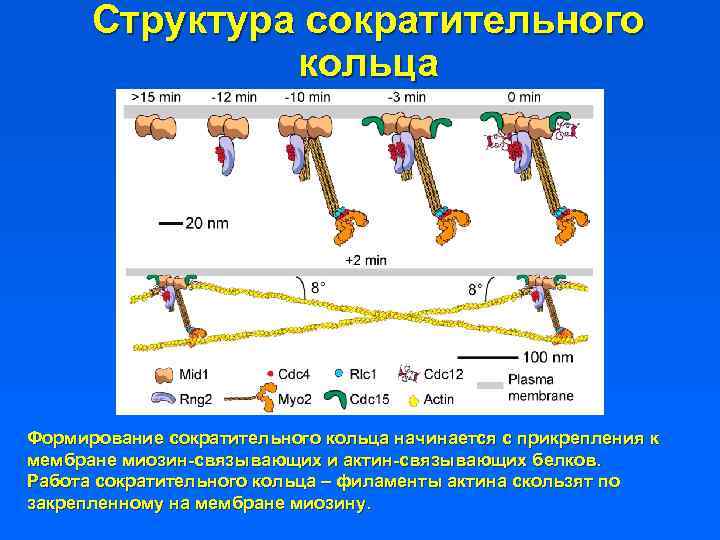 Структура сократительного кольца Формирование сократительного кольца начинается с прикрепления к мембране миозин-связывающих и актин-связывающих белков. Работа сократительного кольца – филаменты актина скользят по закрепленному на мембране миозину.
Структура сократительного кольца Формирование сократительного кольца начинается с прикрепления к мембране миозин-связывающих и актин-связывающих белков. Работа сократительного кольца – филаменты актина скользят по закрепленному на мембране миозину.
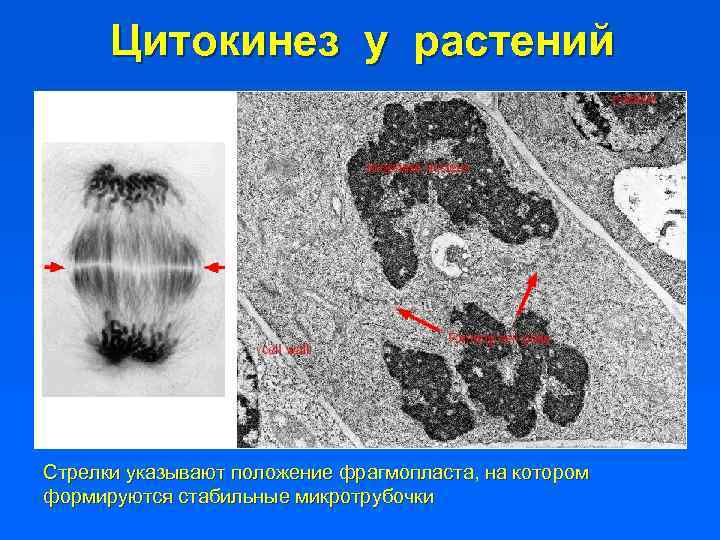 Цитокинез у растений Стрелки указывают положение фрагмопласта, на котором формируются стабильные микротрубочки
Цитокинез у растений Стрелки указывают положение фрагмопласта, на котором формируются стабильные микротрубочки
 Фрагмопласт Формирование фрагмопласта начинается в анафазе с «расчистки» периферического слоя актина. Пузырьки фрагмопласта – производное аппарата Гольджи. Фрагмопласт формирует автономную систему микротрубочек, которые плюс концами направлены к нему, а минус концами в сторону хромосом.
Фрагмопласт Формирование фрагмопласта начинается в анафазе с «расчистки» периферического слоя актина. Пузырьки фрагмопласта – производное аппарата Гольджи. Фрагмопласт формирует автономную систему микротрубочек, которые плюс концами направлены к нему, а минус концами в сторону хромосом.
 Апоптоз – запрограммированная гибель клеток
Апоптоз – запрограммированная гибель клеток
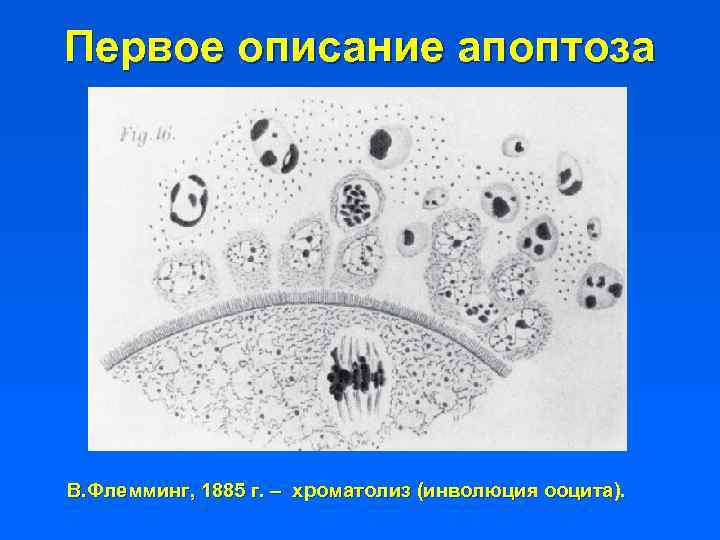 Первое описание апоптоза В. Флемминг, 1885 г. – хроматолиз (инволюция ооцита).
Первое описание апоптоза В. Флемминг, 1885 г. – хроматолиз (инволюция ооцита).
 Апоптоз – история открытия Процесс запрограммированной гибели клеток был впервые описан Р. Флеммингом в 1885 году на примере дегенерации клеток женского фолликула в менструальном цикле – был предложен термин «хроматолиз» . Случаи хроматолиза (физиологическая элиминация клеток) подробно суммированы Грепером (Ludwig Gräper) в 1917 году как нормальный процесс, противоположный митозу. Термин «апоптоз» предложен Керром с соавт. в 1972 году. Первоначальное наименование – некроз со сжатием (shrinkage necrosis). Эксперимент Керра: постепенная атрофия клеток печени после перевязки портальной вены. G. Majno and I. Jorris, 1995
Апоптоз – история открытия Процесс запрограммированной гибели клеток был впервые описан Р. Флеммингом в 1885 году на примере дегенерации клеток женского фолликула в менструальном цикле – был предложен термин «хроматолиз» . Случаи хроматолиза (физиологическая элиминация клеток) подробно суммированы Грепером (Ludwig Gräper) в 1917 году как нормальный процесс, противоположный митозу. Термин «апоптоз» предложен Керром с соавт. в 1972 году. Первоначальное наименование – некроз со сжатием (shrinkage necrosis). Эксперимент Керра: постепенная атрофия клеток печени после перевязки портальной вены. G. Majno and I. Jorris, 1995
 Апоптоз Процесс запрограммированной гибели клеток, который проходит через ряд последовательных стадий, не зависящих от вызвавшей их причины. Характерные черты апоптоза: уменьшение клеточного объема (apoptotic volume decrease – AVD); деполяризация митохондрий без их набухания (mitochondria outer membrane permabilization – MOMP); появление фосфатидилсерина на поверхности плазматической мембраны; активация каспаз и специфических ДНКаз; конденсация хроматина по периферии ядра и фрагментация ядра. На последних стадиях возможно набухание клетки и ее фрагментация (формирование апоптотических тел). В настоящее время описано много вариантов апоптотической гибели клеток, и некоторым предлагают давать отдельные названия (например, анойкис).
Апоптоз Процесс запрограммированной гибели клеток, который проходит через ряд последовательных стадий, не зависящих от вызвавшей их причины. Характерные черты апоптоза: уменьшение клеточного объема (apoptotic volume decrease – AVD); деполяризация митохондрий без их набухания (mitochondria outer membrane permabilization – MOMP); появление фосфатидилсерина на поверхности плазматической мембраны; активация каспаз и специфических ДНКаз; конденсация хроматина по периферии ядра и фрагментация ядра. На последних стадиях возможно набухание клетки и ее фрагментация (формирование апоптотических тел). В настоящее время описано много вариантов апоптотической гибели клеток, и некоторым предлагают давать отдельные названия (например, анойкис).
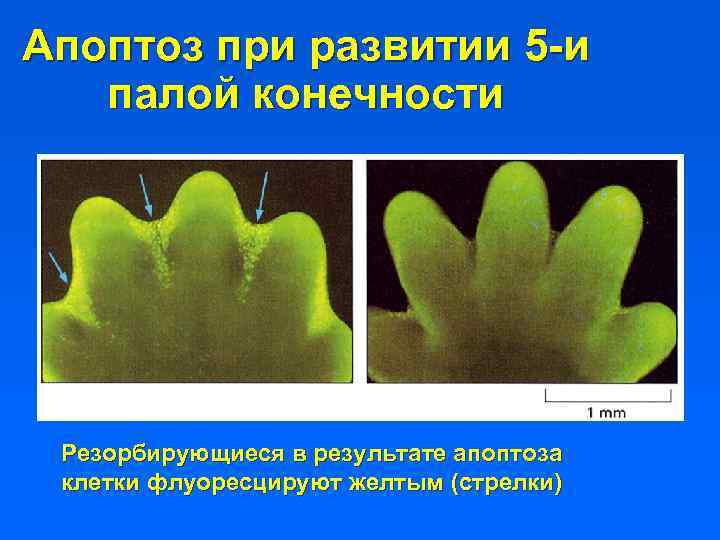 Апоптоз при развитии 5 -и палой конечности Резорбирующиеся в результате апоптоза клетки флуоресцируют желтым (стрелки)
Апоптоз при развитии 5 -и палой конечности Резорбирующиеся в результате апоптоза клетки флуоресцируют желтым (стрелки)
 Апоптоз и «острая смерть» : сравнение Ишемическая (острая) гибель клетки: набухание органелл и всей клетки, быстрое снижение уровня АТФ, потеря целостности плазматической мембраны, выход лизосомных ферментов наружу. Процесс не сопровождается специфическим расщеплением макромолекул. На уровне ткани часто индуцирует воспаление или апоптоз среди окружающих клеток. Апоптоз: первоначальное съеживание клетки и перестройка ее метаболизма, затем “вскипание” поверхности; частичный протеолиз цитоплазматических белков в результате работы специальных ферментов, перестройка хроматина и последовательное расщепление ДНК; фрагментация ядра. Конечные стадии апоптоза: фрагментация клетки и ее фагоцитоз или гибель с нарушением целостности плазматической мембраны. Процесс апоптоза в популяции всегда происходит асинхронно и не вызывает реакции воспаления.
Апоптоз и «острая смерть» : сравнение Ишемическая (острая) гибель клетки: набухание органелл и всей клетки, быстрое снижение уровня АТФ, потеря целостности плазматической мембраны, выход лизосомных ферментов наружу. Процесс не сопровождается специфическим расщеплением макромолекул. На уровне ткани часто индуцирует воспаление или апоптоз среди окружающих клеток. Апоптоз: первоначальное съеживание клетки и перестройка ее метаболизма, затем “вскипание” поверхности; частичный протеолиз цитоплазматических белков в результате работы специальных ферментов, перестройка хроматина и последовательное расщепление ДНК; фрагментация ядра. Конечные стадии апоптоза: фрагментация клетки и ее фагоцитоз или гибель с нарушением целостности плазматической мембраны. Процесс апоптоза в популяции всегда происходит асинхронно и не вызывает реакции воспаления.
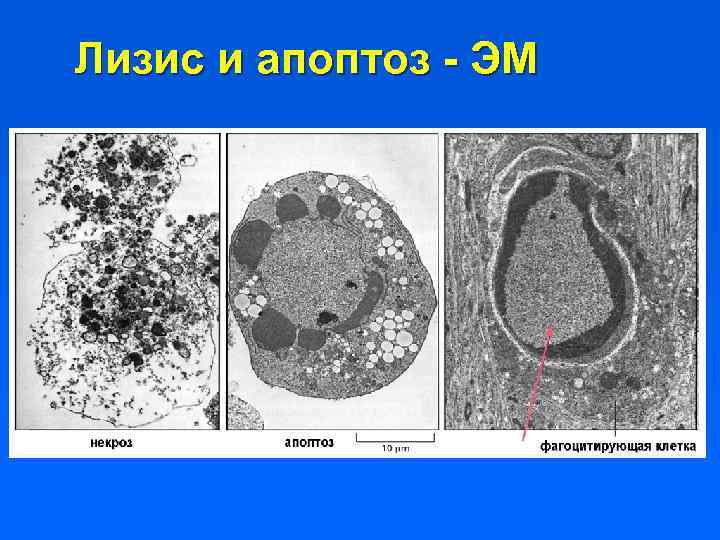 Лизис и апоптоз - ЭМ
Лизис и апоптоз - ЭМ
 Особенности апоптоза 1. Процесс протекает медленно и занимает многие часы (часто – более суток). 2. Процесс состоит из нескольких «модулей» , которые могут использоваться клеткой по отдельности. 3. Основное отличие острой смерти – быстрое нарушение всей энергетики клетки и вследствие этого – осмотические изменения и разрыв мембраны. При апоптозе даже расщепление ДНК происходит на фоне относительно «нормальной» энергетики. 4. Апоптоз не является эволюционно-консервативным процессом, хотя протекает у всех организмов аналогичным образом. У разных организмов необходимые для апоптоза функции выполняют не гомологичные белки.
Особенности апоптоза 1. Процесс протекает медленно и занимает многие часы (часто – более суток). 2. Процесс состоит из нескольких «модулей» , которые могут использоваться клеткой по отдельности. 3. Основное отличие острой смерти – быстрое нарушение всей энергетики клетки и вследствие этого – осмотические изменения и разрыв мембраны. При апоптозе даже расщепление ДНК происходит на фоне относительно «нормальной» энергетики. 4. Апоптоз не является эволюционно-консервативным процессом, хотя протекает у всех организмов аналогичным образом. У разных организмов необходимые для апоптоза функции выполняют не гомологичные белки.
 Триггерность апоптоза В клетках имеется большой набор ферментов для апоптоза, которые в норме неактивны благодаря ингибиторам (эндонуклеазы) или находятся в неактивной форме (каспазы). Сборка пор на наружной мембране митохондрий – результат активации и олигомеризации Bax/Bak. Она становится возможной, когда уровень этих белков превышает уровень bcl-2, который защищает клетки от апоптоза. После формирования митохонриальной поры цитохром с, smac-Diablo и другие белки выходят из митохондрий в течение нескольких минут. Они индуцируют сборку комплексов Apaf 1, которые олигомеризуются и в дальнейшем активируют исполняющие каспазы. Одновременно с выходом белков из митохондрий происходит нарушение ионного баланса в цитоплазме в результате открытия каналов в плазматической мембране (вход ионов Na+, выход ионов K+ и Cl-) и быстрое уменьшение клеточного объема на 20 -40%.
Триггерность апоптоза В клетках имеется большой набор ферментов для апоптоза, которые в норме неактивны благодаря ингибиторам (эндонуклеазы) или находятся в неактивной форме (каспазы). Сборка пор на наружной мембране митохондрий – результат активации и олигомеризации Bax/Bak. Она становится возможной, когда уровень этих белков превышает уровень bcl-2, который защищает клетки от апоптоза. После формирования митохонриальной поры цитохром с, smac-Diablo и другие белки выходят из митохондрий в течение нескольких минут. Они индуцируют сборку комплексов Apaf 1, которые олигомеризуются и в дальнейшем активируют исполняющие каспазы. Одновременно с выходом белков из митохондрий происходит нарушение ионного баланса в цитоплазме в результате открытия каналов в плазматической мембране (вход ионов Na+, выход ионов K+ и Cl-) и быстрое уменьшение клеточного объема на 20 -40%.
 Запуск апоптоза Внешний путь – Fas, TNF-рецептор (фактор некроза опухоли) и др. Связываются с лигандом (например, на поверхности другой клетки) и через каскад реакций активируют каспазу 8. Внутренний путь – формирование поры во внешней мембране митохондрий, формирование комплекса цитохром с - Apaf 1 (1 -й фактор активации ферментов апоптоза) и активация каспазы 9 в результате разрушения комплекса. Внутренний путь может запускаться относительно специфическими сигналами (например, через олигомеризацию митохондриальных белков Bak/Bax). Ключевая стадия – пермеабилизация наружной мембраны митохондрий, а затем – исполнительных каспаз. Запуск митохондриальной фазы апоптоза регулируется балансом активностей проапоптотических (Bax и др. ) и антиапоптотических (Bcl-2 и др. ) белков, регулирующих проницаемость наружной митохондриальной мембраны. Прямой путь апоптоза – активация каспаз с помощью перфорина и гранзима В (лимфоциты-киллеры).
Запуск апоптоза Внешний путь – Fas, TNF-рецептор (фактор некроза опухоли) и др. Связываются с лигандом (например, на поверхности другой клетки) и через каскад реакций активируют каспазу 8. Внутренний путь – формирование поры во внешней мембране митохондрий, формирование комплекса цитохром с - Apaf 1 (1 -й фактор активации ферментов апоптоза) и активация каспазы 9 в результате разрушения комплекса. Внутренний путь может запускаться относительно специфическими сигналами (например, через олигомеризацию митохондриальных белков Bak/Bax). Ключевая стадия – пермеабилизация наружной мембраны митохондрий, а затем – исполнительных каспаз. Запуск митохондриальной фазы апоптоза регулируется балансом активностей проапоптотических (Bax и др. ) и антиапоптотических (Bcl-2 и др. ) белков, регулирующих проницаемость наружной митохондриальной мембраны. Прямой путь апоптоза – активация каспаз с помощью перфорина и гранзима В (лимфоциты-киллеры).
 Митохондриальный путь 1. Выход цитохрома С и smac-Diablo из митохондрий. Первый активирует комплекс Apaf-1 (активирует каспазу 9), второй подавляет ингибиторы каспаз (IAPs). 2. Сброс мембранного потенциала на внутренней митохондриальной мембране и остановка работы электронтранспортной цепи. В пределах одной клетки оба события занимают 5 -10 минут. 3. Выход из митохондрий AIF и эндонуклеазы G. Оба белка прочно связаны с внутренней мембраной, выход происходит позднее, чем цитохрома С. Выйдя из митохондрий они попадают в ядро, где расщепляют ДНК сначала на большие фрагменты (50 к. Б), а затем на небольшие (около 200 нуклеотидов и менее – «лестница» ).
Митохондриальный путь 1. Выход цитохрома С и smac-Diablo из митохондрий. Первый активирует комплекс Apaf-1 (активирует каспазу 9), второй подавляет ингибиторы каспаз (IAPs). 2. Сброс мембранного потенциала на внутренней митохондриальной мембране и остановка работы электронтранспортной цепи. В пределах одной клетки оба события занимают 5 -10 минут. 3. Выход из митохондрий AIF и эндонуклеазы G. Оба белка прочно связаны с внутренней мембраной, выход происходит позднее, чем цитохрома С. Выйдя из митохондрий они попадают в ядро, где расщепляют ДНК сначала на большие фрагменты (50 к. Б), а затем на небольшие (около 200 нуклеотидов и менее – «лестница» ).
 Апоптоз – последовательность событий Сигналы: продолжительная активация р53 или образование комплекса лиганда с Fas/TNF-рецептором. Съеживание клетки в результате выхода ионов калия и входа ионов натрия; «вскипание» поверхности. Процесс происходит одновременно с МОМР. Появление фосфатидилсерина на поверхности плазмалеммы. Активация регуляторной каспазы (8 или 9), а затем запуск исполняющих каспаз (активация каспазы 3 и каспаз 6 и 7). Активация исполняющих каспаз происходит всегда после МОМР, а регуляторных может быть до МОМР. Активация нескольких эндонуклеаз и деградация хроматина с расщеплением ДНК – запускается каспазами, но может происходить независимо от них. Нарушение целостности плазмалеммы или поглощение клетки ее соседями (фагоцитоз). Апоптоз, по-видимому, может быть остановлен до стадии МОМР, но не может быть остановлен после активации исполняющих каспаз.
Апоптоз – последовательность событий Сигналы: продолжительная активация р53 или образование комплекса лиганда с Fas/TNF-рецептором. Съеживание клетки в результате выхода ионов калия и входа ионов натрия; «вскипание» поверхности. Процесс происходит одновременно с МОМР. Появление фосфатидилсерина на поверхности плазмалеммы. Активация регуляторной каспазы (8 или 9), а затем запуск исполняющих каспаз (активация каспазы 3 и каспаз 6 и 7). Активация исполняющих каспаз происходит всегда после МОМР, а регуляторных может быть до МОМР. Активация нескольких эндонуклеаз и деградация хроматина с расщеплением ДНК – запускается каспазами, но может происходить независимо от них. Нарушение целостности плазмалеммы или поглощение клетки ее соседями (фагоцитоз). Апоптоз, по-видимому, может быть остановлен до стадии МОМР, но не может быть остановлен после активации исполняющих каспаз.
 Каспазы Семейство цистеин-зависимых протеаз с м. в. около 30 к. Д. В апоптозе участвуют каспазы регуляторные (активируются раньше других и дополнительно регулируются ингибиторами) – 2, 8, 9, 10 и исполняющие (активируются позднее и не регулируются) – 3, 6, 7. Все каспазы синтезируются в виде прокаспаз, содержащих три домена – ингибиторный и два каталитических. В нормальной клетке находятся в цитозоле и неактивны. Активируются за счет отщепления ингибиторного домена, перестройки каталитических фрагментов молекул и их последующей олигомеризации. Активные каспазы обладают автокаталитической активностью. В активной форме каспазы расщепляют белки на крупные фрагменты по некоторым остаткам аспарагиновой кислоты. Активность регуляторных каспаз ингибируется в клетке, и они могут в течение продолжительного времени не запускать активацию исполняющих каспаз.
Каспазы Семейство цистеин-зависимых протеаз с м. в. около 30 к. Д. В апоптозе участвуют каспазы регуляторные (активируются раньше других и дополнительно регулируются ингибиторами) – 2, 8, 9, 10 и исполняющие (активируются позднее и не регулируются) – 3, 6, 7. Все каспазы синтезируются в виде прокаспаз, содержащих три домена – ингибиторный и два каталитических. В нормальной клетке находятся в цитозоле и неактивны. Активируются за счет отщепления ингибиторного домена, перестройки каталитических фрагментов молекул и их последующей олигомеризации. Активные каспазы обладают автокаталитической активностью. В активной форме каспазы расщепляют белки на крупные фрагменты по некоторым остаткам аспарагиновой кислоты. Активность регуляторных каспаз ингибируется в клетке, и они могут в течение продолжительного времени не запускать активацию исполняющих каспаз.
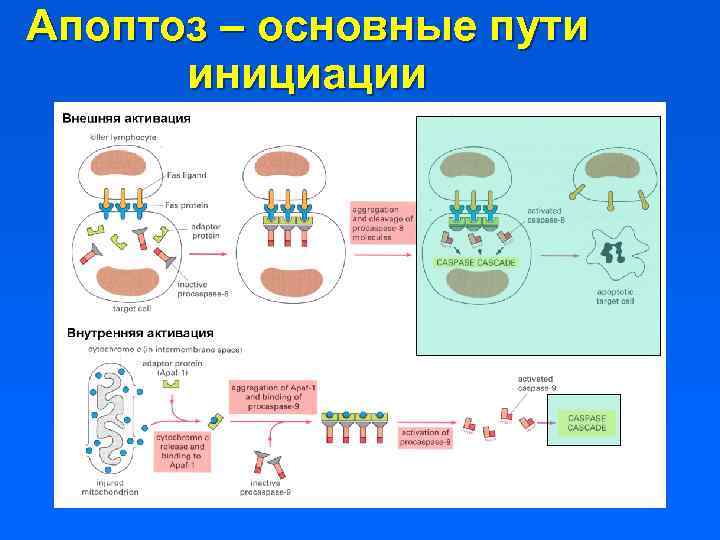 Апоптоз – основные пути инициации
Апоптоз – основные пути инициации
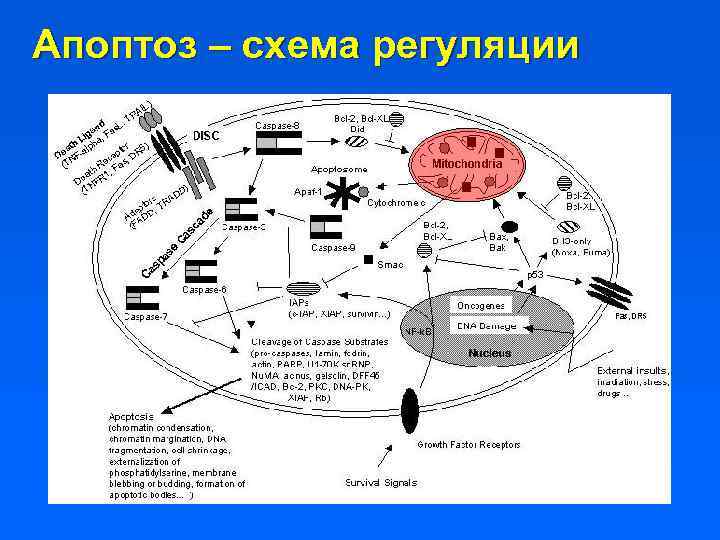 Апоптоз – схема регуляции
Апоптоз – схема регуляции
 Морфологические проявления апоптоза Отделение клеток от субстрата и друг от друга. Съеживание клетки (уменьшение объема) без разрушения плазматической мембраны. Потеря (снижение) митохондриального потенциала без значительного набухания митохондрий. Появление аннексина V на поверхности плазматической мембраны Вскипание цитоплазмы (блэббинг) и отделение пузырей. Конденсация хроматина и съеживание ядра.
Морфологические проявления апоптоза Отделение клеток от субстрата и друг от друга. Съеживание клетки (уменьшение объема) без разрушения плазматической мембраны. Потеря (снижение) митохондриального потенциала без значительного набухания митохондрий. Появление аннексина V на поверхности плазматической мембраны Вскипание цитоплазмы (блэббинг) и отделение пузырей. Конденсация хроматина и съеживание ядра.
 Апоптоз – запрограммированная гибель клеток
Апоптоз – запрограммированная гибель клеток
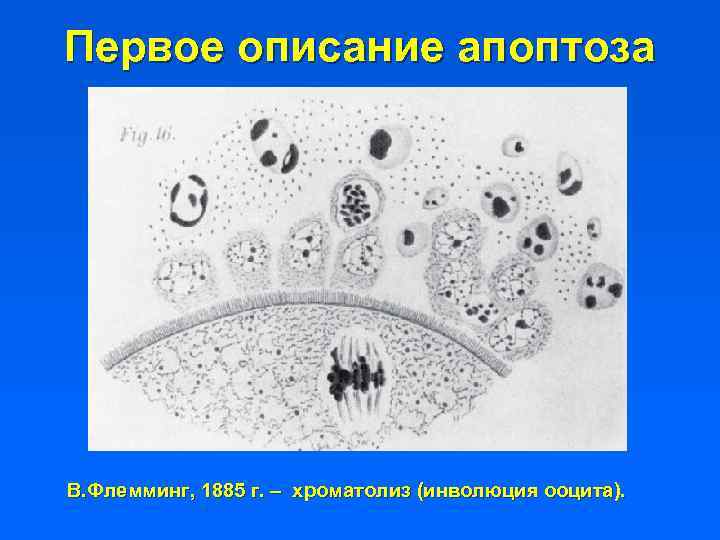 Первое описание апоптоза В. Флемминг, 1885 г. – хроматолиз (инволюция ооцита).
Первое описание апоптоза В. Флемминг, 1885 г. – хроматолиз (инволюция ооцита).
 Апоптоз – история открытия Процесс запрограммированной гибели клеток был впервые описан Р. Флеммингом в 1885 году на примере дегенерации клеток женского фолликула в менструальном цикле – был предложен термин «хроматолиз» . Случаи хроматолиза (физиологическая элиминация клеток) подробно суммированы Грепером (Ludwig Gräper) в 1917 году как нормальный процесс, противоположный митозу. Термин «апоптоз» предложен Керром с соавт. в 1972 году. Первоначальное наименование – некроз со сжатием (shrinkage necrosis). Эксперимент Керра: постепенная атрофия клеток печени после перевязки портальной вены. G. Majno and I. Jorris, 1995
Апоптоз – история открытия Процесс запрограммированной гибели клеток был впервые описан Р. Флеммингом в 1885 году на примере дегенерации клеток женского фолликула в менструальном цикле – был предложен термин «хроматолиз» . Случаи хроматолиза (физиологическая элиминация клеток) подробно суммированы Грепером (Ludwig Gräper) в 1917 году как нормальный процесс, противоположный митозу. Термин «апоптоз» предложен Керром с соавт. в 1972 году. Первоначальное наименование – некроз со сжатием (shrinkage necrosis). Эксперимент Керра: постепенная атрофия клеток печени после перевязки портальной вены. G. Majno and I. Jorris, 1995
 Апоптоз Процесс запрограммированной гибели клеток, который проходит через ряд последовательных стадий, не зависящих от вызвавшей их причины. Характерные черты апоптоза: уменьшение клеточного объема (apoptotic volume decrease – AVD); деполяризация митохондрий без их набухания (mitochondria outer membrane permabilization – MOMP); появление фосфатидилсерина на поверхности плазматической мембраны; активация каспаз и специфических ДНКаз; конденсация хроматина по периферии ядра и фрагментация ядра. На последних стадиях возможно набухание клетки и ее фрагментация (формирование апоптотических тел).
Апоптоз Процесс запрограммированной гибели клеток, который проходит через ряд последовательных стадий, не зависящих от вызвавшей их причины. Характерные черты апоптоза: уменьшение клеточного объема (apoptotic volume decrease – AVD); деполяризация митохондрий без их набухания (mitochondria outer membrane permabilization – MOMP); появление фосфатидилсерина на поверхности плазматической мембраны; активация каспаз и специфических ДНКаз; конденсация хроматина по периферии ядра и фрагментация ядра. На последних стадиях возможно набухание клетки и ее фрагментация (формирование апоптотических тел).
 Апоптоз и «острая смерть» : сравнение Ишемическая (острая) гибель клетки: набухание органелл и всей клетки, быстрое снижение уровня АТФ, потеря целостности плазматической мембраны, выход лизосомных ферментов наружу. Процесс не сопровождается специфическим расщеплением макромолекул. На уровне ткани часто индуцирует воспаление или апоптоз среди окружающих клеток. Апоптоз: первоначальное съеживание клетки и перестройка ее метаболизма, затем “вскипание” поверхности; частичный протеолиз цитоплазматических белков в результате работы специальных ферментов, перестройка хроматина и последовательное расщепление ДНК; фрагментация ядра. Конечные стадии апоптоза: фрагментация клетки и ее фагоцитоз или гибель с нарушением целостности плазматической мембраны. Процесс апоптоза в популяции всегда происходит асинхронно и не вызывает реакции воспаления.
Апоптоз и «острая смерть» : сравнение Ишемическая (острая) гибель клетки: набухание органелл и всей клетки, быстрое снижение уровня АТФ, потеря целостности плазматической мембраны, выход лизосомных ферментов наружу. Процесс не сопровождается специфическим расщеплением макромолекул. На уровне ткани часто индуцирует воспаление или апоптоз среди окружающих клеток. Апоптоз: первоначальное съеживание клетки и перестройка ее метаболизма, затем “вскипание” поверхности; частичный протеолиз цитоплазматических белков в результате работы специальных ферментов, перестройка хроматина и последовательное расщепление ДНК; фрагментация ядра. Конечные стадии апоптоза: фрагментация клетки и ее фагоцитоз или гибель с нарушением целостности плазматической мембраны. Процесс апоптоза в популяции всегда происходит асинхронно и не вызывает реакции воспаления.
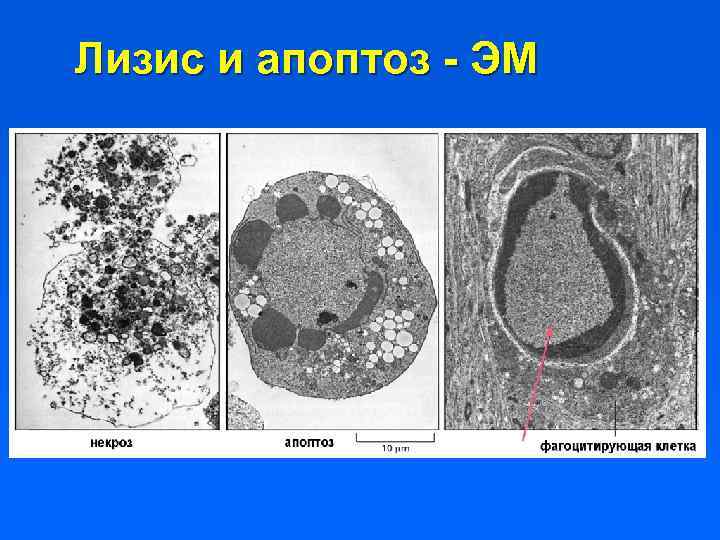 Лизис и апоптоз - ЭМ
Лизис и апоптоз - ЭМ
 Физиологическая роль апоптоза • Эмбриональное развитие (формирование конечностей) • Метаморфоз (головастик) • Контроль качества (дифференцировка Ти В -лимфоцитов) • Баланс делений и гибели (удаление части органа) • Контрольные точки в клеточном цикле
Физиологическая роль апоптоза • Эмбриональное развитие (формирование конечностей) • Метаморфоз (головастик) • Контроль качества (дифференцировка Ти В -лимфоцитов) • Баланс делений и гибели (удаление части органа) • Контрольные точки в клеточном цикле
 Особенности апоптоза 1. Процесс протекает медленно и занимает многие часы (часто – более суток). 2. Процесс состоит из нескольких «модулей» , которые могут использоваться клеткой по отдельности. 3. Основное отличие острой смерти – быстрое нарушение всей энергетики клетки и вследствие этого – осмотические изменения и разрыв мембраны. При апоптозе даже расщепление ДНК происходит на фоне относительно «нормальной» энергетики. 4. Апоптоз не является эволюционно-консервативным процессом, хотя протекает у всех организмов аналогичным образом. У разных организмов необходимые для апоптоза функции выполняют не гомологичные белки.
Особенности апоптоза 1. Процесс протекает медленно и занимает многие часы (часто – более суток). 2. Процесс состоит из нескольких «модулей» , которые могут использоваться клеткой по отдельности. 3. Основное отличие острой смерти – быстрое нарушение всей энергетики клетки и вследствие этого – осмотические изменения и разрыв мембраны. При апоптозе даже расщепление ДНК происходит на фоне относительно «нормальной» энергетики. 4. Апоптоз не является эволюционно-консервативным процессом, хотя протекает у всех организмов аналогичным образом. У разных организмов необходимые для апоптоза функции выполняют не гомологичные белки.
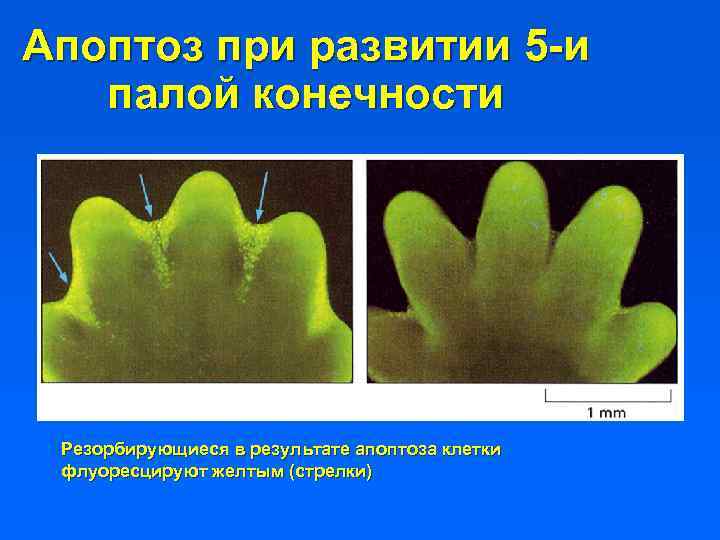 Апоптоз при развитии 5 -и палой конечности Резорбирующиеся в результате апоптоза клетки флуоресцируют желтым (стрелки)
Апоптоз при развитии 5 -и палой конечности Резорбирующиеся в результате апоптоза клетки флуоресцируют желтым (стрелки)
 Каспазы – основные ферменты апоптоза • Цистеиновые протеазы • Режут по апспарагину • Присутствуют в виде прокаспаз • Активируются разрезанием • Прокаспаза режется на две субьединицы(гетеродимер), два гетеродимера образуют активный тетрамер • Каспазы бывают регуляторные (2, 8, 9, 10), эффекторные (3, 6, 7) и воспалительные (1, 4, 5)
Каспазы – основные ферменты апоптоза • Цистеиновые протеазы • Режут по апспарагину • Присутствуют в виде прокаспаз • Активируются разрезанием • Прокаспаза режется на две субьединицы(гетеродимер), два гетеродимера образуют активный тетрамер • Каспазы бывают регуляторные (2, 8, 9, 10), эффекторные (3, 6, 7) и воспалительные (1, 4, 5)
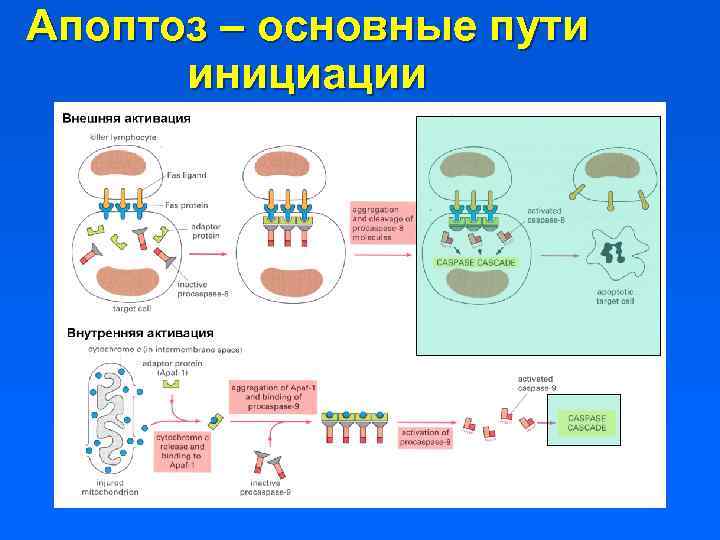 Апоптоз – основные пути инициации
Апоптоз – основные пути инициации
 Внешний путь апоптоза – рецепторы смерти • Наиболее известные – TNF и Fas-R • Гомотримеры, лиганды – тоже гомотримеры • Имеют в составе DD (death domain) • Результат активации DR – формирование DISC (death-inducing signalling complex)
Внешний путь апоптоза – рецепторы смерти • Наиболее известные – TNF и Fas-R • Гомотримеры, лиганды – тоже гомотримеры • Имеют в составе DD (death domain) • Результат активации DR – формирование DISC (death-inducing signalling complex)
 Запуск апоптоза Внешний путь – Fas, TNF-рецептор (фактор некроза опухоли) и др. Связываются с лигандом (например, на поверхности другой клетки) и через каскад реакций активируют каспазу 8. Внутренний путь – формирование поры во внешней мембране митохондрий, формирование комплекса цитохром с - Apaf 1 (1 -й фактор активации ферментов апоптоза) и активация каспазы 9 в результате разрушения комплекса. Внутренний путь может запускаться относительно специфическими сигналами (например, через олигомеризацию митохондриальных белков Bak/Bax). Ключевая стадия – пермеабилизация наружной мембраны митохондрий, а затем – исполнительных каспаз. Запуск митохондриальной фазы апоптоза регулируется балансом активностей проапоптотических (Bax и др. ) и антиапоптотических (Bcl-2 и др. ) белков, регулирующих проницаемость наружной митохондриальной мембраны. Прямой путь апоптоза – активация каспаз с помощью перфорина и гранзима В (лимфоциты-киллеры).
Запуск апоптоза Внешний путь – Fas, TNF-рецептор (фактор некроза опухоли) и др. Связываются с лигандом (например, на поверхности другой клетки) и через каскад реакций активируют каспазу 8. Внутренний путь – формирование поры во внешней мембране митохондрий, формирование комплекса цитохром с - Apaf 1 (1 -й фактор активации ферментов апоптоза) и активация каспазы 9 в результате разрушения комплекса. Внутренний путь может запускаться относительно специфическими сигналами (например, через олигомеризацию митохондриальных белков Bak/Bax). Ключевая стадия – пермеабилизация наружной мембраны митохондрий, а затем – исполнительных каспаз. Запуск митохондриальной фазы апоптоза регулируется балансом активностей проапоптотических (Bax и др. ) и антиапоптотических (Bcl-2 и др. ) белков, регулирующих проницаемость наружной митохондриальной мембраны. Прямой путь апоптоза – активация каспаз с помощью перфорина и гранзима В (лимфоциты-киллеры).
 Митохондриальный путь 1. Выход цитохрома С и smac-Diablo из митохондрий. Первый активирует комплекс Apaf 1 (активирует каспазу 9), второй подавляет ингибиторы каспаз (IAPs). 2. Сброс мембранного потенциала на внутренней митохондриальной мембране и остановка работы электрон-транспортной цепи. В пределах одной клетки оба события занимают 5 -10 минут. 3. Выход из митохондрий AIF и эндонуклеазы G. Оба белка прочно связаны с внутренней мембраной, выход происходит позднее, чем цитохрома С. Выйдя из митохондрий они попадают в ядро, где расщепляют ДНК сначала на большие фрагменты (50 к. Б), а затем на небольшие (около 200 нуклеотидов и менее – «лестница» ).
Митохондриальный путь 1. Выход цитохрома С и smac-Diablo из митохондрий. Первый активирует комплекс Apaf 1 (активирует каспазу 9), второй подавляет ингибиторы каспаз (IAPs). 2. Сброс мембранного потенциала на внутренней митохондриальной мембране и остановка работы электрон-транспортной цепи. В пределах одной клетки оба события занимают 5 -10 минут. 3. Выход из митохондрий AIF и эндонуклеазы G. Оба белка прочно связаны с внутренней мембраной, выход происходит позднее, чем цитохрома С. Выйдя из митохондрий они попадают в ядро, где расщепляют ДНК сначала на большие фрагменты (50 к. Б), а затем на небольшие (около 200 нуклеотидов и менее – «лестница» ).
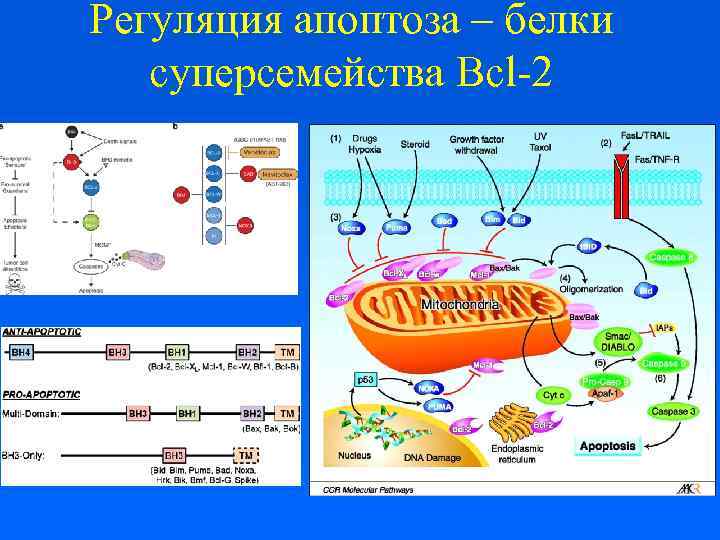 Регуляция апоптоза – белки суперсемейства Bcl-2
Регуляция апоптоза – белки суперсемейства Bcl-2
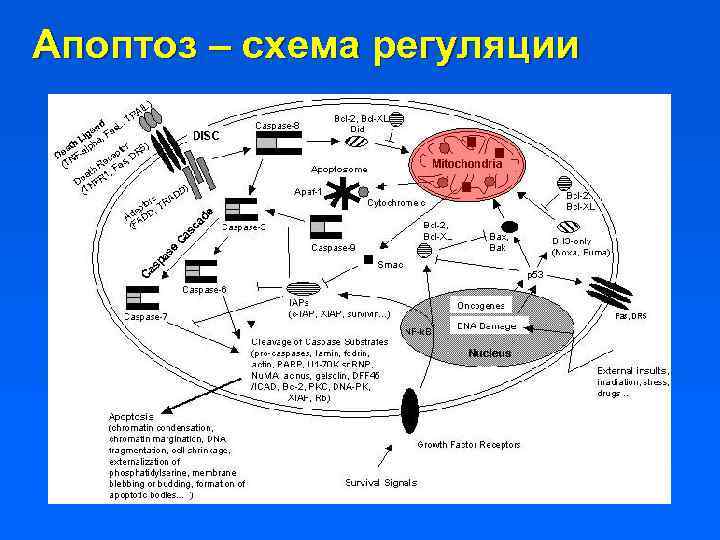 Апоптоз – схема регуляции
Апоптоз – схема регуляции
 Морфологические проявления апоптоза Отделение клеток от субстрата и друг от друга. Съеживание клетки (уменьшение объема) без разрушения плазматической мембраны. Потеря (снижение) митохондриального потенциала без значительного набухания митохондрий. Появление аннексина V на поверхности плазматической мембраны Вскипание цитоплазмы (блэббинг) и отделение пузырей. Конденсация хроматина и съеживание ядра.
Морфологические проявления апоптоза Отделение клеток от субстрата и друг от друга. Съеживание клетки (уменьшение объема) без разрушения плазматической мембраны. Потеря (снижение) митохондриального потенциала без значительного набухания митохондрий. Появление аннексина V на поверхности плазматической мембраны Вскипание цитоплазмы (блэббинг) и отделение пузырей. Конденсация хроматина и съеживание ядра.
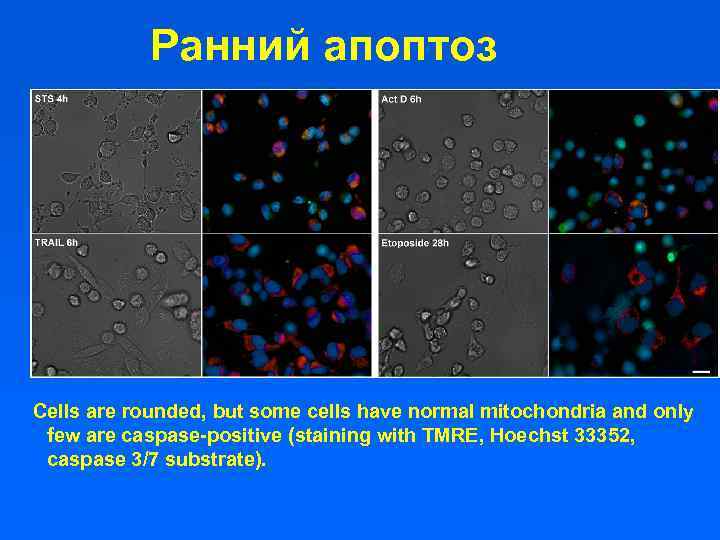 Ранний апоптоз Cells are rounded, but some cells have normal mitochondria and only few are caspase-positive (staining with TMRE, Hoechst 33352, caspase 3/7 substrate).
Ранний апоптоз Cells are rounded, but some cells have normal mitochondria and only few are caspase-positive (staining with TMRE, Hoechst 33352, caspase 3/7 substrate).
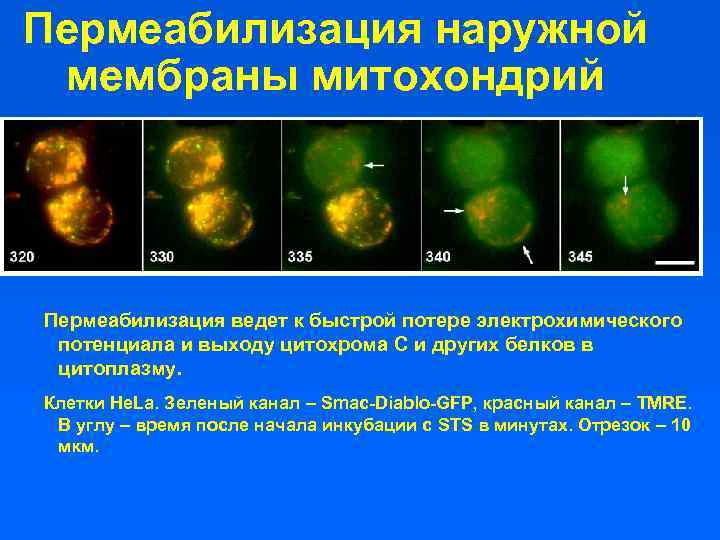 Пермеабилизация наружной мембраны митохондрий Пермеабилизация ведет к быстрой потере электрохимического потенциала и выходу цитохрома С и других белков в цитоплазму. Клетки He. La. Зеленый канал – Smac-Diablo-GFP, красный канал – TMRE. В углу – время после начала инкубации с STS в минутах. Отрезок – 10 мкм.
Пермеабилизация наружной мембраны митохондрий Пермеабилизация ведет к быстрой потере электрохимического потенциала и выходу цитохрома С и других белков в цитоплазму. Клетки He. La. Зеленый канал – Smac-Diablo-GFP, красный канал – TMRE. В углу – время после начала инкубации с STS в минутах. Отрезок – 10 мкм.
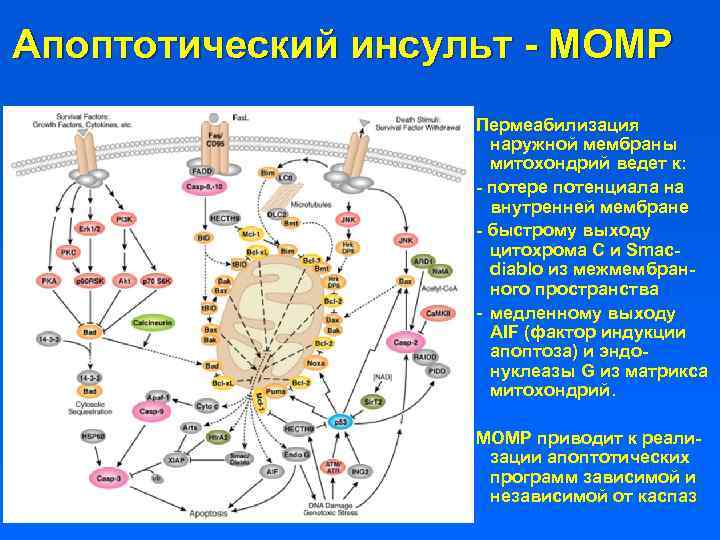 Апоптотический инсульт - MOMP Пермеабилизация наружной мембраны митохондрий ведет к: - потере потенциала на внутренней мембране - быстрому выходу цитохрома C и Smacdiablo из межмембранного пространства - медленному выходу AIF (фактор индукции апоптоза) и эндонуклеазы G из матрикса митохондрий. MOMP приводит к реализации апоптотических программ зависимой и независимой от каспаз
Апоптотический инсульт - MOMP Пермеабилизация наружной мембраны митохондрий ведет к: - потере потенциала на внутренней мембране - быстрому выходу цитохрома C и Smacdiablo из межмембранного пространства - медленному выходу AIF (фактор индукции апоптоза) и эндонуклеазы G из матрикса митохондрий. MOMP приводит к реализации апоптотических программ зависимой и независимой от каспаз
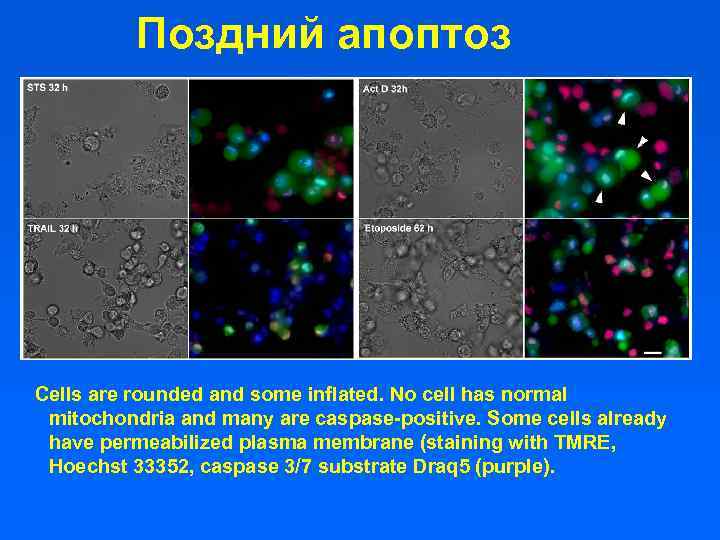 Поздний апоптоз Cells are rounded and some inflated. No cell has normal mitochondria and many are caspase-positive. Some cells already have permeabilized plasma membrane (staining with TMRE, Hoechst 33352, caspase 3/7 substrate Draq 5 (purple).
Поздний апоптоз Cells are rounded and some inflated. No cell has normal mitochondria and many are caspase-positive. Some cells already have permeabilized plasma membrane (staining with TMRE, Hoechst 33352, caspase 3/7 substrate Draq 5 (purple).
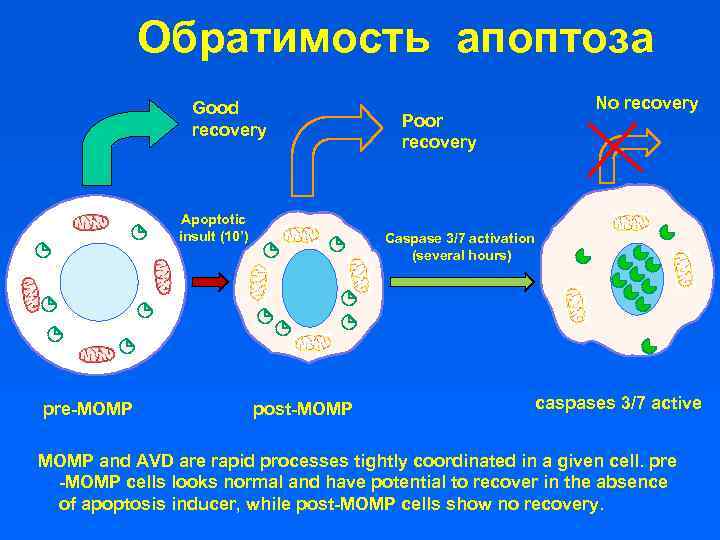 Обратимость апоптоза Good recovery Apoptotic insult (10’) pre-MOMP Poor recovery No recovery Caspase 3/7 activation (several hours) post-MOMP caspases 3/7 active MOMP and AVD are rapid processes tightly coordinated in a given cell. pre -MOMP cells looks normal and have potential to recover in the absence of apoptosis inducer, while post-MOMP cells show no recovery.
Обратимость апоптоза Good recovery Apoptotic insult (10’) pre-MOMP Poor recovery No recovery Caspase 3/7 activation (several hours) post-MOMP caspases 3/7 active MOMP and AVD are rapid processes tightly coordinated in a given cell. pre -MOMP cells looks normal and have potential to recover in the absence of apoptosis inducer, while post-MOMP cells show no recovery.
 Ингибирование апоптоза - инактивация Fas-рецептора или Fas-зависимого пути - инактивация генов-супрессоров опухолевого роста (TGF-b и др. ) - инактивация р53 зависимого пути и/или Rb-зависимого пути - гиперэкспрессия антиапоптотических белков (bcl-2, IAPs и др. ) в результате активации соответствующих генов - подавление проапоптотических генов и снижение уровня экспрессии проапоптотических белков, связанных с митохондриями (bax, bid и др. ) Инактивация (ингибирование) каспаз замедляет процесс запрограммированной гибели клеток, но не предотвращает апоптоза – он реализуется за счет других ферментов.
Ингибирование апоптоза - инактивация Fas-рецептора или Fas-зависимого пути - инактивация генов-супрессоров опухолевого роста (TGF-b и др. ) - инактивация р53 зависимого пути и/или Rb-зависимого пути - гиперэкспрессия антиапоптотических белков (bcl-2, IAPs и др. ) в результате активации соответствующих генов - подавление проапоптотических генов и снижение уровня экспрессии проапоптотических белков, связанных с митохондриями (bax, bid и др. ) Инактивация (ингибирование) каспаз замедляет процесс запрограммированной гибели клеток, но не предотвращает апоптоза – он реализуется за счет других ферментов.
 Апоптоз y Caenorhabditis elegans В онтогенезе у этого круглого червя формируется 1090 клеток, из которых 131 погибает, и 959 остается во взрослом состоянии – количество клеток постоянно у всех особей.
Апоптоз y Caenorhabditis elegans В онтогенезе у этого круглого червя формируется 1090 клеток, из которых 131 погибает, и 959 остается во взрослом состоянии – количество клеток постоянно у всех особей.


