лекция 12 гетроциклы и сахара.ppt
- Количество слайдов: 25
 Лекция 12 Гетероциклические соединения. Сахара
Лекция 12 Гетероциклические соединения. Сахара
 Гетероциклические соединения Номенклатура производных гетероциклических соединений отличается тем, что нумерация атомов в цикле всегда начинается с гетероатома (старшинство гетероатомов определяется их атомной массой) и увеличивается по направлению к другим ближайшим гетероатомам (если они есть), или как в производных бензола по направлению к наиболее старшей функциональной группе.
Гетероциклические соединения Номенклатура производных гетероциклических соединений отличается тем, что нумерация атомов в цикле всегда начинается с гетероатома (старшинство гетероатомов определяется их атомной массой) и увеличивается по направлению к другим ближайшим гетероатомам (если они есть), или как в производных бензола по направлению к наиболее старшей функциональной группе.
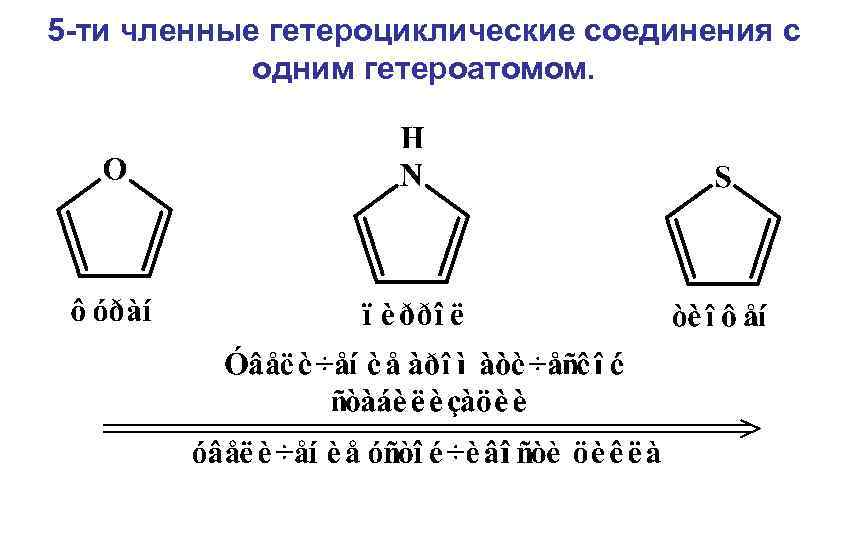 5 -ти членные гетероциклические соединения с одним гетероатомом.
5 -ти членные гетероциклические соединения с одним гетероатомом.
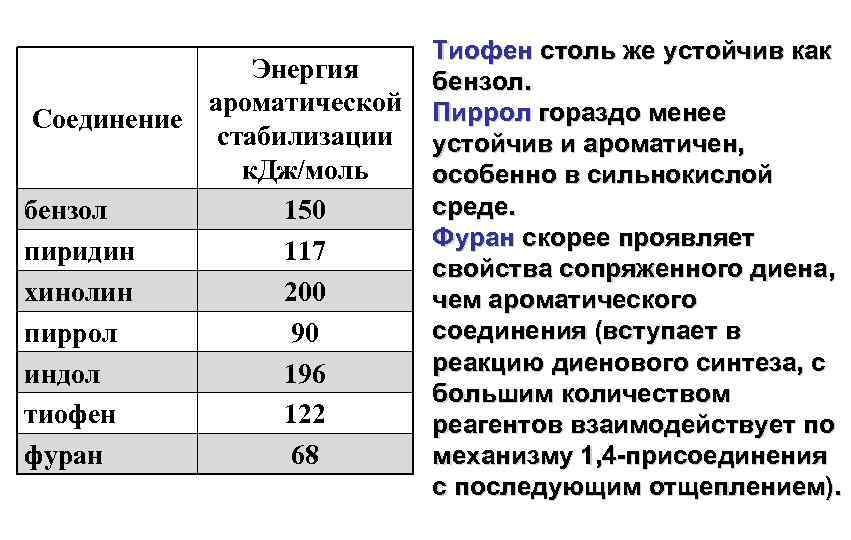 Энергия ароматической Соединение стабилизации к. Дж/моль бензол 150 пиридин 117 хинолин 200 пиррол 90 индол 196 тиофен 122 фуран 68 Тиофен столь же устойчив как бензол. Пиррол гораздо менее устойчив и ароматичен, особенно в сильнокислой среде. Фуран скорее проявляет свойства сопряженного диена, чем ароматического соединения (вступает в реакцию диенового синтеза, с большим количеством реагентов взаимодействует по механизму 1, 4 -присоединения с последующим отщеплением).
Энергия ароматической Соединение стабилизации к. Дж/моль бензол 150 пиридин 117 хинолин 200 пиррол 90 индол 196 тиофен 122 фуран 68 Тиофен столь же устойчив как бензол. Пиррол гораздо менее устойчив и ароматичен, особенно в сильнокислой среде. Фуран скорее проявляет свойства сопряженного диена, чем ароматического соединения (вступает в реакцию диенового синтеза, с большим количеством реагентов взаимодействует по механизму 1, 4 -присоединения с последующим отщеплением).
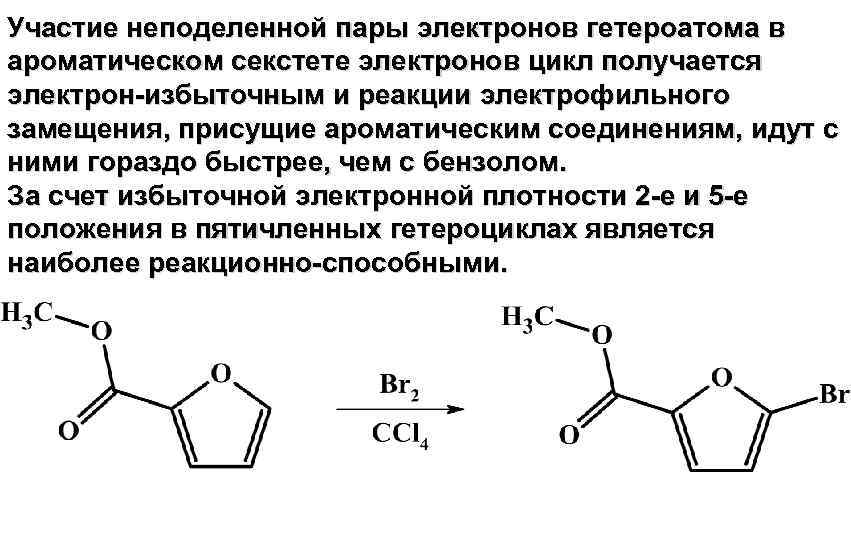 Участие неподеленной пары электронов гетероатома в ароматическом секстете электронов цикл получается электрон-избыточным и реакции электрофильного замещения, присущие ароматическим соединениям, идут с ними гораздо быстрее, чем с бензолом. За счет избыточной электронной плотности 2 -е и 5 -е положения в пятичленных гетероциклах является наиболее реакционно-способными.
Участие неподеленной пары электронов гетероатома в ароматическом секстете электронов цикл получается электрон-избыточным и реакции электрофильного замещения, присущие ароматическим соединениям, идут с ними гораздо быстрее, чем с бензолом. За счет избыточной электронной плотности 2 -е и 5 -е положения в пятичленных гетероциклах является наиболее реакционно-способными.
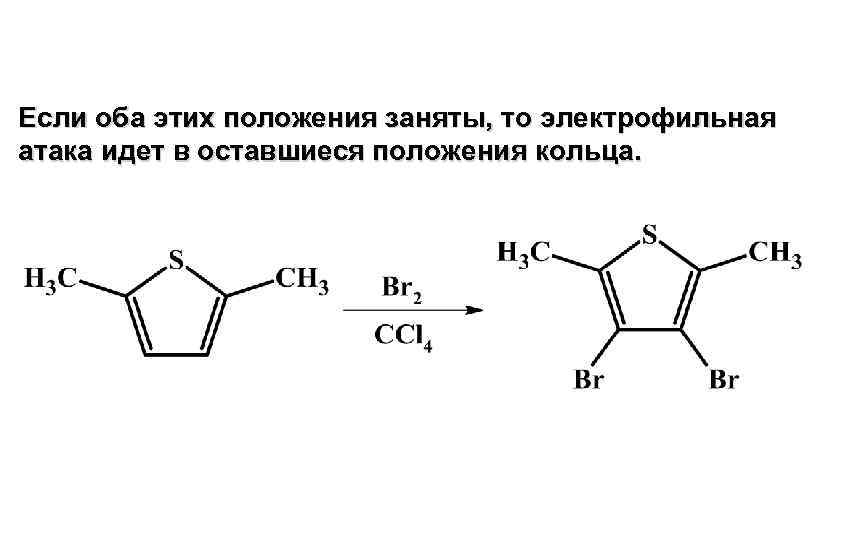 Если оба этих положения заняты, то электрофильная атака идет в оставшиеся положения кольца.
Если оба этих положения заняты, то электрофильная атака идет в оставшиеся положения кольца.
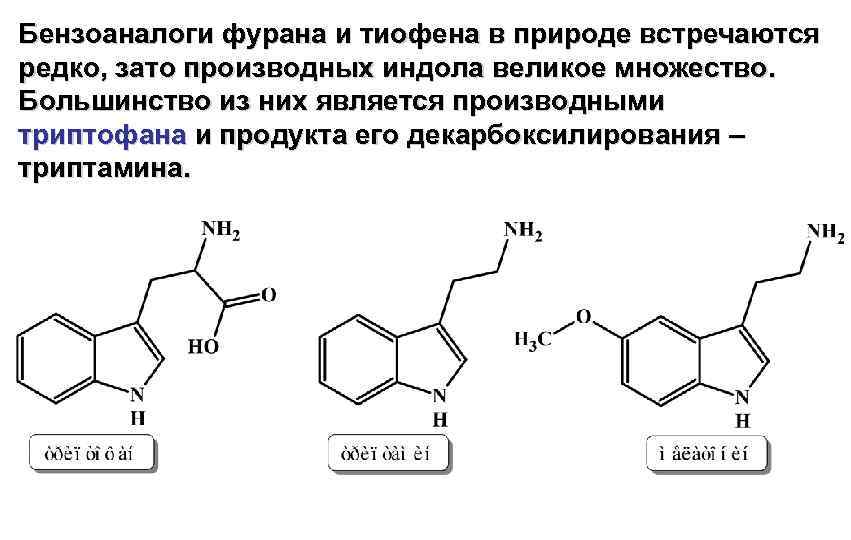 Бензоаналоги фурана и тиофена в природе встречаются редко, зато производных индола великое множество. Большинство из них является производными триптофана и продукта его декарбоксилирования – триптамина.
Бензоаналоги фурана и тиофена в природе встречаются редко, зато производных индола великое множество. Большинство из них является производными триптофана и продукта его декарбоксилирования – триптамина.
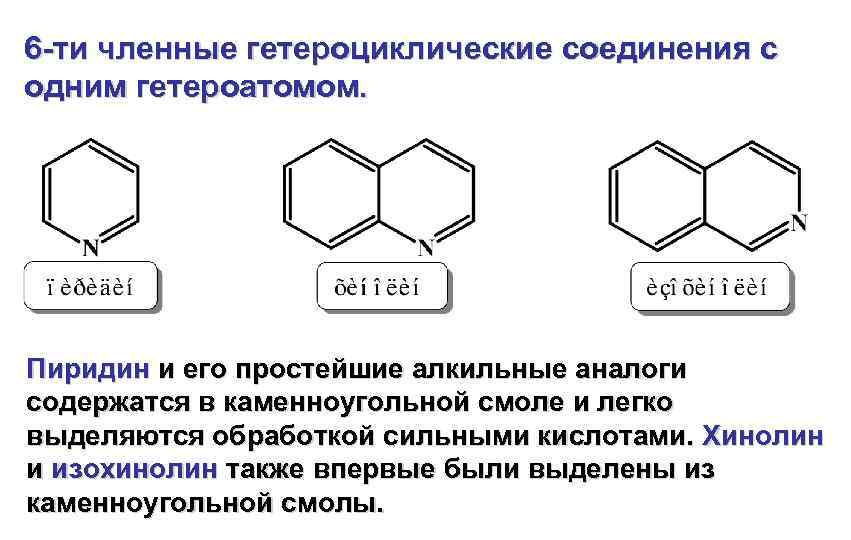 6 -ти членные гетероциклические соединения с одним гетероатомом. Пиридин и его простейшие алкильные аналоги содержатся в каменноугольной смоле и легко выделяются обработкой сильными кислотами. Хинолин и изохинолин также впервые были выделены из каменноугольной смолы.
6 -ти членные гетероциклические соединения с одним гетероатомом. Пиридин и его простейшие алкильные аналоги содержатся в каменноугольной смоле и легко выделяются обработкой сильными кислотами. Хинолин и изохинолин также впервые были выделены из каменноугольной смолы.
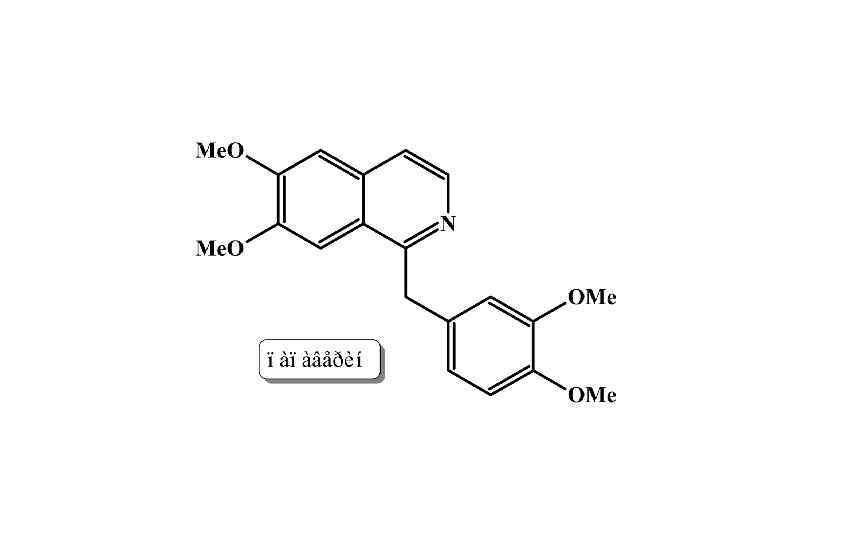
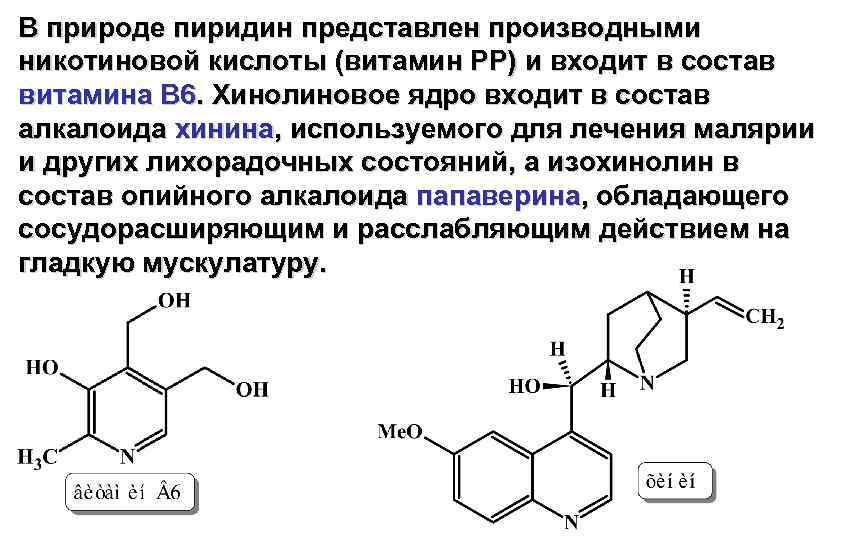 В природе пиридин представлен производными никотиновой кислоты (витамин РР) и входит в состав витамина В 6. Хинолиновое ядро входит в состав алкалоида хинина, используемого для лечения малярии и других лихорадочных состояний, а изохинолин в состав опийного алкалоида папаверина, обладающего сосудорасширяющим и расслабляющим действием на гладкую мускулатуру.
В природе пиридин представлен производными никотиновой кислоты (витамин РР) и входит в состав витамина В 6. Хинолиновое ядро входит в состав алкалоида хинина, используемого для лечения малярии и других лихорадочных состояний, а изохинолин в состав опийного алкалоида папаверина, обладающего сосудорасширяющим и расслабляющим действием на гладкую мускулатуру.
 Производные пиридина и хинолина, в которых неподеленная пара азота не участвует в сопряжении, за счет высокой электро-отрицательности атома азота оказываются обедненными электронной плотностью. В связи с этим, Пиридин очень медленно и в очень жестких условиях вступает в реакции электрофильного замещения. В основном, электрофильное замещение в пиридиновом ядре протекает по 3 -му положению кольца. Хинолин реагирует с электрофилами только по бензольному кольцу, причем азот соседнего кольца играет роль заместителя II-го рода с соответствующим направлением электрофильной атаки. Так же как и в случае ароматических соединений содержащих акцепторные группы, пиридин не алкилируется и не ацилируется по Фриделю-Крафтсу.
Производные пиридина и хинолина, в которых неподеленная пара азота не участвует в сопряжении, за счет высокой электро-отрицательности атома азота оказываются обедненными электронной плотностью. В связи с этим, Пиридин очень медленно и в очень жестких условиях вступает в реакции электрофильного замещения. В основном, электрофильное замещение в пиридиновом ядре протекает по 3 -му положению кольца. Хинолин реагирует с электрофилами только по бензольному кольцу, причем азот соседнего кольца играет роль заместителя II-го рода с соответствующим направлением электрофильной атаки. Так же как и в случае ароматических соединений содержащих акцепторные группы, пиридин не алкилируется и не ацилируется по Фриделю-Крафтсу.
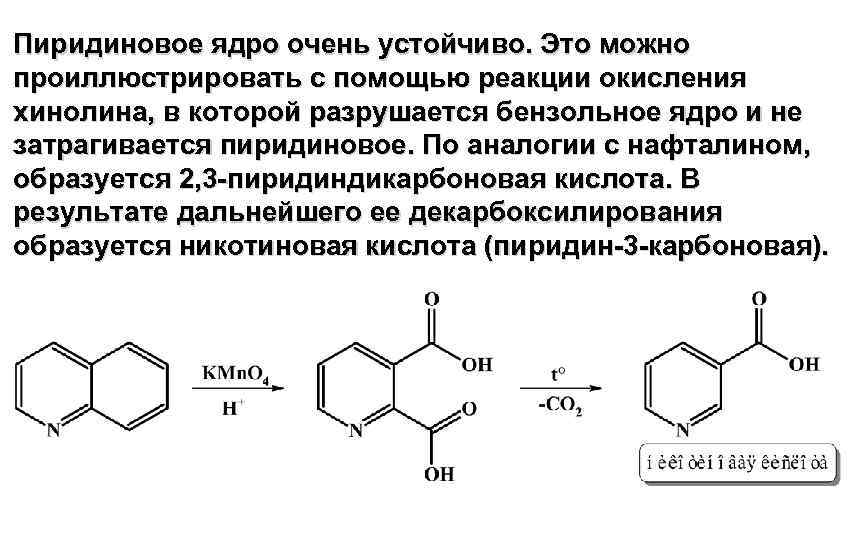 Пиридиновое ядро очень устойчиво. Это можно проиллюстрировать с помощью реакции окисления хинолина, в которой разрушается бензольное ядро и не затрагивается пиридиновое. По аналогии с нафталином, образуется 2, 3 -пиридиндикарбоновая кислота. В результате дальнейшего ее декарбоксилирования образуется никотиновая кислота (пиридин-3 -карбоновая).
Пиридиновое ядро очень устойчиво. Это можно проиллюстрировать с помощью реакции окисления хинолина, в которой разрушается бензольное ядро и не затрагивается пиридиновое. По аналогии с нафталином, образуется 2, 3 -пиридиндикарбоновая кислота. В результате дальнейшего ее декарбоксилирования образуется никотиновая кислота (пиридин-3 -карбоновая).
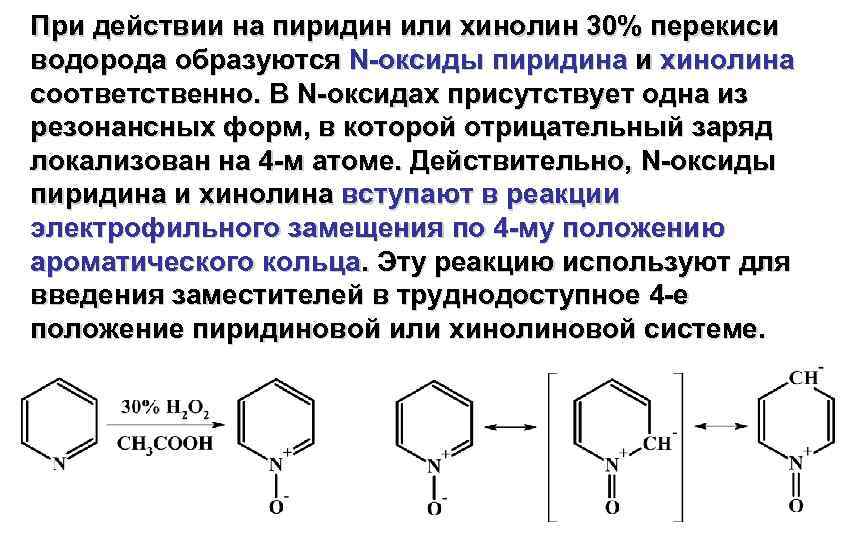 При действии на пиридин или хинолин 30% перекиси водорода образуются N-оксиды пиридина и хинолина соответственно. В N-оксидах присутствует одна из резонансных форм, в которой отрицательный заряд локализован на 4 -м атоме. Действительно, N-оксиды пиридина и хинолина вступают в реакции электрофильного замещения по 4 -му положению ароматического кольца. Эту реакцию используют для введения заместителей в труднодоступное 4 -е положение пиридиновой или хинолиновой системе.
При действии на пиридин или хинолин 30% перекиси водорода образуются N-оксиды пиридина и хинолина соответственно. В N-оксидах присутствует одна из резонансных форм, в которой отрицательный заряд локализован на 4 -м атоме. Действительно, N-оксиды пиридина и хинолина вступают в реакции электрофильного замещения по 4 -му положению ароматического кольца. Эту реакцию используют для введения заместителей в труднодоступное 4 -е положение пиридиновой или хинолиновой системе.
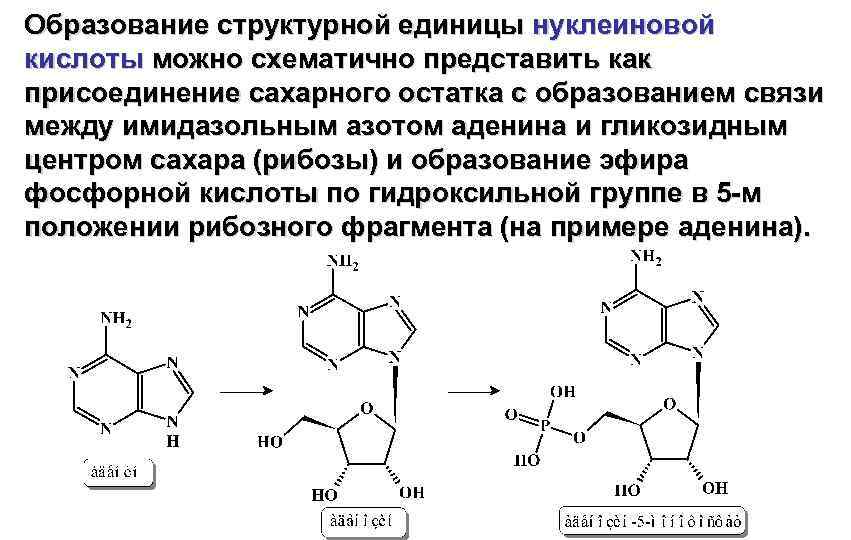 Образование структурной единицы нуклеиновой кислоты можно схематично представить как присоединение сахарного остатка с образованием связи между имидазольным азотом аденина и гликозидным центром сахара (рибозы) и образование эфира фосфорной кислоты по гидроксильной группе в 5 -м положении рибозного фрагмента (на примере аденина).
Образование структурной единицы нуклеиновой кислоты можно схематично представить как присоединение сахарного остатка с образованием связи между имидазольным азотом аденина и гликозидным центром сахара (рибозы) и образование эфира фосфорной кислоты по гидроксильной группе в 5 -м положении рибозного фрагмента (на примере аденина).
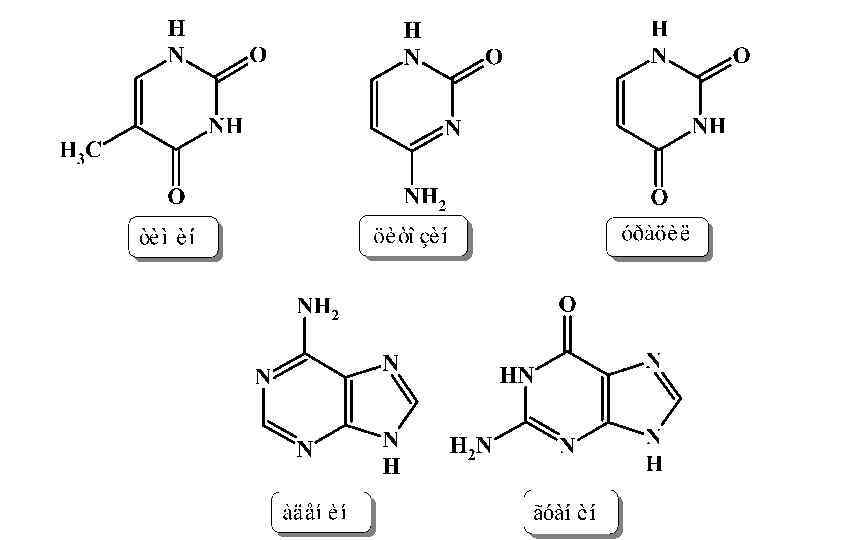
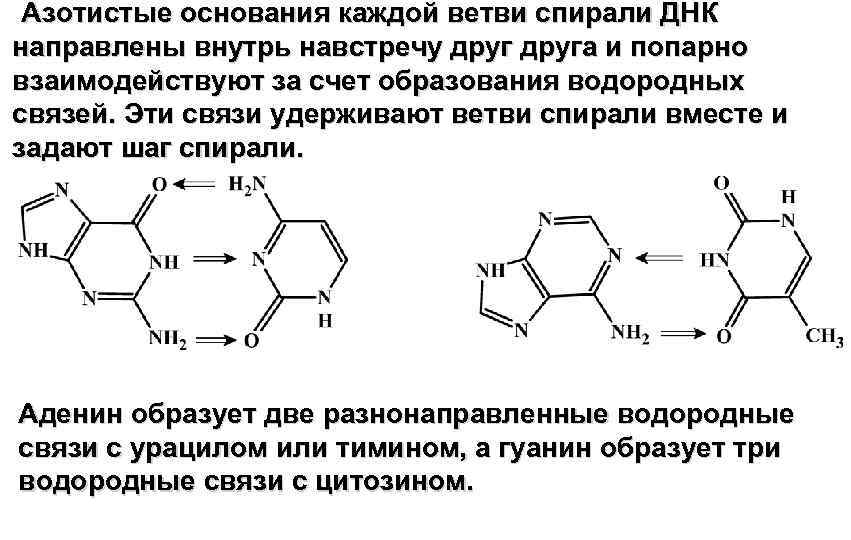 Азотистые основания каждой ветви спирали ДНК направлены внутрь навстречу друга и попарно взаимодействуют за счет образования водородных связей. Эти связи удерживают ветви спирали вместе и задают шаг спирали. Аденин образует две разнонаправленные водородные связи с урацилом или тимином, а гуанин образует три водородные связи с цитозином.
Азотистые основания каждой ветви спирали ДНК направлены внутрь навстречу друга и попарно взаимодействуют за счет образования водородных связей. Эти связи удерживают ветви спирали вместе и задают шаг спирали. Аденин образует две разнонаправленные водородные связи с урацилом или тимином, а гуанин образует три водородные связи с цитозином.
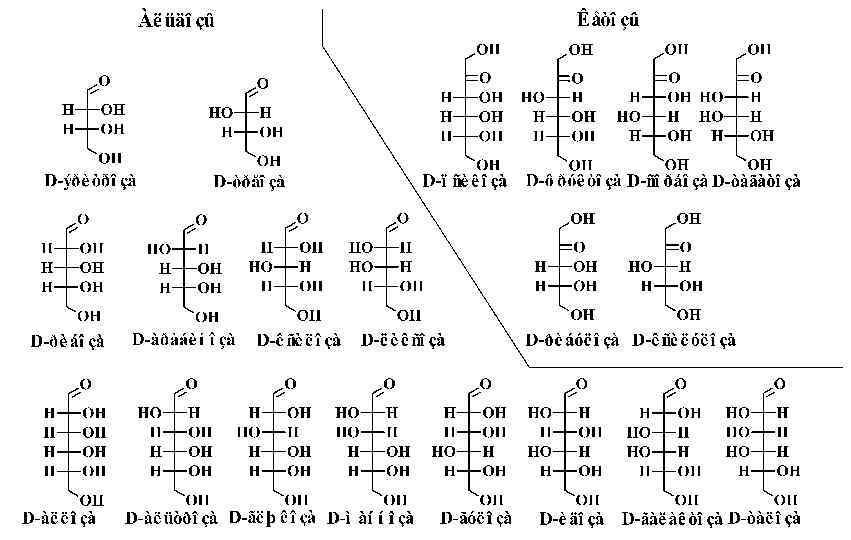
 Сахара (углеводы) Номенклатура сахаров. В систематической номенклатуре для обозначения принадлежности молекулы к классу сахаров используют окончание -оза. Однако, сами названия в основном тривиальные. Сахара (углеводы) подразделяются по количеству атомов углерода в цепи (треозы, тетрозы, пентозы, гексозы и т. д. ), по наличию альдегидной или кетонной функции (альдозы и кетозы), по размеру цикла в циклических формах (фуранозы – пятичленный цикл и пиранозы – шестичленный цикл), а также по количеству сахарных остатков в молекуле (моносахариды, олигосахариды и полисахариды).
Сахара (углеводы) Номенклатура сахаров. В систематической номенклатуре для обозначения принадлежности молекулы к классу сахаров используют окончание -оза. Однако, сами названия в основном тривиальные. Сахара (углеводы) подразделяются по количеству атомов углерода в цепи (треозы, тетрозы, пентозы, гексозы и т. д. ), по наличию альдегидной или кетонной функции (альдозы и кетозы), по размеру цикла в циклических формах (фуранозы – пятичленный цикл и пиранозы – шестичленный цикл), а также по количеству сахарных остатков в молекуле (моносахариды, олигосахариды и полисахариды).
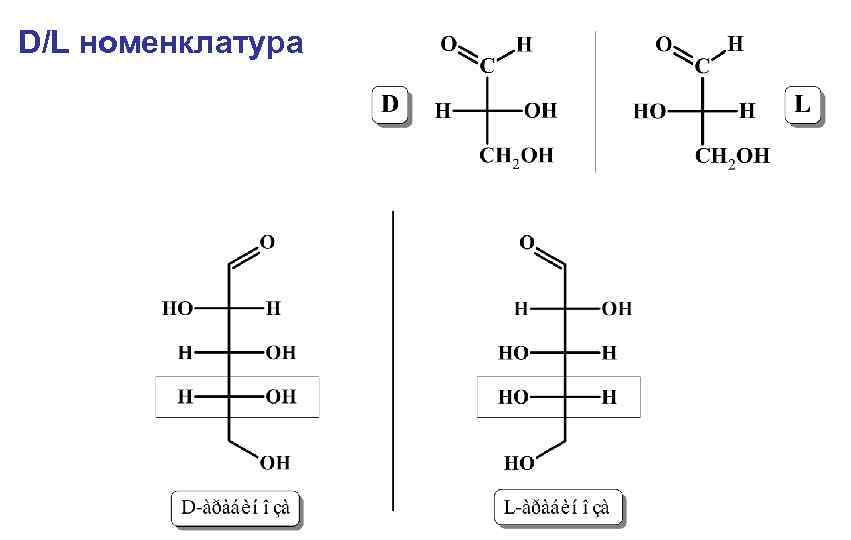 D/L номенклатура
D/L номенклатура
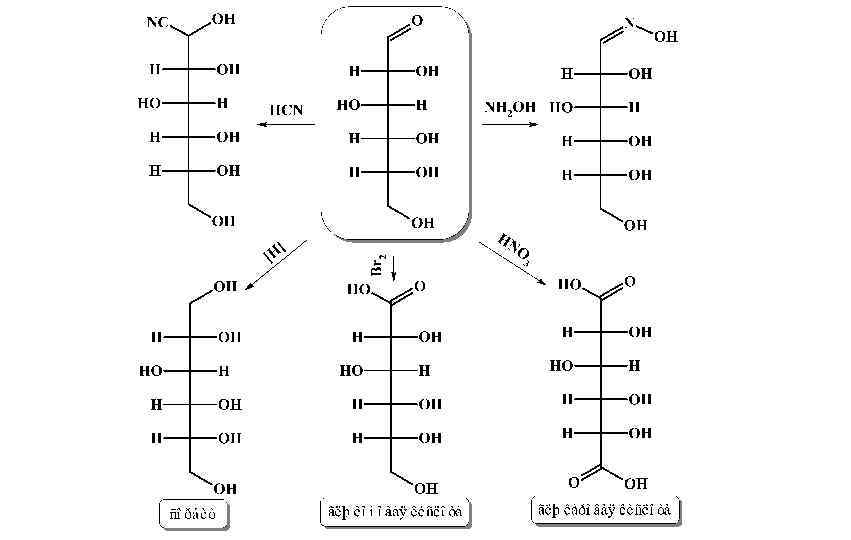
 Химические свойства моносахаридов. Свойства сахаров обусловлены спиртовыми и карбонильной функциональными группами. Большинство химических реакций связано с модификацией этих групп или нуклеофильным замещением гидроксилов. Однако не следует рассматривать эти группы в отдельности, ибо их взаимное влияние сильно меняет химические свойства сахаров по сравнению с монофункциональными соединениями. Для пространственного представления этих структур часто используют проекции Хеуорса, в которых цикл представляется плоским, а заместители направлены вертикально вверх или вниз. Проекция Хеуорса, по сути, является проекцией Фишера свернутой в кольцо.
Химические свойства моносахаридов. Свойства сахаров обусловлены спиртовыми и карбонильной функциональными группами. Большинство химических реакций связано с модификацией этих групп или нуклеофильным замещением гидроксилов. Однако не следует рассматривать эти группы в отдельности, ибо их взаимное влияние сильно меняет химические свойства сахаров по сравнению с монофункциональными соединениями. Для пространственного представления этих структур часто используют проекции Хеуорса, в которых цикл представляется плоским, а заместители направлены вертикально вверх или вниз. Проекция Хеуорса, по сути, является проекцией Фишера свернутой в кольцо.
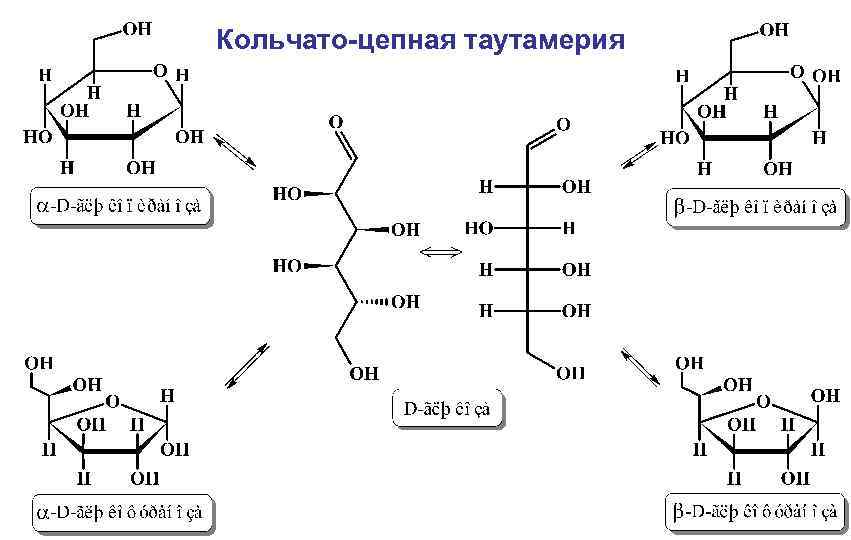 Кольчато-цепная таутамерия
Кольчато-цепная таутамерия
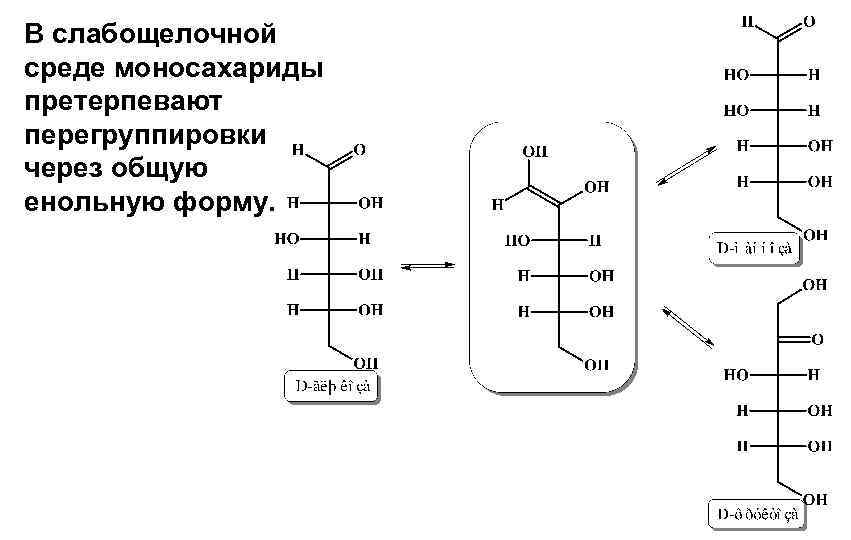 В слабощелочной среде моносахариды претерпевают перегруппировки через общую енольную форму.
В слабощелочной среде моносахариды претерпевают перегруппировки через общую енольную форму.
 В слабощелочном растворе D-глюкозы устанавливается равновесие, где основным продуктом является D-глюкоза – 69%, 29% D-фруктозы и 3% Dманнозы. В кислой среде моносахариды достаточно стабильны, но при нагревании способны отщеплять воду (дегидратироваться) с образованием производных фурана. Аналогичные процессы, правда, с низкими выходами протекают при термолизе сахаров. Альдопентозы при нагревании или обработке кислотами отщепляют три молекулы воды с образованием фурфурола, а альдогексозы – 5 -замещенного фурфурола.
В слабощелочном растворе D-глюкозы устанавливается равновесие, где основным продуктом является D-глюкоза – 69%, 29% D-фруктозы и 3% Dманнозы. В кислой среде моносахариды достаточно стабильны, но при нагревании способны отщеплять воду (дегидратироваться) с образованием производных фурана. Аналогичные процессы, правда, с низкими выходами протекают при термолизе сахаров. Альдопентозы при нагревании или обработке кислотами отщепляют три молекулы воды с образованием фурфурола, а альдогексозы – 5 -замещенного фурфурола.
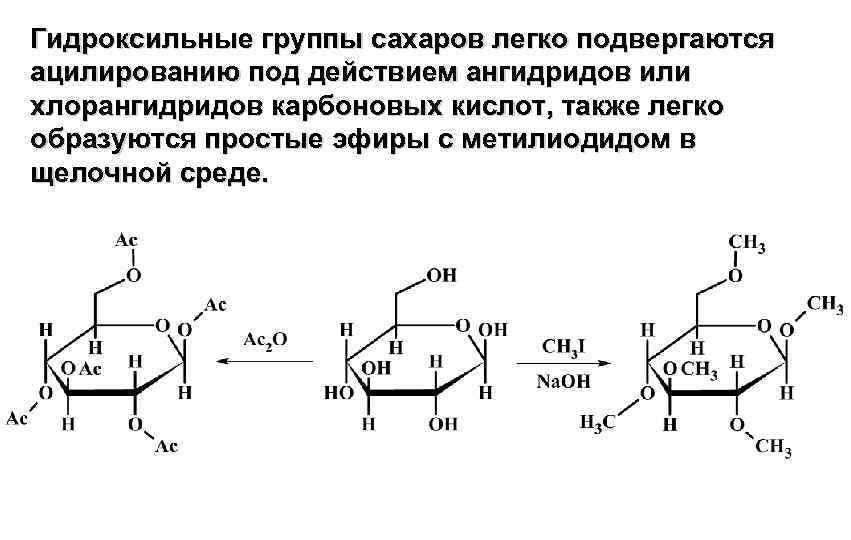 Гидроксильные группы сахаров легко подвергаются ацилированию под действием ангидридов или хлорангидридов карбоновых кислот, также легко образуются простые эфиры с метилиодидом в щелочной среде.
Гидроксильные группы сахаров легко подвергаются ацилированию под действием ангидридов или хлорангидридов карбоновых кислот, также легко образуются простые эфиры с метилиодидом в щелочной среде.