2010_LYeKTsIYa_12_AZOT.ppt
- Количество слайдов: 30
 ЛЕКЦИЯ 12 Элементы подгруппы азота
ЛЕКЦИЯ 12 Элементы подгруппы азота
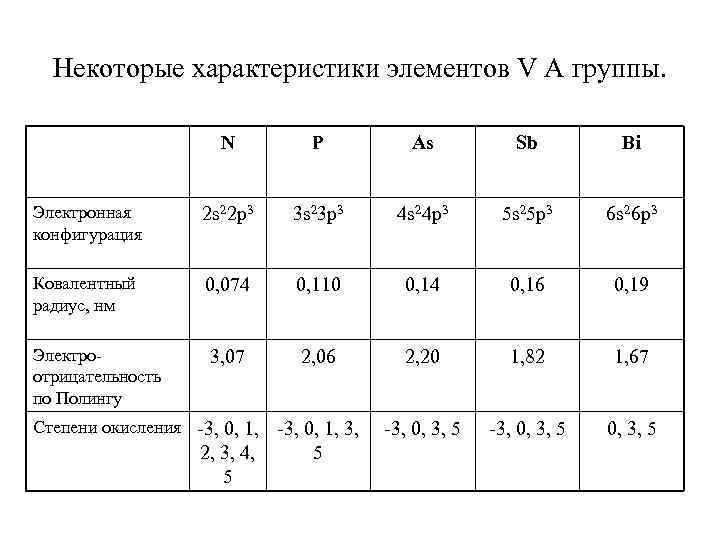 Некоторые характеристики элементов V А группы. N P As Sb Bi Электронная конфигурация 2 s 22 p 3 3 s 23 p 3 4 s 24 p 3 5 s 25 p 3 6 s 26 p 3 Ковалентный радиус, нм 0, 074 0, 110 0, 14 0, 16 0, 19 Электроотрицательность по Полингу 3, 07 2, 06 2, 20 1, 82 1, 67 -3, 0, 1, 3, 5 -3, 0, 3, 5 Степени окисления -3, 0, 1, 2, 3, 4, 5
Некоторые характеристики элементов V А группы. N P As Sb Bi Электронная конфигурация 2 s 22 p 3 3 s 23 p 3 4 s 24 p 3 5 s 25 p 3 6 s 26 p 3 Ковалентный радиус, нм 0, 074 0, 110 0, 14 0, 16 0, 19 Электроотрицательность по Полингу 3, 07 2, 06 2, 20 1, 82 1, 67 -3, 0, 1, 3, 5 -3, 0, 3, 5 Степени окисления -3, 0, 1, 2, 3, 4, 5
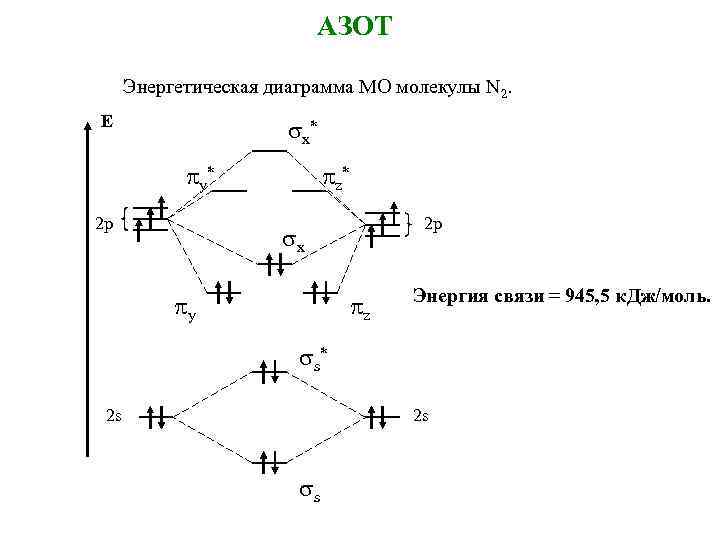 АЗОТ Энергетическая диаграмма МО молекулы N 2. E s x* p y* 2 p p z* 2 p sx py pz Энергия связи = 945, 5 к. Дж/моль. ss * 2 s 2 s ss
АЗОТ Энергетическая диаграмма МО молекулы N 2. E s x* p y* 2 p p z* 2 p sx py pz Энергия связи = 945, 5 к. Дж/моль. ss * 2 s 2 s ss
 СВОЙСТВА АЗОТА.
СВОЙСТВА АЗОТА.
 Получение азота. Промышленный способ – сжижение и последующая фракционная перегонка воздуха. Лабораторный способ –
Получение азота. Промышленный способ – сжижение и последующая фракционная перегонка воздуха. Лабораторный способ –
 Аммиак и соли аммония. Промышленный способ получения аммиака: Лабораторный способ получения аммиака:
Аммиак и соли аммония. Промышленный способ получения аммиака: Лабораторный способ получения аммиака:
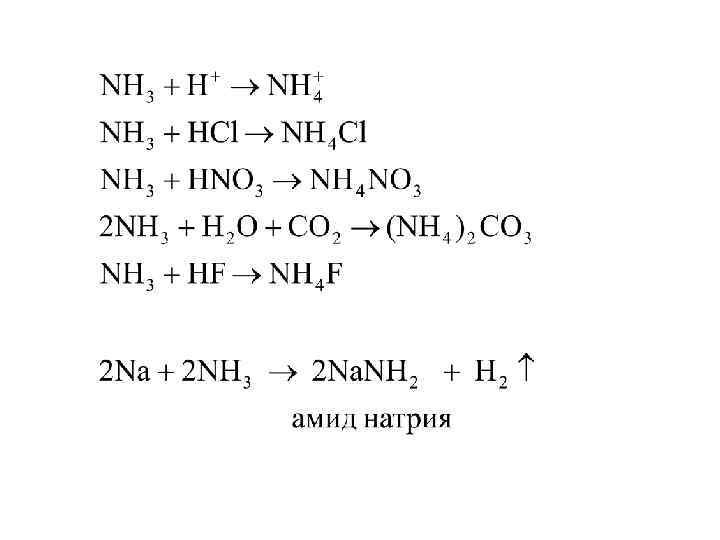
 ХИМИЧЕСКИЕ СВОЙСТВА АММИАКА.
ХИМИЧЕСКИЕ СВОЙСТВА АММИАКА.
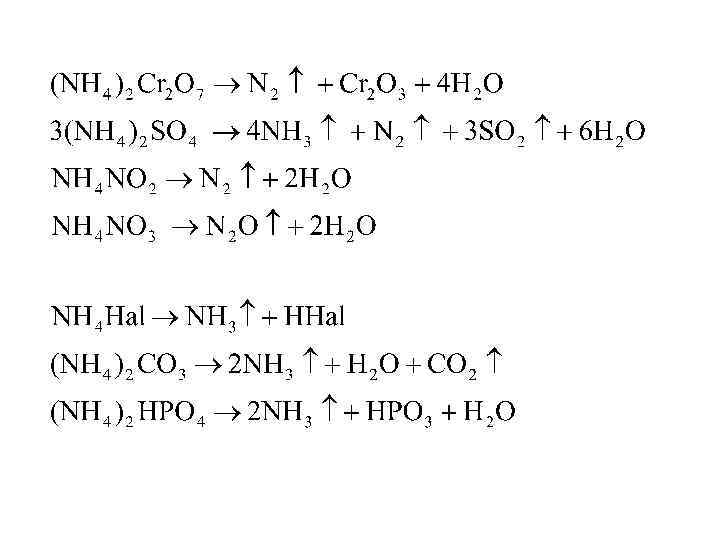

 КИСЛОРОДНЫЕ СОЕДИНЕНИЯ АЗОТА. Азот образует с кислородом кислотные оксиды N 2 O 3 и N 2 O 5 и безразличные оксиды N 2 O, NO 2.
КИСЛОРОДНЫЕ СОЕДИНЕНИЯ АЗОТА. Азот образует с кислородом кислотные оксиды N 2 O 3 и N 2 O 5 и безразличные оксиды N 2 O, NO 2.
 Оксид азота (I) или закись азота N 2 O – «веселящий газ» . Получение: термолиз нитрата аммония NH 4 NO 3 →N 2 O + 2 H 2 O Химические свойства N 2 O 2 N 2 O + C → CO 2 + 2 N 2 5 N 2 O + 2 P → P 2 O 5 + 5 N 2 N 2 O + Mg → Mg. O + N 2
Оксид азота (I) или закись азота N 2 O – «веселящий газ» . Получение: термолиз нитрата аммония NH 4 NO 3 →N 2 O + 2 H 2 O Химические свойства N 2 O 2 N 2 O + C → CO 2 + 2 N 2 5 N 2 O + 2 P → P 2 O 5 + 5 N 2 N 2 O + Mg → Mg. O + N 2
 Оксид азота (II), окись азота NO Бесцветный ядовитый газ. NO - и окислитель, и восстановитель. Восстановительные свойства. 2 NO + O 2 → 2 NO 2 2 NO + K 2 Cr 2 O 7 + 4 H 2 SO 4 → 2 HNO 3 + Cr 2(SO 4)3 + K 2 SO 4 + 3 H 2 O Окислительные свойства. 4 P + 10 NO → 2 P 2 O 5 + 5 N 2 2 H 2 + 2 NO → N 2 + 2 H 2 O
Оксид азота (II), окись азота NO Бесцветный ядовитый газ. NO - и окислитель, и восстановитель. Восстановительные свойства. 2 NO + O 2 → 2 NO 2 2 NO + K 2 Cr 2 O 7 + 4 H 2 SO 4 → 2 HNO 3 + Cr 2(SO 4)3 + K 2 SO 4 + 3 H 2 O Окислительные свойства. 4 P + 10 NO → 2 P 2 O 5 + 5 N 2 2 H 2 + 2 NO → N 2 + 2 H 2 O
 Получение NO. Промышленный способ: «Горение воздуха» - при температуре выше 10000 С: По этой реакции NO образуется при электрических разрядах во время грозы.
Получение NO. Промышленный способ: «Горение воздуха» - при температуре выше 10000 С: По этой реакции NO образуется при электрических разрядах во время грозы.
 Оксид азота (III), триоксид азота, азотистый ангидрид, N 2 O 3. При температуре ниже -40 0 С – жидкость голубого цвета. Получение: NO + NO 2 ↔ N 2 O 3 + 40, 2 к. Дж В холодной воде: N 2 O 3 + H 2 O → 2 HNO 2 азотистая кислота В лаборатории: Na. NO 2 + H 2 SO 4(конц. ) → HNO 2 + KHSO 4 Kд = 6, 9*10 -4 3 HNO 2 → HNO 3 + 2 NO↑ + H 2 O
Оксид азота (III), триоксид азота, азотистый ангидрид, N 2 O 3. При температуре ниже -40 0 С – жидкость голубого цвета. Получение: NO + NO 2 ↔ N 2 O 3 + 40, 2 к. Дж В холодной воде: N 2 O 3 + H 2 O → 2 HNO 2 азотистая кислота В лаборатории: Na. NO 2 + H 2 SO 4(конц. ) → HNO 2 + KHSO 4 Kд = 6, 9*10 -4 3 HNO 2 → HNO 3 + 2 NO↑ + H 2 O
 Химические свойства N 2 O 3 и HNO 2. N 2 O 3 + 2 Na. OH → 2 Na. NO 2 + H 2 O HNO 2 + Na. OH → Na. NO 2 + H 2 O 2 HNO 2 + 2 KI + H 2 SO 4 → K 2 SO 4 + I 2 + 2 NO↑ + 2 H 2 O HNO 2 + Br 2 + H 20 → HNO 3 + 2 HBr
Химические свойства N 2 O 3 и HNO 2. N 2 O 3 + 2 Na. OH → 2 Na. NO 2 + H 2 O HNO 2 + Na. OH → Na. NO 2 + H 2 O 2 HNO 2 + 2 KI + H 2 SO 4 → K 2 SO 4 + I 2 + 2 NO↑ + 2 H 2 O HNO 2 + Br 2 + H 20 → HNO 3 + 2 HBr
 Оксид азота (IV), диоксид азота, NO 2. При температуре выше 21, 20 С – газ бурого цвета. Безразличный оксид. Получение: 2 NO + O 2 → 2 NO 2 2 Pb(NO 3)2 → 2 Pb. O + 4 NO 2 + O 2 Cu + 4 HNO 3(конц. ) → Cu(NO 3)2 + 2 NO 2↑ + 2 H 2 O Химические свойства. 2 NO 2 + H 2 O → HNO 2 + HNO 3
Оксид азота (IV), диоксид азота, NO 2. При температуре выше 21, 20 С – газ бурого цвета. Безразличный оксид. Получение: 2 NO + O 2 → 2 NO 2 2 Pb(NO 3)2 → 2 Pb. O + 4 NO 2 + O 2 Cu + 4 HNO 3(конц. ) → Cu(NO 3)2 + 2 NO 2↑ + 2 H 2 O Химические свойства. 2 NO 2 + H 2 O → HNO 2 + HNO 3
 Окислительные свойства NO 2. 8 P + 10 NO 2 → 2 P 4 O 10 + 5 N 2 2 C + 2 NO 2 → 2 CO 2 + N 2 Восстановительные свойства NO 2. 4 NO 2 + 2 H 2 O → 4 HNO 3
Окислительные свойства NO 2. 8 P + 10 NO 2 → 2 P 4 O 10 + 5 N 2 2 C + 2 NO 2 → 2 CO 2 + N 2 Восстановительные свойства NO 2. 4 NO 2 + 2 H 2 O → 4 HNO 3
 Оксид азота (V), пентоксид азота, азотный ангидрид N 2 O 5. Белое твердое вещество. Получение: 2 HNO 3 + P 2 O 5 → N 2 O 5 + 2 HPO 3 2 NO 2 + O 3 → N 2 O 5 + O 2 2 N 2 O 5 → 4 NO 2 + O 2 N 2 O 5 – сильный окислитель. N 2 O 5 + I 2 → I 2 O 5 + N 2 O 5 + H 2 O→ 2 HNO 3
Оксид азота (V), пентоксид азота, азотный ангидрид N 2 O 5. Белое твердое вещество. Получение: 2 HNO 3 + P 2 O 5 → N 2 O 5 + 2 HPO 3 2 NO 2 + O 3 → N 2 O 5 + O 2 2 N 2 O 5 → 4 NO 2 + O 2 N 2 O 5 – сильный окислитель. N 2 O 5 + I 2 → I 2 O 5 + N 2 O 5 + H 2 O→ 2 HNO 3
 Азотная кислота HNO 3. Чистая азотная кислота HNO 3 – бесцветная летучая жидкость с Ткип. = 84 0 С. Химические свойства HNO 3 + + NO HNO 3 → H 3 4 HNO 3(конц. ) → 4 NO 2 + 2 H 2 O Соли азотной кислоты – нитраты. Mg(OH)2 + 2 HNO 3 → Mg(NO 3)2 + 2 H 2 O Mg. O + 2 HNO 3 → Mg(NO 3)2 + H 2 O NH 3 + HNO 3 → NH 4 NO 3
Азотная кислота HNO 3. Чистая азотная кислота HNO 3 – бесцветная летучая жидкость с Ткип. = 84 0 С. Химические свойства HNO 3 + + NO HNO 3 → H 3 4 HNO 3(конц. ) → 4 NO 2 + 2 H 2 O Соли азотной кислоты – нитраты. Mg(OH)2 + 2 HNO 3 → Mg(NO 3)2 + 2 H 2 O Mg. O + 2 HNO 3 → Mg(NO 3)2 + H 2 O NH 3 + HNO 3 → NH 4 NO 3
 Свойства нитратов. 2 Na. NO 3 → 2 Na. NO 2 + O 2 2 Pb(NO 3)2 → Pb. O + 4 NO 2 + O 2 Hg(NO 3)2 → O 2 + 2 NO 2 + Hg 2 KNO 3 + S + 3 C → K 2 S + N 2 + 3 CO 2 + 615 к. Дж
Свойства нитратов. 2 Na. NO 3 → 2 Na. NO 2 + O 2 2 Pb(NO 3)2 → Pb. O + 4 NO 2 + O 2 Hg(NO 3)2 → O 2 + 2 NO 2 + Hg 2 KNO 3 + S + 3 C → K 2 S + N 2 + 3 CO 2 + 615 к. Дж
 Свойства азотной кислоты. Fe + 6 HNO 3 → Fe(NO 3)3 + 3 NO 2↑ + 3 H 2 O Fe + 4 HNO 3 → Fe(NO 3)3 + NO↑ + 2 H 2 O 8 Fe + 30 HNO 3 → 8 Fe(NO 3)3 + 3 NH 4 NO 3 + 9 H 2 O Au + HNO 3 +4 HCl → H[Au. Cl 4] + NO + 2 H 2 O 3 P + 5 HNO 3 + 2 H 2 O → 5 NO + 3 H 3 PO 4 S + 6 HNO 3 → H 2 SO 4 + 6 NO 2 + 2 H 2 O
Свойства азотной кислоты. Fe + 6 HNO 3 → Fe(NO 3)3 + 3 NO 2↑ + 3 H 2 O Fe + 4 HNO 3 → Fe(NO 3)3 + NO↑ + 2 H 2 O 8 Fe + 30 HNO 3 → 8 Fe(NO 3)3 + 3 NH 4 NO 3 + 9 H 2 O Au + HNO 3 +4 HCl → H[Au. Cl 4] + NO + 2 H 2 O 3 P + 5 HNO 3 + 2 H 2 O → 5 NO + 3 H 3 PO 4 S + 6 HNO 3 → H 2 SO 4 + 6 NO 2 + 2 H 2 O
 Получение азотной кислоты.
Получение азотной кислоты.
 ФОСФОР Р (белый) → Р (красный); ∆Но 298 = -18, 41 к. Дж Переход возможен при хранении в обычных условиях и ускоряется при нагревании или на свету. Р (белый) → Р (черный); Т – 200 0 С, р = 12000 атм. ∆Но 298 = -42, 0 к. Дж
ФОСФОР Р (белый) → Р (красный); ∆Но 298 = -18, 41 к. Дж Переход возможен при хранении в обычных условиях и ускоряется при нагревании или на свету. Р (белый) → Р (черный); Т – 200 0 С, р = 12000 атм. ∆Но 298 = -42, 0 к. Дж
 Химические свойства фосфора. Р 4 + 3 О 2 → Р 4 О 6 + 2 О 2 → Р 4 О 10 2 Р + 3 Наl 2 → 2 PHal 3 + Hal 2 → PHal 5 2 P + 3 S → P 2 S 3 + 2 S → P 2 S 5 3 P + 5 HNO 3 + 2 H 2 O → 3 H 3 PO 4 + 5 NO↑ 3 Na + P → Na 3 P- фосфид натрия Ca 3 P 2 + 6 H 2 O → 3 Ca(OH)2 + 2 PH 3 ↑
Химические свойства фосфора. Р 4 + 3 О 2 → Р 4 О 6 + 2 О 2 → Р 4 О 10 2 Р + 3 Наl 2 → 2 PHal 3 + Hal 2 → PHal 5 2 P + 3 S → P 2 S 3 + 2 S → P 2 S 5 3 P + 5 HNO 3 + 2 H 2 O → 3 H 3 PO 4 + 5 NO↑ 3 Na + P → Na 3 P- фосфид натрия Ca 3 P 2 + 6 H 2 O → 3 Ca(OH)2 + 2 PH 3 ↑
 Получение фосфора. 2 Ca 3(PO 4)2 + 10 C + 6 Si. O 2 → 6 Ca. Si. O 3 + 10 CO + P 4 ВОДОРОДНЫЕ СОЕДИНЕНИЯ ФОСФОРА. Самый устойчивый гидрид фосфора – фосфин РН 3. Это слабое основание. РН 3, г + HIг →PH 4 Iк РН 3 + HCl. O 4 → PH 4 Cl. O 4 РН 3 + 2 O 2 → HPO 3 + H 2 O
Получение фосфора. 2 Ca 3(PO 4)2 + 10 C + 6 Si. O 2 → 6 Ca. Si. O 3 + 10 CO + P 4 ВОДОРОДНЫЕ СОЕДИНЕНИЯ ФОСФОРА. Самый устойчивый гидрид фосфора – фосфин РН 3. Это слабое основание. РН 3, г + HIг →PH 4 Iк РН 3 + HCl. O 4 → PH 4 Cl. O 4 РН 3 + 2 O 2 → HPO 3 + H 2 O
 Кислородные соединения фосфора. Оксид фосфора (III), фосфористый ангидрид, P 4 O 6. Белое кристаллическое вещество, очень ядовитое. P 4 O 6 - кислотный оксид. P 4 O 6 + 6 Н 2 О → 4 Н 3 РО 3 – фосфористая кислота. 2 Na. OH + H 2 PO 3 H → Na 2 PO 3 H + 2 H 2 O Na. OH + H 2 PO 3 H → Na. HPO 3 H + H 2 O
Кислородные соединения фосфора. Оксид фосфора (III), фосфористый ангидрид, P 4 O 6. Белое кристаллическое вещество, очень ядовитое. P 4 O 6 - кислотный оксид. P 4 O 6 + 6 Н 2 О → 4 Н 3 РО 3 – фосфористая кислота. 2 Na. OH + H 2 PO 3 H → Na 2 PO 3 H + 2 H 2 O Na. OH + H 2 PO 3 H → Na. HPO 3 H + H 2 O
 Оксид фосфора (V), фосфорный ангидрид, пентоксид фосфора, Р 4 О 10. Белое кристаллическое вещество. Р 4 О 10 + 4 HCl. O 4 → 2 Cl 2 O 7 + 4 HPO 3 P 4 O 10 +2 H 2 O → (HPO 3)4 – циклическое строение. (HPO 3)4 + Н 2 О → Н 6 Р 4 О 13 – тетраполифосфорная кислота Н 6 Р 4 О 13 + Н 2 О → Н 3 РО 4 + Н 5 Р 3 О 10 – триполифосфорная кислота Н 5 Р 3 О 10 + Н 2 О → Н 3 РО 4 + Н 4 Р 2 О 7 – диполифосфорная кислота Н 4 Р 2 О 7 + Н 2 О → 2 Н 3 РО 4 – ортофосфорная кислота
Оксид фосфора (V), фосфорный ангидрид, пентоксид фосфора, Р 4 О 10. Белое кристаллическое вещество. Р 4 О 10 + 4 HCl. O 4 → 2 Cl 2 O 7 + 4 HPO 3 P 4 O 10 +2 H 2 O → (HPO 3)4 – циклическое строение. (HPO 3)4 + Н 2 О → Н 6 Р 4 О 13 – тетраполифосфорная кислота Н 6 Р 4 О 13 + Н 2 О → Н 3 РО 4 + Н 5 Р 3 О 10 – триполифосфорная кислота Н 5 Р 3 О 10 + Н 2 О → Н 3 РО 4 + Н 4 Р 2 О 7 – диполифосфорная кислота Н 4 Р 2 О 7 + Н 2 О → 2 Н 3 РО 4 – ортофосфорная кислота
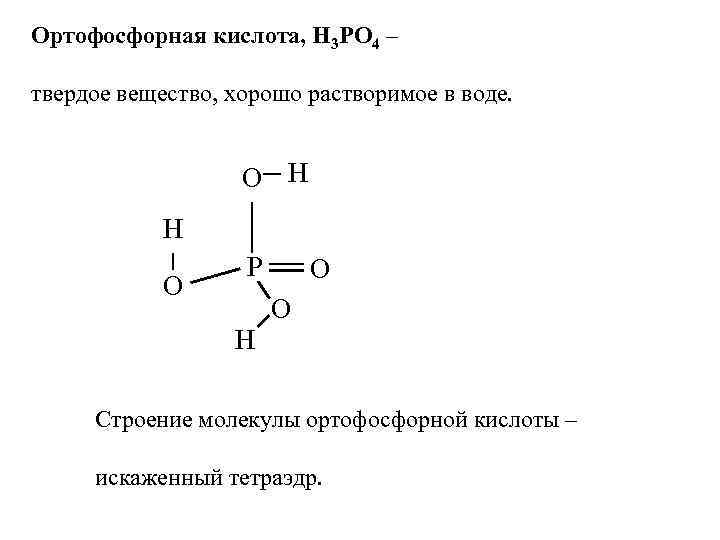 Ортофосфорная кислота, Н 3 РО 4 – твердое вещество, хорошо растворимое в воде. О Н Н О Р О О Н Строение молекулы ортофосфорной кислоты – искаженный тетраэдр.
Ортофосфорная кислота, Н 3 РО 4 – твердое вещество, хорошо растворимое в воде. О Н Н О Р О О Н Строение молекулы ортофосфорной кислоты – искаженный тетраэдр.
 В водных растворах соли ортофосфорной кислоты гидролизуются. Растворимые фосфаты и гидрофосфаты вследствие гидролиза создают в растворах щелочную среду. Дигидрофосфат-ион Н 2 РО 4 - амфолит. К 1 >> К 2 р. Н <7
В водных растворах соли ортофосфорной кислоты гидролизуются. Растворимые фосфаты и гидрофосфаты вследствие гидролиза создают в растворах щелочную среду. Дигидрофосфат-ион Н 2 РО 4 - амфолит. К 1 >> К 2 р. Н <7


