Лекция № 12 Биохимия нуклеиновых кислот. Матричные биосинтезы.


Лекция № 12 Биохимия нуклеиновых кислот. Матричные биосинтезы.

www.themegallery.com План лекции: Структура и функции ДНК (закономерности нуклеотидного состава, структура, гистоны, укладка ДНК в хроматине). Репликация ДНК (механизмы, ферменты). Повреждения ДНК. Репарация повреждений и ошибок репликации (механизы, ферменты). Структура и функции РНК (разновидности, структура). Биосинтез РНК и ее процессинг. Обмен нуклеотидов (состав, биосинтез, катаболизм). Нарушение обмена азотистых оснований (подагра). Биосинтез белков. Аминокислотный код. Этапы трансляции (подготовительный, элонгация, пострибосомная трансформация полипептидной цепи). Ингибиторы трансляции.

1. Структура и функции ДНК (закономерности нуклеотидного состава, структура, гистоны, укладка ДНК в хроматине).

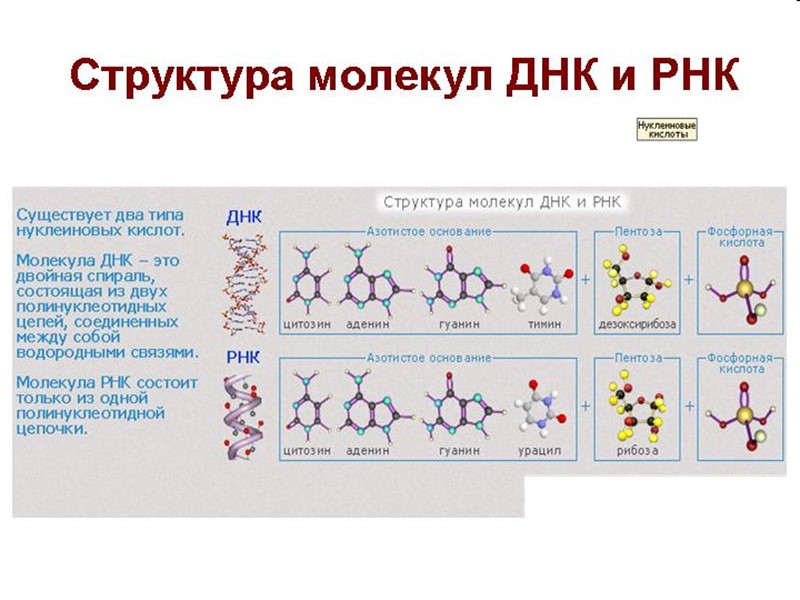
www.themegallery.com РНК и ДНК В клетке имеются два типа нуклеиновых кислот: рибонуклеиновая кислота (РНК) и дезоксирибонуклеиновая кислота (ДНК). И ДНК, и РНК – полимерные цепочки, состоящие из отдельных звеньев – нуклеотидов.

Химическая организация гена А. Строение нуклеозида. Нуклеозиды состоят из азотистых оснований и углевода – пентоза. Название пуриновых нуклеозидов имеют окончание – ОЗИН, а пиримидиновых нуклеозидов окончание – ИДИН. Б. Строение нуклеотидов. Нуклеотиды являются мономерами нуклеиновых кислот они состоят из азотистых оснований углевода – пентоза и фосфорной кислоты. Нуклеотиды хорошо растворимы в воде и обладают кислотными свойствами → нуклеотиды являются кислотами. Разные нуклеотиды отличатся между собой природой углеводов и азотистых оснований.

В. Строение и виды азотистых оснований: Азотистые основания нуклеотидов делятся на 2 типа: 1. Пиримидиновые – они состоят из 1 шестичленного кольца; 2. Пуриновые - состоят из 2 конденсированных 5 и 6-членных колец.
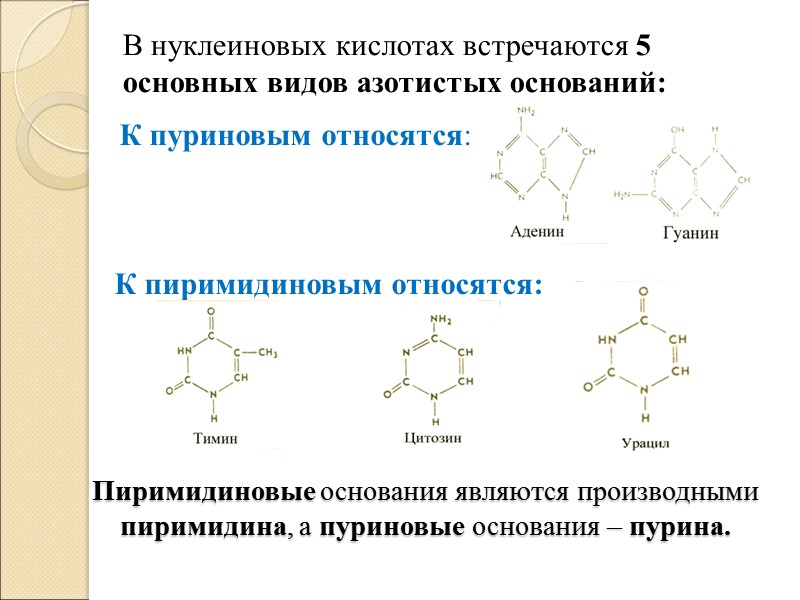
Пиримидиновые основания являются производными пиримидина, а пуриновые основания – пурина. В нуклеиновых кислотах встречаются 5 основных видов азотистых оснований: К пуриновым относятся: К пиримидиновым относятся:
www.themegallery.com
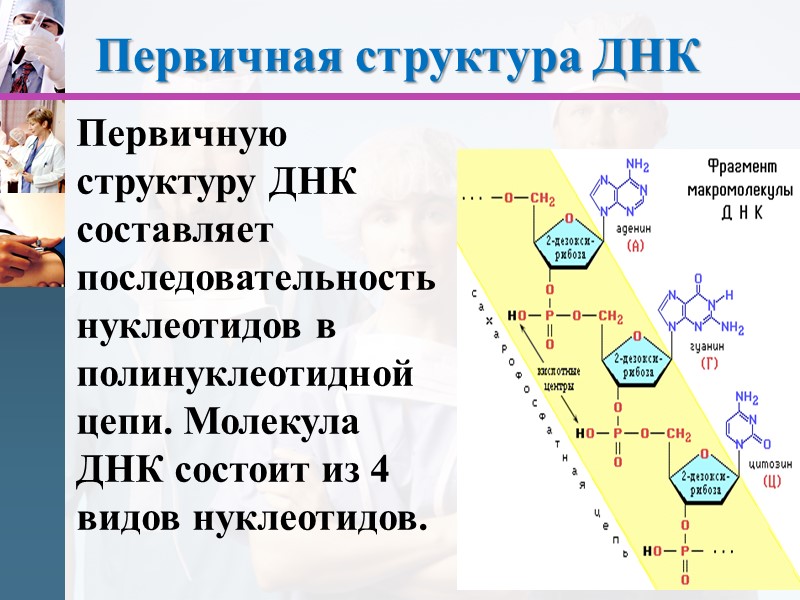
Первичная структура ДНК Первичную структуру ДНК составляет последовательность нуклеотидов в полинуклеотидной цепи. Молекула ДНК состоит из 4 видов нуклеотидов.

Больших успехов в определении структуры ДНКдостигли Эрвин Чаргафф и его сотрудники (1950г.) Используя метод хроматографии, они впервые определили нуклеотидный состав ДНК. Они установили, что соотношение азотистых оснований ДНК подчиняется универсальным. Правила Чаргаффа: 1. Сумма пуриновых нуклеотидов = сумме пиримидиновых нуклеотидов. 2. Молярное содержание аденинов = молярному содержанию тиминов и их отношение =1. 3. Количество аденина = количеству цитозина, а количество гуанина = количеству тимина, сумма аденина и цитозина = сумме гуанина и тимина.

www.themegallery.com Вторичная структура ДНК Основу цепочек ДНК составляет «сахаро-фосфатный остов» – остатки дезоксирибозы, соединенные через остатки фосфорной кислоты. В этой цепочке азотистое основание присоединено к первому углеродному атому дезоксирибозы, «свой» фосфат – к пятому, а по третьему атому данное нуклеотидное звено соединяется с фосфатом другого звена Молекула ДНК представляет собой две цепочки нуклеотидов, спирально закрученные вокруг общей оси. Азотистые основания двух цепочек располагаются друг напротив друга перпендикулярно оси спирали. На один виток спирали приходится 10 пар азотистых оснований, диаметр спирали составляет 2,37 нанометра.
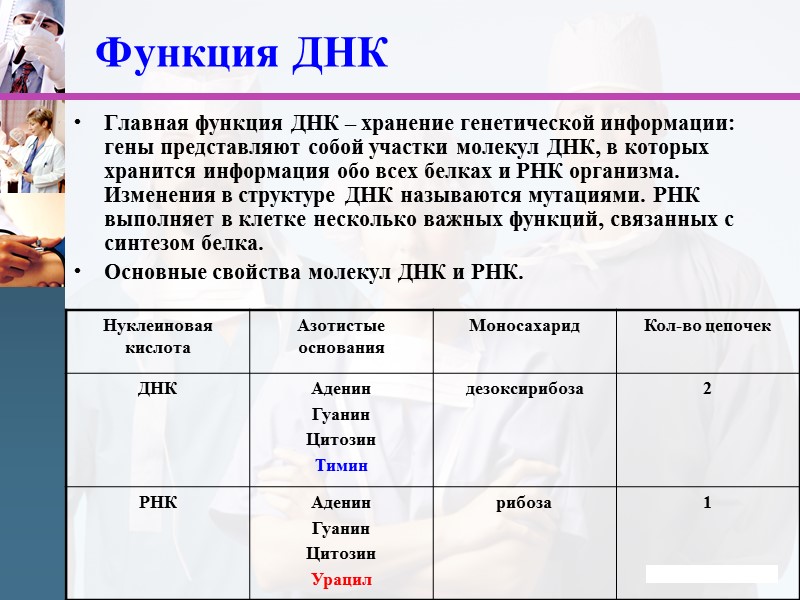
www.themegallery.com Функция ДНК Главная функция ДНК – хранение генетической информации: гены представляют собой участки молекул ДНК, в которых хранится информация обо всех белках и РНК организма. Изменения в структуре ДНК называются мутациями. РНК выполняет в клетке несколько важных функций, связанных с синтезом белка. Основные свойства молекул ДНК и РНК.
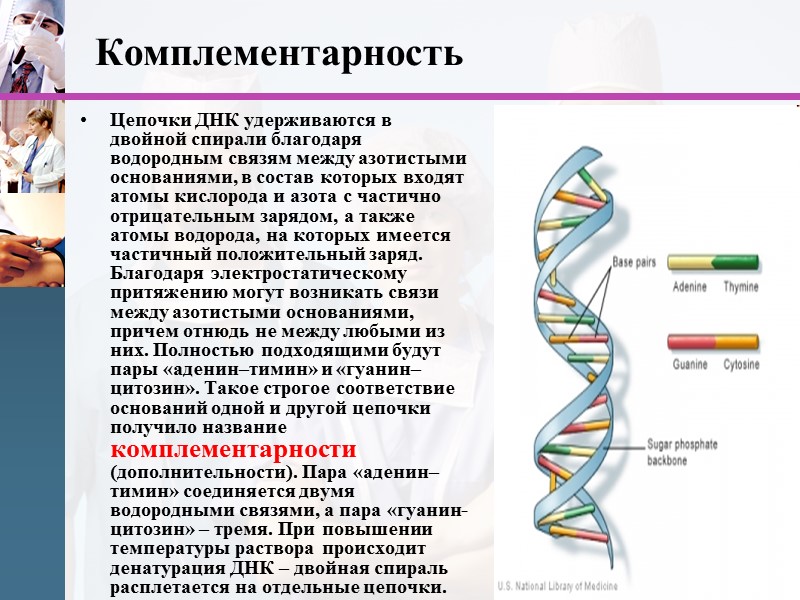
www.themegallery.com Комплементарность Цепочки ДНК удерживаются в двойной спирали благодаря водородным связям между азотистыми основаниями, в состав которых входят атомы кислорода и азота с частично отрицательным зарядом, а также атомы водорода, на которых имеется частичный положительный заряд. Благодаря электростатическому притяжению могут возникать связи между азотистыми основаниями, причем отнюдь не между любыми из них. Полностью подходящими будут пары «аденин–тимин» и «гуанин–цитозин». Такое строгое соответствие оснований одной и другой цепочки получило название комплементарности (дополнительности). Пара «аденин–тимин» соединяется двумя водородными связями, а пара «гуанин-цитозин» – тремя. При повышении температуры раствора происходит денатурация ДНК – двойная спираль расплетается на отдельные цепочки.

Это супер спираль или кольцо более высокого порядка, представляет собой дальнейшую спирализацию и суперспирализацию молекулы ДНК. Третичная структура ДНК
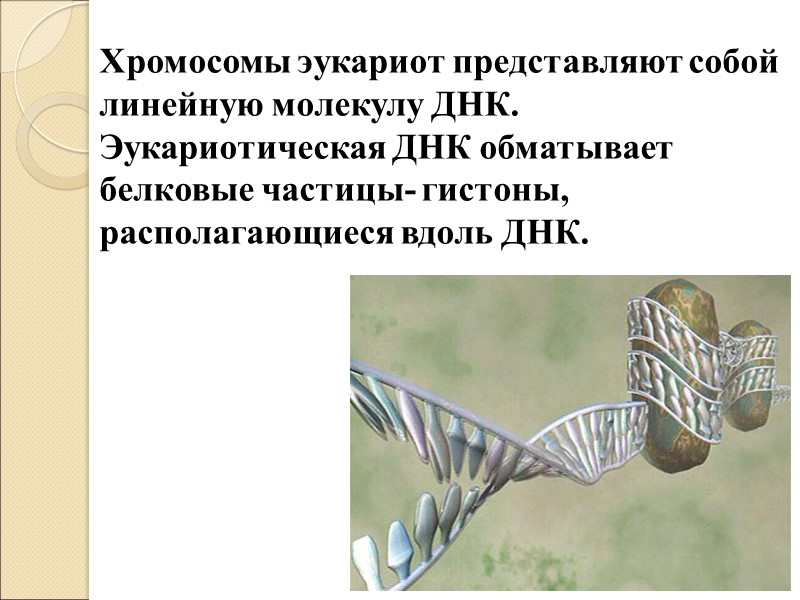
Хромосомы эукариот представляют собой линейную молекулу ДНК. Эукариотическая ДНК обматывает белковые частицы- гистоны, располагающиеся вдоль ДНК.
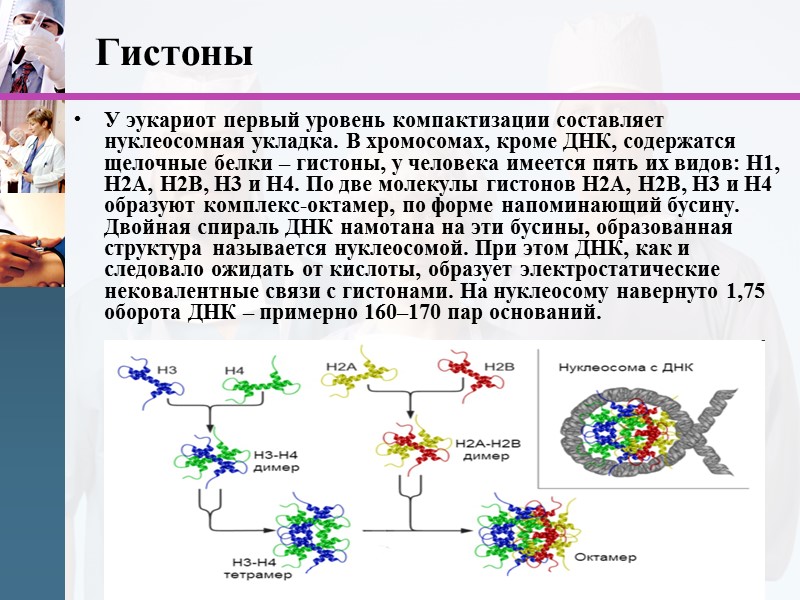
www.themegallery.com Гистоны У эукариот первый уровень компактизации составляет нуклеосомная укладка. В хромосомах, кроме ДНК, содержатся щелочные белки – гистоны, у человека имеется пять их видов: Н1, H2A, H2B, H3 и H4. По две молекулы гистонов H2A, H2B, H3 и H4 образуют комплекс-октамер, по форме напоминающий бусину. Двойная спираль ДНК намотана на эти бусины, образованная структура называется нуклеосомой. При этом ДНК, как и следовало ожидать от кислоты, образует электростатические нековалентные связи с гистонами. На нуклеосому навернуто 1,75 оборота ДНК – примерно 160–170 пар оснований.
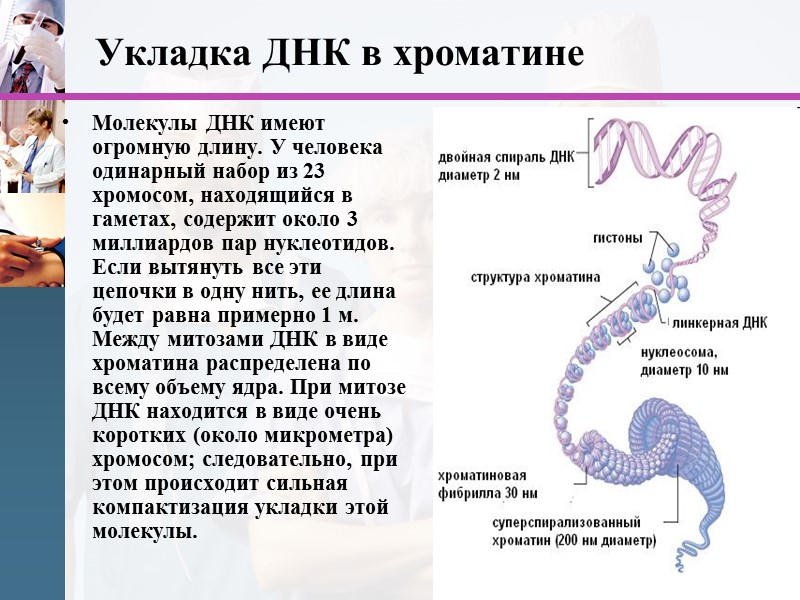
www.themegallery.com Укладка ДНК в хроматине Молекулы ДНК имеют огромную длину. У человека одинарный набор из 23 хромосом, находящийся в гаметах, содержит около 3 миллиардов пар нуклеотидов. Если вытянуть все эти цепочки в одну нить, ее длина будет равна примерно 1 м. Между митозами ДНК в виде хроматина распределена по всему объему ядра. При митозе ДНК находится в виде очень коротких (около микрометра) хромосом; следовательно, при этом происходит сильная компактизация укладки этой молекулы.

www.themegallery.com Нуклеосома Накрученная на нуклеосому двойная спираль в 7 раз короче свободной. «Бусы» из нуклеосом соединяются друг с другом с помощью гистона Н1, что обеспечивает еще большую компактизацию. Дальнейшие уровни укладки ДНК пока изучены не достаточно, однако доказано, что цепочки ДНК по всей длине хромосомы нигде не прерываются. Укладка ДНК влияет на генетическую активность. В целом, чем компактнее уложена ДНК, тем менее она активна – в хромосомах во время митоза почти не происходит ни активной работы генов, ни синтеза новой ДНК.

www.themegallery.com Хроматин Через определённые интервалы образуется хроматин- это волокно из которого состоят хромосомы. Под хроматином они понимают вещество хромосомы, как таковое. Исходя из представления о сохранении структурной целостности хромосом в клеточном цикле, подчеркивается, что химический состав хроматина и плотность его упаковки различаются по длине хромосомы в зависимости от стадии этого цикла.

www.themegallery.com Местонахождение ДНК в клетке В клетках эукариот ДНК содержится в: ядре митохондриях хлоропластах

www.themegallery.com Реакции матричного синтеза Реакции матричного синтеза – особая категория химических реакций, происходящих в клетках живых организмов. Во время этих реакций происходит синтез полимерных молекул по плану, заложенному в структуре других полимерных молекул-матриц. На одной матрице может быть синтезировано неограниченное количество молекул-копий.

www.themegallery.com Виды реакций матричного синтеза Репликация (самоудвоение ДНК) Рекомбинация (обмен участками между молекулами ДНК) Репарация (самовосстановление ДНК) Транскрипция (синтез РНК на ДНК) Обратная транскрипция (синтез ДНК на РНК – у некоторых вирусов) Трансляция Мутирование (изменение строения ДНК)
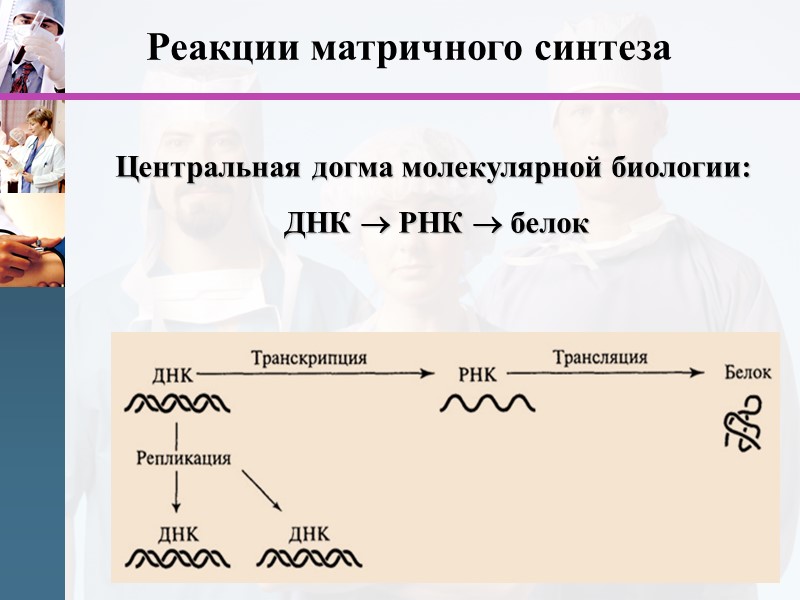
www.themegallery.com Центральная догма молекулярной биологии: ДНК РНК белок Реакции матричного синтеза
2. Репликация ДНК (механизмы, ферменты). Повреждения ДНК. Репарация повреждений и ошибок репликации (механизмы, ферменты).

www.themegallery.com Реплика́ция (от лат. replicatio — возобновление) — процесс синтеза дочерней молекулы дезоксирибонуклеиновой кислоты на матрице родительской молекулы ДНК. В ходе последующего деления материнской клетки каждая дочерняя клетка получает по одной копии молекулы ДНК, которая является идентичной ДНК исходной материнской клетки. Этот процесс обеспечивает точную передачу генетической информации из поколения в поколение. Репликацию ДНК осуществляет сложный ферментный комплекс, состоящий из 15-20 различных белков, называемый реплисомой.
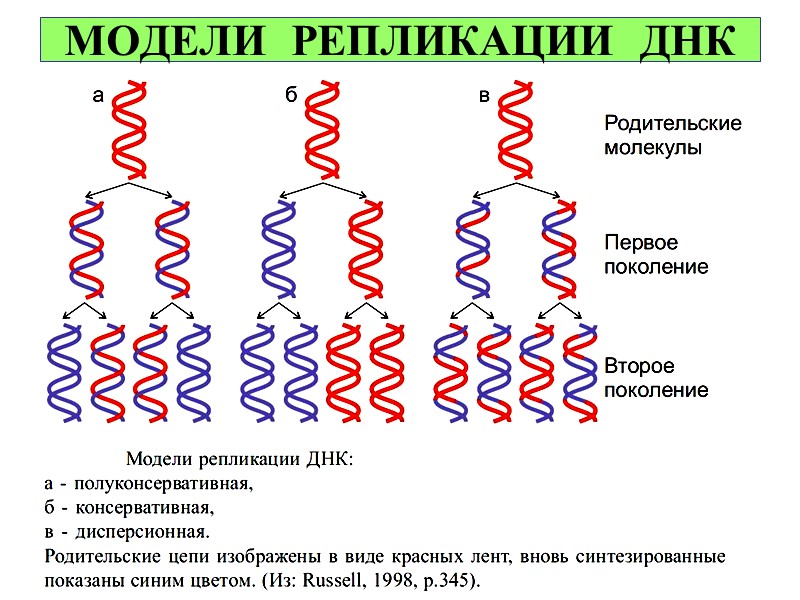
МОДЕЛИ РЕПЛИКАЦИИ ДНК

www.themegallery.com УСЛОВИЯ ДЛЯ РЕПЛИКАЦИИ Достаточное количество дезоксирибонуклеотидов (д ATФ, дTTФ, д ГTФ, д ЦTФ) Расплетение двойной спирали ДНК Образование затравки (праймера (РНК) Наличие необходимых ферментов

www.themegallery.com Стадии репликации ДНК Процесс репликации состоит из: инициации (начало процесса) элонгации (собственно синтез, удлинение, приращение) терминации (окончание процесса)

Репликон Единица, с помощью которой клетка контролирует отдельные акты репликации, получила название репликона. Каждый репликон в каждом клеточном цикле активизируется только один раз. В нем обязательно должны присутствовать необходимые для репликации контролирующие элементы: точка начала (origin), в которой инициируется репликация, точка окончания (terminus), в которой репликация останавливается.

www.themegallery.com Репликация ДНК Стадия инициации Репликация ДНК всегда идет от 5’– конца нити ДНК (то есть содержащего 5’-дезоксинуклеотидную группу) к 3’-концу (то содержащему свободную 3-ОН-группу) и нуждается в наличии ранее синтезированного фрагмета нити ДНК в качестве затравки для реакции полимеризации. Такой ДНК-фрагмент, имеющий свободный 3’-конец, называется праймером. Ферменты, катализирующие праймер-зависимую, детерминируемую ДНК-матрицей реакцию присоединения дезоксинуклеотидов, называются ДНК-полимеразами.
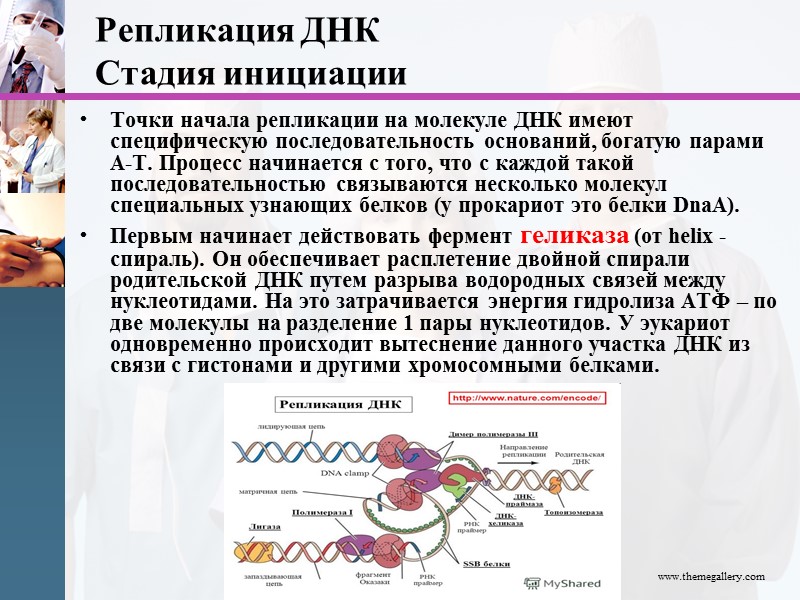
www.themegallery.com Репликация ДНК Стадия инициации Точки начала репликации на молекуле ДНК имеют специфическую последовательность оснований, богатую парами А-Т. Процесс начинается с того, что с каждой такой последовательностью связываются несколько молекул специальных узнающих белков (у прокариот это белки DnaA). Первым начинает действовать фермент геликаза (от helix - спираль). Он обеспечивает расплетение двойной спирали родительской ДНК путем разрыва водородных связей между нуклеотидами. На это затрачивается энергия гидролиза АТФ – по две молекулы на разделение 1 пары нуклеотидов. У эукариот одновременно происходит вытеснение данного участка ДНК из связи с гистонами и другими хромосомными белками.

www.themegallery.com Репликация ДНК Стадия инициации Однако расплетение спирали на некотором участке создает суперспирализацию перед этим участком, так как каждая молекула ДНК некоторыми участками зафиксирована на ядерном матриксе. Поэтому она не может свободно вращаться при какого-то своего участка. Это и вызывает суперспирализацию, что препятствует дальнейшему расплетению цепи. Эта проблема решается с помощью ферментов топоизомераз. Существует два типа топоизомераз (топоизомераза типа I и топоизомераза типа II). Топоизомераза I разрывает одну из цепей ДНК, и переносит один свободный конец на себя. Это позволяет участку ДНК от места расплетения до места разрыва вращаться вокруг целой цепи, что предупреждает образование супервитков. Впоследствии концы разорванной цепи вновь замыкаются. Топоизомераза II разрывает обе цепи ДНК, перенося соответствующие концы на себя. Это позволяет более эффективно решать проблему суперспирализации при расплетении ДНК. После расплетения двойной спирали хеликазой, с каждой из двух нитей связываются специальные SSB-белки. Они обладают повышенным сродством к одноцепочечным участкам ДНК и стабилизируют их в таком состоянии. Механизм действия основных ферментов репликации ДНК-полимераз таков, что синтез новой полинуклеотидной цепи не может начаться с включения в нее первого нуклеотида. Синтез идет только как удлинение уже существующего полинуклеотида, который комплементарен матрице и образует с ней двуспиральный комплекс матрица-затравка. Во всех живых системах такой затравкой служит не ДНК, а короткая РНК. РНК-затравка синтезируется ферментом праймазой (или РНК-полимеразой).

www.themegallery.com Вилка репликации По мере движения вилки одновременно должны синтезироваться две дочерние цепи. Вилка движется в направлении от 5' к 3’ на одной цепи и от 3’ к 5' – на другой. Однако нуклеиновые кислоты синтезируются только от 5'– к 3'-концу. Проблема решается таким образом, что на одной из родительских нитей новая нить синтезируется непрерывно в направлении 5'-3', что совпадает с движением вилки репликации. Это называется лидирующей или ведущей. Другая нить называется отстающей или запаздывающей, так как синтез на ней идет с некоторой задержкой по сравнению с лидирующей нитью. Это связано с тем, что ДНК на этой нити синтезируется также от 5' к 3', но в направлении, противоположном движению вилки, и короткими фрагментами. Благодаря этому разнонаправленный синтез ДНК может осуществляться в рамках одной структуры – репликативной вилки.

www.themegallery.com Репликация ДНК Стадия элонгации На этой стадии осуществляется синтез цепей ДНК. Каждый нуклеотид включается в цепь лишь в случае его комплементарности нуклеотиду, занимающему данную позицию в составе матрицы. Ферментный комплекс функционирует так, что одна из двух цепей растет с некоторым опережением по сравнению с другой цепью. Соответственно, первая цепь называется лидирующей, а вторая – запаздывающей. Важнейшее обстоятельство состоит в том, что лидирующая цепь образуется в виде непрерывного очень длинного фрагмента. Запаздывающая цепь образуется в виде серии относительно коротких фрагментов – примерно по 1500 нуклеотидов. Это т.н. фрагменты Оказаки. В виде фрагментов Оказаки синтезируется та цепь, направление образования которой противоположно направлению движения соответствующей репликативной вилки. Рост цепей ДНК осуществляется ферментами ДНК-полимеразами. Удлиннение цепи ДНК (или отдельного ее фрагмента) всегда происходит в направлении от 5’-конца к 3’-концу. Это означает, что очередной новый нуклеотид присоединяется к 3’-концу растущей цепи.

www.themegallery.com Ферменты стадии элонгации Элонгацию обеих полинуклеотидных цепей ДНК катализирует фермент δ ДНК-полимераза. Кроме собственно фермента, в репликативный комплекс входят белки RFC - Replication Factor C и PCNA - Proliferating Cell Nuclear Antigen. Первый блокирует наращивание РНК-праймера на 3'-конце сверх требуемой длины. Второй играет роль «прищепки» или зажима, крепящего δ ДНК-полимеразу к реплицируемой полинуклеотидной цепи.
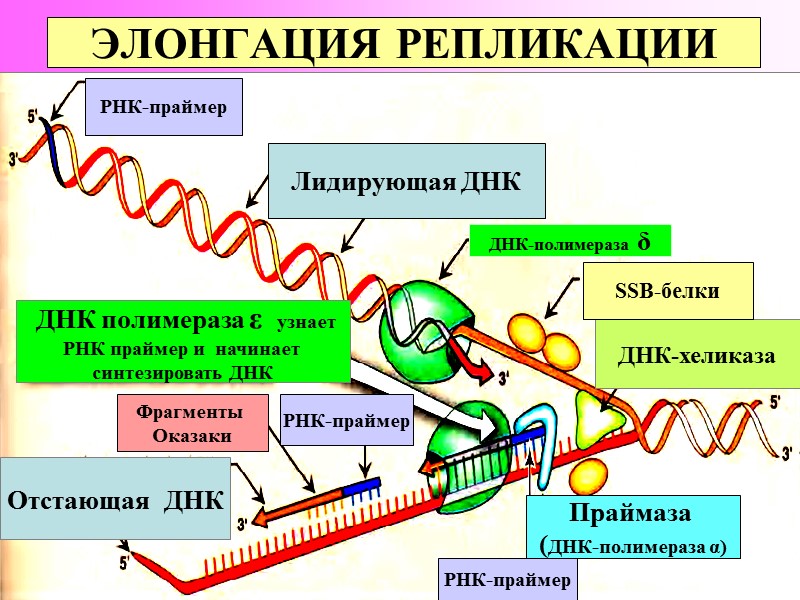
ЭЛОНГАЦИЯ РЕПЛИКАЦИИ РНК-праймер ДНК-хеликаза РНК-праймер РНК-праймер Фрагменты Оказаки Праймаза (ДНК-полимераза α) ДНК-полимераза δ ДНК полимераза ε узнает РНК праймер и начинает синтезировать ДНК SSB-белки Лидирующая ДНК Отстающая ДНК

www.themegallery.com Для завершения репликации (стадия терминации) используются ферменты ДНК-лигаза и теломераза. В результате действия предыдущих ферментов новосинтезированная запаздывающая цепь оказывается состоящей из фрагментов, вплотную примыкающих друг к другу (кроме кольцевой ДНК). «Сшивание» соседних фрагментов осуществляется ДНК-лигазой (фермент образует фосфодиэфирную связь). Для осуществления реакции требуется гидролиз АТФ. ДНК-полимеразная система оставляет недореплицированными 3’-концы материнских цепей ДНК, т.е. новые цепи оказываются укороченными с 5’-концов. В каждой новой цепи фрагмент Оказаки, находящейся у 5’-конца, как и обычно, начинается с короткой РНК-затравки (у 5’-конца лидирующей цепи тоже находится РНК-затравка). РНК-затравки удаляются специальной нуклеазой. Но застроиться дезоксинуклеотидами образующаяся «брешь» не может, поскольку ДНК-полимеразы не способны действовоать «с нуля», а лишь удлиняют 3’-конец уже имеющегося полинуклеотида. Поэтому получается, что новая цепь должна быть короче старой. Эта проблема решается при помощи фермента теломеразы. Теломераза удлинняет не новую, укороченную цепь, а старую, более длинную. К 3’-концу старой (родительской) цепи теломераза последовательно пристраивает несколько сотен повторяющихся последовательнотей. После чего значительно удлинненная старая цепь становиться способной выступать в качестве матрицы для образования еще одного фрагмента Оказаки новой (укороченной) цепи.
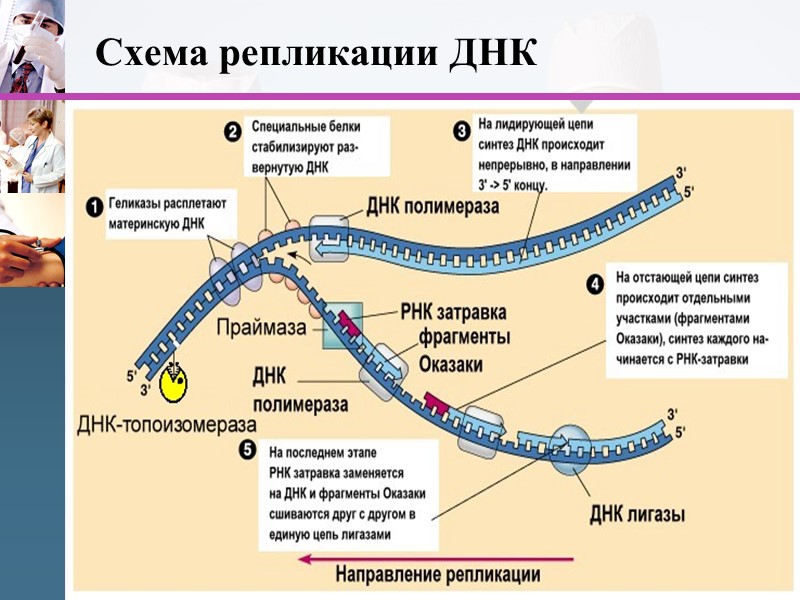
www.themegallery.com Схема репликации ДНК

www.themegallery.com Репарация ДНК Репарация (от лат. reparatio — восстановление) — особая функция клеток, заключающаяся в способности исправлять химические повреждения и разрывы в молекулах ДНК, повреждённой при нормальном биосинтезе ДНК в клетке или в результате воздействия физических или химических агентов. Осуществляется специальными ферментными системами клетки. Ряд наследственных болезней (напр., пигментная ксеродерма) связан с нарушениями систем репарации.

www.themegallery.com Источники повреждения ДНК Ультрафиолетовое излучение Радиация Химические вещества Ошибки репликации ДНК Апуринизация — отщепление азотистых оснований от сахарофосфатного остова Дезаминирование — отщепление аминогруппы от азотистого основания

www.themegallery.com Основные типы повреждения ДНК Повреждение одиночных нуклеотидов Повреждение пары нуклеотидов Разрыв цепи ДНК Образование поперечных сшивок между основаниями одной цепи или разных цепей ДНК
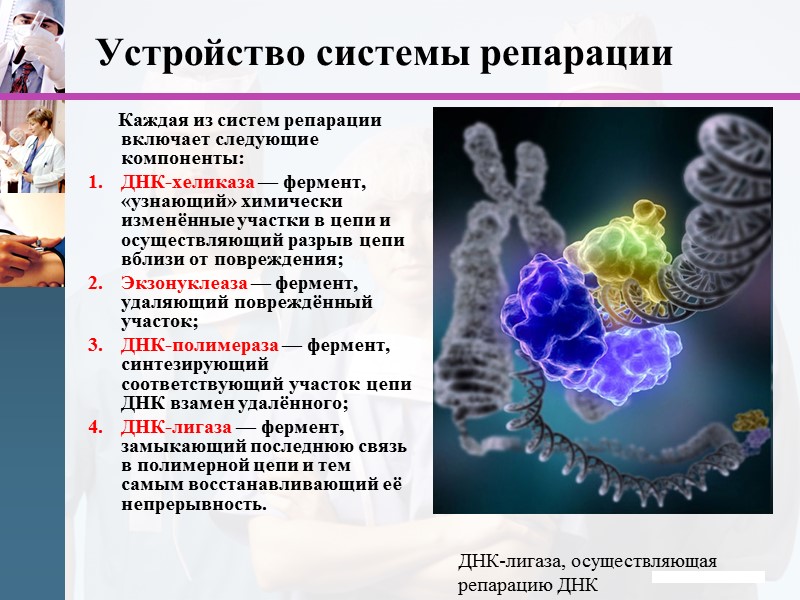
www.themegallery.com Устройство системы репарации Каждая из систем репарации включает следующие компоненты: ДНК-хеликаза — фермент, «узнающий» химически изменённые участки в цепи и осуществляющий разрыв цепи вблизи от повреждения; Экзонуклеаза — фермент, удаляющий повреждённый участок; ДНК-полимераза — фермент, синтезирующий соответствующий участок цепи ДНК взамен удалённого; ДНК-лигаза — фермент, замыкающий последнюю связь в полимерной цепи и тем самым восстанавливающий её непрерывность. ДНК-лигаза, осуществляющая репарацию ДНК

www.themegallery.com Типы механизмов репарации ДНК Прямая репарация — наиболее простой путь устранения повреждений в ДНК, в котором обычно задействованы специфические ферменты, способные быстро (как правило, в одну стадию) устранять соответствующее повреждение, восстанавливая исходную структуру нуклеотидов. Так действует, например, O6-метилгуанин-ДНК-метилтрансфераза, которая снимает метильную группу с азотистого основания на один из собственных остатков цистеина. Эксцизионная репарация (англ. excision — вырезание) включает удаление повреждённых азотистых оснований из ДНК и последующее восстановление нормальной структуры молекулы. Пострепликативная репарация - тип репарации, имеющей место в тех случаях, когда процесс эксцизионной репарации недостаточен для полного исправления повреждения: после репликации с образованием ДНК, содержащей поврежденные участки, образуются одноцепочечные бреши, заполняемые в процессе гомологичной рекомбинации при помощи белка RecA. Пострепликативная репарация была открыта в клетках E.Coli, не способных выщеплять тиминовые димеры. Это единственный тип репарации, не имеющий этапа узнавания повреждения.

3. Структура и функции РНК (разновидности, структура). Биосинтез РНК и ее процессинг.

www.themegallery.com Типы РНК В биосинтезе белков в эукариотических клетках задействованы три типа РНК: рибосомные, или рРНК (РНК-полимеразы I), информационная (матричная), или и(м)РНК (РНК-полимеразы II), транспортная или тРНК (РНК-полимеразы III).

www.themegallery.com Транскрипция РНК Транскри́пция (от лат. transcriptio — переписывание) — процесс синтеза РНК с использованием ДНК в качестве матрицы, происходящий во всех живых клетках. Другими словами, это перенос генетической информации с ДНК на РНК.

www.themegallery.com Транскрипция катализируется ферментом ДНК-зависимой РНК-полимеразой. Соответственно, в этих клетках имеется три РНК-полимеразы I, II и III. РНК-полимераза I участвует в синтезе молекулы-предшественницы пре-рРНК, РНК-полимераза II - ключевой фермент в транскрипции структурных (смысловых) генов, кодирующих аминокислотные последовательности белков, а также нуклеотидные последовательности snoPHK и некоторых snRNA (англ. small nuclear RNA или малых ядерных РНК). РНК-полимераза III участвует в транскрипции генов тРНК, некоторых snRNA и других преимущественно низкомолекулярных видов РНК. Отдельные РНК-полимеразы эукариот различают «свои» промоторы, чем объясняется транскрибирование ими разных видов РНК.

www.themegallery.com Что необходимо для транскрипции Цепь ДНК – матрица Ферменты (РНК-полимераза) Свободные дезоксирибонуклеозидфосфаты (АТФ, УТФ, ГТФ, ЦТФ).

www.themegallery.com Нить ДНК, которая служит матрицей для синтеза РНК при транскрипции называется смысловой или матричной. Вторая нить ДНК называется некодирующей (комплементарная ей РНК не кодирует белки, она "бессмысленная").

www.themegallery.com Отличие транскрипции от репликации В отличие от репликации, когда обе полинуклеотидных цепи двойной спирали ДНК функционируют в качестве матриц, матрицей для образования РНК служит одна (матричная) полинуклеотидная цепь, комплементарная второй (кодогенной) цепи, на которой, собственно, и расположены гены. Таким образом, процесс транскрипции является асимметричным. Особенность матричной цепи ДНК состоит в том, что на ней формируется открытый для РНК-полимеразы 3'-конец.
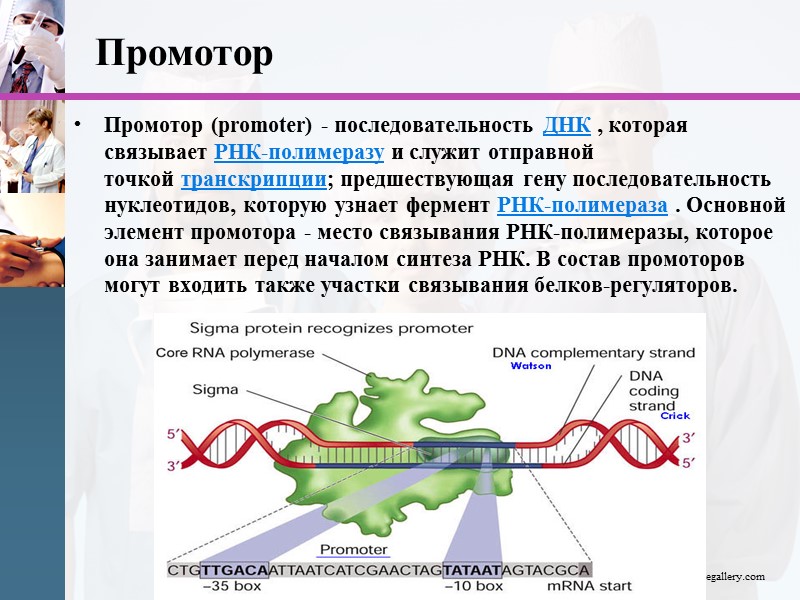
Промотор Промотор (promoter) - последовательность ДНК , которая связывает РНК-полимеразу и служит отправной точкой транскрипции; предшествующая гену последовательность нуклеотидов, которую узнает фермент РНК-полимераза . Основной элемент промотора - место связывания РНК-полимеразы, которое она занимает перед началом синтеза РНК. В состав промоторов могут входить также участки связывания белков-регуляторов. www.themegallery.com

Специфическая последовательность ДНК (сайт), в которой РНК-полимераза связывается с матрицей и начинает синтез РНК, называется промотором, а последовательность, на которой завершается синтез РНК, - сайтом терминации. Участок ДНК, ограниченный промотором и сайтом терминации, представляет собой единицу транскрипции -транскриптон. У эукариотов в состав транскриптона, как правило, входит только один ген.

Структура РНК-полимеразы РНК-полимераза — достаточно большая молекула. Основной фермент содержит 5 субъединиц (~400 кДа): α2: две α-субъединицы связывают остальные элементы фермента и распознают регулирующие факторы. Каждая субъединица состоит из двух доменов: αСКД (С-концевой домен) связывает первый элемент промотора, и αNКД (N-концевой домен) связывается с остальными компонентами полимеразы. β: эта субъединица обладает собственно полимеразным действием, катализируя синтез РНК. Она осуществляет инициацию процесса и управляет элонгацией. β': неспецифически связывается с ДНК. ω: восстанавливает денатурированную РНК-полимеразу обратно в дееспособную форму in vitro. Также обнаружено ее защитное/шаперонное действие на β'-субъединицу у Mycobacterium smegmatis. Для связывания с промоторными областями ДНК, основной фермент нуждается в еще одной субъединице — сигма (σ). Сигма-фактор значительно снижает сродство РНК-полимеразы к неспецифичным областям ДНК, и в то же время повышает ее чувствительность к определенным промоторам, в зависимости от своей структуры. С его помощью транскрипция начинается с нужного участка ДНК.

Эукариоты обладают различными типами РНК-полимераз, классифицируемыми по типам РНК, которые они производят: РНК-полимераза I, синтезирующая 45S-предшественника рРНК, превращающуюся затем в рРНК 28S, 18S и 5,8S, которые уже образуют главные РНК-секциирибосомы. РНК-полимераза II, производящая предшественников для мРНК, а также для большинства мяРНК и миРНК. Это наиболее хорошо изученный тип РНК-полимеразы. Ввиду того, что транскрипция должна происходить под строгим контролем, РНК-полимеразе II для связывания с промоторами требуется целый набор факторов транскрипции. РНК-полимераза III, синтезирующая тРНК, 5S рРНК и другие малые РНК, присутствующее в ядре и цитозоле.

www.themegallery.com Стадии транскрипции РНК Процесс транскрипции состоит из: инициации (начало процесса) элонгации (собственно синтез, удлинение, приращение) терминации (окончание процесса)

www.themegallery.com Стадиям транскрипции РНК предшествует узнавание промотора или подготовительная стадия, на которой РНК-полимераза узнает промотор и связывается с ним. Одновременно происходит локальное расплетение ДНК примерно на 10 пар нуклеотидов.

Стадия инициации «Активация» промотора происходит с помощью белка, который получил название ТАТА-фактора, потому что он взаимодействует со специфической последовательностью нуклеотидов промотора -ТАТА-. ТАТА-фактор облегчает взаимодействие промотора с РНК-полимеразой. Связывание РНК-полимеразы с промотором увеличивает сродство фермента к факторам инициации (А, В), которые обеспечивают раскручивание примерно одного витка двойной спирали ДНК.
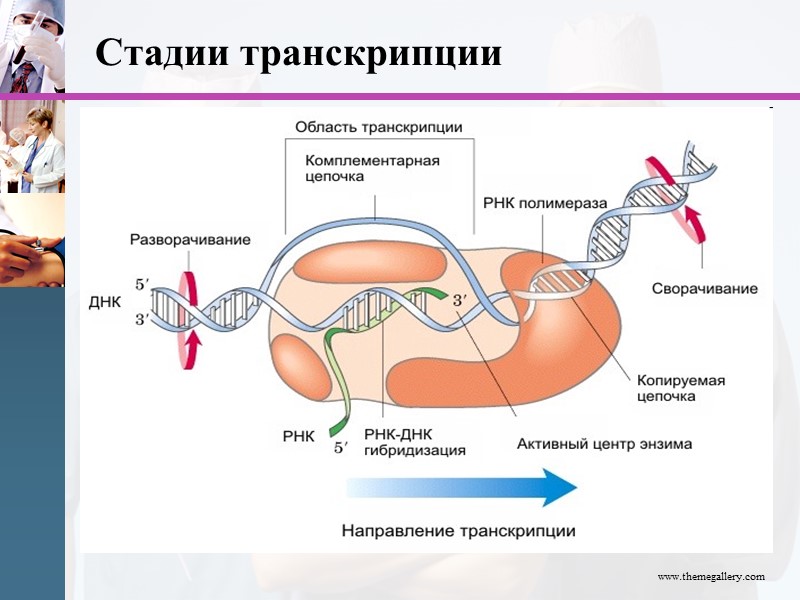
www.themegallery.com Стадии транскрипции
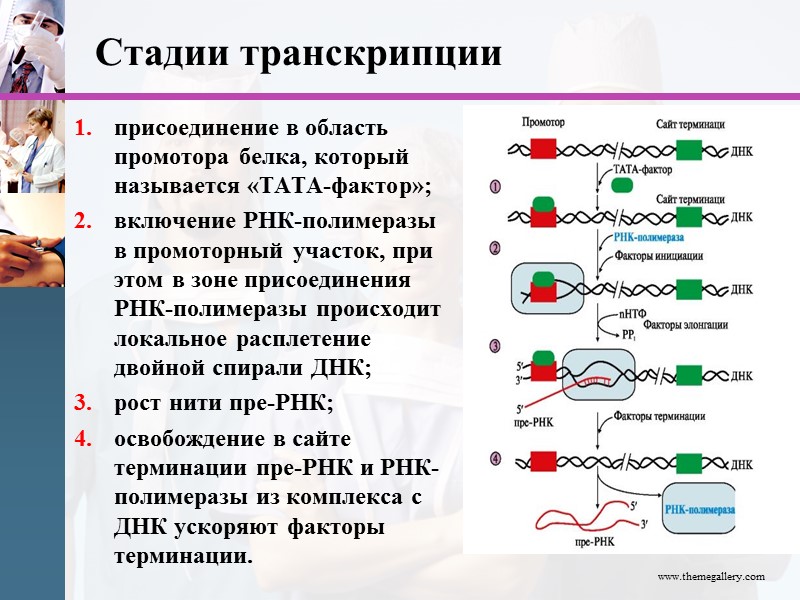
Стадии транскрипции присоединение в область промотора белка, который называется «ТАТА-фактор»; включение РНК-полимеразы в промоторный участок, при этом в зоне присоединения РНК-полимеразы происходит локальное расплетение двойной спирали ДНК; рост нити пре-РНК; освобождение в сайте терминации пре-РНК и РНК-полимеразы из комплекса с ДНК ускоряют факторы терминации. www.themegallery.com

www.themegallery.com Стадия элонгации Факторы элонгации (E, H, F) повышают активность РНК-полимеразы и облегчают локальное расхождение нуклеотидных цепей. Синтез молекулы РНК идет от 5 - к 3-концу на матричной цепи ДНК по принципу комплементарности и антипараллельности. По мере продвижения РНК-полимеразы по цепи ДНК в направлении от 3'- к 5'-концу впереди нее происходит расхождение, а позади - восстановление двойной спирали.

Стадия терминации Расхождение двойной спирали ДНК в области сайта терминации делает его доступным для факторов терминации. Когда РНК-полимераза достигает сайта терминации, транскрипция прекращается. Факторы терминации облегчают отделение первичного транскрипта от матрицы. www.themegallery.com

Посттранскрипционные модификации Прежде чем выйти из ядра, каждый первичный транскрипт после ряда ковалентных модификаций превращается в «зрелую» молекулу РНК. www.themegallery.com

Сплайсинг пре-мРНК Модификации пре-мРНК начинаются на стадии элонгации. Когда длина первичного транскрипта достигает примерно 30 нуклеотидов, происходит «кэпирование» 5'-конца. Остаток ГТФ присоединяется своим 5'-концом к 5'-концу фрагмента пре-мРНК с образованием 5'-, 5'-фосфодиэфирной связи. Последующее метилирование гуанина в составе ГТФ завершает образование «кэпа».

Сплайсинг пре-мРНК (продолжение) По завершении транскрипции на 3'-конце первичного транскрипта мРНК специальным ферментом поли-А-полимеразой синтезируется поли-Апоследовательность, которая состоит из 100-200 остатков адениловой кислоты. Наличие поли-А-последовательности на 3'-конце облегчает выход мРНК из ядра и замедляет ее гидролиз в цитоплазме. Молекулы тРНК и рРНК не содержат «кэпа» и поли-А-последовательности. Первичный транскрипт или пре-мРНК комплементарен гену, содержит как экзоны - последовательности, кодирующие определенные участки молекулы белка, так и интроны - некодирующие последовательности. В процессе образования молекул «зрелой» мРНК интроны вырезаются из первичного транскрипта, концы экзонов соединяются друг с другом - эту реакцию называют сплайсингом РНК.
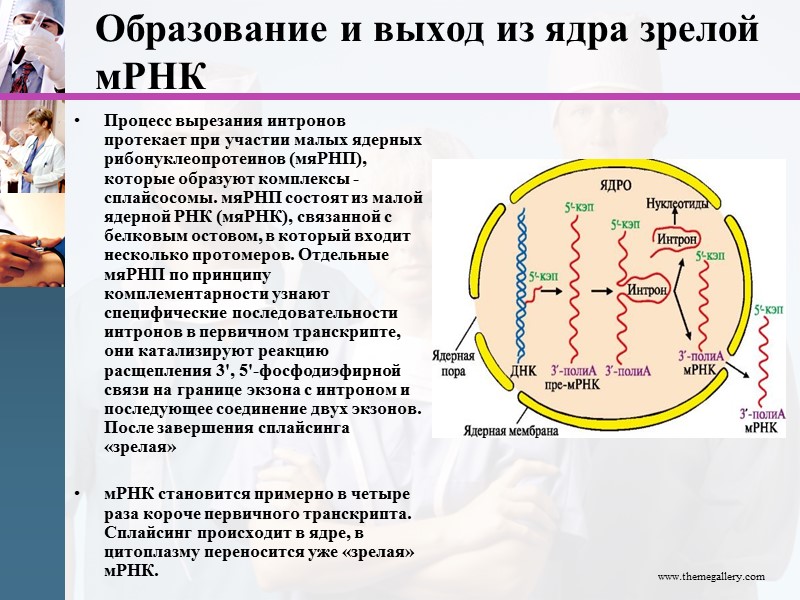
Образование и выход из ядра зрелой мРНК Процесс вырезания интронов протекает при участии малых ядерных рибонуклеопротеинов (мяРНП), которые образуют комплексы - сплайсосомы. мяРНП состоят из малой ядерной РНК (мяРНК), связанной с белковым остовом, в который входит несколько протомеров. Отдельные мяРНП по принципу комплементарности узнают специфические последовательности интронов в первичном транскрипте, они катализируют реакцию расщепления 3', 5'-фосфодиэфирной связи на границе экзона с интроном и последующее соединение двух экзонов. После завершения сплайсинга «зрелая» мРНК становится примерно в четыре раза короче первичного транскрипта. Сплайсинг происходит в ядре, в цитоплазму переносится уже «зрелая» мРНК. www.themegallery.com

Модификации пре-тРНК В процессе посттранскрипционных модификаций первичных транскриптов тРНК: • молекулы укорачиваются с 5'- и 3'-концов и удаляется интрон; • 10-15% азотистых оснований в молекулах модифицируется; • на 3'-конце формируется акцепторный участок (-ССА) для присоединения аминокислот, а в средней части антикодон - триплет нуклеотидов, обеспечивающий взаимодействие тРНК с кодоном мРНК.

Посттранскрипционные модификации пре-тРНК удаляются участки полинуклеотидной цепи на 5'- и 3'-концах молекулы претРНК и интрон в центральной области молекулы; модифицируются азотистые основания (■), к 3'-концу присоединяется триплет-ССА; в цитоплазму выходят зрелые тРНК www.themegallery.com

Посттранскрипционные модификации пре-рРНК Посттранскрипционные модификации пре-рРНК сопровождаются образованием из высокомолекулярного предшественника 28S, 18S и 5,8S «зрелых» рРНК, входящих в рибосому - органеллу клетки, участвующую в биосинтезе белка. В состав рибосом входят рРНК и белки, выполняющие структурную, регуляторную и каталитическую функции. Рибосома эукариотов (80S) состоит из двух (большой и малой) субъединиц - 60S и 40S. Величина S характеризует скорость оседания (седиментации) субъединиц рибосом при ультрацентрифугировании. Она пропорциональна молекулярной массе частиц. Рибосома прокариотов (70S) состоит из 50S и 30S. Рибосомы эукариотов и прокариотов различаются по молекулярной массе субъединиц, количеству рРНК, массе рРНК, количеству и разнообразию белков, способных связывать специфические лиганды. Строение эукариотических рибосом

Обратная транскрипция Некоторые вирусы (такие как ВИЧ, вызывающий СПИД), имеют возможность транскрибировать РНК в ДНК. ВИЧ имеет РНК-геном, который встраивается в ДНК. В результате, ДНК вируса может быть объединено с геномом клетки-хозяина. Главный фермент, ответственный за синтез ДНК из РНК, называется ревертазой. Одной из функций ревертазы является создание комплементарной ДНК (кДНК) из вирусного генома. Ассоциированый фермент рибонуклеаза H расщепляет РНК, а ревертаза синтезирует кДНК из двойной спирали ДНК. кДНК интегрируется в геном клетки-хозяина с помощью интегразы. Результатом является синтез вирусных протеинов клеткой-хозяином, которые образуют новые вирусы. В случае с ВИЧ так же программируется апоптоз (смерть клетки) Т-лимфоцитов. В иных случаях клетка может остаться распростанителем вирусов. Некоторые клетки эукариотов содержат фермент теломеразу, так же проявляющую активность обратной транскрипции. С её помощью синтезируются повторяющиеся последовательности в ДНК. Теломераза часто активирутся в раковых клетках для бесконечной дупликации генома без потери кодирующей протеины последовательности ДНК.
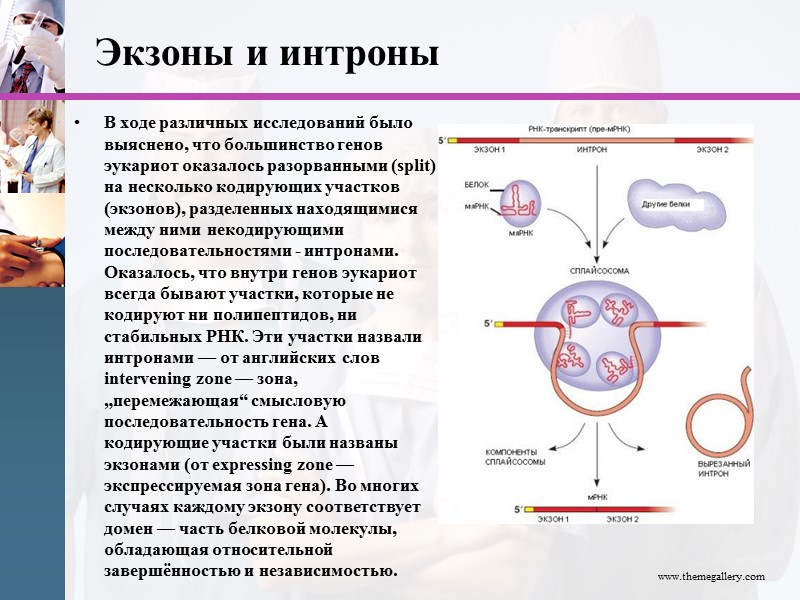
Экзоны и интроны В ходе различных исследований было выяснено, что большинство генов эукариот оказалось разорванными (split) на несколько кодирующих участков (экзонов), разделенных находящимися между ними некодирующими последовательностями - интронами. Оказалось, что внутри генов эукариот всегда бывают участки, которые не кодируют ни полипептидов, ни стабильных РНК. Эти участки назвали интронами — от английских слов intervening zone — зона, „перемежающая“ смысловую последовательность гена. А кодирующие участки были названы экзонами (от expressing zone — экспрессируемая зона гена). Во многих случаях каждому экзону соответствует домен — часть белковой молекулы, обладающая относительной завершённостью и независимостью. www.themegallery.com
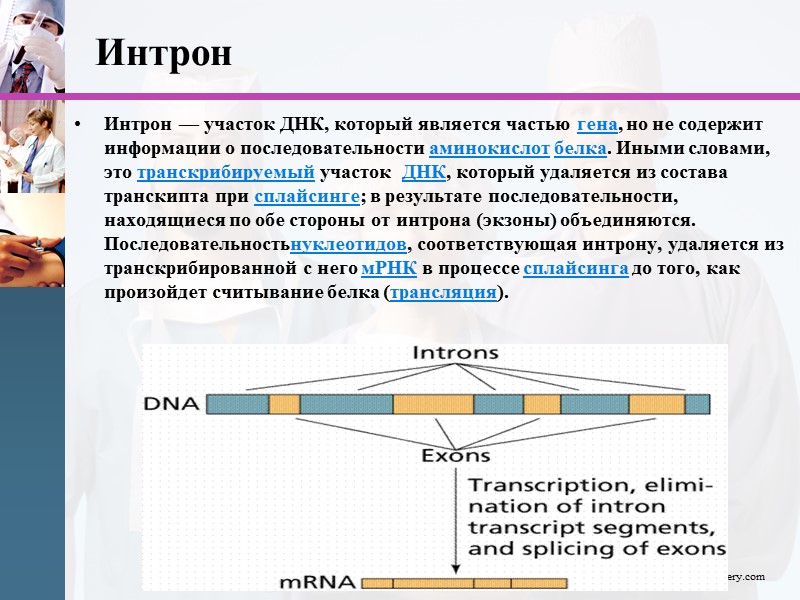
Интрон Интрон — участок ДНК, который является частью гена, но не содержит информации о последовательности аминокислот белка. Иными словами, это транскрибируемый участок ДНК, который удаляется из состава транскипта при сплайсинге; в результате последовательности, находящиеся по обе стороны от интрона (экзоны) объединяются. Последовательностьнуклеотидов, соответствующая интрону, удаляется из транскрибированной с него мРНК в процессе сплайсинга до того, как произойдет считывание белка (трансляция). www.themegallery.com

Классификация интронов Существует четыре группы интронов: Ядерные интроны Интроны группы I Интроны группы II Интроны группы III Иногда интроны группы III также относят к группе II, потому что они похожи по структуре и функции. Ядерные, или спалайсосомные интроны подвергаются сплайсингу при помощи сплайсосомы и малых ядерных РНК (мяРНК, snRNA). В последовательности РНК, содержащей ядерные интроны, есть специальные сигнальные последовательности, которые узнаются сплайсосомой. Интроны I, II и III группы способны к автосплайсингу и встречаются реже, чем сплайсосомные интроны.

4. Обмен нуклеотидов (состав, биосинтез, катаболизм). Нарушение обмена азотистых оснований (подагра).

Метаболизм нуклеотидов

ФУНКЦИИ НУКЛЕОТИДОВ
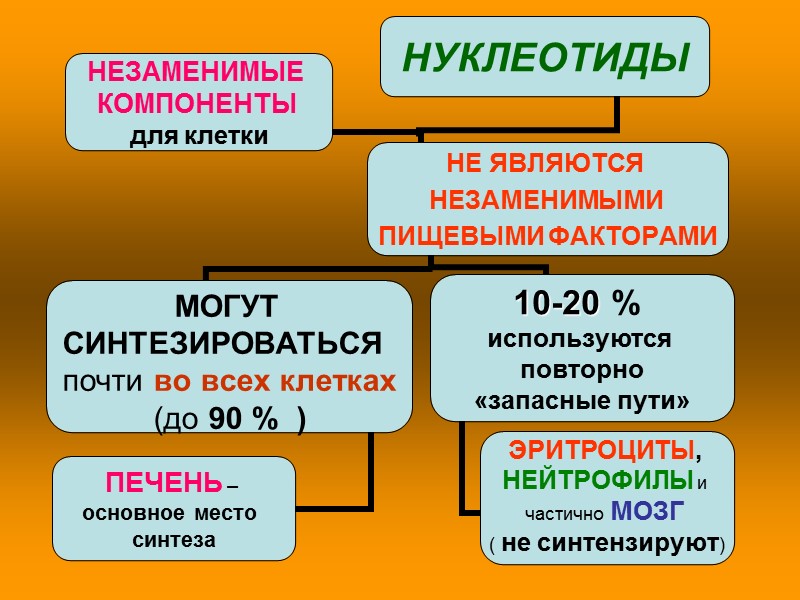
ПЕРЕВАРИВАНИЕ НУКЛЕИНОВЫХ КИСЛОТ Ротовая полость ДНК РНК ДНК РНК Желудок Поджелудочная железа рН=1,5 денатурация ДНК и РНК Денатурированные ДНК и РНК Нуклеазы Олигонуклеотиды ДЕЗОКСИРИБО-НУКЛЕАЗЫ (ДНК) и РИБОНУКЛЕАЗЫ (РНК) расщепляют 3', 5' – фосфо-диэфирные связи

Поджелудочная железа Олигонуклеотиды Фосфодиэстеразы Мононуклеотиды Нуклеотидазы Нуклеозиды Нуклеозидазы Пиримидины Пурины (Дезокси) рибоза Кровоток Мочевая кислота Моча Тонкий кишечник Ф Энтероцит

МЕТАБОЛИЗМ ПУРИНОВ

ИСТОЧНИКИ АТОМОВ В ПУРИНОВЫХ ОСНОВАНИЯХ АСПАРТАТ ГЛИЦИН ГЛУТАМИН ФОРМИЛ ТГФК СЕРИН

Особенность синтеза пуринов Атомы С и N поэтапно добавляются к рибозе 5-фосфат.
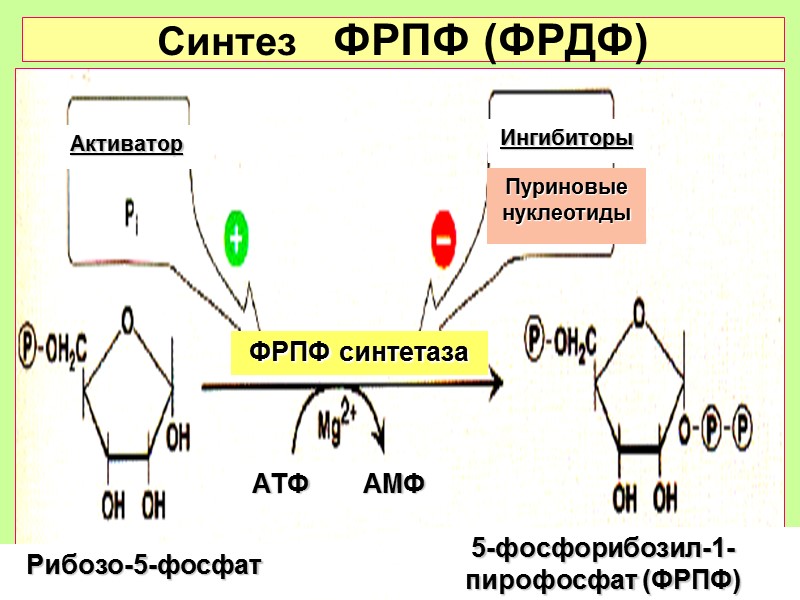
Синтез ФРПФ (ФРДФ) Активатор Ингибиторы Пуриновые нуклеотиды Рибозо-5-фосфат 5-фосфорибозил-1-пирофосфат (ФРПФ) АТФ АМФ ФРПФ синтетаза

ЛИМИТИРУЮЩАЯ РЕАКЦИЯ 5-фосфорибозиламин Глутамин Глутамат Ингибиторы АМФ, ГМФ, ИМФ 5-фосфорибозил 1-пирофосфат (ФРПФ) Глутамин фосфорибозил пирофосфат амидо- трансфераза [S]

5-Фосфорибозиламин ИМФ 1 Глицин O 2 C – TГФК H 2 TГФК 1 Глутамин 1 Аспартат Глутамат Фумарат 4 ATФ 4 AДФ + 4 Фн Серин Глицин МЕТОТРЕКСАТ - B9 у человека ПАБК бактерии СУЛЬФОНИЛАМИДЫ -

ИНГИБИТОРЫ СИНТЕЗА НУКЛЕОТИДОВ ТОКСИЧНЫ как ДЛЯ РАКОВЫХ КЛЕТОК так и ДЛЯ ЗДОРОВЫХ (анемия, диарея, выпадение волос)
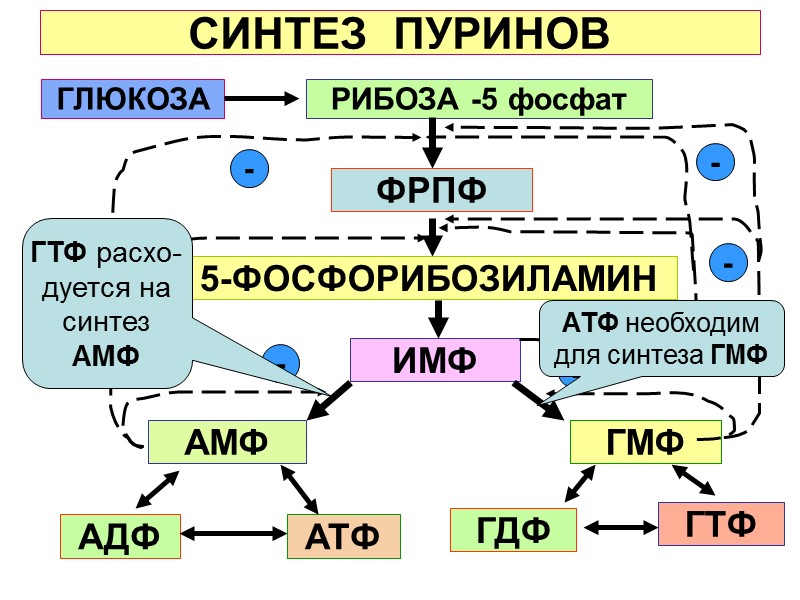
СИНТЕЗ ПУРИНОВ РИБОЗА -5 фосфат ФРПФ 5-ФОСФОРИБОЗИЛАМИН ИМФ АМФ ГМФ АДФ АТФ ГДФ ГТФ ГЛЮКОЗА - - - - - - ГТФ расхо-дуется на синтез АМФ АТФ необходим для синтеза ГМФ

Нуклеозид монофосфат киназы аденилат киназа гуанилат киназа Нуклеозид дифосфат киназа АМФ АТФ АДФ ГМФ АТФ ГДФ АДФ ГДФ АТФ ГТФ АДФ ЦДФ АТФ ЦТФ АДФ

Гипоксантин Гуанин Аденин АМФ ФРПФ ГМФ ИМФ ФРПФ ФРПФ Гипоксантин-гуанин фосфорибозилтрансфераза Гипоксантин-гуанин фосфорибозилтрансфераза Аденин фосфорибозилтрансфераза Синдром ЛЕША-НИХЕНА ПФ ПФ ПФ «Запасные пути»- 10-20%

СИНДРОМ ЛЕША-НИХЕНА СИМПТОМЫ - 1. НЕВРОЛОГИЧЕСКИЕ самоувечья (укусы гыб, языка, пальцев), церебральные параличи, умственная отсталость. 2. ПОДАГРА (гиперурикемия)
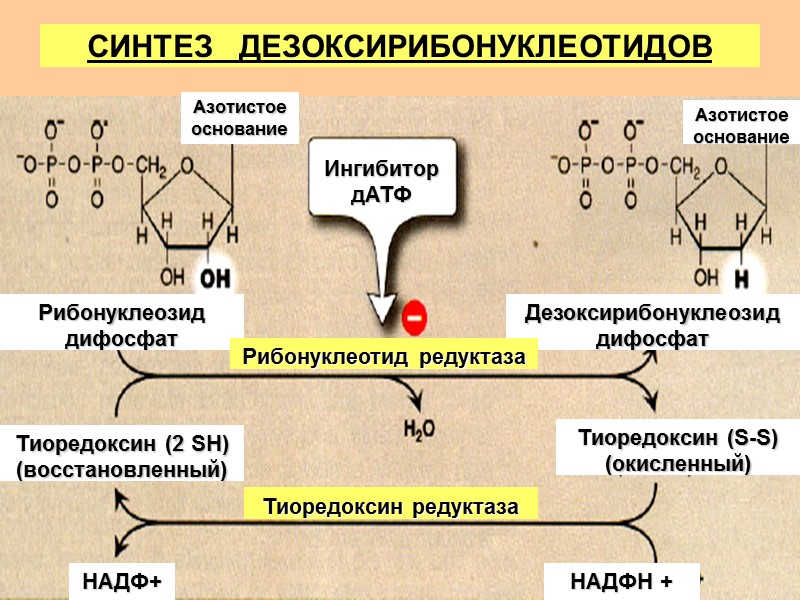
СИНТЕЗ ДЕЗОКСИРИБОНУКЛЕОТИДОВ Азотистое основание Азотистое основание Рибонуклеозид дифосфат Дезоксирибонуклеозид дифосфат Тиоредоксин (2 SH) (восстановленный) Тиоредоксин (S-S) (окисленный) Ингибитор дАТФ Рибонуклеотид редуктаза Тиоредоксин редуктаза НАДФ+ НАДФН + Н+
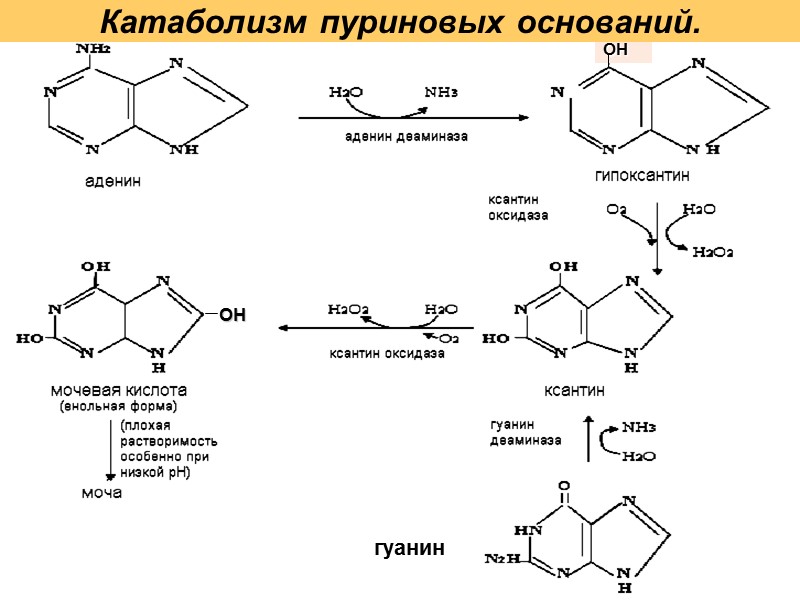
ОН Катаболизм пуриновых оснований. ОН гуанин

Мочевая кислота и ураты Мочевая кислота Урат ион
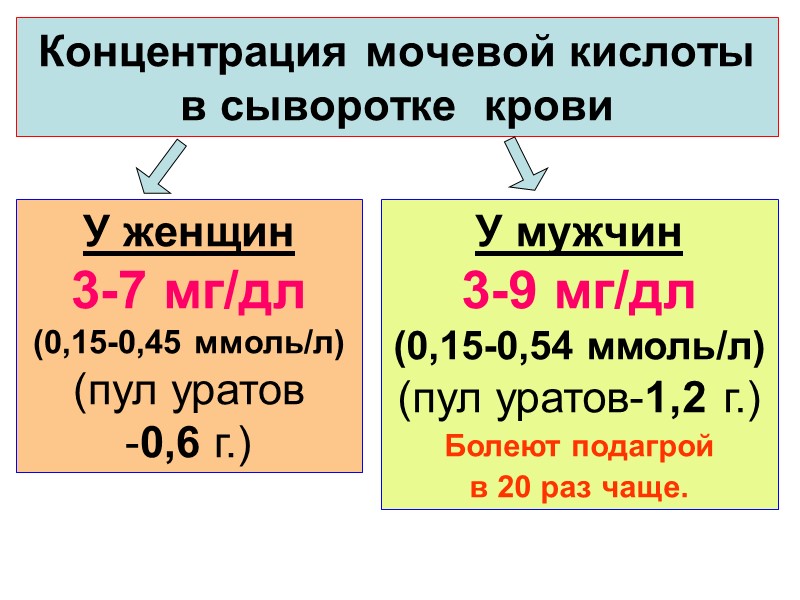
Концентрация мочевой кислоты в сыворотке крови У мужчин 3-9 мг/дл (0,15-0,54 ммоль/л) (пул уратов-1,2 г.) Болеют подагрой в 20 раз чаще. У женщин 3-7 мг/дл (0,15-0,45 ммоль/л) (пул уратов -0,6 г.)
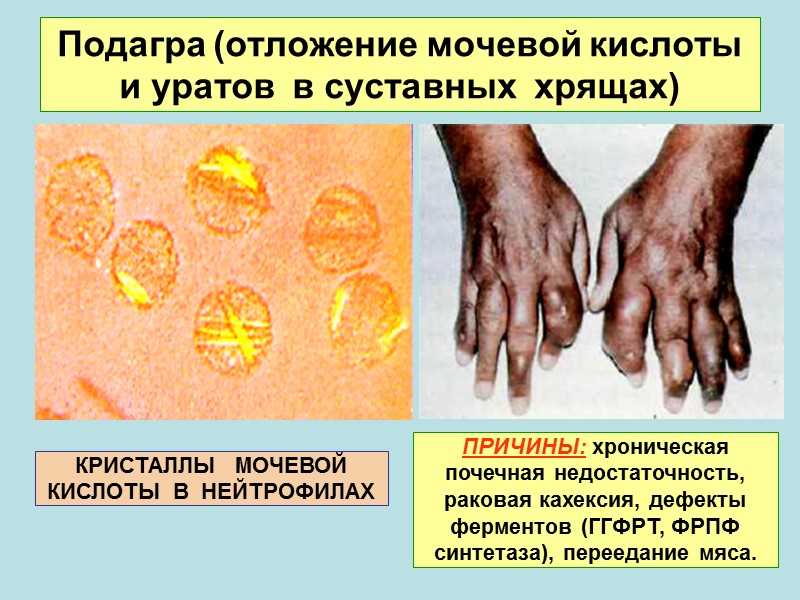
Подагра (отложение мочевой кислоты и уратов в суставных хрящах) КРИСТАЛЛЫ МОЧЕВОЙ КИСЛОТЫ В НЕЙТРОФИЛАХ ПРИЧИНЫ: хроническая почечная недостаточность, раковая кахексия, дефекты ферментов (ГГФРТ, ФРПФ синтетаза), переедание мяса.
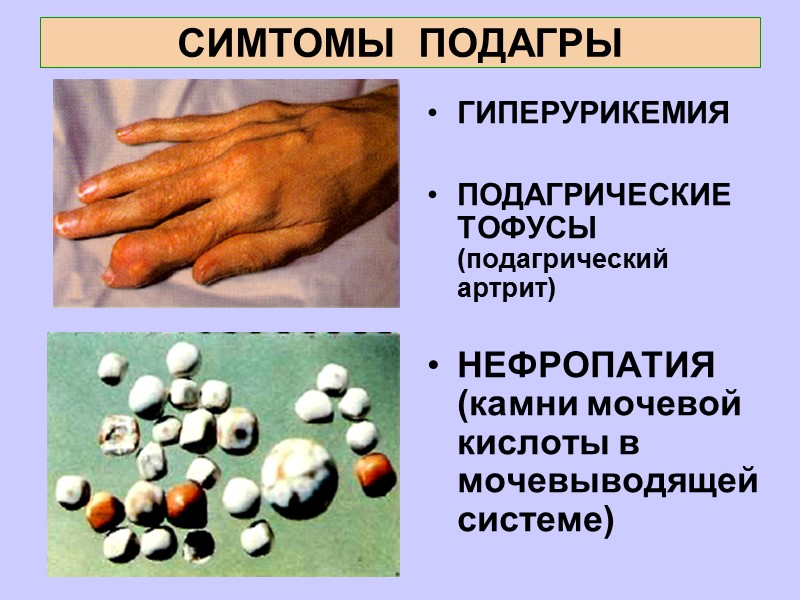
СИМТОМЫ ПОДАГРЫ ГИПЕРУРИКЕМИЯ ПОДАГРИЧЕСКИЕ ТОФУСЫ (подагрический артрит) НЕФРОПАТИЯ (камни мочевой кислоты в мочевыводящей системе)
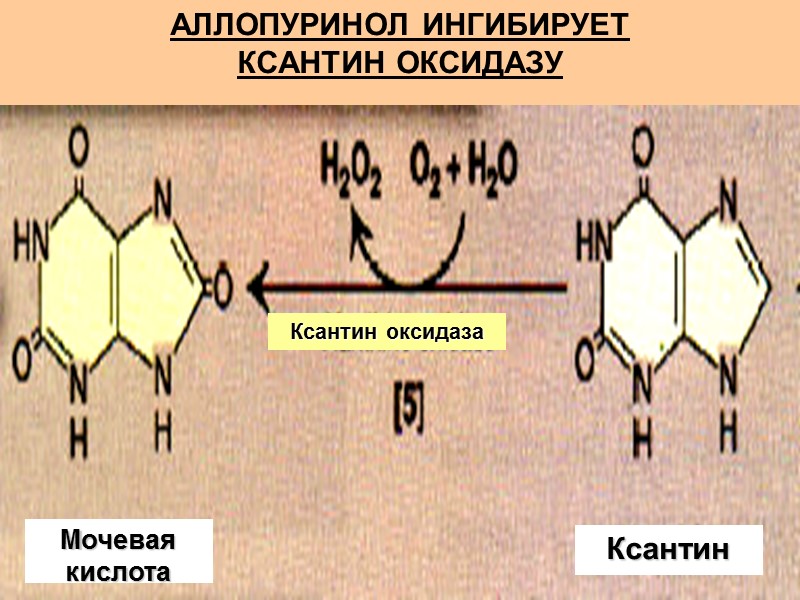
АЛЛОПУРИНОЛ ИНГИБИРУЕТ КСАНТИН ОКСИДАЗУ Ксантин оксидаза Ксантин Мочевая кислота

МЕТАБОЛИЗМ ПИРИМИДИНОВ
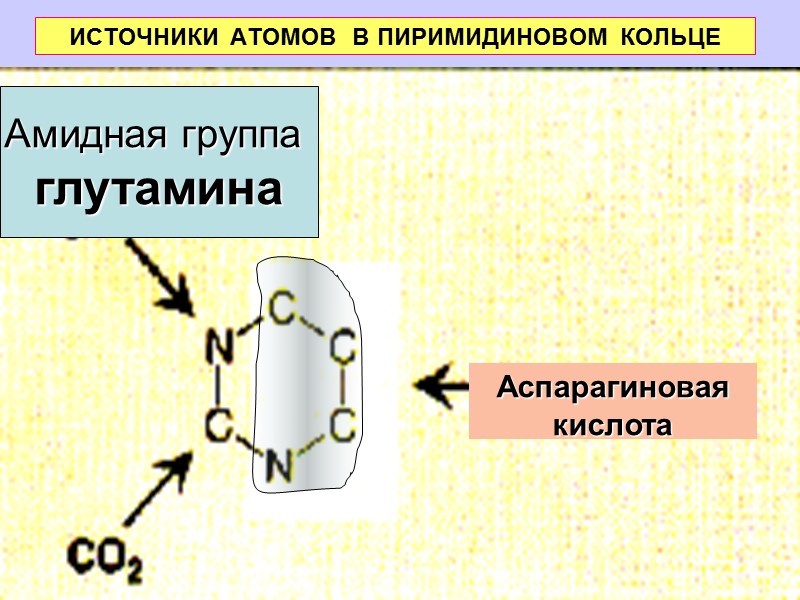
ИСТОЧНИКИ АТОМОВ В ПИРИМИДИНОВОМ КОЛЬЦЕ Аспарагиновая кислота Амидная группа глутамина

Особенность синтеза пиримидинов Вначале синтезируется пиримидиновое кольцо и уже затем оно связы-вается с рибозо 5-фос-фатом (от ФРПФ) .

СИНТЕЗ ПИРИМИДИНОВ (ЛИМИТИРУЮЩАЯ РЕАКЦИЯ ) 2 АДФ + Глутамат Глутамин Карбамоил Фосфат Синтетаза II Карбамоил Фосфат
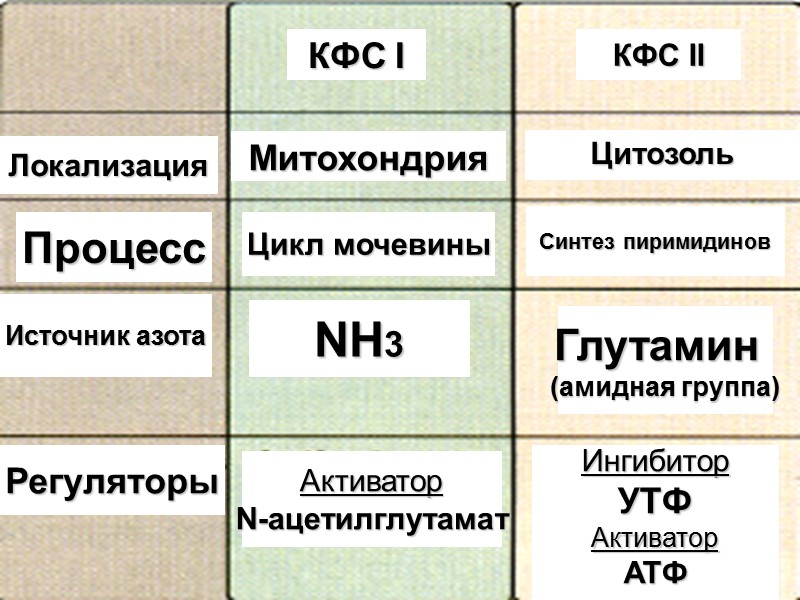
Митохондрия Цитозоль Локализация Процесс Цикл мочевины Синтез пиримидинов КФС I КФС II Источник азота NH3 Глутамин (амидная группа) Регуляторы Активатор N-ацетилглутамат Ингибитор УТФ Активатор АТФ

Синтез пиримидинов Карбамоил аспартат Аспартат Аспартат транскарба-моилаза Дигидро-оротаза Дигидро-оротат Карбамоил фосфат
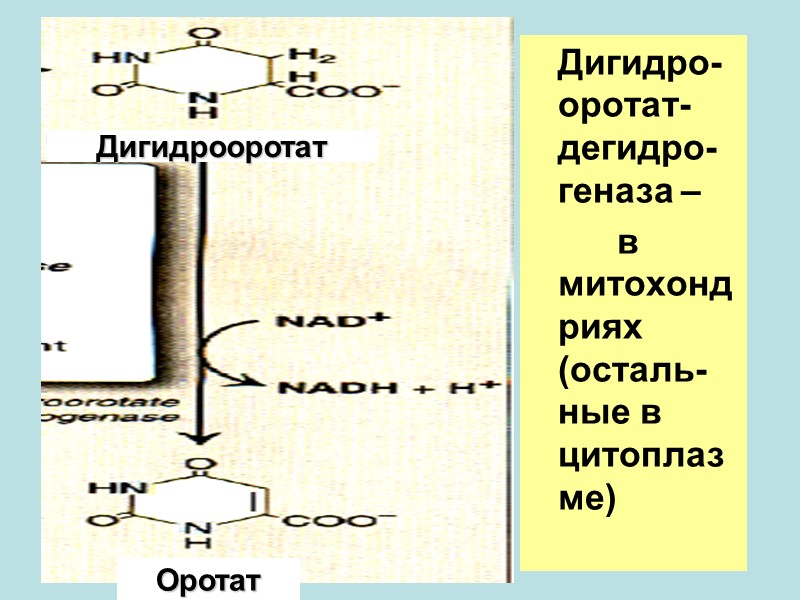
Дигидро-оротат-дегидро-геназа – в митохондриях (осталь-ные в цитоплазме) Дигидрооротат Оротат
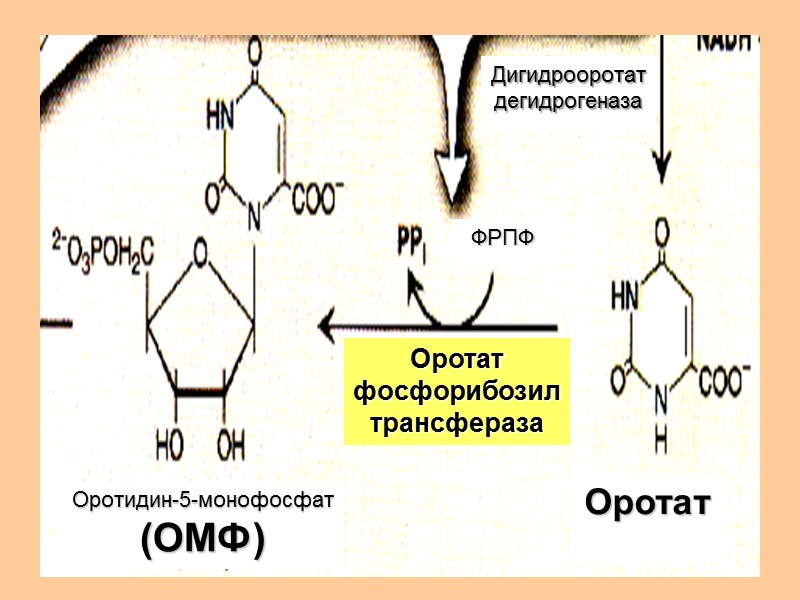
Дигидрооротат дегидрогеназа Оротидин-5-монофосфат (ОМФ) Оротат Оротат фосфорибозил трансфераза ФРПФ

ОМФ Декарбоксилаза Уридин 5-монофосфат (УМФ) Оротидин 5- монофосфат (ОМФ)

Оротат ацидурия – снижение интеллекта, работы сердца, почек и ЖКТ, иммунной системы Дефект УМФ синтазы (2-а вида активности – оротатфосфорибозил трансфераза и ОМФ декарбоксилаза). Мегалобластная анемия (не поддается лечению препаратами фолиевой кислоты) Гиперэкскреция оротовой кислоты – нарушения со стороны мочевыводящей системы и образование камней Лечение – уридин (0,5 - 1 г/сут) по «запасному» пути превращается в УМФ

Синтез ЦТФ из УТФ Глутамин Глутамат синтетаза АТФ АДФ + Ф УТФ ЦТФ ЦТФ
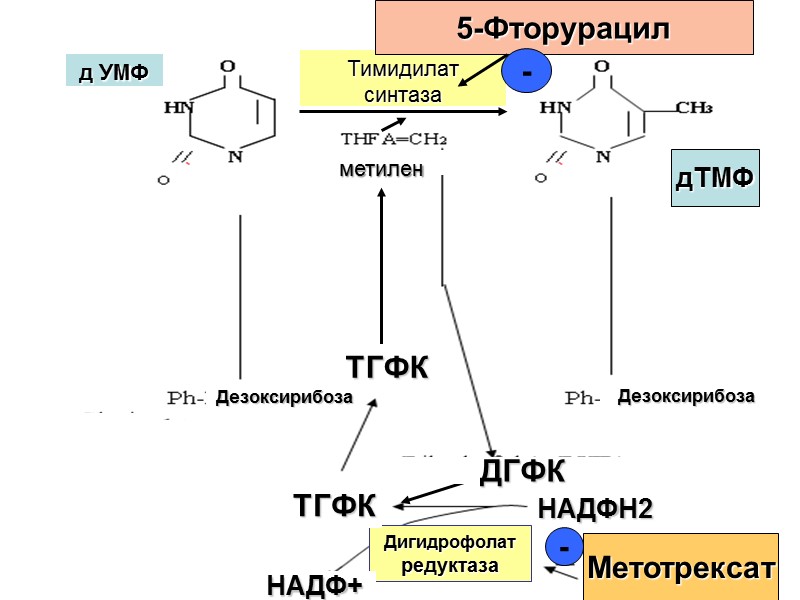
д УМФ Тимидилат синтаза метилен Глицин Серин ТГФК Дезоксирибоза Дезоксирибоза Дигидрофолат редуктаза 5-Фторурацил дТМФ ДГФК Метотрексат НАДФН2 ТГФК НАДФ+ - -
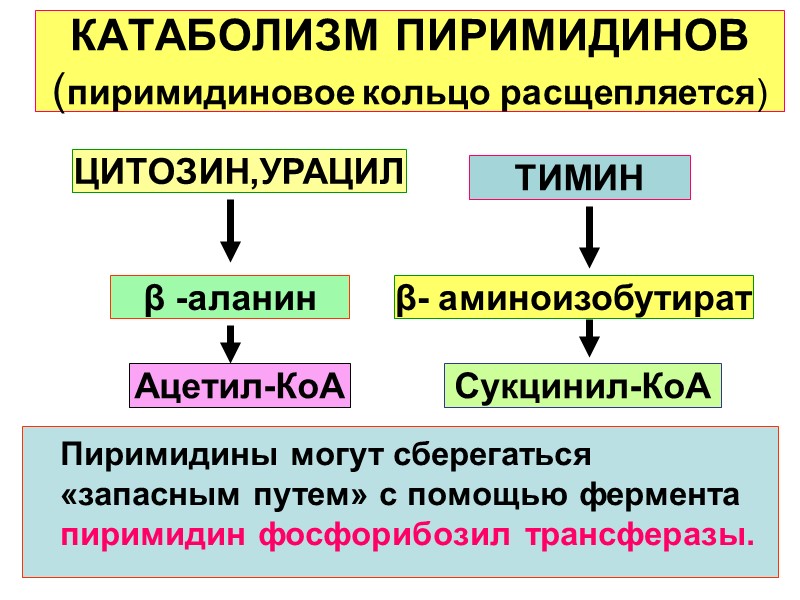
КАТАБОЛИЗМ ПИРИМИДИНОВ (пиримидиновое кольцо расщепляется) Пиримидины могут сберегаться «запасным путем» с помощью фермента пиримидин фосфорибозил трансферазы. ЦИТОЗИН,УРАЦИЛ ТИМИН β -аланин β- аминоизобутират Ацетил-КоА Сукцинил-КоА
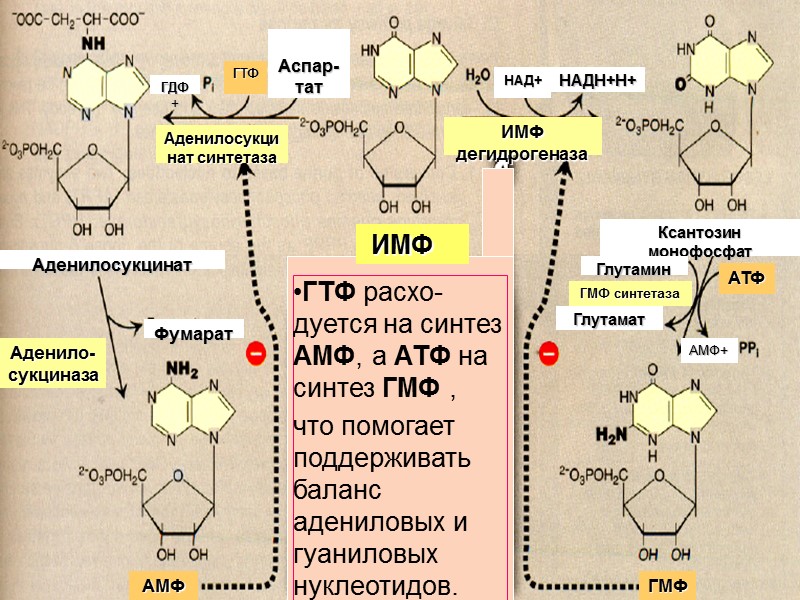
ИМФ дегидрогеназа Ксантозин монофосфат Глутамин Глутамат ГМФ синтетаза АТФ АМФ+ Аденилосукцинат Фумарат Аденило-сукциназа АМФ ГМФ Аденилосукцинат синтетаза НАД+ НАДН+Н+ Аспар-тат ГДФ+ ГТФ ИМФ ГТФ расхо-дуется на синтез АМФ, а АТФ на синтез ГМФ , что помогает поддерживать баланс адениловых и гуаниловых нуклеотидов.

Пурины могут использоваться для повторного синтеза нуклеотидов по «запасным путям», но не более 10-20% общего фонда. Гипоксантин-гуанин фосфорибозилтрансфераза Аденин фосфорибозилтрансфераза ПФ ПФ ПФ

5. Биосинтез белков. Аминокислотный код. Этапы трансляции (подготовительный, элонгация, пострибосомная трансформация полипептидной цепи). Ингибиторы трансляции.

Синтез белка отличается от других матричных биосинтезов тем, что между матрицей (мРНК) и продуктом-белком нет комплементарного соответствия. Поскольку матрица построена из 4 нуклеотидов, а продукт - полипептидная цепь из 20 аминокислот, то существует определенный закон шифрования аминокислот в нуклеотидной последовательности матрицы, т.е. биологический или генетический код. www.themegallery.com

www.themegallery.com Генети́ческий код — свойственный всем живым организмам способ кодирования аминокислотной последовательности белков при помощи последовательности нуклеотидов. В ДНК используется четыре азотистых основания — аденин (А), гуанин (G), цитозин (С), тимин (T), которые в русскоязычной литературе обозначаются буквами А, Г, Ц и Т. Эти буквы составляют алфавит генетического кода. В РНК используются те же нуклеотиды, за исключением нуклеотида, содержащего тимин, который заменён похожим нуклеотидом, содержащим урацил, который обозначается буквой U (У в русскоязычной литературе). В молекулах ДНК и РНК нуклеотиды выстраиваются в цепочки и, таким образом, получаются последовательности генетических букв. Белки практически всех живых организмов построены из аминокислот всего 20 видов. Эти аминокислоты называют каноническими. Каждый белок представляет собой цепочку или несколько цепочек аминокислот, соединённых в строго определённой последовательности. Эта последовательность определяет строение белка, а следовательно все его биологические свойства. Реализация генетической информации в живых клетках (то есть синтез белка, кодируемого геном) осуществляется при помощи двух матричных процессов: транскрипции (то есть синтеза мРНК на матрице ДНК) и трансляции генетического кода в аминокислотную последовательность (синтез полипептидной цепи на мРНК). Для кодирования 20 аминокислот, а также сигнала «стоп», означающего конец белковой последовательности, достаточно трёх последовательных нуклеотидов. Набор из трёх нуклеотидов называется триплетом. Принятые сокращения, соответствующие аминокислотам и кодонам, изображены на рисунке.

Свойства биологического кода Триплетность и наличие терминирующих кодонов - кодовое число равно 3. Три нуклеотидных остатка (триплет) кодируют одну аминокислоту. Терминирующие триплеты - UАА, UАG, UGА не кодируют аминокислот, а являются сигналами к прекращению синтеза белка Специфичность - каждый триплет кодирует только одну аминокислоту Вырожденность - одну аминокислоту могут кодировать несколько триплетов (от 2 до 6) Универсальность - почти у всех видов организмов биологический код одинаков Однонаправленность - информация, записанная в зрелой мРНК в виде линейной последовательности кодонов (триплетов), считывается в направлении от 5'- к 3'-концу Колинеарность - последовательность кодонов в зрелой мРНК соответствует последовательности аминокислот в синтезированном белке

Основные компоненты белок-синтезирующей системы и их функции в процессе трансляции Аминокислоты - субстраты для синтеза белков тРНК - выполняют функцию адапторов - приспособителей аминокислот к кодонам мРНК. Акцепторным концом (-ССА) они взаимодействуют с аминокислотами, а антикодоном - с кодоном мРНК Аминоацил-тРНКсинтетазы - каждый фермент катализирует реакцию специфического связывания 1 из 20 аминокислот с соответствующей тРНК мРНК - матрица содержит линейную последовательность кодонов, определяющих первичную структуру белков Рибосомы - рибонуклеопротеиновые субклеточные структуры, являющиеся местом синтеза белков АТФ, ГТФ -источники энергии Белковые факторы инициации (IF), элонгации (EF), терминации (RF) - специфические внерибосомные белки, необходимые для процесса трансляции Ионы магния - кофактор, стабилизирующий структуру рибосом
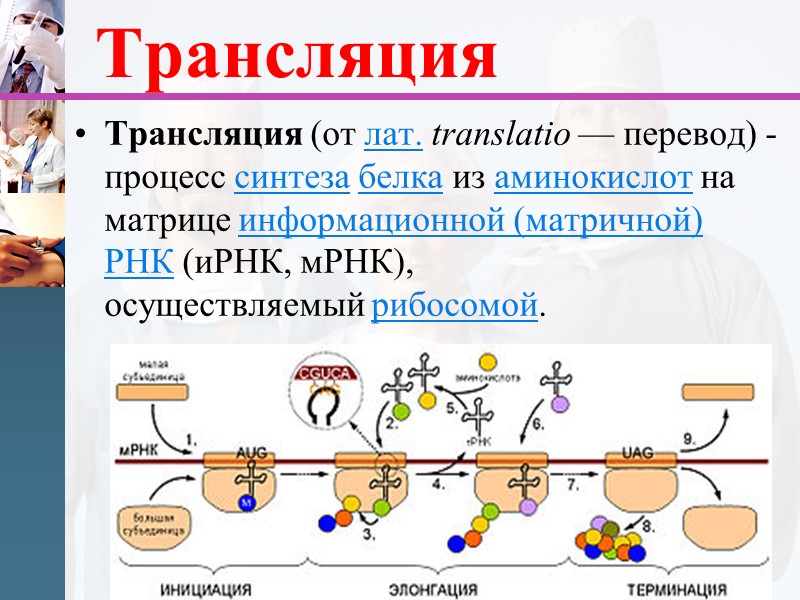
Трансляция Трансляция (от лат. translatio — перевод) - процесс синтеза белка из аминокислот на матрице информационной (матричной) РНК (иРНК, мРНК), осуществляемый рибосомой.

Процесс трансляции разделяют на инициацию — узнавание рибосомой стартового кодона и начало синтеза. элонгацию — собственно синтез белка. терминацию — узнавание терминирующего кодона (стоп-кодона) и отделение продукта.

Реакция активации аспартата, катализируемая аспарагил-тРНК-синтетазой Аминоацил-тРНК-синтетазы катализируют синтез аминоацил-тРНК - соединений, которые обеспечивают включение аминокислот в полипептидную цепь. Они обладают абсолютной специфичностью к аминокислоте и относительной к тРНК, так как в связи с вырожденностью кода разных типов тРНК больше, чем аминокислот. Существуют изоакцепторные тРНК, отличающиеся по строению антикодона, но связывающиеся с одной и той же аминокислотой. Указанием на способность тРНК присоединять определенную аминокислоту служит индекс в верхнем правом углу: тРНК, связывающаяся с глутаматом, обозначается как тРНКГлу, а с аланином - тРНКАла. Название каждой из 20 аминоацил-тРНК-синтетаз отражает название аминокислоты, которая активируется в ходе этой реакции. Так, реакцию активации аспартата катализирует аспарагил-тРНК-синтетаза, которая присоединяет α-СООН-группу аминокислоты к 3'-ОН концу тРНК за счет энергии АТФ.
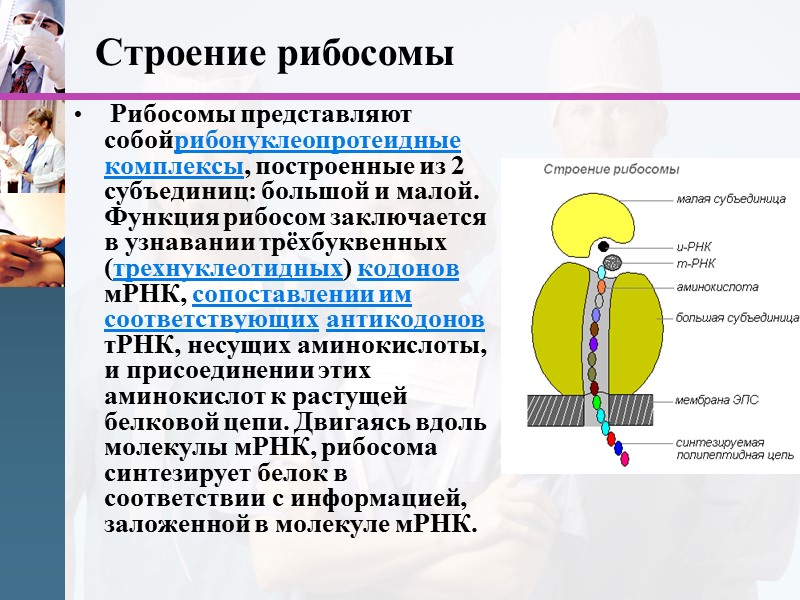
Строение рибосомы Рибосомы представляют собойрибонуклеопротеидные комплексы, построенные из 2 субъединиц: большой и малой. Функция рибосом заключается в узнавании трёхбуквенных (трехнуклеотидных) кодонов мРНК, сопоставлении им соответствующих антикодонов тРНК, несущих аминокислоты, и присоединении этих аминокислот к растущей белковой цепи. Двигаясь вдоль молекулы мРНК, рибосома синтезирует белок в соответствии с информацией, заложенной в молекуле мРНК.
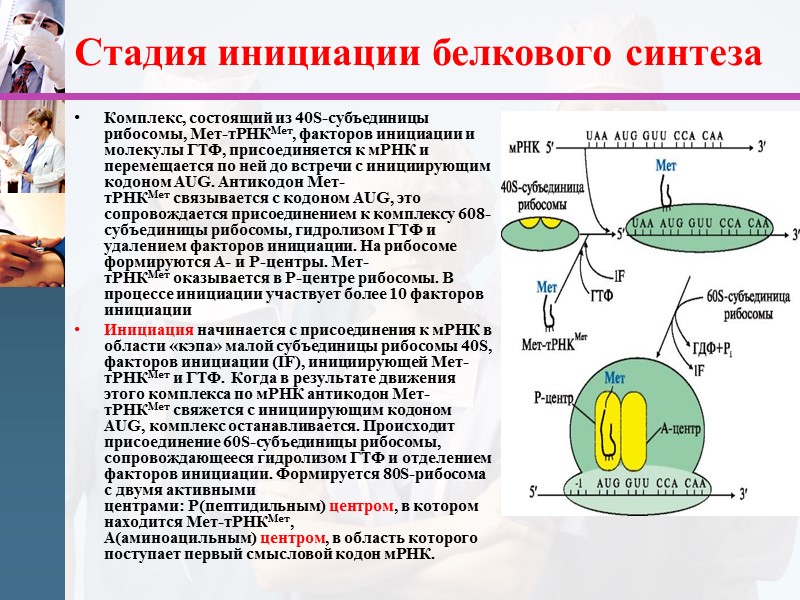
Стадия инициации белкового синтеза Комплекс, состоящий из 40S-субъединицы рибосомы, Мет-тРНКМет, факторов инициации и молекулы ГТФ, присоединяется к мРНК и перемещается по ней до встречи с инициирующим кодоном AUG. Антикодон Мет-тРНКМет связывается с кодоном AUG, это сопровождается присоединением к комплексу 608-субъединицы рибосомы, гидролизом ГТФ и удалением факторов инициации. На рибосоме формируются А- и Р-центры. Мет-тРНКМет оказывается в Р-центре рибосомы. В процессе инициации участвует более 10 факторов инициации Инициация начинается с присоединения к мРНК в области «кэпа» малой субъединицы рибосомы 40S, факторов инициации (IF), инициирующей Мет-тРНКМет и ГТФ. Когда в результате движения этого комплекса по мРНК антикодон Мет-тРНКМет свяжется с инициирующим кодоном АUG, комплекс останавливается. Происходит присоединение 60S-субъединицы рибосомы, сопровождающееся гидролизом ГТФ и отделением факторов инициации. Формируется 80S-рибосома с двумя активными центрами: Р(пептидильным) центром, в котором находится Мет-тРНКМет, А(аминоацильным) центром, в область которого поступает первый смысловой кодон мРНК.
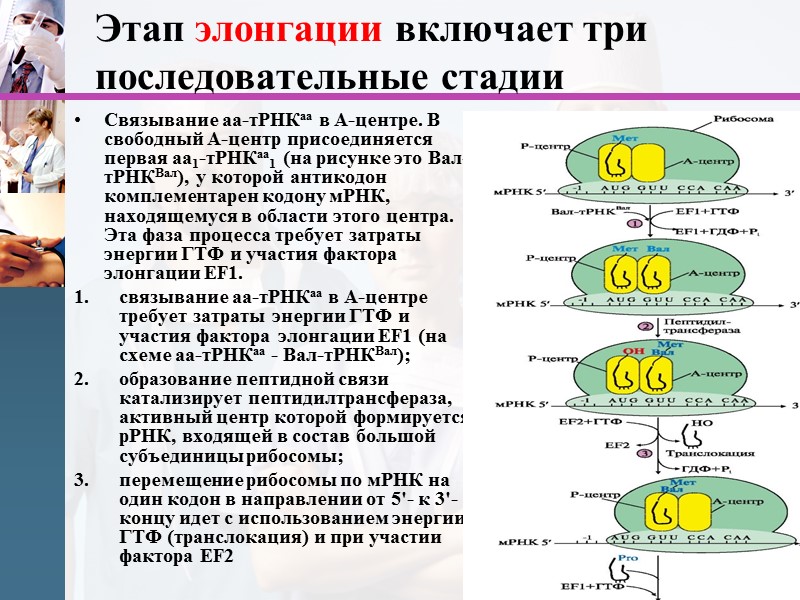
Этап элонгации включает три последовательные стадии Связывание аа-тРНКаа в А-центре. В свободный А-центр присоединяется первая аа1-тРНКаа1 (на рисунке это Вал-тРНКВал), у которой антикодон комплементарен кодону мРНК, находящемуся в области этого центра. Эта фаза процесса требует затраты энергии ГТФ и участия фактора элонгации EF1. связывание аа-тРНКаа в А-центре требует затраты энергии ГТФ и участия фактора элонгации EF1 (на схеме аа-тРНКаа - Вал-тРНКВал); образование пептидной связи катализирует пептидилтрансфераза, активный центр которой формируется рРНК, входящей в состав большой субъединицы рибосомы; перемещение рибосомы по мРНК на один кодон в направлении от 5'- к 3'-концу идет с использованием энергии ГТФ (транслокация) и при участии фактора EF2

Этап элонгации (продолжение) При попадании в А-центр стоп-кодона вновь синтезированный пептид высвобождается из связи с тРНК и рибосомой с участием факторов терминации и энергии ГТФ Образование пептидной Пептидил-тРНК связи. На этой стадии происходит пептидилтрансферазная реакция, в ходе которой метионин от Мет-тРНКМет, входящей в Р-центр, переносится на α-аминогруппу аминокислоты (валина), находящейся в А-центре в составе аа-тРНКаа, с образованием дипептидилтРНК. В пептидилтрансферазной реакции ферментативную активность проявляет рРНК большой субъединицы рибосомы.

Транслокация Транслокация - перемещение рибосомы по мРНК. В ходе этой стадии рибосома сдвигается на один кодон в направлении от 5'- к 3'-концу мРНК за счет энергии ГТФ и при участии фактора элонгации EF2. В результате дипептидил-тРНК (Мет-Вал-тРНК) из А-центра попадает в Р-центр, а в А-центре оказывается следующий кодон. Свободная тРНКМет теряет связь с Р-центром и покидает рибосому. Далее процесс продолжается по описанной схеме, повторяя стадии: Η 2 -> 3.
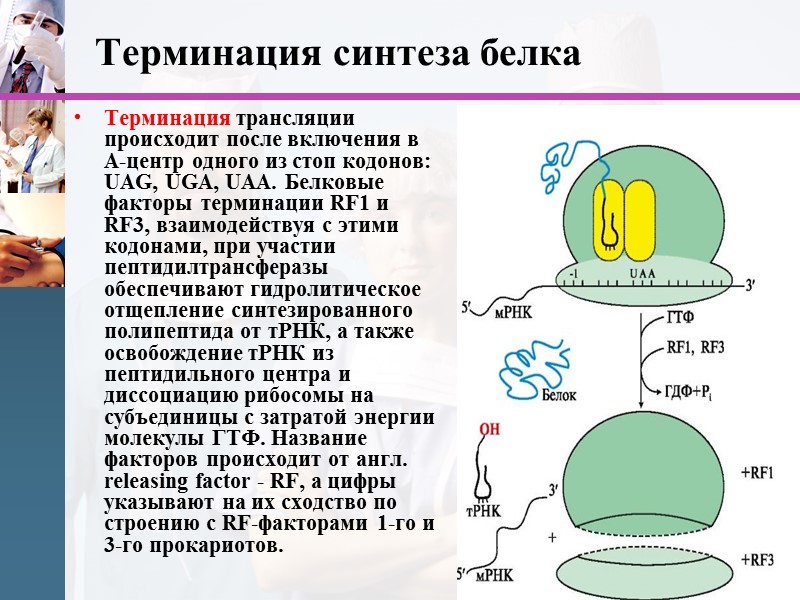
Терминация синтеза белка Терминация трансляции происходит после включения в А-центр одного из стоп кодонов: UAG, UGA, UAA. Белковые факторы терминации RF1 и RF3, взаимодействуя с этими кодонами, при участии пептидилтрансферазы обеспечивают гидролитическое отщепление синтезированного полипептида от тРНК, а также освобождение тРНК из пептидильного центра и диссоциацию рибосомы на субъединицы с затратой энергии молекулы ГТФ. Название факторов происходит от англ. releasing factor - RF, а цифры указывают на их сходство по строению с RF-факторами 1-го и 3-го прокариотов. www.themegallery.com

Полисома Одновременно несколько рибосом могут участвовать в трансляции одной мРНК. Каждая рибосома занимает участок, равный примерно 80 нуклеотидам мРНК. Таким образом, рибосомы располагаются на мРНК с интервалами около 100 нуклеотидов, образуя комплекс, называемый полисомой.

Функционально активные белки образуются в результате посттрансляционных модификаций полипептидных цепей, синтезированных на рибосомах. Они включают: частичный протеолиз; фолдинг, или формирование пространственной структуры, в котором принимают участие белки-шапероны, обеспечивающие образование функционально активной конформации полипептидной цепи; модификации аминокислот: карбоксилирование, фосфорилирование, йодирование, гидроксилирование, ацилирование и гликозилирование; образование дисульфидных связей между остатками цистеина, участвующими в формировании трехмерной структуры белка; присоединение простетических групп; образование олигомерных структур, которое также осуществляется при участии шаперонов.
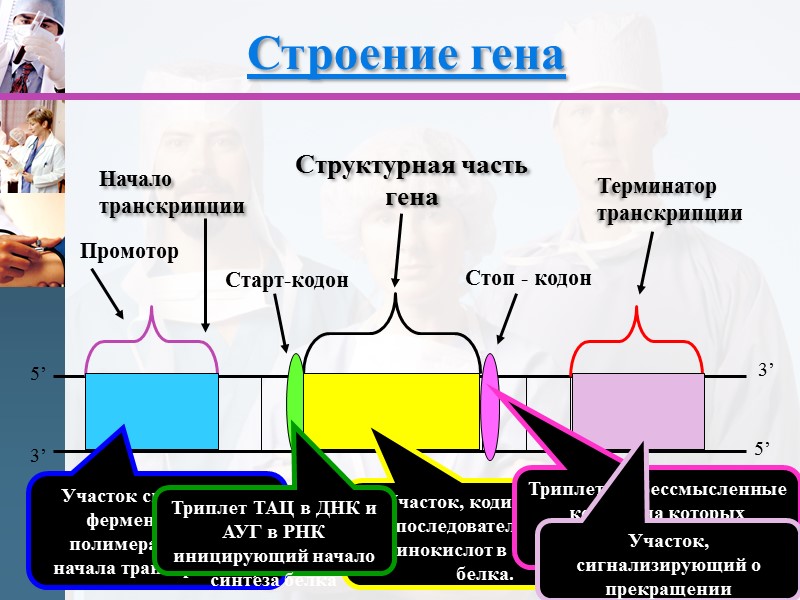
Структурная часть гена Промотор Начало транскрипции Старт-кодон Стоп - кодон 5’ 3’ 3’ 5’ Терминатор транскрипции Строение гена Участок связывания фермента РНК-полимеразы (место начала транскрипции) Участок, кодирующий последовательность аминокислот в молекуле белка. Триплет ТАЦ в ДНК и АУГ в РНК иницирующий начало синтеза белка Триплеты – бессмысленные кодоны на которых завершается трансляция Участок, сигнализирующий о прекращении транскрипции

Виды оперонов Оперон — это тесно связанная последовательность структурных генов, определяющих синтез группы белков, которые участвуют в одной цепи биохимических преобразований. К наиболее хорошо изученным оперонам бактерий относят: Лактозный (lac)-оперон Галактозный (gal)-оперон Триптофановый (trp)-оперон

Лактозный оперон Оперон – участок бактериальной хромосомы, включающий следующие участки ДНК: Р – промотор, О – оператор, Z, Y, А – структурные гены, Т –терминатор. (В состав других оперонов может входить до 10 структурных генов.) Промотор – место присоединения РНК- полимеразы. Оператор – участок оперона, к которому присоединяются белки-репрессоры или активаторы транскрипции. Структурные гены – гены кодирующие ферменты, участвующие в метаболизме лактозы. Терминатор служит для отсоединения РНК-полимеразы после окончания синтеза иРНК, соответствующей ферментам Z, Y, А, необходимым для усвоения лактозы.
www.themegallery.com Ингибиторы трансляции

www.themegallery.com Ингибиторы транскрипции Рифамицин - ингибирует РНК-полимеразу (в ядре). Актиномицин D – связывается с ДНК матрицей и препятствует продвижению РНК-полимеразы . Олигомицин Дактиномицин

www.themegallery.com Ингибиторы трансляции Тетрациклины – блокируют связывание аминоацил-тРНК к А-центру, связываются с 30S субъединицей (ингибируют элонгацию). Стрептомицин связывается с 30S субъединицей и (ингибирует инициацию). Эритромицин присоединяется к 50S субъединице и (ингибирует транслокацию). 4) Хлорамфеникол (левомицетин) – ингибирует пептидил трансферазу (транспептидацию). 5) Пуромицин – похож на аминоацил-тРНК, вызывает преждевременную терминацию. 6) Линкомицин – как хлорамфеникол.

www.themegallery.com Благодарю за внимание
27844-lektsia_12_biokhimia_nukleinovykh_kislot_2c_ma.ppt
- Количество слайдов: 134

